Изобретение относится к области фармацевтической химии и касается способов количественного определения биологически активных веществ, в частности суммарного содержания флавоноидов - веществ с выраженными антиоксидантными свойствами.
В литературных данных широко представлены методы определения как индивидуальных, так и суммы флавоноидов. Наиболее распространенными методом определения суммы флавоноидов является спектрофотометрические методы. Одним из них является метод авторов (В.Якштас, В.Янулис, Ю.Лабокас. Изучение флавонойдного состава растительного сырья // Электронный сборник статей «Технологии 21 века и фитотерапия», http://treskunov.narod.ru/conference2004/technology21.htm).
Предварительно проводят стадию пробоподготовки, связанную с многоступенчатой экстракцией флавоноидов в спиртовый раствор.
Полученный экстракт концентрируют до сухого остатка. Полученный раствор сухого остатка фильтруют и разбавляют до 50 мл, применяют для последующего количественного определения. К очищенному экстракту добавляют раствор уксусной кислоты и раствор алюминия хлорида. После образования комплекса флавоноидов с ионами алюминия добавляли раствор гексаметилентетрамина, полученный раствор спектрофотометрируют при длине волны 407 нм. Содержание суммы флавоноидов осуществляют в пересчете на рутин.
Одним из недостатком метода является использование трудоемкой стадии пробоподготовки, которая может привести к потере определяемых веществ.
Чувствительное и селективное определение флавоноидов (гиперозида, кверцитина, витексина, витексинрамнозида, рутина, кверцитрина) в растительном возможно с использованием метода ВЭЖХ с спектрофотометрическим детектированием при переменной длине волны (В.Якштас, В.Янулис, Ю.Лабокас. Изучение флавонойдного состава растительного сырья // Электронный сборник статей «Технологии 21 века и фитотерапия», http://treskunov.narod.ru/conference2004/technology21.htm).
Недостатком этого метода является использование дорогого оборудования и расходных реактивов.
Достаточно редко для количественного определения флавоноидов применяют электрохимические методы анализа. Однако в литературе представлено сочетание различных методов разделения и электрохимического детектирования. В работе (Ting Wu, Yueqing Guan, Jiannong Ye. Determination of flavonoids by capillary electrophoresis // Food Chemistry 100, 2007, p.1573-1579) показана возможность определения флавоноидов и аскорбиновой кислоты в соке грейпфрута с помощью капиллярного электрофореза с электрохимическим детектированием. Линейность концентрационной характеристики сохранялась в диапазоне 1.4·10-7÷1·10-6 г/мл в боратном буфере pH 9.0. Авторами из Китая было предложено использование капиллярного электрофореза с электрохимическим детектированием для определения флавоноидов (кампферол, апегинин, кверцетин и лютеолин) в различных растениях (Xueqin Xu, Lishuang Yu, Guonan Chen. Electrochemical method for determination of flavonoids // Journal of Pharmaceutical and Biomedical Analysis, 2006, V.41, p.493-499).
В данной работе определения проводились в кислой среде на стеклографитовом электроде в диапазоне потенциалов 0-1 B методом циклической вольтамперометрии. Во всех представленных работах предполагается, что электроактивность флавоноидов зависит от количества OH-групп и их положения в структуре соединений.
Недостатками этих методов является трудоемкость анализа (используется сочетание 2-х методов), его длительность, высокая стоимость оборудования и реактивов для анализа.
Наиболее близким к теме изобретения (прототипом) является использование метода, сочетающего хроматографическое разделение сложных объектов с последующим электрохимическим детектированием. Авторами работы (R.Aguilar-Sanchez, F.Ahuatl-Garcia, M.M.Davila-Jimenez, M.P.Elizalde-Gonzalez, M.R.G.Guevara-Villam Chromatographic study of flavonoids // Journal of Pharmaceutical and Biomedical Analysis, 2005, V.38, p.239-249) показана возможность детектирования кверцетина и кэмпферола с помощью дифференциально-импульсной вольтамперометрии. Определения проводились на графитовом электроде в трехэлектродной ячейке на 0.1 M спиртовом растворе NaClO4. По полученным данным можно говорить о количественном определении кверцетина и кэмпферола после хроматографического разделения в фармакологических препаратах.
К недостаткам способа можно отнести сложность и высокую стоимость оборудования, трудоемкость анализа, так как используется сочетание 2-х методов, определение всего 2-х флавоноидов (кверцетина и кэмпферола).
Новой технической задачей является увеличение чувствительности и экспрессности, а также уменьшение себестоимости и трудоемкости способа определения суммарного содержания флавоноидов в растительном сырье методом вольтамперометрии.
В растительном сырье флавоноиды на 90% представлены такими соединениями, как рутин, кверцетин, дигидрокверцетин, катехин. Поэтому для поставленной задачи были изучены электрохимические свойства некоторых флавоноидов (кверцетина, дигидрокверцетина, катехина, рутина) как индивидуально, так и при совместном присутствии. Экспериментальное исследование проводилось в условиях дифференциального режима постоянно-токовой вольтамперометрии на вольтамперометрическом анализаторе ТА-2 (производство ООО «Томьаналит» г.Томск) в комплекте с персональным компьютером. В качестве рабочего и вспомогательного электродов использовались стеклоуглеродные электроды (СУЭ), а электродом сравнения служил хлорид-серебряный электрод. Съемка вольтамперных кривых проводилась при скорости развертки потенциала W 0.04 В/с, в диапазоне потенциалов (E) от +0.1 B до +0.5 B. Фоновым электролитом служил 0.025 M водный раствор фосфатного буфера pH 6.86. Перед измерениями кислород из раствора удаляли продувкой раствора азотом, подаваемым в ячейку под давлением. Растворы исследуемых флавоноидов готовились из навески сухого вещества, концентрация составляла 10-3 г/мл.
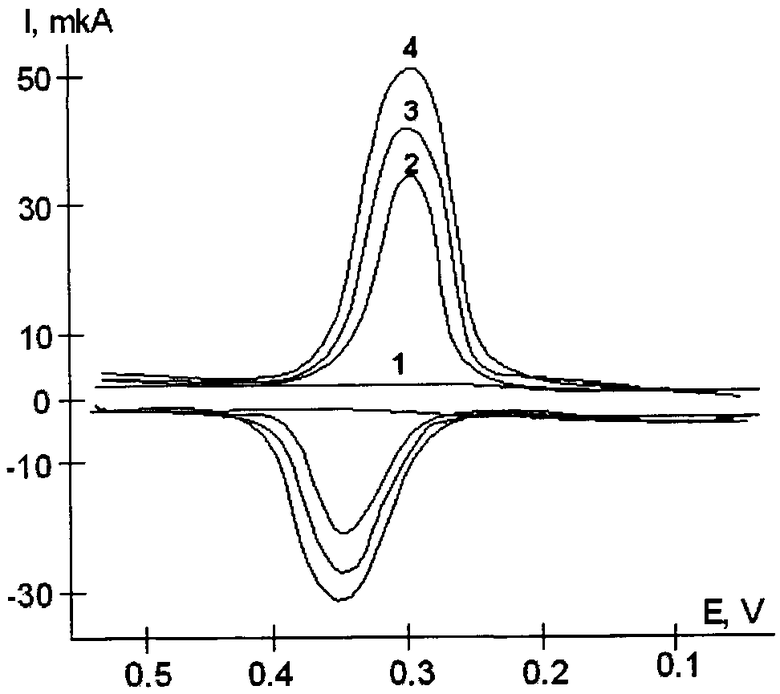
На чертеже дана циклическая вольтамперограмма дигидрокверцетина в фосфатном буфере pH 6.86 на СУЭ при скорости развертки 0.04 В/с: 0.1×10-3 моль/л (2), 0.2×10-3 моль/л (3), 0.3×10-3 моль/л (4), (1) - фоновая линия
В таблице 1 приведены потенциалы пиков окисления и восстановления ряда флавоноидов.
Как видно из таблицы, все исследованные флавоноиды в данных условиях эксперимента показали одинаковые потенциалы окисления и восстановления на стеклоуглеродном электроде относительно хлорид-серебряного электрода сравнения. Следовательно данный аналитический сигнал можно использовать для определения суммарного содержания флавоноидов в растительном сырье.
При использовании данного сигнала для разработки методики количественного определения суммарного содержания флавоноидов одним из важнейших вопросов является исследование зависимостей тока окисления и восстановления от концентрации объектов в растворе. Полученные зависимости предельного тока электроокисления суммарного содержания флавоноидов от их концентрации в фоновом растворе носили линейный характер в области концентраций (0÷6)×10-5 моль/л. Данный диапазон концентраций достаточен для определения флавоноидов в растительном сырье и БАД, а также фармацевтических препаратах.
Новым в способе является использование в качестве аналитического сигнала тока окисления флавоноидов на стеклоуглеродном электроде при потенциале E +0.3 B относительно хлорид-серебряного электрода сравнения в фосфатном буферном растворе с pH 6.86.
Пример 1. Определение суммарного содержания флавоноидов (рутин, кверцетин, дигидрокверцетин, катехин) в субстанции методом циклической вольтамперометрии.
В кварцевый стаканчик вместимостью 20 мл вносят 10,0 мл раствора фонового электролита 0.025 моль/л фосфатного буфера pH 6.86 в водном растворе и помещают в электрохимическую ячейку вольтамперометрического анализатора. Опускают в раствор электроды: индикаторный и вспомогательный - стеклоуглеродные, электрод сравнения - насыщенный хлорид-серебряный. С помощью стеклянной трубки фоновый раствор продувают газом азотом в течение 10 минут с целью вытеснения кислорода. Перемешивают 10 с, успокаивают 20 с, затем фиксируют циклическую вольтамперограмму фонового раствора в диапазоне потенциалов от +0.1 B до +0.5 B при скорости развертки потенциала 0.04 В/с. Отсутствие пиков свидетельствует о чистоте фона. Затем в стаканчик с фоновым раствором вносят аликвоту 1% раствора, содержащего суммарное количество флавоноидов (рутина, кверцетина, дигидрокверцетина, катехина в равных пропорциях) в воде объемом 0.5 мл. Перемешивают раствор 10 с, успокаивают 20 с и вновь снимают вольтамперограмму в тех же условиях. Анодный пик регистрируют при потенциале +0.3 B. Концентрацию суммарного содержания флавоноидов по высоте анодного пика определяют методом градуировочного графика, построенного по стандартным растворам одного из флавоноидов (например, дигидрокверцетина) с точно известными концентрациями, измеряя высоту полученного анодного пика.
Пример 2. Определение суммарного содержания флавоноидов в листьях брусники.
Листья брусники отделяют от стебля и помещают в чашку Петри на смоченную дистиллированной водой фильтровальную бумагу. Растительный материал (300 мг сырых листьев) растирают в ступке с небольшим количеством 0.025 М фосфатного буферного раствора рН 6.86 (1-2 мл), с добавлением стеклянного песка. Гомогенат переносят в центрифужную пробирку, обмывая ступку небольшим (0.5 мл) количеством буфера. Общий объем используемого буфера - 4 мл. Гомогенат центрифугируют 10 мин при 9 тысячах оборотах в минуту. Надосадочный раствор сливают в пробирку.
В кварцевый стаканчик вместимостью 20 мл вносят 10,0 мл раствора фонового электролита фосфатного буферного раствора рН 6.86 и помещают в электрохимическую ячейку вольтамперометрического анализатора. Опускают в раствор электроды: индикаторный и вспомогательный - стеклоуглеродные, электрод сравнения - насыщенный хлорид-серебряный. С помощью стеклянной трубки фоновый раствор продувают газом азотом в течение 10 минут с целью вытеснения кислорода. Перемешивают 10 с, успокаивают 20 с, затем фиксируют циклическую вольтамперограмму в диапазоне потенциалов от +0.1 B до +0.5 B при скорости развертки напряжения 0.04 В/с. Отсутствие пиков свидетельствует о чистоте фона. Затем в стаканчик с фоновым раствором вносят аликвоту (0.1 мл) надосадочного раствора экстракта листьев брусники. Перемешивают раствор 10 с, успокаивают 20 с и вновь снимают вольтамперограмму в тех же условиях. Анодный пик регистрируют при потенциале +0.3 B. Концентрацию суммарного содержания флавоноидов определяют методом градуировочного графика, построенного по стандартным растворам одного из флавоноидов (например, дигидрокверцетина) с точно известными концентрациями, измеряя высоту полученного анодного пика (E +0.3 B) на вольтамперограмме.
Предложенный способ количественного определения суммарного содержания флавоноидов отличается простотой, не требует больших трудозатрат, значительного количества реактивов и отличается высокой экспрессностью и чувствительностью.
Предложенный способ может быть использован для количественного определения суммарного содержания флавоноидов в растительном сырье. Метрологические характеристики данного способа: предел обнаружения составляет 1·10-5 г/мл, Относительная ошибка определения: 5%, область определяемых содержаний суммарного содержания флавоноидов от 1·10-5 г/мл до 1·10-4 г/мл.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ АНТИОКСИДАНТА КОЭНЗИМА Q В СУБСТАНЦИИ МЕТОДОМ ЦИКЛИЧЕСКОЙ ВОЛЬТАМПЕРОМЕТРИИ | 2010 |
|
RU2454660C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ СТАМПИРИНА В ПРЕПАРАТАХ С АНТИОКСИДАНТНЫМИ СВОЙСТВАМИ МЕТОДОМ ВОЛЬТАМПЕРОМЕТРИИ | 2010 |
|
RU2441226C1 |
| ВОЛЬТАМПЕРОМЕТРИЧЕСКИЙ СПОСОБ ОПРЕДЕЛЕНИЯ КОЭНЗИМА Q10 В КРЕМАХ КОСМЕТИЧЕСКИХ | 2015 |
|
RU2613897C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПОКАЗАТЕЛЯ СУММАРНОЙ АНТИОКСИДАНТНОЙ АКТИВНОСТИ БИОЛОГИЧЕСКИХ ОБЪЕКТОВ МЕТОДОМ КАТОДНОЙ ВОЛЬТАМПЕРОМЕТРИИ | 2010 |
|
RU2449275C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СУММАРНОГО СОДЕРЖАНИЯ АНТИОКСИДАНТОВ ТИОЛОВОЙ ПРИРОДЫ В РАСТИТЕЛЬНЫХ ОБЪЕКТАХ МЕТОДОМ КАТОДНОЙ ВОЛЬТАМПЕРОМЕТРИИ | 2010 |
|
RU2447444C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АСКОРБАТА ЛИТИЯ В ЛЕКАРСТВЕННОЙ ФОРМЕ МЕТОДОМ ВОЛЬТАМПЕРОМЕТРИИ | 2012 |
|
RU2510018C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ РТУТИ КАТОДНО-АНОДНОЙ ВОЛЬТАМПЕРОМЕТРИЕЙ | 2013 |
|
RU2533337C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АСКОРБАТА КАЛЬЦИЯ В БИОЛОГИЧЕСКИ АКТИВНЫХ ДОБАВКАХ МЕТОДОМ ВОЛЬТАМПЕРОМЕТРИИ | 2012 |
|
RU2510017C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СУММАРНОГО СОДЕРЖАНИЯ СЕРУСОДЕРЖАЩИХ СОЕДИНЕНИЙ В БИОЛОГИЧЕСКИХ ОБЪЕКТАХ | 2015 |
|
RU2613898C1 |
| Вольтамперометрический способ определения общего холестерина в биологических объектах | 2016 |
|
RU2629836C1 |
Изобретение относится к области фармацевтической химии и касается способов количественного определения биологически активных веществ, в частности суммарного содержания флавоноидов - веществ с выраженными антиоксидантными свойствами. Сущность: перевод веществ из пробы (растительное сырье) в раствор с последующим вольтамперометическим определением, которое проводят с использованием индикаторного стеклоуглеродного электрода относительно насыщенного хлорид-серебряного электрода на фоне 0,1 моль/л фосфатного буфера (рН 6.86) с последующей регистрацией анодных пиков при постоянно-токовой форме развертки потенциала со скоростью 0.04 В/с. Концентрацию суммарного содержания флавоноидов в растительном сырье определяют по высоте анодного пика окисления веществ в диапазоне потенциалов от +0.1 В до +0.5 В относительно насыщенного хлорид-серебряного электрода. Область определяемых содержаний суммарного количества флавоноидов от 1·10-5 г/мл до 1-10-4 г/мл. Технический результат изобретения: повышение чувствительности, экспрессности, уменьшение трудоемкости и себестоимости определения суммарного содержания флавоноидов в растительном сырье. 1 ил., 1 табл.
Способ количественного определения суммарного содержания флавоноидов в растительном сырье, включающий перевод веществ из пробы в раствор с последующим вольтамперометрическим определением, отличающийся тем, что проводят вольтамперометрическое определение с использованием индикаторного стеклоуглеродного электрода относительно насыщенного хлорид-серебряного электрода на фоне 0.025 моль/л фосфатного буфера рН 6.86 с последующей регистрацией анодных пиков при постоянно-токовой форме развертки потенциала со скоростью 0.04 В/с, концентрацию суммарного содержания флавоноидов в растительном сырье определяют по высоте анодного пика окисления веществ в диапазоне потенциалов от +0.1 В до +0.5 В относительно насыщенного хлорид-серебряного электрода, область определяемых содержаний суммарного количества флавоноидов от 1·10-5 г/мл до 1·10-4 г/мл.
| Aguilar-Sanchez R., Ahuatl-Garcia F., Davila-Jimenez M.M., Elizalde-Gonzalez M.P., Guevara-Villam M.R.G | |||
| Chromatographic study of flavonoids // Journal of Pharmaceutical and Biomedical Analysis, 2005, V.38, p.239-249 | |||
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ГЕСПЕРИДИНА МЕТОДОМ ДИФФЕРЕНЦИАЛЬНОЙ ВОЛЬТАМПЕРОМЕТРИИ | 2008 |
|
RU2381502C2 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ФЛАВОНОИДОВ МЕТОДОМ ДИФФЕРЕНЦИАЛЬНОЙ ВОЛЬТАМПЕРОМЕТРИИ | 2002 |
|
RU2215288C2 |
Авторы
Даты
2012-01-27—Публикация
2010-10-12—Подача