УРОВЕНЬ ТЕХНИКИ
Системы биодатчиков обычно обеспечивают анализ одного или более исследуемых веществ в биологических жидкостях. Анализ типично включает в себя количественное определение исследуемого вещества в биологической жидкости. Анализ полезен при диагностике и лечении физиологических патологий. Например, определение уровня глюкозы в крови является важным для лиц, больных диабетом, которые часто проверяют свой уровень глюкозы крови для контроля диеты и/или медикаментозного лечения. Для других лиц может быть важным контроль мочевой кислоты, лактата, холестерина и т.п.
Системы биодатчиков могут быть реализованы с использованием настольных, портативных и других измерительных устройств. Портативные устройства могут быть ручными и обычно включают в себя измерительное устройство и пластинку датчика. Типично образец биологической жидкости вводится на пластинку датчика, которая помещается в измерительное устройство для анализа. Системы биодатчиков могут быть предназначены для анализа одного или более исследуемых веществ и могут использовать разные объемы биологических жидкостей. Некоторые системы биодатчиков могут анализировать единственную каплю цельной крови (WB), такую как от 1 до 15 микролитров (мкл) по объеме.
Системы биодатчиков обычно измеряют выходной сигнал, чтобы определять концентрацию исследуемого вещества в образце биологической жидкости. Выходной сигнал вырабатывается из окислительной/восстановительной или окислительно-восстановительной реакции исследуемого вещества. Ферменты или подобные препараты могут добавляться к образцу для усиления окислительно-восстановительной реакции. Выходной сигнал может быть электрическим сигналом, светом или светом, преобразованным в электрический сигнал. Система биодатчиков может формировать выходной сигнал с использованием системы оптических датчиков или системы электрохимических датчиков.
В оптических системах концентрация исследуемого вещества определяется посредством измерения светового излучения, которое провзаимодействовало с идентифицируемыми светом препаратами, такими как исследуемое вещество, либо реакция или продукт, образованный из химического индикатора, вступающего в окислительно-восстановительную реакцию с исследуемым веществом. Падающий возбуждающий пучок из источника света направляется на образец. Идентифицируемые светом препараты поглощают или сдвигают длину волны части падающего пучка, таким образом, изменяя длину волны или снижая интенсивность падающего пучка. Детектор собирает и измеряет ослабленный пучок или падающий пучок с измененной длиной волны, который является выходным сигналом. В других оптических системах химический индикатор флуоресцирует или испускает свет в ответ на окислительно-восстановительную реакцию исследуемого вещества, когда освещается возбуждающим пучком. Детектор собирает и измеряет световое излучение, которое является выходным сигналом.
В электрохимических системах концентрация исследуемого вещества определяется посредством измерения электрического сигнала, такого как ток или потенциал. Типично исследуемое вещество подвергается окислительно-восстановительной реакции, когда сигнал возбуждения прикладывается к образцу. Сигналом возбуждения обычно является электрический сигнал, такой как ток или потенциал. Окислительно-восстановительная реакция вырабатывает выходной сигнал в ответ на сигнал возбуждения. Выходным сигналом обычно является электрический сигнал, такой как ток или потенциал, который может быть измерен и соотнесен с концентрацией исследуемого вещества.
В электрохимических системах измерительное устройство обычно имеет электрические контакты, которые соединяются с электрическими проводниками на пластинке датчика. Электрические соединители присоединены проводниками к электродам, которые тянутся в образец биологической жидкости. Измерительное устройство прикладывает сигнал возбуждения через электрические контакты к электрическим проводникам, которые передают сигнал возбуждения в образец через электроды. Окислительно-восстановительная реакция исследуемого вещества вырабатывает выходной сигнал в ответ на сигнал возбуждения. Измерительное устройство определяет концентрацию исследуемого вещества в ответ на выходной сигнал. Примеры портативных измерительных устройств включают в себя измерители Ascensia Breeze® и Elite® корпорации Bayer; биодатчики Precision®, доступные для приобретения у компании Abbott в Эббот-Парк, шт. Иллинойс; биодатчики Accucheck®, доступные для приобретения у компании Roche в Индианаполисе, шт. Индиана; и биодатчики OneTouch Ultra®, доступные для приобретения у компании Lifescan в Мильпитасе, шт. Калифорния. Примеры настольных измерительных устройств включают в себя анализатор BAS 100B, доступный для приобретения у компании BAS Instruments в Уэст-Лафайете, шт. Индиана; Electrochemical Workstation (электрохимическая рабочая станция) от CH Instruments, доступная для приобретения у компании CH Instruments в Остине, шт. Техас; Electrochemical Workstation от Cypress, доступная для приобретения у компании Cypress Systems в Лоуренсе, шт. Канзас; и Electrochemical Instrument (электрохимический прибор) от EG&G, доступный от компании Princeton Research Instruments в Принстоне, шт. Нью-Джерси.
Пластинки датчиков могут включать в себя реактивы, которые вступают в реакцию с исследуемым веществом в образце биологической жидкости. Реактивы включают в себя ионизирующий агент для облегчения окислительно-восстановительной реакции исследуемого вещества, а также медиаторы или другие вещества, которые способствуют переносу электронов между исследуемым веществом и проводником. Ионизирующий агент может быть специфичным исследуемому веществу ферментом, таким как глюкооксидаза или дегидрогеназа глюкозы, чтобы катализировать окисление глюкозы в образце WB. Реактивы могут включать в себя связующее вещество, которое удерживает фермент и медиатор вместе. В оптических системах реактивы включают в себя химический индикатор наряду с другим ферментом или подобными препаратами, чтобы усиливать реакцию химического индикатора с исследуемым веществом или продуктами окислительно-восстановительной реакции исследуемого вещества.
Большинство систем биодатчиков используют уравнения зависимости или калибровочные характеристики для определения концентрации исследуемого вещества в образце биологической жидкости. Уравнения зависимости представляют собой зависимость между выходными сигналами и концентрациями исследуемого вещества. По каждому уравнению зависимости концентрация исследуемого вещества может быть рассчитана для конкретного выходного сигнала. Уравнения зависимости являются зависимыми от температуры образца. Выходной сигнал для конкретной концентрации исследуемого вещества может меняться из-за влияния температуры на окислительно-восстановительную реакцию исследуемого вещества, ферментативную кинетику, диффузию и тому подобное. Уравнение зависимости может быть необходимым для каждой возможной температуры образца для того, чтобы рассчитывать концентрацию исследуемого вещества по выходному сигналу при конкретной температуре образца.
Чтобы сократить количество уравнений зависимости, используемых при анализе образца, многие системы биодатчиков стремятся выдавать концентрации исследуемого вещества с использованием одного или более уравнений зависимости для конкретной эталонной температуры. Концентрация исследуемого вещества при температуре образца обычно компенсируется разницей между температурой образца и эталонной температурой, чтобы выдавать концентрацию исследуемого вещества при эталонной температуре.
Некоторые системы биодатчиков компенсируют температуру изменением выходного сигнала перед расчетом концентрации исследуемого вещества по уравнению зависимости. Выходной сигнал обычно умножается на температурный поправочный коэффициент или тому подобное. Выходной сигнал с поправкой на температуру используется для определения концентрации исследуемого вещества. Системы биодатчиков, использующие выходной сигнал с поправкой на температуру, описаны в патентах США № 4,750,496 и № 6,576,117.
Другие системы биодатчиков компенсируют температуру изменением концентрации исследуемого вещества, рассчитанной по уравнению зависимости. Концентрация исследуемого вещества, рассчитанная по уравнению зависимости, обычно подвергается процедуре поправки на температуру, чтобы выдавать концентрацию исследуемого вещества с поправкой на температуру. Системы биодатчиков, использующие концентрацию исследуемого вещества с поправкой на температуру, описаны в патентах США № 5,366,609; 5,508,171 и № 6,391,645.
Дополнительные системы биодатчиков компенсируют температуру изменением выходного сигнала перед расчетом концентрации исследуемого вещества по уравнению зависимости и/или изменением концентрации исследуемого вещества, рассчитанной по уравнению зависимости. Системы биодатчиков, использующие выходной сигнал с поправкой на температуру и/или концентрацию исследуемого вещества с поправкой на температуру, описаны в патентах США № 4,431,004 и № 5,395,504.
Несмотря на то, что эти способы температурной компенсации уравновешивают различные преимущества и недостатки, ни один из них не является идеальным. Эти способы не могут полностью объединять различные влияния разных температур образца на окислительно-восстановительную реакцию исследуемого вещества, ферментативную и медиаторную кинетику и диффузию. Эти способы не могут в достаточной мере реагировать на влияния различных концентраций исследуемого вещества на ферментативную кинетику и диффузию при разных температурах образца. Эти способы также не могут в достаточной мере реагировать на влияния разных концентраций исследуемого вещества в окислительно-восстановительной реакции при различных температурах образца. В дополнение изменения в отношении выходного сигнала и/или рассчитанной концентрации исследуемого вещества могут вносить или увеличивать погрешности, имеющие отношение к определению концентрации исследуемого вещества по выходному сигналу.
Соответственно есть насущная потребность в усовершенствованных системах биодатчиков, особенно в тех, которые могут выдавать точные и прецизионные концентрации исследуемого вещества при эталонной температуре. Системы, устройства и способы по настоящему изобретению преодолевают, по меньшей мере, один из недостатков, ассоциативно связанных с традиционными системами биодатчиков.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение предлагает систему биодатчиков, которая определяет концентрацию исследуемого вещества в образце биологической жидкости по выходному сигналу, вырабатываемому окислительно-восстановительной реакцией исследуемого вещества. Система биодатчиков вносит поправку в зависимость между концентрациями исследуемого вещества и выходными сигналами при эталонной температуре, чтобы определять концентрации исследуемого вещества по выходным сигналам при других температурах. Система биодатчиков использует зависимость с поправкой на температуру для определения концентрации исследуемого вещества по выходному сигналу при некоторой температуре образца.
В способе для определения концентрации исследуемого вещества в образце биологической жидкости определяется температура образца. Выходной сигнал формируется в ответ на окислительно-восстановительную реакцию исследуемого вещества в образце. Зависимость между концентрациями исследуемого вещества и выходными сигналами при эталонной температуре подвергается поправке в ответ на температуру. Концентрация исследуемого вещества определяется по зависимости с поправкой на температуру и выходному сигналу при температуре образца.
В способе для внесения поправки в зависимость между концентрациями исследуемого вещества и выходными сигналами при эталонной температуре в ответ на температуру зависимости между концентрациями исследуемого вещества и выходными сигналами определяются для эталонной температуры и при, по меньшей мере, одной другой температуре. Нормированные температурные функции крутизны и отсекаемого отрезка строятся для зависимости эталонной температуры. Зависимость эталонной температуры подвергается поправке в ответ на нормированные температурные функции крутизны и отсекаемого отрезка.
Биодатчик для определения концентрации исследуемого вещества в биологической жидкости включает в себя измерительное устройство и пластинку датчика. Измерительное устройство содержит процессор, присоединенный к интерфейсу датчика и температурному датчику. Пластинка датчика имеет область контакта с образцом на основании. Область контакта с образцом является прилегающей к резервуару, образованному основанием. Процессор вносит поправку в зависимость между концентрациями исследуемого вещества и выходными сигналами при эталонной температуре в ответ на температуру образца из температурного датчика. Процессор определяет концентрацию исследуемого вещества по зависимости с поправкой на температуру в ответ на выходной сигнал из области контакта с образцом.
Следующие определения включены в состав для обеспечения более ясного и более целостного понимания описания изобретения и формулы изобретения.
«Исследуемое вещество» определено в качестве одного или более веществ, присутствующих в образце. Анализ определяет наличие и/или концентрацию исследуемого вещества, присутствующего в образце.
«Образец» определен в качестве состава, который может содержать неизвестное количество исследуемого вещества. Типично образец для электрохимического анализа находится в жидком виде, и, предпочтительно, образец является водной смесью. Образец может быть биологическим образцом, таким как кровь, моча или слюна. Образец также может быть производным от биологического образца, таким как вытяжка, раствор, фильтрат или воспроизведенный осадок.
«Проводник» определен в качестве токопроводящего вещества, которое остается неизменным во время электрохимического анализа.
«Точность» определена в качестве того, насколько близко количество исследуемого вещества, измеренное системой датчиков, соответствует истинному количеству исследуемого вещества в образце. Точность может быть выражена в показателях систематической погрешности показаний исследуемого вещества системой датчиков по сравнению с эталонным показанием исследуемого вещества. Большие значения систематической погрешности отражают меньшую точность.
«Прецизионность» определена в качестве того, насколько близки многочисленные измерения исследуемого вещества для одного и того же образца. Прецизионность может быть выражена в показателях разброса или дисперсии между многочисленными измерениями.
«Окислительно-восстановительная реакция» определена в качестве химической реакции между двумя препаратами, влекущей за собой перенос, по меньшей мере, одного электрона с первого препарата на второй препарат. Таким образом, окислительно-восстановительная реакция включает в себя окисление и восстановление. Окислительный полуэлемент реакции влечет за собой потерю, по меньшей мере, одного электрона первым препаратом, наряду с тем, что восстановительный полуэлемент влечет за собой добавление, по меньшей мере, одного электрона во второй препарат. Ионный заряд препарата, который окисляется, делается более положительным на величину, равную количеству унесенных электронов. Подобным образом, ионный заряд препарата, который восстанавливается, делается менее положительным на величину, равную количеству полученных электронов.
«Медиатор» определен в качестве вещества, которое может окисляться или восстанавливаться и которое может переносить один или более электронов. Медиатором является реактив в электрохимическом анализе и не является интересующим исследуемым веществом, но предусматривает косвенное измерение исследуемого вещества. В упрощенческой системе медиатор подвергается окислительно-восстановительной реакции в ответ на окисление или восстановление исследуемого вещества. Затем окисленный или восстановленный медиатор подвергается обратной реакции на рабочем электроде пластинки датчика и регенерируется до своей исходной степени окисления.
«Связующее вещество» определено в качестве вещества, которое обеспечивает поддержку и сдерживание распространения для реактивов наряду с обладанием химической совместимостью с реактивами.
«Установившееся состояние» определено в качестве того, когда изменение сигнала по отношению к его независимой входной переменной (времени, и т.п.) является по существу неизменным, таким как в пределах ±10 или ±5%.
«Невозвратная точка» определена в качестве значения сигнала, полученного как функция времени, когда возрастающая скорость диффузии переходит в относительно постоянную скорость диффузии. До невозвратной точки сигнал является быстро изменяющимся во времени. Подобным образом, после невозвратной точки, скорость затухания сигнала становится относительно постоянной, таким образом, отражая относительно постоянную скорость диффузии.
«Ручное устройство» определено в качестве устройства, которое может удерживаться в руке человека, и является портативным. Примером ручного устройства является измерительное устройство, сопровождающее элитную систему контроля глюкозы крови (Elite Blood Glucose Monitoring System) Ascensia®, доступную для приобретения в Bayer HealthCare, LLC, Элкхарт, шт. Индиана.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Изобретение может быть лучше понято со ссылкой на последующие чертежи и описание. Компоненты на фигурах не обязательно должны представлять в определенном масштабе, взамен, акцент ставится на иллюстрации принципов изобретения. Более того, на фигурах одинаковые номера ссылок обозначают соответствующие части на всем протяжении разных изображений.
Фиг. 1 представляет способ для определения концентрации исследуемого вещества в образце биологической жидкости.
Фиг. 2 представляет способ для внесения поправки в зависимость между концентрациями исследуемого вещества и выходными сигналами при эталонной температуре в ответ на температуру образца.
Фиг. 3 − график, иллюстрирующий зависимости между концентрациями исследуемого вещества и выходными сигналами.
Фиг. 4 − график, иллюстрирующий нормированную крутизну в качестве функции температуры для зависимостей между концентрациями глюкозы в цельной крови и током для времени исследования в 7 секунд.
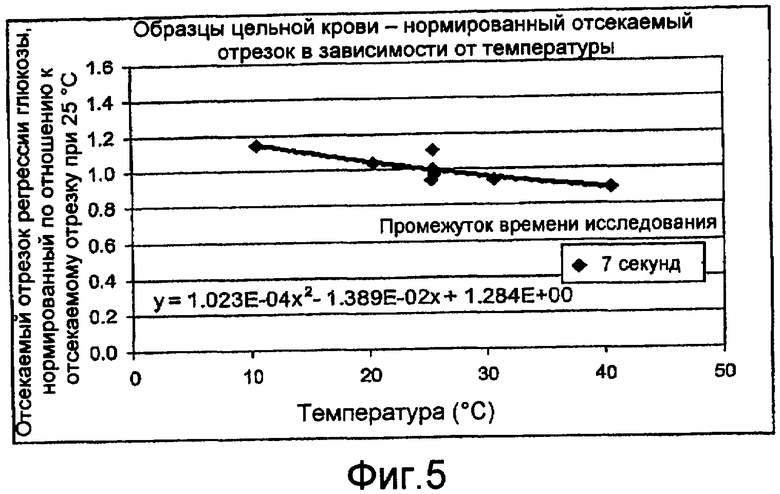
Фиг. 5 − график, иллюстрирующий нормированные отсекаемые отрезки в качестве функции температуры для зависимостей между концентрациями глюкозы в цельной крови и током для времени исследования в 7 секунд.
Фиг. 6 − график, иллюстрирующий нормированную крутизну в качестве функции температуры для зависимостей между концентрациями глюкозы в цельной крови и током для нескольких промежутков времени исследования.
Фиг. 7 − график, иллюстрирующий нормированные отсекаемые отрезки в качестве функции температуры для зависимостей между концентрациями глюкозы в цельной крови и током для нескольких промежутков времени исследования.
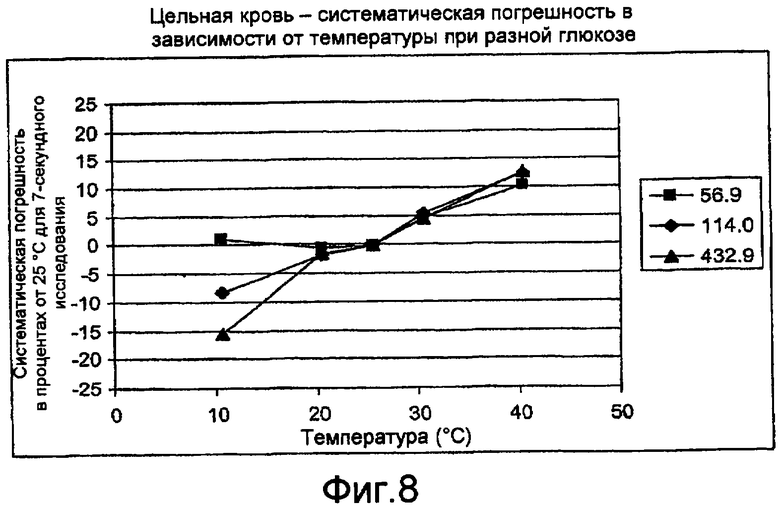
Фиг. 8 - график, иллюстрирующий систематическую погрешность от эталонной температуры рассчитанных концентраций глюкозы без какой бы то ни поправки на температуру.
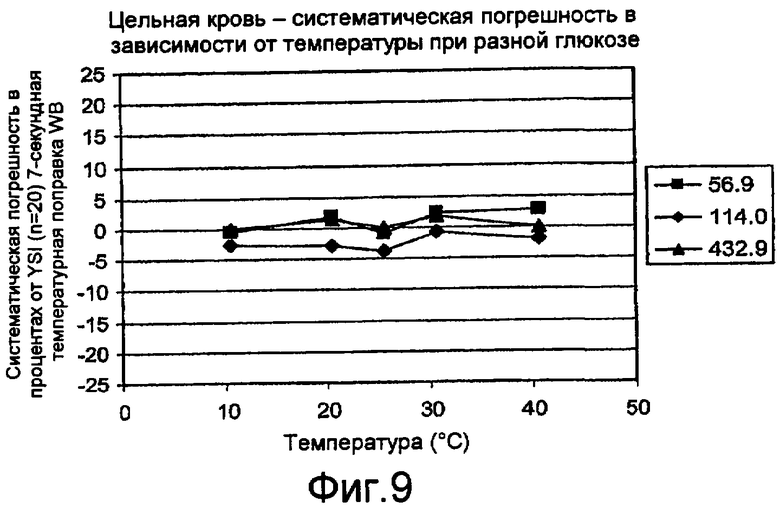
Фиг. 9 - график, иллюстрирующий систематическую погрешность от эталонной температуры рассчитанных концентраций глюкозы с поправкой на температуру.
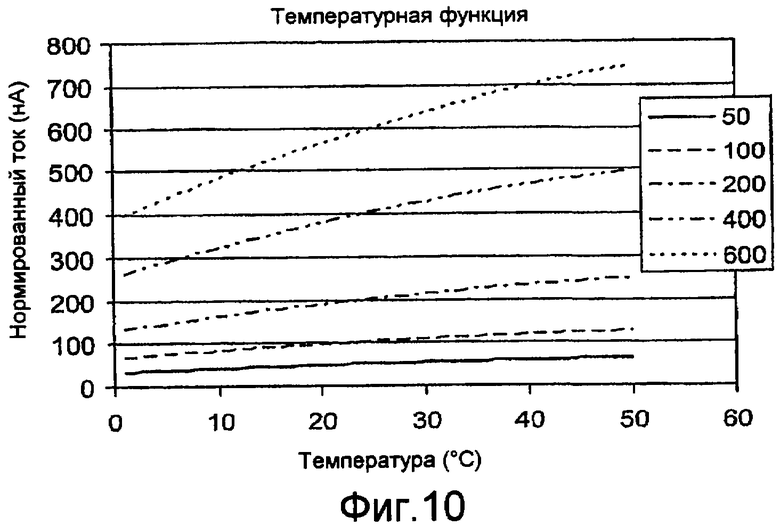
Фиг. 10 - график, иллюстрирующий температурную функцию тока из датчика глюкозы с нормированной крутизной и отсекаемым отрезком.
Фиг. 11 - график, иллюстрирующий функцию температурного коэффициента для нормированного тока по фиг. 10 относительно температуры.
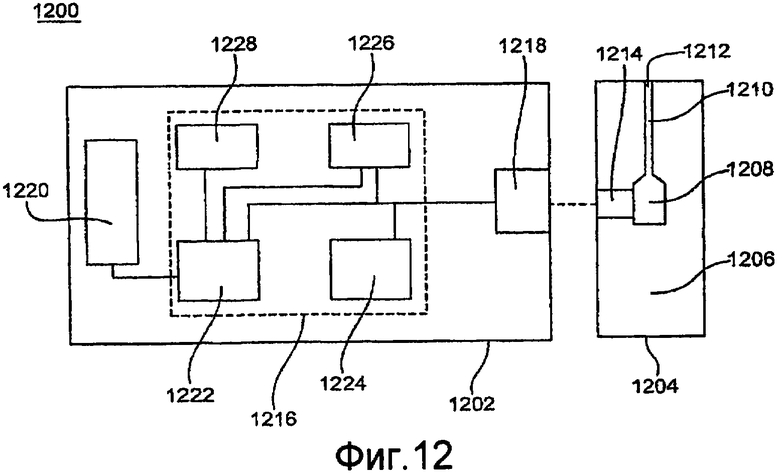
Фиг. 12 изображает схематическое представление биодатчика, который определяет концентрацию исследуемого вещества в образце биологической жидкости.
ПОДРОБНОЕ ОПИСАНИЕ
Описана система биодатчиков, которая определяет исследуемое вещество в образце биологической жидкости. Система биодатчиков определяет концентрацию исследуемого вещества по выходному сигналу, вырабатываемому окислительной/восстановительной или окислительно-восстановительной реакцией исследуемого вещества. Система вносит поправку в уравнение зависимости для определения концентраций исследуемого вещества по выходным сигналам при одной температуре, чтобы определять концентрации исследуемого вещества по выходным сигналам при других температурах, таких как температура образца. Зависимости с поправкой на температуру повышают точность и прецизионность системы биодатчиков при определении концентрации исследуемого вещества образца. Система биодатчиков может определять концентрации исследуемого вещества по выходным сигналам при температуре образца с использованием уравнения зависимости с поправкой на температуру для эталонной температуры. Уравнения зависимости между концентрациями исследуемого вещества и выходными сигналами могут быть представлены графически, математически, их сочетанием и тому подобным. Уравнения зависимости могут быть представлены таблицей номеров программы (PNA), иной справочной таблицей или тому подобным. Система биодатчиков может использоваться для определения концентраций исследуемого вещества, такого как глюкоза, мочевая кислота, лактат, холестерин, билирубин и тому подобное.
Фиг. 1 представляет способ для определения концентрации исследуемого вещества в образце биологической жидкости. На 102 определяется температура образца. На 104 выходной сигнал формируется в ответ на окислительно-восстановительную реакцию исследуемого вещества в образце. На 106 зависимость между концентрациями исследуемого вещества и выходными сигналами при эталонной температуре подвергается поправке в ответ на температуру. На 108 концентрация исследуемого вещества определяется из зависимости с поправкой на температуру и выходному сигналу при температуре образца. На 110 концентрация исследуемого вещества отображается и может сохраняться для будущего обращения.
На 102 по фиг. 1 температура образца может определяться с использованием различных технологий. Температура образца может измеряться с использованием термистора, термометра или другого термочувствительного устройства. Температура образца может рассчитываться по выходному сигналу электрохимической реакции в образце. Температура образца может предполагаться идентичной или подобной измерению температуры окружающей среды или температуры устройства, реализующего систему биодатчиков. Могут использоваться другие технологии для определения температуры образца.
На 104 по фиг. 1 выходной сигнал формируется в ответ на окислительную/восстановительную или окислительно-восстановительную реакцию исследуемого вещества в образце. Выходной сигнал может формироваться с использованием системы оптических датчиков, системы электрохимических датчиков, или тому подобного.
Системы оптических датчиков обычно измеряют количество света, поглощенного или сформированного реакцией химического индикатора с окислительно-восстановительной реакцией исследуемого вещества. Химическим индикатором может содержаться фермент для улучшения кинетики реакции. Выходной сигнал или свет из оптической системы может преобразовываться в электрический сигнал, такой как ток или потенциал.
В оптических системах с поглощением света химический индикатор порождает продукт реакции, который поглощает свет. Может использоваться химический индикатор, такой как тетразолий, наряду с ферментом, таким как диафораза. Тетразолий обычно образует формазан (хромаген) в ответ на окислительно-восстановительную реакцию исследуемого вещества. Падающий возбуждающий пучок, из источника света, направляется на образец. Источник света может быть лазером, светоизлучающим диодом или тому подобным. Падающий пучок может иметь длину волны, подобранную для поглощения продуктом реакции. По мере того, как падающий пучок проходит через образец, продукт реакции поглощает часть падающего пучка, таким образом, ослабляя или снижая интенсивность падающего пучка. Падающий пучок может отражаться обратно или пропускаться через образец в детектор. Детектор собирает и измеряет ослабленный падающий пучок (выходной сигнал). Количество света, ослабленного продуктом реакции, является признаком концентрации исследуемого вещества в образце.
В оптических системах со световозбуждением химический детектор флуоресцирует или испускает свет в ответ на окислительно-восстановительную реакцию исследуемого вещества. Детектор собирает и измеряет вырабатываемый свет (выходной сигнал). Количество света, выработанного химическим индикатором, является признаком концентрации исследуемого вещества в образце.
Электрохимические системы прикладывают входной сигнал к образцу биологической жидкости. Входной сигнал может быть потенциалом или током и может быть постоянным, переменным или их сочетанием, таким как когда сигнал переменного тока прикладывается со смещением на сигнал постоянного тока. Входной сигнал может прикладываться в качестве одиночного импульса или многочисленными импульсами, последовательностями или циклами. Исследуемое вещество подвергается окислительно-восстановительной реакции, когда входной сигнал прикладывается к образцу. Фермент или подобные препараты могут использоваться для ускорения окислительно-восстановительной реакции исследуемого вещества. Медиатор может использоваться для поддержания состояния окисления фермента. Окислительно-восстановительная реакция вырабатывает выходной сигнал, который может измеряться непрерывно или периодически во время переходного и/или установившегося выходного сигнала. Могут использоваться различные электрохимические процессы, такие как амперометрия, кулонометрия, вольтамперометрия или тому подобное. Также могут использоваться стробированная амперометрия и стробированная вольтамперометрия.
При амперометрии потенциал или напряжение прикладывается к образцу биологической жидкости. Окислительно-восстановительная реакция исследуемого вещества вырабатывает ток в ответ на потенциал. Ток измеряется в течение промежутка временем для определения количества исследуемого вещества в образце. Амперометрия обычно измеряет скорость, на которой исследуемое вещество окисляется или восстанавливается, для определения концентрации исследуемого вещества в образце. Системы биодатчиков, использующие амперометрию, описаны в патентах США № 5,620,579; № 5,653,863; № 6,153,069 и № 6,413,411.
При кулонометрии потенциал прикладывается к образцу биологической жидкости, чтобы полностью окислить или восстановить исследуемое вещество в образце. Потенциал порождает ток, который интегрируется в течение промежутка времени окисления/восстановления для выработки электрического заряда, представляющего концентрацию исследуемого вещества. Кулонометрия обычно фиксирует общее количество исследуемого вещества в образце. Система биодатчиков, использующая кулонометрию для измерения глюкозы цельной крови, описана в патенте США № 6,120,676.
При вольтамперометрии переменный потенциал прикладывается к образцу биологической жидкости. Окислительно-восстановительная реакция исследуемого вещества вырабатывает ток в ответ на приложенный потенциал. Ток измеряется в течение промежутка времени для определения количества исследуемого вещества в образце. Вольтамперометрия обычно измеряет скорость, на которой исследуемое вещество окисляется или восстанавливается, для определения концентрации исследуемого вещества в образце. Дополнительная информация о вольтамперометрии может быть найдена в «Electrochemical Methods: Fundamentals and Applications» by A.J. Bard and L.R. Faulkner, 1980 («Электрохимические методы: Основы и применения» от А.Дж. Барда и Л.Р. Фолкнера, 1980 г.).
При стробированной амперометрии и стробированной вольтамперометрии импульсные возбуждения используются так, как описано в предварительных заявках на выдачу патента США № 60/700,787, зарегистрированной 20 июля 2005 г., и № 60/722,584, зарегистрированной 30 сентября 2005 г., соответственно, которые включены в состав посредством ссылки.
На 106 по фиг. 1 зависимость между концентрациями исследуемого вещества и выходными сигналами при эталонной температуре подвергается поправке в ответ на температуру. Зависимость может быть представлена уравнением зависимости или калибровочной характеристикой, которые рассчитывают концентрации исследуемого вещества по выходным сигналам при эталонной температуре. Уравнение зависимости для эталонной температуры подвергается поправке для расчета концентраций исследуемого вещества в ответ на выходные сигналы при других температурах, таких как температура образца. Уравнение зависимости может быть для эталонной температуры в 25°С. Могут использоваться уравнения зависимости для других эталонных температур.
Уравнение зависимости может быть реализовано для манипулирования выходным сигналом ради определения концентрации исследуемого вещества. Уравнение зависимости также может быть реализовано в качестве таблицы назначения номера программы (PNA) крутизны и отсекаемого отрезка для уравнения зависимости, другой справочной таблицы, или тому подобного для сравнения с электрическим выходным сигналом, чтобы определять концентрацию исследуемого вещества.
Влияние температуры на уравнение зависимости или калибровочную характеристику является чувствительным к поведению диффузионной и ферментативной реакций во время окислительно-восстановительной реакции. Например, температура влияет на окисление и диффузию глюкозы в образце цельной крови. В дополнение температура влияет на диффузию оптически активных молекул.
Уравнения зависимости могут быть линейными или почти линейными и могут быть описаны полиномом второго порядка. В общем виде уравнение зависимости может быть представлено, как изложено ниже:
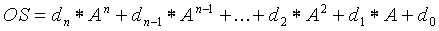 (1)
(1)
где А − концентрация исследуемого вещества, OS − входной сигнал, и коэффициенты dn, dn-1, d2, d1, d0 описывают температурно-зависимый весовой коэффициент для каждого члена характеристики биодатчика.
Уравнение зависимости может быть описано обратным выражением, где концентрация исследуемого вещества выражена в качестве функции выходного сигнала. Это снижает необходимость решать уравнение n го порядка, для того чтобы находить концентрацию исследуемого вещества. Таким образом, уравнение зависимости для концентрации исследуемого вещества может быть представлено, как изложено ниже:
 (2)
(2)
где cn, cn-1, c2 , c1, и c0 - коэффициенты, которые описывают температурно-зависимый весовой коэффициент для каждого члена характеристики биодатчика. Концентрация исследуемого вещества А может быть концентрацией глюкозы в образце цельной крови. Выходной сигнал может быть током или потенциалом электрохимической системы, спектральной поглощательной способностью или коэффициентом пропускания в процентах оптической системы, или тому подобным.
Уравнение зависимости между концентрацией исследуемого вещества и выходными сигналами может быть представлено характеристикой второго порядка, как изложено ниже:
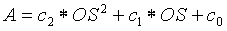 (3)
(3)
Уравнение зависимости может быть представлено линейной характеристикой между концентрацией исследуемого вещества и выходными сигналами, как изложено ниже:
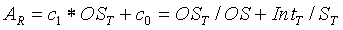 (4)
(4)
где c1=1/ST, c0=IntT/ST, и где AR − концентрация исследуемого вещества при эталонной температуре, OST − выходной сигнал, ST − произведение крутизны при эталонной температуре и нормированной температурной функции крутизны, а IntT − произведение отсекаемого отрезка при эталонной температуре и нормированной температурной функции отсекаемого отрезка.
Уравнение (4) может быть переписано для выражения выходного сигнала в ответ на концентрацию исследуемого вещества, как изложено ниже:
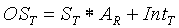 (5)
(5)
где OST − выходной сигнал при другой температуре, такой как температура образца, AR − концентрация исследуемого вещества при эталонной температуре, ST может быть выражено как произведение константы и нормированной температурной функции крутизны, а IntT может быть выражено как произведение константы и нормированной температурной функции отсекаемого отрезка.
Уравнение (5) указывает, что выходной сигнал OST является функцией температуры в показателях влияния температуры на крутизну ST и отсекаемый отрезок IntT при концентрации исследуемого вещества AR. Крутизна ST и отсекаемый отрезок IntT вводят поправку в крутизну и отсекаемый отрезок уравнения зависимости при эталонной температуре с использованием нормированных температурных функций крутизны и отсекаемого отрезка. Крутизна и отсекаемый отрезок с поправкой на температуру зависимости для эталонной температуры могут использоваться с выходным сигналом при другой температуре, такой как температура образца, чтобы рассчитывать концентрацию исследуемого вещества.
Соответственно уравнение (5) зависимости может быть переписано для расчета концентраций исследуемого вещества с использованием крутизны и отсекаемого отрезка с поправкой на температуру зависимости для эталонной температуры и выходных сигналов при другой температуре, как изложено ниже:
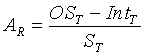 (6)
(6)
где AR − концентрация исследуемого вещества при эталонной температуре, OST − выходной сигнал при другой температуре, IntT − отсекаемый отрезок зависимости для эталонной температуры, подвергнутый поправке с помощью нормированной температурной функции для отсекаемого отрезка в ответ на другую температуру, и ST − крутизна зависимости для эталонной температуры, подвергнутая поправке с помощью нормированной температурной функции для крутизны в ответ на другую температуру.
Крутизна зависимости для эталонной температуры подвергается поправке в ответ на температуру образца, как изложено ниже:
 (7)
(7)
где SR − крутизна зависимости для эталонной температуры, а f(T) − температурная функция, которая вносит поправку в крутизну на температуру образца.
Температурная функция крутизны f(T) вносит поправку в крутизну зависимости для эталонной температуры до крутизны зависимости для другой температуры. Крутизна с поправкой на температуру может использоваться для расчета концентрации исследуемого вещества, или глюкозы с использованием выходного сигнала, или тока, вырабатываемого при другой температуре. Для построения температурной функции крутизны f(T) крутизна зависимостей для других температур нормируется по отношению к крутизне зависимости для эталонной температуры. Нормированная крутизна зависимости для конкретной температуры является безразмерным коэффициентом, который вносит поправку в крутизну зависимости для эталонной температуры до крутизны зависимости для конкретной температуры. Нормированная крутизна зависимости для эталонной температуры по существу является таковой, указывающей, что есть небольшая или никакая поправка по отношению к крутизне зависимости для эталонной температуры. Нормированная крутизна анализируется графически и/или математически, например, с помощью регрессивного анализа для построения температурной функции крутизны f(T). Еще один способ нормирования может использоваться для построения температурной функции.
Температурная функция крутизны f(T) может быть полиномом второго порядка, таким как изложено ниже:
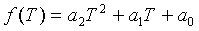 (8)
(8)
где Т − температура образца a2, a1 и a0 − коэффициенты регрессивного анализа, представляющие нормированную крутизну. Несмотря на то, что представлена в качестве полинома, температурная функция крутизны f(T) может быть представлена в качестве константы, экспоненциальной, тригонометрической или другой функции, их сочетания и тому подобного.
Отсекаемый отрезок зависимости для эталонной температуры подвергается поправке в ответ на температуру образца, как изложено ниже:
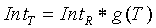 (9)
(9)
где IntP − отсекаемый отрезок зависимости для эталонной температуры, а g(T) − температурная функция, которая вносит поправку в отсекаемый отрезок для температуры образца.
Температурная функция отсекаемого отрезка g(T) вносит поправку в отсекаемый отрезок зависимости для эталонной температуры до отсекаемого отрезка зависимости для другой температуры. Отсекаемый отрезок с поправкой на температуру может использоваться для расчета концентрации исследуемого вещества, или глюкозы с использованием выходного сигнала, или тока, вырабатываемого при другой температуре. Для построения температурной функции отсекаемого отрезка g(T) отсекаемые отрезки зависимостей для других температур нормируют по отношению к отсекаемому отрезку зависимости для эталонной температуры. Нормированный отсекаемый отрезок зависимости для конкретной температуры является безразмерным коэффициентом, который вносит поправку в отсекаемый отрезок зависимости для эталонной температуры до отсекаемого отрезка зависимости для конкретной температуры. Нормированный отсекаемый отрезок зависимости для эталонной температуры по существу является таковым, указывающим, что есть небольшая или никакая поправка в отношении отсекаемого отрезка зависимости для эталонной температуры. Нормированные отсекаемые отрезки анализируются графически и/или математически, например, с помощью регрессивного анализа для построения температурной функции отсекаемого отрезка g(T). Еще один способ нормирования может использоваться для построения температурной функции.
Температурная функция отсекаемого отрезка g(T) может быть полиномом второго порядка, таким как следующий:
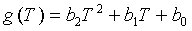 (10)
(10)
где Т − температура образца, а b2, b1, и b0 − коэффициенты регрессивного анализа, представляющие нормированные отсекаемые отрезки. Несмотря на то, что представлена в качестве полинома, температурная функция отсекаемого отрезка g(T) может быть представлена в качестве константы, экспоненциальной, тригонометрической или другой функции, их сочетания, и тому подобного.
На 108 по фиг. 1 концентрация исследуемого вещества из образца определяется по уравнению зависимости (6) с поправкой на температуру и выходному сигналу при температуре образца. Температурные функции крутизны и отсекаемого отрезка f(T) и g(T) вычисляются с использованием уравнений (8) и (10), соответственно. ST и IntT, крутизна и отсекаемый отрезок зависимости для эталонной температуры, подвергнутые поправке в ответ на температуру образца, вычисляются с использованием уравнений (7) и (9), соответственно.
На 110 по фиг. 1 концентрация исследуемого вещества, рассчитанная с использованием уравнения зависимости (6) с поправкой на температуру, и выходного сигнала при температуре образца может быть отображена или сохранена для будущего обращения.
Может анализироваться влияние изменений крутизны и отсекаемого отрезка на концентрацию исследуемого вещества по отношению к изменению температуры. Температурные коэффициенты определяют изменение параметра по отношению к изменению температуры. Для параметров, таких как концентрация исследуемого вещества, крутизна и отсекаемый отрезок, температурные коэффициенты могут определяться, как изложено ниже:
 (11)
(11)
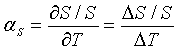 (12)
(12)
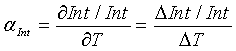 (13)
(13)
где αA, αS, и αInt − температурные коэффициенты концентрации исследуемого вещества, крутизны и отсекаемого отрезка, соответственно, А − концентрация исследуемого вещества, S − крутизна, Int − отсекаемый отрезок и Т - температура.
Для постоянного входного сигнала, такого как ток, относительное изменение концентрации исследуемого вещества A по отношению к изменениям крутизны S и отсекаемого отрезка Int может быть задано, как изложено ниже, с использованием уравнения (6) расчета концентрации исследуемого вещества, как изложено ниже:
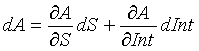 (14)
(14)
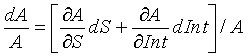 (15)
(15)
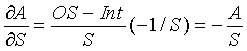 (16)
(16)
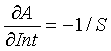 (17)
(17)
где OS − выходной сигнал, такой как ток.
Подстановка уравнений (16) и (17) в уравнение (15) дает следующие соотношения для относительного изменения концентрации исследуемого вещества, такого как глюкоза:
 (18)
(18)
 (19)
(19)
Подстановка температурных коэффициентов из уравнений (11)-(13) и обновление уравнения (19) дают следующие соотношения:
 (20)
(20)
 (21)
(21)
Уравнение (21) указывает, что влияние температурного коэффициента крутизны эквивалентно концентрации исследуемого вещества, но противоположно по величине. Однако влияние температурного коэффициента отсекаемого отрезка может быть меньшим по величине, в зависимости от крутизны, отсекаемого отрезка и измеряемой концентрации исследуемого вещества.
Для исследуемого вещества, такого как глюкоза в цельной крови, влияние изменений температурного коэффициента отсекаемого отрезка на температурный коэффициент глюкозы является небольшим при более высоких концентрациях глюкозы. Если отношением отсекаемого отрезка к крутизне Int/S является 50, а концентрацией глюкозы являются 150 мг/дл, только одна треть температурного коэффициента отсекаемого отрезка оказывает влияние на температурный коэффициент глюкозы (влияние температуры на температурный коэффициент концентрации глюкозы включает в себя только одну треть влияния температуры на температурный коэффициент отсекаемого отрезка). При более низких концентрациях глюкозы влияние температурного коэффициента отсекаемого отрезка на температурный коэффициент глюкозы более заметно. Если отношением отсекаемого отрезка к крутизне Int/S является 50, а концентрацией глюкозы являются 50 мг/дл, весь температурный коэффициент отсекаемого отрезка оказывает влияние на температурный коэффициент глюкозы (влияние температуры на температурный коэффициент концентрации глюкозы включает в себя все влияние температуры на температурный коэффициент отсекаемого отрезка). Меньшее отношение Int/S уменьшает влияние температурного коэффициента отсекаемого отрезка на температурный коэффициент глюкозы.
Фиг. 2 представляет способ для внесения поправки в зависимость между концентрациями исследуемого вещества и выходными сигналами при эталонной температуре в ответ на температуру. На 202 зависимости между концентрациями исследуемого вещества и выходными сигналами определяются для эталонной температуры и по меньшей мере одной другой температуры. На 204 строятся нормированные температурные функции крутизны и отсекаемого отрезка для зависимости при эталонной температуре. На 206 зависимость при эталонной температуре подвергается поправке в ответ на нормированные температурные функции крутизны и отсекаемого отрезка. Этот способ может использоваться со способом описанным в отношении фиг. 1, подобным способом или иным образом.
На 202 по фиг. 2 зависимости между концентрациями исследуемого вещества и выходными сигналами определяются для эталонной температуры и, по меньшей мере, одной другой температуры. Выходные сигналы могут вырабатываться электрохимической реакцией исследуемого вещества в образце, как обсуждалось ранее. Для каждой температуры выходные сигналы формируются экспериментально посредством электрохимических реакций при разных концентрациях исследуемого вещества. Экспериментальные результаты анализируются для построения зависимости между концентрациями исследуемого вещества и выходными сигналами для каждой температуры.
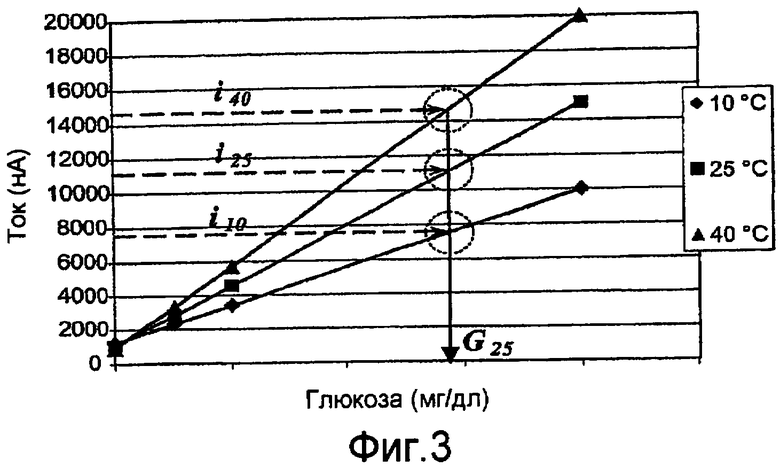
Фиг. 3 − график, иллюстрирующий зависимости между концентрациями исследуемого вещества и выходными сигналами. На этой иллюстрации каждый выходной сигнал является током, вырабатываемым из электрохимической реакции, такой как стробированная амперометрия. Концентрациями исследуемого вещества являются концентрации глюкозы в цельной крови. Зависимости между током и концентрациями глюкозы показаны графически для эталонной температуры в 25°C и двух других температур - 10 и 40°C. Несмотря на то, что зависимость при 25°C была выбрана в качестве эталонной температуры, зависимости при других температурах (в том числе не показанные) могут выбираться в качестве эталонной температуры. Несмотря на то, что иллюстрация направлена на конкретные признаки, такие как количество зависимостей, выходные сигналы, концентрации исследуемого вещества, температуры и тому подобное, иллюстрация не подразумевается ограничивающей объем, применение, реализацию или тому подобное.
Каждая из графических зависимостей является линейной и может быть представлена уравнением зависимости, имеющим общий вид, как изложенный ниже:
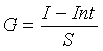 (22)
(22)
где G - концентрация глюкозы, I - ток, Int - точка пересечения линии зависимости с осью y, а S − крутизна линии зависимости. Несмотря на то, что линейные соотношения показаны для зависимостей между концентрацией глюкозы и током, другие зависимости могут иметь другие соотношения, такие как полиномиальное, экспоненциальное, тригонометрическое, их сочетание, и тому подобное.
На 204 по фиг. 2 строятся нормированные температурные функции крутизны и отсекаемого отрезка для зависимости при эталонной температуре. Температурные функции вносят поправку в крутизну и отсекаемый отрезок зависимости для эталонной температуры до крутизны и отсекаемого отрезка зависимости для другой температуры. Крутизна и отсекаемый отрезок с поправкой на температуру могут использоваться для расчета концентрации исследуемого вещества или глюкозы с использованием выходного сигнала или тока, вырабатываемого при другой температуре.
Для построения температурных функций крутизна и отсекаемые отрезки нормируются по отношению к крутизне и отсекаемому отрезку для эталонной температуры. Нормированная крутизна зависимости для конкретной температуры является безразмерным коэффициентом, который вносит поправку в крутизну зависимости для эталонной температуры до крутизны зависимости для конкретной температуры. Нормированный отсекаемый отрезок зависимости для конкретной температуры является безразмерным коэффициентом, который вносит поправку в отсекаемый отрезок зависимости для эталонной температуры до отсекаемого отрезка зависимости для конкретной температуры. Оба, нормированная крутизна и нормированный отсекаемый отрезок зависимости для эталонной температуры, по существу являются таковыми, указывающими, что есть небольшая или никакая поправка в отношении крутизны и отсекаемого отрезка зависимости для эталонной температуры. Могут использоваться другие способы нормирования.
Нормированная крутизна зависимостей может использоваться для построения температурной функции крутизны f(T) графически и/или математически с использованием регрессивного анализа или тому подобного. Температурная функция крутизны f(T) из регрессивного анализа может быть полиномом второго порядка, как изложено ниже:
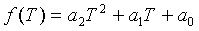 (23)
(23)
где Т − температура образца, а a2, a1 и a0 − коэффициенты регрессивного анализа, представляющие нормированную крутизну. Несмотря на то, что представлена в качестве полинома, регрессивный анализ может представлять температурную функцию крутизны f(T) в виде другой функции.
Нормированные отсекаемые отрезки зависимостей могут использоваться для построения температурной функции отсекаемого отрезка g(T) графически и/или математически, с использованием регрессивного анализа или тому подобного. Температурная функция отсекаемого отрезка g(T) из регрессивного анализа может быть полиномом второго порядка, таким как следующий:
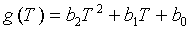 (24)
(24)
где Т − температура образца, а b2, b1, и b0 − коэффициенты регрессивного анализа, представляющие нормированные отсекаемые отрезки. Несмотря на то, что представлена в качестве полинома, регрессивный анализ может представлять температурную функцию отсекаемого отрезка g(T) в виде другой функции.
Фиг. 3 иллюстрирует, что зависимости между током и концентрациями глюкозы при 10, 25 и 40°C рассчитывают одинаковую концентрацию глюкозы G25 из токов i40, i25 и i10, которые вырабатываются электрохимическими реакциями исследуемого вещества в образце при таких соответственных температурах. Крутизна и отсекаемые отрезки зависимостей могут нормироваться по отношению к крутизне и отсекаемому отрезку зависимости для эталонной температуры 25 °C. Нормированные крутизна и отсекаемые отрезки зависимостей могут использоваться для построения температурной функции крутизны f(T) и температурной функции отсекаемого отрезка g(T).
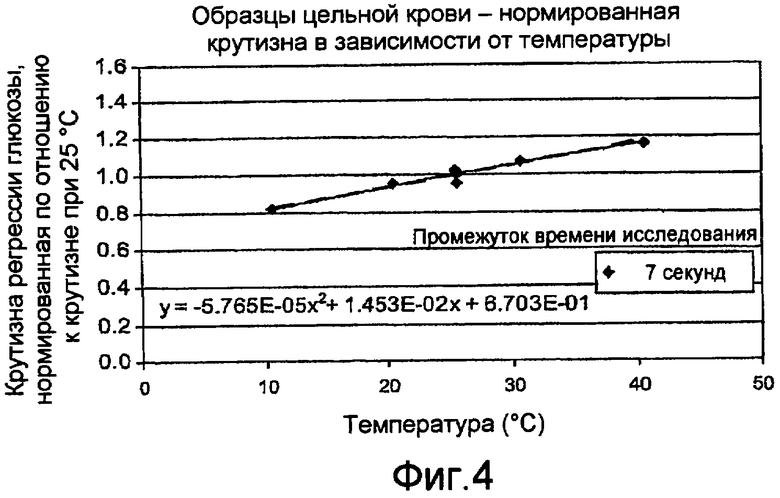
Фиг. 4 и 5 - графики, иллюстрирующие нормированные крутизну и отсекаемые отрезки, соответственно, в качестве функции температуры для зависимостей между концентрациями глюкозы в цельной крови и током. Зависимости формировались из электрохимических реакций с использованием стробированной амперометрии с промежутком времени исследования в 7 секунд (с). Нормированные крутизна и отсекаемые отрезки происходят из зависимостей при 10, 20, 25, 30 и 40°C. Нормированные крутизна и отсекаемые отрезки нормировались по отношению к крутизне и отсекаемому отрезку зависимости при эталонной температуре в 25°C. Несмотря на то, что эти иллюстрации направлены на конкретные признаки, такие как нормированная крутизна, температуры и тому подобное, иллюстрации не подразумеваются ограничивающими объем, применение, реализацию или тому подобное.
На фиг. 4 регрессивный анализ нормированной крутизны формирует температурную функцию крутизны f(T) как изложено ниже:
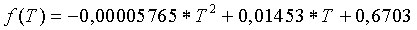 (25)
(25)
Температурная функция крутизны f(T), показанная в уравнении (25), может использоваться для внесения поправки в крутизну зависимости для эталонной температуры 25°C до крутизны зависимости для другой температуры, такой как температура образца. Т является другой температурой. Крутизна с поправкой на температуру может использоваться для расчета концентрации глюкозы с использованием тока, вырабатываемого при другой температуре. Могут использоваться другие температурные функции крутизны.
На фиг. 5 регрессивный анализ нормированных отсекаемых отрезков формирует температурную функцию отсекаемого отрезка g(T), как изложено ниже:
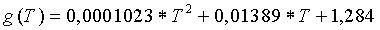 (26)
(26)
Температурная функция отсекаемого отрезка g(T), показанная в уравнении (26), может использоваться для внесения поправки в отсекаемый отрезок зависимости для эталонной температуры 25°C до отсекаемого отрезка зависимости для другой температуры, такой как температура образца. Т является другой температурой. Отсекаемый отрезок с поправкой на температуру может использоваться для расчета концентрации глюкозы с использованием тока, вырабатываемого при другой температуре. Могут использоваться другие температурные функции для отсекаемого отрезка.
Отдельные температурные функции для крутизны и отсекаемого отрезка могут использоваться с таблицей назначения номера программы (PNA) крутизны и отсекаемого отрезка зависимости для эталонной температуры. В дополнение, нормированные крутизна и отсекаемый отрезок дают диапазон, в котором собственные температурные свойства системы биодатчиков могут быть независимыми от выходного сигнала или величины тока, вырабатываемого электрохимической реакцией. Собственные температурные свойства обычно зависят от конструкции и изготовления пластинки датчика. Система биодатчиков может изменять температурные функции и/или уравнение(я) зависимости в ответ на используемый тип и партию пластинки датчика. Изменения температурной функции и уравнения зависимости могут производиться изменением таблицы PNA, когда используется другая или новая пластинка датчика.
Фиг. 6 и 7 - графики, иллюстрирующие нормированные крутизну и отсекаемые отрезки, соответственно, в качестве функции температуры для зависимостей между концентрациями глюкозы в цельной крови и током. Зависимости формировались из электрохимических реакций с использованием стробированной амперометрии с промежутком времени исследования в 5,5, 7, 8,5, 10, 11,5, 13 и 14,5 секунд. Нормированные крутизна и отсекаемые отрезки происходят из зависимостей при 10, 20, 25, 30 и 40°C. Нормированные крутизна и отсекаемые отрезки были нормированы по отношению к крутизне и отсекаемому отрезку зависимости при эталонной температуре 25°C. Несмотря на то, что эти иллюстрации направлены на конкретные признаки, такие как нормированная крутизна, температуры и тому подобное, иллюстрации не подразумеваются ограничивающими объем, применение, реализацию или тому подобное.
Фиг. 6 и 7 иллюстрируют нормированные крутизну и отсекаемые отрезки для электрохимических реакций, использующих стробированную амперометрию с многочисленными промежутками времени исследования. При определении температурных функций для нормированных крутизны и отсекаемых отрезков в электрохимических способах, основанных на многочисленных импульсах, есть многочисленные калибровочные точки в отдельных импульсах последовательности импульсов. Использованием токов, сформированных при разных температурах и разных промежутках времени исследования в разных импульсах, крутизна и отсекаемые отрезки по разным температурам могут быть нормированы по отношению к крутизне и отсекаемому отрезку при 25°C. Нормированные крутизна и отсекаемые отрезки могут быть представлены графически и/или математически в качестве функции температуры. Математическое представление может производиться посредством регрессивного анализа, который формирует полином второго порядка. В способах с многочисленными импульсами может быть много калибровочных точек в диапазоне промежутков времени, таком как от 5,5 с до 7, 8,5 и 10 с. В пределах этого диапазона собственное температурное свойство биодатчика должно быть устойчивым, если реактивы достаточно гидратированы.
На фиг. 6 температурные функции нормированной крутизны по существу перекрывают друг друга за исключением промежутка времени исследования в 5,5 секунд, которое отражает собственную устойчивость термочувствительности системы биодатчиков. В дополнение температурные функции нормированной крутизны вполне симметричны относительно эталонной температуры в 25°C. Нормированная крутизна при 10°C является примерно на 20% меньшей, чем нормированная крутизна при 25°C. Нормированная крутизна при 40°C является примерно на 20% большей, чем нормированная крутизна при 25°C.
На фиг. 7 температурные функции для нормированных отсекаемых отрезков очень похожи для промежутков времени исследования между 5,5 и 10 с. При более длительных промежутках времени влияние температуры на нормированный отсекаемый отрезок становится большим.
На 206 по фиг. 2 зависимость при эталонной температуре подвергается поправке в ответ на нормированные температурные функции крутизны и отсекаемого отрезка. Зависимость между концентрациями исследуемого вещества и выходными сигналами для эталонной температуры является следующей:
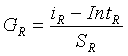 (27)
(27)
где GR - концентрация исследуемого вещества при эталонной температуре, iR - выходной сигнал при эталонной температуре, IntR - отсекаемый отрезок зависимости для эталонной температуры, а SR - крутизна зависимости для эталонной температуры.
Зависимость для эталонной температуры, представленная уравнением (27), может подвергаться поправке в ответ на температуру образца. Концентрации исследуемого вещества при эталонной температуре могут рассчитываться с использованием крутизны и отсекаемых отрезков зависимости с поправкой на температуру для эталонной температуры и выходных сигналов при температуре образца, как изложено ниже:
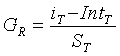 (28)
(28)
где GR - концентрация исследуемого вещества при эталонной температуре, iT - выходной сигнал при температуре образца, IntT - отсекаемый отрезок зависимости для эталонной температуры, подвергнутый поправке в ответ на температуру образца, и ST - крутизна зависимости для эталонной температуры, подвергнутая поправке для температуры образца.
Крутизна зависимости для эталонной температуры, подвергнутая поправке в ответ на температуру образца ST, может быть рассчитана, как изложено ниже:
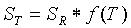 (29)
(29)
где SR − крутизна зависимости для эталонной температуры и f(T) − температурная функция, которая вносит поправку в крутизну для температуры образца.
Отсекаемый отрезок зависимости для эталонной температуры, подвергнутый поправке в ответ на температуру образца IntT, может рассчитываться, как изложено ниже:
 (30)
(30)
где IntR − отсекаемый отрезок зависимости для эталонной температуры, а g(T) − температурная функция, которая вносит поправку в отсекаемый отрезок для температуры образца.
Зависимость для эталонной температуры, подвергнутая поправке в ответ на температуру образца, как представлено уравнением (28), может быть переписана посредством подстановки уравнений (29) и (30) для ST и IntT, как изложено ниже:
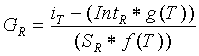 (31)
(31)
где GR - концентрация исследуемого вещества при эталонной температуре, iT - выходной сигнал при температуре образца, IntR - отсекаемый отрезок для зависимости при эталонной температуре, g(T) - нормированная температурная функция для отсекаемого отрезка, SR - крутизна для зависимости при эталонной температуре и f(T) - нормированная температурная функция для крутизны.
Зависимость для эталонной температуры, подвергнутая поправке в ответ на температуру образца, как представлено уравнением (31), может быть переписана для использования с примерами, проиллюстрированными на фиг. 3-5, как изложено ниже:
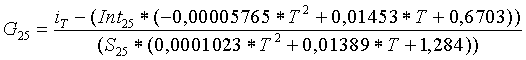 (32)
(32)
где G25 - концентрация исследуемого вещества при эталонной температуре в 25°C, iT - выходной сигнал при температуре образца, Int25 - отсекаемый отрезок зависимости для эталонной температуры в 25°C, S25 - крутизна зависимости для эталонной температуры в 25°C и T - температура образца.
Фиг. 8 и 9 - графики, иллюстрирующие значения систематической погрешности концентрации глюкозы от эталонной температуры в качестве функции температуры. Фиг. 8 - график, иллюстрирующий систематическую погрешность рассчитанных концентраций глюкозы без какой бы то ни было поправки на температуру. Фиг. 9 - график, иллюстрирующий систематическую погрешность рассчитанных концентраций глюкозы с поправкой на температуру, как описывалось ранее. Эти графики иллюстрируют систематическую погрешность в процентах концентрации от концентрации при эталонной температуре в 25°C для концентраций глюкозы плазмы в 56,9, 114,0 и 432,9 мг/дл в цельной крови. Анализ производился по электрохимическим реакциям с использованием стробированной амперометрии с промежутками времени исследования в 7 с, при температурах образца в 10, 20, 25, 30 и 40°C. Несмотря на то, что иллюстрации направлены на конкретные признаки, такие как температуры, концентрации глюкозы и тому подобное, иллюстрации не подразумеваются ограничивающими объем, применение, реализацию или тому подобное.
На фиг. 8 и 9 значения систематической погрешности в процентах при 10, 20 и 25°C для концентрации глюкозы 56,9 мг/дл показывают незначительное, если оно имеет место, изменение после поправки на температуру, особенно значение систематической погрешности в процентах при 10°C. Фиг. 8 указывает, что концентрации глюкозы по зависимости без температурной компенсации обычно имеют отрицательную систематическую погрешность при температурах ниже эталонной температуры в 25°C. Фиг. 8 также указывает, что концентрации глюкозы по зависимости без температурной поправки обычно имеют положительную систематическую погрешность при температурах выше эталонной температуры в 25°C. Фиг. 9 указывает, что значения систематической погрешности в процентах сходятся в более узкий диапазон, приблизительно +/- 5%, когда используются зависимости с температурной поправкой.
Функция температурного коэффициента любого конкретного параметра может использоваться, чтобы дополнительно показать внутреннюю устойчивость температурной функции для поправки уравнений зависимости между концентрациями исследуемого вещества и выходными сигналами. Температурный коэффициент (собственное свойство) выходного сигнала OS может быть определен, как изложено ниже:
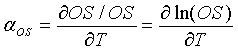 (33)
(33)
где αOS - температурный коэффициент выходного сигнала, OS - выходной сигнал, а Т - температура.
Фиг. 10 и 11 - графики, иллюстрирующие влияние на функцию температурного коэффициента уравнений зависимости с поправкой на температуру между концентрациями исследуемого вещества и выходными сигналами. Фиг. 10 иллюстрирует температурную функцию тока из датчика глюкозы с нормированными крутизной и отсекаемым отрезком. Фиг. 11 иллюстрирует функцию температурного коэффициента для нормированного тока по фиг. 10 относительно температуры. Нормированный ток и температурные коэффициенты (TempCo) имеют место в ответ на концентрации глюкозы в 50, 100, 200 мг/дл, 400 и 600 мг/дл. На фиг. 10 ток при 25°C должен быть равным значению глюкозы согласно уравнению (5) для нормированных крутизны и отсекаемого отрезка. Фиг. 11 указывает, что температурные коэффициенты являются функциями температуры - чем ниже температура, тем больше температурный коэффициент. В пределах диапазона температур от приблизительно 10°C до приблизительно 40°C температурный коэффициент находится в диапазоне от приблизительно 1,85%/°C до приблизительно 0,75%/°C. В дополнение функции температурных коэффициентов являются независимыми от концентрации глюкозы. Несмотря на то, что иллюстрации направлены на конкретные признаки, такие как температура, концентрации глюкозы, и тому подобное, иллюстрации не подразумеваются ограничивающими объем, применение, реализацию или тому подобное.
Фиг. 12 изображает схематическое представление биодатчика 1200, который определяет концентрацию исследуемого вещества в образце биологической жидкости. Биодатчик 1200 включает в себя измерительное устройство 1202 и пластинку 1204 датчика, которые могут быть реализованы в качестве настольного устройства, портативного или ручного устройства или тому подобного. Измерительное устройство 1202 и пластинка 1204 датчика могут быть приспособлены для реализации системы электрохимических датчиков, системы оптических датчиков, их сочетания или тому подобного. Биодатчик 1200 вносит поправку в зависимость для определения концентраций исследуемого вещества по выходным сигналам при одной температуре для определения концентраций исследуемого вещества по выходным сигналам при других температурах, таких как температура образца, как обсуждалось ранее. Зависимости с поправкой на температуру повышают точность и прецизионность биодатчика 1200 при определении концентрации исследуемого вещества из образца. Биодатчик 1200 может использоваться для определения концентраций исследуемого вещества, в том числе концентраций глюкозы, мочевой кислоты, лактата, холестерина, билирубина и тому подобного. Несмотря на то, что показана конкретная конфигурация, биодатчик 1200 может иметь другие конфигурации, в том числе конфигурации с дополнительными компонентами.
Пластинка 1204 датчика имеет основание 1206, которое образует резервуар 1208 и канал 1210 с проемом 1212. Резервуар 1208 и канал 1210 могут закрываться крышкой с вентиляционным отверстием. Резервуар 1208 определяет частично замкнутый объем (чашеобразную выемку). Резервуар 1208 может содержать структуру, которая способствует удержанию жидкого образца, такую как допускающие набухание в воде полимеры или пористые полимерные матрицы. Реактивы могут размещаться в резервуаре 1208 и/или канале 1210. Реактивы могут включать в себя один или более ферментов, связующих веществ, медиаторов и подобные препараты. Реактивы могут включать в себя химический индикатор для оптической системы. Пластинка 1204 датчика также может иметь область 1214 контакта с образцом, расположенную прилегающей к резервуару 1208. Область 1214 контакта с образцом может окружать резервуар 1208 частично или полностью. Пластинка1204 датчика может иметь другие конфигурации.
В системе оптических датчиков область 1214 контакта с образцом имеет оптический портал или щель для визирования образца. Оптический портал может быть покрыт по существу прозрачным материалом. Область контакта с образцом может иметь оптические порталы на противоположных сторонах резервуара 1208.
В электрохимической системе область 1214 контакта с образцом содержит проводники, присоединенные к рабочему электроду и противоэлектроду. Электроды могут находиться по существу в одной и той же плоскости. Электроды могут быть отделены более чем на 200 или 250 мкм и могут быть отделены от крышки по меньшей мере на 100 мкм. Электроды могут быть нанесены на поверхность основания 1206, которое образует резервуар 1208. Электроды могут тянуться или выступать в чашеобразную выемку, образованную резервуаром 1208. Слой диэлектрика может частично покрывать проводники и/или электроды. Область 1214 контакта с образцом может иметь другие электроды и проводники.
Измерительное устройство 1202 включает в себя электрическую схему 1216, присоединенную к интерфейсу 1218 датчика, и устройству 1220 отображения. Электрическая схема 1216 включает в себя процессор 1222, присоединенный к генератору 1224 сигналов, температурный датчик 1226 и запоминающий носитель 1228.
Генератор 1224 сигналов выдает электрический входной сигнал на интерфейс 1218 датчика в ответ на процессор 1222. В оптических системах электрический входной сигнал может использоваться для приведения в действие или управления детектором и источником света в интерфейсе 1218 датчика. В электрохимических системах электрический входной сигнал может передаваться интерфейсом 1218 датчика в область 1214 контакта с образцом, чтобы прикладывать электрический входной сигнал к образцу биологической жидкости. Входной сигнал может быть напряжением или током и может быть постоянным, переменным или их сочетанием, например, когда прикладывается сигнал переменного тока со смещением сигнала постоянного тока. Электрический входной сигнал может прикладываться в качестве одиночного импульса или многочисленными импульсами, последовательностями или циклами. Генератор 1224 сигналов также может записывать выходной сигнал из интерфейса датчика, как генератор-регистратор.
Температурный датчик 1226 определяет температуру образца в резервуаре пластинки 1204 датчика. Температура образца может измеряться, рассчитываться по выходному сигналу или предполагаться идентичной или подобной измерению температуры окружающей среды или температуры устройства, реализующего систему биодатчиков. Температура может измеряться с использованием термистора, термометра или другого термочувствительного устройства. Могут использоваться другие технологии для определения температуры образца.
Запоминающий носитель 1228 может быть магнитной, оптической или полупроводниковой памятью, другим машиночитаемым устройством хранения данных или тому подобным. Запоминающий носитель 1228 может быть стационарным устройством памяти или съемным устройством памяти, таким как карта памяти.
Процессор 1222 реализует анализ исследуемого вещества и обработку данных с использованием машиночитаемой машинной программы и данных, хранимых на запоминающем носителе 1228. Процессор 1222 может начинать анализ исследуемого вещества в ответ на присутствие пластинки 1204 датчика в интерфейсе 1218 датчика, нанесение образца на пластинку 1204 датчика в ответ на пользовательский ввод или тому подобное. Процессор 1222 управляет генератором 1224 сигналов, чтобы обеспечить электрический входной сигнал на интерфейс 1218 датчика. Процессор 1222 принимает температуру образца с температурного датчика 1226. Процессор 1222 принимает выходной сигнал из интерфейса 1218 датчика. Выходной сигнал формируется в ответ на окислительно-восстановительную реакцию исследуемого вещества в образце. Выходной сигнал может формироваться с использованием оптической системы, электрохимической системы или тому подобного. Процессор 1222 определяет концентрации исследуемого вещества по выходным сигналам при температуре образца с использованием уравнения зависимости для эталонной температуры с поправкой на температуру, как обсуждалось выше. Результаты анализа исследуемого вещества выводятся на устройство 1220 отображения и могут сохраняться на запоминающем носителе 1228.
Уравнения зависимости между концентрациями исследуемого вещества и выходными сигналами могут быть представлены графически, математически, их сочетанием или тому подобным. Уравнения зависимости могут быть представлены таблицей номера программы (PNA), другой справочной таблицей или тому подобным, которые хранятся на запоминающем носителе 1228. Команды касательно реализации анализа исследуемого вещества могут быть предусмотрены машиночитаемой машинной программой, хранимой на запоминающем носителе 1228. Эта программа может быть объектным кодом или любым другим кодом, описывающим или управляющим функциональными возможностями, описанными в материалах настоящей заявки. Данные от анализа исследуемого вещества могут быть подвергнуты одной или более обработкам данных, в том числе определению скоростей затухания, констант К, крутизны, отсекаемых отрезков и/или температуры образца, в процессоре 1222. В электрохимических системах интерфейс 1218 датчика имеет контакты, которые соединяют или поддерживают электрическую связь с проводниками в области 1214 контакта с образцом пластинки 1204 датчика. Интерфейс 1218 датчика передает электрический входной сигнал с генератора 1224 сигналов через контакты на соединители в области 1214 контакта с образцом. Интерфейс 1218 датчика также передает выходной сигнал с образца через контакты в процессор 1222 и/или генератор 1224 сигналов.
В оптических системах со светопоглощением и световозбуждением интерфейс 1208 датчика включает в себя детектор, который собирает и измеряет световое излучение. Детектор принимает свет с датчика жидкости через оптический портал в области 1214 контакта с образцом. В оптической системе со светопоглощением интерфейс 1208 датчика также включает в себя источник света, такой как лазер, светоизлучающий диод или тому подобное. Падающий пучок может иметь длину волны, подобранную для поглощения продуктом реакции. Интерфейс 1208 датчика направляет падающий пучок из источника света через оптический портал в область 1214 контакта с образцом. Детектор может быть расположен под углом, таким как 45°, к оптическому порталу, чтобы принимать свет, отраженный обратно с образца. Детектор может быть расположен прилегающим к оптическому порталу на другой стороне образца от источника света, чтобы принимать свет, пропущенный через образец.
Устройство 1220 отображения может быть аналоговым или цифровым. Устройство отображения может быть LCD (жидкокристаллическим) дисплеем, приспособленным для отображения числовых показаний.
В употреблении жидкий образец для анализа переносится в чашеобразную выемку, образованную резервуаром 1208, посредством введения жидкости в проем 1212. Жидкий образец протекает через канал 1210 в резервуар 1208, заполняя чашеобразную выемку наряду с вытеснением содержащегося ранее воздуха. Жидкий образец химически реагирует с реактивами, размещенными в канале 1210 и/или резервуаре 1208.
Пластинка 1202 датчика расположена прилегающей к измерительному устройству 1202. Прилегающее включает в себя положения, где область 1214 контакта с образцом находится в электрической и/или оптической связи с интерфейсом 1208 датчика. Электрическая связь включает в себя перенос входных и/или выходных сигналов между контактами в интерфейсе 1218 датчика и проводниками в области 1214 контакта с образцом. Оптическая связь включает в себя перенос светового излучения между оптическим порталом в области 1202 контакта с образцом и детектором в интерфейсе 1208 датчика. Оптическая связь также включает в себя перенос светового излучения между оптическим порталом в области 1202 контакта с образцом и источником светового излучения в интерфейсе 1208 датчика.
Процессор 1222 принимает температуру образца с температурного датчика 1226. Процессор 1222 управляет генератором 1224 сигналов для выдачи входного сигнала в интерфейс 1218 датчика. В оптической системе интерфейс 1218 датчика приводит в действие детектор и источник светового излучения в ответ на входной сигнал. В электрохимической системе интерфейс 1218 датчика выдает входной сигнал на образец через область контакта 1214 с образцом. Процессор 1222 принимает выходной сигнал, сформированный в ответ на окислительно-восстановительную реакцию исследуемого вещества в образце, как обсуждалось выше.
Процессор 1222 определяет концентрацию исследуемого вещества образца. Измерительное устройство вносит поправку в зависимость между концентрациями исследуемого вещества и выходными сигналами при эталонной температуре в ответ на температуру образца. Концентрация исследуемого вещества определяется по зависимости с поправкой на температуру и выходному сигналу при температуре образца. На 110 концентрация исследуемого вещества отображается и может сохраняться для будущего обращения.
Без ограничения объема, применения или реализации способы и системы, описанные ранее, могут быть реализованы с использованием следующего алгоритма:
Этап 1: Включить питание измерителя
Этап 2: Выполнить самотестирование биодатчика
Этап 3: Выполнить градуировку электроники биодатчика
Этап 4: Измерить температуру Т
Этап 5: Проверить диапазон температур
если (T>THi), то установить режим ошибки, «Температура слишком высока»
если (T<TLow), то установить режим ошибки, «Температура слишком низка»
Этап 6: приложить входной сигнал к образцу
Этап 7: измерить выходной сигнал, i
Этап 8: отыскать крутизну и отсекаемый отрезок в таблице назначения номера программы (PNA)
S=значение крутизны для тока
Int=отсекаемый отрезок для тока
Этап 9: внести поправку в крутизну и отсекаемый отрезок на влияние температуры.
ST=S * (a2*T1 2+a1*T1+a0)
IntT=Int * (b2*T1 2+b1*T1+b0)
Этап 10: вычислить концентрацию глюкозы при 25 °C
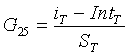
Этап 11: проверить на предельные уровни глюкозы
если (G25>Gmax), то установить режим ошибки, «Уровень глюкозы слишком высок»
Этап 12: отобразить результат
Таблица назначения номера программы (PNA), которая может использоваться в алгоритме, задана в таблице 1, приведенной ниже. Константы, которые могут использоваться в алгоритме, заданы в таблице 2, приведенной ниже. Могут использоваться другие таблицы PNA и/или константы.
Несмотря на то что были описаны различные варианты осуществления изобретения, специалистам в данной области техники будет очевидно, что возможны другие варианты осуществления и реализации в пределах объема изобретения.




Изобретение относится к измерительной технике и может быть использовано в медицине в различных диагностических целях. Заявлена система биодатчиков, определяющих концентрацию исследуемого вещества по выходному сигналу, вырабатываемому окислительно-восстановительной реакцией исследуемого вещества. Система биодатчиков вносит поправку в зависимость для определения концентраций исследуемого вещества по выходным сигналам при одной температуре для определения концентраций исследуемого вещества по выходным сигналам при другой температуре. Зависимость с поправкой на температуру между концентрациями исследуемого вещества и выходными сигналами при эталонной температуре может использоваться для определения концентраций исследуемого вещества по выходным сигналам при температуре образца. Технический результат: повышение точности определения концентрации исследуемого вещества. 3 н. и 26 з.п. ф-лы, 12 ил., 2 табл.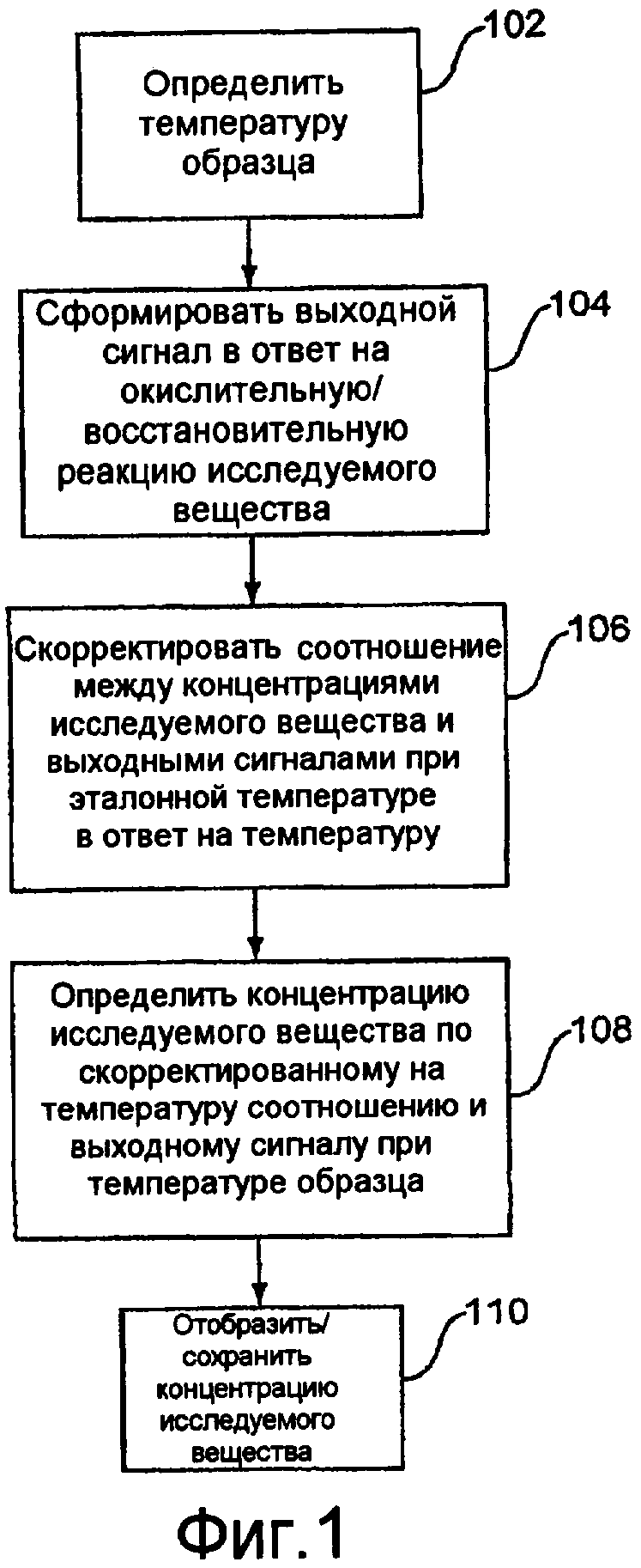
1. Способ определения концентрации исследуемого вещества в образце биологической жидкости, состоящий в том, что:
определяют температуру образца;
формируют выходной сигнал в ответ на окислительно-восстановительную реакцию исследуемого вещества в образце;
в ответ на температуру образца вносят поправку в зависимость между выходными сигналами при эталонной температуре и концентрациями исследуемого вещества, чтобы получить зависимость с поправкой на температуру между выходными сигналами при температуре образца и концентрациями исследуемого вещества; и
определяют концентрацию исследуемого вещества по зависимости с поправкой на температуру и выходному сигналу при температуре образца, при этом
зависимость с поправкой на температуру между концентрациями исследуемого вещества и выходными сигналами представлена следующим образом:
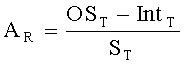 ,
,
где AR - концентрация исследуемого вещества при эталонной температуре,
OSт - выходной сигнал при температуре образца, IntR - отсекаемый отрезок, подвергнутый поправке нормированной температурной функцией для отсекаемого отрезка, и ST - крутизна, подвергнутая поправке нормированной температурной функцией для крутизны.
2. Способ по п.1, дополнительно состоящий в том, что вносят поправку в зависимость в ответ на нормированную температурную функцию крутизны и нормированную температурную функцию отсекаемого отрезка.
3. Способ по п.1, в котором нормированная температурная функция для крутизны содержит регрессивный анализ нормированной крутизны.
4. Способ по п.3, в котором нормированная температурная функция для крутизны, f(T), представлена следующим образом:
f(T)=a2T2+a1T+a0,
где Т - температура образца, а2, а1, и а0 - коэффициенты регрессивного анализа, представляющие нормированную крутизну.
5. Способ по п.1, в котором нормированная температурная функция для отсекаемого отрезка содержит регрессивный анализ нормированных отсекаемых отрезков.
6. Способ по п.5, в котором нормированная температурная функция для отсекаемого отрезка, g(T), представлена следующим образом:
g(T)=b2T2+b1T+b0,
где Т - температура образца, b2, b1 и b0 - коэффициенты регрессивного анализа, представляющие нормированные отсекаемые отрезки.
7. Способ по п.1, дополнительно состоящий в том, что выходной сигнал формируют в ответ на электрохимический процесс.
8. Способ по п.1, в котором выходной сигнал представляет собой свет.
9. Способ по п.1, в котором выходной сигнал представляет собой электрический сигнал.
10. Способ по п.1, дополнительно состоящий в том, что выходной сигнал формируют в ответ на импульсные входные сигналы.
11. Способ по п.1, в котором исследуемое вещество содержит глюкозу, а биологическая жидкость содержит цельную кровь.
12. Способ внесения поправки в зависимость между выходными сигналами при эталонной температуре и концентрациями исследуемого вещества в ответ на температуру, состоящий в том, что:
определяют зависимости между концентрациями исследуемого вещества и выходными сигналами для эталонной температуры и, по меньшей мере, одной другой температуры;
строят нормированные температурные функции крутизны и отсекаемого отрезка для зависимости эталонной температуры; и
вносят поправку в зависимость эталонной температуры в ответ на нормированные температурные функции крутизны и отсекаемого отрезка, при этом
зависимость эталонной температуры с поправкой на температуру представлена следующим образом:
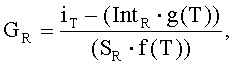
где GR - концентрация исследуемого вещества при эталонной температуре, iT - выходной сигнал при температуре образца, IntR - отсекаемый отрезок зависимости для эталонной температуры, g(T) - нормированная температурная функция для отсекаемого отрезка, SR - крутизна зависимости для эталонной температуры, и f(T) - нормированная температурная функция для крутизны.
13. Способ по п.12, в котором нормированная температурная функция для крутизны содержит регрессивный анализ нормированной крутизны.
14. Способ по п.13, в котором нормированная температурная функция для крутизны, f(T), представлена следующим образом:
f(T)=a2T2+a1T+a0,
где Т - температура образца, а2, а1 и а0 - коэффициенты регрессивного анализа, представляющие нормированную крутизну.
15. Способ по п.12, в котором нормированная температурная функция для отсекаемого отрезка содержит регрессивный анализ нормированных отсекаемых отрезков.
16. Способ по п.15, в котором нормированная температурная функция для отсекаемого отрезка, g(T), представлена следующим образом:
g(7)=b2T2+b1T+b0,
где Т - температура образца, b2, b1 и b0 - коэффициенты регрессивного анализа, представляющие нормированные отсекаемые отрезки.
17. Способ по п.12, в котором зависимость между концентрациями исследуемого вещества и выходными сигналами для эталонной температуры представлена следующим образом:
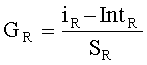 ,
,
где GR - концентрация исследуемого вещества при эталонной температуре, iR - выходной сигнал при эталонной температуре, IntR - отсекаемый отрезок зависимости для эталонной температуры, и SR - крутизна зависимости для эталонной температуры.
18. Способ по п.12, в котором выходные сигналы представляют собой свет.
19. Способ по п.12, в котором выходные сигналы представляют собой электрический сигнал.
20. Способ по п.12, дополнительно состоящий в том, что выходные сигналы формируют в ответ на импульсные входные сигналы.
21. Способ по п.12, в котором исследуемое вещество содержит глюкозу, а биологическая жидкость содержит цельную кровь.
22. Биодатчик для определения концентрации исследуемого вещества в биологической жидкости, содержащий:
измерительное устройство, содержащее процессор, присоединенный к интерфейсу датчика, и температурный датчик;
пластинку датчика, имеющую область контакта с образцом в основании, где область контакта с образцом является прилегающей к резервуару, образованному основанием;
при этом в ответ на температуру образца с температурного датчика процессор вносит поправку в зависимость между выходными сигналами при эталонной температуре и концентрациями исследуемого вещества, чтобы получить зависимость с поправкой на температуру между выходными сигналами при температуре образца и концентрациями исследуемого вещества, и
при этом процессор определяет концентрацию исследуемого вещества по зависимости с поправкой на температуру в ответ на выходной сигнал из области контакта с образцом,
при этом зависимость эталонной температуры с поправкой на температуру представлена следующим образом:
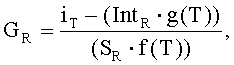
где GR - концентрация исследуемого вещества при эталонной температуре, iT - выходной сигнал при температуре образца, IntR - отсекаемый отрезок зависимости для эталонной температуры, g(T) - нормированная температурная функция для отсекаемого отрезка, SR - крутизна зависимости для эталонной температуры, и f(T) - нормированная температурная функция для крутизны.
23. Биодатчик по п.22, в котором процессор вносит поправку в зависимость в ответ на нормированную температурную функцию крутизны и нормированную температурную функцию отсекаемого отрезка.
24. Биодатчик по п.22, в котором нормированная температурная функция для крутизны, f(T), представлена следующим образом:
f(T)=a2T2+a1T+a0,
где Т - температура образца, а2, a1 и а0 - коэффициенты регрессивного анализа, представляющие нормированную крутизну.
25. Биодатчик по п.22, в котором нормированная температурная функция для отсекаемого отрезка, g(T), представлена следующим образом:
g(T)=b2T2+b1T+b0,
где Т - температура образца, b2, b1 и b0 - коэффициенты регрессивного анализа, представляющие нормированные отсекаемые отрезки.
26. Биодатчик по п.22, в котором выходной сигнал представляет собой свет.
27. Биодатчик по п.22, в котором выходной сигнал представляет собой электрический сигнал.
28. Биодатчик по п.22, в котором выходной сигнал чувствителен к импульсным входным сигналам.
29. Биодатчик по п.22, в котором исследуемое вещество содержит глюкозу, а биологическая жидкость содержит цельную кровь.
| US 6233471 В1, 15.05.2001 | |||
| US 4431004 А, 14.02.1984 | |||
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КИСЛОТНОСТИ (PH) МОЛОКА И МОЛОЧНЫХ ПРОДУКТОВ | 2000 |
|
RU2202784C2 |
Авторы
Даты
2012-07-20—Публикация
2007-02-23—Подача