Изобретение относится к прикладной электрохимии и может быть использовано для приготовления жидкого антиоксиданта, стимулирующего и нормализующего процессы в биологических объектах. В частности, оно может быть использовано в таких областях человеческой деятельности, как сельское хозяйство, животноводство и медицина.
Под жидкостями - антиоксидантами подразумеваются жидкости, у которых значения окислительно-восстановительного потенциала Eh при данных значениях водородного показателя pH сдвинуты в отрицательном направлении относительно значений Eh жидкостей, находящихся в равновесном состоянии с окружающей средой.
Под жидкостями - оксидантами (акцепторами электронов, окислителями) подразумеваются жидкости, у которых значения Eh при данных значениях pH сдвинуты в положительном направлении.
Следует отметить, что чем значительнее сдвинут редокс-потенциал жидкости в область отрицательных значений, тем более высокими антиоксидантными свойствами обладает жидкость.
Все жидкие среды человека, включая слюну, кровь, лимфу, мочу, желудочный сок, грудное молоко, так же как и свежеприготовленные соки овощей, фруктов и ягод, являются антиоксидантами. Организм молодых здоровых людей способен вырабатывать достаточное количество антиоксидантов, устраняющих избыток свободных радикалов, если молодые люди регулярно употребляют пищу и/или жидкости, являющиеся антиоксидантами. Регулярное употребление пищевых продуктов и жидкостей, не являющихся антиоксидантами, постепенно приводит к ухудшению здоровья молодых людей. При искусственном вскармливании ребенка грудного возраста молочными смесями (не являющимися антиоксидантами) проблемы со здоровьем у ребенка возникают вскоре после его рождения. К пищевым продуктам, не являющимися антиоксидантами, в частности, относятся вареное и жареное мясо, колбасы, кипяченое и пастеризованное молоко, минеральная вода, разлитая в бутылки и бутыли, соки и компоты, находящиеся в пакетах и банках.
Интенсивность окислительно-восстановительных реакций зависит от активности электронов в водных растворах, которая характеризуется величиной окислительно-восстановительного потенциала (ОВП), или, как его еще называют, редокс-потенциала (Eh), измеряемого в милливольтах. Чем выше ОВП, тем среда «кислее», тем больше она способна к разрушению межмолекулярных связей, к окислению молекул, и наоборот, чем ниже ОВП среды, тем выше ее восстановительная способность. И за то и за другое ответственна активность электронов, которые в случае высокого ОВП активно отбираются у молекулярных групп, а в случае низкого ОВП активно передаются, «навязываются» им, стимулируя соответствующие химические реакции.
ОВП внутренней среды организма здорового человека всегда меньше нуля и находится в пределах от минус 100 до минус 200 мВ. ОВП любой промышленно очищенной питьевой воды всегда больше нуля и составляет от +100 до +400 мВ.
Указанные различия ОВП внутренней среды организма человека и питьевой воды означают, что активность электронов во внутренней среде организма человека намного выше, чем активность электронов в питьевой воде. Когда обычная питьевая вода проникает в ткани человеческого (или иного) организма, она отнимает электроны от клеток и тканей, которые состоят из воды на (80-90)%. В результате этого биологические структуры организма (клеточные мембраны, органоиды клеток, нуклеиновые кислоты и другие) подвергаются окислительному разрушению. Так организм изнашивается, стареет, жизненно важные органы теряют постепенно свою функцию. Если поступающая в организм питьевая вода имеет ОВП близкий к значению ОВП внутренней среды организма человека, то электрическая энергия клеточных мембран (жизненная энергия организма) не расходуется на коррекцию активности электронов воды, и вода тотчас же усваивается, поскольку обладает биологической совместимостью по этому параметру. Если питьевая вода имеет более отрицательный ОВП, чем ОВП внутренней среды организма, то она подпитывает организм этой энергией, которая используется клетками как энергетический резерв антиоксидантной защиты организма от неблагоприятного влияния внешней среды.
Известен способ получения жидкого щелочного стимулятора-антиоксиданта из воды, обработку которой ведут в катодной камере диафрагменного электролизера до достижения католитом значения окислительно-восстановительного потенциала (редокс-потенциала) Eh в пределах (-150÷-800) мВ.
Недостатком такого стимулятора является то, что он имеет неоптимальное для большинства биологических объектов соотношение между значением водородного показателя pH и значением окислительно-восстановительного потенциала Eh.
Анолит антиоксидантными свойствами не обладает.
Наиболее близким к заявляемому способу получения жидкого стимулятора-антиоксиданта является способ изготовления стимулятора роста и развития растений путем проведения электролиза воды в диафрагменном электролизере в течение времени, необходимого для получения католита с pH (9,5÷11,0), и последующего смешивания полученного католита с частью или всем полученным анолитом [1].
Способ-прототип имеет ряд недостатков. Во-первых, оптимальное значение водородного показателя pH получаемого антиоксиданта-стимулятора имеет конкретное оптимальное значение, зависящее от того, для чего предполагается использовать получаемую смесь жидкого стимулятора-антиоксиданта. Например, если получаемая смесь жидкого стимулятора-антиоксиданта предназначается для стимуляции жизнедеятельности человека, то оптимальным значением водородного показателя в этом случае является значение pH, равное 8 [2]. Если смесь жидкого стимулятора-антиоксиданта предназначена для подкормки пчел, то его оптимальное значение водородного показателя pH равняется 9 [2].
Иными словами, приготовление жидкого стимулятора-антиоксиданта осуществляется в каждом конкретном случае по определенному рецепту, в зависимости от назначения жидкого стимулятора-антиоксиданта, причем в каждом рецепте оговаривается конкретное значение оптимальной величины pH.
Во-вторых, из способа-прототипа неясно, в каких соотношениях нужно смешать католит, имеющий значение водородного показателя, равное некоторой величине (pH)1, и анолит, имеющий значение водородного показателя (pH)2, для того, чтобы получить конкретную оптимальную величину (pH)* изготавливаемой смеси жидкого стимулятора-антиоксиданта, в соответствии с рецептом, обусловленным назначением приготавливаемого стимулятора-антиоксиданта. Для того чтобы способом-прототипом получить смесь из анолита и католита, с заданным конкретным значением водородного показателя (pH)*, величина которого лежит в диапазоне между измеренными значениями водородного показателя католита (pH)1, и измеренным значением водородного показателя анолита (pH)2, требуется провести многократные опыты, смешивая католит и анолит в разных соотношениях, и, используя метод последовательных итераций, постепенно приближаться к заданному значению водородного показателя смеси (pH)*.
В-третьих, способ-прототип не позволяет совместить требуемую по рецепту величину водородного показателя (pH)* с низким отрицательным значением редокс-потенциала, придающим получаемой смеси антиоксидантные свойства.
К недостаткам приготовления смеси по способу-прототипу следует отнести то, что для придания получаемой смеси антиоксидантных свойств необходимо, чтобы католит имел достаточно низкое отрицательное значение редокс-потенциала Eh, лежащее в диапазоне (-400÷-800) мВ. Такое значение редокс-потенциала можно получить только с использованием солевых растворов в специальных электролизерах, что существенно усложняет способ-прототип.
Кроме того, нужно, чтобы объем анолита, редокс-потенциал которого может достигать положительной величины, лежащей в диапазоне (1000÷1100) мВ, в приготавливаемой смеси был значительно меньше, чем объем католита в этой смеси. Однако при любых соотношениях смешиваемых объемов католита и анолита редокс-потенциал смеси всегда будет сдвинут в область более положительных значений относительно редокс-потенциала католита. То есть, жидкий стимулятор-антиоксидант, приготовленный по способу-прототипу, будет всегда обладать либо более низкими антиоксидантными свойствами, чем католит, либо вообще не будет обладать антиоксидантными свойствами.
Анолит является неравновесным окислителем (акцептором электронов), у которого при всех его значениях pH значение Eh отклонено относительно его равновесного значения в сторону больших положительных значений. Это сужает диапазон получаемых значений Eh смеси при каждом значении pH (снижает диапазон антиоксидантных свойств смеси). Необходимость иметь жидкости - антиоксиданты в широком диапазоне значений pH обусловлена разнообразием биологических объектов, а у каждого объекта - разнообразием его отдельных органов, в частности слизистых оболочек, в которых процессы протекают нормально при различных значениях pH. Так, одни растения предпочитают нейтральные почвы, другие - слабокислые или слабощелочные. Микробы лучше всего развиваются в диапазоне pH (7,0÷7,4). Для использования в косметологии лучше всего подходят жидкости, имеющие pH 5,5.
Целью заявляемого способа является повышение биологической эффективности приготовленного жидкого стимулятора-антиоксиданта и повышение точности его приготовления в соответствии с выбранным рецептом.
Поставленная цель достигается тем, что в способе получения жидкого стимулятора-антиоксиданта, включающем смешивание полученного из воды католита, имеющего значение водородного показателя в пределах (10÷11), с анолитом, имеющим значение водородного показателя в пределах (1,5÷6), предварительно измеряют значение водородного показателя (pH)1 католита и значение водородного показателя (pH)2 анолита. После измерения водородных показателей у анолита и католита задаются конкретным оптимальным значением водородного показателя (pH)* в соответствии с выбранным рецептом приготавливаемой смеси. Значение водородного показателя (pH)* должно лежать в диапазоне значений (pH)2≤(pH)*≤(pH)1. Для получения смеси с заданным оптимальным значением водородного показателя (pH)* смешивают католит и анолит между собой в объемном соотношении 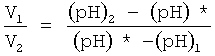 , где V1 - объем католита в смеси, V2 - объем анолита в смеси.
, где V1 - объем католита в смеси, V2 - объем анолита в смеси.
После процедуры смешивания католита и анолита у полученной смеси снижают редокс-потенциал в область отрицательных значений путем ее насыщения водородом. Для смещения редокс-потенциала в область отрицательных значений смесь разливают в герметичные сосуды и заполняют их водородом, пропуская водород через полученную смесь.
Сущность изобретения заключается в следующем. Смесь католита и анолита представляет собой статистическую двухкомпонентную смесь, которую можно описать при помощи уравнения Лихтенеккера-Ротера [3].
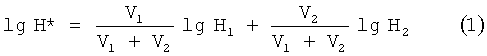
где Н* - концентрация ионов водорода в смеси католита и анолита; H1 - концентрация ионов водорода в католите; Н2 - концентрация ионов водорода в анолите; V1 - объем католита в статистической двухкомпонентной смеси; V2 - объем анолита в статистической двухкомпонентной смеси; (V1+V2) - суммарный объем смеси анолита и католита. Умножим левую и правую часть выражения (1) на величину - 1, получим
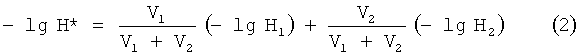
Учтем, что водородный показатель pH - величина, характеризующая концентрацию ионов водорода в растворе. Величина pH численно равна отрицательному десятичному логарифму концентрации ионов водорода в растворе pH=-lg[H+] [4]. -lgH*=(pH)* - водородный показатель смеси католита и анолита; -lgH1=(pH)1 - водородный показатель католита; -lgH2=(pH)2 - водородный показатель анолита.
С учетом введенных обозначений уравнение (2) можно переписать в виде
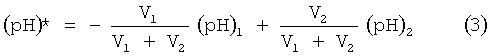
Из выражения (3) следует
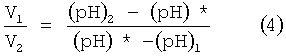
Таким образом, чтобы получить любое заданное, конкретное значение водородного показателя (pH)*, лежащее в диапазоне (pH)2≤(pH)*≤(pH)1 получаемой смеси из католита и анолита, имеющих значения водородного показателя (pH)1 и (pH)2 соответственно, необходимо смешать католит и анолит в объемных соотношениях, определяемых выражением (4).
Однако получение заданного оптимального значения смеси католита и анолита путем их смешивания в объемном соотношении, определяемом выражением (4), еще не означает того, что полученная смесь будет иметь свойства стимулятора-антиоксиданта. Для того чтобы полученная смесь приобрела свойства стимулятора-антиоксиданта, необходимо иметь соответствующее отрицательное значение редокс-потенциала Eh полученной смеси. Покажем это на конкретном примере.
Допустим, что в диафрагменном электролизере были получен католит, со значением водородного показателя (pH)1, равным 11, и редокс-потенциала (Eh)1=-800 мВ, и анолит, со значением водородного показателя (pH)1, равным 1,5, и редокс-потенциалом (Eh)2=+1100 мВ. Предположим, что заданное оптимальное значение водородного показателя получаемой смеси (pH)* равно 7,2. Тогда для получения значения смеси с водородным показателем (pH)*, равным 7,2, нужно смешать католит и анолит в соответствии с выражением (4), в следующем объемном соотношении
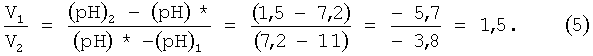
Из выражения (5) следует, что V1=1,5 V2. Иными словами, если объем V2 анолита равен 1000 мл, то объем католита должен быть равен 1500 мл. Только при таком соотношении объемов католита и анолита можно будет получить (pH)*, равное 7,2. Однако, если смешать в таком объемном соотношении католит и анолит, то редокс-потенциал, полученной смеси, сместится в область положительных значений, поскольку редокс-потенциал (Eh)1 католита равен минус 800 мВ, и редокс-потенциал (Eh)2 анолита равен плюс 1100 мВ, а вся смесь, несмотря на оптимальное значение водородного показателя (pH)*, будет иметь положительное значение редокс-потенциала, лежащее в диапазоне +(150÷250) мВ. Такая смесь не будет обладать стимулирующими антиоксидантными свойствами, а, наоборот, будет являться оксидантом. Поэтому, для того чтобы полученная смесь стала стимулятором-антиоксидантом, ей необходимо придать антиоксидантные свойства. Этого можно достичь только путем насыщения полученной смеси католита и анолита молекулярным водородом, пропуская его через полученную смесь.
Пример 1 конкретного выполнения. В катодной камере диафрагменного электролизера был получен католит. Измеренная величина (pH)1 католита была равна 11, а редокс-потенциал был равен (Eh)1=-800 мВ. В анодной камере диафрагменного электролизера был получен анолит. Измеренная величина (pH)2 анолита имела значение водородного показателя (pH)2, равного 1,5, и значение редокс-потенциал (Eh)2=+1100 мВ. Смесь должна была иметь оптимальное значение водородного показателя (pH)*, равного 7,4. Редокс-потенциал приготавливаемой смеси не должен был превышать минус 250 мВ.
Задаемся конкретным оптимальным значением водородного показателя (pH)* в соответствии с выбранным рецептом приготавливаемой смеси. Выбранное значение водородного показателя (pH)* получаемой смеси, должно лежать в диапазоне значений (pH)2≤(pH)*≤(pH)1. Для получения смеси с заданным значением водородного показателя (pH)*, равным 7,4, смешивали католит и анолит между собой в объемном соотношении, получаемом из выражения 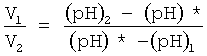 , где V1 - объем католита в смеси, V2 - объем анолита в смеси.
, где V1 - объем католита в смеси, V2 - объем анолита в смеси.
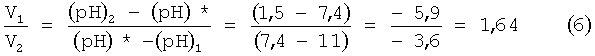
Из выражения (6) следует, что V1=1,64 V2. Иными словами, если объем V2 анолита равен 1000 мл, то объем католита должен быть равен 1640 мл. Только при таком соотношении объемов католита и анолита можно будет получить (pH)*, равное 7,4. Однако, если смешать в таком объемном соотношении католит и анолит, то редокс-потенциал полученной смеси сместится в область положительных значений, поскольку редокс-потенциал (Eh)1 католита равен минус 800 мВ, а редокс-потенциал (Eh)2 анолита равен плюс 1100 мВ, а вся смесь, несмотря на оптимальное значение водородного показателя, имела положительное значение редокс-потенциала (Eh)*=+150 мВ, и не обладала антиоксидантными стимулирующими свойствами, а, наоборот, являлась оксидантом. Поэтому полученной смеси следовало придать антиоксидантные свойства. Для придания таких свойств полученной смеси у нее снижали редокс-потенциал в область отрицательных значений, путем насыщения указанной смеси водородом. Для насыщения смеси водородом ее разливали в герметичные сосуды, после чего сосуды заполняли водородом, пропуская его через полученную смесь. Смесь заливали в герметичный стеклянный сосуд объемом 0,5 л.
Растворимость водорода составляет 1,78 мл в 100 мл воды при 20°С. В объеме 0,5 л растворится 8,9 мл водорода. Поэтому для получения воды, насыщенной водородом, в пол-литровый герметичный стеклянный сосуд следовало вводить не менее 9 мл водорода. Стеклянный герметичный сосуд заправляли водородом таким образом, чтобы над поверхностью воды оставался пузырек газа-водорода не менее 10 мл. После введения требуемого количества водорода выдерживали смесь в герметичном сосуде в течение некоторого времени, после чего заливали примерно 250 мл смеси в специальный сосуд для измерения редокс-потенциала (Eh)* испытываемой жидкой смеси католита и анолита. Редокс-потенциал (Eh)* измеряли хлорсеребряным и платиновым электродами. В процессе измерений, при погружении электродов в исследуемый раствор, показания измерительного прибора сначала уменьшались, достигали минимума, потом увеличивались. Время достижения минимального отсчета составляло, для разных растворов, от 1 до 30 минут. Увеличение отсчета редокс-потенциала происходило намного медленнее, чем его уменьшение.
Учитывалось, что собственный потенциал хлорсеребряного электрода относительно нормального водородного элемента (н.в.э.) согласно данным завода-изготовителя составлял +201 мВ для 3М раствора KCl при 20°С. За величину потенциала принимался минимальный отсчет милливольтметра. Отсюда на основе соотношения Eh=Е (мВ) + 201 мВ, где Е - потенциал, непосредственно измеренный прибором, получали значение Eh (потенциал относительно н.в.э.). Концентрация кислорода, растворенного в воде, определялась электродом Кларка. Все измерения проводились прибором «Эксперт-001» фирмы "Эконикс". Использовались стандартные хлорсеребряный и платиновый электрод.
Количество водорода, подаваемого в герметичный сосуд, составляло (40÷50) мл и контролировалось по величине газового пузырька над поверхностью воды, который занимал объем не менее 40 см3.
Минимальное время выдержки бутыли с водородом составляло 2 минуты. За это время устанавливалось значение редокс-потенциала (Eh)* на уровне минус 250 мВ. В течение часа редокс-потенциал (Eh)* уменьшался примерно до значения минус 350 мВ. Это значение практически не изменялось в течение (4÷5) часов. Затем через (12÷15) часов после введения водорода редокс-потенциал (Eh)* достигал значения около минус 450 мВ. При выдержке полученной смеси более 15 часов редокс-потенциал (Eh)* сохранялся на уровне минус 450 мВ.
Таким образом, приготовленная смесь по заявляемому способу имела заданное значение (pH)*, равное 7,4. Редокс-потенциал полученной смеси после выдержки ее в течение 2 минут был ниже минус 250 мВ. После выдержки смеси в течение (4÷5) часов ее редокс-потенциал стал меньше минус 350 мВ. После выдержки смеси в течение (12÷15) часов ее редокс-потенциал был равен минус 600 мВ. Таким образом, полученная смесь обладала стимулирующими антиоксидантными свойствами, которые после насыщения этой смеси увеличивались с течением времени.
Смесь, с заданной оптимальной величиной водородного показателя (pH)*, равной 7,4, по способу-прототипу приготавливалась в течение длительного времени. Это было обусловлено тем, что заданное значение водородного показателя смеси, равное 7,4, при значениях водородного показателя католита (pH)1=11 и водородного показателя анолита (pH)2=1,5 можно было получить только в процессе проведения многократных экспериментов, используя последовательное итерационное приближение к заданному значению (pH)*.
После того, как по способу-прототипу в результате многочисленных экспериментов была достигнута заданная оптимальная величина водородного показателя смеси (pH)*, равного 7,4, полученная смесь не обладала свойствами антиоксиданта, так как ее редокс-потенциал (Eh)* был равен плюс 150 мВ.
Пример 2 конкретного выполнения. В катодной камере диафрагменного электролизера был получен католит. Измеренная величина (pH)1 католита была равна 10 и редокс-потенциала (Eh)1=-800 мВ. В анодной камере диафрагменного электролизера был получен анолит. Измеренная величина (pH)2 анолита имела значение водородного показателя (pH)2, равного 1,5, и значение редокс-потенциала (Eh)2=+1100 мВ.
По данным работы [2] оптимальным стимулятором-антиоксидантом для человека является вода, которая должна иметь (pH)*=8; (Eh)*=(-250)-(350) мВ, ХСЭ (по показателям платинового электрода при хлорсеребряном электроде сравнения).
Смесь должна была иметь оптимальное значение водородного показателя (pH)*, равного 8. Редокс-потенциал приготавливаемой смеси не должен был превышать минус 250 мВ. Задаемся конкретным оптимальным значением водородного показателя (pH)* в соответствии с выбранным рецептом приготавливаемой смеси. Выбранное значение водородного показателя (pH)* приготавливаемой смеси лежит в диапазоне значений (pH)2≤(pH)*≤(pH)1. Для получения смеси с заданным значением водородного показателя (pH)*, равным 8, смешивали католит и анолит между собой в объемном соотношении 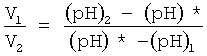 , где V1 - объем католита в смеси, V2 - объем анолита в смеси.
, где V1 - объем католита в смеси, V2 - объем анолита в смеси.
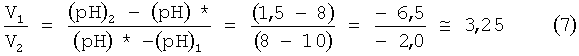
Из выражения (7) следует, что V1=3,25 V2. Иными словами, если объем V2 анолита равен 1000 мл, то объем католита должен быть равен 3250 мл. Только при таком соотношении объемов католита и анолита можно будет получить (pH)*, равное 8. Однако, если смешать в таком объемном соотношении католит и анолит, то редокс-потенциал полученной смеси сместится в область положительных значений, поскольку редокс-потенциал (Eh)1 католита равен минус 800 мВ, а редокс-потенциал (Eh)2 анолита равен плюс 1100 мВ, а вся смесь, несмотря на оптимальное значение водородного показателя, хотя и имела отрицательное значение редокс-потенциала (Eh)*=-180 мВ, но это значение было больше требуемой оптимальной рецептурной величины (Eh)*, которая должна была быть не выше величины минус 250 мВ. Поэтому у полученной смеси следовало усилить антиоксидантные свойства. Для достижения этой цели у полученной смеси снижали редокс-потенциал в область отрицательных значений путем насыщения указанной смеси водородом. Для этого смесь разливали в герметичные сосуды, которые заполняли водородом, пропуская его через полученную смесь. Смесь заливали в герметический стеклянный сосуд объемом 0,5 л.
Количество водорода составляло (40 - 50) мл и контролировалось по величине газового пузырька над поверхностью воды, который занимал не менее 40 см3.
Минимальное время выдержки бутыли с водородом составляло 2 минуты. За это время успевало установиться значение редокс-потенциала на уровне -350 мВ. В течение часа ОВП уменьшалось примерно до минус 500 мВ. Это значение практически не менялось в течение (4÷5) часов. Затем через (12÷15) часов после введения водорода редокс-потенциал достигал значения около минус 700 мВ. При хранении более 15 часов редокс-потенциал сохранялся на уровне минус 700 мВ.
Пример 3 конкретного выполнения. В катодной камере диафрагменного электролизера был получен католит. Измеренная величина (pH)1 католита была равна 9,5 и редокс-потенциала (Eh)1=-800 мВ. В анодной камере диафрагменного электролизера был получен анолит. Измеренная величина (pH)2 анолита имела значение водородного показателя (pH)2, равное 1,5, и редокс-потенциал (Eh)2=+1100 мВ.
Требовалось приготовить оптимальный стимулятор-антиоксидант для косметических целей. Стимулятор-антиоксидант для косметических целей должен был иметь (pH)*=5,5; (Eh)*=(-250)-(350)мВ, ХСЭ (по показателям платинового электрода при хлорсеребряном электроде сравнения).
То есть, иными словами, смесь должна была иметь оптимальное значение водородного показателя (pH)*, равного 5,5, а редокс-потенциал приготавливаемой смеси не должен был превышать минус 250 мВ.
Задаемся конкретным оптимальным значением водородного показателя (pH)* в соответствии с выбранным рецептом приготавливаемой смеси. Выбранное значение водородного показателя (pH)* приготавливаемой смеси должно было лежать в диапазоне значений (pH)2≤(pH)*≤(pH)1. Для получения смеси с заданным значением водородного показателя (pH)*, равным 8, смешивали католит и анолит между собой в объемном соотношении 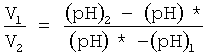 , где V1 - объем католита в смеси, V2 - объем анолита в смеси.
, где V1 - объем католита в смеси, V2 - объем анолита в смеси.
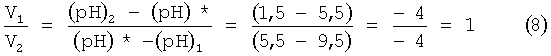
Из выражения (8) следует, что V1=V2. Иными словами, если объем V2 анолита равен 1000 мл, то объем католита должен быть равен 600 мл. Только при таком соотношении объемов католита и анолита можно будет получить (pH)*, равное 5,5. Однако, если смешать в таком объемном соотношении католит и анолит, то редокс-потенциал полученной смеси сместится в область положительных значений, поскольку редокс-потенциал (Eh)1 католита равен минус 800 мВ, а редокс-потенциал (Eh)2 анолита равен плюс 1100 мВ. Вся смесь, несмотря на оптимальное значение водородного показателя, принимала значение редокс-потенциала (Eh)*=+250 мВ. В связи с тем, что значение редокс-потенциала смеси (Eh)*=+250 мВ, она не обладала свойствами антиоксиданта, а наоборот, являлась оксидантом. Поэтому полученной смеси следовало придать антиоксидантные свойства. Для достижения этой цели у полученной смеси снижали редокс-потенциал в область отрицательных значений путем ее насыщения водородом. Для этого смесь разливали в герметичный сосуд, который заполняли водородом, пропуская его через полученную смесь. Объем герметичного стеклянного сосуда был равен 0,5 л.
Выполнив процедуры, аналогичные тем, что описаны в примере 1 конкретного выполнения, были получены следующие результаты.
При минимальном времени выдержки смеси в герметичном сосуде, заполненном водородом 2 минуты, значение редокс-потенциала успевало установиться на уровне минус 150 мВ. В течение часа редокс-потенциал уменьшался примерно до минус 300 мВ. Это значение практически не менялось в течение (4÷5) часов. Затем через (12÷15) часов после введения водорода ОВП достигало значения около минус 350 мВ. При хранении более 15 часов ОВП сохранялся на уровне минус 400 мВ.
Таким образом, приготовленная смесь по заявляемому способу имела заданное значение (pH)*, равное 5,5. Редокс-потенциал приготавливаемой смеси был ниже минус 150 мВ после выдержки смеси католита и анолита в течение 2 минут. После выдержки смеси в течение (4÷5) часов редокс-потенциал полученной смеси был меньше минус 300 мВ. После выдержки смеси в течение (12÷15) часов редокс-потенциал полученной смеси был равен минус 400 мВ. Таким образом, полученная смесь обладала стимулирующими антиоксидантными свойствами, которые после насыщения этой смеси водородом усиливались с течением времени.
Смесь с заданной оптимальной величиной водородного показателя (pH)*, равной 5,5, по способу-прототипу приготавливалась в течение длительного времени. Это было обусловлено тем, что заданное значение водородного показателя смеси, равное 5,5, при значениях водородного показателя католита (pH)1=9,5 и водородного показателя анолита (pH)2=1,5 можно было получить только многократными экспериментами, используя последовательное итерационное приближение к заданному значению (pH)*.
Кроме того, после того, как в результате многочисленных экспериментов была достигнута заданная оптимальная величина водородного показателя смеси (pH)*, равного 5,5, полученная смесь не обладала антиоксидантными свойствами, так как ее редокс-потенциал (Eh)* был равен плюс 250 мВ.
Таким образом, заявляемый способ получения стимулятора-антиоксиданта имеет следующие преимущества перед способом-прототипом:
- заявляемый способ позволяет получить конкретные, заданные в соответствии с рецептурой, оптимальные значения водородного показателя (pH)* и редокс-потенциала (Eh)* приготовляемого стимулятора-антиоксиданта, что не позволяет осуществить способ-прототип;
- заявляемый способ позволяет добиться повышения биологической эффективности приготовленного жидкого стимулятора-антиоксиданта и точности его приготовления в соответствии с выбранным рецептом, чего нельзя достичь способом-прототипом.
Источники информации
1. А.с. СССР №1574196, кл. A01N 59/00, заявл. 01.04.1986 г. Опубл. 30.06.1990 г. Бюл. №24 - прототип.
2. В.И.Прилуцкий, В.М.Бахир "Электрохимически активная вода: аномальные свойства, механизм биологического действия", Москва, ВНИИИМТ АО НПО "Экран", 1997 г.
3. Тареев Б.М. Физика диэлектрических материалов / М.: Энергия, 1973. - 328 с.
4. Политехнический словарь. Издательство «Советская энциклопедия» / М.: 1977, стр.83.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРИГОТОВЛЕНИЯ БИОЛОГИЧЕСКИ АКТИВНОГО ЛЬДА | 2010 |
|
RU2448309C2 |
| СПОСОБ ПОЛУЧЕНИЯ КАТОЛИТА-АНТИОКСИДАНТА И УСТРОЙСТВО ДЛЯ ЕГО РЕАЛИЗАЦИИ | 2010 |
|
RU2456246C2 |
| СПОСОБ ПРИГОТОВЛЕНИЯ БЕТОННОЙ СМЕСИ | 2011 |
|
RU2479525C2 |
| СПОСОБ ЛЕЧЕНИЯ ОСТРЫХ И ХРОНИЧЕСКИХ РАН | 2013 |
|
RU2555392C2 |
| Способ получения католитов-антиоксидантов электроактивированных водных растворов солей и их хранение | 2019 |
|
RU2712614C1 |
| СПОСОБ ПОЛУЧЕНИЯ АКТИВИРОВАННОЙ ВОДЫ | 2012 |
|
RU2524927C2 |
| Способ лечения больных артериальной гипертонией | 2016 |
|
RU2632619C1 |
| СПОСОБ ПРИГОТОВЛЕНИЯ БИОЛОГИЧЕСКИ АКТИВНОГО ЛЬДА | 2007 |
|
RU2357164C1 |
| СПОСОБ ПОЛУЧЕНИЯ АКТИВИРОВАННОЙ ВОДЫ | 2012 |
|
RU2515243C2 |
| ПРОТОЧНЫЙ ДИАФРАГМЕННЫЙ ЭЛЕКТРОЛИЗЕР | 2007 |
|
RU2375313C2 |
Изобретение относится к прикладной электрохимии и может быть использовано для приготовления жидкого антиоксиданта, стимулирующего и нормализующего процессы в биологических объектах. Из питьевой воды получают в катодной камере диафрагменного электролизера католит, имеющий значение водородного показателя (pH)1 в пределах 10-11, а в анодной камере - анолит, имеющий значение водородного показателя (рН)2 в пределах 1,5-6. Из католита и анолита, полученных в электролизере, приготавливают жидкий стимулятор - антиоксидант, для чего задаются конкретным оптимальным значением водородного показателя (рН)* смеси, лежащим в диапазоне значений от (pH)2≤(pH)*≤(pH)1. Для получения смеси с заданным значением водородного показателя (рН)* смешивают католит и анолит между собой в объемном соотношении 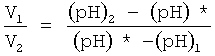 , где V1 - объем католита в смеси. V2 - объем анолита в смеси. У полученной смеси снижают редокс-потенциал в область отрицательных значений путем ее насыщения водородом. Для насыщения смеси водородом ее разливают в герметичные сосуды, заполняют указанные сосуды водородом, пропуская его через полученную смесь. Способ позволяет получить стимулятор-антиоксидант с конкретными, оптимальными значениями водородного показателя (рН)* и редокс-потенциала (Eh)*.
, где V1 - объем католита в смеси. V2 - объем анолита в смеси. У полученной смеси снижают редокс-потенциал в область отрицательных значений путем ее насыщения водородом. Для насыщения смеси водородом ее разливают в герметичные сосуды, заполняют указанные сосуды водородом, пропуская его через полученную смесь. Способ позволяет получить стимулятор-антиоксидант с конкретными, оптимальными значениями водородного показателя (рН)* и редокс-потенциала (Eh)*.
Способ получения жидкого стимулятора-антиоксиданта, включающий смешивание полученного из воды в катодной камере диафрагменного электролизера католита, имеющего значение водородного показателя рН в пределах (10÷11), с анолитом, полученным из воды в анодной камере диафрагменного электролизера, имеющим значение водородного показателя рН в пределах (1,5÷6), отличающийся тем, что измеряют значение водородного показателя (pH)1 у католита и значение водородного показателя (рН)2 у анолита, задаются конкретным, оптимальным значением водородного показателя (рН)* в соответствии с выбранным рецептом приготавливаемой смеси, лежащим в диапазоне значений от (pH)2≤(pH)*≤(pH)1, и для получения смеси с заданным значением водородного показателя (рН)* смешивают католит и анолит между собой в объемном соотношении 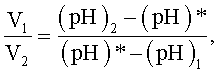 где V1 - объем католита в смеси, V2 - объем анолита в смеси, затем у полученной смеси снижают редокс-потенциал в область отрицательных значений путем ее насыщения водородом, для чего смесь разливают в герметичные сосуды, заполняют указанные сосуды водородом, пропуская его через полученную смесь.
где V1 - объем католита в смеси, V2 - объем анолита в смеси, затем у полученной смеси снижают редокс-потенциал в область отрицательных значений путем ее насыщения водородом, для чего смесь разливают в герметичные сосуды, заполняют указанные сосуды водородом, пропуская его через полученную смесь.
| Способ получения стимулятора роста и развития растений | 1986 |
|
SU1574196A1 |
| СПОСОБ СНИЖЕНИЯ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНОГО ПОТЕНЦИАЛА ВОДЫ | 2007 |
|
RU2351546C2 |
| RU 2004101402 A, 10.05.2005 | |||
| WO 2005058761 A1, 30.06.2005. | |||
Авторы
Даты
2012-02-10—Публикация
2010-04-23—Подача