Изобретение относится к медицине, а именно к реконструктивно-восстановительной и торакальной хирургии, и может найти применение при замещении циркулярных дефектов трахеи.
Оптимальным вариантом завершения циркулярной резекции трахеи является наложение трахеального анастомоза по типу «конец в конец». Однако у части больных это невыполнимо ввиду распространенного поражения трахеи как опухолевого, так и неопухолевого генеза, и невозможности создания прямого анастомоза после радикального удаления патологического участка, либо формирование трахеального анастомоза при таких условиях сопровождается высокой частотой несостоятельности [1].
Известны способы замещения циркулярных дефектов трахеи аллотрансплантатами (консервированная и не консервированная трахея, твердая мозговая оболочка, перикард, свежая и декальцинированная кость, фрагмент аорты и нижней полой вены и т.д.) [2]. Недостатками способов являются низкая биосовместимость аллотрансплантата с тканями и, как следствие, его лизирование и потеря каркасных свойств после операции. Возникающая воспалительная реакция тканей на трансплантат способствует избыточному формированию соединительнотканного регенерата, что может стать причиной стеноза и облитерации на уровне замещенного участка.
В качестве пластического материала для замещения циркулярных дефектов трахеи предлагались различные монолитные и пористые синтетические материалы (плексиглаз, стекло, ивалон, капрон, полиэтилен, хлорвинил, марлекс, дакрон, политетрафторэтилен и т.д.) [3, 4]. Недостатками способов являются недостаточная биохимическая и биомеханическая совместимость. Реакция тканей на них, как на инородное тело, способствует избыточному формированию соединительной ткани с развитием стеноза на уровне замещенного участка трахеи. Кроме того, синтетические материалы не устойчивы к инфекции и поддерживают воспаление в дыхательных путях, большинство из них обладают низкой интеграцией с тканями трахеи, в результате чего нередко развиваются несостоятельность анастомоза трахея-имплантат и трахеальные свищи, аррозивные кровотечения. Протезы из монолитного материала зачастую мигрируют и вызывают обтурацию дыхательных путей, пористые - недостаточно ригидные и не поддерживают просвет трахеи, через них просачивается воздух, что препятствует их применению для пластики грудного отдела трахеи в связи с угрозой развития напряженного пневмоторакса.
Известны способы замещения циркулярных дефектов трахеи танталовыми и стальными сетками, снаружи покрытыми аутофибрином, свободным кожным и фасциальным аутолоскутом [3]. Недостатки способов связаны с тем, что сетка непосредственно контактирует с просветом трахеи, вследствие чего инфицируется, формируя очаг хронического воспаления, что способствует бурному росту грануляционной ткани на металлической сетке и замедленной эпителизации. Поэтому эпителий, идущий с краев дефекта трахеи, не успевает выстлать значительную внутреннюю поверхность замещенного участка трахеи, что приводит к беспрепятственному росту грануляционной ткани в просвет трахеи с развитием стеноза трахеи. Кроме того, способы малоэффективны для замещения грудного отдела трахеи, т.к. первоначально ненадежно аэрогерметичны, либо становятся воздухопроницаемыми в раннем послеоперационном периоде, что приведет к жизнеугрожающему пневмомедиастинуму и напряженному пневмотораксу.
Известны способы замещения циркулярных дефектов трахеи сетчатыми протезами, проращенными аутотканью. В качестве таких протезов использовали синтетические материалы: сетку из марлекса, капрона, тефлона, которые предварительно имплантировали между кожей и фасцией бедра, под кожу спины, в грудинно-ключично-сосцевидную или прямую мышцу живота, большой сальник, а уже проросший соединительной тканью трансплантат использовали для замещения грудного и шейного отделов трахеи [3]. Недостатки способов связаны с недостаточной биосовместимостью этих синтетических материалов. В связи с чем, большинство из них обладают низкой интеграцией с тканями, что приводит к неравномерному и неконтролируемому формированию соединительнотканного регенерата на поверхности протеза. Кроме того, на внутренней поверхности протеза, проращенного аутотканью, отсутствует эпителиальная выстилка, препятствующая избыточному росту грануляционной ткани в просвет трахеи и развитию стеноза замещенного участка трахеи.
Наиболее перспективным ввиду биологической совместимости является применение аутотрансплантатов для замещения дефектов трахеи, обладающих необходимой ригидностью для поддержания просвета дыхательных путей и содержащих в своем составе внутреннюю эпителиальную выстилку, препятствующую разрастанию грануляций на уровне реконструированного участка и развитию стеноза в отдаленном послеоперационном периоде.
Известны способы замещения циркулярных дефектов трахеи аутотрансплантатами (мышечно-реберным и мышечно-надкостничным лоскутом, сегментом толстой и тонкой кишки, пищеводом, фрагментом аорты и полой вены, стенкой мочевого пузыря) [4, 5]. Однако эти аутотрансплантаты с эпителиальной выстилкой не обладают необходимой ригидностью для поддержания просвета дыхательных путей и адекватного дыхания. Кроме того, способы замещения дефектов трахеи стенкой пищевода, крупных сосудов, мочевого пузыря технически сложны в исполнении и связаны с высокой травматичностью, обусловленной забором этих аутотрансплантатов и необходимостью повреждения изначально интактных и важных анатомических структур, что потенциально может привести к их патологии, развитию жизнеугрожающих осложнений.
Наиболее близким к предлагаемому (прототипом) является способ замещения циркулярных дефектов трахеи марлексовым протезом, покрытым снаружи аутоперикардом, выбранный в качестве прототипа [6]. Недостатки способа связаны с недостаточной биохимической и биомеханической совместимостью укрепляющей сетки марлекс. Кроме того, длительно напрямую контактирующая с просветом трахеи и соответственно с внешней средой внутренняя поверхность сетчатого протеза является инфицированной, что существенно нарушает его интеграцию в тканях, сроки заживления и эпителизацию, способствует возникновению послеоперационных осложнений (несостоятельность анастомоза, трахеальные свищи, аррозия сосудов и т.д.) и снижает состоятельность операции.
Новая техническая задача - снижение послеоперационных осложнений и повышение состоятельности операции.
Для решения поставленной задачи в способе замещения циркулярных дефектов трахеи, включающем закрытие дефекта комбинированным трансплантатом, в который входят перикардиальный аутотрансплантат и сетчатый имплантат, предварительно для формирования комбинированного трансплантата на переднюю и/или боковую поверхность перикарда помещают сетчатый имплантат с размерами ячейки 200-500 мкм, сплетенный из сверхэластичной никелидотитановой нити диаметром 60-90 мкм, и фиксируют не проникающими в полость перикарда швами, после 3-4-недельного перерыва перикардиальный аутотрансплантат забирают в едином комплексе тканей с сетчатым имплантатом, далее, формируют из него прямоугольник, на противоположных краях которого разделяют между собой ткань перикарда и имплантат на протяжении 10-12 мм, выворачивают свободный край перикарда по направлению к поверхности сетчатого имплантата, получая дупликатуру, после чего, немобилизованные края комбинированного трансплантата совмещают, располагая серозную оболочку кнутри трансплантата, и со стороны сетчатого имплантата непрерывным обвивным швом ушивают так, что получают из него трубчатую структуру, соответствующую поперечным размерам просвета трахеи, при этом захватывают по торцам дупликатуру перикарда, комбинированный трансплантат анастомозируют с краями дефекта трахеи, свободные края сетчатого имплантата в составе комбинированного трансплантата фиксируют внеслизистыми швами к трахее.
Способ осуществляют следующим образом.
На иллюстрациях, поясняющих способ, представлено:
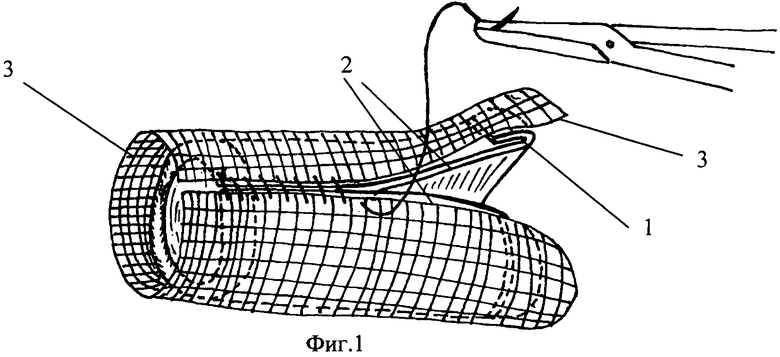
Фиг.1. - схема формирования трубчатого протеза из выкроенного комбинированного трансплантата.
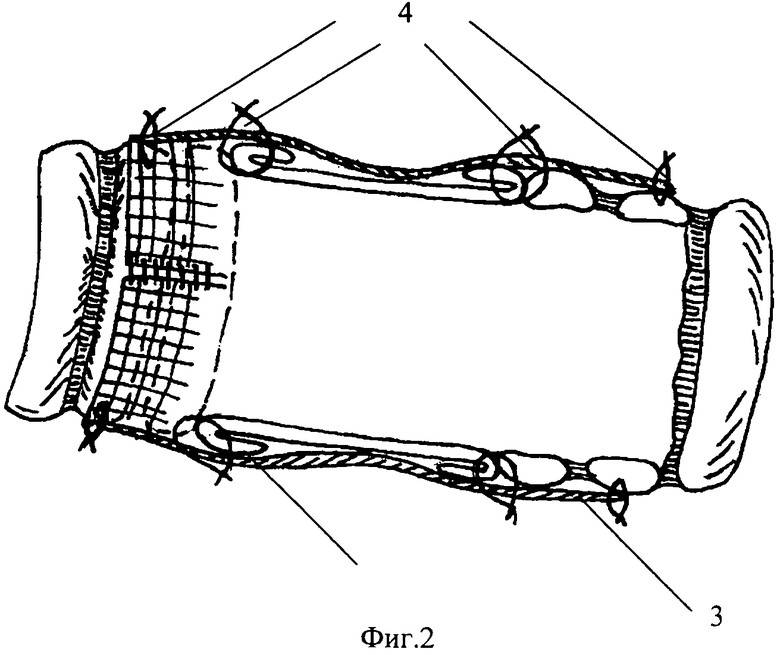
Фиг.2. - схема анастомоза между краем дефекта трахеи и комбинированным протезом,
где 1 - свободный край лоскута из перикарда в виде дупликатуры, 2 - не мобилизованные края протеза, сшиваемые непрерывным швом, 3 - свободный край сетчатого никелидотитанового имплантата, 4 - фиксирующие швы.
Предварительно до циркулярной резекции трахеи выполняют торакотомию, на переднюю и/или боковую поверхность наружной поверхности перикарда укладывают сетчатый имплантат с размерами ячейки 200-500 мкм, сплетенный из сверхэластичной никелидотитановой нити диаметром 60-90 мкм, и фиксируют не проникающими в полость перикарда швами. Для снижения травматичности этого этапа оперативного вмешательства можно использовать малоинвазивный торакоскопический и загрудинный внеплевральный через нижнюю грудную апертуру доступы, в том числе и видеоассистированные. Затем осуществляют реторакотомию, после 3-4-недельного перерыва комбинированный трансплантат, в который входит перикардиальный аутотрансплантат и сетчатый имплантат, забирают в едином комплексе тканей, далее, формируют из него прямоугольник, на противоположных краях которого разделяют между собой ткань перикарда и имплантат на протяжении 10-12 мм, выворачивают свободный край перикарда к поверхности сетчатого имплантата, получая дупликатуру (1), после чего, не мобилизованные края комбинированного трансплантата совмещают, располагая серозную оболочку кнутри, и со стороны сетчатого имплантата непрерывным обвивным швом ушивают так (2), что получают из него трубчатую структуру, соответствующую поперечным размерам просвета трахеи, при этом захватывают по торцам дупликатуру перикарда, комбинированный трансплантат анастомозируют с краями дефекта трахеи, свободные края сетчатого имплантата (3) в составе комбинированного трансплантата фиксируют внеслизистыми швами к трахее (4).
Новизна предлагаемого способа выполнения операции состоит в том, что в качестве армирующего материала используют биоадаптированный сетчатый имплантат на основе никелидотитановой нити и иного, по сравнению с прототипом, расположения объектов, замещающих дефект трахеи. В предлагаемом способе циркулярный дефект трахеи непосредственно замещается воздухонепроницаемым комбинированным трансплантатом, в состав которого входит аутотрансплантат с серозной выстилкой, обращенной в просвет трахеи, что придает протезу устойчивость к бактериальному обсеменению, тем самым, создаются оптимальные условия для заживления на уровне реконструированного участка трахеи. Этому способствует также расположение армирующей части в составе комбинированного протеза вне инфицированной области. Хотя и биосовместимый, но инородный по своей природе, никелидотитановый имплантат менее противостоит инфекции, чем собственные ткани организма, при его инфицировании значительно замедляются репаративные процессы в тканях. Пористая чешуйчатая поверхность никелидтитановой нити придает ей высокую адаптированность в тканях организма. Имплантат на основе никелидотитановой нити быстро и без образования капсулы интегрируется с окружающими тканями, формирует с ними единый тканевой комплекс, при этом, не изменяя структуру и свойства контактирующих с ним тканей. Образованный комплекс легко моделируется до трубчатой структуры. Сроки забора укрепленного перикарда после 3-4-недельного перерыва обусловлены тем, что к этому времени происходит заполнение пор нитей и ячеек сетчатого имплантата соединительнотканным регенератом и надежное сращение перикарда с имплантатом, а также купируется острый воспалительный процесс в ответ на имплантацию. Размер ячейки 200-500 мкм, толщина нити для плетения имплантата 60-90 мкм подобраны экспериментальным путем и являются оптимальными для создания каркаса и надежного фиксирования тканей. Сетчатая структура и общая толщина имплантата (не менее 120 мкм), предложенного нами, обеспечивает достаточную механическую устойчивость и при прорастании соединительной тканью не препятствует минимальной подвижности на замещенном участке трахеи, необходимой для адекватного трахеобронхиального дренажа и во время акта дыхания. Общая толщина имплантата не более 200 мкм не препятствует тесному контакту аутотрансплантата с окружающими тканями, облегчает сращение их между собой. Сетчатый имплантат на основе сверхэластичной никелидотитановой нити является хорошим пластическим материалом, позволяет легко и просто моделировать любую необходимую форму в имплантационной области. Комбинированный трансплантат с эпителиальной выстилкой представлен двумя воздухонепроницаемыми слоями: перикард и проращенный собственными тканями сетчатый никелидотитановый протез, что придает повышенную герметичность и ригидность протезу, а также возможность его использования в грудном отделе трахеи. Сформированный край перикардиального лоскута в виде дупликатуры и второй ряд швов вдали от первого увеличивают надежность анастомоза трахея-трансплантат. Кроме того, эластичные свойства трахеи и комплекса перикард-никелидотитановый сетчатый имплантат сходны, поэтому при «нагрузке-разгрузке» образованного сложного комплекса тканей деформация получается согласованной. Это снижает риск послеоперационных осложнений, повышает прочность соединения, обеспечивает анатомо-физиологическое восстановление данной области, тем самым повышает состоятельность операции.
Предлагаемое техническое решение не основано на известных специалисту рекомендациях, что свидетельствует о соответствии предложения авторами критериям патентоспособности «новизна» и «изобретательский уровень». Изобретение иллюстрируется схемами выполнения конкретных приемов и примерами отдельных операций в эксперименте.
Проверочным тестом достижимости технического результата является экспериментальная апробация предлагаемого способа замещения циркулярных дефектов шейного и грудного отдела трахеи на 6 беспородных собаках массой тела 8-14 кг. Эксперименты на животных выполнены в отделе экспериментальной хирургии Центральной научно-исследовательской лаборатории ГОУ ВПО СибГМУ г. Томска. Исследование проводили согласно этическим принципам, изложенным в "Европейской конвенции по защите позвоночных животных, используемых для экспериментальных и других научных целей", все манипуляции и выведение животных из опытов проводили под общей анестезией. В послеоперационном периоде проводилось клиническое наблюдение, лучевой и эндоскопический контроль, гистологическое исследование препаратов.
Пример 1 (беспородная собака массой тела 14 кг). После обработки операционного поля антисептиками под общей анестезией с управляемым дыханием выполнили торакотомию в 5 межреберье слева, для формирования комбинированного трансплантата на переднюю и боковую поверхности перикарда поместили и фиксировали сетчатый имплантат с размерами ячейки 500 мкм, сплетенный из сверхэластичной никелидотитановой нити диаметром 90 мкм, не проникающими в полость перикарда викриловыми швами. Плевральную полость дренировали. Операционную рану ушили послойно. После расправления легкого плевральный дренаж удалили. После 3-недельного перерыва осуществили реторакотомию слева, комбинированный трансплантат, в который входит перикардиальный аутотрансплантат и сетчатый имплантат, забрали в едином комплексе тканей, дефект перикарда пластически заместили сетчатым имплантатом из никелида титана. Затем осуществили цервикотомию, выполнили мобилизацию и циркулярную резекцию шейного отдела трахеи. С помощью ножниц сформировали из комбинированного трансплантата прямоугольник, на противоположных краях которого разделили между собой ткань перикарда и имплантата на протяжении 10-12 мм, вывернули свободные края перикарда к поверхности сетчатого имплантата, получая дупликатуру, после чего, не мобилизованные края комбинированного трансплантата совместили на никелидотитановом цилиндре с гладкой наружной поверхностью, выступающем в качестве формопридающей модели, располагая серозную оболочку кнутри, и со стороны сетчатого имплантата непрерывным обвивным швом ушили так, что получили из него трубчатую структуру (комбинированный протез трубчатой формы), соответствующую поперечным размерам шейного отдела трахеи, при этом захватывали по торцам дупликатуру перикарда. В дефект шейного отдела трахеи поместили комбинированный трансплантат трубчатой формы и анастомозировали его с краями дефекта, свободные края сетчатого имплантата в составе комбинированного трансплантата фиксировали внеслизистыми викриловыми швами к трахее. Плевральную полость дренировали. Операционные раны ушили послойно. После расправления легкого плевральный дренаж удалили. Комбинированный трансплантат прижился. Нарушений дыхания не наблюдалось.
Пример 2 (беспородная собака массой тела 12 кг). После обработки операционного поля антисептиками под общей анестезией с управляемым дыханием выполнили торакотомию в 4 межреберье справа, для формирования комбинированного трансплантата на переднюю и боковую поверхности перикарда поместили и фиксировали сетчатый имплантат с размерами ячейки 200 мкм, сплетенный из сверхэластичной никелидотитановой нити диаметром 60 мкм, не проникающими в полость перикарда викриловыми швами. Плевральную полость дренировали. Операционную рану ушили послойно. После расправления легкого плевральный дренаж удалили. После 4-недельного перерыва осуществили реторакотомию справа, комбинированный трансплантат, в который входит перикардиальный аутотрансплантат и сетчатый имплантат, забрали в едином комплексе тканей, дефект перикарда пластически заместили сетчатым имплантатом из никелида титана. С помощью ножниц сформировали из комбинированного аутотрансплантата прямоугольник, на противоположных краях которого разделили между собой перикард и имплантат на протяжении 10-12 мм, вывернули свободный край перикарда к поверхности сетчатого имплантата, получая дупликатуру, после чего, не мобилизованные края комбинированного трансплантата совместили на 10 мл одноразовом шприце, выступающем в качестве формопридающей модели, располагая серозную оболочку кнутри, и со стороны сетчатого имплантата непрерывным обвивным швом ушили так, что получили из него трубчатую структуру, соответствующую поперечным размерам грудного отдела трахеи, при этом захватывали по торцам дупликатуру перикарда. Далее, перевязали и пересекли непарную вену, выполнили мобилизацию и в условиях шунт-дыхания циркулярную резекцию грудного отдела трахеи. В дефект поместили комбинированный трансплантат трубчатой формы и анастомозировали его с краями дефекта трахеи, свободные края сетчатого имплантата в составе комбинированного трансплантата фиксировали внеслизистыми викриловыми швами к трахее. Плевральную полость дренировали. Операционную рану ушили послойно. После расправления легкого плевральный дренаж удалили. Комбинированный трансплантат прижился. Нарушений дыхания не наблюдалось.
Результаты экспериментальной апробации подтверждают работоспособность предлагаемого способа и достижимость технического результата. Готовность операции к клиническому применению свидетельствует о соответствии предложения критерию «промышленно применимо».
Таким образом, предлагаемый способ позволяет снизить послеоперационные осложнения и повысить состоятельность операции.
Источники информации
1. Аничкин В.В., Карпицкий А.С., Оладько А.А. Трахеобронхопластические операции. Витебск, 1996. С.106.
2. Амиров Ф.Ф. Пластические операции на трахее и бронхах. Т.: Госмедиздат УзССР, 1962.С.89-116.
3. Аничкин В.В., Карпицкий А.С., Оладько А.А. Трахеобронхопластические операции. Витебск, 1996. С.107-140.
4. Grillo H.C. Tracheal replacement: a critical review // Ann. Thorac. Surg. - 2002. - V.73. - P.1995-2004.
5. Амиров Ф.Ф. Пластические операции на трахее и бронхах. Т.: Госмедиздат УзССР, 1962. C.116-123.
6. Аничкин В.В., Карпицкий А.С., Оладько А.А. Трахеобронхопластические операции. Витебск, 1996. С.121 (прототип).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПЛАСТИЧЕСКОГО ЗАМЕЩЕНИЯ ДЕФЕКТА ПЕРИКАРДА | 2009 |
|
RU2400152C1 |
| СПОСОБ ЗАМЕЩЕНИЯ ПРОТЯЖЕННОГО ЦИРКУЛЯРНОГО ДЕФЕКТА ТРАХЕИ | 2011 |
|
RU2449740C1 |
| СПОСОБ ПЛАСТИКИ ОБШИРНЫХ ДЕФЕКТОВ ДИАФРАГМЫ | 2009 |
|
RU2400153C1 |
| СПОСОБ ЗАМЕЩЕНИЯ ОКОНЧАТЫХ ДЕФЕКТОВ ТРАХЕИ И ГОРТАНИ | 2010 |
|
RU2440789C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ТРАХЕОПИЩЕВОДНЫХ СВИЩЕЙ НЕОПУХОЛЕВОГО ГЕНЕЗА | 2010 |
|
RU2421161C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ЭКСПИРАТОРНОГО СТЕНОЗА ТРАХЕИ И ГЛАВНЫХ БРОНХОВ | 2009 |
|
RU2376949C1 |
| СПОСОБ ОБРАБОТКИ КУЛЬТИ ГЛАВНОГО БРОНХА | 2004 |
|
RU2271155C2 |
| СПОСОБ ЗАМЕЩЕНИЯ ЦИРКУЛЯРНЫХ ДЕФЕКТОВ ТРАХЕИ | 2014 |
|
RU2556855C1 |
| СПОСОБ УКРЫТИЯ ОБШИРНЫХ ОКОНЧАТЫХ ТОРАКОАБДОМИНАЛЬНЫХ ДЕФЕКТОВ | 2015 |
|
RU2600849C1 |
| СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ РУБЦОВЫХ СТЕНОЗОВ ГОРТАНИ И ТРАХЕИ | 2009 |
|
RU2388477C1 |
Изобретение относится к области медицины, а именно к реконструктивно-восстановительной и торакальной хирургии, и может найти применение при замещении циркулярных дефектов трахеи. Способ включает закрытие дефекта комбинированным трансплантатом, который состоит из перикардиального аутотрансплантата и сетчатого имплантата. При этом, предварительно для формирования комбинированного трансплантата на переднюю и/или боковую поверхность перикарда помещают сетчатый имплантат с размерами ячейки 200-500 мкм, сплетенный из сверхэластичной никелидотитановой нити диаметром 60-90 мкм. Его фиксируют не проникающими в полость перикарда швами. После 3-4-недельного перерыва перикардиальный аутотрансплантат забирают в едином комплексе тканей с сетчатым имплантатом. Далее формируют из него прямоугольник, на противоположных краях которого разделяют между собой ткань перикарда и имплантат на протяжении 10-12 мм. Выворачивают свободный край перикарда по направлению к поверхности сетчатого имплантата, получая дупликатуру. После этого, немобилизованные края комбинированного трансплантата совмещают, располагая серозную оболочку кнутри трансплантата. Затем со стороны сетчатого имплантата непрерывным обвивным швом ушивают так, что получают из него трубчатую структуру, соответствующую поперечным размерам просвета трахеи. Захватывают по торцам дупликатуру перикарда. Комбинированный трансплантат анастомозируют с краями дефекта трахеи. Свободные края сетчатого имплантата в составе комбинированного трансплантата фиксируют внеслизистыми швами к трахее. Использование данного изобретения позволяет снизить сроки заживления, операционного риска и повысить состоятельность операции. 2 пр., 2 ил.
Способ замещения циркулярных дефектов трахеи, включающий закрытие дефекта комбинированным трансплантатом, в который входят перикардиальный аутотрансплантат и сетчатый имплантат, отличающийся тем, что предварительно для формирования комбинированного трансплантата на переднюю и/или боковую поверхность перикарда помещают сетчатый имплантат с размерами ячейки 200-500 мкм, сплетенный из сверхэластичной никелидотитановой нити диаметром 60-90 мкм, и фиксируют не проникающими в полость перикарда швами, после 3-4-недельного перерыва перикардиальный аутотрансплантат забирают в едином комплексе тканей с сетчатым имплантатом, далее формируют из него прямоугольник, на противоположных краях которого разделяют между собой ткань перикарда и имплантат на протяжении 10-12 мм, выворачивают свободный край перикарда по направлению к поверхности сетчатого имплантата, получая дупликатуру, после чего немобилизованные края комбинированного трансплантата совмещают, располагая серозную оболочку кнутри трансплантата, и со стороны сетчатого имплантата непрерывным обвивным швом ушивают так, что получают из него трубчатую структуру, соответствующую поперечным размерам просвета трахеи, при этом захватывают по торцам дупликатуру перикарда, комбинированный трансплантат анастомозируют с краями дефекта трахеи, свободные края сетчатого имплантата в составе комбинированного трансплантата фиксируют внеслизистыми швами к трахее.
| АНИЧКИН В.В | |||
| и др | |||
| Трахеобронхопластические операции | |||
| - Витебск, 1996, с.121 | |||
| СПОСОБ ЛЕЧЕНИЯ РУБЦОВЫХ СТЕНОЗОВ ТРАХЕИ | 2005 |
|
RU2302829C1 |
| СПОСОБ ФОРМИРОВАНИЯ АУТОТРАНСПЛАНТАТА | 2009 |
|
RU2398529C2 |
| ЛОПУХИН Ю.М | |||
| Экспериментальная хирургия | |||
| - М.: Медицина, 1971, с.140-141 | |||
| АМИРОВ Ф.Ф | |||
| и др | |||
| Аллопластика трахеи и бронхов (Эксперимент | |||
| Исследование) | |||
| - Ташкент: Медицина, 1973, с.64-85 | |||
| OKUMUS A | |||
| et al. | |||
Авторы
Даты
2012-03-20—Публикация
2010-11-25—Подача