Область техники
Настоящее изобретение относится к фитоэстрогенам и их получению, а также к фармацевтическим композициям и пищевым добавкам, которые включают такие фитоэстрогены.
Уровень техники
Хмель (Humulus Lupulus L.) применяли веками в качестве основного сырья для пивоварения, которое придавало пиву горьковатый вкус и особый запах. В последние несколько лет это растение привлекло к себе повышенное внимание в качестве источника пренилфлавоноидов, подкласса флавоноидов, содержащих неполярную пренильную боковую цепь, связанную с одним из фенольных колец. Они присутствуют в лупулиновых железах, обнаруженных в основании брактеолей шишек хмеля женского растения. Из этих пренилфлавоноидов наибольшее внимание сейчас привлекают два халкона (ксантогумол (Х) и дезметилксантогумол (DMX)) и три флавонона (изоксантогумол (IX), 8-пренилнарингенин (8-PN) и 6-пренилнарингенин (6-PN)) (Фиг.2) благодаря их потенциальным оздоровительным свойствам. Х идентифицировали как сильный противораковый агент, тогда как для 8-PN было показано, что он является одним из наиболее сильнодействующих фитоэстрогенов, идентифицированных до настоящего времени, со значительно более высокой активностью, чем у хорошо известных соевых фитоэстрогенов. Было продемонстрировано, что 8-PN in vivo проявляет эстрогенную активность, предупреждая потерю костной массы у крыс, ингибируя ангиогенез и метастазирование, а также было показано, что 8-PN проявляет антиандрогенную активность.
Х присутствует в качестве доминирующего пренилхалкона в женских хмелевых шишках в концентрации до 1% (вес./вес.), тогда как DMX присутствует в более низких концентрациях (De Keukeleire et al. (2003) J. of Agric. and Food Chem. 51, 4436-4441). Соотношение X/DMX различается у разных сортов хмеля. Путем изомеризации Х трансформируется в IX, и DMX превращается в 8-PN и 6-PN.
Эстрогенные эффекты хмеля были обнаружены в последние десятилетия. Хмелевые ванны применяли для лечения гинекологических заболеваний, а у женщин, собиравших хмель, часто наблюдались менструальные нарушения. В 1999 году Milligan et al. [J. Clin. Endocrinol. Metab. 84, 2249-2252] идентифицировали новый фитоэстроген хмеля, 8-пренилнарингенин. Хотя он гораздо слабее, чем 17β-эстрадиол (<1%), он является одним из наиболее сильнодействующих фитоэстрогенов, идентифицированных до настоящего времени, со значительно большей активностью, чем у других фитоэстрогенов, полученных из сои, таких как соединения генистеин и даидзеин.
Обсуждалось, действительно ли воздействие эстрогенов из пищи и/или окружающей среды представляет собой фактор риска для здоровья, такой как эндокринное нарушение. В случае хмелевых пренилфлавоноидов пиво является их главным пищевым источником. В Соединенных Штатах в 2001 году среднее потребление пива на человека составило по расчетам примерно 225 мл пива в день (USDA, 2003). Когда предположили, что если бы такое количество потреблялось в виде самого распространенного в США бренда легкого пильзенского пива (500-1000 мкг пренилфлавоноидов/л пива), то ежедневное потребление пренилфлавоноидов составило бы около 0,14 мг. Однако обнаруженные в пиве концентрации (и, таким образом, среднее потребление) сильно зависят от процесса пивоварения, так крепкие сорта пива содержат до 4 мг пренилфлавоноидов/л. Хотя Х представляет собой доминирующий пренилфлавоноид, присутствующий в хмеле (0,1-1% от сухого веса), большая его часть трансформируется в IX путем термической изомеризации в процессе пивоварения. Таким образом, IX является самым распространенным пренилфлавоноидом, обнаруженным в пиве, и присутствует в концентрациях от 500 мкг/л (легкого пильзенского пива) до 4 мг/л (крепкого пива). Подобным образом, DMX превращается в 8-PN, достигая конечных концентраций в пиве до 100 мкг 8-PN/Л. Но, несмотря на высокую активность 8-PN, общая эстрогенная активность в пиве остается в 500-1000 раз меньше, чем концентрация, представляющая опасность с точки зрения in vivo активности (~100 мг/л) (Milligan et al. (2002) Reproduction 123, 235-242). Кроме того, многие сорта пива готовят сейчас с применением экстрактов хмеля вместо цельного хмеля, что обеспечивает пониженные концентрации 8-PN или его полное отсутствие. Таким образом, в основном это согласуется с тем, что, основываясь на современных знаниях, никакие вредные для здоровья эффекты не могут быть обусловлены фитоэстрогенами при среднем потреблении пива.
С другой стороны, сейчас многие данные соотносят преднамеренное потребление фитоэстрогена с возможной пользой для здоровья (Magee & Rowland (2004) Br. J. Nutr. 91, 513-531). Кроме пива, продаются пищевые добавки на основе хмеля с заявлением таких эффектов, как увеличение груди или уменьшение приливов. Все воздействия фитоэстрогенов на здоровье потенциально являются результатом действия комбинации многих индивидуальных фитохимикатов с разнообразными и, возможно, аддитивными или противодействующими активностями. До настоящего момента только изофлавоны и лигнаны считали значимыми фитоэстрогенами в питании человека, особенно потому что концентрации в пиве 8-PN считали слишком низкими для положительных или отрицательных воздействий на здоровье.
Несколько патентных публикаций описывают благотворные воздействия на здоровье пищевых флавоноидов, например, применение IX для предупреждения понижения плотности костной ткани (WO04089359), применение экстрактов хмеля в лекарственных средствах, имеющих эстрогенные свойства (WO02085393), и применение IX или X в пищевых продуктах с заявлением противовоспалительных или антивозрастных свойств (патент WO03090555). Кроме того, также предлагалось применение 8-PN в косметических средствах для ухода за кожей (СА2426467).
Для того чтобы in vivo осуществить воздействия, выявленные in vitro, пищевые флавоноиды должны всосаться из кишечника и достичь своих мишеней без изменений. В основном мономерные флавоноиды проходят без модификаций через желудок в тонкий кишечник, где может происходить всасывание из кишечника в мезентериальную кровеносную систему. Исследования in vitro выявили при всасывании существенную биотрансформацию X в печени (Yilmazer et al. (2001a) FEBS Lett. 491, 252-256) и 8-PN (Nicolic et al. (2004) Drug Metabolism and Disposition 32, 272-279). Однако степень пищевого всасывания полифенолов в тонком кишечнике довольно ограниченная (10-20%), таким образом, предполагается, что большая часть флавоноидов достигает толстой кишки. Нарингенин, не пренилированный аналог 8-PN, продемонстрировал интенсивную микробную биотрансформацию в кишечнике, включая расщепление кольца и дегидроксилирование (Rechner et al. (2004) Free Radic. Biol. Med. 36, 212-225) с последующим всасыванием и мочевыделением. Мало известно о кишечных трансформациях пренилфлавоноидов. Nookandeh et al. (2004) Phytochemistry 65, 561-570, вводили Х крысам по 1000 мг/кг веса тела и выделили 22 метаболита из фекалий. Однако большую часть (89%) из полученных флавоноидов представлял собой не измененный Х. Оставшаяся фракция состояла из малых количеств различных метаболитов, включая некоторое количество IX. Avula et al. (2004) [J. Chromatogr. Sci. 42:378-382] осуществили подобный эксперимент с крысами и обнаружили преимущественно не измененный Х, а также некоторое количество не идентифицированных метаболитов.
Возможность того, что IX может действовать как проэстроген, предположили Coldham et al. (2002) Food Addit. Contam. 19:1138-1147. Предположение было основано на способности печени к разносторонней биотрансформации, которая включает деметилирование. Однако воздействие на IX микросом печени не приводило к увеличению эстрогенной активности, из чего заключили, что 8-PN не производился. Напротив, Nicolic et al. описывают, что микросомы печени могут деметилировать IX, но не X (Nicolic et al. (2005) J. of Mass Spectrom. 40, 289-299). Однако было показано, что кроме деметилирования микросомы также модифицируют боковую пренильную цепь с получением, в конечном счете, большого разнообразия минорных продуктов деградации. Schaefer et al. (2003) (J. Steroid Biochem. Mol. Biol. 84, 359-360) идентифицировали низкий уровень 8-PN в моче двух тестируемых субъектов после перорального потребления IX, и связали этот факт с деметилированием в печени.
Кроме печени, толстая кишка человека также является важным местом трансформации веществ в теле человека. Толстая кишка содержит ~1012 микроорганизмов/см3 (около 400 различных видов) с огромным каталитическим и гидролитическим потенциалом. Важность этого микробного сообщества в метаболизме фитоэстрогенов в основном хорошо изучена. Wang et al. (2000) Chem. Pharm. Bull. 48, 1606-1610, идентифицировали два вида бактерий, ответственных за трансформацию лигнанов, и Decroos et al. (2005) Arch. Microbiol. 183, 45-55, недавно выделили микробный консорциум, способный к трансформации соевого фитоэстрогена даидзеина в эквол. Кроме того, было показано, что биодоступность фитоэстрогенов усиливают некоторые кишечные бактерии, так как они содержат β-глюкозидазы, которые необходимы для гидролиза гликозидов фитоэстрогенов (Rowland et al. (2003) Br. J. Nutr 89, s45-S58). Таким образом, предполагается, что микробиота кишечника является важным фактором для биодоступности фитоэстрогенов (Turner et al. (2003) Nutr. Rev. 61, 204-213).
Так как экономический интерес представляют только присутствующие в женских хмелевых шишках эфирное масло и альфа-кислоты, как важные ингредиенты пивоварения, то были разработаны различные методы экстракции хмеля с целью специфически экстрагировать только эти соединения. С одной стороны, СО2 в настоящий момент является наиболее общепринятым растворителем при производстве экстрактов хмеля (Palmer & Ting (1995) Food Chem. 52, 345-352). По сравнению со способами, в которых применяют традиционные органические растворители (этанол, гексан, метанол или метилен хлорид), СО2-экстракция обеспечивает более селективные экстракты, которые при производстве пива могут применяться в качестве хорошей альтернативы цельному хмелю или хмелевым гранулам. СО2-экстракты образуют основу для большого числа дополнительно выделенных и очищенных продуктов, таких как изо-альфа-кислоты и восстановленные производные. Другой способ для дополнительной очистки СО2-экстрактов путем удаления нежелательных пренилфлавоноидов описан в патенте US3794744.
С другой стороны, различные способы были разработаны для специфического получения и очистки пренилфлавоноидов (главным образом Х). Примеры этих способов экстракции описаны в патенте US 4121040 и в немецком патенте DE19939350. Применяя эти процессы, можно было легко получить ксантогумол, поэтому проявлялся небольшой интерес к разработке способа химического синтеза Х. Однако 8-PN гораздо труднее получить из натуральных экстрактов из-за его низких концентраций, присутствующих в хмелевой шишке. Таким образом, были разработаны стратегии синтеза, чтобы получить 8-PN путем пренилирования коммерчески доступного нарингенина. Сначала 8-PN получили из нарингенина или из флороацетофенона путем малопродуктивного не селективного прямого С-пренилирования. Эффективный мелкомасштабный синтез был выполнен с помощью перегруппировки Кляйзена, катализируемой европием(III) (Gester et al. (2001) Tetrahedron 57, 1015-1018). Недавно в европейском патенте EP1524269 была описана продукция в промышленном масштабе, основанная на этом способе.
Несмотря на всестороннее промышленное применение хмеля и экстрактов хмеля, не существует эффективного способа получения из натурального источника биоактивных пренилированных фитоэстрогенов, таких как 8-PN.
Сущность изобретения
Целью настоящего изобретения является предложение эффективного способа продукции биоактивных пренилированных фитоэстрогенов, таких как 8-PN, из 5-алкоксифлавоноидов, которые могут быть получены из натурального источника, а также предложение фармацевтических композиций и пищевых добавок, в которых используют такие биоактивные пренилированные фитоэстрогены.
В первом аспекте в настоящем изобретении предлагаются композиции, имеющие 5-алкоксифлавоноид-трансферазную (5-AO-FT) и/или 6'-алкоксихалкон-трансферазную (6'-AO-CT) активность. Более конкретно, в изобретении предлагаются композиции, имеющие 5-метоксифлавоноид-трансферазную (5-MO-FMT) и/или 6'-метоксихалкон-трансферазную (6'-MO-CMT) активность. Следующее воплощение настоящего изобретения относится к композициям, способным деалкилировать пренилированные 5-алкоксифлавоноиды и/или пренилированные 6'-алкоксихалконы. В конкретном воплощении настоящего изобретения предлагаются композиции, способные деалкилировать 6'-алкоксихалкон ксантогумол (Х) и/или 5-алкоксифлавоноид изоксантогумол (IX). Таким образом, композиции по настоящему изобретению способны к продукции биоактивных фитоэстрогенов, более конкретно пренилированных фитоэстрогенов, более конкретно 8-PN.
Согласно конкретному воплощению композиции, имеющие 5-алкоксифлавоноид- и/или 6'-алкоксихалкон деалкилирующую активность, представляют собой композиции, включающие или полученные из материала не животного происхождения, более конкретно прокариотического происхождения. Более конкретно композиции по настоящему изобретению включают бактериальные клетки или экстракты, супернатант или другой очищенный или частично очищенный материал таких бактериальных клеток. Конкретное воплощение настоящего изобретения относится к композиции, включающей гомоацетогенную бактерию, такую как Eubacterium sp. или Peptostreptococcus sp., более конкретно Eubacterium limosum или Peptostreptococcus productus или их экстракты, супернатант или другой очищенный или частично очищенный материал на их основе.
Другое конкретное воплощение изобретения включает бактериальные штаммы и/или композиции, включающие клетки, их экстракты, супернатант или другой очищенный или частично очищенный материал на их основе, с помощью которого обогащали продукцию 5-алкоксифлавоноид-трансферазной (5-AO-FT) и/или 6'-алкоксихалкон-трансферазной (6'-AO-CT) активности, более конкретно с помощью повторных инкубаций с 5-алкоксифлавоноидом, таким как 5-метоксипренилфлавоноид.
Еще одно конкретное воплощение изобретения включает композиции, включающие 5-метокси(пренил)флавоноид метилтрансферазу и/или 6'-метокси(пренил)халкон метилтрансферазу из гомоацетогенного бактериального штамма, более конкретно из Eubacterium sp., и еще более конкретно из Eubacterium limosum.
Конкретное воплощение композиций по настоящему изобретению относится к композициям, включающим обогащенную активность 5-алкоксифлавоноид трансферазы (5-AO-FT) и/или 6'-алкоксихалкон трансферазы (6'-AO-CT), полученной из бактериального штамма Eubacterium limosum, депонированного в Бельгийских Координированных коллекциях Микроорганизмов (BCCM) в BCCM/LMG коллекции под депозитным номером LMG P-23546.
В следующем аспекте в настоящем изобретении предлагаются способы продукции фитоэстрогенов, включающие деалкилирование 5-алкоксифлавоноидов по положению 5 или деалкилирование 6'-алкоксихалконов по соответствующему положению 6', отличающиеся тем, что их осуществляют in vitro с применением эукариотического или прокариотического материала не животного происхождения. В конкретном воплощении способы применяются для получения 8-PN. Согласно конкретному воплощению деалкилирование в способах по изобретению представляет собой деметилирование и осуществляется с применением эукариотического или прокариотического материала не животного происхождения. Более конкретно не животный материал представляет собой бактериальный штамм, более конкретно гомоацетогенную бактерию или очищенные, или частично очищенные фракции или компоненты на его основе, такие как частично очищенные или выделенные ферменты. Конкретное воплощение относится к деалкилированию с применением материала из Eubacterium sp. или Peptostreptococcus sp., такого как Eubacterium limosum. Следующие конкретные воплощения способа по изобретению включают способы деалкилирования пренилированных 5-алкоксифлавоноидов и/или пренилированных 6'-алкоксихалконов.
Согласно следующему конкретному воплощению предлагаются способы деалкилирования 5-алкоксифлавоноидов и/или 6'-алкоксихалконов растительного происхождения, более конкретно с происхождением из хмеля. Согласно конкретным воплощениям предлагаются способы деалкилирования 6'-алкоксихалкона ксантогумола и/или 5-алкоксифлавоноида изоксантогумола.
Следующий аспект изобретения представляет собой применение бактериальной клеточной линии для in vitro деалкилирования 5-алкоксифлавоноидов и/или 6'-алкоксихалконов, более конкретно для деметилирования 5-метоксифлавоноидов и/или 6'-метоксихалконов. Более конкретно бактериальные клетки являются клетками из гомоацетогенного бактериального штамма, такого как Eubacterium limosum. Следующее конкретное воплощение представляет собой применение бактериальных клеток, в которых увеличена продукция 5-алкоксифлавоноид трансферазной (5-AO-FT) и/или 6'-алкоксихалкон-трансферазной (6'-AO-CT) активности, например, с помощью повторных инкубаций с 5-алкоксифлавоноидом, таким как 5-метоксипренилфлавоноид.
Еще в одном аспекте изобретения предлагаются способы продукции фитоэстрогенов in vitro, которые включают стадии а) предоставления бактериального штамма бактерии, более конкретно гомоацетогенной бактерии или экстракта на его основе и b) введение в контакт композиции, включающей 5-алкоксифлавоноиды, более конкретно 5-метоксифлавоноиды и/или 6'-алкоксихалконы, более конкретно 6'-метоксихалконы с бактериальным штаммом или экстрактом на его основе, так чтобы дать возможность деалкилирования 5-алкоксифлавоноидов и/или 6'-алкоксихалконов с помощью бактериального штамма или экстракта на его основе. Необязательно способы дополнительно включают идентификацию и/или очистку полученного деалкилированного флавоноида.
Конкретные воплощения этих способов представляют собой способы, которые включают приготовление экстракта бактериального штамма, который дополнительно включает стадию обогащения и необязательно очистки бактериального экстракта для того, чтобы содержать обогащенную или очищенную 5-алкоксифлавоноид-трансферазную (5-AO-FT) активность и/или обогащенную или очищенную 6'-алкоксихалкон-трансферазную (6'-AO-CT) активность.
Дополнительно или альтернативно способы по настоящему изобретению включают стадию обогащения продукции бактериального штамма 5-AO-FT и/или 6'-AO-CT активностью с помощью повторных инкубаций с 5-алкоксифлавоноидом, таким как 5-метоксипренилфлавоноид.
Еще в одном аспекте изобретения предлагается 5-метоксипренилфлавоноид метилтрансфераза или 6'-метоксипренилхалкон метилтрансфераза из Eubacterium limosum.
Еще в одном аспекте изобретения предлагаются фармацевтические композиции и пищевые добавки, включающие биоактивные фитоэстрогены, полученные с помощью способов по настоящему изобретению.
В другом аспекте изобретения предлагаются фармацевтические композиции и пищевые добавки, включающие два компонента для одновременного или последовательного введения, где первый компонент включает гомоацетогенную бактерию, или экстракт, или компонент на ее основе, имеющий 5-алкоксифлавоноид-трансферазную (5-AO-FT) и/или 6'-алкоксихалкон-трансферазную (6'-AO-CT) активность, и второй компонент, включающий 5-алкоксифлавоноиды или 6'-алкоксихалконы или их источник, такой как экстракт хмеля. Согласно конкретным воплощениям флавоноид представляет собой 6'-алкоксихалкон ксантогумол или 5-алкоксифлавоноид изоксантогумол. Следующие конкретные воплощения относятся к фармацевтическим композициям и пищевым добавкам согласно изобретению, где гомоацетогенной бактерией является Eubacterium limosum. Необязательно бактерии в фармацевтической композиции по изобретению представлены в виде состава для специфической доставки в прямую кишку.
В настоящем изобретении описано, что IX может быть деметилирован до 8-PN с помощью живых организмов не животного происхождения, таких как бактерии кишечника человека или животных, особенно позвоночных или млекопитающих, и что IX может, таким образом, действовать как проэстроген. В настоящем изобретении дополнительно идентифицированы микроорганизмы, способные осуществлять превращение IX в 8-PN, например, in vitro продукцией 8-PN с применением культур таких микроорганизмов. Дополнительно в настоящем изобретении предлагается способ селекции других штаммов, способных количественно получать 8-PN из IX.
В настоящем изобретении дополнительно продемонстрировано, что процесс превращения метилированных предшественников флавоноидных фитоэстрогенов in vivo с помощью микробной флоры является очень вариабельным и зависит от композиции микробной флоры индивидуума (между индивидуумами или у одного и того же индивидуума в различные моменты). Вероятно это имеет важные последствия при воздействии фитоэстрогенов на индивидуумов. Действительно в экстрактах хмеля, в пиве и в пищевых продуктах или добавках менее эстрогенный IX присутствует в более высоких концентрациях, чем 8-PN.
С помощью представленных способов продукции активированных фитоэстрогенов (in vitro или in vivo) в настоящем изобретении дополнительно предлагается интересная альтернатива или дополнение современным пищевым экстрактам хмеля. Непредсказуемый выход при превращении метилированных предшественников флавоноидных фитоэстрогенов (например, IX) в их активные деметилированные соединения можно контролировать с помощью in vitro предварительного превращения или in vivo/in situ деалкилирования. Это дает возможность осуществления контроля за воздействием активного компонента на каждого индивидуума, несмотря на индивидуальные различия в кишечной микрофлоре, или конкретно принимать эти различия во внимание.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Подразумевается, что чертежи иллюстрируют настоящее изобретение, но не следует считать, что имеются в виду какие-либо ограничения изобретения представленными здесь воплощениями.
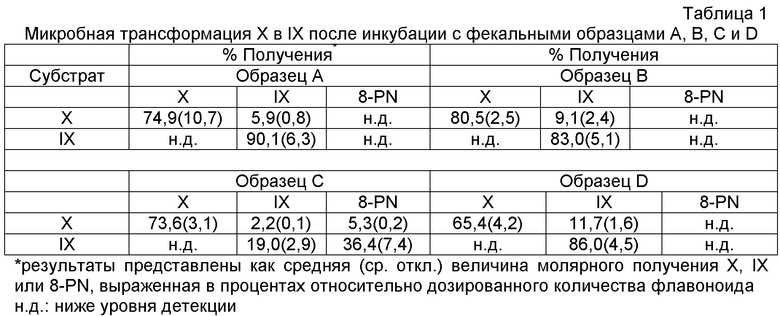
Фиг.1: Основные структуры флавоноидов.
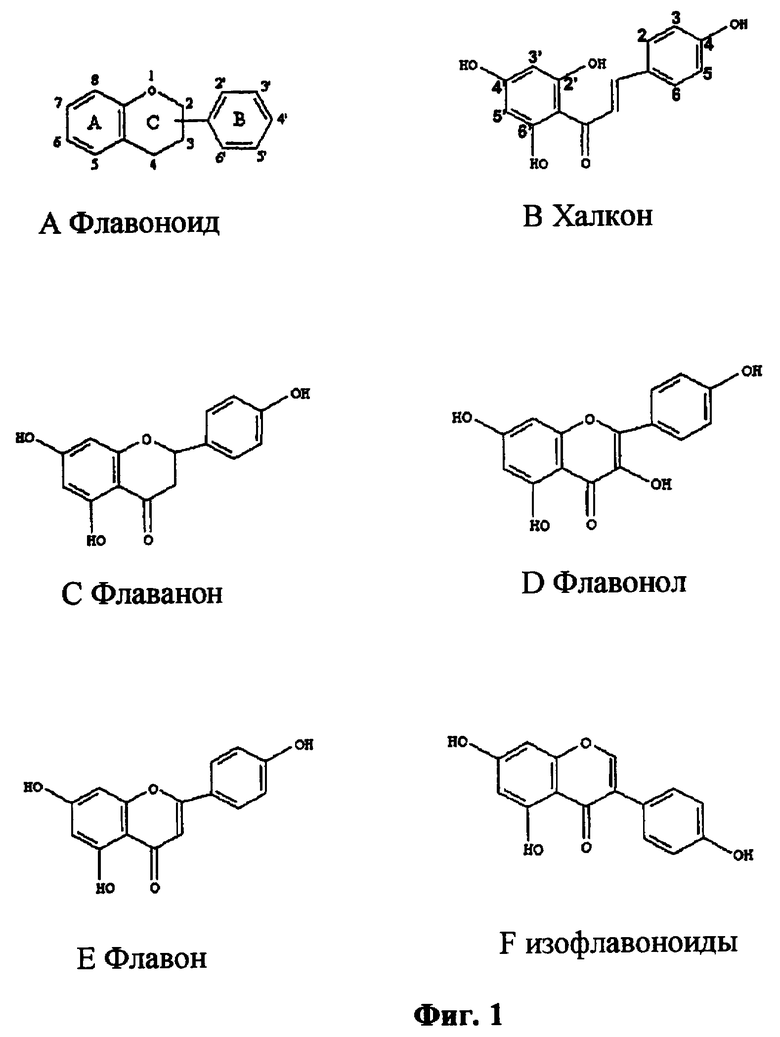
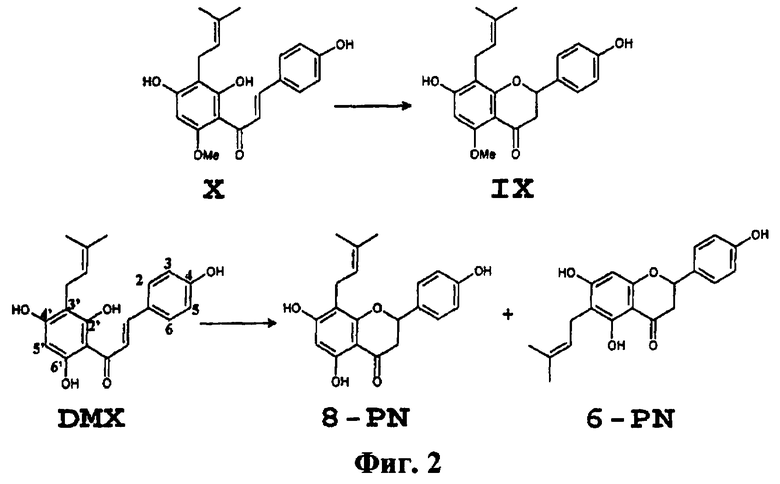
Фиг.2: Структуры пренилфлавоноидов хмеля и их превращение.
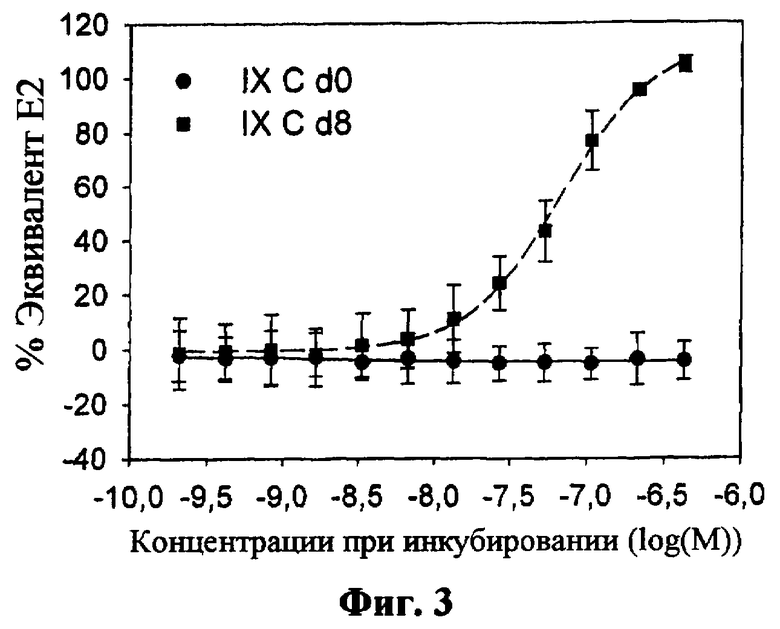
Фиг.3: Реакция на эстроген (среднее + ст. откл.) фекальной культуры (С), инкубированной с IX (0 и 8 дней инкубации) (n=3).
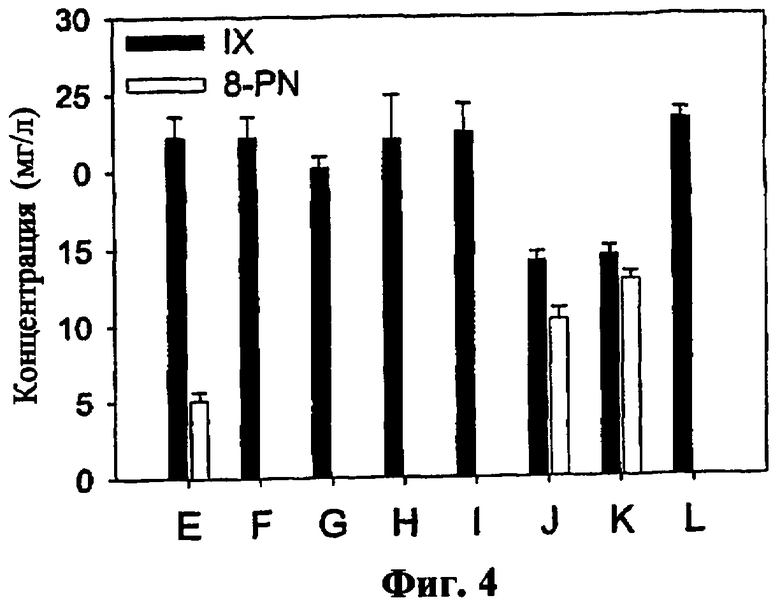
Фиг.4: Трансформация IX (25 мг/л) человеческими фекальными культурами (E-L) в 8-PN через 3 дня [среднее + ст. откл. (n=3)].
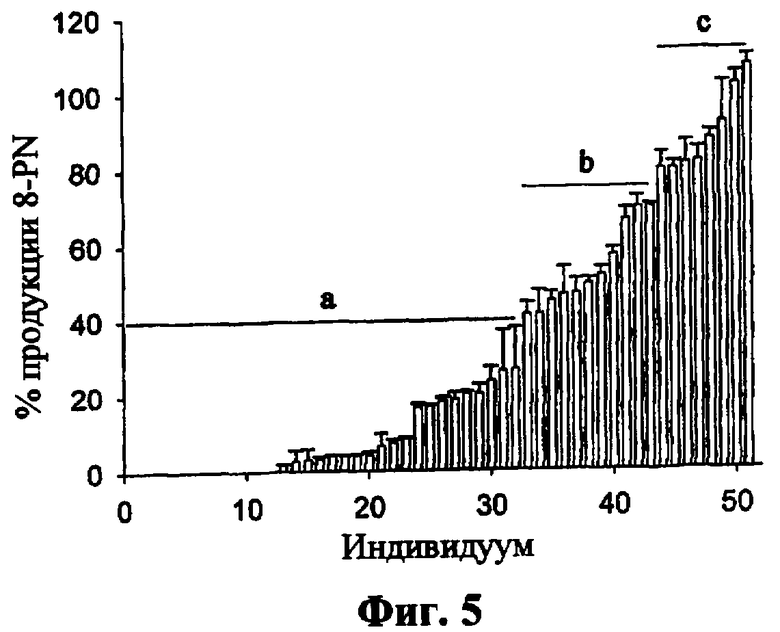
Фиг.5: Превращение изоксантогумола (IX) в 8-пренилнарингенин (8-PN) с помощью кишечных бактерий от 51 человеческого индивидуума. Индивидуумы были распределены по возрастанию продукции 8-PN, и результаты представлены как величина, выражающая % превращения IX в 8-PN (n=3) (+/- станд. откл.).
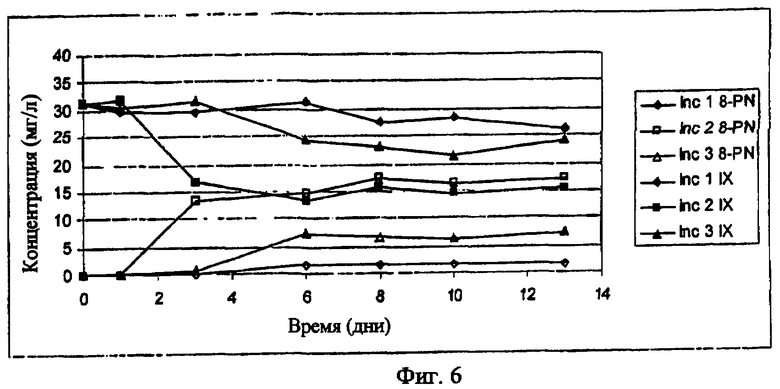
Фиг.6: Превращение IX (25 мг/л) в 8-PN с помощью P. productus (три культуры: Inc 1, Inc 2 и Inc 3). Исчезновение IX (закрашенные символы) и продукцию 8-PN
(незакрашенные символы) детектировали в течение 13 дней.
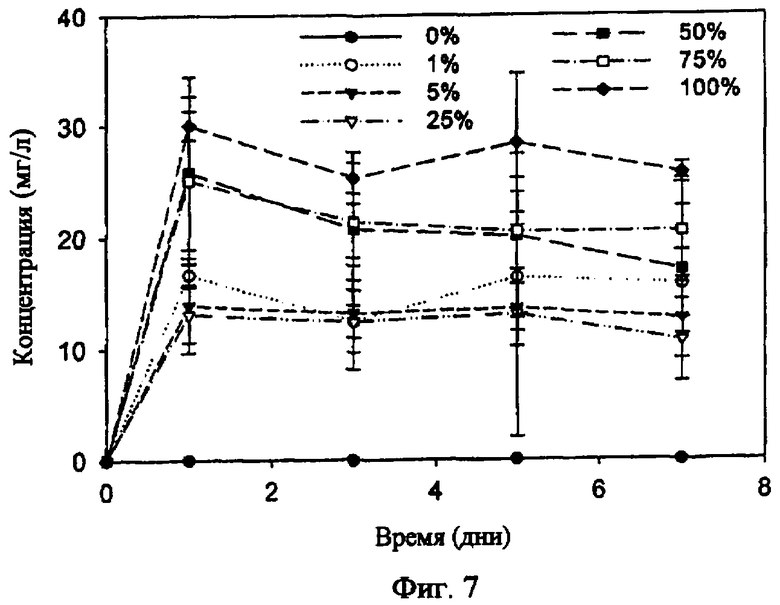
Фиг.7: Превращение IX в 8-PN после добавления культуры E. Limosum к фекальной культуре В (E. Limosum в процентном выражении от 0% (только фекальный образец) до 100% (не зараженная культура E. Limosum)) (n=3).
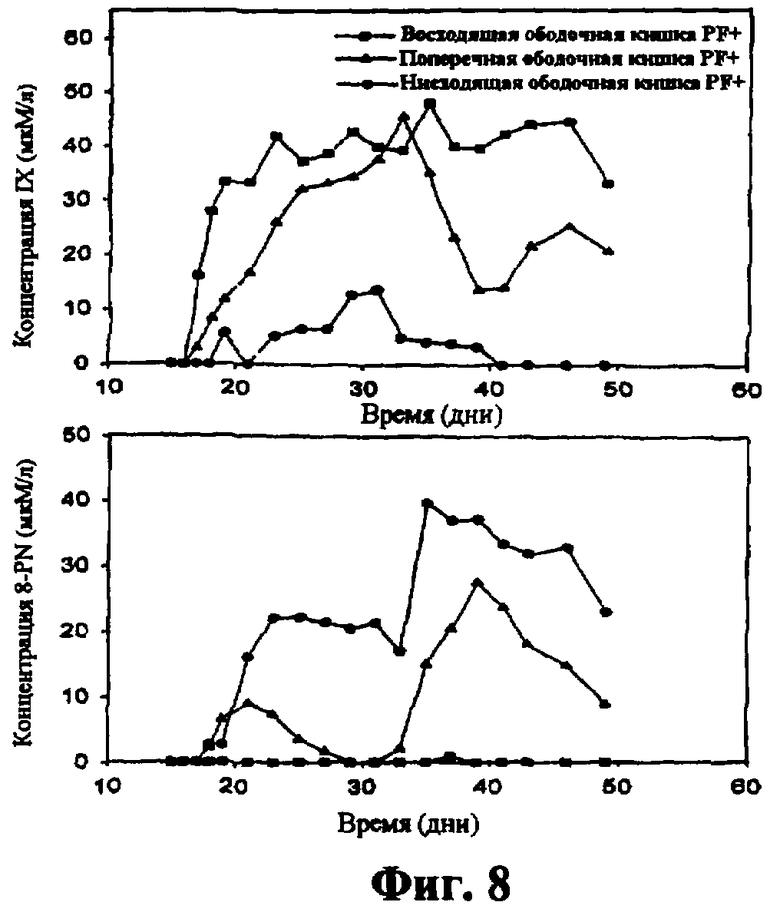
Фиг.8: Превращение IX в 8-PN в микробной экосистеме, моделирующей человеческий кишечник, при условиях, дающих возможность активации метилированных метилфлавоноидов. PF+ отделение TWIN SHIME.
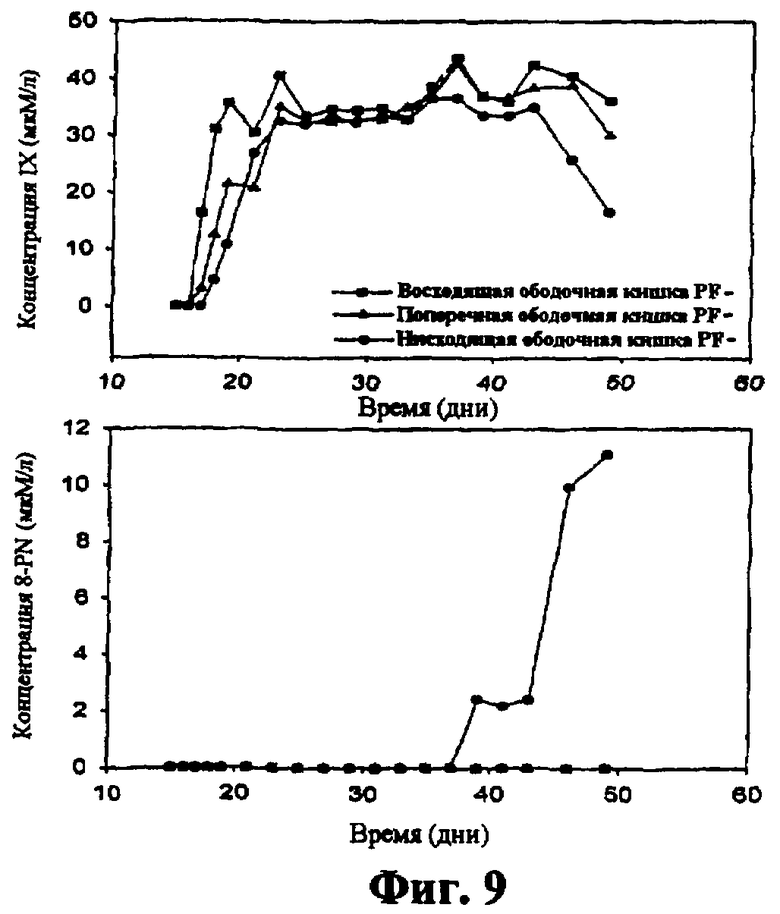
Фиг.9: Превращение IX в 8-PN в микробной экосистеме, моделирующей человеческий кишечник, при условиях, не дающих возможности активации метилированных метилфлавоноидов.
Определения
На протяжении настоящей заявки использовались следующие сокращения:
Х: ксантогумол;
DMX: дезметилксантогумол;
IX: изоксантогумол;
8-PN: 8-пренилнарингенин;
6-PN: 6-пренилнарингенин;
5-AO-FT: 5-алкоксифлавоноид алкилтрансфераза;
5-MO-FMT: 5-метоксифлавоноид метилтрансфераза;
6'-AO-CT: 6'-алкоксихалкон алкилтрансфераза;
6'-MO-CMT: 6'-метоксихалкон метилтрансфераза.
Термин «флавоноиды» обозначает группу органических молекул, на основе остова из 15 атомов углерода, содержащего хромановое кольцо и имеющего второе ароматическое кольцо В в положении 2, 3 или 4 (Фиг.1А). Фиг.1А демонстрирует традиционную нумерацию для заместителей, которая также применяется в настоящем изобретении. Подгруппами флавоноидов являются халконы, флаваноны, флавоны, флаванолы и изофлавоноиды. Халконы (Фиг.1В) являются изомерами флаванонов (Фиг.1С). Фиг.1В и 2 демонстрируют традиционную нумерацию халконов. Флаваноны отличаются от флавонов (Фиг.1Е) тем, что они лишены двойной связи в положениях 2, 3. Флавоны (Фиг.1Е) являются флавоноидами, лишенными 3-ОН группы флаванолов (Фиг.1Е). Изофлавоноиды являются флавоноидами, где фенильное кольцо В локализовано в положении 3 (Фиг.1F). Все эти подгруппы имеют кетоновую функцию в положении 4.
Термин «пренилфлавоноид», использованный в настоящем изобретении, относится к флавоноидам, содержащим неполярную пренильную боковую цепь, присоединенную к одному из фенольных колец. Пренильная цепь чаще находится в положении 8, но может также быть в положении 6, или в обоих положениях 6 и 8 [в халконах пренильная цепь локализована в положении 3' и/или 5']. В хмеле пренилфлавоноиды, главным образом, находятся в лупулиновых железах, располагающихся в основании брактеолей в хмелевых шишках женского растения. Другие натуральные источники пренилфлавоноидов представляют собой, например, Dendrolobium lanceolatum, Sophora flavescens, Sophora tomentosa, Artocarpus communus и Marshallia grandiflora. Примерами пренилфлавоноидов являются халконы (такие как ксантогумол (Х) и дезметилксантогумол (DMX), дегидроциклоксантогумол) и флаваноны (такие как изоксантогумол (IX), 8-пренилнарингенин (8-PN) и 6-пренилнарингенин (6-PN)).
Термин «геранилфлавоноид» относится к флавоноиду, содержащему неполярную геранильную боковую цепь, присоединенную к одному из фенольных колец. Примерами являются тетрагидроксигеранилхалкон, 6-геранилнарингенин, 3'-геранилхалконарингенин и 8-геранилнарингенин. Все эти геранилированные соединения были выделены из хмелевых шишек и 8-геранилнарингенину была приписана эстрогенная активность (Milligan et al. (2000) J. Clin. Endocrinol. Metab. 85, 4912-4915).
Термин «ферментативное деалкилирование или деметилирование», использованный здесь, обозначает удаление из соединения с применением фермента алкильной или метильной группы, соответственно.
Термин «5-алкокси деалкилирование» или «5-метокси деметилирование», использованный здесь, обозначает удаление алкильной группы из алкокси группы или метильной из метокси (-OCH3) группы, соответственно, локализованной в положении 5 флавоноида (нумерацию кольца смотри в Фиг.1А). В этом контексте «5-метокси» и «5-О-метил» имеют одно и тоже значение.
Термин «5-алкокси(пренил)флавоноид трансфераза (5-AO-(P)FT)» обозначает фермент, способный обеспечить 5-алкокси деалкилирование 5-алкокси(пренил)флавоноидов.
Конкретной группой флавоноидов являются халконы, где нумерация кольца отличается. Таким образом, что касается халконов, настоящее изобретение относится к удалению алкильной группы из халконового соединения, более конкретно к 6'-алкокси деметилированию, т.е. к удалению метильной группы из алкокси группы, такой как метокси (-OCH3), локализованной в 6' положении халкона (нумерацию кольца смотри в Фиг.1В). Здесь «6'-метокси» и «6'-О-метил-» имеют одно и то же значение. Ферменты, обеспечивающие 6'-алкокси деалкилирование и, более конкретно, 6'-метокси деметилирование также обозначены здесь как «6'-алкокси(пренил)халкон трансфераза (6'-AO-(P)CT)» и «6'-метокси(пренил)халкон метилтрансфераза (6'-MO-(P)CMT)», соответственно.
Термин «микроорганизм», использованный здесь, включает и бактерии, и грибы. Он относится к штаммам индивидуальных микроорганизмов, микробным консорциумам или микробным сообществам, таким как микробное сообщество кишечника животных или любой другой части тела животных (включая человека), или из любого источника в окружающей среде.
Термин «in vitro способ», использованный в контексте настоящего изобретения, относится к способам, осуществленным вне многоклеточных организмов, и включает как способы, осуществленные в отсутствии живых клеток (применяя, например, лизированные клетки, белковые экстракты или рекомбинантные белки), так и процессы, осуществленные с применением живых клеток, более конкретно культур выделенных клеток. Когда ссылаются на in vitro способы, то, таким образом подразумевается, что исключаются такие процессы, как встречающиеся в природе в интактных шишках хмеля или в кишечнике живых животых.
Когда ссылаются на «in situ» деалкилирующую, деметилирующую активность in vivo, то подразумевается, что это происходит в одном или более конкретном органе тела.
Когда здесь ссылаются на «бактерии», то подразумеваются и аэробные, и анаэробные бактерии.
«Гомоацетогены», по отношению к бактериям, являются анаэробными бактериями, которые восстанавливают СО2 до ацетата или до окисленного ацетата через путь ацетил-CoA. Характерными гомоацетогенными бактериями являются, например, Acetoanaerobium noterae, Acetobacterium woodii, Acetobacterium wieringae, Acetogenum kivui, Acetitomaculum ruminis, Clostridium aceticum, Clostridium thermoaceticum, Clostridium formicoaceticum, Desulfotomaculum orientis, Sporomusa paucivorans, Peptostreptococcus sp. и Eubacteum sp.
Термины первый, второй, третий и подобные в описании и в формуле изобретения используются для обозначения различий между похожими элементами и не являются необходимыми для описания последовательного или хронологического порядка. Следует понимать, что используемые таким образом термины являются заменяемыми при соответствующих обстоятельствах, и описанные здесь воплощения по изобретению способны действовать в другом порядке, по сравнению с описанным или иллюстрированным здесь.
Согласно настоящему изобретению ферментативное деалкилирование и, более конкретно, 5-алкокси деалкилирование флавоноидов можно осуществить с помощью ферментов, в основном обозначенных как 5-алкокси-трансферазы, более конкретно с помощью 5-метоксифлавоноид метилтрансферазы (5-МО-FMT) и/или 6'-метоксихалкон метилтрансферазы (6'-МО-CMT), так же как с помощью интактной живой или инактивированной клетки (или клеточного материала), производящей 5-алкоксифлавоноид алкилтрансферазу или фермент 6'-алкоксихалкон алкилтрансферазу, с помощью лизата такой клетки, с помощью фракции лизата такой клетки (например, мембраны или цитоплазмы), с помощью обогащенной или очищенной белковой фракции, включающей указанную 5-алкоксифлавоноид алкилтрансферазу и/или 6'-алкоксихалкон алкилтрансферазу, или с помощью экспрессирующейся рекомбинантной 5-алкоксифлавоноид алкилтрансферазы и/или 6'-алкоксихалкон алкилтрансферазы. В случае, если рекомбинантный деалкилированный фермент секретируется клетками, то может быть использована подходящая среда. В случае, если рекомбинантный фермент локализован в цитоплазме, то сигналы секреции могут быть добавлены к рекомбинантной ДНК, чтобы получить белок, который может быть выделен из ростовой среды.
В изобретении предлагаются алкокси-деалкилазы, более конкретно ферменты, способные к удалению алкильной группы у алкоксифлавоноидов. Алкильная группа может представлять собой линейный или разветвленный алкил. Более конкретно алкильная группа представляет собой С1-С6 алкил. В конкретном воплощении алкил является метилом.
Согласно настоящему изобретению предлагаются 5-алкокси-алкилтрансферазы, более конкретно 5-алкоксифлавоноид алкилтрансферазы, которые имеют прокариотическое или эукариотическое не животное происхождение, включая 5-алкокси-алкилтрансферазы, имеющие происхождение из растительной клетки или микроорганизма.
Первый аспект настоящего изобретения относится к клеткам, экстрактам и обогащенным частично очищенным или очищенным белкам (так же, как к композициям, включающим один из этих компонентов или более), способных к деалкилированию 5-алкоксифлавоноидов, более конкретно способных к деметилированию 5-метоксифлавоноидов и/или 6'-метоксихалконов. Согласно конкретному воплощению настоящего изобретения клетки, экстракты и белки, включающие активность 5-AO-FMT (и/или 6'-AO-CMT), имеют бактериальное происхождение. Более конкретно бактерии представляют собой гомоацетогенные бактерии. Следующее воплощение изобретения относится к гомоацетогенным бактериям, выбранным из видов Eubacterium и Peptostreptococcus. Гомоацетогенные бактерии можно культивировать в анаэробных условиях с сахарами, одноуглеродными соединениями, такими как формиат, метанол, СО и СО2 плюс Н2, также как с алкоксилированными ароматическими соединениями в качестве источника углерода. Бактериальные штаммы с увеличенной или обогащенной пренилфлавоноид деалкилирующей или деметилирующей активностью могут быть получены с помощью селекции, основанной на повторной инкубации с соответствующим субстратом, как здесь описано в разделе примеров. Обогащение активности, как здесь обозначено, относится к активности, примерно от 1,5 до 10 раз превышающей активность в исходном штамме, более конкретно до ~3 раз превышающей активность в исходном штамме. Дополнительно или альтернативно способ обогащения по настоящему изобретению обеспечивает ферментативную активность, которая достигает 90-100% превращения субстрата (используя, например, 25 мг/л IX). Таким образом, настоящее изобретение также относится к способам обогащения 5-алкоксифлавоноид трансферазной (5-AO-FT) и/или 6'-алкоксихалкон трансферазной (6'-АО-CT) активностью бактериальных штаммов, включающим стадию инкубации штамма на среде с 5-алкоксифлавоноидом, таким как 5-метоксипренилфлавоноид (или 6'-метоксихалкон), более конкретно включающим стадию рассеивания бактерий на среде, включающей IX (или X), с последующей селекцией колонии с наивысшим продуцированием. Более конкретно штамм несколько раз высевают на среде, включающей субстрат, как, например, 2-10 раз, более конкретно 3-4 раза, с последующей селекцией колонии с наивысшей 5-алкоксифлавоноид-трансферазной (5-AO-FT) и/или 6'-алкоксихалкон-трансферазной (6'-АО-CT) активностью. Эту активность можно измерить, например, на основании продукции конечного продукта реакции. Согласно конкретному воплощению этот способ обогащения осуществляют на гомоацетогенном бактериальном штамме, более конкретно на штамме Eubacterium или Peptostreptococcus, более конкретно E. limosum или P. productus. Конкретный пример обогащенного бактериального штамма Eubacterium limosum депонирован Willy Verstraete 15 марта 2006 года в Бельгийских Координированных коллекциях Микроорганизмов (BCCM) в BCCM/LMG коллекции под депозитным номером LMG P-23546, Laboratorium voor Microbiologie, Universiteit Gent (UGent), K.L. Ledeganckstraat 35, B-9000 Gent, Belgium.
Таким образом, в настоящем изобретении предлагается способ получения обогащенной частично очищенной и/или очищенной 5-алкоксифлавоноид трансферазы, более конкретно 5-метоксипренилфлавоноид метилтрансферазы, который включает стадии получения бактериального штамма, более конкретно гомоацетогенного штамма, такого как Eubacterium limosum с увеличенной/обогащенной 5AO-FT активностью, более конкретно с увеличенной 5MO-FMT активностью, и обогащение, частичную очистку или очистку фермента проводили с использованием классических методов очистки, включая осаждение сульфатом аммония, ионно-обменную хроматографию и гель-фильтрационную хроматографию.
В настоящем изобретении предлагаются бактериальные штаммы в качестве источника, где алкил- или метилтрансфераза присутствует в высоких концентрациях и/или где присутствует природный мутант с высокой активностью. В обоих случаях ссылаются на «обогащенный» бактериальный штамм.
Согласно еще одному воплощению изобретения клетка, включающая 5-алкокси деалкилирующую активность, более конкретно 5-метоксифлавоноид деметилирующую активность (и/или 6'-метоксихалкон деметилирующую активность), является трансгенной клеткой, полученной путем введения в микроорганизм или в растительную клетку последовательности ДНК, кодирующей 5-алкокси-алкилтрансферазу, более конкретно 5-MO-FMT (и/или 6'-MO-CMT). Генетически модифицированные растительные клетки с обогащенной 5-MO-FMT (и/или 6'-MO-CMT) активностью, которая может быть объединена с высоким природным или искусственно индуцированным уровнем флавоноидов (например, метилфлавоноидов), полученным в результате “in planta” продукции фитоэстрогенов. Таким образом, в настоящем изобретении предлагаются, но не ограничиваются ими, генетически модифицированные растения с увеличенным содержанием фитоэстрогенов, такие как хмелевые растения.
Согласно другому воплощению клетки, экстракты и белки, включающие 5-алкокси деалкилирующую активность, более конкретно 5-метокси деметилирующую активность, представляют собой растительные клетки Humulus lupulus или других растений, где синтезируется 8-PN, таких как Marshallia grandiflora и Sophora tomentosa. Для крупномасштабного превращения можно провести скрининг растений, где повышенное природное превращение X или IX в 8-PN, для того чтобы обнаружить природные мутанты по 5-MO-FMT (и/или 6'-MO-CMT) или суперэкспрессию 5-MO-FMT (и/или 6'-MO-CMT).
Клетки или композиции можно протестировать на предмет наличия активности 5-AO-FT (и/или 6'-AO-CT), более конкретно 5-MO-FMT (и/или 6'-MO-CMT), используя тест, где исследуют превращение тестируемого субстрата 5-О-метилированного флавоноида (6'-О-метилированного халкона) в его деметилированную форму. Тестируемым субстратом является предпочтительно пренилированный 5-метоксифлавоноид. Согласно конкретному воплощению соединение IX используют в качестве субстрата, и превращение в 8-PN можно протестировать с помощью масс-спектрометрии, HPLC или другим аналитическим методом. Ферментативную специфичность клетки, экстракта или композиции, включающей 5-метокси деметилирующую активность, можно протестировать с использованием флавоноида в виде субстрата с метоксигруппами в других положениях. Например, подходящим субстратом для теста является тангеретин, который содержит метоксигруппы в положениях 4', 5, 6, 7 и 8. Этот тест дает возможность провести различие между деалкилирующей активностью 5-AO-FT (и/или 6'-AO-CT) или деметилирующей активностью 5-MO-FMT (и/или 6'-MO-CMT) бактериального происхождения и деметилирующей активностью микросом млекопитающих или растительных клеток. Экстракты бактериальных или растительных клеток, содержащие 5-метокси деметилирующую активность, получают стандартными методами белковой экстракции. Очищенные белки, имеющие 5-MO-FMT (и/или 6'-MO-CMT) активность, получают методами очистки белков вместе с проведением скрининга на активность очищенных фракций.
Второй аспект изобретения относится к применению бактерий, продуцирующих 5-алкоксифлавоноид трансферазу (5-AO-FT) и/или 6'-алкоксихалкон трансферазу (6'-AO-CT), или более конкретно 5-метоксифлавоноид метилтрансферазу (5-MO-FMT) и/или 6'-метокси халконметилтрансферазу (6'-MO-CMT), или экстракта, или очищенных белков на их основе, включающих эту активность, для деалкилирования или деметилирования природных или синтетических 5-метоксифлавоноидов, включая пренилированные или геранилированные 5-метокифлавоноиды.
В конкретном воплощении изобретения для рентабельной in vitro продукции 8-PN и родственных соединений применяют клетки, более конкретно микроорганизмы, способные превращать 5-метилированные флавоноиды, такие как IX, в 8-PN. Разработаны различные воплощения, такие как инкубация, например, бактериального деметилирующего штамма с экстрактами хмеля или (частично) с очищенными полученными из хмеля соединениями; нанесение, например, бактериального деметилирующего штамма, клеточного экстракта или, в конечном счете, подходящей среды поверх экстрактов хмеля или (частично) очищенных полученных из хмеля соединений; или погружение последних в среду, содержащую штамм, например, деметилирующих бактерий или клеточный экстракт или, в конечном счете, в подходящую среду, возможно с последующей инактивацией штамма через определенное время. Таким образом, в настоящем изобретении также предлагаются способы крупномасштабной рентабельной in vitro продукции фитоэстрогенов.
Согласно настоящему изобретению бактерии, содержащие 5-AO-FT (и/или 6'-MO-CT) активность, экстракты и/или белки, можно использовать для продукции активных эстрогенов, более конкретно фитоэстрогенов из 5-алкоксифлавоноидов. Одно конкретное воплощение настоящего изобретения относится к применению 5-MO-FMT и/или 6'-MO-CMT активности для деметилирования растительных флавоноидов, более конкретно полученных из хмеля (Humulus lupulus). Следующее конкретное воплощение настоящего изобретения относится к превращению IX в 8-PN, или к деметилированию производных IX до производных 8-PN, имеющих по существу ту же биологическую активность. Согласно конкретному воплощению определенные производные деметилированных пренилфлавоноидов, таких как 8-PN, могут быть получены с помощью начальной модификации структуры легкодоступных метилированных предшественников с последующим деметилированием согласно настоящему изобретению, посредством чего получают деметилированные производные пренилфлавоноидов. Возможные модификации представляют собой такие, как включение боковых цепей или насыщенных, или ненасыщенных связей.
Кроме того, клетки и экстракты по настоящему изобретению, содержащие 5-AO-FT и/или 6'-AO-CT, более конкретно 5-MO-FMT и/или 6'-MO-CMT активность, можно использовать для деалкилирования 5-алкоксифлавоноидов. Более конкретно согласно настоящему изобретению были разработаны также в качестве субстратов другие 5-метоксифлавоноиды (или 6'-метоксихалконы), отличные от IX (или X), такие как 5-метоксифлавоноиды или 6'-метоксихалконы, содержащие заместители в положениях 4, 6, 7, 8, 2', 3', 4', 5' и 6' (согласно нумерации флавоноидов), каждый из которых был независимо выбран из группы, состоящей из Н, С1-С6 алкильной группы, С1-С6 алкоксигруппы и С1-С6 ацильной группы, галогенов, более длинных углеродных цепей, ароматических производных, одного или более остатка(ов) сахара или спиртов сахаров, эфиров, сложных эфиров, фосфатов, сульфатов, аминов и т.д.
Согласно конкретному воплощению изобретения 5-алкоксифлавоноид, более конкретно 5-метоксифлавоноид характеризуется гидроксильной группой в положении 7 и/или двойной связью между положениями 2 и 3 и/или гидроксильной группой в положении 4'. Более конкретно настоящее изобретение относится к применению 5-MO-FMT активности для деметилирования 5-метоксифлавоноидных соединений, включающих пренильную или геранильную группу в положении 6 и/или 8. Эту пренильную или геранильную группу необязательно можно дополнительно модифицировать с помощью модификаций, таких как введение двойной связи, трансформация в изопреноиды и замещения, но не ограничиваясь этими модификациями. В определенных воплощениях эти 5-метоксифлавоноиды являются 6'-метоксихалконами или 5-метоксифлаванонами, включая их пренилированные и геранилированные версии. В конкретных воплощениях они выбраны из группы ксантогумола (Х) (2',4,4'-тригидрокси-3'-пренил-6'-метоксихалкон) (нумерация халконов изображена на Фиг.1В и Фиг.2) и изоксантогумола (IX) (5-О-метил-8-пренилнарингенин) или их производных, с подобной по существу биологической активностью (или посредством деметилирования этих соединений получают в результате соединение с подобной по существу биологической активностью).
Другое воплощение настоящего изобретения относится к применению бактерий или экстрактов на их основе, включающих 5-алкоксифлавоноид трансферазную (5-AO-FT) и/или 6'-алкоксихалкон трансферазную (6'АО-СТ) активность для деалкилирования соединений, выбранных из группы следующих молекул, содержащих кроме 5-метоксигруппы: 4'-ацетил-7-пренилоксинарингенин, (+/-)-(Е)-8-(4''-гидроксиизопентенил)нарингенин (8-PN-OH), (+/-)-(Е)-8-(4''-оксоизопентенил)нарингенин (8-PN=O) и 6,8-дипренилнарингенин.
В настоящем изобретении предлагаются улучшенные способы получения деметилированных пренилфлавоноидов in vitro с применением не животного эукариотического или прокариотического материала. Это представляет особый интерес для тех деметилированных пренилфлавоноидов, которые имеют коммерческую ценность, такие как 8-PN. Как упомянуто выше, 8-PN демонстрирует in vivo эстрогенную активность, предупреждает потерю костной массы, ингибирует ангиогенез и метастазирование и проявляет антиандрогенную активность. Следовательно, соединения, полученные способами по настоящему изобретению, могут быть использованы для лечения или предупреждения таких заболеваний, как остеопороз и рак. Деметилированные пренилфлавоноиды и геранилфлавоноиды с эстрогенными свойствами, полученные с помощью способов по настоящему изобретению, могут быть включены в предназначенные для потребления человеком или животным пищевые продукты или пищевые добавки, такие как напитки, включая пиво, а также в косметические средства, предназначенные для использования по уходу за кожей человека или животного. Таким образом, в настоящем изобретении еще предлагаются улучшенные способы для продукции таких пищевых продуктов или пищевых добавок и лекарственных средств.
Другой аспект настоящего изобретения относится к in situ активации метилированных флавоноидов в кишечнике или любой другой части тела человека или животного путем введения клеток, клеточных экстрактов или очищенных ферментов с 5-MO-FMT или 6'-MO-CMT активностью. Согласно конкретному воплощению введение 5-MO-FMT и/или 6'-MO-CMT активности объединено с введением метилированных флавоноидов или их источника по отдельности или в одной композиции, одновременно или последовательно. Как композиция, включающая ферментативную активность, так и композиция, включающая субстрат, может быть представлена в виде фармацевтической композиции или пищевой добавки. Источники метилированных флавоноидов включают, но не ограничиваются ими, части растения (например, хмеля), или экстракты, или очищенные метилированные флавоноидные соединения. С помощью продукции деметилированных пренилфлавоноидов in situ, более конкретно с помощью продукции 8-PN предлагается альтернативный способ лечения и/или предупреждения заболеваний и состояний, но не ограничиваясь ими, которые можно лечить с помощью эстрогенов, таких заболеваний, как потеря костной массы, патологический ангиогенез, метастазирование, и предлагается применение в качестве антиандрогенной терапии.
Необязательно могут быть разработаны различные стратегии введения для специфической доставки в толстую кишку алкилированных флавоноидов. Этого можно достичь, например, путем инкапсулирования композиции, которое приводит к высвобождению в толстой кишке, или путем коньюгации с получением коньюгата, выбранного из группы, состоящей из глюкуронида, сульфата, ацетата, пропионата, глюкозида, ацетилглюкозида, малонилглюкозида и их смеси.
Другой аспект настоящего изобретения относится к фармацевтической композиции и/или пищевой добавке, включающей или состоящей из клетки, экстракта или очищенного белка на ее основе, имеющей 5-MO-FMT и/или 6'-MO-CMT активность. Согласно конкретному воплощению этого аспекта изобретения клетка является клеткой или микроорганизмом, более конкретно бактериальной клеткой гомоацетогена, такого как гомоацетогены Eubacterium и Peptostreptococcus. Необязательно фармацевтические композиции или пищевые добавки дополнительно включают источник метилированных пренилфлавоноидов или геранилфлавоноидов, которые в виде деметилированных соединений проявляют сильную эстрогенную активность. Таким источником может быть растительный экстракт (особенно хмеля) или его обогащенная фракция. Это может быть также синтетический метилированный пренилфлавоноид. Как микроорганизмы, так и метилированные флавоноиды могут быть представлены в/с отдельными фармацевтическими носителями для одновременного или последовательного введения, или могут быть объединены в один и тот же фармацевтический носитель, распределенный гомогенно или асимметрично. Соответственно, в изобретении предлагаются комбинации фармацевтических композиций, комбинации фармацевтических композиций и пищевых добавок, и комбинации пищевых добавок. Кроме того, в настоящем изобретении предлагаются способы лечения, включающие стадии последовательного или одновременного введения фармацевтических композиций по настоящему изобретению нуждающемуся в этом пациенту. Точно также в настоящем изобретении предлагается применение композиций, включающих 5-алкоксиалкил-трансферазную активность и/или композиций, включающих описанные здесь 5-алкоксифлавоноиды, для промышленного производства лекарственного средства. Обычно композиции по настоящему изобретению вводят в виде эстрогенных добавок и/или применяют в эстрогензамещающей терапии нуждающегося в этом пациента.
Количество метилированного IX или X (которое будет деметилировано до 8-PN), которое должно быть введено, находится в пределах между 10 и 20000 микрограмм/день/75 кг, между 50 и 10000 микрограмм/день/75 кг или между 50 и 7000 микрограмм/день/75 кг, например около 5, 10 или 20 миллиграмм/день/75 кг. Метилированные формы менее сильных флавоноидов могут быть соответственно введены в больших дозах после сравнения эстрогенной активности этой деметилированной формы с 8-PN.
Еще в одном аспекте настоящего изобретения предлагается фармацевтическая композиция, включающая бактерии или бактериальный экстракт, имеющий 5-алкокси-алкилтрансферазную активность по настоящему изобретению и фармацевтический носитель. Для того чтобы достичь оптимальной эффективности, фармацевтический носитель предпочтительно высвобождает микроорганизмы в толстой кишке. Специфичное введение лекарственных средств в толстую кишку хорошо известно и описано, например, Chourasia & Jain (2004) Drug. Deliv. 11(2), 129-148. В настоящее время доступны различные стратегии для специфичного высвобождения лекарственных средств в толстой кишке, включая образование пролекарства, покрытого рН-чувствительными полимерами, применение специфичных для толстой кишки биодеградируемых полимеров, систем с контролируемым во времени высвобождением, осмотических систем и систем доставки лекарственного средства с контролем давления. Среди различных способов достижения специфичного высвобождения лекарственного средства в толстой кишке - применение специфичных для толстой кишки биодеградируемых полимеров подает большие надежды. Полисахаридазы являются бактериальными ферментами, которые доступны в достаточном количестве, чтобы использоваться для специфичной доставки лекарственных средств в толстую кишку. На основе этого способа исследовали разнообразные полисахариды для специфичного высвобождения лекарственных средств в толстой кишке. Эти полисахариды включают пектин, гуар-гум, амилозу, инулин, декстран, хитозан и хондроитин сульфат. Это семейство природных полимеров является привлекательным для доставки лекарственных средств, поскольку оно включает полимеры с большим количеством заменяемых групп, широкий предел по молекулярному весу, варьирование химических композиций и, по большей части, низкую токсичность и, кроме того, высокую стабильность биодеградации. Наиболее предпочтительным свойством этих веществ является разрешение для их применения в качестве фармацевтических вспомогательных веществ.
Чтобы предотвратить деградацию с внутренней стороны деалкилирующими бактериями по настоящему изобретению, бактерии могут быть сначала помещены в не деградируемый бактериями фармацевтический носитель и затем покрыты полимером, который может разрушаться под действием микробной флоры толстой кишки. Затем бактерии могут высвобождаться, например, с помощью механизмов контролируемого рН или контролируемого во времени высвобождения лекарственного средства или, пользуясь преимуществом увеличения люминального давления в толстой кишке, благодаря сильной перистальтике, как описано Leopold (1999) Med Klin. 94 Suppl 1, 6-11.
Также известны системы специфичной доставки в толстую кишку, которые не зависят от ферментативной активности кишечных микроорганизмов. Например, Европейский патент EP0673645 описывает систему специфичной доставки лекарственных средств в толстую кишку, включающую три части: (1) энтеросолюбильное покрытие, чтобы предотвратить проникновение желудочной жидкости в систему доставки, таким образом, предотвращая любое высвобождение лекарственного средства в желудке; (2) деградируемый полимерный слой, который подвергается воздействию и частично деградирует во время прохождения по верхнему кишечному тракту, и (3) внутренняя часть, которая является содержащей активный ингредиент(ы) обычной таблеткой или гранулой, которая легко дезинтегрируется и последовательно высвобождает лекарственное средство в месте специфической доставки - в толстой кишке после эрозии разрушаемого полимерного слоя.
Европейская патентная заявка ЕР0453001 описывает фармацевтические композиции со свойством специфического контролируемого высвобождения активных элементов, которые оказывают фармакологическое действие в кишечнике и, более конкретно, в толстой кишке и в концевой части подвздошной кишки. Активный элемент готовят в мультикомпонентной мультидозовой форме и покрывают, по меньшей мере, двумя мембранами, одной с рН-зависимой растворимостью и другой нерастворимой, но проницаемой для кишечных жидкостей. В то время как покрытый оболочкой активный элемент остается в желудке и в начальной части кишечника, то есть пока рН меньше, чем 5,5, то он не высвобождается. Только когда он достигает места, где рН выше (тонкий кишечник или толстая кишка), происходит рН-зависимое растворение мембраны для того, чтобы началось высвобождение активного элемента. Начиная с этого момента вторая мембрана, которая является рН-независимой, но проницаемой для жидкостей кишечника, действует, замедляя и контролируя растворение лекарственного средства внутри тракта тонкого кишечника-толстой кишки.
ЕР0778778 описывает композицию с одним или более пробиотическими микроорганизмами, такими как Eubacterium, и носителем, чтобы доставлять микроорганизмы в толстую кишку. Носитель является модифицированным или не модифицированным стойким крахмалом, более конкретно крахмалом с высоким содержанием амилозы, который действует как ростовая или поддерживающая среда для микроорганизмов в толстой кишке. Патентная заявка US 2004175389 описывает лекарственный состав для сохранения пробиотических бактерий во время прохождения через желудок с возможностью высвобождения только в кишечнике, более конкретно в толстой кишке, и который практически не активен в воде и, соответственно, имеет длинный срок годности. Лекарственный состав включает по существу безводную смесь пробиотических бактерий с одновалентными альгинатными солями, где смесь была сформирована и поддерживалась, по существу, в безводной среде. Альгинатные соли включают альгинат натрия и альгинат калия, но не включают двухвалентных солей, таких как альгинат магния или альгинат кальция. В основном для лекарственного состава предлагается энтеросолюбильное покрытие (например, желатиновое или целлюлозное инкапсулирование).
Следует понимать, что хотя конкретные воплощения, конкретные конструкции и конфигурации, а также материалы обсуждают в следующем разделе примеров, они являются только иллюстративными, и могут быть произведены различные изменения или модификации в форме и детализации, не выходя за рамки границ и сущности этого изобретения.
ПРИМЕРЫ
Пример 1: Деметилирование изоксантогумола (IX) с помощью фекальных культур человека
Фекальные образцы были получены от 12 здоровых людей в возрасте от 20 до 35 лет и были обозначены от А до L. Не один из этих пациентов не имел истории желудочно-кишечной болезни, и пациенты не принимали антибиотики в течение 3 месяцев перед доставкой образца. Были приготовлены фекальные суспензии из 20%(вес./об.) свежих фекальных образцов путем гомогенизации фекалий в фосфатной буферной соли (0,1М, рН7), содержащей 1г/л тиогликолята натрия в качестве восстанавливающего агента. Материал в виде частиц удаляли путем центрифугирования (1 мин, 500xg). Супернатант затем обозначали как «культура».
Способность культур, полученных из фекальных образцов A, B, C и D (в дальнейшем обозначенных как культуры A-D), разрушать или трансформировать пренилфлавоноид IX хмеля протестировали путем инкубации фекальных культур (10% (об./об.)) в питательной среде с сердечно-мозговым экстрактом (с 0,5 г/л цистеина-HCl) с 25 мг/л изоксантогумола в течение 8 дней при анаэробных условиях. Инкубационные экстракты на 0 и 8 день тестировали на предмет биоактивной трансформации продуктов IX с использованием дрожжевой тест-системы для оценки эстрогенной активности, согласно De Boever et al. (2001) Env. Health Perspectives 109, 691-697, основываясь на работе Routledge & Sumpter (1996) Environ. Toxicol. Chem. 15, 241-248. Коротко, Saccharomyces cerevisiae трансформировали человеческим геном эстрогенного рецептора (ERα) вместе с экспрессирующими плазмидами, содержащими респонсивные элементы и LacZ репортерный ген (кодирующий фермент β-галактозидазу). Активность β-галактозидазы количественно оценивали при 540 нм с помощью превращения хромогенного вещества хлорфенола красного-β-D-галактопиранозида в хлорфеноловый красный. Ответ биотеста выражается как поглощение при 540 нм, деленное на оптическую плотность при 630 нм [(А540/А630)net]. Эстрогенная активность образцов была выражена в процентном эквиваленте к 10 нМ эстрадиола (Е2), который вызывал 100% ответ биотеста на эстрогенную активность. Биотесты осуществляли в 96-луночных платах, в которых 10 мкл тестируемых соединений тестировали и инкубировали с 240 мкл генетически модифицированных дрожжей (оптической плотностью 0,25 при 610 нм). Серийные разведения тестируемых соединений были произведены в диметилсульфоксиде, который дает возможность получения дозозависимых респонсивных кривых для доз (ось ординат) в зависимости от активности (ось абсцисс). Данные обрабатывали с помощью 4-параметрической логистической модели с использованием Marquardt-Levenberg алгоритма (Sigmaplot 4.0, SPSS Inc., Chicago, Illinois, USA) (De Boever et al. (2001) Env. Health Perspectives 109, 691-697).
Результаты представлены на Фиг.3. Ни одна из инкубаций не демонстрирует эстрогенного ответа в день 0. Через 8 дней сильное увеличение эстрогенных свойств наблюдали в культуре С (Фиг.3), но не в культурах A, B и D (данные не показаны). Эти результаты выявляют способность фекальной культуры С превращать IX в соединения с увеличенными эстрогенными свойствами. Чтобы дополнительно протестировать эту трансформацию, культуры A-D (10% (об./об.)) инкубировали в течение 8 дней в питательной среде с сердечно-мозговым экстрактом (с 0,5 г/л цистеина-HCl) с Х или IX при концентрации 25 мг/л при анаэробных условиях, и продукты превращения детектировали с помощью HPLC (Таблица 1). Было доказано, что IX является устойчивым к трансформации в культурах A, B и D, что соответствует результатам, полученным с помощью дрожжевой тест-системы для оценки эстрогенной активности. Однако в культуре С получили почти 40% 8-PN, что объясняет увеличение эстрогенных свойств культуры С. Х в незначительной степени превращался в IX во всех образцах, но, как уже детектировали, при инкубации Х с автоклавированными культурами, это превращение представляло собой не ферментативную изомеризацию. В культуре С также детектировали небольшое количество 8-PN, которое получалось в результате превращения IX человеческими фекальными бактериями.
Настоящие результаты демонстрируют способность кишечных бактерий трансформировать X или IX в 8-PN посредством процесса ферментативного О-деметилирования метоксигруппы в положении 5 компонентов. Но не все культуры имели возможность осуществлять эту реакцию. Таким образом, оставшиеся культуры E-L (10% (об./об.)) инкубировали в течение 3 дней в питательной среде с сердечно-мозговым экстрактом (с 0,5 г/л цистеина-HCl) с IX с концентрацией 25 мг/л при анаэробных условиях (Фиг.4). Микробное О-деметилирование IX детектировали только в образцах E, J и K.
Настоящий пример демонстрирует, что метилированные пренилфлавоноиды не являются метаболически инертными после приема внутрь, но могут активироваться в биологически (более) активные деметилированные производные. Однако эта способность к трансформации сильно зависит от композиции и активности микробного сообщества кишечника, поскольку активация IX встречается только в трети тестируемых образцов.
Чтобы дополнительно исследовать эти внутренние индивидуальные различия, всего инкубировали 51 фекальный образец в течение 3 дней в питательной среде с сердечно-мозговым экстрактом (с 0,5 г/л цистеина-HCl), содержащим IX в концентрации 25 мг/л, при анаэробных условиях (Фиг.5). Результаты представлены как % продукции 8-PN по отношению к концентрации инкубированного IX, и образцы располагали по увеличению способности к продукции 8-PN. Данные анализировали с помощью двухступенчатого кластерного анализа, и обнаружили три группы (обозначенные a, b и c) с существенно различными значениями (Р<0,01, Kruskal-Wallis).
Эти данные демонстрируют, что активация метилированных пренилфлавоноидов зависит от микробного сообщества кишечника, разделяющего индивидуумов на сильных (группа с, 16%), средних (группа b, 22%) и слабых (группа а, 63%) продуцентов 8-PN. В основном конечное воздействие на активные компоненты будет зависеть в большей степени от комбинации концентрации предшественника и потенциала трансформации микробного сообщества кишечника.
Пример 2. Применение микроорганизмов для получения соединений с эстрогенными свойствами типа 8-пренилнарингенина
Настоящий пример описывает способность двух хорошо охарактеризованных кишечных анаэробных бактерий к превращению IX в 8-PN.
Eubacterium limosum ATCC 8486 и Peptostreptococcus productus ATCC 27340 были получены из Немецкой Коллекции Микроорганизмов и Клеточных Культур (DSMZ, Braunschweig, Germany). E. limosum инкубировали в течение 13 дней в питательной среде с сердечно-мозговым экстрактом (с 0,5 г/л цистеина-HCl), с IX и 8-PN в концентрации 25 мг/л, при анаэробных условиях (Таблица 2). Этот штамм был способен превращать IX в 8-PN. Штамм не подвергал дополнительной деградации 8-PN, поскольку все 8-PN, предоставленные в качестве субстрата, могли быть получены через 13 дней инкубации. Этот путь совершенно отличается от метаболического пути, какой наблюдается в микросомах печени, где 8-PN в дальнейшем существенно метаболизируется [Nikolic et al. (2005) J. of Mass Spectrom. 40, 289-299; Nikolic et al. (2004) Drug Metabolism and Disposition 32, 272-279].
н.д.: ниже уровня детекции
Благодаря способности E. limosum. трансформировать IX в 8-PN, процедуру селекции осуществляли, чтобы получить штамм, способный количественно производить 8-PN. Процедура селекции состояла из 6 параллельных инкубаций E. Limosum. [культуры, полученные от единственных колоний] с 25 мг/л IX, и инкубации в течение 8 дней. Затем культуру, которая производила наибольшее количество 8-PN, селектировали и использовали для инокуляции для следующего раунда 6 параллельных инкубаций (Таблица 3). В то время как в первом раунде селекции низший уровень продукции составлял только 2%, то через три стадии селекции обнаружили его увеличение до 82%, и наиболее эффективная культура трансформировала все введенные IX в 8-PN. Средняя величина продукции всех шести инкубаций в каждом раунде увеличивалась от 22,5% до 90,5%, и стандартное отклонение уменьшалось от 20% до 7% после процедуры селекции. Это значит, что только после трех раундов селектировали штамм, который превращал почти все IX (высокая средняя величина), а также был стабилен (низкое стандартное отклонение).
Чтобы протестировать способность P. productus осуществлять ферментативное превращение IX в 8-PN, штамм инкубировали трижды в течение 13 дней в питательной среде с сердечно-мозговым экстрактом (с 0,5 г/л цистеина-HCl), с 25 мг/л IX при анаэробных условиях. Образцы анализировали каждые 2 дня и определяли концентрации IX и 8-PN (Фиг.6). В зависимости от инкубации P. productus трансформировал от 10% до 50% инкубированного IX в 8-PN. Этот факт демонстрирует, что данный штамм также является подходящим для продукции 8-PN. P. productus штаммы можно было дополнительно селектировать на увеличенную деметилирующую активность, что логически обосновано, как описано для E. limosum.
Конкретный пример бактериального штамма Eubacterium limosum, который был обогащен, был депонирован Willy Verstraete в Бельгийских Координированных коллекциях Микроорганизмов (BCCM) в BCCM/LMG коллекции под депозитным номером LMG P-23546 15 марта.
Пример 3. Применение микроорганизмов для превращения метилированных пренилфлавоноидов в ферментационной установке
Эксперимент с ферментацией периодического действия с подпиткой разработали, чтобы применять селектированный штамм Eubacterium limosum, как получено выше, для превращения метилированных пренилфлавоноидов в ферментационной установке. Ферментацию осуществляли в ферментере Braun Biostat® M (2 л чан), наполненный 1,5 л питательной среды с сердечно-мозговым экстрактом (с 0,5 г/л цистеина-HCl). Впоследствии ферментер стерилизовали автоклавированием в течение 30 мин при 121°С. Перед инокуляцией в ферментере создают анаэробные условия путем продувки системы в течение 1ч газообразным азотом. После этого ферментер инокулировали 2-дневной культурой E. Limosum и добавляли к ферментационной жидкости 25 мг/л IX. Ферментацию осуществляли при 37°С в течение 2 недель без рН-контроля. Начиная с 1 дня, трижды в день добавляли в реактор со скоростью 10 мл/мин 200 мл анаэробной питательной среды с сердечно-мозговым экстрактом (с 0,5 г/л цистеина-HCl), содержащей 25 мг/л IX, и одновременно удаляли из системы содержимое ферментера со скоростью 200мл/мин. Из оттока брали 10 мл образца для химического анализа. Это было проделано в дни 0, 1, 2 и затем каждые 2 дня. Данные представляли в виде % превращения (8-PN/(IX + 8-PN)). Было получено превращение IX в 8-PN 0% (день 0), 43% (день 1) и 100% (день 2 и последующие дни).
Этот пример демонстрирует, что селектированный штамм способен превращать IX в высокоэстрогенный 8-PN с помощью стратегии, основанной на ферментации, приводящей к применениям, таким как получение продуктов с эстрогенными свойствами из предшественников, с целью очистить интересующее соединение для использования в качестве ингредиента для других применений или чтобы активировать предшественник в экстрактах хмеля или других растительных экстрактах, включающих метилированные пренилфлавоноиды.
Пример 4: Добавление штамма инициирует ex vivo превращение IX в 8-PN
Наиболее эффективный штамм E. limosum, полученный в результате эксперимента по селекции примера 2, добавляли к не способной к превращению в обычных условиях культуре В примера 1, чтобы оценить способность этого штамма инициировать продукцию 8-PN в комплексной среде фекальной суспензии. Штамм добавляли к культуре в пропорциях, находящихся в пределах от 0% до 100% (об./об.). Смесь инкубировали с 10% (об./об.) 25 мг/л IX в течение семи дней в питательной среде с сердечно-мозговым экстрактом (с 0,5 г/л цистеина-HCl) в анаэробных условиях. Концентрацию 8-PN детектировали каждые два дня (Фиг.7). Результаты демонстрируют, что при увеличении добавления E. limosum продукция 8-PN увеличивалась. Равное количество культуры E. limosum и фекального образца (100% на Фиг.7) составляли друг другу конкуренцию в превращении IX в 8-PN, но даже при добавлении 1% половина добавленного IX трансформировалась в 8-PN уже через один день. Интересно, что максимум концентрации 8-PN достигался при всех инкубациях на первый день, что выявляет, что весь доступный IX немедленно трансформировался. Никакого дальнейшего превращения 8-PN не детектировали, поскольку концентрации 8-PN в первый день и седьмой существенно не отличались (Student T-test, p>0,05).
Этот пример демонстрирует, что селектированный штамм был способен превращать IX в высокоэстрогенный 8-PN в комплексной среде фекальной культуры, приводя к возможным применениям, таким как in situ превращение предшественников в продукты с эстрогенными свойствами с другими отличными материалами, такими как экстракты хмеля или другие растительные экстракты, включающие метилированные пренилфлавоноиды.
Пример 5. Превращение метилированных пренилфлавоноидов в динамичной in vitro имитационной модели кишечного тракта
Следующая стадия заключалась в применении динамичной in vitro имитационной модели кишечного тракта, чтобы продемонстрировать in situ превращение предшественников, таких как IX в продукты с эстрогенными свойствами, такие как 8-PN (имитатор человеческой кишечной микробной экосистемы (SHIME)), (Molly et al. (1993) Appl. Microbiol. Biotechnol. 39, 254-258). SHIME состоит из последовательности из пяти реакторов, которые представляют различные части желудочно-кишечного тракта человека. Первые два реактора (желудок [реактор 1] и тонкий кишечник [реактор 2]) являются элементами периодического наполнения, чтобы имитировать различные стадии приема пищи и пищеварения, с перистальтическими насосами, подающими определенное количество SHIME пищи (3 раза/день), и панкреатическую, и желчную жидкость в желудок и в отделение двенадцатиперстной кишки, и опустошающими соответствующие реакторы через определенные интервалы. Последние три отделения (соотв. восходящая ободочная [реактор 3], поперечная ободочная [реактор 4] и нисходящая ободочная кишка [реактор 5]) представляют собой проточные реакторы с мешалкой с постоянным объемом и рН-контролем. Продолжительность отстаивания и рН в различных чанах выбирали для того, чтобы воссоздать in vivo условия в различных частях желудочно-кишечного тракта. Прохождение пищи в тонком кишечнике имитировали в реакторе 2 путем добавления 60 мл искусственной панкреатической и желчной жидкости, панкреатина и NaHCO3. Температуру системы поддерживали 37°С с помощью термостата, и систему поддерживали в анаэробных условиях путем ее продувки с N2 в течение 15 мин каждый день. Посевной материал готовили из фекального вещества, как описано De Boever et al. (2000) J. Nutrition 130, 2599-2606. Реакторы 3, 4 и 5 наполняли питательной средой и рН регулировали до соответствующего предела рН. В конце добавляли 50 мл посевного материала в последние три реактора.
Для настоящего эксперимента две из вышеописанных систем были объединены как два полностью разделенных реактора, которые управляются одинаковыми насосами (насосы, имеющие две высоты напора, позволяющие добавлять точно одинаковые количества жидкости в обе системы), имеют идентичное рН и температурный контроль и которые получают одинаковую жидкую пищу. Таким образом, все параметры полностью контролировались и были идентичными, за исключением кишечных микробных сообществ в системе 2, которые можно ввести отдельно. В этом случае мы вводили сообщество, которое способно активировать метилированные пренилфлавоноиды (PF+) и которое не способно (PF-). Через две недели стабилизационного периода, во время которого добавляли нормальную SHIME пищу, 25 мг/л IX вводили к SHIME пище в течение 4 недель (день 15-44). В последние две недели селектированный штамм Eubacterium limosum примера 2 также вводили в первое отделение толстой кишки, чтобы имитировать применение штамма в качестве пробиотика (день 30-44).
Фиг.7 и 8 демонстрируют концентрации IX и 8-PN в частях восходящей ободочной, поперечной ободочной и нисходящей ободочной кишки для PF+ и PF- сообществ. В PF+ отделении обнаружили активацию метоксилированных пренилфлавоноидов в отдаленных частях толстой кишки, когда вводили только IX (день 15-30), тогда как никакого превращения не встречалось в PF- отделении. После добавления бактериального штамма (начиная с дня 30) активирующий потенциал увеличился в PF+ отделении и также в PF- отделении, и продукцию эстрогенно-активного 8-PN детектировали в отдаленной части толстой кишки.
Пример демонстрирует, что селектированный штамм примера 2 имел способность активировать метилированные пренилфлавоноиды в условиях, имитирующих человеческий кишечник.
Пример 6: Демонстрация in vivo 5-алкоксипренилфлавоноид деметилирующей способности селектированного штамма примера 2
Эксперимент с аксеническими и зараженными человеческой флорой (HFA) крысами осуществляли, чтобы протестировать способность селектированного штамма примера 2 активировать метилированные пренилфлавоноиды in vivo. Всего 12 аксенических крыс использовали для исследования. Когда крысы были в возрасте 5 недель, 3 HFA крысы были заражены путем перорального введения через желудочный зонд свежевыделенной, гомогенизированной фекальной культурой, которая имеет пренилфлавоноидную деметилирующую активность. Эти HFA крысы были обозначены как PF+ крысы.
В то же самое время 3 HFA крысы были заражены путем перорального введения через желудочный зонд свежевыделенной, гомогенизированной фекальной культурой без пренилфлавоноидной деметилирующей активности. Эти HFA крысы были обозначены как PF- крысы. Всех крыс держали в отдельных, закрытых общих клетках перед началом эксперимента.
Через 3 недели стабилизации микробных культур в кишечнике крыс был начат первый эксперимент. После помещения крыс в индивидуальные камеры для исследования метаболизма каждой крысе ежедневно вводили по 2 мг IX/кг веса тела в течение 5 дней и каждый день собирали общую мочу за 24 ч. Через 3 дня количественно оценили выделение с мочой IX и 8-PN. Превращение [8-PN/(IX+8-PN)] представлено в Таблице 4. Затем крыс поместили обратно в общие клетки за две недели до второй части эксперимента.
Здесь 6 аксенических крыс заражали штаммом E. limosum примера 2 в течение 7 дней путем ежедневного перорального введения через желудочный зонд Iog9 бактериальной суспензии. На второй день крыс поместили в индивидуальные камеры для исследования метаболизма для сбора общей мочи за 24 ч. Начиная со 2 дня по 7 день крысам вводили 7,2 мг IX/кг веса тела путем перорального введения через желудочный зонд. На 7 день количественно оценили выделение с мочой IX и 8-PN. Превращение [8-PN/(IX+8-PN)] представлено в Таблице 4.
Этот пример демонстрирует, что активация метилированных пренилфлавоноидов является исключительно микробным явлением, поскольку аксенические крысы не производили 8-PN. Кроме того, различия в способности кишечной трансформации приводят к различному выделению 8-PN, поскольку в моче PF+ крыс степень 8-PN была выше по сравнению с PF- крысами. Наконец, этот пример выявляет, что селектированный штамм E. limosum может активировать метилированные пренилфлавоноиды in vivo, поскольку аксенические крысы начинали производить 8-PN после заражения бактериями.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПОЛУЧЕНИЕ ЭКСТРАКТОВ ХМЕЛЯ, ОБЛАДАЮЩИХ ЭСТРОГЕННОЙ И АНТИПРОЛИФЕРАТИВНОЙ БИОАКТИВНОСТЬЮ | 2004 |
|
RU2370273C2 |
| КОСМЕТИЧЕСКИЙ СПОСОБ ЛЕЧЕНИЯ КОЖИ | 2001 |
|
RU2287321C2 |
| БИОЛОГИЧЕСКИ АКТИВНАЯ ДОБАВКА К ПИЩЕ ORIGITEA ОМОЛОЖЕНИЕ | 2010 |
|
RU2435453C1 |
| ХМЕЛЕВЫЙ ЭКСТРАКТ | 2007 |
|
RU2344167C2 |
| КОМПОЗИЦИЯ ДЛЯ УХОДА ЗА КОЖЕЙ | 1998 |
|
RU2202336C2 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ПАТОЛОГИЧЕСКИХ ПРОЯВЛЕНИЙ КЛИМАКТЕРИЧЕСКОГО СИНДРОМА | 2008 |
|
RU2376026C1 |
| КОМПОЗИЦИИ И СПОСОБЫ | 2014 |
|
RU2664479C2 |
| Способ получения релаксирующей, седативной биологически активной фармакологической композиции, применяемой в вечернее время суток для профилактики дисфункций центральной нервной системы | 2022 |
|
RU2800280C2 |
| КОСМЕТИЧЕСКОЕ СРЕДСТВО НА ОСНОВЕ ФИТОЭСТРОГЕННОГО БИОКОМПЛЕКСА | 2009 |
|
RU2414885C1 |
| ПРИМЕНЕНИЕ ХМЕЛЯ И ОРНИТИНА В КОСМЕТИКЕ | 2001 |
|
RU2281782C2 |
Изобретение относится к биотехнологии. Способ получения 8-пренилнарингенина in vitro включает: а) предоставление первой композиции, включающей культуру бактериальных клеток вида Eubacterium limosum или вида Peptostreptococcus productus, имеющей 5-алкоксифлавоноид-деалкилирующую активность, и b) приведение в контакт второй композиции, включающей 5-алкоксифлавоноиды, с указанной первой композицией, так чтобы сделать возможным деалкилирование указанных 5-алкоксифлавоноидов с помощью указанной культуры бактериальных клеток. Представлена комбинация для получения 8-пренилнарингенина in vitro и применение культуры бактериальных клеток вида Eubacterium limosum или вида Peptostreptococcus productus имеющей 5-алкоксифлавоноид-деалкилирующую активность, для получения 8-пренилнарингенина in vitro. Способ обогащения 5-алкоксифлавоноид-деалкилирующей активности культуры бактериальных клеток вида Eubacterium limosum или вида Peptostreptococcus productus включает стадию посева указанной культуры бактериальных клеток на среду, включающую 5-алкоксифлавоноиды, и стадию селекции колонии, имеющей наивысшую 5-алкоксифлавоноид-деалкилирующую активность. Штамм Eubacterium limosum LMG Р-23546 имеет 5-алкоксифлавоноид-деалкилирующую активность и способен к превращению изоксантогумола в 8-пренилнарингенин. Изобретение позволяет повысить эффективность получения фитоэкстрагена, такого как 8-пренилнарингенина. 5 н. и 9 з.п. ф-лы, 9 ил., 4 табл., 6 пр.
1. Способ получения 8-пренилнарингенина in vitro, включающий:
a) предоставление первой композиции, включающей культуру бактериальных клеток вида Eubacterium limosum или вида Peptostreptococcus productus, имеющей 5-алкоксифлавоноид-деалкилирующую активность, и
b) приведение в контакт второй композиции, включающей 5-алкоксифлавоноиды, с указанной первой композицией, так чтобы сделать возможным деалкилирование указанных 5-алкоксифлавоноидов с помощью указанной культуры бактериальных клеток.
2. Способ по п.1, где указанные 5-алкоксифлавоноиды являются 5-метоксифлавоноидами.
3. Способ по п.1, который дополнительно включает обогащение деалкилирующей активности указанной культуры бактериальных клеток с помощью повторных инкубаций с 5-метоксипренилфлавоноидом.
4. Способ по п.1, где указанным 5-алкоксифлавоноидом является изоксантогумол.
5. Способ по п.1, где указанный 5-алкоксифлавоноид имеет растительное происхождение.
6. Способ по п.5, где указанное растение является хмелем.
7. Применение культуры бактериальных клеток вида Eubacterium limosum или вида Peptostreptococcus productus, имеющей 5-алкоксифлавоноид-деалкилирующую активность, для получения 8-пренилнарингенина in vitro.
8. Комбинация для получения 8-пренилнарингенина in vitro, включающая первую фармацевтическую композицию, содержащую культуру бактериальных клеток вида Eubacterium limosum или вида Peptostreptococcus productus, имеющую 5-алкоксифлавоноид-деалкилирующую активность, и вторую фармацевтическую композицию, включающую источник 5-алкоксифлавоноидов.
9. Комбинация по п.8, где указанный источник 5-алкоксифлавоноидов является экстрактом хмеля.
10. Комбинация по п.8 или 9, где указанный 5-алкоксифлавоноид является изоксантогумолом.
11. Комбинация по п.8, где указанная культура бактериальных клеток представлена в виде состава для специфической доставки в толстую кишку.
12. Способ обогащения 5-алкоксифлавоноид-деалкилирующей активности культуры бактериальных клеток вида Eubacterium limosum или вида Peptostreptococcus productus, включающий стадию посева указанной культуры бактериальных клеток на среду, включающую 5-алкоксифлавоноиды, и стадию селекции колонии, имеющей наивысшую 5-алкоксифлавоноид-деалкилирующую активность.
13. Способ по п.12, где указанную стадию повторяют, по меньшей мере, два раза.
14. Селектированный бактериальный штамм Eubacterium limosum LMG Р-23546, имеющий 5-алкоксифлавоноид-деалкилирующую активность и способный к превращению изоксантогумола в 8-пренилнарингенин.
| HUR Н | |||
| Biotransformation of the isoflavonoids biochanin A, formononetin and glycitein by Eubacterium limosum // FEMS Microbiol Lett | |||
| ЩИТОВОЙ ДЛЯ ВОДОЕМОВ ЗАТВОР | 1922 |
|
SU2000A1 |
| DEJAN NIKOLIC | |||
| Metabolism of xanthohumol and isoxanthohumol, prenylated flavonoids from hops (Humulus lupulus L.), by human liver microsomes // JOURNAL OF MASS SPECTROMETRY, 2005; 40: 289-299 | |||
| СПОСОБ ПОЛУЧЕНИЯ ИЗОМЕРИЗОВАННОГО ЭКСТРАКТА ХМЕЛЯ | 1994 |
|
RU2122417C1 |
Авторы
Даты
2012-04-27—Публикация
2006-03-27—Подача