Настоящее изобретение относится к новым винилогическим производным кислот формулы (I),
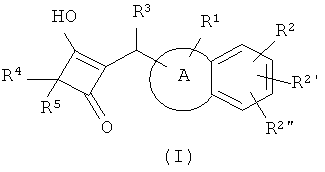
в которой
А обозначает фенильное кольцо, или
гетероарильное кольцо, которое представляет собой моноциклическое ароматическое кольцо, содержащее 5 или 6 кольцевых атомов, содержащее 1 или
2 кольцевых гетероатома, выбранных из группы, включающей N, О и S, остальными являются атомы С, или
гетероциклильное кольцо, которое представляет собой неароматическое моноциклическое кольцо, содержащее 5 или 6 кольцевых атомов, содержащее 1 или 2 кольцевых гетероатома, выбранных из группы, включающей N и S(O)n (где n является целым числом, равным от 0 до 2), остальными являются атомы С, один из кольцевых атомов углерода гетероциклильного кольца необязательно заменен карбонильной группой;
R1 обозначает водород, галоген, нитрогруппу, цианогруппу, аминогруппу, C1-С6-алкил, гетсроалкил, С3-С7-циклоалкил, С2-С6-алкенил, С2-С6-алкинил, гидроксигруппу, C1-С6-алкоксигруппу,
-NR'R", -(С0-С6-алкилен)-NR'R”, где R' и R" независимо выбраны из группы, включающей водород, C1-С6-алкил, гетероалкил, формил, C1-С6-алкилкарбонил, необязательно замещенный С3-С7-циклоалкилкарбонил, необязательно замещенный арилкарбонил, необязательно замещенный гетероарилкарбонил, необязательно замещенный гетероциклилкарбонил, C1-С6-алкилсульфонил, необязательно замещенный С3-С7-циклоалкилсульфонил, необязательно замещенный арилсульфонил, необязательно замещенный гетероарилсульфонил и необязательно замещенный гетероциклилсульфонил, или
-(С0-С6-алкилен)-ОR', где R' обозначает водород, C1-С6-алкил, гетероалкил, формил или C1-С6-алкилкарбонил;
R2, R2' и R2" независимо обозначают водород, галоген, цианогруппу, нитрогруппу, аминогруппу, моно- или ди-C1-С6-алкилзамещенную аминогруппу, C1-С6-алкил, C2-С6-алкенил, C2-С6-алкинил, гетероалкил, гидроксигруппу или C1-С6-алкоксигруппу;
R3 обозначает водород, галоген, цианогруппу, нитрогруппу, аминогруппу, моно- или ди- C1-С6-алкилзамещенную аминогруппу, C1-С6-алкил, C2-С6-алкенил, С2-С6-алкинил, гетероалкил, гидроксигруппу, C1-С6-алкоксигруппу, необязательно замещенный С3-С7-циклоалкил, необязательно замещенный арил, необязательно замещенный гетероарил, необязательно замещенный гетероциклил, необязательно замещенный С3-С7-циклоалкил-C1-С6-алкил, необязательно замещенный арил-C1-С6-алкил, необязательно замещенный гетероарил-C1-С6-алкил или необязательно замещенный гетероциклил-C1-С6-алкил;
R4 обозначает водород, галоген, цианогруппу, нитрогруппу, аминогруппу, моно- или ди- C1-С6-алкилзамещенную аминогруппу, C1-С6-алкил, C2-С6-алкенил, С2-С6-алкинил, гетероалкил, гидроксигруппу, C1-С6-алкоксигруппу, необязательно замещенный С3-С7-циклоалкил, необязательно замещенный арил, необязательно замещенный гетероарил, необязательно замещенный гетероциклил, необязательно замещенный С3-С7-циклоалкил-C1-С6-алкил, необязательно замещенный арил-C1-С6-алкил, необязательно замещенный гетероарил-C1-С6-алкил или необязательно замещенный гетероциклил-C1-С6-алкил;
R5 обозначает водород, галоген или C1-С6-алкил; или R4 и R5 вместе с атомом углерода, к которому они присоединены, образуют необязательно замещенное С3-С7-циклоалкильное кольцо или необязательно замещенное гетероциклильнос кольцо;
и к их пролекарствам и фармацевтически приемлемым солям.
Кроме того, настоящее изобретение относится к способу и промежуточному продукту для получения указанных выше соединений, к фармацевтическим препаратам, которые содержат такие соединения, к применению этих соединений для приготовления фармацевтических препаратов, а также к способу получения промежуточного продукта.
Соединения формулы (I) ингибируют химазу. Химаза представляет собой серинпротеазу, выработка которой ограничивается только подгруппой мастоцитов (Мст - мастоцит). Химаза активируется только при активации и дегрануляции мастоцита, что ограничивает активность фермента тканями, содержащими Мст. Химаза специфически расщепляет ряд связанных с патологиями субстратов (Raymond, W.W., S.W.Ruggles, et al.; JBC 2003 278(36):34517-34524) и при этом она может активировать ангиотензин II, эндотелин, TGFb, I11, SCF, коллагеназу и разрушать белки, такие как тромбин, FN, АРО А1,2. Такие характеристики делают химазу привлекательным объектом воздействия в случае аллергических, воспалительных и фиброзных заболеваний. В действительности, целый ряд успешных исследований на животных с использованием ингибиторов химазы продемонстрировал эффективность в случае аллергических проявлений у животных, поражений сосудов и атеросклероза (Doggrell SA, Wanstall JC Can J Physiol Pharmacol. 2005 Feb; 83(2):123-30; Lindstedt KA, Kovanen PT. Curr Opin Lipidol. 2004 Окт; 15(5):567-73; Reed СЕ, Kita H.J Allergy dm Immunol. 2004 Nov; 114(5):997-1008; Takai S, et al,. Eur J Pharmacol. 2004 Окт 6;501(1-3):1-8; Takai S, et al, Trends Pharmacol Sci. 2004 Окт; 25(10):518-22; Takai S, Miyazaki M. Curr Vase Pharmacol. 2003 Jun; 1(2):217-24).
Таким образом, ингибирование химазы представляется полезной методикой воздействия при аллергии, астме, окклюзионном поражении периферических артерий, критической ишемии конечностей, для пациентов с нестабильными атеросклеротическими бляшками, нестабильной стенокардии, застойной сердечной недостаточности, гипертрофии левого желудочка, ишемическом реперфузионном поражении, кардиомиопатии, рестенозе, ревматоидном артрите, диабетической нефропатии, синдроме раздраженной толстой кишки, болезни Крона, заживлении ран (ожогов/язв при диабете/КИК (критическая ишемия конечностей).
Настоящее изобретение относится к новым соединениям формулы (I), которые являются ингибиторами химазы.
Если не указано иное, то приведенные ниже определения предназначены для иллюстрации и определения значений и области действия различных терминов, использованных при описании настоящего изобретения.
Термин "галоген" означает фтор, хлор, бром или йод, причем хлор и фтор являются предпочтительными.
Термин "C1-С6алкил", по отдельности или в комбинации с другими группами, означает обладающий разветвленной или линейной цепью одновалентный алкильный радикал, содержащий от 1 до 6 атомов углерода. Примерами значений этого термина также являются такие радикалы, как метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, трет-бутил. C1-С4Алкил является более предпочтительным.
Термин "гетероалкил" означает C1-С6-алкил, содержащий один или большее количество заместителей, независимо выбранных из группы, включающей нитрогруппу, гидроксигруппу, галоген, цианогруппу, C1-С6-алкоксигруппу, формил, C1-С6-алкилкарбонил, карбоксигруппу, C1-С6-алкилтио, C1-С6-алкилсульфинил, C1-С6-алкилсульфонил, амино- и моно- или ди- C1-С6-алкилзамещенную аминогруппу. Примерами значений этого термина также являются такие радикалы, как 2-гидроксиэтил, перфторметил. C1-С6-Алкил, замещенный одной гидроксигруппой или одним - тремя одинаковыми или разными атомами галогенов, является предпочтительным.
Термин "С3-С7-циклоалкил", по отдельности или в комбинации с другими группами, означает насыщенный одновалентный циклический углеводородный радикал, содержащий от 1 до 7 кольцевых атомов углерода, например циклопропил, циклобутил, циклогексил.
Термин "C1-С6-алкоксигруппа", по отдельности или в комбинации с другими группами, означает группу R'-O-, в которой R' обозначает C1-С6-алкил.
Термин "С2-С6-алкенил", по отдельности или в комбинации с другими группами, означает обладающий разветвленной или линейной цепью углеводородный остаток, содержащий двойную связь, содержащий от 2 до 6 атомов углерода, такой как, например, этинил, 2-пропенил.
Термин "C2-С6-алкинил", по отдельности или в комбинации с другими группами, означает обладающий разветвленной или линейной цепью углеводородный остаток, содержащий тройную связь, содержащий от 2 до 6 атомов углерода, такой как, например, этинил, 2-пропинил.
Термин "C0-С6-алкилен" означает связь или обладающую разветвленной или линейной цепью двухвалентную насыщенную алифатическую углеводородную группу, содержащую от 1 до 6 атомов углерода. С0-Алкилен означает связь.
Термин "арил", по отдельности или в комбинации с другими группами, означает фенильную или нафтильную группу, предпочтительно фенильную группу.
Термин "гетероциклил", по отдельности или в комбинации с другими группами, означает неароматические моно- или бициклические радикалы, содержащие от 3 до 8 кольцевых атомов, в которых 1 или 2 кольцевых атома являются гетероатомами, выбранными из группы, включающей N, О и S(O)n (где n является целым числом, равным от 0 до 2), остальными являются атомы С.
Термин "гетероарил" означает моноциклический или биоциклический радикал, содержащий от 5 до 12 кольцевых атомов, содержащий по меньшей мере одно ароматическое кольцо, содержащее 1, 2 или 3 кольцевых гетероатомов, выбранных из группы, включающей N, О и S, остальными являются атомы С. Предпочтительно, если положение присоединения гетероарильного радикала находится в ароматическом кольце.
Термин "необязательно замещенный арил", "необязательно замещенный гетероарил", "необязательно замещенный гетероциклил" и "необязательно замещенный С3-С7-циклоалкил" означает соответственно арил, гетероарил, гетероциклил и С3-С7-циклоалкил, необязательно содержащий один или большее количество заместителей, независимо выбранных из группы, включающей галоген, нитрогруппу, цианогруппу, аминогруппу, C1-С6-алкил, C2-С6-алкенил, C2-С6-алкинил, гидроксигруппу, C1-С6-алкоксигруппу, моно- или ди-C1-С6-алкилзамещенную аминогруппу и гетероалкил.
Предпочтительными радикалами для химических групп, определения которых приведены выше, являются те, которые специально указаны в примерах в качестве примеров.
Соединения формулы (I) могут образовывать фармацевтически приемлемые соли присоединения с кислотами. Примерами таких фармацевтически приемлемых солей являются соли соединений формулы (I) с физиологически совместимыми неорганическими кислотами, такими как хлористоводородная кислота, серная кислота, сернистая кислота или фосфорная кислота; или с органическими кислотами, такими как метансульфоновая кислота, n-толуолсульфоновая кислота, уксусная кислота, молочная кислота, трифторуксусная кислота, лимонная кислота, фумаровая кислота, малеиновая кислота, винная кислота, янтарная кислота или салициловая кислота. Термин "фармацевтически приемлемые соли" означает такие соли. Соединения формулы (I), в которых содержится группа СООН, также могут образовывать соли с основаниями. Примерами таких солей являются соли щелочных и щелочноземельных металлов и аммония, такие как, например, соли Na, K, Са и триметиламмония. Термин "фармацевтически приемлемые соли" означает и такие соли. Соли присоединения с кислотами, описанные выше, являются предпочтительными.
"Необязательно" или "необязательный" означает, что последующее описанное событие или обстоятельство может, но не должно осуществиться, и что описание включает случаи, когда событие или обстоятельство осуществляется, и случаи, когда оно не осуществляется. Например, "арильная группа, необязательно замещенная алкильной группой", означает, что алкильная группа может, но не должна содержаться, и описание включает случаи, когда арильная группа замещена алкильной группой, и случаи, когда арильная группа не замещена алкильной группой.
"Фармацевтически приемлемый инертный наполнитель" означает инертный наполнитель, который является пригодным для приготовления фармацевтической композиции, обычно безопасный, нетоксичный и биологически и в других отношениях не являющийся нежелательным, и включает инертные наполнители, которые приемлемы для ветеринарии, а также для применения в фармацевтических средствах, предназначенных для людей. "Фармацевтически приемлемый инертный наполнитель" при использовании в настоящем изобретении включает один или более чем один такой инертный наполнитель.
Соединения, которые обладают одинаковыми молекулярными формулами, но различаются по природе и последовательности связывания атомов или по расположению атомов в пространстве, называются "изомерами". Изомеры, которые различаются по расположению атомов в пространстве, называются "стереоизомерами". Стереоизомеры, которые не являются зеркальными отображениями друг друга, называются "диастереоизомерами" и те, зеркальные отображения которых не налагаются друг на друга, называются "энантиомерами". Если соединение содержит асимметрический центр, например, если атом углерода связан с четырьмя разными группами, возможно образование пары энантиомеров. Энантиомер можно охарактеризовать абсолютной конфигурацией его асимметрического центра и она описывается с помощью правил последовательности R- и S-конфигураций Кана, Ингольда и Прелога или путем указания того, как молекула вращает плоскость поляризованного света, т.е. является ли она правовращающей или левовращающей (т.е. указываются (+) или (-)-изомеры соответственно). Хиральное соединение может существовать в виде отдельных энантиомеров или в виде их смеси. Смесь, содержащая одинаковые количества энантиомеров, называется "рацемической смесью".
Соединения формулы (I) может содержать один или большее количество асимметрических центров. Если не указано иное, то описание или название конкретного соединения в описании изобретения и формуле изобретения включает отдельные энантиомеры и их смеси, рацемические и другие, а также индивидуальные эпимеры и их смесь. Методики определения стереохимической конфигурации и разделения стереоизомеров хорошо известны в данной области техники (см. обсуждение в гл. 4 публикации "Advanced Organic Chemistry", 4th edition J. March, John Wiley and Sons, New York, 1992).
Хотя выше описан наиболее широкий вариант настоящего изобретения, соединения формулы (I), содержащие некоторые радикалы, являются предпочтительными.
В соединениях формулы (I),
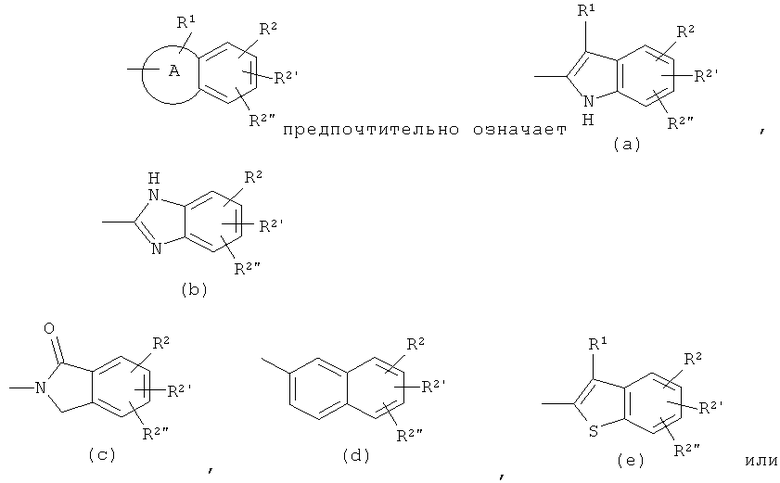
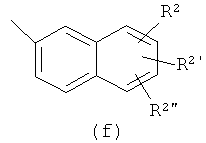 , более предпочтительно - (a), (d), (e) или (f), еще более предпочтительно (а), (e) или (f) и особенно предпочтительным является (а).
, более предпочтительно - (a), (d), (e) или (f), еще более предпочтительно (а), (e) или (f) и особенно предпочтительным является (а).
В соединениях формулы (I), R3 предпочтительно обозначает C1-С6-алкил, необязательно замещенный арил, необязательно замещенный гетероарил, необязательно замещенный арил-C1-С6-алкил или необязательно замещенный гетероарил-C1-С6-алкил, более предпочтительно, если R3 обозначает C1-С6-алкил, фенил, необязательно замещенный 1-3 атомами фтора, гетероарил, необязательно замещенный 1-3 атомами фтора, где гетероарил представляет собой моноциклический ароматический радикал, содержащий 5 или 6 кольцевых атомов, содержащий 1 или 2 кольцевых атома азота, или фенил-C1-С6-алкил, и R3 предпочтительно обозначает фенил.
В соединениях формулы (I) R1 предпочтительно обозначает водород, С1-С6-алкил, C1-С6-алкоксигруппу, -(C0-С6-алкилен)-NR'R", где R' и R" независимо выбраны из группы, включающей водород, формил, C1-С6-алкилкарбонил, необязательно замещенный арилкарбонил, необязательно замещенный гетероарилкарбонил, необязательно замещенный арилсульфонил и необязательно замещенный гетероарилсульфонил или -(С0-С6-алкилен)-ОR', где R' обозначает водород или C1-С6-алкилкарбонил. Более предпочтительно, если R1 обозначает C1-С6-алкил, -(С2-С6-алкилен)-NR'R", где R' и R" независимо выбраны из группы, включающей водород, формил, ацетил, арилкарбонил, где арил необязательно замещен одной или двумя перфторметильными группами, и арилсульфонил или -(С2-С6-алкилен)-ОR', где R' обозначает водород или ацетил. Еще более предпочтительно, если R1 обозначает 2-аминоэтил, 2-ацетиламиноэтил, 2-(N-формил-N-метиламино)этил, 2-ацетиламино-2,2-диметилэтил, метил, изопропил или 2-гидроксиэтил. Предпочтительно, если R1 обозначает метил, 2-ацетиламиноэтил, 2-ацетиламино-2,2-диметилэтил или 2-(N-формил-N-метиламино)этил.
В соединениях формулы (1), R2, R2' и R2" предпочтительно независимо обозначают водород, галоген, C1-С6-алкил или C1-С6-алкоксигруппу. Более предпочтительно, если два из R2, R2' и R2" обозначают водород и третий обозначает водород, галоген, C1-С6-алкил или C1-С6-алкоксигруппу. Еще более предпочтительно, если два из R2, R2' и R2" обозначают водород и третий обозначает водород, хлор, фтор, метил, этил или метоксигруппу. Предпочтительно, если два из R2, R2' и R2" обозначают водород и третий обозначает водород, фтор или метил.
В соединениях формулы (1), R4 предпочтительно обозначает водород, С1-С6-алкил, необязательно замещенный С3-С7-циклоалкил, необязательно замещенный арил, необязательно замещенный С3-С7-циклоалкил-C1-С6-алкил или необязательно замещенный арил-C1-С6-алкил; или R4 и R5 вместе с атомом углерода, к которому они присоединены, образуют необязательно замещенное С3-С7-циклоалкильное кольцо. Более предпочтительно, если R4 обозначает С1-С6-алкил, необязательно замещенный арил или необязательно замещенный арил-C1-С6-алкил, и R5 обозначает галоген или C1-С6-алкил. Предпочтительно, если R4 обозначает фенил или 4-метилфенил, и R5 обозначает метил.
Предпочтительным соединением, предлагаемым в настоящем изобретении, является соединение формулы (I), которое представляет собой
N-(2-{2-[(2-Гидрокси-3-метил-4-оксо-3-фенилциклобут-1-енил)-фенилметил]-6-метил-1Н-индол-3-ил}-1,1-диметилэтил)-ацетамид,
3-Гидрокси-4-метил-2-[(3-метил-1Н-индол-2-ил)-фенилметил]-4-фенилциклобут-2-енон,
2-[(3,5-Диметил-1Н-индол-2-ил)-фенилметил]-3-гидрокси-4-метил-4-фенилциклобут-2-енон,
2-[(3,6-Диметил-1Н-индол-2-ил)-фенилметил]-3-гидрокси-4-метил-4-фенилциклобут-2-енон,
2-[(5-Фтор-3-метил-1Н-индол-2-ил)-фенилметил]-3-гидрокси-4-метил-4-фенилциклобут-2-енон,
N-{2-[(2-Гидрокси-3-метил-4-оксо-3-фенилциклобут-1-енил)-фенилметил]-6-метил-1Н-индол-3-илметил}-ацетамид,
3-Гидрокси-4-метил-2-[(3-метил-1Н-индол-2-ил)-фенилметил]-4-п- толилциклобут-2-енон,
2-[(3,5-Диметил-1Н-индол-2-ил)-фенилметил]-3-гидрокси-4-метил-4-п-толилциклобут-2-енон,
2-[(3,6-Диметил-1Н-индол-2-ил)-фенилметил]-3-гидрокси-4-метил-4-п-толилциклобут-2-енон,
2-[(5-Фтор-3-метил-1Н-индол-2-ил)-фенилметил]-3-гидрокси-4-метил-4-п-толилциклобут-2-енон,
N-{2-[(2-Гидpoкcи-3-мeтил-4-oкco-3-п-тoлилциклoбyт-1-eнил)-фeнилмeтил]-6-метил-1Н-индол-3-илметил}-ацстамид или
N-{2-[(2-Гидрокси-3-метил-4-оксо-3-п-толилциклобут-1-енил)-фенилметил]-6-метил-1Н-индол-3-илметил}-N-метилформамид.
Соединения, предлагаемые в настоящем изобретении, можно получить, например, по общим методикам синтеза, описанным ниже.
Общие методики синтеза
I) Соединения формулы (I), в которой
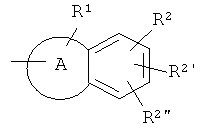
обозначает
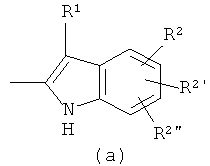
(где R1, R2, R2' и R2” являются такими, как определено выше) можно получить в соответствии с приведенной ниже схемой 1:

R3, R4 и R5 являются такими, как определено выше. Аr обозначает
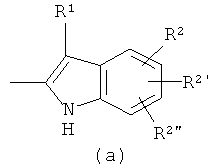
и Аr' обозначает
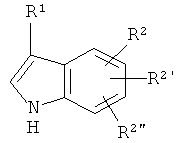 ,
,
где R1, R2, R2', R2” являются такими, как определено выше.
Сочетание дикетона II (существует в виде равновесной смеси кето- и енольной формы), альдегида III и ароматического соединения IV с образованием винилогической кислоты 1 можно провести в растворителе, таком как СН3СN, или в кислоте, такой как карбоновая кислота, например муравьиная кислота, или, предпочтительно, уксусная кислота, при температуре в диапазоне 22-100°С, предпочтительно - при 22°С в течение 1-20 ч.
II) Соединения формулы (I),
в которой
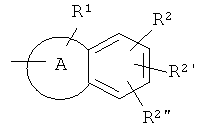
обозначает
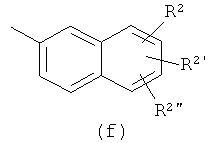
или
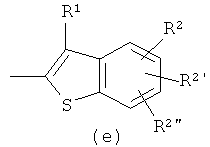
(где R1, R2, R2' и R2" являются такими, как определено выше), можно получить в соответствии с приведенной ниже схемой 2:
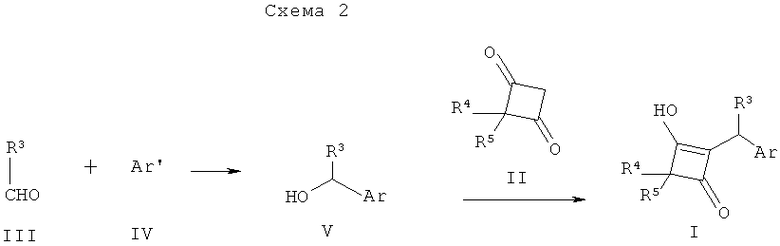 R3, R4 и R5 являются такими, как определено выше. Аr обозначает
R3, R4 и R5 являются такими, как определено выше. Аr обозначает
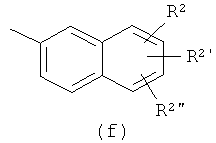
или
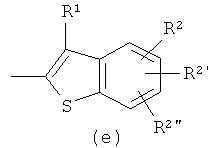
и Ar' обозначает
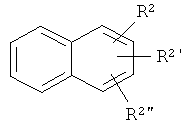
или
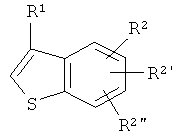
(где R1, R2, R2' и R2" являются такими, как определено выше).
Ароматическое соединение Аr IV, такое как 2-галогензамещенные производные нафталина или производные бензотиофена, можно литиировать в положении 2 алкиллитиевым реагентом, таким как н-бутиллитий, в растворителе, таком как, например, этиловый эфир, или, предпочтительно, тетрагидрофуран при температуре от -100 до 60°С, предпочтительно при -80°С. Полученный литиированный промежуточный продукт можно ввести в реакцию с альдегидом III при температуре от -80 до 22°С и получить спирт V.
Спирт V можно ввести в реакцию с дикетоном II в присутствии карбоновой кислоты, например уксусной кислоты, или, предпочтительно, трифторуксусной кислоты в растворителе, таком как простой эфир или, предпочтительно, дихлорметан при температуре в диапазоне 22-50°С, предпочтительно при 22°С в течение 1-20 ч, и получить винилогическую кислоту I.
III) Исходные вещества формулы II можно получить в соответствии с приведенной ниже схемой 3:
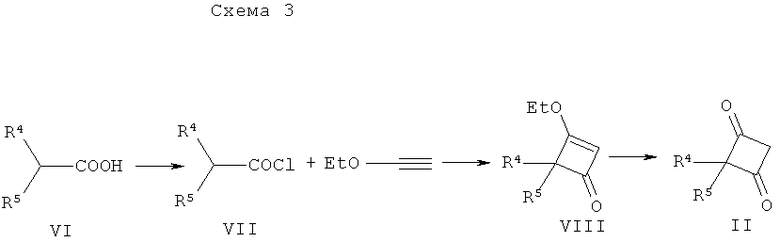 R4 и R5 являются такими, как определено выше.
R4 и R5 являются такими, как определено выше.
Кислоту VI можно превратить в хлорангидрид кислоты по стандартным методикам с использованием оксалилхлорида или, предпочтительно, тионилхлорида и получить хлорангидрид кислоты VII. Хлорангидрид кислоты можно ввести в реакцию с этоксиацетиленом в присутствии основания, такого как алкиламин, предпочтительно триэтиламин в растворителе, таком как простой эфир, предпочтительно диэтиловый эфир, при температуре 0-40°С, предпочтительно - при 40°С, и получить этиловый сложный эфир VIII. Гидролиз этилового эфира VIII можно провести с помощью сильной неорганической кислоты, предпочтительно хлористоводородной кислоты в растворителе, таком как простой эфир, предпочтительно тетрагидрофуран при температуре 0-60°С, предпочтительно при 22°С и получить дикетон II.
Исходное вещество формулы II можно получить в соответствии с указанной ниже литературой:
1) Brand, Stephen et al., Organic Letters (2003), 5(13), 2343-2346.
IV) Исходные вещества формулы III имеются в продаже.
V) Большинство ароматических соединений формулы IV имеется в продаже или специалист в данной области техники может их получить на основе своей подготовки. Соединения формулы IV также можно получить в соответствии с указанной ниже литературой:
2) Kreighbaum, William E. et al., J. Med. Chem. (1980), 23(3), 285-9.
3) Yang, Shyh-Chyun et al., Indian Journal of Chemistry, Section B: Organic Chemistry Including Medicinal Chemistry (1999), 38B(8), 897-904.
4) Tsuchiya, Michihiro et al., international patent application, WO8200032 (1982).
5) Hengartner, Urs et al., Journal of Organic Chemistry (1979), 44(22), 3741-7.
6) Somei, Masanori et al., Heterocycles (1992), 33(1), 77-80.
VI) Все исходные вещества формулы VI имеются в продаже.
Как указано выше, соединения формулы (I) являются активными соединениями и ингибируют химазу. Следовательно, эти соединения предотвращают активацию ангиотензина II, эндотелина, TGFb, I11, SCF, коллагеназы и разрушение белков, таких как тромбин, FN, АРО А1,2. Поэтому их можно использовать для предупреждения и/или лечения аллергических, воспалительных и/или фиброзных заболеваний, таких как аллергия, астма, окклюзионное поражение периферических артерий, критическая ишемия конечностей, для пациентов с нестабильными атеросклеротическими бляшками, нестабильная стенокардия, застойная сердечная недостаточность, гипертрофия левого желудочка, ишемическое реперфузионное поражение, удар, кардиомиопатия, рестеноз, ревматоидный артрит, диабетическая нефропатия, синдром раздраженной толстой кишки, болезнь Крона, атеротромбоз и/или ожоги/язвы при диабете/КИК.
Предупреждение и/или лечение аллергических, воспалительных или фиброзных заболеваний, предпочтительно атеротромбоза или астмы, является предпочтительным показанием.
Поэтому настоящее изобретение также относится к фармацевтическим композициям, включающим соединение, определенное выше, и фармацевтически приемлемый инертный наполнитель.
Настоящее изобретение также относится к соединениям, описанным выше, предназначенным для применения в качестве терапевтически активных веществ, предпочтительно в качестве терапевтически активных веществ, предназначенных для лечения и/или профилактики аллергических, воспалительных и/или фиброзных заболеваний, более предпочтительно в качестве терапевтически активных веществ, предназначенных для лечения и/или профилактики аллергии, астмы, окклюзионного поражения периферических артерий, критической ишемии конечностей, для пациентов с нестабильными атеросклеротическими бляшками, нестабильной стенокардии, застойной сердечной недостаточности, гипертрофии левого желудочка, ишемического реперфузионного поражения, удара, кардиомиопатии, рестеноза, ревматоидного артрита, диабетической нефропатии, синдрома раздраженной толстой кишки, болезни Крона, атеротромбоза и/или ожогов/язв при диабете/КИК.
Настоящее изобретение также относится к применению соединений, описанных выше, для приготовления лекарственных средств, предназначенных для терапевтического и/или профилактического лечения аллергических, воспалительных и/или фиброзных заболеваний, предпочтительно терапевтического и/или профилактического лечения аллергии, астмы, окклюзионного поражения периферических артерий, критической ишемии конечностей, для пациентов с нестабильными атеросклеротическими бляшками, нестабильной стенокардии, застойной сердечной недостаточности, гипертрофии левого желудочка, ишемического реперфузионного поражения, удара, кардиомиопатии, рестеноза, ревматоидного артрита, диабетической нефропатии, синдрома раздраженной толстой кишки, болезни Крона, атеротромбоза и/или ожогов/язв при диабете/КИК. Такие лекарственные средства содержат соединение, описанное выше.
Настоящее изобретение также относится к способу и промежуточным продуктам для получения соединений формулы (I), а также к способу получения промежуточных продуктов.
Ингибирование химазы соединениями, предлагаемыми в настоящем изобретении, можно продемонстрировать с помощью исследования пептидного субстрата, описанного ниже в настоящем изобретении.
Для химазы выбран субстрат, представляющий собой содержащий 4 аминокислоты пептид AAPF, являющийся стандартным субстратом для соединений типа химотрипсина (сукцинил-Аlа-Аlа-Pro-Phe-[7-амино-4-метилкумарин];Lockhart BE, et al., "Recombinant human mast-cell chymase: an improved procedure for expression in Pichia pastoris and purification of the highly active enzyme." Вiotechnol Appl Biochem, published as immediate publication 26 May 2004 as manuscript BA20040074). Пептид чистотой 95% синтезирован фирмой Bachem, Bubendorf, Switzerland)). Химазу, выделенную из мастоцитов кожи человека, получали от фирмы Calbiochem (Merck Biosciences, San Diego, California, USA). Использовали буфер для анализа, содержащий 0,15 М NaCl, 0,05М, Tris-HCl [Tris - трис(гидроксиметиламинометан)], 0,05% CHAPS (3-[(3-холамидопропил)-диметиламмонио]-1-пропансульфонат), 0,1 мг/мл гепарин (натриевая соль гепарина, Sigma, из слизистой оболочки кишечника свиньи), 0,02 мМ субстрат AAPF, 1 нМ химаза при рН 7,4. Исследование проводили в 96-луночных планшетах (Packard Optiplate) при объеме, равном 0,05 мл, при комнатной температуре. Активность химазы оценивали по начальной скорости усиления флуоресценции при 340/440 нм (возбуждение/испускание) свободного 7-амино-4-метилкумарина, выделяющегося из субстрата. Ингибирование активности ингибирующими соединениями определяли после проводимой в течение 30 мин предварительной инкубации с химазой при комнатной температуре в буфере для анализа, к которому не прибавляли субстрат AAPF. Затем прибавляли субстрат AAPF в указанной концентрации и начинали исследование.
Значения IC50 для активных соединений, предлагаемых в настоящем изобретении, предпочтительно составляют примерно от 1000 до 1 нМ, предпочтительно примерно от 50 до 1 нМ.
Соединения формулы (I) и/или их фармацевтически приемлемые соли можно использовать в качестве лекарственных средств, например, в форме фармацевтических препаратов для энтерального, парентерального или местного введения. Их можно вводить, например, перорально, например в форме таблеток, таблеток с покрытием, драже, капсул из твердого или мягкого желатина, растворов, эмульсий или суспензий, ректально, например в форме суппозиториев, парентерально, например в форме растворов для инъекций или растворов для вливания, или местно, например в форме мазей, кремов или масел. Пероральное введение является предпочтительным.
Приготовление фармацевтических препаратов можно осуществлять способом, который известен любому специалисту в данной области техники, путем внесения описанных соединений формулы 1 и/или их фармацевтически приемлемых солей, необязательно в комбинации с другими терапевтически ценными веществами, в галенову дозированную форму совместно с подходящими нетоксичными, инертными, терапевтически совместимыми твердыми или жидкими носителями и при необходимости с обычными фармацевтическими вспомогательными веществами.
Подходящими носителями являются не только неорганические носители, но и органические носители. Так, например, лактозу, кукурузный крахмал или его производные, тальк, стеариновую кислоту или ее соли и т.п. можно использовать в качестве носителей для таблеток, таблеток с покрытием, драже и капсул из твердого желатина. Для капсул из мягкого желатина подходящими носителями являются, например, растительные масла, воска, жиры и полужидкие и жидкие полиолы (однако в зависимости от природы активного вещества в случае капсул из мягкого желатина носитель обычно не требуется). Носителями, подходящими для приготовления растворов и сиропов, являются, например, вода, полиолы, сахароза, инвертный сахар и т.п. Носителями, подходящими для растворов для инъекций, являются, например, вода, спирты, полиолы, глицерин и растительные масла. Носителями, подходящими для суппозиториев, являются, например, натуральные или отвержденные масла, воска, жиры и полужидкие и жидкие полиолы. Носителями, подходящими для препаратов местного действия, являются глицериды, полусинтетические и синтетические глицериды, гидрированные масла, жидкие воска, жидкие парафины, жидкие жирные спирты, стерины, полиэтиленгликоли и производные целлюлозы.
В качестве фармацевтических вспомогательных веществ в рассмотрение включаются обычные стабилизаторы, консерванты, смачивающие и эмульгирующие агенты, улучшающие консистенцию агенты, улучшающие вкус агенты, соли для регулирования осмотического давления, буферные вещества, солюбилизаторы, красители и маскирующие агенты и антиоксиданты.
Дозировка соединений формулы (I) может меняться в широких пределах в зависимости от подвергающегося лечению заболевания, возраста и индивидуального состояния пациента и пути введения и, разумеется, в каждом конкретном случае будет меняться в соответствии с индивидуальными потребностями. Для взрослых пациентов в рассмотрение включается суточная доза, составляющая примерно от 1 до 1000 мг, предпочтительно примерно от 1 до 300 мг. В зависимости от тяжести заболевания и точного фармакокинетического профиля соединение можно вводить в виде одной или нескольких разовых доз в сутки, например в виде 1-3 разовых доз.
Фармацевтические препараты обычно содержат примерно 1-500 мг, предпочтительно 1-100 мг соединения формулы (I).
Примеры
Приведенные ниже примеры предназначены для более подробной иллюстрации настоящего изобретения. Однако они не предназначены для какого-либо ограничения объема настоящего изобретения.
Общая методика А: Получение дикетона II
А1. Смесь кислоты VI (30 ммолей) в толуоле (10 мл) обрабатывали тионилхлоридом (90 ммолей) и кипятили с обратным холодильником в течение примерно 1 ч до прекращения выделения газа. Смесь выпаривали досуха и получали хлорангидрид кислоты VII, который использовали без дополнительной очистки.
А2. К раствору хлорангидрида кислоты VII (30 ммолей) и этоксиацетилена (40% в гексане, 60 ммолей) в диэтиловом эфире (70 мл) при 22°С при перемешивании прибавляли триэтиламин (50 ммолей) и продолжали перемешивание при кипячении с обратным холодильником в течение 20 ч. Суспензию фильтровали, фильтрат выпаривали и остаток хроматографировали на диоксиде кремния и получали сложный этиловый эфир VIII.
A3. Смесь сложного этилового эфира VIII (2 ммоля) и водного раствора хлористоводородной кислоты (25%, 1,5 мл) в тетрагидрофуране (2 мл) перемешивали при 22°С в течение 16 ч. Смесь выпаривали и остаток подвергали распределению между водным раствором хлористоводородной кислоты (1 н.) и этилацетатом. Органический слой выпаривали досуха и хроматографировали на диоксиде кремния и получали дикетон II.
Общая методика В: Получение спиртов V
К раствору замещенного 2-бромнафталина (10 ммолей) или замещенного бензотиофена (10 ммолей) в тетрагидрофуране (150 мл) при -78°С прибавляли н-бутиллитий (1,6 М в н-гексане, 11 ммолей) и перемешивание продолжали при -78°С в течение 1 ч (в случае замещенных бензотиофснов перемешивание продолжали при 22°С, затем охлаждали до -78°С). Смесь обрабатывали раствором альдегида III (10 ммолей) в тетрагидрофуране (20 мл) и перемешивание продолжали в течение 30 мин. Реакцию останавливали насыщенным раствором NH4Cl и смесь экстрагировали этилацетатом. Органический слой выпаривали досуха и остаток хроматографировали на диоксиде кремния и получали спирты V.
Общая методика С: Реакция сочетания дикетона II, альдегида III и ароматического соединения, такого как индол IV
Раствор дикетона II (1 ммоль), альдегида III (1,3 ммоля) и индола IV (1 ммоль) в уксусной кислоте (4 мл) перемешивали при 22°С в течение 16 ч. Суспензию фильтровали и остаток промывали пентаном. Если не выпадал осадок, то раствор очищали с помощью препаративной ВЖЭХ (высокоэффективная жидкостная хроматография) (RP-18, CH3CN/H2O, градиентный режим) и получали винилогические кислоты I
Общая методика D: Реакция сочетания дикетона II и спирта V
Раствор дикетона II (0,2 ммоля) и спирта V (0,2 ммоля) в дихлорметане (2 мл) прибавляли к трифторуксусной кислоте (0,4 ммоля) и перемешивание продолжали при 22°С в течение 6 ч. Суспензию выпаривали и остаток промывали н-пентаном. Если не выпадал осадок, то раствор очищали с помощью препаративной ВЖЭХ (RP-18, СН3СN/Н2О, градиентный режим) и получали винилогические кислоты I.
Пример 1
N-(2-{2-[(2-Гидрокси-3-изобутил-3-метил-4-оксоцикло6ут-1-енил)-фенилметил]-6-метил-1Н-индол-3-ил}-1,1-диметилэтил)-ацетамид
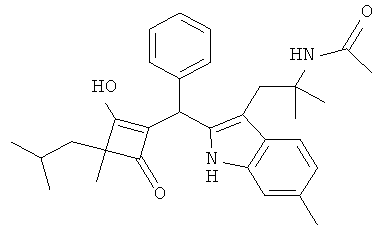
1.1. С использованием общей методики А 2,4-диметилпентановую кислоту превращали в 2-изобутил-2-метилциклобутан-1,3-дион, который получали в виде коричневого масла. МС (масс-спектрометрия): 153,4 ([М-Н]-).
1.2. Раствор 1,1-диметил-2-(6-метил-1Н-индол-3-ил)-этиламина(2 ммоля, получали так, как описано в публикации 2) и ангидрида уксусной кислоты (2,2 ммоля) в дихлорметане (3 мл) обрабатывали триэтиламином (6 ммолей) и смесь перемешивали при 22°С в течение 18 ч. Смесь промывали водным раствором хлористоводородной кислоты (1 н.), органический слой сушили и выпаривали и получали N-[1,1-диметил-2-(6-метил-1Н-индол-3-ил)-этил]-ацетамид в виде коричневатого твердого вещества. МС: 243,2 ([М-Н]-).
1.3. С использованием общей методики С 2-изобутил-2-метилциклобутан-1,3-дион вводили в реакцию с бензальдегидом и N-[1,1-диметил-2-(6-метил-1Н-индол-3-ил)-этил]-ацетамидом и получали N-(2-{2-[(2-гидрокси-3-изобутил-3-метил-4-оксоциклобут-1-енил)-фенилметил]-6-метил-1Н-индол-3-ил}-1,1-диметилэтил)-ацетамид в виде бледно-коричневого твердого вещества. МС: 485,6 ([М-Н]-).
Пример 2
N-(2-{2-[(3-Бензил-2-гидрокси-3-метил-4-оксоциклобут-1-енил)-фенилметил]-6-метил-1Н-индол-3-ил}-1,1-диметилэтил)-ацетамид
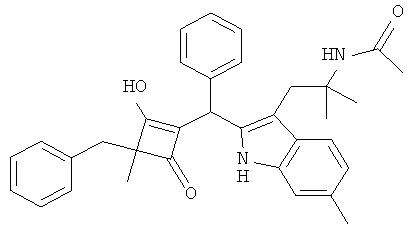
С использованием общей методики С 2-бензил-2-метилциклобутан-1,3-дион (публикация 1) вводили в реакцию с бензальдегидом и N-[1,1-диметил-2-(6-метил-1Н-индол-3-ил)-этил]-ацетамидом (из примера 1.2) и получали искомое соединение в виде красного твердого вещества. МС: 519,5 ([М-Н]-).
Пример 3
N-(2-{2-[(2-Гидрокеи-3-метил-4-оксо-3-фенилциклобут-1-енил)-фенилмстил]-6-метил-1 Н-индол-3-ил}-1,1-диметилэтил)-ацетамид
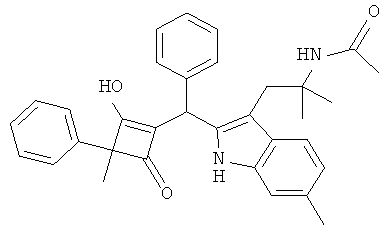
С использованием общей методики С 2-метил-2-фенилциклобутан-1,3-дион (публикация 1) вводили в реакцию с бензальдегидом и N-[1,1-диметил-2-(6-метил-1Н-индол-3-ил)-этил]-ацетамидом (из примера 1.2) и получали искомое соединение в виде бледно-желтого твердого вещества. МС: 505,5 ([М-Н]-).
Пример 4
N-(2-{2-[(2-Гидрокси-3-метил-4-оксо-3-п-толилциклобут-1-енил)-фенилметил]-6-метил-1Н-индол-3-ил}-1,1-диметилэтил)-ацетамид
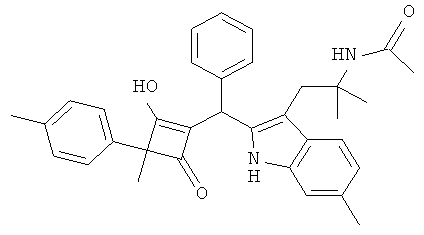
4.1. С использованием общей методики А 2-п-толилпропионовую кислоту превращали в 2-метил-2-п-толилциклобутан-1,3-дион, который получали в виде коричневого масла. МС: 187,4 ([М-Н]-).
4.2. С использованием общей методики С 2-метил-2-п-толилциклобутан-1,3-дион вводили в реакцию с бензальдегидом и N-[1,1-диметил-2-(6-метил-1Н-индол-3-ил)-этил]-ацетамидом (из примера 1.2) и получали N-(2-{2-[(2-гидрокси-3-метил-4-оксо-3-п-толилциклобут-1-енил)-фенилметил]-6-метил-1Н-индол-3-ил}-1,1-диметилэтил)-ацетамид в виде бледно-желтого твердого вещества. МС: 519,5 ([М-Н]-).
Пример 5
N-[2-(2-{[3-(4-Хлорфенил)-2-гидрокси-3-метил-4-оксоциклобут-1-енил]-фенилметил}-6-метил-1Н-индол-3-ил)-1,1-диметилэтил]-ацетамид
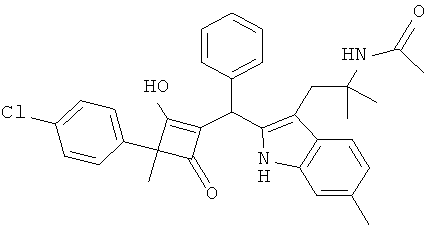
5.1. С использованием общей методики А 2-(4-хлорфенил)-пропионовую кислоту превращали в 2-(4-хлорфенил)-2-метилциклобутан-1,3-дион, который получали в виде коричневого масла. МС: 206,9 ([М-Н]-).
5.2. С использованием общей методики С 2-(4-хлорфенил)-2-метилциклобутан-1,3-дион вводили в реакцию с бензальдегидом и N-[1,1-диметил-2-(6-метил-1Н-индол-3-ил)-этил]-ацетамидом (из примера 1.2) и получали N-[2-(2-{[3-(4-хлорфенил)-2-гидрокси-3-метил-4-оксоциклобут-1-енил]-фенилметил}-6-метил-1Н-индол-3-ил)-1,1-диметилэтил]-ацетамид в виде бледно-желтого твердого вещества. МС: 539,5 ([М-Н]-).
Пример 6
3-Гидрокси-4-метил-2-[(3-метил-1Н-индол-2-ил)-фенилметил]-4-фенилциклобут-2-енон
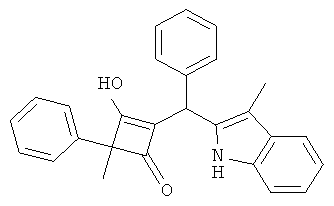
С использованием общей методики С 2-метил-2-фенилциклобутан-1,3-дион (публикация 1) вводили в реакцию с бензальдегидом и 3-метил-1H-индолом и получали искомое соединение в виде бесцветного твердого вещества. МС: 392,3 ([М-Н]-).
Пример 7
2-[(3,5-Диметил-1Н-индол-2-ил)-фенилметил]-3-гидрокси-4-метил-4-фенилциклобут-2-енон
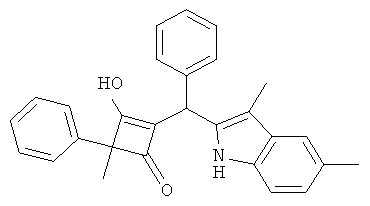
С использованием общей методики С 2-метил-2-фенилциклобутан-1,3-дион (публикация 1) вводили в реакцию с бензальдегидом и 3,5-диметил-1Н-индолом (публикация 3) и получали искомое соединение в виде бесцветного твердого вещества. МС: 406,5 ([М-Н]-).
Пример 8
2-[(3,6-Диметил-1Н-индол-2-ил)-фенилметил]-3-гидрокси-4-метил-4-фенилциклобут-2-енон
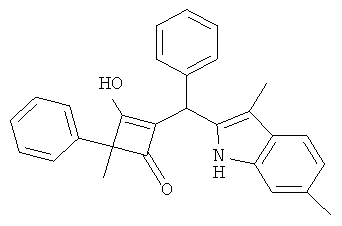
С использованием общей методики С 2-метил-2-фенилциклобутан-1,3-дион (публикация 1) вводили в реакцию с бензальдегидом и 3,6-диметил-1H-индолом (публикация 4) и получали искомое соединение в виде бесцветного твердого вещества. МС: 406,4 ([М-Н]-).
Пример 9
2-[(5-Фтор-3-метил-1Н-индол-2-ил)-фенилметил]-3-гидрокси-4-метил-4-фенилциклобут-2-снон
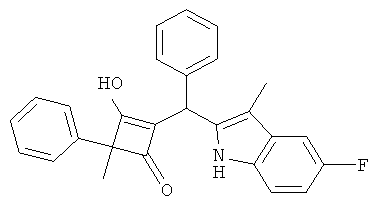
С использованием общей методики С 2-метил-2-фенилциклобутан-1,3-дион (публикация 1) вводили в реакцию с бензальдегидом и 5-фтор-3-метил-1H-индолом и получали искомое соединение в виде бесцветного твердого вещества. МС: 410,3 ([М-Н]-).
Пример 10
N-{2-[(2-Гидрокси-3-метил-4-оксо-3-фенилциклобут-1-енил)-фенилметил]-6-метил-1Н-индол-3-илметил}-ацетамид
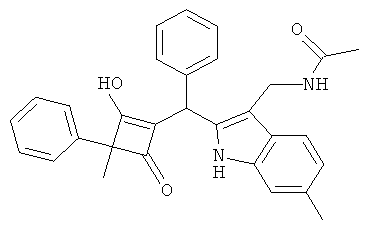
10.1. К раствору 6-метил-1Н-индол-3-карбальдегида (0,96 г, публикация 5) в этаноле (30 мл) при 22°С прибавляли гидроксиламингидрохлорид (0,46 г) и ацетат натрия (0,54 г) и смесь перемешивали в течение 3 ч. Смесь выпаривали и остаток растирали с водой и смесью дихлорметан/н-гептан (1:1) и сушили и получали 6-метил-1H-индол-3-карбальдегидоксим (0,96 г) в виде розового твердого вещества. МС: 175,3 ([М+Н]+).
10.2. К смеси 6-метил-1H-индол-3-карбальдегидоксима (0,66 г) и NiCl2·6H2O (0,97 г) в метаноле (60 мл) при 22°С порциями прибавляли борогидрид натрия (3,04 г). Суспензию фильтровали и фильтрат выпаривали. Остаток подвергали распределению между водным раствором NН3 (1%) и этилацетатом, органический слой сушили и выпаривали и получали неочищенный С-(6-метил-1Н-индол-3-ил)-метиламин в виде желтого полутвердого вещества (0,68 г).
10.3. К раствору С-(6-метил-1Н-индол-3-ил)-метиламина (0,24 г) в дихлорметане (4 мл) прибавляли ангидрид уксусной кислоты (0,14 мл) и пиридин (0,13 мл) и перемешивание продолжали при 22°С в течение 20 мин. Смесь промывали водным раствором НСl (1 н.), органический слой сушили и выпаривали. Остаток хроматографировали на диоксиде кремния с использованием смеси дихлорметан/метанол (70:1) и получали N-(6-метил-1Н-индол-3-илметил)-ацетамид в виде бесцветного вспененного вещества (0,15 г). МС: 203,1 ([М+Н]+).
10.4. С использованием общей методики С 2-метил-2-фенилциклобутан-1,3-дион (публикация 1) вводили в реакцию с бензальдегидом и N-(6-метил-1Н-индол-3-илметил)-ацетамидом и получали N-{2-[(2-гидрокси-3-метил-4-оксо-3-фенилциклобут-1-енил)-фенилметил]-6-метил-1Н-индол-3-илметил}-ацетамид в виде бледно-красного твердого вещества. МС: 463,4 ([М-Н]-).
Пример 11
3-Гидрокси-4-метил-2-[(3-метил-1Н-индол-2-ил)-фенилметил]-4-п-толилциклобут-2-енон
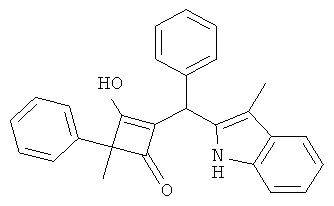
С использованием общей методики С 2-метил-2-п-толилциклобутан-1,3-дион (из примера 4.1) вводили в реакцию с бензальдегидом и 3-метил-1Н-индолом и получали искомое соединение в виде бесцветного твердого вещества. МС: 406,6 ([М-Н]-).
Пример 12
2-[(3,5-Диметил-1Н-индол-2-ил)-фенилметил]-3-гидрокси-4-метил-4-п-толилциклобут-2-енон
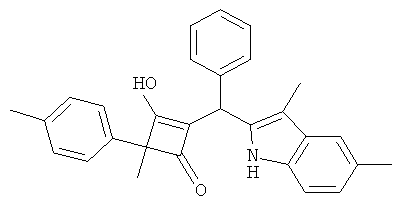
С использованием общей методики С 2-метил-2-п-толилциклобутан-1,3-дион (из примера 4.1) вводили в реакцию с бензальдегидом и 3,5-диметил-1Н-индолом (публикация 3) и получали искомое соединение в виде бесцветного твердого вещества. МС: 420,5 ([М-Н]-).
Пример 13
2-[(3,6-Диметил-1Н-индол-2-ил)-фенилметил]-3-гидрокси-4-метил-4-п-толилциклобут-2-енон
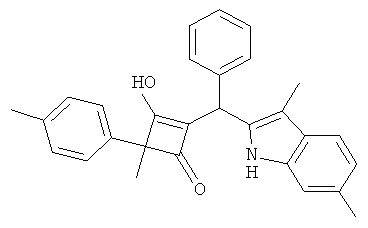
С использованием общей методики С 2-метил-2-п-толилциклобутан-1,3-дион (из примера 4.1) вводили в реакцию с бензальдегидом и 3,6-диметил-1Н-индолом (публикация 4) и получали искомое соединение в виде бесцветного твердого вещества. МС: 420,5 ([М-Н]-).
Пример 14
2-[(5-Фтор-3-метил-1Н-индол-2-ил)-фенилметил]-3-гидрокси-4-метил-4-п-толилциклобут-2-енон
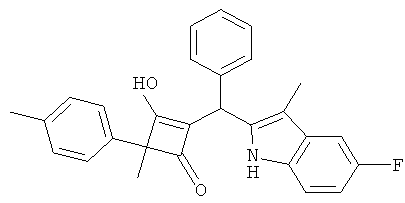
С использованием общей методики С 2-метил-2-п-толилцикло6утан-1,3-дион (из примера 4.1) вводили в реакцию с бензальдегидом и 5-фтор-3-метил-1H-индолом и получали искомое соединение в виде красного твердого вещества. МС: 424,5 ([М-Н]-).
Пример 15
N-{2-[(2-Гидрокси-3-метил-4-оксо-3-п-толилциклобут-1-енил)-фенилметил]-1Н-индол-3-илметил}-ацетамид
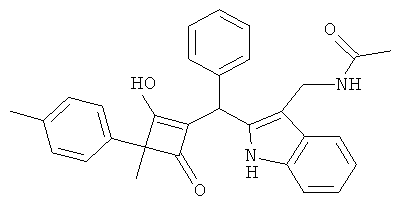
С использованием общей методики С 2-метил-2-п-толилциклобутан-1,3-дион (из примера 4.1) вводили в реакцию с бензальдегидом и N-(1Н-индол-3-илметил)-ацетамидом (публикация 6) и получали искомое соединение в виде почти белого твердого вещества. МС: 463,4 ([М-Н]-).
Пример 16
N-{6-Хлор-2-[(2-гидрокси-3-метил-4-оксо-3-п-толилциклобут-1-енил)-фенилметил]-1Н-индол-3-илметил}-ацетамид
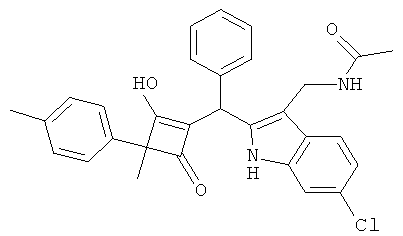
С использованием общей методики С 2-метил-2-п-толилциклобутан-1,3-дион (из примера 4.1) вводили в реакцию с бензальдегидом и N-(6-xлop-1H-индол-3-илметил)-ацетамидом (получали из С-(6-хлор-1Н-индол-3-ил)-метиламина путем ацилирования в соответствии с примером 1.2) и получали искомое соединение в виде почти белого твердого вещества. МС: 497,3 ([М-Н]-).
Пример 17
N-{2-[(2-Гидрокси-3-метил-4-оксо-3-п-толилциклобут-1-енил)-фенилметил]-7-метил-1Н-индол-3-илметил}-ацетамид
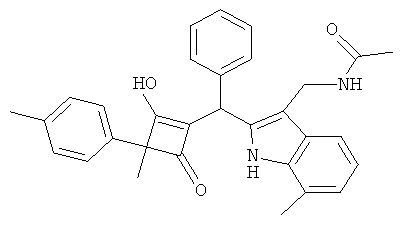
С использованием общей методики С 2-метил-2-п-толилциклобутан-1,3-дион (из примера 4.1) вводили в реакцию с бензальдегидом и N-(7-метил-1Н-индол-3-илметил)-ацетамидом (получали из 7-метил-1H-индол-3-карбальдегида в соответствии с примерами 10.1-10.3) и получали искомое соединение в виде почти белого твердого вещества. МС: 477,4 ([М-Н]-).
Пример 18
N-{2-[(2-Гидрокси-3-метил-4-оксо-3-п-толилциклобут-1-енил)-фенилметил]-6-метил-1Н-индол-3-илметил}-ацетамид
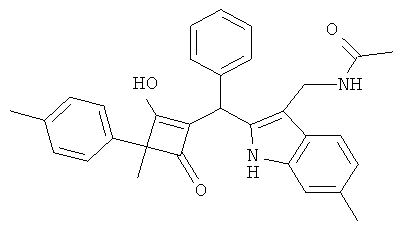
С использованием общей методики С 2-метил-2-п-толилциклобутан-1,3-дион (из примера 4.1) вводили в реакцию с бензальдегидом и N-(6-метил-1Н-индол-3-илметил)-ацетамидом (из примера 10.3) и получали искомое соединение в виде бледно-красного твердого вещества. МС: 477,3 ([М-Н]-).
Пример 19
N-{2-[(2-Гидрокси-3-метил-4-оксо-3-п-толилциклобут-1-енил)-фенилметил]-6-метил-1Н-индол-3-илметил}-N-метилформамид
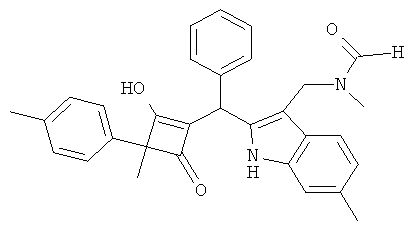
19.1. К суспензии 6-метил-1H-индол-3-карбальдегида (0,96 г, публикация 5) в метаноле (15 мл) при 22°С прибавляли уксусную кислоту (1,7 мл) и раствор метиламина в тетрагидрофуране (2 М, 12,0 мл). После перемешивания в течение 1 ч 5 порциями прибавляли цианоборогидрид натрия (0,76 г) и перемешивание продолжали в течение 2 ч. Смесь выпаривали и остаток подвергали распределению между водным раствором хлористоводородной кислоты (1 н.) и дихлорметаном. С помощью гидроксида натрия значение рН водного слоя доводили до 14, затем водный слой экстрагировали дихлорметаном. Органический слой сушили и выпаривали и получали неочищенный метил-(6-метил-1 Н-индол-3-илметил)-амин.
19.2. К раствору неочищенного метил-(6-метил-1Н-индол-3-илметил)-амина (87 мг) в ацетонитриле (1 мл) прибавляли диизопропилэтиламин (0,25 мл) и 4-нитрофенилформат (90 мг) и перемешивание продолжали в течение 3 ч. Смесь разбавляли метанолом и уксусную кислоту выпаривали и остаток хроматографировали на диоксиде кремния с использованием смеси н-гептан/AcOEt (1:1) и получали N-метил-N-(6-метил-1 Н-индол-3-илметил)-формамид в виде бесцветного масла. МС: 202,9 ([М]+).
19.3. С использованием общей методики С 2-метил-2-п-толилциклобутан-1,3-дион (из примера 4,1) вводили в реакцию с бензальдегидом и N-метил-N-(6-метил-1Н-индол-3-илметил)-формамидом и получали искомое соединение в виде красного твердого вещества. МС: 476,6 ([М-Н]-).
Пример 20
3-Гидрокси-4-метил-2-(нафталин-2-илфенилметил)-4-фенилциклобут-2-енон
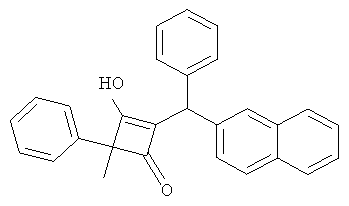
20.1. С использованием общей методики В 2-бромнафталин вводили в реакцию с бензальдегидом и получали нафталин-2-илфенилметанол в виде бесцветного твердого вещества.
20.2. С использованием общей методики D 2-метил-2-фенилциклобутан-1,3-дион (публикация 1) вводили в реакцию с нафталин-2-илфенилметанолом и получали искомое соединение в виде бесцветного твердого вещества. МС: 389,5 ([М-Н]-).
Пример 21
3-Гидрокси-2-[(6-метоксинафталин-2-ил)-фенилметил]-4-метил-4-фенилциклобут-2-снон
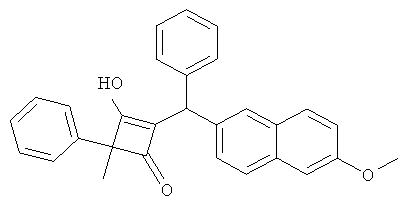
21.1 С использованием общей методики B 2-бром-6-метоксинафталин вводили в реакцию с бензальдегидом и получали (6-метоксинафталин-2-ил)-фенилметанол в виде бесцветного твердого вещества.
21.2. С использованием общей методики D 2-метил-2-фснилциклобутан-1,3-дион (публикация 1) вводили в реакцию с (6-метоксинафталин-2-ил)-фенилметанолом и получали искомое соединение в виде бесцветного твердого вещества. МС: 419,3 ([М-Н]-).
Пример 22
2-(Бензо[b]тиофен-2-илфенилметил)-3-гидрокси-4-метил-4-фенилциклобут-2-енон
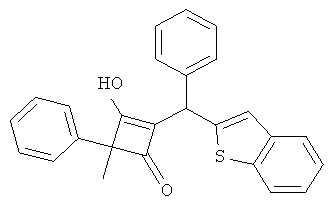
22.1. С использованием общей методики В бензо[b]тиофен вводили в реакцию с бензальдегидом и получали бензо[b]тиофен-2-илфенилметанол в виде бесцветного твердого вещества. МС: 223,1 ([М+Н-Н2О]+).
22.2. С использованием общей методики D 2-метил-2-фенилциклобутан-1,3-дион (публикация 1) вводили в реакцию с 6ензо[b]тиофен-2-илфенилметанолом и получали искомое соединение в виде бесцветного твердого вещества. МС: 395,3 ([М-Н]-).
Пример 23
2-[(3,5-Диметилбензо[b]тиофен-2-ил)-фенилметил]-3-гидрокси-4-метил-4-фенилциклобут-2-енон
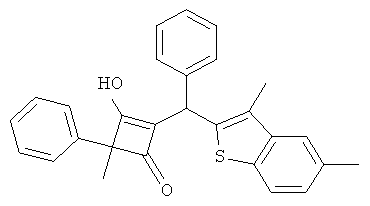
23.1. С использованием общей методики В 3,5-диметилбензо[b]тиофен вводили в реакцию с бензальдегидом и получали (3,5-диметилбензо[b]тиофен-2-ил)-фенилметанол в виде бесцветного масла. МС: 251,4 ([М+Н-Н2О+).
23.2. С использованием общей методики D 2-метил-2-фенилциклобутан-1,3-дион (публикация 1) вводили в реакцию с (3,5-диметилбензо[b]тиофен-2-ил)-фенилметанолом и получали искомое соединение в виде бесцветного твердого вещества. МС: 423,5 ([М-Н]-).
Пример 24
3-Гидрокси-4-метил-2-[(3-метилбензо[b]тиофен-2-ил)-фенилметил]-4-фенилциклобут-2-енон
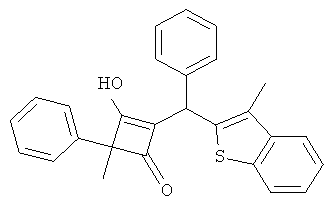
24.1. С использованием общей методики В 3-метилбензо[b]тиофен вводили в реакцию с бензальдегидом и получали (3-метилбензо[b]тиофен-2-ил)-фенилметанол в виде бледно-желтого твердого вещества. МС: 236,8 ([М+Н-Н2O]+).
24.2. С использованием общей методики D 2-метил-2-фенилциклобутан-1,3-дион (публикация 1) вводили в реакцию с (3-метилбензо[b]тиофен-2-ил)-фенилметанолом и получали искомое соединение в виде бесцветного твердого вещества. МС: 409,5 ([М-Н]-).
Пример 25
2-[(5-Фтор-3-метилбензо[Ь]тиофен-2-ил)-фенилметил]-3-гидрокси-4-метил-4-фенилциклобут-2-енон
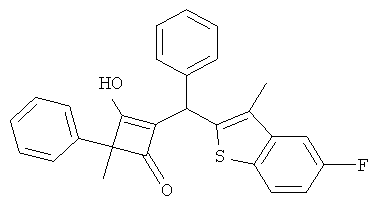
25.1. С использованием общей методики В 5-фтор-3-метилбензо[b]тиофен вводили в реакцию с бензальдегидом и получали (5-фтор-3-метилбензо[b]тиофен-2-ил)-фенилмстанол в виде бледно-желтого масла. МС: 255,3 ([М+Н-Н2О]+).
25.2. С использованием общей методики D 2-метил-2-фенилциклобутан-1,3-дион (публикация 1) вводили в реакцию с (5-фтор-3-метилбензо[b]тиофен-2-ил)-фенилметанолом и получали искомое соединение в виде бесцветного твердого вещества. МС: 427,5 ([М-Н]-).
Пример 26
3-Гидрокси-4-метил-2-[(5-метилбензо[b]тиофен-2-ил)-фенилметил]-4-фенилциклобут-2-енон
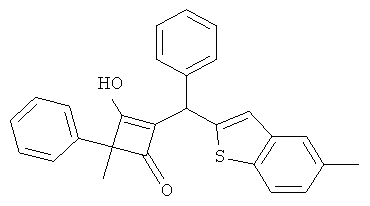
26.1. С использованием общей методики В 5-метилбензо[b]тиофен вводили в реакцию с бензальдегидом и получали (5-метил6ензо[b]тиофен-2-ил)-фенилметанол в виде бесцветного твердого вещества. МС: 237,1 ([М+Н-Н2O]+).
26.2. С использованием общей методики D 2-метил-2-фенилцикло6утан-1,3-дион (публикация 1) вводили в реакцию с (5-метилбензо[b]тиофен-2-ил)-фенилметанол и получали искомое соединение в виде бесцветного твердого вещества. МС: 409,3 ([М-Н]-).
Пример 27
3-Гидрокси-4-метил-2-[(6-метилбензо[b]тиофен-2-ил)-фенилметил]-4-фенилциклобут-2-енон
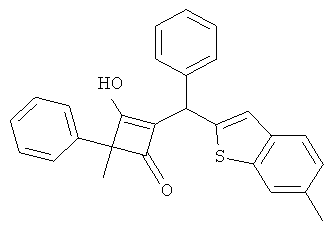
27.1. С использованием общей методики В 6-метилбензо[b]тиофен вводили в реакцию с бензальдегидом и получали (6-метилбензо[b]тиофен-2-ил)-фенилметанол в виде почти белого твердого вещества. МС: 236,9 ([М+Н-Н2О]+).
27.2. С использованием общей методики D 2-метил-2-фенилциклобутан-1,3-дион (публикация 1) вводили в реакцию с (6-метилбензо[b]тиофен-2-ил)-фенилметанолом и получали искомое соединение в виде бледно-желтого твердого вещества. МС: 409,3 ([М-Н]-).
Пример А
Таблетки с пленочным покрытием, содержащие приведенные ниже ингредиенты, можно изготовить по обычной методике:
Активный ингредиент просеивают и смешивают с микрокристаллической целлюлозой и смесь гранулируют с раствором поливинилпирролидона в воде. Гранулят смешивают с натриевой солью гликолята крахмала и стеаратом магния и прессуют и получают ядра массой 120 или 350 мг соответственно. На ядра наносят слой лака с помощью водного раствора/суспензии указанного выше материала, предназначенного для нанесения пленочного покрытия.
Пример В
Капсулы, содержащие приведенные ниже ингредиенты, можно изготовить по обычной методике:
Ингредиенты просеивают и смешивают и помещают в капсулы размера 2.
Пример С
Растворы для инъекции могут обладать следующим составом:
Активный ингредиент растворяют в смеси полиэтиленгликоля 400 и воды для инъекций (часть). Значение рН доводят до 5,0 с помощью уксусной кислоты. Объем раствора доводят до 1,0 мл путем прибавления оставшегося количества воды. Раствор фильтруют, помещают в ампулы с соответствующим избытком и стерилизуют.
Пример D
Капсулы из мягкого желатина, содержащие приведенные ниже компоненты, можно изготовить по обычной методике:
Активный ингредиент растворяют в теплом расплаве остальных компонентов и смесь помещают в капсулы из мягкого желатина подходящего размера. Заполненные капсулы из мягкого желатина обрабатывают по обычным методикам.
Пример Е
Пакетики, содержащие приведенные ниже компоненты, можно изготовить по обычной методике:
Активный ингредиент смешивают с лактозой, микрокристаллической целлюлозой и натриевой солью карбоксиметилцеллюлозы и гранулируют с раствором поливинилпирролидона в воде. Гранулят смешивают со стеаратом магния и вкусовыми добавками и помещают в пакетики.
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЕ ПРОИЗВОДНЫЕ ВИНИЛОГЕННЫХ КИСЛОТ | 2006 |
|
RU2425830C2 |
| ПИРАЗОЛОПИРИДИНОВЫЕ ПРОИЗВОДНЫЕ КАК ИНГИБИТОРЫ НАДФН-ОКСИДАЗЫ | 2009 |
|
RU2548022C2 |
| ПИРАЗОЛОПИРИДИНОВЫЕ ПРОИЗВОДНЫЕ КАК ИНГИБИТОРЫ НАДФН-ОКСИДАЗЫ | 2009 |
|
RU2532161C2 |
| ПИРАЗОЛОПИРИДИНОВЫЕ ПРОИЗВОДНЫЕ КАК ИНГИБИТОРЫ НАДФН-ОКСИДАЗЫ | 2009 |
|
RU2538041C2 |
| ЗАМЕЩЕННЫЕ ИНДОЛЬНЫЕ ОСНОВАНИЯ МАННИХА | 2000 |
|
RU2265594C2 |
| 1,3-ДИАРИЛЗАМЕЩЕННЫЕ МОЧЕВИНЫ КАК МОДУЛЯТОРЫ КИНАЗНОЙ АКТИВНОСТИ | 2006 |
|
RU2402544C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ УЛУЧШЕНИЯ КОГНИТИВНЫХ ФУНКЦИЙ | 2012 |
|
RU2665021C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ УЛУЧШЕНИЯ КОГНИТИВНЫХ ФУНКЦИЙ | 2012 |
|
RU2792010C2 |
| НОВЫЕ 1Н-ИНДОЛ-3-АЦЕТАМИДЫ КАК ИНГИБИТОРЫ SPLA И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1994 |
|
RU2162463C2 |
| ПРОИЗВОДНЫЕ СПИРООКСИНДОЛА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ТЕРАПЕВТИЧЕСКИХ АГЕНТОВ | 2006 |
|
RU2415143C2 |
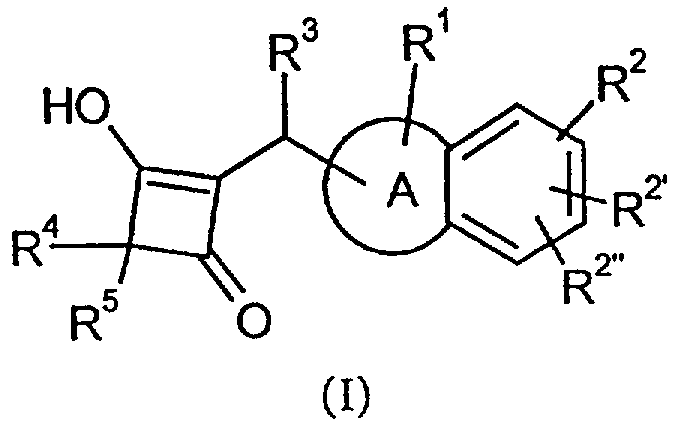
В заявке описаны новые винилогические производные кислот формулы
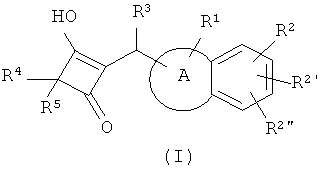
в которой кольцо А является такими, как определено в 1 описании, R1 обозначает водород, C1-С6-алкил или-NR'R", -(С0-С6-алкилен)-NR'R", где R' и R" независимо выбраны из группы, включающей водород, C1-С6-алкил, формил, С1-С6-алкилкарбонил; R2, R2' и R2" независимо обозначают водород, галоген, C1-С6-алкил или С1-С6-алкоксигруппу; R3 обозначает фенил; R4 обозначает водород, C1-C6-алкил, необязательно замещенный фенил или фенил-С1-С6-алкил; R5 обозначает водород или С1-С6-алкил; а также их физиологически приемлемые соли. Эти соединения ингибируют химазу и могут использоваться в качестве лекарственных средств. 2 н. и 13 з.п. ф-лы, 27 пр.
1. Соединения формулы (I)

в которой
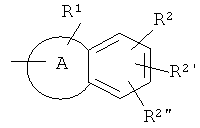 означает
означает  ,
, 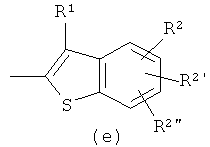 или
или 
R1 обозначает водород, C1-С6-алкил или
-NR'R", -(С0-С6-алкилен)-NR'R", где R' и R" независимо выбраны из группы, включающей водород, C1-С6-алкил, формил, C1-С6-алкилкарбонил;
R2, R2' и R2'' независимо обозначают водород, галоген, C1-С6-алкил или C1-С6-алкоксигруппу;
R3 обозначает фенил;
R4 обозначает водород, C1-С6-алкил, необязательно замещенный фенил или фенил-С1-С6-алкил;
R5 обозначает водород или C1-С6-алкил;
и фармацевтически приемлемые соли;
где, если не приведено другое определение,
термин "необязательно замещенный фенил" означает соответственно фенил, необязательно содержащий один или большее количество заместителей, независимо выбранных из группы, включающей галоген, нитрогруппу, цианогруппу, аминогруппу, С1-С6-алкил, гидроксигруппу, C1-С6-алкоксигруппу и моно- или ди-С1-С6-алкилзамещенную аминогруппу.
2. Соединения по п.1, в которых
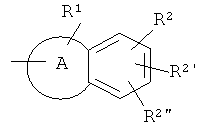 означает
означает 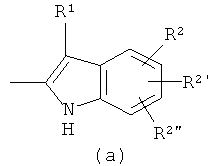
3. Соединения по п.1, в которых R1 обозначает C1-С6-алкил, -(С2-С6-алкилен)-NR'R", где R' и R" независимо выбраны из группы, включающей водород, формил и ацетил.
4. Соединения по п.3, в которых R1 обозначает 2-аминоэтил, 2-ацетиламиноэтил, 2-(N-формил-N-метиламино)этил, 2-ацетиламино-2,2-диметилэтил, метил или изопропил.
5. Соединения по п.4, в которых R1 обозначает метил, 2-ацетиламиноэтил, 2-ацетиламино-2,2-диметилэтил или 2-(N-формил-N-метиламино)этил.
6. Соединения по п.5, в которых R2, R2' и R2" независимо обозначают водород, галоген, С1-С6-алкил или C1-С6-алкоксигруппу.
7. Соединения по п.6, в которых два из R2, R2' и R2" обозначают водород и третий обозначает водород, галоген, С1-С6-алкил или C1-С6-алкоксигруппу.
8. Соединения по п.7, в которых два из R2, R2' и R2" обозначают водород и третий обозначает водород, хлор, фтор, метил, этил или метоксигруппу.
9. Соединения по п.8, в которых два из R2, R2' и R2" обозначают водород и третий обозначает водород, фтор или метил.
10. Соединения по п.1, в которых
R4 обозначает C1-С6-алкил, необязательно замещенный фенил или фенил-C1-С6-алкил, и
R5 обозначает С1-С6-алкил.
11. Соединения по п.10, в которых
R4 обозначает фенил или 4-метилфенил, и
R5 обозначает метил.
12. Соединения по п.1, которые представляют собой
N-(2-{2-[(2-гидрокси-3-метил-4-оксо-3-фенилциклобут-1-енил)-фенилметил]-6-метил-1Н-индол-3-ил}-1,1-диметилэтил)-ацетамид,
3-гидрокси-4-метил-2-[(3-метил-1Н-индол-2-ил)-фенилметил]-4-фенилциклобут-2-енон,
2-[(3,5-диметил-1Н-индол-2-ил)-фенилметил]-3-гидрокси-4-метил-4-фенилциклобут-2-енон,
2-[(3,6-диметил-1Н-индол-2-ил)-фенилметил]-3-гидрокси-4-метил-4-фенилциклобут-2-енон,
2-[(5-фтор-3-метил-1Н-индол-2-ил)-фенилметил]-3-гидрокси-4-метил-4-фенилциклобут-2-енон,
N-{2-[(2-гидрокси-3-метил-4-оксо-3-фенилциклобут-1-енил)-фенилметил]-6-метил-1Н-индол-3-илметил}-ацетамид,
3-гидрокси-4-метил-2-[(3-метил-1Н-индол-2-ил)-фенилметил]-4-п-толилциклобут-2-енон,
2-[(3,5-диметил-1Н-индол-2-ил)-фенилметил]-3-гидрокси-4-метил-4-п-толилциклобут-2-енон,
2-[(3,6-диметил-1Н-индол-2-ил)-фенилметил]-3-гидрокси-4-метил-4-п-толилциклобут-2-енон,
2-[(5-фтор-3-метил-1Н-индол-2-ил)-фенилметил]-3-гидрокси-4-метил-4-п-толилциклобут-2-енон,
N-{2-[(2-гидрокси-3-метил-4-оксо-3-п-толилциклобут-1-енил)-фенилметил]-6-метил-1Н-индол-3-илметил}-ацетамид или
N-{2-[(2-гидрокси-3-метил-4-оксо-3-п-толилциклобут-1-енил)-фенилметил]-6-метил-1Н-индол-3-илметил}-N-метилформамид.
13. Фармацевтические композиции, включающие соединение, обладающее активностью ингибиторов химазы по п.1 и фармацевтически приемлемый наполнитель.
14. Соединения по п.1, предназначенные для применения в качестве терапевтически активных веществ, обладающих активностью ингибиторов химазы.
15. Соединения по п.1, предназначенные для применения в качестве терапевтически активных веществ, предназначенных для лечения и/или профилактики атеротромбоза или астмы.
| ЕР 1099690 A1, 16.05.2001 | |||
| EP 1136488 A1, 26.09.2001 | |||
| Гидравлическая сцепная муфта | 1926 |
|
SU4268A1 |
Авторы
Даты
2012-05-20—Публикация
2007-10-04—Подача