Изобретение относится к новым производным винилогенных кислот формулы (I),
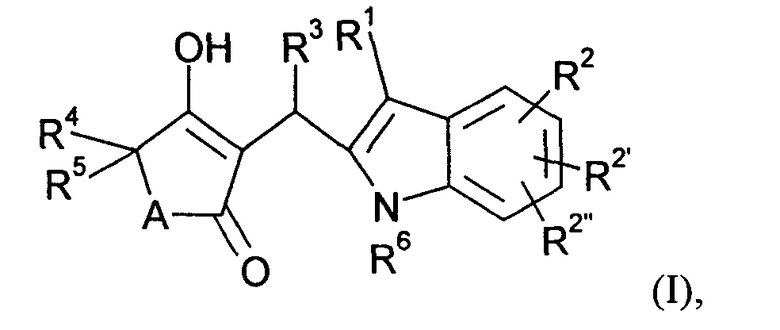
где
А обозначает -СН2-, -О- или -NR′-, в котором R′ обозначает водород или C1-6алкил, или
R′ и R4 образуют С2-5алкилен;
R1 обозначает водород, галоген, нитрогруппу, цианогруппу, аминогруппу, C1-6алкил, гетероалкил, С3-7циклоалкил, С3-6алкенил, С3-6алкинил, гидроксигруппу,
С1-6алкоксигруппу,
-NR′R″, -(С0-6алкилен)-NR′R″, где R′ и R″ независимо выбирают из группы, включающей водород, С1-6алкил, гетероалкил, формил, C1-6алкилкарбонил, необязательно замещенный С3-7циклоалкилкарбонил, необязательно замещенный арилкарбонил, необязательно замещенный гетероарилкарбонил, необязательно замещенный гетероциклилкарбонил, C1-6алкилсульфонил, необязательно замещенный С3-7циклоалкилсульфонил, необязательно замещенный арилсульфонил, необязательно замещенный гетероарилсульфонил и необязательно замещенный гетероциклилсульфонил, или
-(С0-6алкилен)-OR′, в котором R′ обозначает водород, C1-6алкил, гетероалкил, формил или С1-6алкилкарбонил;
R2, R2′ и R2″ независимо обозначают водород, галоген, цианогруппу, нитрогруппу, аминогруппу, моно- или ди-С1-6алкилзамещенную аминогруппу, С1-6алкил,
С2-6алкенил, С2-6алкинил, гетероалкил, гидроксигруппу или С1-6алкоксигруппу;
R3 обозначает водород, галоген, нитрогруппу, цианогруппу, аминогруппу, моно- или ди- С1-6алкилзамещенную аминогруппу, С1-6алкил, С2-6алкенил, С2-6алкинил, гетероалкил, гидроксигруппу, С1-6алкоксигруппу, необязательно замещенный
С3-7циклоалкил, необязательно замещенный арил, необязательно замещенный гетероарил, необязательно замещенный гетероциклил, необязательно замещенный
С3-7 циклоалкилС1-6алкил, необязательно замещенный арилС1-6алкил, необязательно замещенный гетероарилС1-6алкил или необязательно замещенный гетероциклилС1-6алкил;
R4 обозначает водород, галоген, нитрогруппу, цианогруппу, аминогруппу, моно- или ди-С1-6алкилзамещенную аминогруппу, С1-6алкил, С2-6алкенил, С2-6алкинил, гетероалкил, гидроксигруппу, С1-6алкоксигруппу, необязательно замещенный С3-7циклоалкил, необязательно замещенный арил, необязательно замещенный гетероарил, необязательно замещенный гетероциклил, необязательно замещенный
С3-7циклоалкилС1-6алкил, необязательно замещенный арилС1-6алкил, необязательно замещенный гетероарилС1-6алкил или необязательно замещенный гетероциклилС1-6алкил;
R5 обозначает водород или С1-6алкил; или
R4 и R5 вместе с атомом углерода, к которому они присоединены, образуют необязательно замещенное С3-7циклоалкильное кольцо или необязательно замещенное гетероциклильное кольцо;
R6 обозначает водород или С1-6алкил;
и их пролекарства и фармацевтически приемлемые соли.
Кроме того, изобретение относится к способу и промежуточному соединению для получения вышеназванных соединений, фармацевтическим препаратам, содержащим такие соединения, применению этих соединений для получения фармацевтических препаратов, а также к способу получения промежуточного соединения.
Соединения формулы (I) ингибируют химазу. Химаза представляет собой серинпротеиназу с системой экспрессии, строго лимитируемой субпопуляцией тучных клеток (МСТ тучная клетка). Химаза активируется только при активации тучных клеток и дегрануляции, которая ограничивает ферментную активность в МСТ положительных тканях. Химаза специфически расщепляет ряд патологически релевантных субстратов (Raymond W.W., S.W.Ruggles et al.; JBC 2003 278 (36): 34517-34524), вследствие чего может активировать ангиотензин II, эндотелин, TGFb, Il1, SCF, коллагеназу и разлагать белки, подобные тромбину, FN, АРО А1,2. Эта особенность превращает химазу в привлекательную мишень при аллергических, воспалительных и фиброзных болезнях. Действительно, ряд успешных экспериментов на животных с ингибиторами химазы продемонстрировали эффективность при атопических заболеваниях животных, сосудистом нарушении и атеросклерозе (Doggrell S.A, Wanstall J.С., Can. J. Physiol. Pharmacol. 2005, Feb; 83(2):123-30; Lindstedt К.А., Kovanen Р.Т., Curr. Opin. Lipidol, 2004, Oct; 15(5):567-73; Reed С.E., Kita H., J. Allergy Clin. Immunol., 2004, Nov; 114(5):997-1008; Takai S. et al., Eur. J. Pharmacol., 2004, Oct 6; 501(1-3):1-8; Takai S. et al., Trends Pharmacol. Sci., 2004, Oct; 25(10):518-22; Takai S., Miyazaki M., Curr. Vase. Pharmacol., 2003, Jun; 1(2):217-24).
Оказалось, что ингибирование химазы применимо для моделирования аллергии, астмы, периферической артериальной окклюзивной болезни, критической ишемии конечностей, при уязвимости пациентов со склеротическими бляшками, нестабильной стенокардии, застойной сердечной недостаточности, гипертрофии левого желудочка, ишемического реперфузионного нарушения, кардиопатии, рестеноза, ревматоидного артрита, диабетической нефропатии, болезни Боуэла, болезни Крона, заживления ран (ожоги/язвы при диабете/CLI).
Настоящее изобретение предлагает новые соединения формулы (I), являющиеся ингибиторами химазы.
Если не указано иначе, предлагаются следующие определения для иллюстрации и объяснения значения и объема различных терминов, используемых в описании настоящего изобретения.
Термин "галоген" или "галогруппа" обозначают фтор, хлор, бром и йод, при этом предпочтительны фтор и хлор.
Термин "С1-6алкил", один или в сочетании с другими группами, обозначает разветвленный или линейный моновалентный алкильный радикал, содержащий от одного до шести атомов углерода. Этот термин может быть проиллюстрирован такими радикалами, как метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, трет-бутил. С1-4алкил является более предпочтительным.
Термин "гетероалкил" означает С1-6алкил, замещенный одним или более заместителями, независимо выбранными из группы, включающей нитрогруппу, гидроксигруппу, галоген, цианогруппу, С1-6алкоксигруппу, формил, C1-6алкилкарбонил, карбоксил, С1-6алкилтиогруппу, С1-6алкилсульфинил, C1-6алкилсульфонил, аминогруппу и моно- или ди-С1-6алкилзамещенную аминогруппу. Этот термин может быть проиллюстрирован такими радикалами, как 2-гидроксиэтил, перфторметил.
С1-6алкил, замещенный одной гидроксигруппой или от одного до трех различными атомами галогена, является предпочтительным.
Термин "С3-7циклоалкил", один или в сочетании с другими группами, означает насыщенный моновалентный циклический углеводородный радикал, содержащий от трех до семи кольцевых атомов углерода, например циклопропил, циклобутил, циклогексил.
Термин "C1-6алкоксигруппа", один или в сочетании с другими группами, означает группу R′-O-, где R′ обозначает С1-6алкил.
Термин "С2-6алкенил", один или в сочетании с другими группами, означает линейный или разветвленный углеводородный остаток, включающий олефиновую связь и содержащий от двух до шести атомов углерода, такой как, например, этенил, 2-пропенил.
Термин "С2-6алкинил", один или в сочетании с другими группами, означает линейный или разветвленный углеводородный остаток, включающий тройную связь и содержащий от двух до шести атомов углерода, такой как, например, этинил, 2-пропинил.
Термин "С0-6алкилен" означает связь или линейную или разветвленную дивалентную насыщенную алифатическую углеводородную группу, содержащую от 1 до 6 атомов углерода. С0алкилен означает связь.
Термин "арил", один или в сочетании с другими группами, означает фенильную или нафтильную группу, предпочтительно фенильную группу.
Термин "гетероциклил", один или в комбинации с другими группами, означает неароматические моно- или бициклические радикалы, содержащие от 3 до 8 атомов в кольце, в которых один или два кольцевых атома являются гетероатомами, которые выбирают из N, О или S(O)n (где n обозначает целое число от 0 до 2), при этом оставшиеся кольцевые атомы являются атомами углерода.
Термин "гетероарил" означает моноциклический или бициклический радикал с от 5 до 12 кольцевыми атомами, содержащий по крайней мере одно ароматическое кольцо с одним, двумя или тремя кольцевыми гетероатомами, выбранными из N, О и S, при этом оставшиеся кольцевые атомы являются атомами углерода. Предпочтительно, точкой присоединения гетероарильного радикала служит ароматическое кольцо.
Термин "необязательно замещенный арил", "необязательно замещенный гетероарил", "необязательно замещенный гетероциклил" и "необязательно замещенный С3-7никлоалкил" означает соответственно арил, гетероарил, гетероциклил и
С3-7циклоалкил, необязательно замещенные одним или более заместителями, независимо выбранными из группы, включающей галоген, нитрогруппу, цианогруппу, аминогруппу, C1-6алкил, С2-6алкенил, С2-6алкинил, гидроксигруппу, С1-6алкоксигруппу, моно- или ди-С1-6алкилзамещенную аминогруппу и гетероалкил.
Предпочтительные радикалы для химических групп, определения для которых даны выше, специально приведены в примерах.
Соединения формулы (I) могут образовывать фармацевтически приемлемые кислотно-аддитивные соли. Примерами таких фармацевтически приемлемых солей являются соли соединений формулы (I) с физиологически совместимыми минеральными кислотами, такими как хлористоводородная кислота, серная кислота, сернистая кислота или фосфорная кислота; или с органическими кислотами, такими как метансульфоновая кислота, п-толуолсульфоновая кислота, уксусная кислота, молочная кислота, трифторуксусная кислота, лимонная кислота, фумаровая кислота, малеиновая кислота, винная кислота, янтарная кислота или салициловая кислота. Термин "фармацевтически приемлемые соли" относится к таким солям. Соединения формулы (I), в которых присутствует СООН-группа, могут также образовывать соли с основаниями. Примеры таких солей включают щелочные, щелочно-земельные и аммонийные соли, такие как, например, Na-, K-, Са- и триметиламмонийные соли. Термин "фармацевтически приемлемые соли" также относится к таким солям. Кислотно-аддитивные соли по описанию выше являются предпочтительными.
"Необязательный" или "необязательно" обозначают, что описанные случай или обстоятельство впоследствии могут иметь место, но не происходят и что описание включает примеры, где случай или обстоятельство встречаются, и примеры, в которых они не встречаются. Например, "арильная группа, необязательно замещенная алкильной группой" означает, что алкил может присутствовать, а может и не присутствовать, и описание включает ситуации, когда арильная группа замещена алкильной группой и когда арильная группа не замещена алкильной группой.
Термин "фармацевтически приемлемый наполнитель" обозначает наполнитель, который используется при получении фармацевтической композиции, которая в общем безопасна, нетоксична и не является нежелательной с биологической или другий точек зрения и включает наполнитель, приемлемый для ветеринарного применения, а также в фармацевтической медицине. Термин "фармацевтически приемлемый наполнитель", используемый в данном описании и формуле изобретения, включает как один, так и более одного наполнителя.
Соединения, имеющие одинаковые молекулярные формулы, но различающиеся по характеру или последовательности связывания их атомов или расположению их атомов в пространстве, называются «изомерами». Изомеры, различающиеся расположением атомов в пространстве, называются «стереоизомерами». Стереоизомеры, не являющиеся зеркальным отображением друг друга, называются «диастереоизомерами», а стереоизомеры, зеркальные отображения которых не совпадают друг с другом, называются «энантиомерами». Когда соединение имеет асимметрический центр, например, если атом углерода связан с четырьмя различными группами, возможно наличие пары энантиомеров. Энантиомер может характеризоваться абсолютной конфигурацией его асимметрического центра и описываться R- и S-последовательностями согласно правилам Кана, Ингольда и Прелога или типом, по которому молекула вращает плоскость поляризованного света, и обозначаться как правовращающий и левовращающий (например, как (+) или (-)-изомеры соответственно). Хиральное соединение может существовать как в виде индивидуального энантиомера, так и в виде смеси энантиомеров. Смесь, содержащая равные пропорции энантиомеров, называется "рацемической смесью".
Соединения формулы (I) могут обладать одним или более асимметрическим центром. Если не указано иначе, описание или название отдельного соединения в описании и формуле изобретения имеет в виду включение как индивидуальных энантиомеров и смесей, рацемических или иных, а также эпимеров и их смесей. Методы определения стереохимии и разделения стереоизомеров хорошо известны из области техники (см. обсуждение в главе "Advanced Organic Chemistry", 4th edition J. March, John Wiley and Sons, New York, 1992).
В то время как наиболее широкое определение изобретения описано ранее, определенные соединения формулы (I) являются предпочтительными.
i) Предпочтительным соединением по изобретению является соединение формулы (I), где
R3 обозначает С1-6алкил, необязательно замещенный арил, необязательно замещенный гетероарил, необязательно замещенный арилС1-6алкил или необязательно замещенный гетероарил С1-6алкил.
ii) Другим предпочтительным соединением по изобретению является соединение формулы (I), где
R3 обозначает C1-6алкил; фенилС1-6алкил; фенил, необязательно замещенный от одного до трех атомами фтора; или гетероарил, необязательно замещенный от одного до трех атомами фтора, в котором гетероарил является моноциклическим ароматическим радикалом, имеющим 5 или 6 кольцевых атомов, содержащим один или два кольцевых атома азота или один кольцевой атом серы.
iii) Другим предпочтительным соединением по изобретению является соединение формулы (I), где R3 обозначает фенил.
iv) Другим предпочтительным соединением по изобретению является соединение формулы (I), где
R1 обозначает С1-6алкил, -(С0-6алкилен)-NR′R″, в котором R′ и R″ независимо выбирают из группы, включающей водород, С1-6алкилкарбонил, необязательно замещенный арилкарбонил, необязательно замещенный гетероарилкарбонил, необязательно замещенный арилсульфонил и необязательно замещенный гетероарилсульфонил или -(С0-6алкилен)-OR′, в котором R′ обозначает водород или С1-6алкилкарбонил.
v) Другим предпочтительным соединением по изобретению является соединение формулы (I), где
R1 обозначает С1-6 алкил, -(С2-6алкилен)-NR′R″, в котором R′ и R″ независимо выбирают из группы, включающей водород, ацетил, арилкарбонил, в котором арил необязательно замещен одной или двумя перфторметильными группами, и арилсульфонил или -(С2-6алкилен)-OR′, в котором R′ обозначает водород или ацетил.
vi) Другим предпочтительным соединением по изобретению является соединение формулы (I), где
R1 обозначает 2-аминоэтил, 2-ацетиламиноэтил, 2-ацетиламино-2,2-диметилэтил, метил, изопропил или 2-гидроксиэтил.
vii) Другим предпочтительным соединением по изобретению является соединение формулы (I), где
R2, R2′ и R2″ независимо обозначают водород, галоген, С1-6алкил или С1-6алкоксигруппу.
viii) Другим предпочтительным соединением по изобретению является соединение формулы (I), где
два из R2, R2′ и R2″ обозначают водород, а третий обозначает водород, галоген, С1-6алкил или C1-6алкоксигруппу.
ix) Другим предпочтительным соединением по изобретению является соединение формулы (I), где
два из R2, R2′ и R2″ обозначают водород, а третий обозначает водород, хлор, фтор, метил, этил или метоксигруппу.
х) Другим предпочтительным соединением по изобретению является соединение формулы (I), где
два из R2, R2′ и R2″ обозначают водород, а другой находится в 5 или 6 положении индольного кольца и выбран из группы, включающей водород, хлор, фтор, метил и этил.
xi) Другим предпочтительным соединением по изобретению является соединение формулы (I), где R6 обозначает водород.
xii) Другим предпочтительным соединением по изобретению является соединение формулы (I), где
R4 обозначает водород, C1-6алкил, необязательно замещенный С3-7циклоалкил, необязательно замещенный арил, необязательно замещенный С3-7циклоалкилС1-6алкил или необязательно замещенный арилС1-6алкил и
R5 обозначает водород или C1-6алкил; или
R4 и R5 вместе с атомом углерода, к которому они присоединены, образуют необязательно замещенное С3-7циклоалкильное кольцо.
xiii) Другим предпочтительным соединением по изобретению является соединение формулы (I), где А обозначает -СН2-.
xiv) Другим предпочтительным соединением по изобретению является соединение формулы (I), где А обозначает -СН2-, R4 обозначает фенил и R5 обозначает водород.
xv) Другим предпочтительным соединением по изобретению является соединение формулы (I), где А обозначает -NR′-, в котором R′ обозначает водород или С1-6алкил.
xvi) Другим предпочтительным соединением по изобретению является соединение формулы (I), где А обозначает -NR′-, в котором R′ обозначает водород или метил, R4 обозначает изопропил и R5 обозначает водород.
xvii) Другим предпочтительным соединением по изобретению является соединение формулы (I), где А обозначает -O-.
xviii) Другим предпочтительным соединением по изобретению является соединение формулы (I), где А обозначает -O-, R4 обозначает водород, фенил, С1-6алкил, необязательно замещенный С3-7циклоалкилС1-6алкил или необязательно замещенный арилС1-6алкил и R5 обозначает водород или C1-6алкил; или
R4 и R5 вместе с атомом углерода, к которому они присоединены, образуют необязательно замещенное С3-7циклоалкильное кольцо.
xix) Другим предпочтительным соединением по изобретению является соединение формулы (I), где А обозначает -O-, R4 обозначает фенил, бензил, изобутил, 2-циклогексилэтил или фенэтил и R5 обозначает водород или метил.
хх) Другим предпочтительным соединением по изобретению является соединение формулы (I), где
R3 обозначает С1-6алкил, необязательно замещенный арил, необязательно замещенный гетероарил, необязательно замещенный арилС1-6алкил или необязательно замещенный гетероарилС1-6алкил, предпочтительно R3 обозначает С1-6алкил, фенил, необязательно замещенный от одного до трех атомами фтора, гетероарил, необязательно замещенный от одного до трех атомами фтора, в котором гетероарил обозначает моноциклический ароматическим радикал с 5 или 6 кольцевыми атомами, содержащими один или два кольцевых атома азота, или фенилС1-6алкил, в частности фенил;
R1 обозначает C1-6алкил, -(С0-6алкилен)NR′R″, в котором R′ и R″ независимо выбирают из группы, включающей водород, С1-6алкилкарбонил, необязательно замещенный арилкарбонил, необязательно замещенный гетероарилкарбонил, необязательно замещенный арилсульфонил и необязательно замещенный гетероарилсульфонил или -(С0-6алкилен)-OR′, в котором R′ обозначает водород или
С1-6алкилкарбонил, предпочтительно R1 обозначает С1-6алкил, -(С2-6алкилен)-NR′R″, в котором R′ и R″ независимо выбирают из группы, включающей водород, ацетил, арилкарбонил, в котором арил необязательно замещен одной или двумя перфторметильными группами, и арилсульфонил или -(С3-7алкилен)-OR′, в котором R′ обозначает водород или ацетил, в частности 2-аминоэтил, 2-ацетиламиноэтил, 2-ацетиламино-2,2-диметилэтил, метил, изопропил или 2-гидроксиэтил;
R2, R2′ и R2″ независимо обозначают водород, галоген, С1-6алкил или С1-6алкоксигруппу, предпочтительно два из R2, R2′ и R2″ обозначают водород, а третий обозначает водород, галоген, С1-6алкил или C1-6алкоксигруппу, более предпочтительно два из R2, R2′ и R2″ обозначают водород, а третий обозначает водород, хлор, фтор, метил, этил или метоксигруппу, в частности два из R2, R2′ и R2″ обозначают водород, а третий находится в 5 или 6 положении индольного кольца и выбран из группы, включающей водород, хлор, фтор, метил и этил;
R6 обозначает водород;
R4 обозначает водород, C1-6алкил, необязательно замещенный С3-7циклоалкил, необязательно замещенный арил, необязательно замещенный С3-7циклоалкилС1-6алкил или необязательно замещенный арилС1-6алкил;
R5 обозначает водород или C1-6 алкил; или
R4 и R5 вместе с атомом углерода, к которому они присоединены, образуют необязательно замещенное С3-7циклоалкильное кольцо.
xxi) Предпочтительным соединением группы хх) является соединение формулы (I), где
А обозначает -СН2-. Когда А обозначает -СН2-, предпочтительно R обозначает фенил и R5 обозначает водород.
xxii) Другим предпочтительным соединением группы хх) является соединение формулы (I), где
А обозначает -NR′-, в котором R′ обозначает водород или C1-6алкил, предпочтительно водород или метил. Когда А обозначает -NR′-, в котором R′ обозначает водород или метил, предпочтительно R4 обозначает изопропил и R5 обозначает водород.
xxiii) Другим предпочтительным соединением группы хх) является соединение формулы (I), где
А обозначает -O-. Когда А обозначает -O-, предпочтительно R4 обозначает водород, фенил, С1-6алкил, необязательно замещенный С3-7циклоалкилС1-6алкил или необязательно замещенный арилС1-6алкил и R5 обозначает водород или C1-6алкил; или
R4 и R5 вместе с атомом углерода, к которому они присоединены, образуют необязательно замещенное С3-7циклоалкильное кольцо.
Когда А обозначает -O-, более предпочтительно R4 обозначает фенил, бензил, изобутил, 2-циклогексилэтил или фенэтил и R5 обозначает водород или метил.
xxiv) Другим предпочтительным соединением по изобретению является соединение формулы (I), где А обозначает -СН2-, -О- или -NR′-, в котором R′ обозначает водород или С1-6алкил.
xxv) Другим предпочтительным соединением по изобретению является соединение формулы (I), где А обозначает -NR′-, в котором R′ и R4 образуют С2-5алкилен.
xxvi) Другим предпочтительным соединением по изобретению является соединение формулы (I), которое обозначает
3-[(5-Фтор-3-метил-1Н-индол-2-ил)фенилметил]-4-гидрокси-5-изопропил-1,5-дигидропиррол-2-он,
3-[(5-Фтор-3-метил-1Н-индол-2-ил)фенилметил]-4-гидрокси-5-изопропил-1-метил-1,5-дигидропиррол-2-он,
4-Гидрокси-5-изопропил-3-[(3-метил-1Н-индол-2-ил)фенилметил]-1,5-дигидропиррол-2-он,
3-[(5-Фтор-3-изопропил-1Н-индол-2-ил)фенилметил]-4-гидрокси-5-изопропил-1,5-дигидропиррол-2-он,
N-(2-{2-[(5-Бензил-4-гидрокси-2-оксо-2,5-дигидрофуран-3-ил)фенилметил]-6-фтор-1Н-индол-3-ил}этил)ацетамид,
5-Бензил-3-{[6-фтор-3-(2-гидроксиэтил)-1Н-индол-2-ил]фенилметил}-4-гидрокси-5Н-фуран-2-он,
3-{[3-(2-Аминоэтил)-6-фтор-1Н-индол-2-ил]фенилметил}-5-бензил-4-гидрокси-5Н-фуран-2-он; соль с уксусной кислотой,
5-Бензил-3-[(5-фтор-3-метил-1Н-индол-2-ил)фенилметил]-4-гидрокси-5Н-фуран-2-он,
(2-{6-Фтор-2-[(4-гидрокси-5-метил-2-оксо-5-фенил-2,5-дигидрофуран-3-ил)фенилметил]индол-3-ил}этил)ацетамид,
(2-{2-[(4-Гидрокси-5-изобутил-2-оксо-2,5-дигидрофуран-3-ил)фенилметил]индол-3-ил}этил)ацетамид,
N-[2-(2-{[5-(2-Циклогексилэтил)-4-гидрокси-2-оксо-2,5-дигидрофуран-3-ил]фенилметил}-6-фтор-1Н-индол-3-ил)этил]ацетамид,
N-(2-{6-Фтор-2-[(4-гидрокси-2-оксо-5-фенэтил-2,5-дигидрофуран-3-ил)фенилметил]-1Н-индол-3-ил}этил)ацетамид,
N-(2-{2-[(2-Гидрокси-5-оксо-3-фенилциклопент-l-енил)фенилметил]-1H-индол-3-ил} этил)ацетамид,
N-(2-{6-Фтор-2-[(2-гидрокси-5-оксо-3-фенилциклопент-1-енил)фенилметил]-1Н-индол-3-ил}этил)ацетамид,
N-(2-{5-Этил-2-[(2-гидрокси-5-оксо-3-фенилциклопент-1-енил)фенилметил]-1Н-индол-3-ил}этил)ацетамид,
N-(2-{2-[(2-Гидрокси-5-оксо-3-фенилциклопент-1-енил)фенилметил]-5-метил-1Н-индол-3-ил}этил)ацетамид,
2-{[3-(2-Аминоэтил)-6-этил-1Н-индол-2-ил]фенилметил}-3-гидрокси-4-фенилциклопент-2-енон или
N-(2-{6-Хлор-2-[(2-гидрокси-5-оксо-3-фенилциклопент-1-енил)фенилметил]-1Н-индол-3-ил}-1,1-диметилэтил)ацетамид.
Соединения по настоящему изобретению могут быть получены, например, при помощи общих синтетических методов, описанных ниже.
Общие синтетические методы
Аббревиатуры:
ДМСО: диметилсульфоксид
ЛДА: литийдиизопропиламид
ТГФ: тетрагидрофуран
I) Соединения формулы (I) могут быть получены согласно следующей схеме 1:
Схема 1
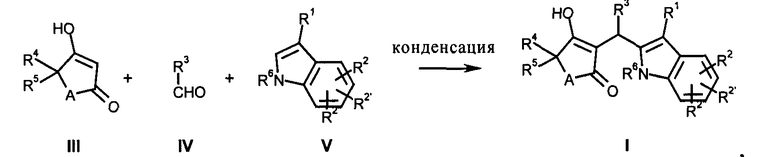
где A, R1, R2, R2′, R2″, R3, R4, R5 и R6 определены выше.
Конденсация винилогенной кислоты III, альдегида IV и индола V, приводящая к винилогенной кислоте I, проводится в растворителе CH3CN или кислоте, такой как карбоновая кислота, например муравьиная кислота или, предпочтительно, уксусная кислота, при температуре в интервале от 20 до 100°С, предпочтительно при 70°С в течение от 1 до 20 ч.
II)-i) Исходные соединения формулы III (А=О) могут быть получены согласно следующей схеме 2:
Схема 2
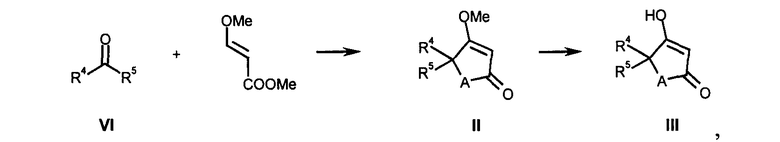
где R4 и R5 определены выше.
Альдегиды или кетоны VI вводят в реакцию с метиловым эфиром 3(Е)-метоксиакриловой кислоты (Miyata, Okiko; Schmidt, Richard R.; Angewandte Chemie (1982), 94(8), 651-2) в растворителях типа диэтилового эфира или ТГФ в присутствии основания, подобного литийдиизопропиламиду, при температуре в интервале от -100°С до -50°С, предпочтительно при -80°С, получая метиловый эфир тетроновой кислоты II (А=О).
Отщепление метоксигруппы в соединении II (А=О) осуществляют с помощью сильной минеральной кислоты, такой как HI, HBr или НСl, предпочтительно HBr, в воде и уксусной кислоте при температуре в интервале от 20°С до 100°С, предпочтительно при 40°С, с получением тетроновой кислоты III (A-О).
II)-ii) Исходные соединения формулы III (А=NH или А=N-С1-6алкил) могут быть получены согласно следующей схеме 3, как описано Hofheinz, Werner et al., Helvetica Chimica Acta (1977), 60(2), 660-9 или Hilpert, Hans et al. US Pat. Appl. Publ. (2005), US 2005119329:
Схема 3
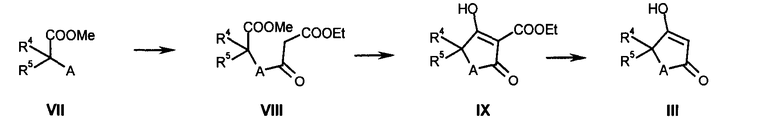
Метиловый эфир аминокислоты VII вводят в реакцию с этиловым эфиром хлоркарбонилуксусной кислоты в растворителях, подобных диэтиловому эфиру, ТГФ или предпочтительно дихлорметану, в присутствии основания, подобного алкиламину, предпочтительно триэтиламину, в температурном интервале от 0°С до 60°С, предпочтительно при 22°С, получая малонамид VIII (А=NH или А=N-C1-6алкил).
Циклизация малонамида VIII может быть проведена с помощью сильного основания, например амилата натрия, трет-бутоксида калия или, предпочтительно, гекаметилдисилазида калия, в растворителе, подобном диэтиловому эфиру, ТГФ, бензолу или, предпочтительно, толуолу, в температурном интервале от 0°С до 60°С, предпочтительно при температуре 22°С, с получением производного тетрамовой кислоты IX (А=NH или А=N-C1-6алкил).
Декарбоксилирование производного тетрамовой кислоты IX может быть проведено в присутствии как слабой, так и сильной кислоты, такой как уксусная кислота и трифторуксусная кислота, при температуре в интервале от 22°С до 100°С предпочтительно при 80°С, с получением тетрамовой кислоты III (A=NH или А=N-С1-6алкил).
II)-iii) Исходные соединения формулы III (А=СН2) могут быть получены согласно Nguyen, Hanh Nho et al., Journal of the American Chemical Society (2003), 125(39), 11818-11819 или Hamer, Neil К. et al., Tetrahedron Letters (1986), 27(19), 2167-8.
II)-iv) Исходные соединения формулы III могут быть получены согласно следующим литературным источникам:
11) Hofheinz, Werner et al., Helvetica Chimica Acta (1977), 60 (2), 660-9;
12) Galeotti, Nathalie et al., Journal of Organic Chemistry (1993), 58 (20), 5370-6;
13) Hilpert, Hans et al., U.S. Pat. Appl. Publ. (2005), US 2005 119329;
14) Krepski, Larry R. et al., Tetrahedron Letters (1985), 26 (8), 981-4;
15) Compain, Philippe et al., Synlett (1994), (11), 943-5;
16) Nguyen, Hanh Nho et al., Journal of the American Chemical Society (2003), 125(39), 11818-11819;
17) Hamer, Neil К. et al.. Tetrahedron Letters (1986), 27 (19), 2167-8;
18) Matsuo, Keizo et al., Chemical & Pharmaceutical Bulletin (1984), 32 (9), 3724-9;
19) Mizuno, Hatsuhiko et al., Chemical & Pharmaceutical Bulletin (1975), 23 (3), 527-37;
III) Исходные соединения формулы IV коммерчески доступны.
IV) Исходные соединения формулы V коммерчески доступны или могут быть получены согласно следующим литературным источникам:
1) Но, Beng Т. et al., Journal of Medicinal Chemistry (1971), 4 (6);
2) Haseg Contour-Galcera, Marie-Odile et al., Bioorganic & Medicinal Chemistry Letters (2005), 5 (15), 3555-3559;
4) Khalil, Ehab M. et al., Journal of Biological Chemistry (1998), 273 (46), 30321-30327;
5) Nenajdenko, Valentine G. et al., Tetrahedron (2004), 60 (51), 11719-11724;
6) Cheve, Gwenael et al., Medicinal Chemistry Research (2002), 11 (7), 361-379;
7) Mor, Marco et al., Journal of Medicinal Chemistry (1998), 41 (20), 3831-3844;
8) Heath-Brown, B. et al., Journal of the Chemical Society, Abstracts (1965), (Dec.), 7165-78;
9) Bastian, Jolie Anne et al., W.O. Pat. Appl. Publ. (2003), WO/2003016307;
10) D. Nagarathnam et al., Synthetic Communications (1993) 23 (14), 2011-2017;
20) Hengartner, Urs et al., Journal of Organic Chemistry (1979), 44 (22), 3741-7;
21) Yang, Shyh-Chyun et al., Indian Journal of Chemistry, Section B: Organic Chemistry Including Medicinal Chemistry (1999), 38B(8), 897-904;
22) Tsuchiya, Michihiro et al., international patent application, W08200032 (1982);
23) Pfister, Jurg R. et al., US patent application US 5436264 (1995).
Как описано выше, соединения формулы (I) являются активными соединениями и ингибируют химазу. Эти соединения, следовательно, предотвращают активацию ангиотензина II, эндотелина, TGFb, Il1, SCF, коллагеназы и разрушают белки, подобные тромбину, FN, АРО А1,2. Они могут также применяться при лечении и/или профилактике аллергических, воспалительных и/или фиброзных болезней, таких как аллергия, астма, периферическая артериальная окклюзивная болезнь, критическая ишемия конечностей, уязвимость пациентов со склеротическими бляшками, нестабильная стенокардия, застойная сердечная недостаточность, гипертрофия левого желудочка, ишемические реперфузионные нарушения, кардиомиопатия, рестеноз, ревматоидный артрит, диабетическая нефропатия, болезнь Боуэла, болезнь Крона, заживление ран (ожоги/язвы при диабете/CLI).
Профилактика и/или лечение аллергических, воспалительных или фиброзных болезней, в частности атеротромбоза или астмы, являются предпочтительными показаниями для применения.
Изобретение поэтому относится также к фармацевтическим композициям, включающим соединение по описанию выше и фармацевтически приемлемый наполнитель.
Изобретение аналогично включает соединения по определению выше для применения в качестве терапевтически активных субстанций, в частности в качестве терапевтически активных субстанций при лечении и/или профилактике аллергических, воспалительных и/или фиброзных болезней, таких как аллергия, астма, периферическая артериальная окклюзивная болезнь, критическая ишемия конечностей, уязвимость пациентов со склеротическими бляшками, нестабильная стенокардия, застойная сердечная недостаточность, гипертрофия левого желудочка, ишемические реперфузионные нарушения, кардиомиопатия, рестеноз, ревматоидный артрит, диабетическая нефропатия, болезнь Боуэла, болезнь Крона, заживление ран (ожоги/язвы при диабете/CLI).
Изобретение относится также к применению соединений по описанию выше для получения лекарственных средств при лечении и/или профилактике аллергических, воспалительных и/или фиброзных болезней, таких как аллергия, астма, периферическая артериальная окклюзивная болезнь, критическая ишемия конечностей, уязвимость пациентов со склеротическими бляшками, нестабильная стенокардия, застойная сердечная недостаточность, гипертрофия левого желудочка, ишемические реперфузионные нарушения, кардиопатия, рестеноз, ревматоидный артрит, диабетическая нефропатия, болезнь Боуэла, болезнь Крона, заживление ран (ожоги/язвы при диабете/CLI). Такие лекарственные средства включают соединение по описанию выше.
Изобретение также относится к способу и промежуточным соединениям для получения соединений формулы (I), а также способу получения промежуточных соединений.
Ингибирование химазы соединениями по настоящему изобретению может быть продемонстрировано с помощью анализа пептидного субстрата, как описано ниже.
Для химазы был выбран субстрат, содержащий 4 аминокислотных пептида (AAPF), в качестве химотрипсинподобных соединений (сукцинил-Ala-Ala-Pro-Phe-[7-амино-4-метилкумарин]; Lockhart BE, et al., Recombinant human mast-cell chymase: an improved procedure for expression in Pichia pasoris and purification of the highly active enzyme. Biotechnol. App. Biochem., published as immediate publication 26 May 2004 as manuscript BA20040074). Пептид был синтезирован с чистотой 95% (фирма Bachem, Bubendorf, Switzerland). Очищенная химаза, образованная тучными клетками человеческой кожи, получена из Calbiochem (фирма Merck Biosciences, San Diego, California, USA). Буфер для анализа содержит 0,15 М NaCl, 0,05 M Tris HCl, 0,05% CHAPS (3-[(3-холамидопропил)диметиламмоний]-1-пропансульфонат), 0,1 мг/мл гепарина (гепарин натрия, фирма Sigma, свиная кишечная мукоза), 0,02 мМ AAPF-субстрата, 1 нМ химазы при рН 7,4. Анализ проводился в 96-ячеистом планшете (Packard Optiplate) с 0,05 мл объемом при комнатной температуре. Активность химазы была охарактеризована посредством начальной скорости увеличения флуоресценции при 340/440 нм (поглощение/эмиссия) из свободного 7-амино-4-метилкумарина, выделяемого субстратом. Ингибирование активности с помощью ингибирующих соединений считывалось после 30-минутного предварительного инкубирования химазой при комнатной температуре в буфере для анализа, не содержащего AAPF-субстрат. Анализ начинался после этого при добавлении указанной концентрации AAPF-субстрата.
Величины IC50 активных соединений по настоящему изобретению предпочтительно составляли приблизительно от (1000) до (1) нМ, в частности приблизительно от (30) до (1) нМ.
Соединения формулы (I) и/или их фармацевтически приемлемые соли могут быть использованы в качестве лекарственных средств, например, в форме фармацевтических препаратов для энтерального, парентерального или топического введения. Они могут быть введены, например, перорально, например, в форме таблеток, таблеток в оболочке, драже, твердых и мягких желатиновых капсул, растворов, эмульсий или суспензий, ректально, например, в форме суппозиториев, парентерально, например, в виде инъекционных или инфузионных растворов или топически, например, в форме мазей, кремов или масел. Оральное введение является предпочтительным.
Приготовление фармацевтических препаратов может осуществляться с использованием методик, хорошо известных специалистам в области техники, и заключается во внесении описанных соединений формулы (I) и их фармацевтически приемлемых солей, необязательно в комбинации с другими терапевтически подходящими субстанциями, в лекарства, приготовленные по официально утвержденной прописи, вместе с подходящими, инертными, терапевтически совместимыми твердыми или жидкими носителями и, при неоходимости, обычными фармацевтическим наполнителями.
В качестве подходящих материалов для носителей могут использоваться как неорганические, так и органические материалы. Так, например, лактоза, кукурузный крахмал или их производные, тальк, стеариновая кислота или ее соли могут быть использованы в качестве носителей для таблеток, таблеток в оболочке, драже и твердых желатиновых капсул. Подходящими носителями для мягких желатиновых капсул могут служить, например, растительные масла, воски, жиры и полутвердые или жидкие полиолы (в зависимости от природы активного ингредиента без носителей, но с носителями в случае мягких желатиновых капсул). Подходящими носителями для получения растворов и сиропов являются, например, вода, полиолы, сахароза, инвертный сахар и им подобные. Подходящими носителями для инъекционных растворов являются, например, вода, спирты, полиолы, глицерин и растительные масла. Подходящими носителями для суппозиториев являются, например, натуральные и гидрированные масла, воски, жиры и полутвердые или жидкие полиолы. Подходящими носителями для топических препаратов являются глицериды, полусинтетические и синтетические глицериды, гидрированные масла, жидкие воски, жидкие парафины, жидкие жирные спирты, стеролы, полиэтиленгликоли и производные целлюлозы.
Обычные стабилизаторы, консерванты, смачивающие и эмульсионные агенты, улучшающие консистенцию агенты, вкусовые агенты, соли для установки осмотического давления, буферные субстанции, солюбилизаторы, красители, маскирующие агенты и оксиданты рассматриваются в качестве фармацевтических наполнителей.
Дозирование соединений формулы (I) может варьироваться в широких пределах в зависимости от подлежащей контролю болезни, возраста и индивидуального состояния пациента и способа введения и должно, конечно, соответствовать индивидуальным требованиям в каждом отдельном случае. Для взрослого пациента рекомендуемая суточная доза составляет от 1 мг до приблизительно 1000 мг, в частности от 1 мг до приблизительно 300 мг. В зависимости от тяжести болезни и определенного фармакокинетического профиля соединение может быть введено в виде одной или нескольких суточных единичных доз, например от 1 до 3 разовых доз.
Фармацевтические препараты содержат соответственно от 1 до 500 мг, предпочтительно от 1 до 100 мг соединения формулы (I).
Следующие примеры иллюстрируют настоящее изобретение более детально. Они, однако, ни в коей мере не лимитируют его объема.
Общий метод А: Получение метиловых эфиров тетроновой кислоты II (А=O)
К раствору 20 мл ЛДА (2-молярный в ТГФ) и 130 мл ТГФ добавляют при температуре от -95°С до -100°С раствор 5,47 г метилового эфира 3(Е)-метоксиакриловой кислоты в 4,5 мл ТГФ в течение 1 мин, перемешивание продолжают при этой же температуре в течение 5 мин, после чего добавляют предварительно охлажденный (-78°С) раствор альдегида (33 ммоль) в 4,5 мл ТГФ в течение 2 мин. После этого перемешивание продолжают при температуре -100°С в течение 30 мин, а затем при -78°С в течение 1 ч. Холодный раствор переносят в 130 мл ледяной воды, рН доводят до 4 с помощью 6,5 мл водного раствора HCl (37%-ный) и слои разделяют. Водный слой дважды экстрагируют дихлорметаном, органические слои промывают рассолом, высушивают и выпаривают. Остаток хроматографируют на силикагеле (н-гептан/AcOEt, в различных соотношениях), получая метиловые эфиры тетроновой кислоты II (А=O).
Общий метод Б: Получение тетроновых кислот III (А=О)
Смесь метиловых эфиров тетроновой кислоты II (А=О, 10 ммоль) и 15 мл водного раствора HCl (37%-ный) перемешивают при температуре 40°С до полного завершения реакции. Образовавшуюся суспензию фильтруют, остаток промывают ледяной водой и высушивают. Масляную реакционную смесь экстрагируют дихлорметаном, органические слои промывают рассолом, высушивают и выпаривают. Остаток или тритурируют со смесью AcOEt/гексан, или хроматографируют, используя смесь дихлорметан/МеОН (в различных соотношениях), получая тетроновые кислоты III (А=О).
Общий метод В: Получение тетрамовых кислот III (А=NH или А=N-C1-6алкил)
К смеси метиловых эфиров аминокислоты VII (А=NH2 или А=N(H)(C1-6алкил), 18 ммоль) в дихлорметане (60 мл) последовательно добавляют при температуре 0°С триэтиламин (56 ммоль) и этиловый эфир хлоркарбонилуксусной кислоты (21,5 ммоль) и перемешивание продолжают в течение ночи. Суспензию фильтруют, фильтрат выпаривают и остаток распределяют между разбавленным водным раствором хлористоводородной кислоты и этилацетатом. Органический слой высушивают, выпаривают и остаток хроматографируют на силикагеле, используя смесь циклогексан/этилацетат (в соотношении 2:1), получая амид малоновой кислоты VIII (А=NH или А=N-C1-6алкил).
Смесь амида малоновой кислоты VIII (А=NH или А=N-C1-6алкил, 7 ммоль) в толуоле (12 мл) обрабатывают при температуре 22°С раствором гексаметилдисилазида калия в ТГФ (0,9-молярный, 7 ммоль) и перемешивание продолжают в течение 1-16 ч. Образовавшуюся суспензию фильтруют и остаток высушивают, получая производное тетрамовой кислоты IX (А=NH или А=N-С1-6алкил).
Смесь производного тетрамовой кислоты IX (А=NH или А=С1-6алкил, 7 ммоль) в уксусной кислоте (40 мл) и трифторуксусной кислоты (4 мл) нагревают с обратным холодильником в течение 1-5 ч. Смесь выпаривают, а остаток хроматографируют на силикагеле, используя диэтиловый эфир и получая тетрамовую кислоту III (A=NH или А=N-C1-6алкил).
Пример А: 4-Гидрокси-5-метил-5-фенил-5Н-фуран-2-он
А1. Используя общий метод А, ацетофенон вводят в реакцию с метиловым эфиром 3(Е)-метоксиакриловой кислоты, получая рац-4-метокси-5-метил-5-фенил-5Н-фуран-2-он в виде бесцветного твердого вещества. МС: 204,1 ([M]+).
А2. рац-4-Метокси-5-метил-5-фенил-5Н-фуран-2-он (0,50 г) отделяют на Chiralpack AD, используя смесь н-гептан/этанол в соотношении 9:1 и получая (S)-4-метокси-5-метил-5-фенил-5Н-фуран-2-он (0,24 г) в виде быстро выходящего пика и (R)-4-метокси-5-метил-5-фенил-5Н-фуран-2-он (0,24 г) в виде медленнее выходящего пика.
A3. Используя общий метод В, (S)-4-метокси-5-метил-5-фенил-5Н-фуран-2-он гидролизуют, получая (S)-4-гидрокси-5-метил-5-фенил-5Н-фуран-2-он в виде бесцветного твердого вещества. МС: 190,2 ([М]+). [α]365нм: -420,4° (1%, CHCl3).
А4. Используя общий метод В, (R)-4-метокси-5-метил-5-фенил-5Н-фуран-2-он гидролизуют, получая (R)-4-гидрокси-5-метил-5-фенил-5Н-фуран-2-он в виде бесцветного твердого вещества. МС: 190,2 ([M]+) [α]365нм: +441,5° (1%, CHCl3).
Пример Б: рац-5-(2-Циклогексилэтил)-4-гидрокси-5Н-фуран-2-он
Б1. Используя общий метод А, циклогексанпропаналь (Stratakis, Manolis et al., Journal of Organic Chemistry (2002), 67 (25), 8758-8763) вводят в реакцию с метиловым эфиром 3(Е)-метоксиакриловой кислоты, получая рац-5-(2-циклогексилэтил)-4-метокси-5Н-фуран-2-он в виде бесцветного твердого вещества. МС: 225,2 ([М+Н]+).
Б2. Используя общий метод Б, рац-5-(2-циклогексилэтил)-4-метокси-5Н-фуран-2-он гидролизуют, получая рац-5-(2-циклогексилэтил)-4-гидрокси-5Н-фуран-2-он в виде коричневого масла. МС: 211,1 ([М+Н]+).
Пример В: рац-1-Гидрокси-7а-метил-5,6,7,7а-тетрагидропирролизин-3-он
Используя общий метод В, метиловый эфир рац-2-метилпирролидин-2-карбоновой кислоты превращают в названное в заголовке соединение, выделяя его в виде желтого твердого вещества. МС: 154,3 ([М+Н]+).
Пример Г: (R)-5-Бензил-4-гидрокси-5-метил-1,5-дигидропиррол-2-он
Используя общий метод В, метиловый эфир (R)-2-амино-2-метил-3-фенилпропионовой кислоты превращают в названное в заголовке соединение, выделяя его в виде белого твердого вещества. МС: 204,1 ([М+Н]+).
Пример Д: (R)-4-Гидрокси-5-изопропил-5-метил-1,5-дигидропиррол-2-он
Используя общий метод В, метиловый эфир (R)-2-амино-2,3-диметилмасляной кислоты превращают в названное в заголовке соединение, выделяя его в виде белого твердого вещества. МС: 156,3 ([М+Н]+).
Пример Е: (R)-4-гидрокси-5-метил-5-фенил-1,5-дигидропиррол-2-он
Используя общий метод В, метиловый эфир (R)-2-амино-2-фенилпропионовой кислоты превращают в названное в заголовке соединение [литературная ссылка 19], выделяя его в виде бесцветного масла, МС: 190,3 ([М+Н]+). [α]365 нм: +360,9° (с=1%, CHCl3).
Общий метод Г: Конденсация винилогенной кислоты III, альдегида IV и индола V
Раствор винилогенной кислоты (1 ммоль), альдегида (1,3 ммоль) и индола (1 ммоль) в уксусной кислоте (2 мл) перемешивают при температуре 70°С в течение 16 ч. Суспензию фильтруют и остаток промывают смесью MeOH/Et2O (в соотношении 1:10). Если не происходит выпадения осадка, раствор очищают с помощью препаративной ВЭЖХ (RP-18, CH3CN/Н2О, градиент).
Пример 1: N-(2-{2-[(4-Гидрокси-5-изопропил-2-оксо-2,5-дигидро-1Н-пиррол-3-ил)фенилметил]-1Н-индол-3-ил}этил)ацетамид
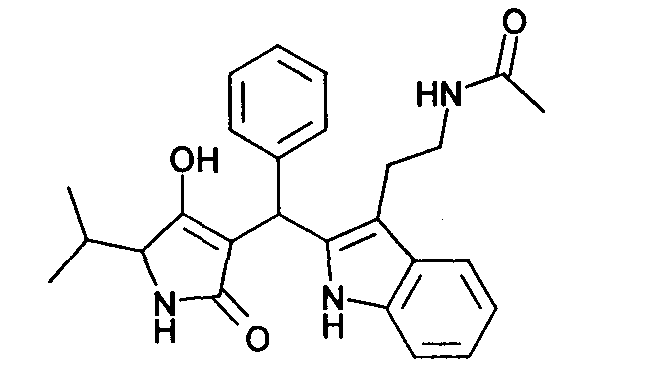
Используя общий метод В, 4-гидрокси-5-изопропил-1,5-дигидропиррол-2-он (литературная ссылка 11) вводят в реакцию с бензальдегидом и N-[2-(1H-индол-3-ил)-этил]ацетамидом, получая названное в заголовке соединение в виде бледно-желтого твердого вещества. МС: 432,5 ([М+Н]+).
Пример 2: N-(2-{2-[(3-фторфенил)-(4-гидрокси-5-изопропил-2-оксо-2,5-дигидро-1Н-пиррол-3-ил)метил]-1Н-индол-3-ил}этил)ацетамид
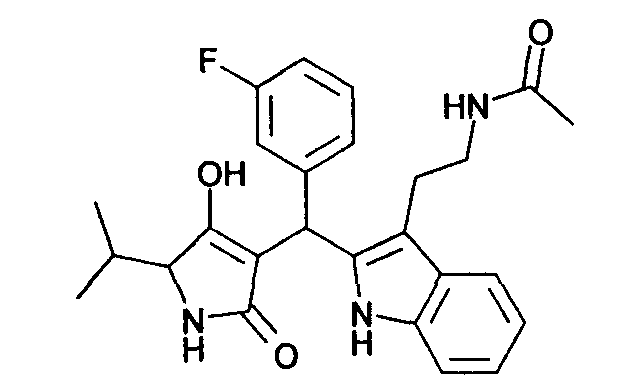
Используя общий метод В, 4-гидрокси-5-изопропил-1,5-дигидропиррол-2-он (литературная ссылка 11) вводят в реакцию с 3-фторбензальдегидом и N-[2-(1Н-индол-3-ил)этил]ацетамидом, получая названное в заголовке соединение в виде желтого твердого вещества. МС: 450,1 ([М+Н]+).
Пример 3: N-(2-{2-[(4-Фторфенил)-(4-гидрокси-5-изопропил-2-оксо-2,5-дигидро-1Н-пиррол-3-ил)метил]-1Н-индол-3-ил}этил)ацетамид
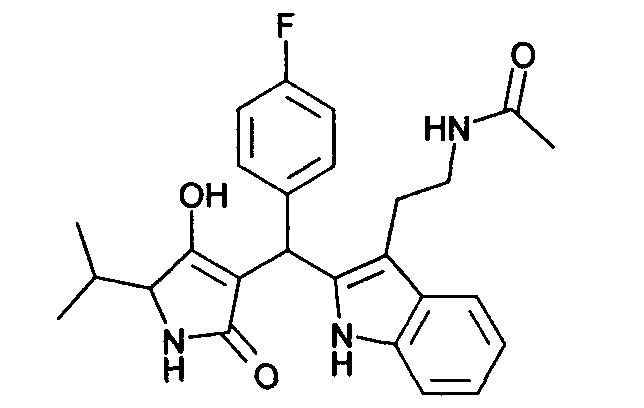
Используя общий метод В, 4-гидрокси-5-изопропил-1,5-дигидропиррол-2-он (литературная ссылка 11) вводят в реакцию с 4-фторбензальдегидом и N-[2-(1Н-индол-3-ил)этил]ацетамидом, получая названное в заголовке соединение в виде желтого твердого вещества. МС: 450,3 ([М+Н]+).
Пример 4: N-(2-{2-[(3,5-Дифторфенил)-(4-гидрокси-5-изопропил-2-оксо-2,5-дигидро-1Н-пиррол-3-ил)метил]-1Н-индол-3-ил}этил)ацетамид
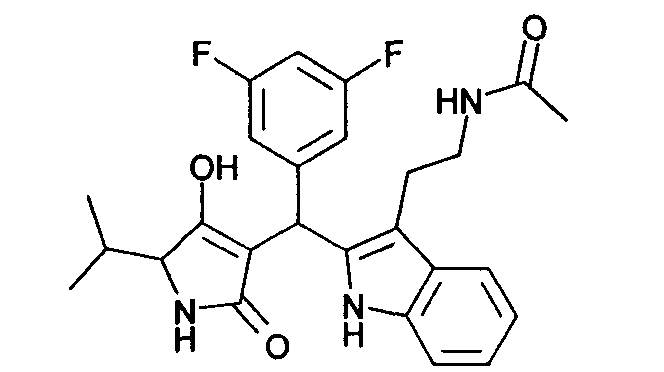
Используя общий метод В, 4-гидрокси-5-изопропил-1,5-дигидропиррол-2-он (литературная ссылка 11) вводят в реакцию с 3,5-дифторбензальдегидом и N-[2-(1Н-индол-3-ил)этил]ацетамидом, получая названное в заголовке соединение в виде желтого твердого вещества. МС: 468,0 ([М+Н]+).
Пример 5: Этиловый эфир 2-{2-[(4-гидрокси-5-изопропил-2-оксо-2,5-дигидро-1Н-пиррол-3-ил)фенилметил]-1Н-индол-3-ил}уксусной кислоты
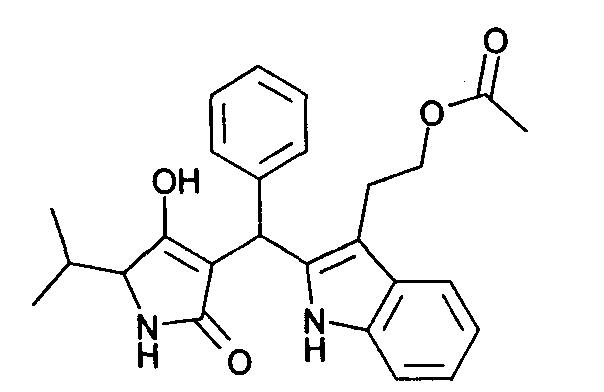
Используя общий метод В, 4-гидрокси-5-изопропил-1,5-дигидропиррол-2-он (литературная ссылка 11) вводят в реакцию с бензальдегидом и 2-(1Н-индол-3-ил)этанолом, получая названное в заголовке соединение в виде оранжевой пены. МС: 433,3 ([M+H]+).
Пример 6: 4-Гидрокси-3-{[3-(2-гидроксиэтил)-1Н-индол-2-ил]фенилметил}-5-изопропил-1,5-дигидропиррол-2-он
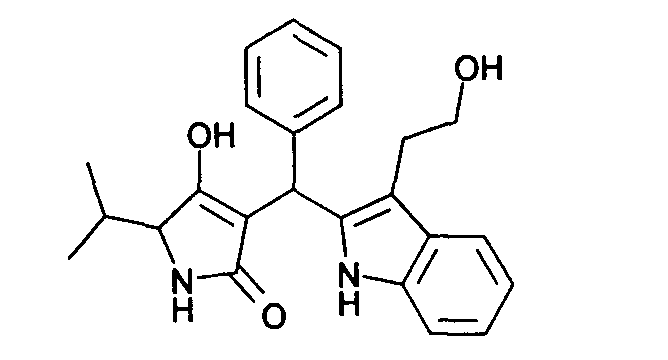
Раствор этилового эфира 2-{2-[(4-гидрокси-5-изопропил-2-оксо-2,5-дигидро-1Н-пиррол-3-ил)фенилметил]-1Н-индол-3-ил}уксусной кислоты (40 мг) и LiOH (8,5 мг) в МеОН (0,5 мл) перемешивают при температуре 22°С в течение 30 мин и выпаривают. Остаток распределяют между 0,1-нормальным водным раствором HCl и AcOEt и органический слой высушивают и выпаривают. Остаток хроматографируют на силикагеле, используя смесь CH2Cl2/МеОН (в соотношении 10:3) и получая названное в заголовке соединение в виде оранжевой пены. МС: 391,1 ([М+Н]+).
Пример 7: N-(2-{2-[(4-Гидрокси-5-изопропил-2-оксо-2,5-дигидро-1Н-пиррол-3-ил)фенилметил]-1Н-индол-3-ил}этил)бензамид
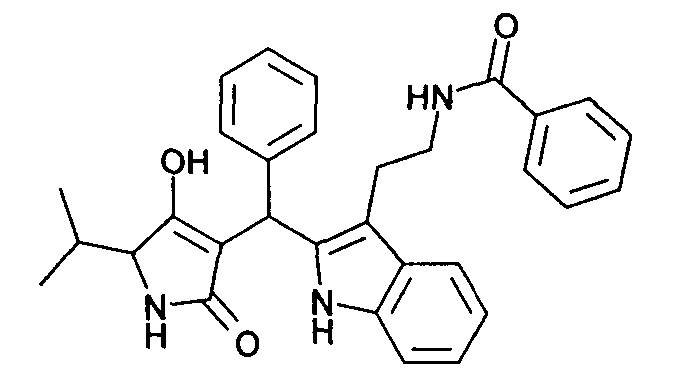
Используя общий метод В, 4-гидрокси-5-изопропил-1,5-дигидропиррол-2-он (литературная ссылка 11) вводят в реакцию с бензальдегидом и N-[2-(1H-индол-3-ил)этил]бензамидом, получая названное в заголовке соединение в виде серого твердого вещества. МС: 494,3 ([М+Н]+).
Пример 8: N-(2-{2-[(4-Гидрокси-5-изопропил-2-оксо-2,5-дигидро-1Н-пиррол-3-ил)фенилметил]-1Н-индол-3-ил}этил)-3,5-бис-трифторметилбензамид
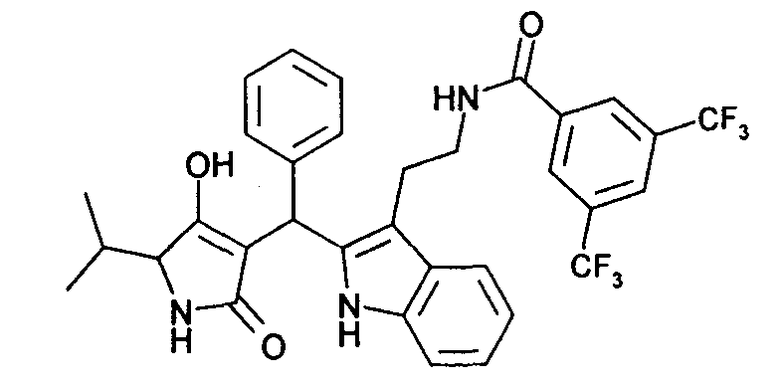
8.1. Получение N-[2-(1Н-индол-3-ил)этил]-3,5-бис-трифторметилбензамида
К раствору 2-(1Н-индол-3-ил)этиламина (1,0 г) в CH2Cl2 добавляют при температуре 22°С NEt3 (1,74 мл) и 3,5-бис-трифторметилбензоилхлорид (1,24 мл), после чего перемешивание проводят при температуре 22°С в течение 16 ч. Смесь промывают водным раствором NaHCO3 и рассолом, а затем органический слой высушивают и выпаривают, получая названное в заголовке соединение в виде коричневого твердого вещества. МС: 401,3 ([М+Н]+).
8.2. Используя общий метод В, 4-гидрокси-5-изопропил-1,5-дигидропиррол-2-он (литературная ссылка 11) вводят в реакцию с бензальдегидом и N-[2-(1Н-индол-3-ил)этил]-3,5-бис-трифторметилбензамидом, получая N-(2-{2-[(4-гидрокси-5-изопропил-2-оксо-2,5-дигидро-1Н-пиррол-3-ил)фенилметил]-1Н-индол-3-ил}этил)-3,5-бис-трифторметилбензамид в виде красного твердого вещества. МС: 630,2 ([М+Н]+).
Пример 9: (2-{2-[(4-гидрокси-5-изопропил-2-оксо-2,5-дигидро-1H-пиррол-3-ил)фенилметил]-1Н-индол-3-ил}этил)амид нафталинсульфоновой кислоты
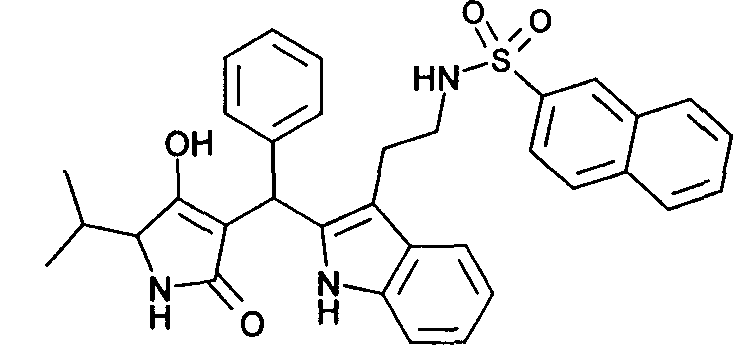
Используя общий метод В, 4-гидрокси-5-изопропил-1,5-дигидропиррол-2-он (литературная ссылка 11) вводят в реакцию с бензальдегидом и [2-(1Н-индол-3-ил)этил]амидом нафталин-2-сульфоновой кислоты (литературная ссылка 1), получая названное в заголовке соединение в виде оранжевого твердого вещества. МС: 580,3 ([М+Н]+).
Пример 10: 3-[(5-Фтор-3-метил-1Н-индол-2-ил)фенилметил1-4-гидрокси-5-изопропил-1,5-дигидропиррол-2-он
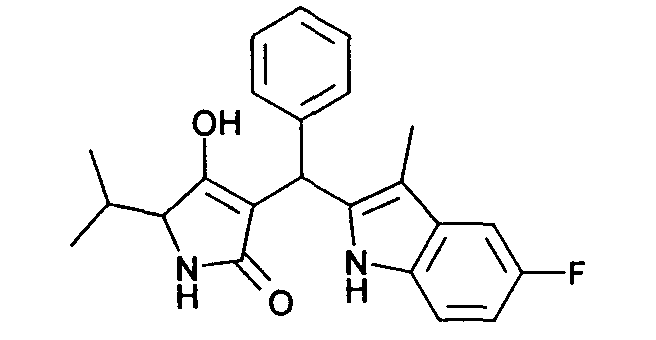
Используя общий метод В, 4-гидрокси-5-изопропил-1,5-дигидропиррол-2-он (литературная ссылка 11) вводят в реакцию с бензальдегидом и 5-фтор-3-метил-1Н-индолом, получая названное в заголовке соединение в виде желтого твердого вещества. МС: 377,1 ([М-Н]-).
Пример 11: 3-[(5-Фтор-3-метил-1Н-индол-2-ил)фенилметил]-4-гидрокси-5-изопропил-1-метил-1,5-дигидропиррол-2-он
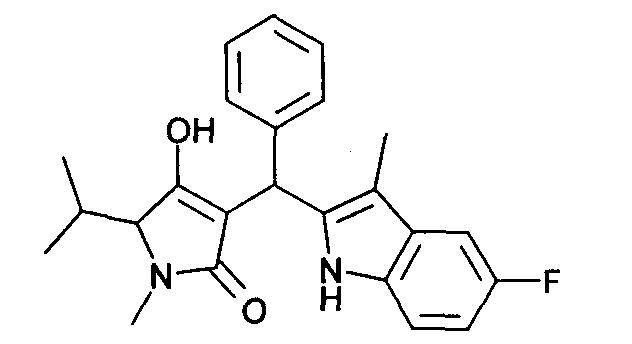
Используя общий метод В, 4-гидрокси-5-изопропил-1-метил-1,5-дигидропиррол-2-он (литературная ссылка 12) вводят в реакцию с бензальдегидом и 5-фтор-3-метил-1Н-индолом, получая названное в заголовке соединение в виде желтого твердого вещества. МС: 391,3 ([М-Н]-).
Пример 12: 4-Гидрокси-5-изопропил-3-[(3-метил-1Н-индол-2-ил)фенилметил]-1,5-дигидропиррол-2-он
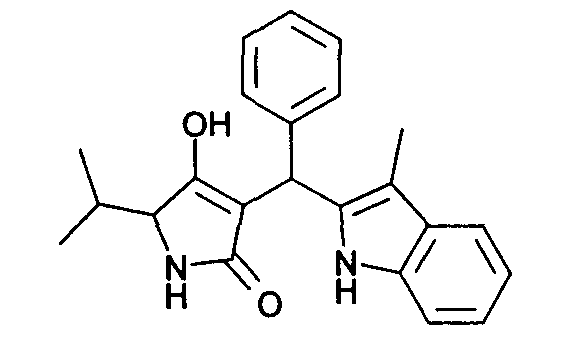
Используя общий метод В, 4-гидрокси-5-изопропил-1,5-дигидропиррол-2-он (литературная ссылка 11) вводят в реакцию с бензальдегидом и 3-метил-1Н-индолом, получая названное в заголовке соединение в виде желтого твердого вещества. МС: 361,0 ([М+Н]+).
Пример 13: 3-[(5-Фтор-3-изопропил-1Н-индол-2-ил)фенилметил1-4-гидрокси-5-изопропил-1,5-дигидропиррол-2-он
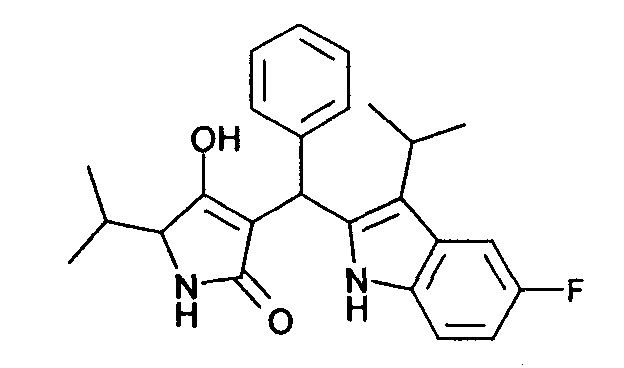
13.1. 5-Фтор-3-изопропил-1Н-индол получают аналогично методу, описанному в литературной ссылке 10, в виде коричневатого масла, МС: 177,0 ([M]+).
13.2. Используя общий метод В, 4-гидрокси-5-изопропил-1,5-дигидропиррол-2-он (литературная ссылка 11) вводят в реакцию с бензальдегидом и 5-фтор-3-изопропил-1Н-индолом, получая 3-[(5-фтор-3-изопропил-1Н-индол-2-ил)фенилметил]-4-гидрокси-5-изопропил-1,5-дигидропиррол-2-он в виде оранжевого твердого вещества. МС: 405,2 ([М-Н]-).
Пример 14: N-(2-{2-[(4-Гидрокси-2-оксо-2,5-дигидрофуран-3-ил)фенилметил]-1Н-индол-3-ил}этил)ацетамид
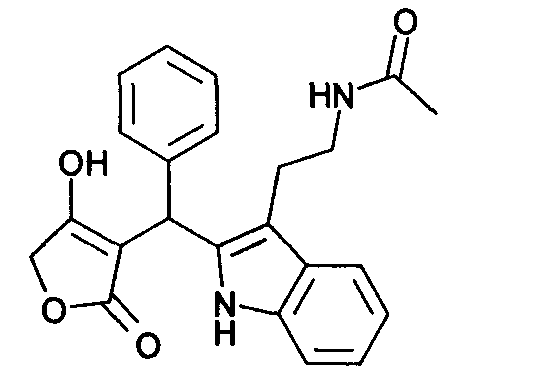
Используя общий метод В, 4-гидрокси-5Н-фуран-2-он вводят в реакцию с бензальдегидом и N-[2-(1H-индол-3-ил)этил]ацетамидом, получая названное в заголовке соединение в виде оранжевой пены. МС: 391,1 ([М+Н]+).
Пример 15: N-(2-{2-[(5-Бензил-4-гидрокси-2-оксо-2,5-дигидрофуран-3-ил)фенилметил]-1Н-индол-3-ил}этил)ацетамид
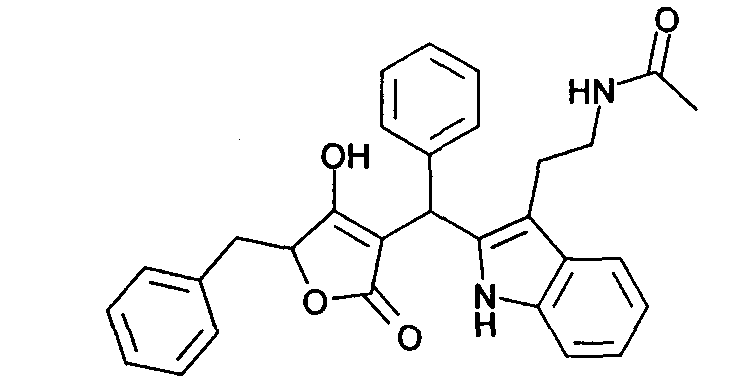
Используя общий метод В, 5-бензил-4-гидрокси-5Н-фуран-2-он (литературная ссылка 13) вводят в реакцию с бензальдегидом и N-[2-(1Н-индол-3-ил)этил]ацетамидом, получая названное в заголовке соединение в виде белого твердого вещества. МС: 481,0 ([М+Н]+).
Пример 16: N-(2-{2-[(5-Бензил-4-гидрокси-2-оксо-2,5-дигидрофуран-3-ил)фенилметил]-6-фтор-1Н-индол-3-ил}этил)ацетамид
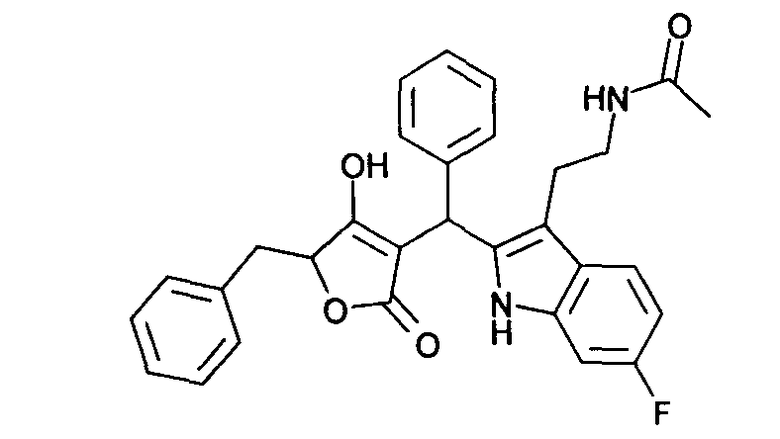
16.1. N-[2-(6-Фтор-1Н-индол-3-ил)этил]ацетамид
К раствору 2-(6-фтор-1Н-индол-3-ил)этиламина (0,88 г) и NEt3 (2,27 мл) в CH2Cl2 (8 мл) добавляют ангидрид уксусной кислоты (0,43 мл) и перемешивают при температуре 22°С в течение 1 ч. Затем смесь промывают 1-нормальным водным раствором HCl, органический слой высушивают и выпаривают. Остаток хроматографируют на силикагеле, используя смесь CH2Cl2/МеОН (в соотношении 25:1), получая названное в заголовке соединение в виде бледно-желтого масла. МС: 219,1 ([M-Н]-).
16.2 Используя общий метод В, 5-бензил-4-гидрокси-5Н-фуран-2-он (литературная ссылка 13) вводят в реакцию с бензальдегидом и N-[2-(6-фтор-1Н-индол-3-ил)этил]ацетамидом, получая N-(2-{2-[(5-бензил-4-гидрокси-2-оксо-2,5-дигидрофуран-3-ил)фенилметил]-6-фтор-1Н-индол-3-ил}этил)ацетамид в виде белого твердого вещества. МС: 497,4 ([М-Н]-).
Пример 17: N-(2-{2-[(5-Бензил-4-гидрокси-2-оксо-2,5-дигидрофуран-3-ил)фенилметил]-5-хлор-1Н-индол-3-ил}этил)ацетамид
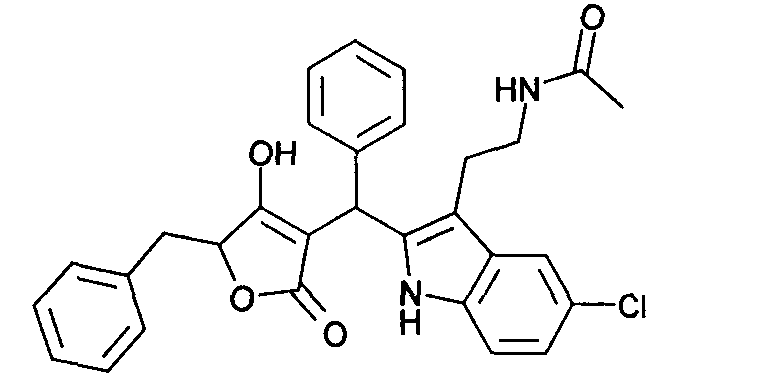
Используя общий метод В, 5-бензил-4-гидрокси-5Н-фуран-2-он (литературная ссылка 13) вводят в реакцию с бензальдегидом и N-[2-(5-хлор-1Н-индол-3-ил)этил]ацетамидом (литературная ссылка 2), получая названное в заголовке соединение в виде белого твердого вещества. МС: 513,1 ([М-Н]-).
Примеры 18 и 19: 5-Бензил-3-{[6-фтор-3-(2-гидроксиэтил)-1Н-индол-2-ил]фенилметил}-4-гидрокси-5Н-фуран-2-он и этиловый эфир 2-{2-[(5-бензил-4-гидрокси-2-оксо-2,5-дигидрофуран-3-ил)фенилметил]-6-фтор-1Н-индол-3-ил}уксусной кислоты
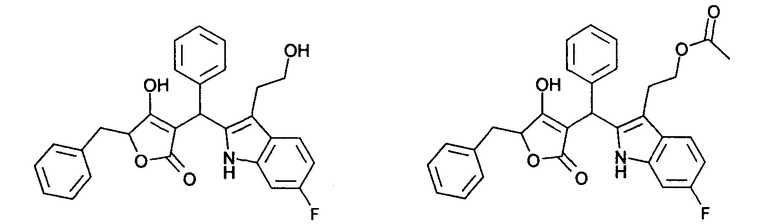
Используя общий метод В, 5-бензил-4-гидрокси-5Н-фуран-2-он (литературная ссылка 13) вводят в реакцию с бензальдегидом и 2-(6-фтор-1Н-индол-3-ил)этанолом (литературная ссылка 3). Смесь разделяют с помощью ВЭЖХ, получая первое названное в заголовке соединение в виде светло-коричневого твердого вещества. МС: 456,3 ([М-Н]-).
Вторая фракция содержит названное в заголовке соединение в виде оранжевого вещества. МС: 498,1 ([М-Н]-).
Пример 20: N-(2-{2-[1-(5-Бензил-4-гидрокси-2-оксо-2,5-дигидрофуран-3-ил)-2-метилпропил]-1Н-индол-3-ил}этил)ацетамид
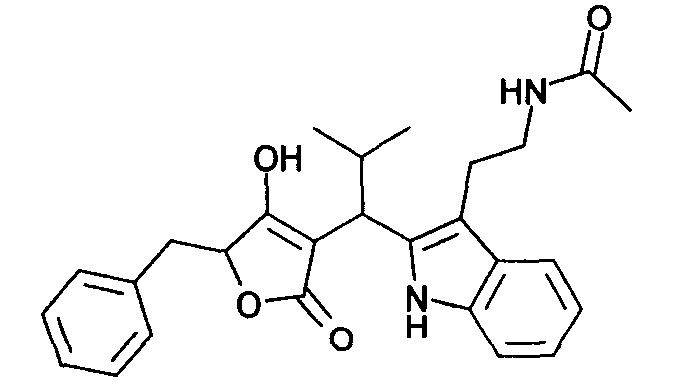
Используя общий метод В, 5-бензил-4-гидрокси-5Н-фуран-2-он (литературная ссылка 13) вводят в реакцию с 2-метилпропиональдегидом и N-[2-(1Н-индол-3-ил)этил]ацетамидом, получая названное в заголовке соединение в виде желтого твердого вещества. МС: 445,1 ([М-Н]-).
Пример 21: N-(2-{2-[1-(5-Бензил-4-гидрокси-2-оксо-2,5-дигидрофуран-3-ил)-3-метилбутил]-1Н-индол-3-ил}этил)ацетамид
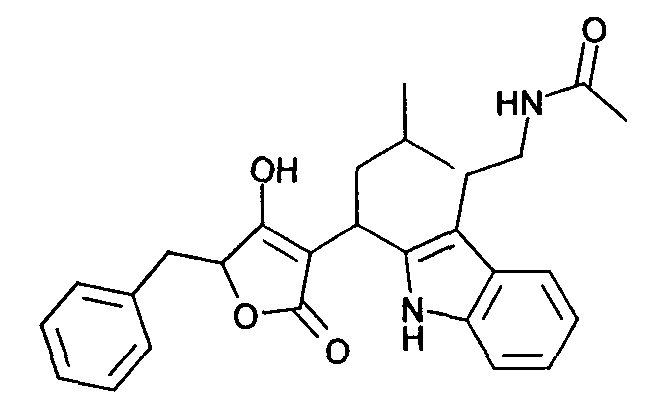
Используя общий метод В, 5-бензил-4-гидрокси-5Н-фуран-2-он (литературная ссылка 13) вводят в реакцию с 3-метилбутиральдегидом и N-[2-(1Н-индол-3-ил)этил]ацетамидом, получая названное в заголовке соединение в виде желтого твердого вещества. МС: 459,1 ([М-Н]-).
Пример 22
N-(2-{2-[1-(5-Бензил-4-гидрокси-2-оксо-2,5-дигидрофуран-3-ил)-пенту1]-1Н-индол-3-ил}этил)ацетамид
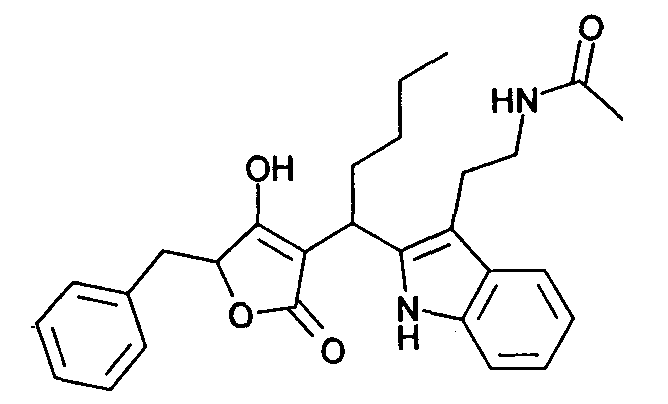
Используя общий метод В, 5-бензил-4-гидрокси-5Н-фуран-2-он (литературная ссылка 13) вводят в реакцию с пентаналем и Н-[2-(1Н-индол-3-ил)этил]ацетамидом, получая названное в заголовке соединение в виде белого твердого вещества. МС: 459,3 ([М-Н]-).
Пример 23: N-(2-{2-[1-(5-Бензил-4-гидрокси-2-оксо-2,5-дигидрофуран-3-ил)-2-фенилэтил]-1Н-индол-3-ил}этил)ацетамид
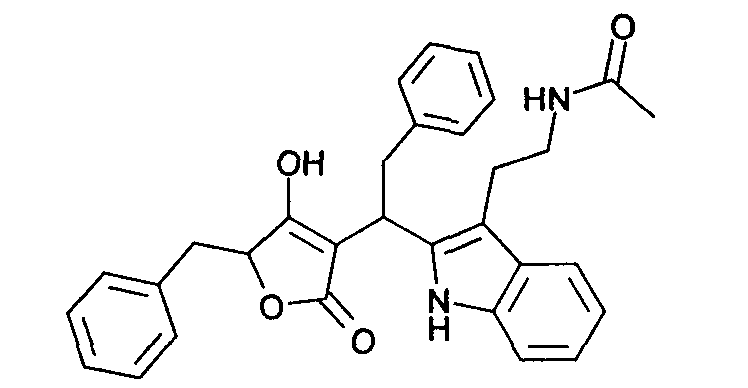
Используя общий метод В, 5-бензил-4-гидрокси-5Н-фуран-2-он (литературная ссылка 13) вводят в реакцию с фенилацетальдегидом и N-[2-(1H-индол-3-ил)-этил]ацетамидом, получая названное в заголовке соединение в виде белого твердого вещества. МС: 493,0 ([М-Н]-).
Пример 24: N-(2-{2-[1-(5-Бензил-4-гидрокси-2-оксо-2,5-дигидрофуран-3-ил)-3-фенилпропил]-1Н-индол-3-ил}этил)ацетамид

Используя общий метод В, 5-бензил-4-гидрокси-5Н-фуран-2-он (литературная ссылка 13) вводят в реакцию с 3-фенилпропиональдегидом и N-[2-(1Н-индол-3-ил)этил]ацетамидом, получая названное в заголовке соединение в виде желтого твердого вещества. МС: 507,2 ([М-Н]-).
Пример 25: N-(2-{2-[(5-Бензил-4-гидрокси-2-оксо-2,5-дигидрофуран-3-ил)-(2-фторфенил)метил]-1Н-индол-3-ил}этил)ацетамид
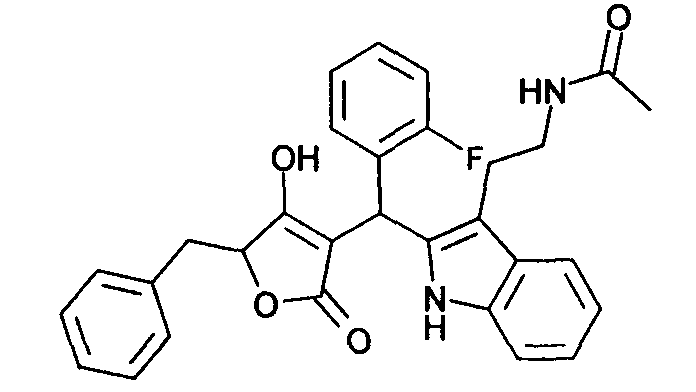
Используя общий метод В, 5-бензил-4-гидрокси-5Н-фуран-2-он (литературная ссылка 13) вводят в реакцию с 2-фторбензальдегидом и N-[2-(1H-индол-3-ил)этил]ацетамидом, получая названное в заголовке соединение в виде белого твердого вещества. МС: 497,3 ([М-Н]-).
Пример 26: 3-{[3-(2-Аминоэтил)-6-фтор-1H-индол-2-ил]фенилметил}-5-бензил-4-гидрокси-5Н-фуран-2-он; соль с уксусной кислотой
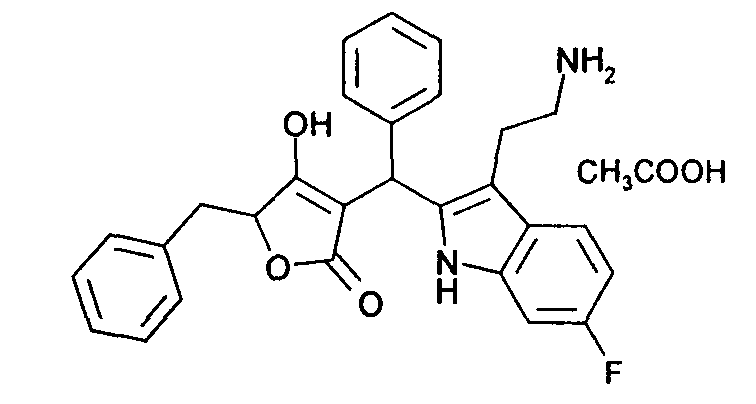
Используя общий метод В, 5-бензил-4-гидрокси-5Н-фуран-2-он (литературная ссылка 13) вводят в реакцию с бензальдегидом и 2-(6-фтор-1Н-индол-3-ил)этиламином, получая названное в заголовке соединение в виде светло-красной пены. МС: 457,1 ([М+Н]+).
Пример 27: N-(2-{2-[(5-Бензил-4-гидрокси-2-оксо-2,5-дигидрофуран-3-ил)фенилметил]-1Н-индол-3-ил}этил)-N-метилацетамид
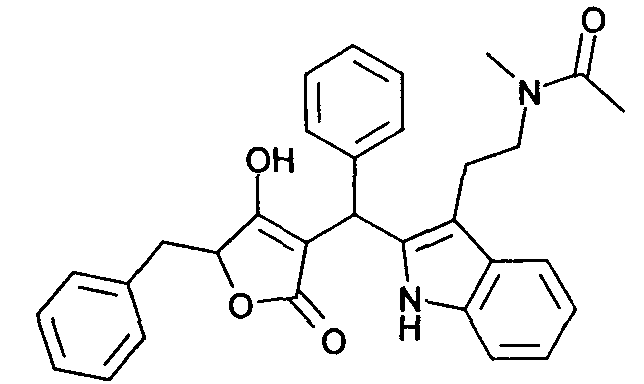
Используя общий метод В, 5-бензил-4-гидрокси-5Н-фуран-2-он (литературная ссылка 13) вводят в реакцию с бензальдегидом и N-[2-(1Н-индол-3-ил)этил]-N-метилацетамидом (литературная ссылка 4), получая названное в заголовке соединение в виде светло-желтого твердого вещества. МС: 493,3 ([М-Н]-).
Пример 28: N-(2-{2-[(5-Бензил-4-гидрокси-2-оксо-2,5-дигидрофуран-3-ил)фенилметил]-5-фтор-1Н-индол-3-ил}этил)ацетамид
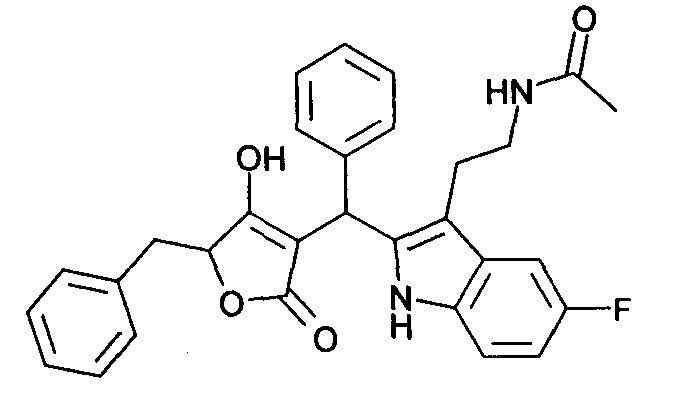
Используя общий метод В, 5-бензил-4-гидрокси-5Н-фуран-2-он (литературная ссылка 13) вводят в реакцию с бензальдегидом и N-[2-(5-фтор-1Н-индол-3-ил)этил]ацетамидом (литературная ссылка 5), получая названное в заголовке соединение в виде бледно-желтого твердого вещества. МС: 497,4 ([М-Н]-).
Пример 29: N-(2-{2-[(5-Бензил-4-гидрокси-2-оксо-2,5-дигидрофуран-3-ил)фенилметил]-1-метил-1Н-индол-3-ил}этил)ацетамид
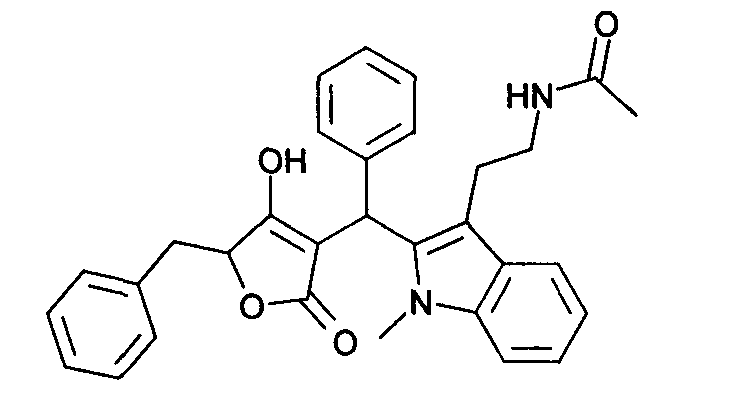
29.1. N-[2-(l-Метил-1Н-индол-3-ил)этил]ацетамид получают из 2-(1-метил-1Н-индол-3-ил)этиламина посредством ацилирования, описанного в примере 16.1, в виде светло-зеленого масла, МС: 217,4 ([М+Н]+).
29.2. Используя общий метод В, 5-бензил-4-гидрокси-5Н-фуран-2-он (литературная ссылка 13) вводят в реакцию с бензальдегидом и N-[2-(1-метил-1Н-индол-3-ил)этил]ацетамидом, получая N-(2-{2-[(5-бензил-4-гидрокси-2-оксо-2,5-дигидрофуран-3-ил)фенилметил]-1-метил-1Н-индол-3-ил}этил)ацетамид в виде красного твердого вещества. МС: 493,3 ([М-Н]-).
Пример 30: 5-Бензил-3-[(5-фтор-3-метил-1Н-индол-2-ил)фенилметил]-4-гидрокси-5Н-фуран-2-он
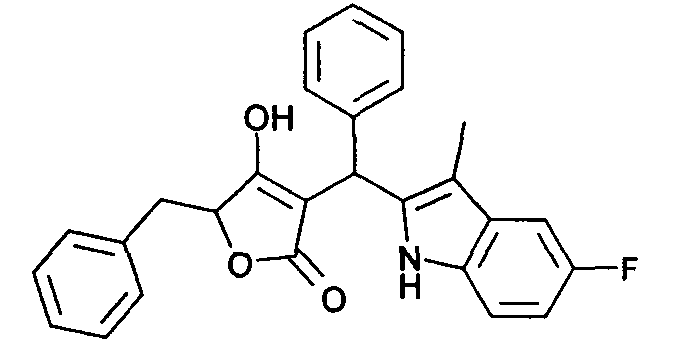
Используя общий метод В, 5-бензил-4-гидрокси-5Н-фуран-2-он (литературная ссылка 13) вводят в реакцию с бензальдегидом и 5-фтор-3-метил-1H-индолом, получая названное в заголовке соединение в виде бесцветного твердого вещества. МС: 426,1 ([М-Н]-).
Пример 31: N-(2-{6-Фтор-2-[(4-гидрокси-2-оксо-5-фенил-2,5-дигидрофуран-3-ил)фенилметил]-1Н-индол-3-ил}этил)ацетамид
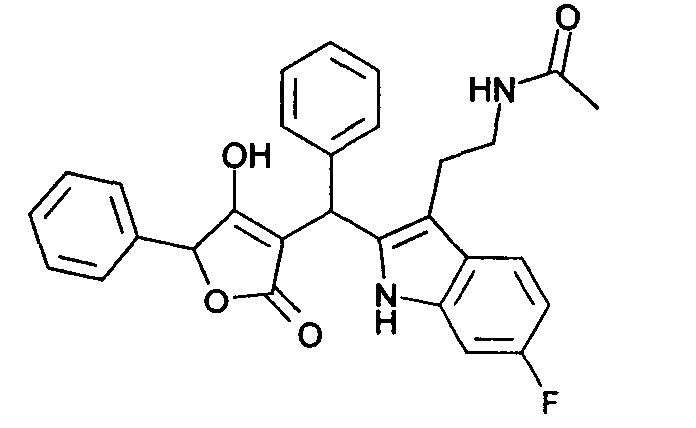
Используя общий метод В, 4-гидрокси-5-фенил-5Н-фуран-2-он (литературная ссылка 14) вводят в реакцию с бензальдегидом и N-[2-(6-фтор-1Н-индол-3-ил)этил]ацетамидом (пример 18.1), получая названное в заголовке соединение в виде светло-коричневого твердого вещества. МС: 485,0 ([М+Н]+).
Пример 32: 3-{[3-(2-Аминоэтил)-6-этил-1Н-индол-2-ил]фенилметил}-4-гидрокси-5-фенил-5Н-фуран-2-он
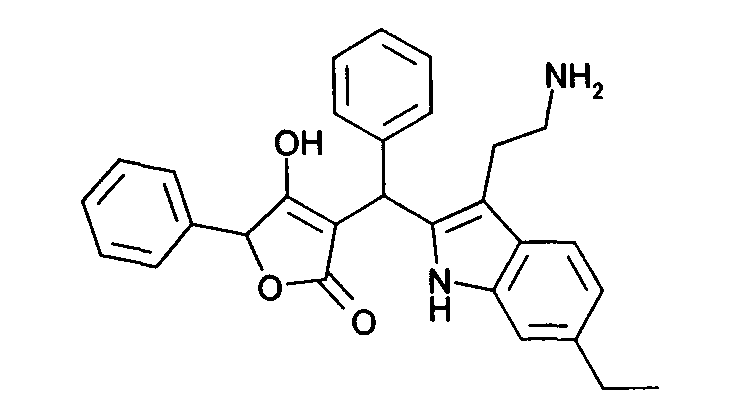
Используя общий метод В, 4-гидрокси-5-фенил-5Н-фуран-2-он (литературная ссылка 14) вводят в реакцию с бензальдегидом и 2-(6-этил-1Н-индол-3-ил)этиламином (литературная ссылка 8), получая названное в заголовке соединение в виде белого твердого вещества. МС: 453,3 ([М+Н]+).
Пример 33: N-(2-{6-Фтор-2-[(4-гидрокси-5-метил-2-оксо-5-фенил-2,5-дигидрофуран-3-ил)фенилметил]-1Н-индол-3-ил}этил)ацетамид
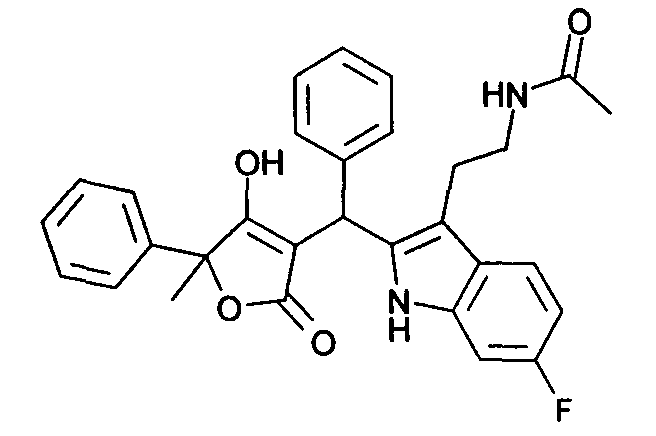
Используя общий метод В, 4-гидрокси-5-метил-5-фенил-5Н-фуран-2-он (пример А2) вводят в реакцию с бензальдегидом и N-[2-(6-фтор-1Н-индол-3-ил)этил]ацетамидом (пример 18.1), получая названное в заголовке соединение в виде светло-коричневого твердого вещества. МС: 499,5 ([М+Н]+).
Пример 34: N-(2-{2-[(4-Гидрокси-5-изобутил-2-оксо-2,5-дигидрофуран-3-ил)фенилметил]-1Н-индол-3-ил}этил)ацетамид
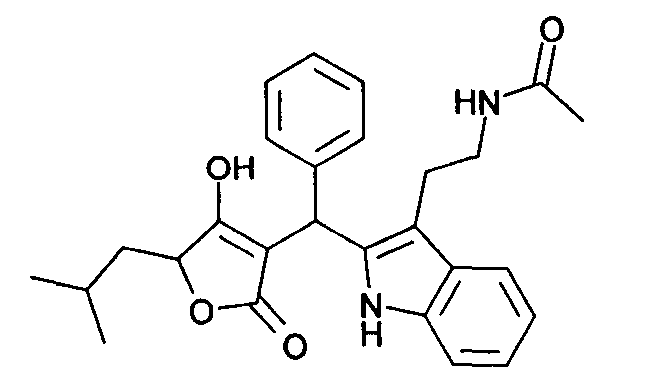
Используя общий метод В, 4-гидрокси-5-изобутил-5Н-фуран-2-он (литературная ссылка 14) вводят в реакцию с бензальдегидом и N-[2-(1Н-индол-3-ил)этил]ацетамидом, получая названное в заголовке соединение в виде белого твердого вещества. МС: 441,1 ([М+Н]+).
Пример 35: этиловый эфир 2-{2-[(4-гидрокси-5-изобутил-2-оксо-2,5-дигидрофуран-3-ил)фенилметил]-1Н-индол-3-ил}уксусной кислоты
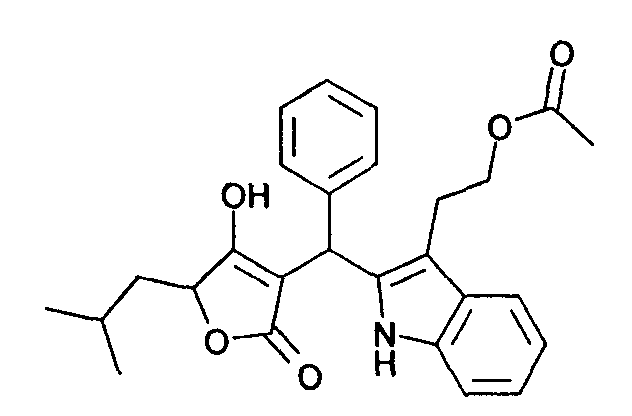
Используя общий метод В, 4-гидрокси-5-изобутил-5Н-фуран-2-он (литературная ссылка 14) вводят в реакцию с бензальдегидом и 2-(1Н-индол-3-ил)этанолом, получая названное в заголовке соединение в виде оранжевого твердого вещества. МС: 448,1 ([М+Н]+).
Пример 36: N-(2-{2-[(4-Гидрокси-2-оксо-1-окса-спиро[4.5]дец-3-ен-3-ил)фенилметил]-1Н-индол-3-ил}этил)ацетамид
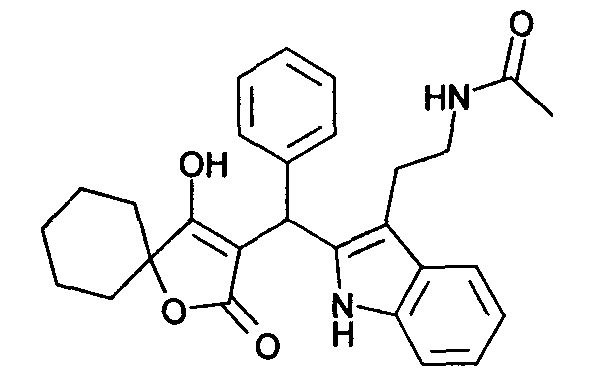
Используя общий метод В, 4-гидрокси-1-окса-спиро[4.5]дец-3-ен-2-он (литературная ссылка 15) вводят в реакцию с бензальдегидом и N-[2-(1Н-индол-3-ил)этил]ацетамидом, получая названное в заголовке соединение в виде белого твердого вещества. МС: 459,1 ([М+Н]+).
Пример 37: N-(2-{2-[(5-Циклогексилметил-4-гидрокси-2-оксо-2,5-дигидрофуран-3-ил)фенилметил]-6-фтор-1Н-индол-3-ил}этил)ацетамид
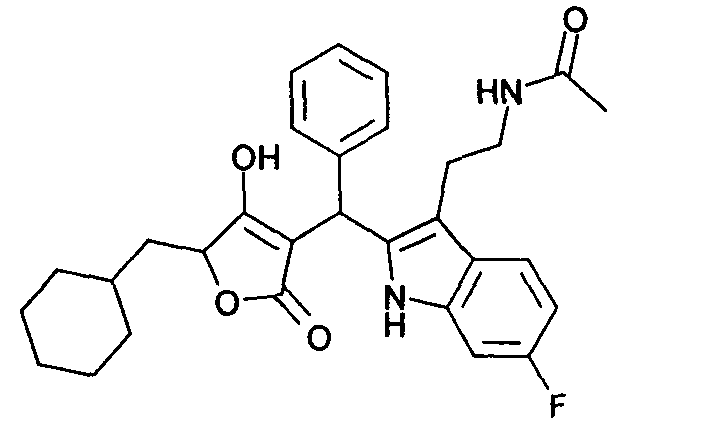
Используя общий метод В, 5-циклогексилметил-4-гидрокси-5Н-фуран-2-он (литературная ссылка 13) вводят в реакцию с бензальдегидом и N-[2-(6-фтор-1Н-индол-3-ил)этил]ацетамидом (пример 18.1), получая названное в заголовке соединение в виде светло-красного твердого вещества. МС: 503,0 ([М-Н]-).
Пример 38: N-[2-(2-{[5-(2-Циклогексилэтил)-4-гидрокси-2-оксо-2,5-дигидрофуран-3-ил]фенилметил}-6-фтор-1Н-индол-3-ил)этил]ацетамид
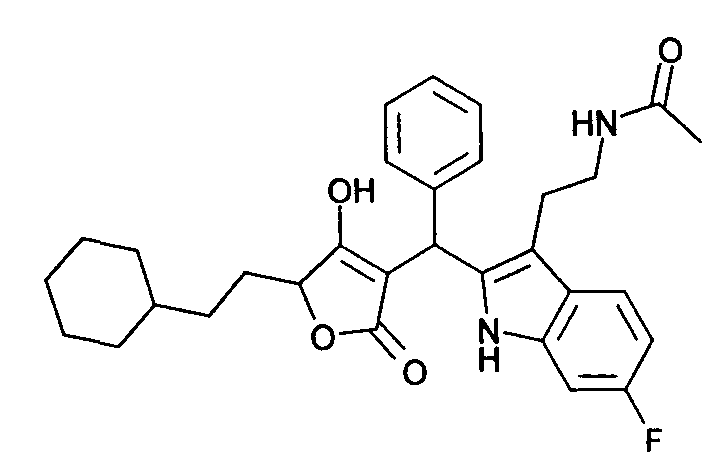
Используя общий метод В, 5-(2-циклогексилэтил)-4-гидрокси-5Н-фуран-2-он (пример Б2) вводят в реакцию с бензальдегидом и N-[2-(6-фтор-1Н-индол-3-ил)этил]ацетамидом (пример 18.1), получая названное в заголовке соединение в виде светло-зеленого твердого вещества. МС: 517,2 ([М-Н]-).
Пример 39: N-(2-{6-Фтор-2-[(4-гидрокси-2-оксо-5-фенэтил-2,5-дигидрофуран-3-ил)фенилметил]-1Н-индол-3-ил}этил)ацетамид
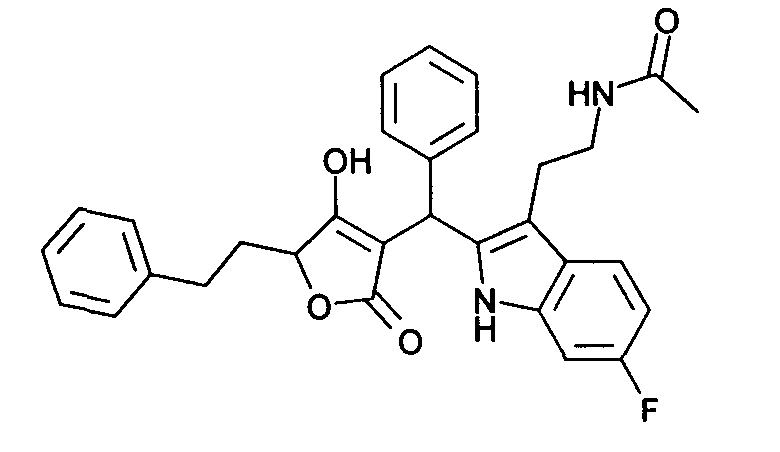
Используя общий метод В, 4-гидрокси-5-фенэтил-5Н-фуран-2-он (литературная ссылка 13) вводят в реакцию с бензальдегидом и N-[2-(6-фтор-1Н-индол-3-ил)этил]ацетамидом (пример 18.1), получая названное в заголовке соединение в виде светло-красного твердого вещества. МС: 511,1 ([М-Н]-).
Пример 40: N-[2-(6-Фтор-2-{[4-гидрокси-2-оксо-5-(3-фенилпропил)-2,5-дигидрофуран-3-ил]фенилметил}-1Н-индол-3-ил)этил]ацетамид
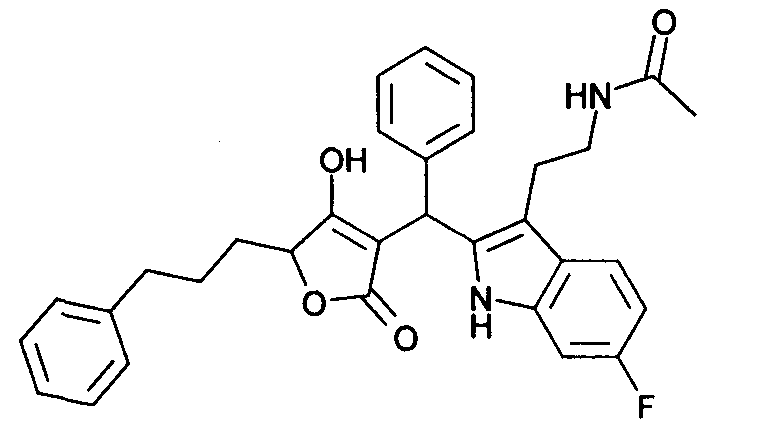
Используя общий метод В, 4-гидрокси-5-(3-фенилпропил)-5Н-фуран-2-он (литературная ссылка 13) вводят в реакцию с бензальдегидом и N-[2-(6-фтор-1Н-индол-3-ил)этил]ацетамидом (пример 18.1), получая названное в заголовке соединение в виде светло-красного твердого вещества. МС: 525,2 ([М-Н]-).
Пример 41: N-(2-{2-[(2-Гидрокси-5-оксоциклопент-1-енил)фенилметил]-1Н-индол-3-ил}этил)ацетамид
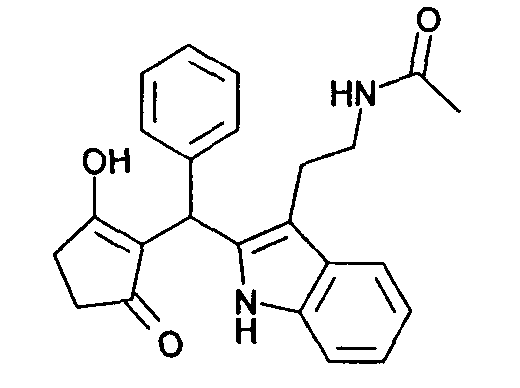
Используя общий метод В, 3-гидроксициклопент-2-енон (литературная ссылка 16) вводят в реакцию с бензальдегидом и N-[2-(1Н-индол-3-ил)этил]ацетамидом, получая названное в заголовке соединение в виде розового твердого вещества. МС: 387,4 ([М-Н]-).
Пример 42: N-(2-{2-[(2-Гидрокси-5-оксо-3-фенилциклопент-1-енил)фенилметил]-1Н-индол-3-ил}этил)ацетамид
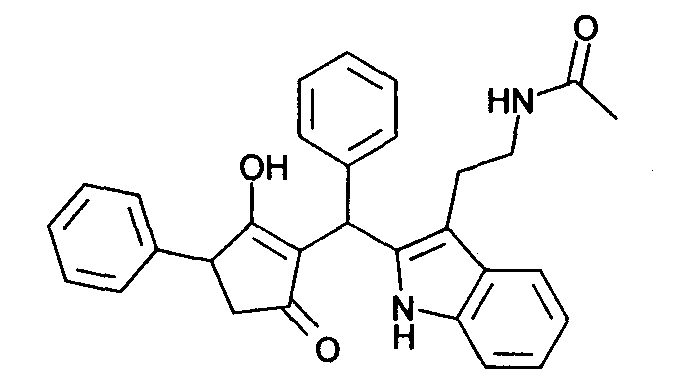
Используя общий метод В, 3-гидрокси-4-фенилциклопент-2-енон (литературная ссылка 17) вводят в реакцию с бензальдегидом и N-[2-(1Н-индол-3-ил)этил]ацетамидом, получая названное в заголовке соединение в виде розового твердого вещества. МС: 465,0 ([М+Н]+).
Пример 43: N-(2-{6-Фтор-2-[(2-гидрокси-5-оксо-3-фенилциклопент-1-енил)фенилметил]-1Н-индол-3-ил}этил)ацетамид
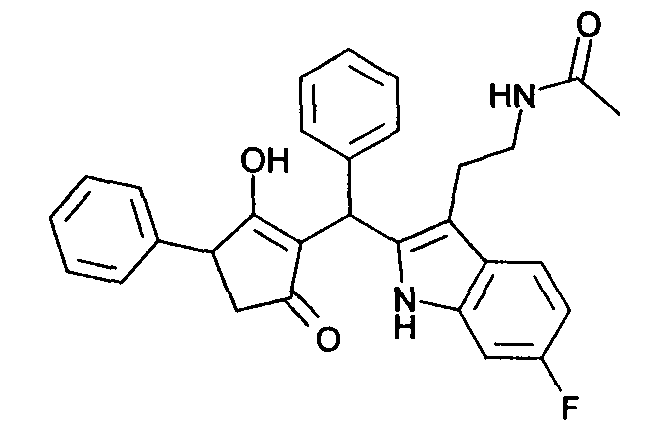
Используя общий метод В, 3-гидрокси-4-фенил-циклопент-2-енон (литературная ссылка 17) вводят в реакцию с бензальдегидом и N-[2-(6-фтор-1Н-индол-3-ил)этил]ацетамидом (пример 18.1), получая названное в заголовке соединение в виде розового твердого вещества. МС: 483,5 ([М+Н]+).
Пример 44: N-(2-{2-[(2-Гидрокси-5-оксо-3-фенилциклопент-1-енил)пиридин-2-ил-метил]-1Н-индол-3-ил}этил)ацетамид
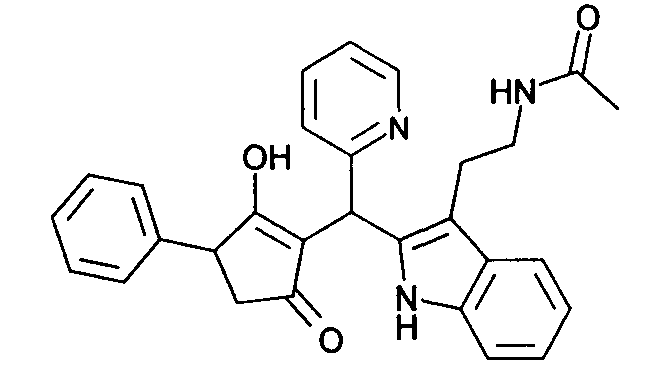
Используя общий метод В, 3-гидрокси-4-фенилциклопент-2-енон (литературная ссылка 17) вводят в реакцию с пиридин-2-карбальдегидом и N-[2-(1Н-индол-3-ил)этил]ацетамидом, получая названное в заголовке соединение в виде белого твердого вещества. МС: 466,3 ([М+Н]+).
Пример 45: N-(2-{2-[(2-Гидрокси-5-оксо-3-фенилциклопент-1-енил)пиридин-3-илметил]-1Н-индол-3-ил}этил)ацетамид
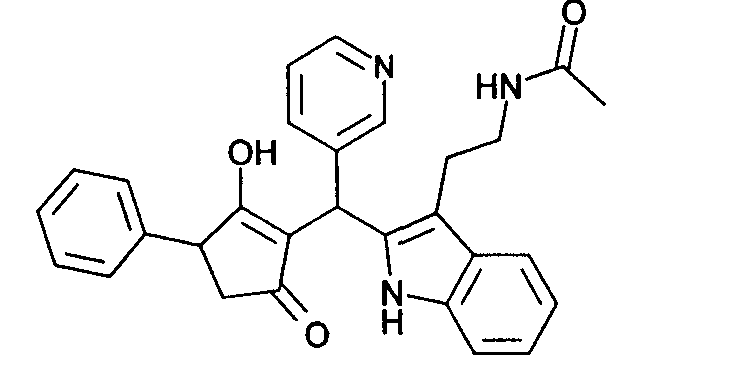
Используя общий метод В, 3-гидрокси-4-фенилциклопент-2-енон (литературная ссылка 17) вводят в реакцию с пиридин-2-карбальдегидом и N-[2-(1Н-индол-3-ил)этил]ацетамидом, получая названное в заголовке соединение в виде светло-коричневого твердого вещества. МС: 466,3 ([М+Н]+).
Пример 46: N-(2-{2-[(2-Гидрокси-5-оксо-3-фенилциклопент-1-енил)-(1Н-имидазол-4-ил)метил]-1Н-индол-3-ил}этил)ацетамид
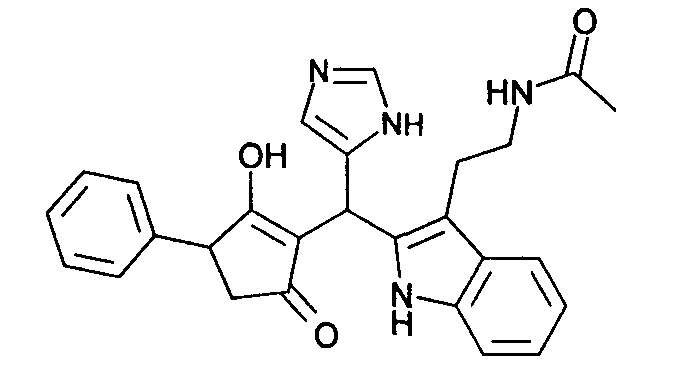
Используя общий метод В, 3-гидрокси-4-фенилциклопент-2-енон (литературная ссылка 17) вводят в реакцию с 3Н-имидазол-4-карбальдегидом и N-[2-(1Н-индол-3-ил)этил]ацетамидом, получая названное в заголовке соединение в виде светло-коричневого твердого вещества. МС: 455,0 ([М+Н]+).
Пример 47: N-(2-{2-[(2-Гидрокси-5-оксо-3-фенилциклопент-1-енил)-(1Н-имидазол-2-ил)метил]-1Н-индол-3-ил}этил)ацетамид
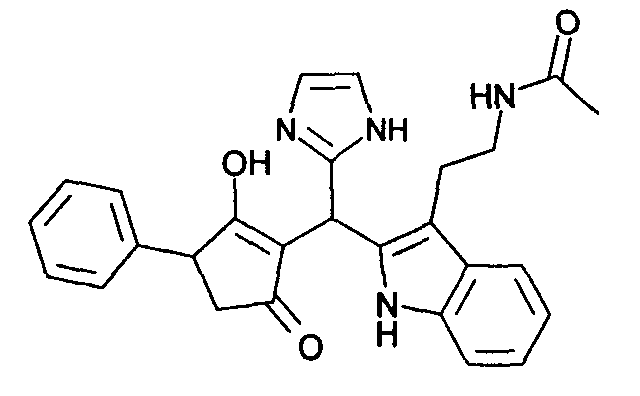
Используя общий метод В, 3-гидрокси-4-фенилциклопент-2-енон (литературная ссылка 17) вводят в реакцию с 1Н-имидазол-2-карбальдегидом и N-[2-(1Н-индол-3-ил)этил]ацетамидом, получая названное в заголовке соединение в виде светло-коричневого твердого вещества. МС: 455,0 ([М+Н]+).
Пример 48: N-(2-{5-Этил-2-[(2-гидрокси-5-оксо-3-фенилциклопент-1-енил)фенилметил]-1Н-индол-3-ил}этил)ацетамид
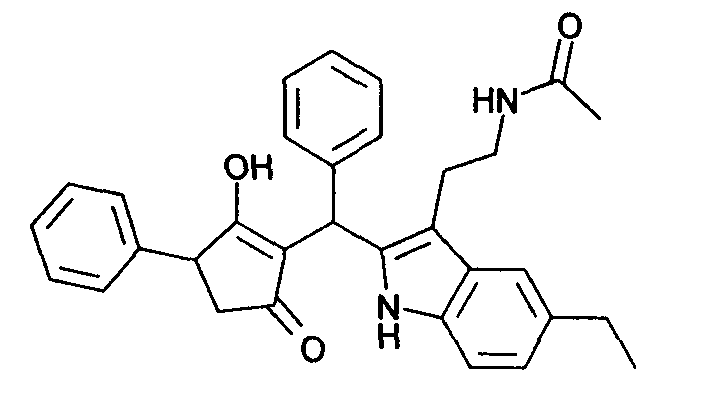
Используя общий метод В, 3-гидрокси-4-фенилциклопент-2-енон (литературная ссылка 17) вводят в реакцию с бензальдегидом и N-[2-(5-этил-1Н-индол-3-ил)этил]ацетамидом (литературная ссылка 6), получая названное в заголовке соединение в виде оранжевого твердого вещества. МС: 493,4 ([М+Н]+).
Пример 49: 2-{[3-(2-Аминоэтил)-5-метил-1Н-индол-2-ил]фенилметил}-3-гидрокси-4-фенилциклопент-2-енон
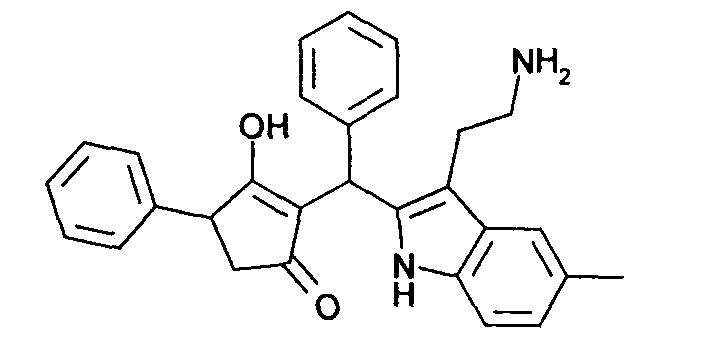
Используя общий метод В, 3-гидрокси-4-фенилциклопент-2-енон (литературная ссылка 17) вводят в реакцию с бензальдегидом и 2-(5-этил-1Н-индол-3-ил)этиламином, получая названное в заголовке соединение в виде оранжевого твердого вещества. МС: 437,1 ([М+Н]+).
Пример 50: N-(2-{2-[(2-Гидрокси-5-оксо-3-фенилциклопент-1-енил)фенилметил]-5-метил-1Н-индол-3-ил}этил)ацетамид
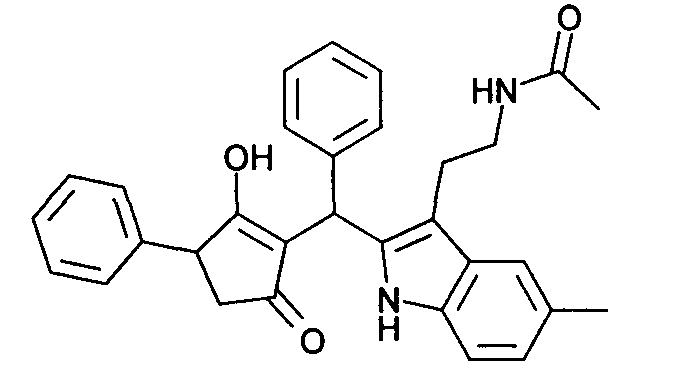
Используя общий метод В, 3-гидрокси-4-фенилциклопент-2-енон (литературная ссылка 17) вводят в реакцию с бензальдегидом и N-[2-(5-метил-1Н-индол-3-ил)этил]ацетамидом (литературная ссылка 7), получая названное в заголовке соединение в виде оранжевого твердого вещества. МС: 479,0 ([М+Н]+).
Пример 51: 2-{[3-(2-Аминоэтил)-6-этил-1Н-индол-2-ил]фенилметил}-3-гидрокси-4-фенилциклопент-2-енон
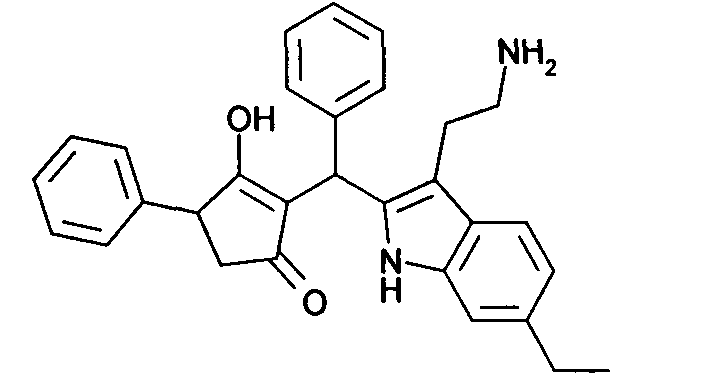
Используя общий метод В, 3-гидрокси-4-фенилциклопент-2-енон (литературная ссылка 17) вводят в реакцию с бензальдегидом и 2-(6-этил-1Н-индол-3-ил)этиламином (литературная ссылка 8), получая названное в заголовке соединение в виде светло-коричневого твердого вещества. МС: 451,0 ([М+Н]+).
Пример 52: N-(2-{6-Этил-2-[(2-гидрокси-5-оксо-3-фенилциклопент-1-енил)фенилметил]-1Н-индол-3-ил}этил)ацетамид
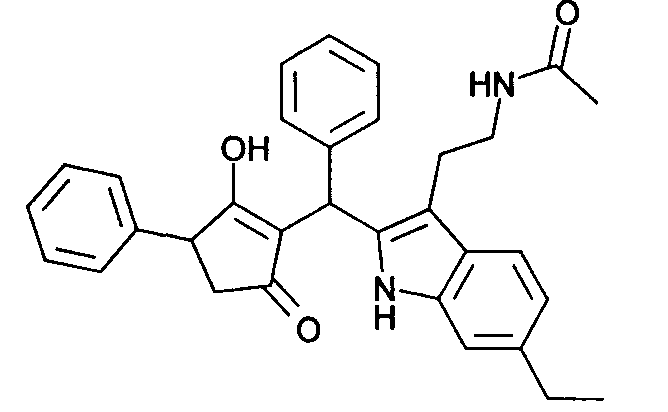
52. N-[2-(6-Этил-1Н-индол-3-ил)этил]ацетамид получают из 2-(6-этил-1Н-индол-3-ил)этиламина (литературная ссылка 8), как описано в примере 16.1.
52.2. Используя общий метод В, 3-гидрокси-4-фенилциклопент-2-енон (литературная ссылка 17) вводят в реакцию с бензальдегидом и Н-[2-(6-этил-1Н-индол-3-ил)этил]ацетамидом, получая N-(2-{6-этил-2-[(2-гидрокси-5-оксо-3-фенилциклопент-1-енил)фенилметил]-1Н-индол-3-ил}этил)ацетамид в виде светло-коричневого твердого вещества. МС: 493,1 ([М+Н]+).
Пример 53: 2-{[3-(2-Амино-2-метилпропил)-6-хлор-1Н-индол-2-ил]фенилметил}-3-гидрокси-4-фенилциклопент-2-енон
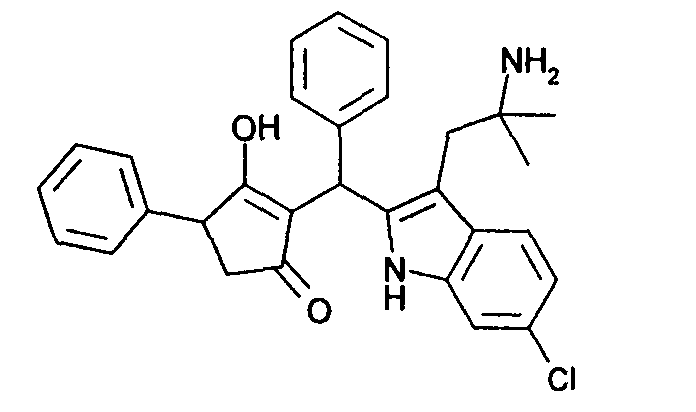
Используя общий метод В, 3-гидрокси-4-фенилциклопент-2-енон (литературная ссылка 17) вводят в реакцию с бензальдегидом и 2-(6-хлор-1Н-индол-3-ил)-1,1-диметилэтиламином (синтезирован аналогично методу, приведенному в литературной ссылке 9), получая названное в заголовке соединение в виде светло-желтого твердого вещества. МС: 485,4 ([М+Н]+).
Пример 54: N-(2-{6-Хлор-2-)(2-гидрокси-5-оксо-3-фенилциклопент-1-енил)фенилметил]-1Н-индол-3-ил}-1,1-диметилэтил)ацетамид
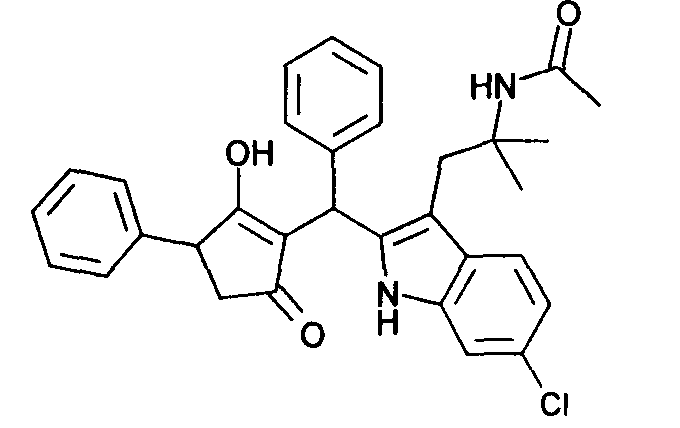
54.1. N-[2-(6-хлор-1Н-индол-3-ил)-1,1-диметилэтил]ацетамид получен из 2-(6-хлор-1Н-индол-3-ил)-1,1-диметилэтиламина (синтезирован аналогично методу, приведенному в литературной ссылке 9) посредством ацилирования, как описано в примере 16.1.
54.2. Используя общий метод В, 3-гидрокси-4-фенилциклопент-2-енон (литературная ссылка 17) вводят в реакцию с бензальдегидом и N-[2-(6-хлор-1H-индол-3-ил)-1,1-диметилэтил]ацетамидом, получая N-(2-{6-хлор-2-[(2-гидрокси-5-оксо-3-фенилциклопент-1-енил)фенилметил]-1Н-индол-3-ил}-1,1-диметилэтил)ацетамид в виде светло-желтого твердого вещества. МС: 527,3 ([М+Н]+).
Пример 55: N-(2-{6-Хлор-2-[(2-гидрокси-5-оксо-3-фенилциклопент-1-енил)фенилметил]-5-метокси-1Н-индол-3-ил}этил)ацетамид
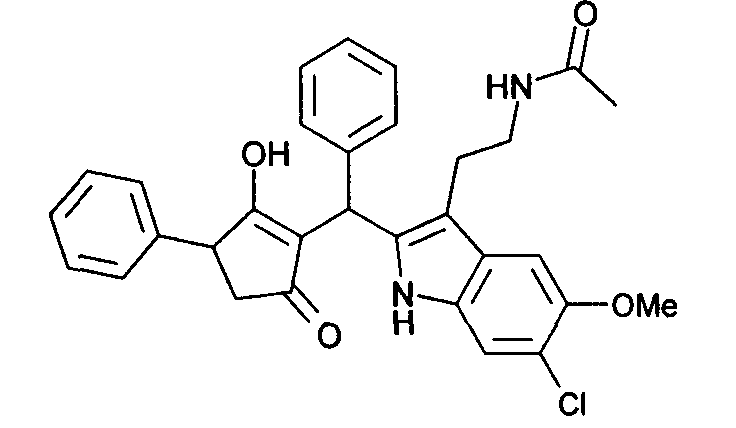
Используя общий метод В, 3-гидрокси-4-фенилциклопент-2-енон (литературная ссылка 17) вводят в реакцию с бензальдегидом и N-[2-(6-[хлор-5-метокси-1Н-индол-3-ил)этил]ацетамидом, получая названное в заголовке соединение в виде светло-красного твердого вещества. МС: 529,3 ([М+Н]+).
Пример 56: N-(2-{2-[(2-Гидрокси-5-оксо-3-фенилциклопент-1-енил)фенилметил]-6-метокси-1Н-индол-3-ил}этил)ацетамид
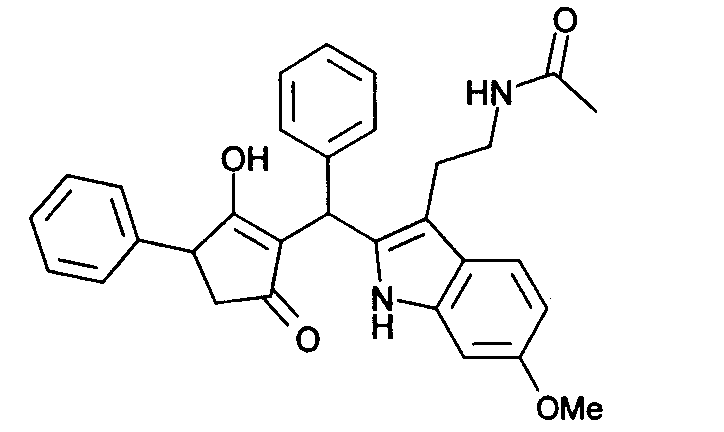
Используя общий метод В, 3-гидрокси-4-фенилциклопент-2-енон (литературная ссылка 17) вводят в реакцию с бензальдегидом и N-[2-(6-метокси-1Н-индол-3-ил)этил]ацетамидом (литературная ссылка 7), получая названное в заголовке соединение в виде светло-красного твердого вещества. МС: 495,5 ([М+Н]+).
Пример 57: N-(2-{2-[(2-Гидрокси-5-оксо-3-фенилциклопент-1-енил)фенилметил]-5-метокси-1Н-индол-3-ил}этил)ацетамид
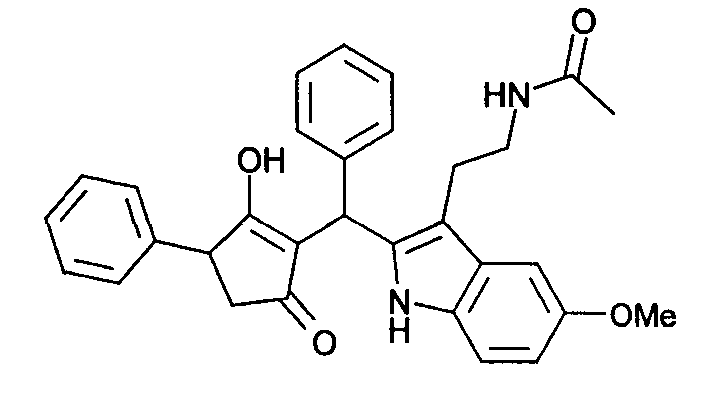
Используя общий метод В, 3-гидрокси-4-фенилциклопент-2-енон (литературная ссылка 17) вводят в реакцию с бензальдегидом и N-[2-(5-метокси-1Н-индол-3-ил)этил]ацетамидом, получая названное в заголовке соединение в виде светло-красного твердого вещества. МС: 495,4 ([М+Н]+).
Пример 58: 3-{[6-Фтор-3-(2-гидроксиэтил)-1Н-индол-2-ил]фенилметил}-4-гидрокси-5-изопропил-1,5-дигидропиррол-2-он
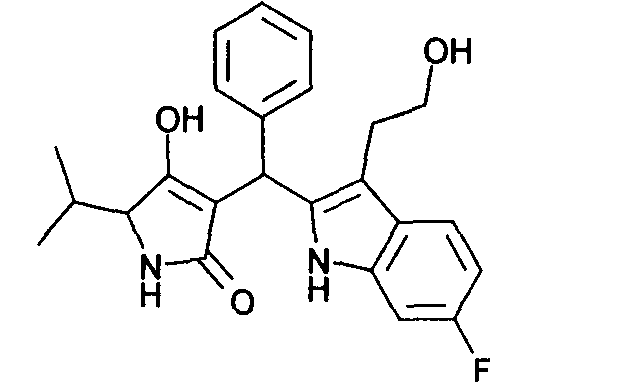
Используя общий метод Г, рац-4-гидрокси-5-изопропил-1,5-дигидропиррол-2-он (литературная ссылка 11) вводят в реакцию с бензальдегидом и 2-(6-фтор-1Н-индол-3-ил)этанолом, получая названное в заголовке соединение в виде светло-желтого твердого вещества. МС: 409,1 ([М+Н]+).
Пример 59: 2-[(5-Фтор-3-метил-1Н-индол-2-ил)фенилметил]-1-гидрокси-7а-метил-5,6,7,7а-тетрагидропирролизин-3-он
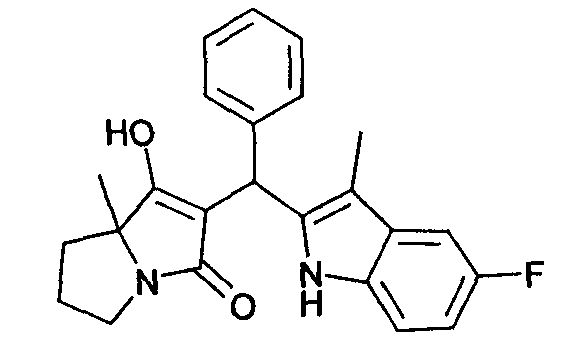
Используя общий метод Г, рац-1-гидрокси-7а-метил-5,6,7,7а-тетрагидропирролизин-3-он (пример В) вводят в реакцию с бензальдегидом и 5-фтор-3-метил-1H-индолом, получая названное в заголовке соединение в виде красного твердого вещества. МС: 391,1 ([М+Н]+).
Пример 60: 3-[(5-Фтор-3-метил-1Н-индол-2-ил)фенилметил]-4-гидрокси-5,5-диметил-1,5-дигидропиррол-2-он
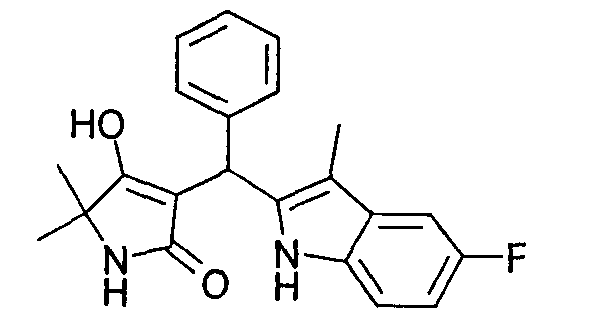
Используя общий метод Г, рац-4-гидрокси-5,5-диметил-1,5-дигидропиррол-2-он (литературная ссылка 18) вводят в реакцию с бензальдегидом и 5-фтор-3-метил-1Н-индолом, получая названное в заголовке соединение в виде желтого твердого вещества. МС: 365,1 ([М+Н]+).
Пример 61: (R)-5-Бензил-3-[(5-фтор-3-метил-1Н-индол-2-ил)фенилметил]-4-гидрокси-5-метил-1,5-дигидропиррол-2-он
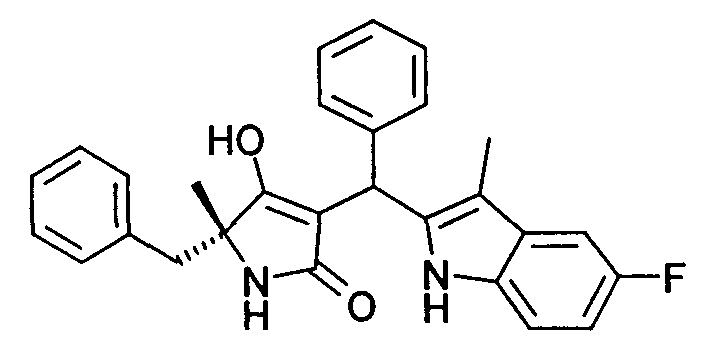
Используя общий метод Г, (R)-5-бензил-4-гидрокси-5-метил-1,5-дигидропиррол-2-он (пример Г) вводят в реакцию с бензальдегидом и 5-фтор-3-метил-1H-индолом, получая названное в заголовке соединение в виде желтого твердого вещества. МС: 441,1 ([М+Н]+).
Пример 62: (R)-3-[(5-Фтор-3-метил-1Н-индол-2-ил)фенилметил]-4-гидрокси-5-изопропил-5-метил-1,5-дигидропиррол-2-он
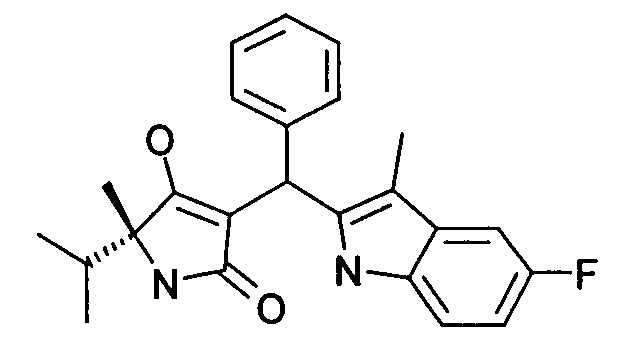
Используя общий метод Г, (R)-4-гидрокси-5-изопропил-5-метил-1,5-дигидропиррол-2-он (пример Д) вводят в реакцию с бензальдегидом и 5-фтор-3-метил-1H-индолом, получая названное в заголовке соединение в виде светло-желтого твердого вещества. МС: 393,1 ([М+Н]+).
Пример 63: N-{2-[((R)-4-Гидрокси-5-метил-2-оксо-5-фенил-2,5-дигидро-1Н-пиррол-3-ил)фенилметил]-6-метил-1Н-индол-3-илметил}ацетамид
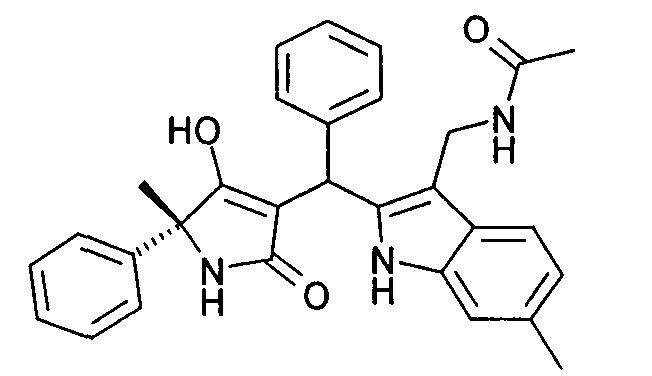
63.1 Оксим 6-метил-1Н-индол-3-карбальдегида
К раствору 6-метил-1H-индол-3-карбальдегида (0,96 г, литературная ссылка 20) в этаноле (30 мл) добавляют при температуре 22°С гидрохлорид гидроксиламина (0,46 г) и ацетат натрия (0,54 г), после чего смесь перемешивают в течение 3 ч. Затем смесь выпаривают, остаток тритурируют с водой и смесью дихлорметан/н-гептан (в соотношении 1:1) и высушивают, получая названное в заголовке соединение (выход 0,96 г) в виде розового твердого вещества. МС: 175,3 ([М+Н]+).
63.2 С-(6-Метил-1Н-индол-3-ил)метиламин
К смеси оксима 6-метил-1H-индол-3-карбальдегида (0,66 г) и NiCl2·6Н2О (0,97 г) в метаноле (60 мл) добавляют отдельными порциями при температуре 22°С борогидрид натрия (3,04 г). Суспензию фильтруют и фильтрат выпаривают. Остаток распределяют между водным раствором NH3 (1%-ный) и этилацетатом, органический слой высушивают и выпаривают, получая сырое названное в заголовке соединение в виде желтого полутвердого вещества (0,68 г).
63.3 Н-(6-Метил-1Н-индол-3-илметил)ацетамид
К раствору С-(6-метил-1Н-индол-3-ил)метиламина (0,24 г) в дихлорметане (4 мл) добавляют уксусный ангидрид (0,14 мл) и пиридин (0,13 мл) и перемешивают при температуре 22°С в течение 20 мин. Смесь промывают водным раствором HCl (1-нормальный), органический слой высушивают и выпаривают. Остаток хроматографируют на силикагеле, используя смесь дихлорметан/метанол (в соотношении 70:1) и получая названное в заголовке соединение в виде бесцветной пены (0,15 г). МС: 203,1 ([М+Н]+).
63.4 Используя общий метод Г, (R)-4-гидрокси-5-метил-5-фенил-1,5-дигидропиррол-2-он (пример Е) вводят в реакцию с бензальдегидом и N-(6-метил-1Н-индол-3-илметил)ацетамидом, получая названное в заголовке соединение в виде белого твердого вещества. МС: 478,4 ([M-Н]-).
Пример 64: (R)-4-Гидрокси-5-метил-3-[(3-метил-1Н-индол-2-ил)фенилметил]-5-фенил-1,5-дигидропиррол-2-он
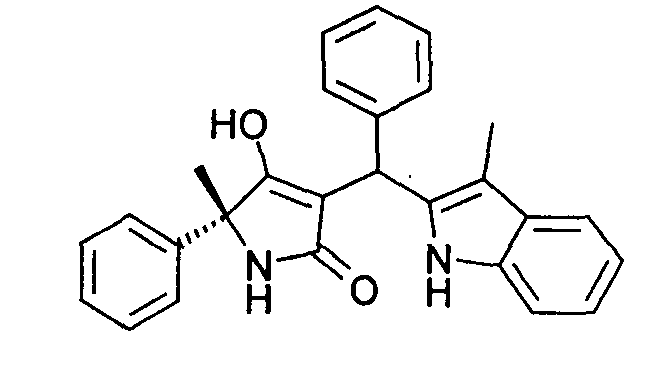
Используя общий метод Г, (R)-4-гидрокси-5-метил-5-фенил-1,5-дигидропиррол-2-он (синтезирован аналогично методу, приведенному в литературной ссылке 11, а также в литературной ссылке 19) вводят в реакцию с бензальдегидом и 3-метил-1H-индолом, получая названное в заголовке соединение в виде желтой пены. МС: 409,2 ([М+Н]+).
Пример 65: (R)-3-[(3,5-Диметил-1Н-индол-2-ил)фенилметил1-4-гидрокси-5-метил-5-фенил-1,5-дигидропиррол-2-он
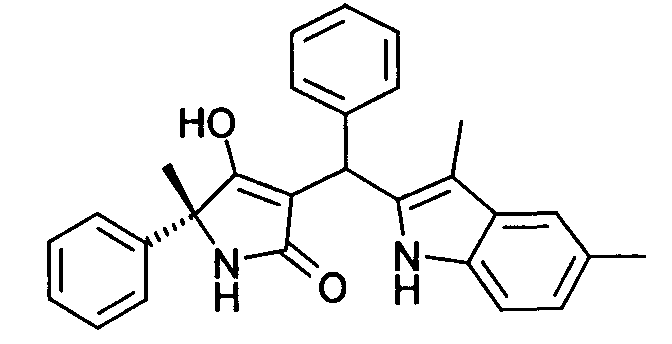
Используя общий метод Г, (R)-4-гидрокси-5-метил-5-фенил-1,5-дигидропиррол-2-он (синтезирован аналогично методу, приведенному в литературной ссылке 11, а также в литературной ссылке 19) вводят в реакцию с бензальдегидом и 3,5-диметил-1Н-индолом (литературная ссылка 21), получая названное в заголовке соединение в виде желтой пены. МС: 423,3 ([М+Н]+).
Пример 66: (R)-3-[(3,6-Диметил-1Н-индол-2-ил)фенилметил]-4-гидрокси-5-метил-5-фенил-1,5-дигидропиррол-2-он
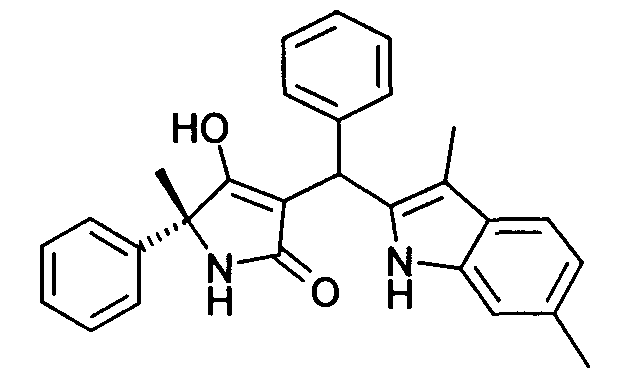
Используя общий метод Г, (R)-4-гидрокси-5-метил-5-фенил-1,5-дигидропиррол-2-он (синтезирован аналогично методу, приведенному в литературной ссылке 11, а также в литературной ссылке 19) вводят в реакцию с бензальдегидом и 3,6-диметил-1Н-индолом (литературная ссылка 22), получая названное в заголовке соединение в виде желтой пены. МС: 423,3 ([М+Н]+).
Пример 67: (R)-3-[(5-Фтор-3-метил-1Н-индол-2-ил)фенилметил]-4-гидрокси-5-метил-5-фенил-1,5-дигидропиррол-2-он
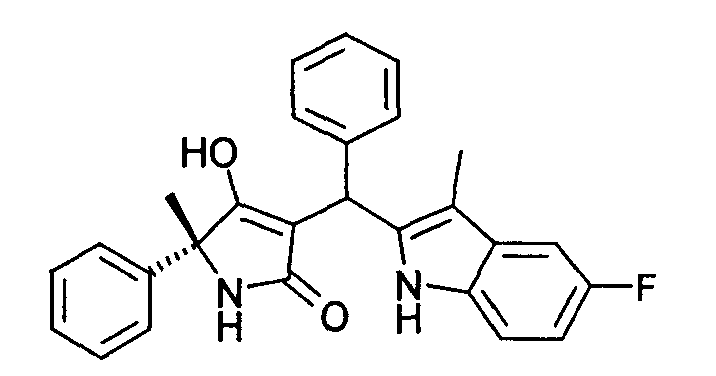
Используя общий метод Г, (R)-4-гидрокси-5-метил-5-фенил-1,5-дигидропиррол-2-он (синтезирован аналогично методу, приведенному в литературной ссылке 11, а также в литературной ссылке 19) вводят в реакцию с бензальдегидом и 5-фтор-3-метил-1Н-индолом, получая названное в заголовке соединение в виде светло-желтой пены. МС: 425,4 ([М-Н]-).
Пример 68: 5-Бензил-3-[(5-фтор-3-метил-1Н-индол-2-ил)тиофен-2-илметил]-4-гидрокси-5Н-фуран-2-он
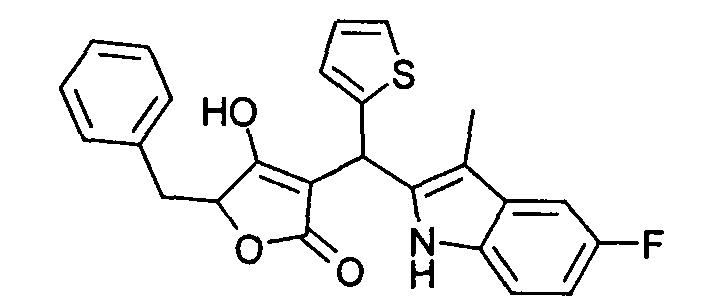
Используя общий метод Г, рац-5-бензил-4-гидрокси-5Н-фуран-2-он (литературная ссылка 13) вводят в реакцию с тиофен-2-карбальдегидом и 5-фтор-3-метил-1H-индолом, получая названное в заголовке соединение в виде красного твердого вещества. МС: 434,3 ([М+Н]+).
Пример 69: 5-Бензил-3-[(5-фтор-3-метил-1Н-индол-2-ил)тиофен-3-илметил]-4-гидрокси-5Н-фуран-2-он
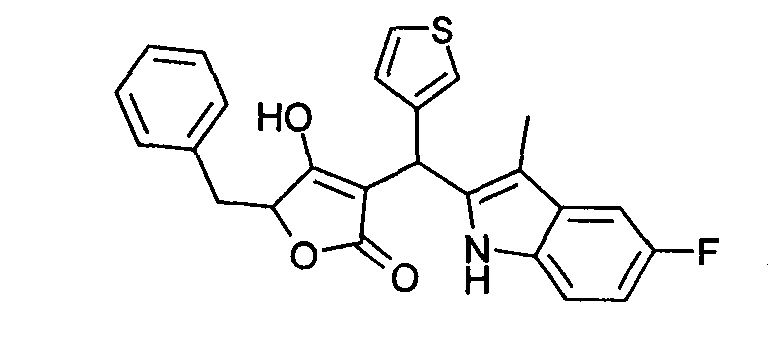
Используя общий метод Г, рац-5-бензил-4-гидрокси-5Н-фуран-2-он (литературная ссылка 13) вводят в реакцию с тиофен-3-карбальдегидом и 5-фтор-3-метил-1H-индолом, получая названное в заголовке соединение в виде бесцветного твердого вещества. МС: 434,3 ([М+Н]+).
Пример 70: N-(2-{6-Хлор-2-[(4-гидрокси-5-метил-2-оксо-5-фенил-2,5-дигидрофуран-3-ил)фенилметил]-1Н-индол-3-ил}-1,1-диметилэтил)ацетамид
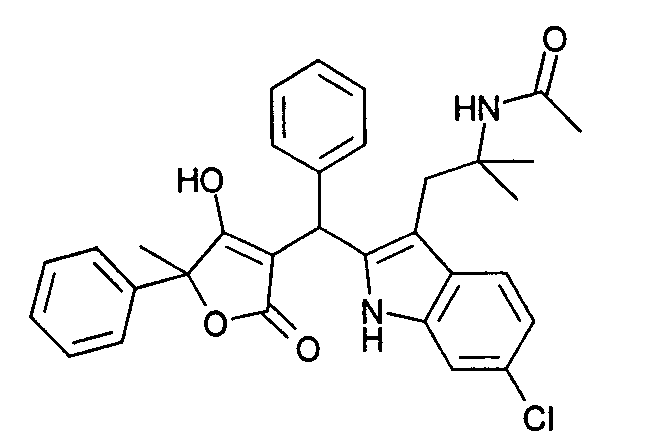
70.1. N-[2-(6-Хлор-1Н-индол-3-ил)-1,1-диметилэтил]ацетамид
2-(6-Хлор-1Н-индол-3-ил)-1,1-диметилэтиламин (синтезированный аналогично методу, приведенному в литературной ссылке 9) ацилируют, как описано в примере 63.3, получая названное в заголовке соединение в виде коричневого полутвердого вещества.
70.2. Используя общий метод Г, рац-4-гидрокси-5-метил-5-фенил-5Н-фуран-2-он (синтезированный согласно примеру A3) вводят в реакцию с бензальдегидом и N-[2-(6-хлор-1Н-индол-3-ил)-1,1-диметилэтил]ацетамидом, получая названное в заголовке соединение в виде светло-коричневого твердого вещества. МС: 543,3 ([М+Н]+).
Пример 71: N-(2-{5-Хлор-2-[(4-гидрокси-5-метил-2-оксо-5-фенил-2,5-дигидрофуран-3-ил)фенилметил]-1Н-индол-3-ил}-1,1-диметилэтил)ацетамид
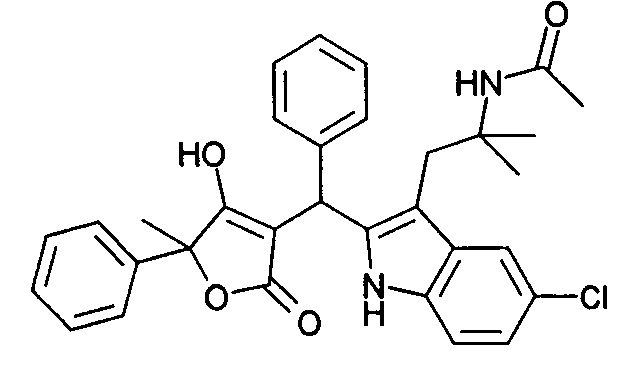
71.1. N-[2-(5-[Хлор-1Н-индол-3-ил)-1,1-диметилэтил]ацетамид
2-(5-Хлор-1Н-индол-3-ил)-1,1-диметилэтиламин (литературная ссылка 23) ацилируют, как описано в примере 63.3, получая названное в заголовке соединение в виде бесцветного твердого вещества. МС: 263,1 ([М-Н]-).
71.2. Используя общий метод Г, рац-4-гидрокси-5-метил-5-фенил-5Н-фуран-2-он (синтезированный согласно примеру A3) вводят в реакцию с бензальдегидом и N-[2-(5-хлор-1Н-индол-3-ил)-1,1-диметилэтил]ацетамидом, получая названное в заголовке соединение в виде светло-коричневого твердого вещества. МС: 543,3 ([M+H]+).
Пример 72: N-{2-[((R)-4-Гидрокси-5-метил-2-оксо-5-фенил-2,5-дигидрофуран-3-ил)фенилметил]-6-метил-1Н-индол-3-илметил}ацетамид
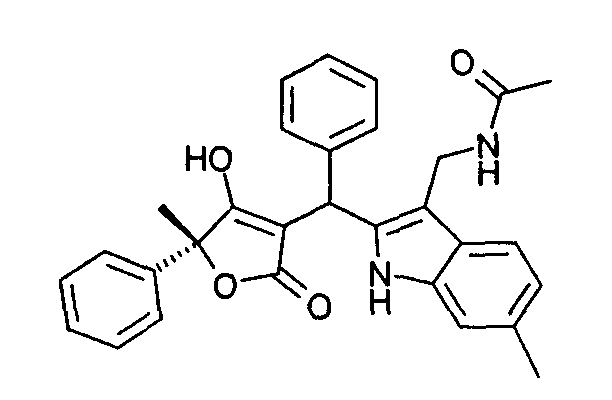
Используя общий метод Г, (R)-4-гидрокси-5-метил-5-фенил-1,5-дигидропиррол-2-он (пример А4) вводят в реакцию с бензальдегидом и N-(6-метил-1Н-индол-3-илметил)ацетамидом (из примера 63.3), получая названное в заголовке соединение в виде желтого твердого вещества. МС: 479,4 ([М-Н]-).
Пример 73: N-{2-[((8)-4-Гидрокси-5-метил-2-оксо-5-фенил-2,5-дигидрофуран-3-ил)фенилметил]-6-метил-1Н-индол-3-илметил}ацетамид
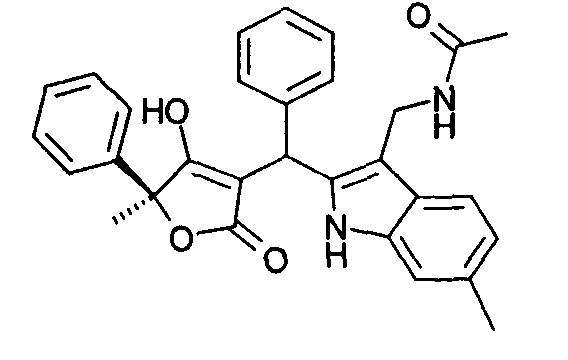
Используя общий метод Г, (S)-4-гидрокси-5-метил-5-фенил-1,5-дигидропиррол-2-он (пример A3) вводят в реакцию с бензальдегидом и N-(6-метил-1Н-индол-3-илметил)ацетамидом (из примера 63.3), получая названное в заголовке соединение в виде желтого твердого вещества. МС: 479,4 ([М-Н]-).
Пример 74: (R)-4-Гидрокси-5-метил-3-[(3-метил-1Н-индол-2-ил)фенилметил]-5-фенил-5Н-фуран-2-он
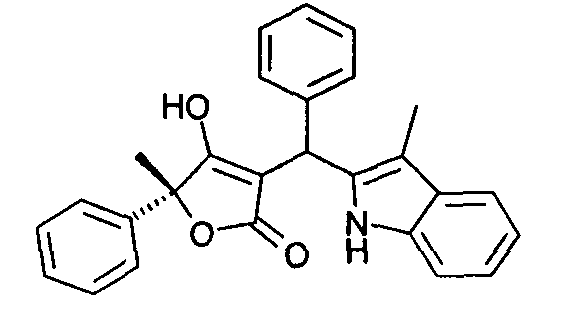
Используя общий метод Г, (R)-4-гидрокси-5-метил-5-фенил-1,5-дигидропиррол-2-он (пример А4) вводят в реакцию с бензальдегидом и 3-метил-1Н-индолом, получая названное в заголовке соединение в виде желтого твердого вещества.
МС: 408,4 ([М-Н]-).
Пример 75: (R)-3-[(3,5-Диметил-1Н-индол-2-ил)фенилметил]-4-гидрокси-5-метил-5-фенил-5Н-фуран-2-он
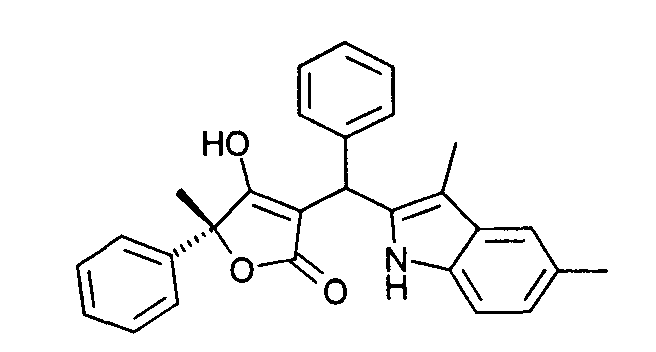
Используя общий метод Г, (R)-4-гидрокси-5-метил-5-фенил-1,5-дигидропиррол-2-он (пример А4) вводят в реакцию с бензальдегидом и 3,5-диметил-1Н-индолом (литературная ссылка 21), получая названное в заголовке соединение в виде светло-коричневого твердого вещества. МС: 422,5 ([М-Н]-).
Пример 76: (R)-3-[(3,6-Диметил-1Н-индол-2-ил)фенилметил]-4-гидоокси-5-метил-5-фенил-5Н-фуран-2-он
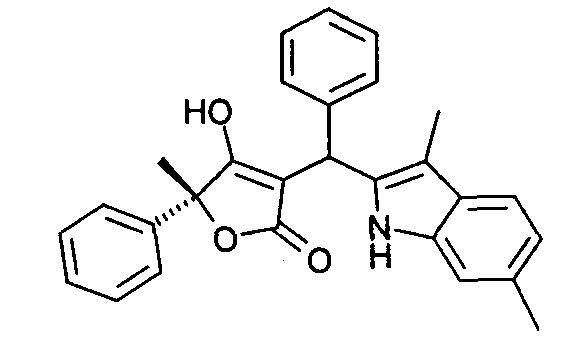
Используя общий метод Г, (R)-4-гидрокси-5-метил-5-фенил-1,5-дигидропиррол-2-он (пример А4) вводят в реакцию с бензальдегидом и 3,6-диметил-1H-индолом (литературная ссылка 22), получая названное в заголовке соединение в виде светло- коричневого твердого вещества. МС: 422,4 ([М-Н]-).
Пример 77: (R)-3-[(5-Фтор-3-метил-1Н-индол-2-ил)фенилметил]-4-гидрокси-5-метил-5-фенил-5Н-фуран-2-он
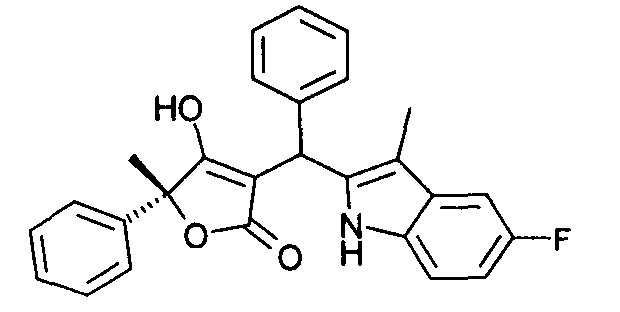
Используя общий метод Г, (R)-4-гидрокси-5-метил-5-фенил-1,5-дигидропиррол-2-он (пример А4) вводят в реакцию с бензальдегидом и 5-фтор-3-метил-1H-индолом, получая названное в заголовке соединение в виде желтого твердого вещества. МС: 426,1 ([М-Н]-).
Пример 78: 3-Гидрокси-2-[(3-метил-1Н-индол-2-ил)фенилметил]-4-фенилциклопент-2-енон
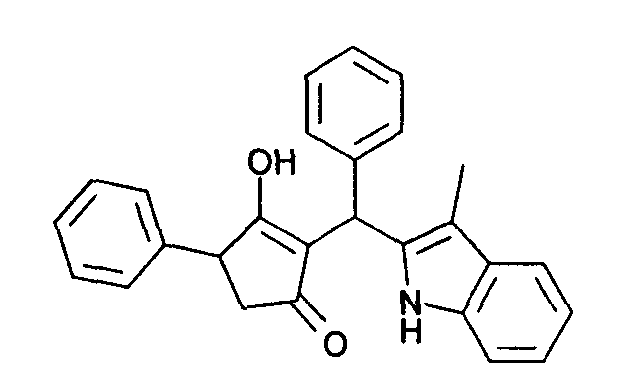
Используя общий метод Г, рац-3-гидрокси-4-фенилциклопент-2-енон (литературная ссылка 17) вводят в реакцию с бензальдегидом и 3-метил-1Н-индолом, получая названное в заголовке соединение в виде красного твердого вещества. МС: 394,1 ([М+Н]+).
Пример 79: 2-[(5-Фтор-3-метил-1Н-индол-2-ил)фенилметил]-3-гидрокси-4-фенилциклопент-2-енон
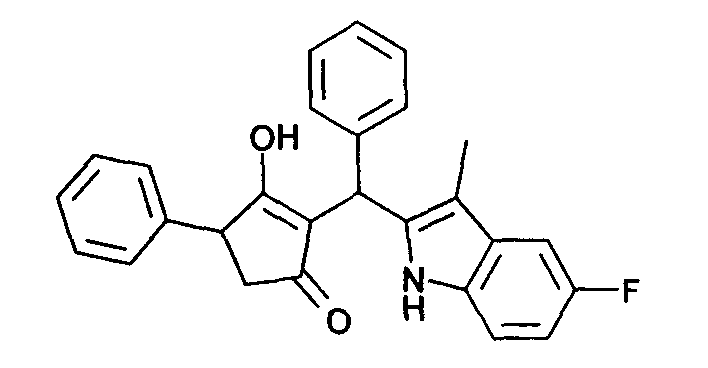
Используя общий метод Г, рац-3-гидрокси-4-фенил-циклопент-2-енон (литературная ссылка 17) вводят в реакцию с бензальдегидом и 5-фтор-3-метил-1H-индолом, получая названное в заголовке соединение в виде красного твердого вещества. МС: 412,0 ([М+Н]+).
Пример А
Покрытые оболочкой таблетки, содержащие следующие ингредиенты, могут быть получены стандартным методом:
Активный ингредиент просеивают и смешивают с микрокристаллической целлюлозой, после чего смесь гранулируют с помощью раствора поливинилпирролидона в воде. Гранулят смешивают с натрий крахмал гликолятом и стеаратом магния и запрессовывают, получая ядра массой 120 или 350 мг соответственно. Ядра лакируют с помощью водного раствора/суспензии выше названной пленочной оболочки.
Пример Б
Капсулы, содержащие следующие ингредиенты, могут быть получены стандартным методом:
Компоненты просеивают, смешивают и этой смесью заполняют капсулы размером 2.
Пример В
Инъекционные растворы имеют следующий состав:
Активный ингредиент растворяют в смеси полиэтиленгликоля 400 с водой для инъекций (используя часть). Значение рН доводят до 5,0 с помощью уксусной кислоты. Объем доводят до 1,0 мл добавлением оставшегося количества воды. Раствор фильтруют, заполняют им пузырьки соответствующего объема и стерилизуют.
Пример Г
Мягкие желатиновые капсулы, содержащие следующие ингредиенты, могут быть получены стандартным методом:
Активный ингредиент растворяют в теплом расплаве других ингредиентов, полученной смесью заполняют мягкие желатиновые капсулы соответствующего размера. Заполненные мягкие желатиновые капсулы обрабатывают согласно обычным процедурам.
Пример Д
Облатки, содержащие следующие ингредиенты, могут быть получены стандартным методом:
Активный ингредиент смешивают с лактозой, микрокристаллической целлюлозой и натрийкарбоксиметилцеллюлозой, после чего смесь гранулируют со смесью поливинилпирролидона в воде. Гранулят смешивают со стеаратом магния и вкусовыми добавками и заполнят смесью облатки.
| название | год | авторы | номер документа |
|---|---|---|---|
| ВИНИЛОГИЧЕСКИЕ ПРОИЗВОДНЫЕ КИСЛОТ КАК ИНГИБИТОРЫ ХИМАЗЫ | 2007 |
|
RU2451013C2 |
| ПРОИЗВОДНЫЕ СПИРООКСИНДОЛА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ТЕРАПЕВТИЧЕСКИХ АГЕНТОВ | 2006 |
|
RU2415143C2 |
| (3-ЦИКЛОАЛКИЛ-2,3,4,5-ТЕТРАГИДРО-1Н-БЕНЗО[d]АЗЕПИН-7-ИЛОКСИ)ПРОИЗВОДНЫЕ, ИХ ПРИМЕНЕНИЕ ДЛЯ ИНГИБИРОВАНИЯ Н3 РЕЦЕПТОРОВ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ПОЛУЧЕНИЯ | 2003 |
|
RU2388752C2 |
| ПРОИЗВОДНЫЕ 2-ИМИНОПИРРОЛИДИНА | 2002 |
|
RU2270192C2 |
| ОКСАЗОЛИДИНОНОВЫЕ ПРОИЗВОДНЫЕ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ НА ИХ ОСНОВЕ | 1998 |
|
RU2215740C2 |
| ПРОИЗВОДНЫЕ 2-АМИНОПИРИДИНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБ ЛЕЧЕНИЯ | 2001 |
|
RU2250898C2 |
| ЗАМЕЩЕННЫЕ ПИРАЗОЛОПИРИМИДИНЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЛЕКАРСТВЕННОГО СРЕДСТВА | 2007 |
|
RU2450004C2 |
| ФАРМАЦЕВТИЧЕСКИЕ СОЕДИНЕНИЯ | 2019 |
|
RU2821941C2 |
| СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЕ ДЛЯ СНИЖЕНИЯ АКТИВНОСТИ ГОРМОН-ЧУВСТВИТЕЛЬНОЙ ЛИПАЗЫ | 2002 |
|
RU2317981C2 |
| ПИРРОЛОПИРАЗИНОВЫЕ ИНГИБИТОРЫ КИНАЗЫ | 2009 |
|
RU2503676C2 |
Изобретение относится к новым соединениям формулы (I)
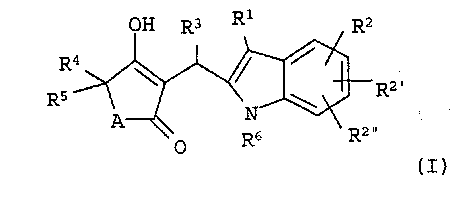 где А обозначает -СН2-, -О- или -NR′-, в котором R′ обозначает водород или C1-6алкил или R′ и R4 образуют С2-5алкилен; R1 обозначает водород, аминогруппу, C1-6алкил, гидроксигруппу, -NR′R′′, (С0-6алкилен)-NR′R′′, где R′ и R′′ независимо выбраны из группы, включающей водород, С1-6алкил, гетероалкил, формил, C1-6алкилкарбонил, арилкарбонил, необязательно замещенный галогеналкилом, C1-6алкилсульфонил, арилсульфонил или -(С0-6алкилен)-OR′, где R′ обозначает водород, C1-6алкил, формил или C1-6алкилкарбонил; R2, R2′ и R2′′ независимо обозначают водород, галоген, C1-6алкил или С1-6алкоксигруппу; R3 обозначает водород, C1-6алкил, арил-С1-6алкил, арил, необязательно замещенный галогеном, или гетероарил, где "гетероарил" означает моноциклическое или бициклическое кольцо, содержащее 5-6 кольцевых атомов, и по крайней мере одно ароматическое кольцо, содержащее один, два или три кольцевых гетероатома, выбранных из N, О и S, при этом оставшиеся кольцевые атомы являются атомами углерода, а точка присоединения гетероарильного радикала должна находиться на ароматическом кольце; R4 обозначает водород, С1-6алкил, арил, С3-7циклоалкил-С1-6алкил, арил-С1-6алкил; R5 обозначает водород или C1-6алкил; или R4 и R5 вместе с атомом углерода, к которому они присоединены, образуют необязательно замещенное С3-7циклоалкильное кольцо; R6 обозначает водород или С1-6алкил; и их фармацевтически приемлемые соли; где термин "арил" означает фенил или нафтил. Кроме того, изобретение относится к фармацевтической композиции на основе соединений формулы I и обладающей ингибирующей активностью в отношении химазы. Технический результат: получены и описаны новые соединения, которые ингибируют химазу и могут быть применены в качестве лекарственных средств. 2 н. и 20 з.п. ф-лы, 1 табл.
где А обозначает -СН2-, -О- или -NR′-, в котором R′ обозначает водород или C1-6алкил или R′ и R4 образуют С2-5алкилен; R1 обозначает водород, аминогруппу, C1-6алкил, гидроксигруппу, -NR′R′′, (С0-6алкилен)-NR′R′′, где R′ и R′′ независимо выбраны из группы, включающей водород, С1-6алкил, гетероалкил, формил, C1-6алкилкарбонил, арилкарбонил, необязательно замещенный галогеналкилом, C1-6алкилсульфонил, арилсульфонил или -(С0-6алкилен)-OR′, где R′ обозначает водород, C1-6алкил, формил или C1-6алкилкарбонил; R2, R2′ и R2′′ независимо обозначают водород, галоген, C1-6алкил или С1-6алкоксигруппу; R3 обозначает водород, C1-6алкил, арил-С1-6алкил, арил, необязательно замещенный галогеном, или гетероарил, где "гетероарил" означает моноциклическое или бициклическое кольцо, содержащее 5-6 кольцевых атомов, и по крайней мере одно ароматическое кольцо, содержащее один, два или три кольцевых гетероатома, выбранных из N, О и S, при этом оставшиеся кольцевые атомы являются атомами углерода, а точка присоединения гетероарильного радикала должна находиться на ароматическом кольце; R4 обозначает водород, С1-6алкил, арил, С3-7циклоалкил-С1-6алкил, арил-С1-6алкил; R5 обозначает водород или C1-6алкил; или R4 и R5 вместе с атомом углерода, к которому они присоединены, образуют необязательно замещенное С3-7циклоалкильное кольцо; R6 обозначает водород или С1-6алкил; и их фармацевтически приемлемые соли; где термин "арил" означает фенил или нафтил. Кроме того, изобретение относится к фармацевтической композиции на основе соединений формулы I и обладающей ингибирующей активностью в отношении химазы. Технический результат: получены и описаны новые соединения, которые ингибируют химазу и могут быть применены в качестве лекарственных средств. 2 н. и 20 з.п. ф-лы, 1 табл.
1. Соединения формулы (I)
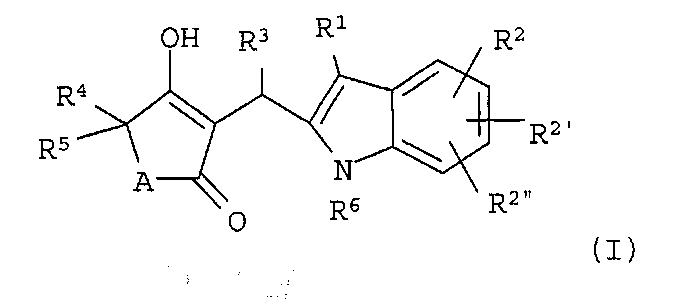
где А обозначает -СН2-, -О- или -NR′-, в котором R′ обозначает водород или C1-6алкил, или R′ и R4 образуют С2-5алкилен;
R1 обозначает водород, аминогруппу, С1-6алкил, гидроксигруппу, -NR′R′′, (C0-6алкилен)-NR′R′′, где R′ и R′′ независимо выбраны из группы, включающей водород, C1-6алкил, гетероалкил, формил, С1-6алкилкарбонил, арилкарбонил необязательно замещенный галогеналкилом, C1-6алкилсульфонил, арилсульфонил или -(С0-6алкилен)-OR′, где R′ обозначает водород, С1-6алкил, формил или С1-6алкилкарбонил;
R2, R2′ и R2′′ независимо обозначают водород, галоген, С1-6алкил или С1-6алкоксигруппу;
R3 обозначает водород, С1-6алкил, арил-С1-6алкил, арил необязательно замещенный галогеном, или гетероарил, где гетероарил означает моноциклическое или бициклическое кольцо, содержащее 5-6 кольцевых атомов, и по крайней мере одно ароматическое кольцо, содержащее один, два или три кольцевых гетероатома, выбранных из N, О и S, при этом оставшиеся кольцевые атомы являются атомами углерода, а точка присоединения гетероарильного радикала должна находиться на ароматическом кольце;
R4 обозначает водород, С1-6алкил, арил, С3-7циклоалкил-С1-6алкил, арил-С1-6алкил;
R5 обозначает водород или С1-6алкил; или
R4 и R5 вместе с атомом углерода, к которому они присоединены, образуют необязательно замещенное С3-7циклоалкильное кольцо;
R6 обозначает водород или С1-6алкил;
и их фармацевтически приемлемые соли;
где термин "арил" означает фенил или нафтил.
2. Соединения по п.1, где R3 обозначает С1-6алкил, арил, необязательно замещенный галогеном, гетероарил, арил-С1-6алкил.
3. Соединения по одному из пп.1 и 2, где R3 обозначает С1-6алкил; фенил-С1-6алкил; фенил, необязательно замещенный от одного до трех атомами фтора; или гетероарил, где гетероарил обозначает моноциклический ароматический радикал с 5 или 6 кольцевыми атомами, содержащий один или два кольцевых атома азота или один кольцевой атом серы.
4. Соединения по одному из пп.1 и 2, где R3 обозначает фенил.
5. Соединения по одному из пп.1 и 2, где R1 обозначает С1-6алкил, -(С0-6алкилен)-NR′R′′, где R′ и R′′ независимо выбраны из группы, включающей водород, C1-6алкилкарбонил, необязательно замещенный галогеналкилом арилкарбонил, арилсульфонил или -(С0-6алкилен)-OR′, где R′ обозначает водород или С1-6алкилкарбонил.
6. Соединения по одному из пп.1 и 2, где R1 обозначает С1-6алкил, -(С2-6алкилен)-NR′R′′, где R′ и R′′ независимо выбраны из группы, включающей водород, ацетил, арилкарбонил, необязательно замещенный одной или двумя перфторметильными группами, и арилсульфонил, или -(С2-6алкилен)-OR′, где R′ обозначает водород или ацетил.
7. Соединения по одному из пп.1 и 2, где R1 обозначает 2-аминоэтил, 2-ацетиламиноэтил, 2-ацетиламино-2,2-диметилэтил, метил, изопропил или 2-гидроксиэтил.
8. Соединения по одному из пп.1 и 2, где два из R2, R2′ и R2′′ обозначают водород, а третий обозначает водород, галоген, С1-6алкил или С1-6алкоксигруппу.
9. Соединения по одному из пп.1 и 2, где два из R2, R2′ и R2′′ обозначают водород, а третий обозначает водород, хлор, фтор, метил, этил или метоксигруппу.
10. Соединения по одному из пп.1 и 2, где два из R2, R2′ и R2′′ обозначают водород, а третий находится в 5 или 6 положении индольного кольца и выбран из группы, включающей водород, хлор, фтор, метил и этил.
11. Соединения по одному из пп.1 и 2, где R6 обозначает водород.
12. Соединения по одному из пп.1 и 2, где А обозначает -СН2-.
13. Соединения по одному из пп.1 и 2, где А обозначает -СН2-, R4 обозначает фенил и R5 обозначает водород.
14. Соединения по одному из пп.1 и 2, где А обозначает -NR′-, где R′ обозначает водород или С1-6алкил.
15. Соединения по одному из пп.1 и 2, где А обозначает -NR′-, где R′ обозначает водород или метил, R4 обозначает изопропил и R5 обозначает водород.
16. Соединения по одному из пп.1 и 2, где А обозначает -О-.
17. Соединения по одному из пп.1 и 2, где А обозначает -О-, R4 обозначает водород, фенил, С1-6алкил, С3-7циклоалкил-С1-6алкил или арил-С1-6алкил, и R5 обозначает водород или С1-6алкил; или R4 и R5 вместе с атомом углерода, к которому они присоединены, образуют необязательно замещенное С3-7циклоалкильное кольцо.
18. Соединения по одному из пп.1 и 2, где А обозначает -О-, R4 обозначает фенил, бензил, изобутил, 2-циклогексилэтил или фенэтил и R5 обозначает водород или метил.
19. Соединения по п.1, выбранные из группы, включающей
3-[(5-фтор-3-метил-1Н-индол-2-ил)фенилметил]-4-гидрокси-5-изопропил-1,5-дигидропиррол-2-он,
3-[(5-фтор-3-метил-1Н-индол-2-ил)фенилметил]-4-гидрокси-5-изопропил-1-метил-1,5-дигидропиррол-2-он,
4-гидрокси-5-изопропил-3-[(3-метил-1Н-индол-2-ил)фенилметил]-1,5-дигидропиррол-2-он,
3-[(5-фтор-3-изопропил-1H-индол-2-ил)фенилметил]-4-гидрокси-5-изопропил-1,5-дигидропиррол-2-он,
N-(2-{2-[(5-бензил-4-гидрокси-2-оксо-2,5-дигидрофуран-3-ил)фенилметил]-6-фтор-1Н-индол-3-ил}этил)ацетамид,
5-бензил-3-{[6-фтор-3-(2-гидроксиэтил)-1Н-индол-2-ил]фенилметил}-4-гидрокси-5Н-фуран-2-он,
3-{[3-(2-аминоэтил)-6-фтор-1H-индол-2-ил]фенилметил}-5-бензил-4-гидрокси-5Н-фуран-2-он; соль с уксусной кислотой,
5-бензил-3-[(5-фтор-3-метил-1Н-индол-2-ил)фенилметил]-4-гидрокси-5Н-фуран-2-он,
(2-{6-фтор-2-[(4-гидрокси-5-метил-2-оксо-5-фенил-2,5-дигидрофуран-3-ил)фенилметил]индол-3-ил}этил)ацетамид,
(2-{2-[(4-гидрокси-5-изобутил-2-оксо-2,5-дигидрофуран-3-ил)фенилметил]индол-3-ил}этил)ацетамид,
N-[2-(2-{[5-(2-циклогексилэтил)-4-гидрокси-2-оксо-2,5-дигидрофуран-3-ил]фенилметил}-6-фтор-1Н-индол-3-ил)этил]ацетамид,
N-(2-{6-фтор-2-[(4-гидрокси-2-оксо-5-фенэтил-2,5-дигидрофуран-3-ил)фенилметил]-1Н-индол-3-ил}этил)ацетамид,
N-(2-{2-[(2-гидрокси-5-оксо-3-фенилциклопент-1-енил)фенилметил]-1Н-индол-3-ил} этил)ацетамид,
N-(2-{6-фтор-2-[(2-гидрокси-5-оксо-3-фенилциклопент-1-енил)фенилметил]-1Н-индол-3-ил}этил)ацетамид,
N-(2-{5-этил-2-[(2-гидрокси-5-оксо-3-фенилциклопент-1-енил)фенилметил]-1Н-индол-3-ил}этил)ацетамид,
N-(2-{2-[(2-гидрокси-5-оксо-3-фенилциклопент-1-енил)фенилметил]-5-метил-1H-индол-3-ил}этил)ацетамид,
2-{[3-(2-аминоэтил)-6-этил-1Н-индол-2-ил]фенилметил}-3-гидрокси-4-фенилциклопент-2-енон или
N-(2-{6-хлор-2-[(2-гидрокси-5-оксо-3-фенилциклопент-1-енил)фенилметил]-1Н-индол-3-ил}-1,1-диметилэтил)ацетамид.
20. Фармацевтическая композиция, обладающая ингибирующей активностью в отношении химазы, включающая соединение по одному из пп.1-19 и фармацевтически приемлемый наполнитель.
21. Соединения по одному из пп.1 и 2, обладающие ингибирующей активностью в отношении химазы.
22. Соединения по одному из пп.1 и 2 для применения в качестве терапевтически активных веществ для лечения и/или профилактики аллергических, воспалительных или фиброзных заболеваний.
| ЕР 1284266 А1, 19.02.2003 | |||
| ЕР 1136488 А1, 26.09.2001 | |||
| TANI MASATO et al | |||
| КОПИРОВАЛЬНЫЙ СТАНОК ДЛЯ ДЕРЕВА | 1925 |
|
SU2809A1 |
| Structural elucidation | |||
| Journal of antibiotics, 57(2), p.89-96, 2004 | |||
| TANI MASATO et al | |||
| КОПИРОВАЛЬНЫЙ СТАНОК ДЛЯ ДЕРЕВА | 1925 |
|
SU2809A1 |
| Taxonomy, fermentation, isolation and | |||
Авторы
Даты
2011-08-10—Публикация
2006-11-22—Подача