ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
По настоящей заявке испрашивается приоритет и преимущество по предварительной заявке на патент США № 60/670573, поданной 11 апреля 2005, описание которой включено в настоящее описание в качестве ссылки.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к генетически модифицированным белкам с уриколитическим действием. Конкретнее, данное изобретение относится к белкам, содержащим укороченную уратоксидазу, и способам их получения.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ДАННОГО ИЗОБРЕТЕНИЯ
Термины уратоксидаза и уриказа используются в настоящем описании взаимозаменяемо. Уратоксидазы (уриказы; E.C. 1.7.3.3) представляют собой ферменты, которые катализируют окисление мочевой кислоты до более растворимого продукта, аллантоина, пуринового метаболита, который легче экскретируется. В организме человека не вырабатывается ферментативно активная уриказа в результате нескольких мутаций в гене урокиназы, приобретенных во время эволюции высших приматов. Wu, X, et al., (1992) J MoI Evol 34:78-84 в полном объеме включено в настоящее описание в качестве ссылки. Вследствие этого у предрасположенных индивидуумов избыточные концентрации мочевой кислоты в крови (гиперурикемия) могут привести к тяжелому артриту (подагра), обезображивающим отложения солей мочевой кислоты (подагрический узел) и почечной недостаточности. У некоторых пораженных индивидуумов доступные лекарственные средства, такие как аллопуринол (ингибитор синтеза мочевой кислоты), вызывают побочные эффекты, ограничивающие лечение, или не облегчают эти состояния в достаточной мере. Hande, KR, et al., (1984) Am J Med 76: 47-56; Fam, AG, (1990) Bailliere's Clin Rheumatol 4: 177-192 каждый включен в настоящее описание в качестве ссылки в полном объеме. Инъекции уриказы могут снизить гиперурикемию и гиперурикозурию, по меньшей мере, временно. Поскольку уриказа является чужеродным белком для человека, даже первая инъекция неизмененного белка, выделенного из Aspergillus flavus, вызывала анафилактические реакции у некоторого процента получавших лечение пациентов (Pui, C-H, et al., (1997) Leukemia 11: 1813-1816 включена в настоящее описание в качестве ссылки в полном объеме), и иммунологические реакции ограничивают его применение для постоянного или периодического лечения. Donadio, D, et al., (1981) Nouv Presse Med 10: 711-712; Leaustic, M, et al., (1983) Rev Rhum Mal Osteoartic 50: 553-554 каждая включена в настоящее описание в качестве ссылки в полном объеме.
Субоптимальный режим доступных схем лечения гиперурикемии принят в течение нескольких десятилетий. Kissel, P, et al., (1968) Nature 217: 72-74 включена в настоящее описание в качестве ссылки в полном объеме. Подобным образом, возможность того, что некоторым группам пациентов с тяжелой подагрой может быть полезна безопасная и эффективная форма инъецируемой уриказы, признана в течение многих лет. Davis, FF, et al., (1978) in GB Broun, et al., (Eds.) Enzyme Engineering, Vol. 4 (pp. 169-173) New York, Plenum Press; Nishimura, H, et al., (1979) Enzyme 24: 261-264; Nishimura, H, et al., (1981) Enzyme 26: 49-53; Davis, S, et al., (1981) Lancet 2(8241): 281-283; Abuchowski, A, et al., (1981) J Pharmacol Exp Ther 219: 352-354; Chen, RH-L, et al., (1981) Biochim Biophys Acta 660: 293-298; Chua, CC, et al., (1988) Ann Int Med 109: 114-117; Greenberg, ML, et al., (1989) Anal Biochem 176: 290-293, каждая включена в настоящее описание в качестве ссылки в полном объеме. Уриказы, полученные из органов животных, являются практически нерастворимыми в растворителях, которые соответствуют безопасному введению посредством инъекции. Патент США № 3616231 включен в настоящее описание в качестве ссылки в полном объеме. Некоторые уриказы, полученные из растений или микроорганизмов, являются более растворимыми в приемлемых с медицинской точки зрения растворителях. Тем не менее, инъекция микробных ферментов быстро вызывает иммунологические реакции, которые могут привести к опасным для жизни аллергическим реакциям или к инактивированию и/или ускорению клиренса уриказы из кровообращения. Donadio, et al., (1981); Leaustic, et al., (1983). Ферменты, основанные на установленных аминокислотных последовательностях уриказ млекопитающих, в том числе свиньи и бабуина, или насекомых, например Drosophila melanogaster или Drosophila pseudoobscura (Wallrath, LL, et al., (1990) Mol Cell Biol 10: 5114-5127 включены в настоящее описание в качестве ссылки в полном объеме), не являются подходящими кандидатами для клинического применения по причине иммуногенности и нерастворимости при физиологическом рН.
Ранее исследователи использовали инъецируемую уриказу для катализа перехода мочевой кислоты в аллантоин in vivo. См. Pui, et al., (1997). Это лежит в основе применения во Франции и Италии уриказы, полученной из грибка Aspergillus flavus (Uricozyme®) для профилактики или временной коррекции гиперурикемии, связанной с цитотоксической терапией гематологических злокачественных новообразований и для временного уменьшения тяжелой гиперурикемии у больных подагрой. Potaux, L, et al., (1975) Nouv Presse Med 4: 1109-1112; Legoux, R, et al., (1992) J Biol Chem 267: 8565-8570; Патенты США №№ 5382518 и 5541098 каждый включен в настоящее описание в качестве ссылки в полном объеме. По причине его короткого времени жизни в кровотоке необходимы ежедневные инъекции Uricozyme®. Более того, этот препарат не подходит для длительного применения по причине его иммуногенности.
Некоторые уриказы используются для получения конъюгатов с полиэтиленкликолем или полиэтиленоксидом (оба обозначены как PEG) для создания терапевтически эффективных форм уриказы, обладающих увеличенным временем полужизни белка и сниженной иммуногенностью. Патенты США 4179337, 4766106, 4847325 и 6576235; публикация патентной заявки США US2003/0082786A1 каждый включен в настоящее описание в качестве ссылки в полном объеме. Конъюгаты уриказы с полимерами, отличными от PEG, также описаны. Патент США 4460683 включен в настоящее описание в качестве ссылки в полном объеме.
Практически во всех описанных попытках пегилирования уриказы (то есть ковалентного связывания PEG с уриказой), PEG присоединен, прежде всего, к аминогруппам, в том числе к аминоконцевому остатку и доступным остаткам лизина. В обычно используемых уриказах общее число лизинов в каждой из четырех идентичных субъединиц находится между 25 (Aspergillus flavus (Патент США 5382518 включен в настоящее описание в качестве ссылки в полном объеме)) и 29 (свинья (Wu, X, et al., (1989) Proc Natl Acad Sci USA 86: 9412-9416 включена в настоящее описание в качестве ссылки в полном объеме)). Некоторые лизины недоступны для пегилирования в нативной конформации фермента. Наиболее распространенный подход к снижению иммуногенности уриказы состоит в соединении большого числа цепей низкомолекулярного PEG. Это всегда приводило к значительному снижению ферментативной активности полученных конъюгатов.
Однократное внутривенное введение препарата уриказы Candida utilis, соединенной с 5 кДа PEG, снижало содержание урата в сыворотке крови до неопределяемых уровней у пяти обследованных человек, у которых средняя концентрация урата в сыворотке до инъекции составляет 6,2 мг/дл, что находится в пределе нормы. Davis, et al., (1981). Этим пяти пациентам вводили дополнительную инъекцию четыре недели спустя, но об их реакциях на нее не сообщалось. Используя относительно нечувствительный метод диффузии в геле, не было выявлено антител к уриказе после второй (и последней) инъекции. В этом источнике не сообщается о результатах хронического и подострого лечения больных людей или экспериментальных животных.
Препарат уриказы, выделенной из Arthrobacter protoformiae, соединенной с 5 кДа PEG, применяли для временного контроля гиперурикемии у одного больного с лимфомой, у которого концентрация урата в сыворотке крови до введения препарата, составляла 15 мг/дл. Chua, et al., (1988). Вследствие критического состояния данного пациента и короткой продолжительности лечения (четыре инъекции в течение 14 дней) невозможно оценить долговременную эффективность и безопасность данного конъюгата.
Улучшенная защита от иммунологического распознавания возможна посредством модификации каждой субъединицы уриказы с помощью 2-10 цепей высокомолекулярного PEG (>5 кД-120 кД) Saifer, et al., (патент США 6576235; (1994) Adv Exp Med Biol 366: 377-387 каждая включена в настоящее описание посредством ссылки в полном объеме). Этот подход делает возможным задержку >75% ферментативной активности уриказы, выделенной из различных биологических видов, после пегилирования, увеличивает время нахождения уриказы в кровотоке и делает возможным повторные инъекции фермента без выявления антител у мышей и кроликов.
Hershfield and Kelly (международная патентная публикация WO 00/08196; заявка США № 60/095489, включенные в настоящее описание в качестве ссылке в полном объеме) разработали средства для обеспечения рекомбинантных белков уриказы, выделенных из организмов разных видов млекопитающих, с оптимальным числом участков пегилирования. Они использовали методы ПЦР для увеличения числа доступных остатков лизина в выбранных участках фермента, что предназначено для уменьшения распознавания иммунной системой, после последующего пегилирования, существенно сохраняя уриколитическое действие фермента. Некоторые из их уриказных белков укорочены на карбокси- и/или аминоконцах. Они не обеспечивают введения других специфических генетически-опосредованных изменений в белке.
В данной заявке термин «иммуногенность» относится к индукции иммунной реакции посредством введения PEG-модифицированной ПЭГ или немодифицированной уриказы (антиген), тогда как термин «антигенность» относится к реакции антигена с предсуществующими антителами. Совместно, антигенность и иммуногенность называются «иммунореактивность». В предыдущих исследованиях PEG-уриказы иммунореактивность оценивали с помощью различных способов, в том числе: 1) реакция in vitro PEG-уриказы с предварительно сформированными антителами; 2) определение индуцированного синтеза антител; и 3) увеличенные иммунные клиренсы после повторных инъекций.
Предыдущие попытки устранения иммуногенности уриказ, выделенных из нескольких источников посредством соединения различного числа цепей PEG с помощью различных линкеров, имели ограниченный успех. Впервые PEG-уриказы были раскрыты FF Davis и Y Inada и их коллегами. Davis, et al., (1978); Патент США 4179337; Nishimura, et al., (1979); Патенты Японии 55-99189 и 62-55079, включенные в настоящее описание посредством ссылки в полном объеме. Конъюгат, раскрытый в патенте США 4179337, синтезирован в результате реакции уриказы произвольного происхождения с 2000-кратным молярным избытком PEG 750 дальтон, означая, что большое число молекул полимера вероятно присоединено к каждой субъединице уриказы. В патенте США 4179337 раскрыто соединение либо PEG, либо поли(пропиленгликоля) с молекулярным весом от 500 до 20000 дальтон, предпочтительно приблизительно от 500 до 5000 дальтон, для обеспечения активных, растворимых в воде, неиммуногенных конъюгатов различных полипептидных гормонов и ферментов, в том числе оксидоредуктаз, среди которых уриказа является одним из трех примеров. Кроме того, в патенте США 4179337 подчеркивается соединение от 10 до 100 цепей полимера на молекулу фермента и задержка, по меньшей мере, 40% ферментативной активности. Не опубликовано никаких результатов относительно степени связывания PEG с доступными аминогруппами уриказы, остаточного специфического уриколитического действия или иммунореактивности конъюгата.
В предшествующих публикациях значительное снижение уриколитической активности, измеренное in vitro, было вызвано соединением различного числа цепей PEG с уриказой, выделенной из Candida utilis. Соединение большого числа цепей PEG 5 кДа с уриказой печени свиньи приводило к подобным результатам, что описано и в публикации Chen, и в докладе этой же научной группы на научной конференции. Chen, et al., (1981); Davis, et al., (1978).
В семи предшествующих исследованиях сообщалось, что иммунореактивность уриказы снижена в результате пегилирования и была устранена в пяти других исследованиях. В трех из последних пяти исследований устранение иммунореактивности связано с основательным снижением уриколитической активности - самое большее до 15%, 28%, или 45% от первоначальной активности. Nishimura, et al., (1979) (15% активности); Chen, et al., (1981) (28% активности); Nishimura, et al., (1981) (45% активности). В четвертой работе сообщалось, что PEG связан с 61% доступных остатков лизина, но остаточная специфическая активность не указана. Abuchowski, et al., (1981). Тем не менее, исследовательская группа, в которую входили двое из тех же самых исследователей и которая использовала те же методы, в другом месте сообщала, что эта степень сцепления обеспечивает остаточную активность только 23-28%. Chen, et al., (1981). В публикациях 1981 Abuchowski et al., and Chen et al. указано, что для существенного уменьшения иммуногенности уриказы PEG должен быть связан приблизительно с 60% доступных остатков лизина. В пятой публикации, в которой сообщалось об устранении иммунореактивности уриказы, не раскрыта степень сцепления PEG, остаточная уриколитическая активность или природа связи PEG-белок. Veronese, FM, et al., (1997) в JM Harris, et al., (Eds.), Poly(ethylene glycol) Chemistry and Biological Applications. ACS Symposium Series 680 (pp. 182-192) Washington, DC: American Chemical Society включена в настоящее описание в качестве ссылки в полном объеме.
Конъюгация PEG с меньшей долей остатков лизина в уриказе снижало, но не устраняло ее иммунореактивность у экспериментальных животных. Tsuji, J, et al., (1985) Int J Immunopharmacol 7: 725-730 включена в настоящее описание в качестве ссылки в полном объеме (связано 28-45% аминогрупп); Yasuda, Y, et al., (1990) Chem Pharm Bull 38: 2053-2056 включена в настоящее описание в качестве ссылки в полном объеме (связано 38% аминогрупп). Остаточные уриколитические активности соответствующих продуктов присоединения находились в пределах от <33% (Tsuji, et al.) до 60% (Yasuda, et al.) от их первоначальных значений. Tsuji, et al., синтезировали конъюгаты PEG-уриказа с 7,5 кДа и 10 кДа PEG, в дополнение к 5 кДа PEG. Все полученные конъюгаты являются до некоторой степени иммуногенными и антигенными, несмотря на то, что проявляют заметно сниженные ферментативные активности.
Сообщается, что пегилированный препарат уриказы, выделенной из Candida utilis, который безопасно вводили дважды каждому из пяти человек, сохранил только 11% от его начальной активности. Davis, et al., (1981). Несколько лет спустя, PEG-модифицированную уриказу, выделенную из Arthrobacter protoformiae, вводили четыре раза пациенту с генерализованной лимфомой и тяжелой гиперурикемией. Chua, et al., (1988). Несмотря на то, что остаточная активность этого препарата фермента не была измерена, Chua, et al., используя твердофазный иммуноферментный анализ (ELISA), продемонстрировали отсутствие антител против уриказы в сыворотке крови пациента через 26 дней после первой инъекции PEG-уриказы.
Предшествующие исследования пегилированной уриказы показали, что каталитическая активность заметно угнетена в результате связывания достаточного числа цепей PEG, для существенного уменьшения ее иммунореактивности. Кроме того, большинство ранних композиций PEG-уриказа синтезированы с использованием PEG, активированного хлорангидридом циануровой кислоты, производного триазина (2,4,6-трихлоро-1,3,5-триазин), который вносит новые антигенные детерминанты и индуцирует формирование антител у кроликов, Tsuji, et al., (1985).
В патенте Японии № 3-148298 A Sano, et al., включенном в настоящее описание в качестве ссылки в полном объеме, раскрыты модифицированные белки, в том числе уриказа, модифицированная PEG, имеющим молекулярную массу 1-12 кДа, которая проявляет уменьшенную антигенность и «улучшенное пролонгированное» действие, и способы получения таких производных пептидов. Тем не менее, нет раскрытия в отношении числа цепей, ферментативного анализа, биологических тестов или значения понятия «улучшенное пролонгирование». В патентах Японии 55-99189 и 62-55079, каждый включен в настоящее описание посредством ссылки в полном объеме, оба принадлежат Y Inada, раскрыты конъюгаты уриказы, полученные с PEG-триазином или bis-PEG-триазином (обозначен как PEG2), соответственно. См. Nishimura, et al., (1979 и 1981). В первом типе конъюгата молекулярная масса PEG составляет 2 кДа и 5 кДа, тогда как во втором использовали только 5 кДа PEG. Nishimura, et al., (1979) сообщали о восстановлении 15% уриколитической активности после модифицирования 43% доступных остатков лизина с помощью линейного 5 кДа PEG, тогда как Nishimura, et al., (1981) сообщали о восстановлении 31% или 45% уриколитической активности после модифицирования с помощью PEG2 46% или 36% остатков лизина, соответственно.
Ранее исследованные белки уриказы были либо природными, либо рекомбинантными белками. Однако исследования с использованием SDS-PAGE и/или вестерн-блоттинга выявили присутствие непредвиденных низкомолекулярных пептидов, которые, по-видимому, являются продуктами деградации и увеличиваются по частоте с течением времени. Настоящее изобретение относится к мутантным рекомбинантным белкам уриказы, имеющим укорочение и увеличенную структурную стабильность.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Настоящее изобретение обеспечивает новые рекомбинантные белки уриказы. В одном варианте осуществления белки по данному изобретению укорочены и имеют мутантные аминокислоты по сравнению с природными белками уриказы. В конкретных вариантах осуществления мутации находятся в или около областей аминокислот в положении 7, 46, 291 и 301. Консервативные мутации в любом участке пептида также рассматриваются как часть данного изобретения.
Данное изобретение обеспечивает мутантную рекомбинантную уриказу, где уриказа укорочена на 1-20 аминокислот и сохраняет уриколитическую активность природной уриказы. Укорочение проводят в или около областей окончания последовательности, таким образом, белок может содержать основные аминокислоты. Эти мутации и укорочения могут увеличивать стабильность белка, содержащего такие мутации.
В другом варианте осуществления настоящее изобретение обеспечивает средства для метаболизирования мочевой кислоты, которые включают новый рекомбинантный белок уриказы, имеющий уриколитическую активность. Уриколитическая активность используется в настоящем описании в отношении ферментативного превращения мочевой кислоты в аллантоин.
Данное изобретение также обеспечивает клетку-хозяина, которая способна продуцировать уриказу, укороченную на 1-20 аминокислот, и имеет мутантные аминокислоты и сохраняет уриколитическую активность.
В одном варианте осуществления обеспечена изолированная укороченная уриказа млекопитающего, содержащая аминокислотную последовательность уриказы млекопитающего, укороченную на аминоконце или карбоксиконце, или и на амино- и на карбоксиконце, приблизительно на 1-13 аминокислот, и дополнительно содержащая аминокислотную замену приблизительно в положении 46. В конкретных вариантах осуществления уриказа содержит аминоконцевую аминокислоту, где данной аминоконцевой аминокислотой является аланин, глицин, пролин, серин или треонин. Также обеспечена уриказа, в которой существует замена на треонин или аланин приблизительно в положении 46. В одном варианте осуществления уриказа содержит аминокислотную последовательность SEQ ID № 8. В одном варианте осуществления уриказа конъюгирована с полимером с образованием, например, конъюгата полиэтиленгликоль-уриказа. В конкретных вариантах осуществления конъюгаты полиэтиленгликоль-уриказа содержат от 2 до 12 молекул полиэтиленгликоля на каждую субъединицу уриказы, предпочтительно от 3 до 10 молекул полиэтиленгликоля на субъединицу уриказы. В конкретных вариантах осуществления каждая молекула полиэтиленгликоля в конъюгате полиэтиленгликоль-уриказа имеет молекулярную массу приблизительно от 1 кД до 100 кД; приблизительно от 1 кД до 50 кД; приблизительно от 5 кД до 20 кД; или приблизительно 10 кД. Также обеспечены фармацевтические композиции, содержащие уриказу по данному изобретению, в том числе конъюгат полиэтиленгликоль-уриказа. В одном варианте осуществления фармацевтическая композиция пригодна для повторного введения.
Также обеспечен способ снижения уровней мочевой кислоты в биологической жидкости субъекта, нуждающегося в этом, включающий введение фармацевтической композиции, содержащей уриказу по данному изобретению. В определенном варианте осуществления данной биологической жидкостью является кровь.
В одном варианте осуществления уриказа содержит пептид, имеющий последовательность от положения 44 до положения 56 Pig-KS-ΔN (SEQ ID № 14).
В одном варианте осуществления белок уриказы содержит на N-конце метионин. В конкретном варианте осуществления уриказа содержит аминокислотную последовательность SEQ ID № 7.
Также обеспечены изолированные нуклеиновые кислоты, в том числе последовательности нуклеиновых кислот, которые кодируют уриказу по данному изобретению, например уриказы, имеющие или содержащие аминокислотные последовательности SEQ ID № 7, SEQ ID № 8, SEQ ID № 12 или SEQ ID № 13. В одном варианте осуществления изолированная нуклеиновая кислота функционально связана с гетерологичным промотором, например промотором osmB. Также обеспечены векторы, содержащие нуклеиновые кислоты, кодирующие уриказу, и клетки-хозяева, содержащие такие векторы. В одном варианте осуществления нуклеиновая кислота имеет последовательность SEQ ID № 7. Также обеспечен способ получения уриказы, включающий стадии культивирования такой клетки-хозяина в условиях, при которых эта уриказа экспрессируется данной клеткой-хозяином, и выделения экспрессированной уриказы.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На фиг.1 представлена структура плазмиды pOUR-P-ΔN-ks-1. Числа после сайтов рестрикции означают положение нуклеотида, относительно сайта HaeII, обозначенном как 1. Сайты рестрикции, которые исчезают во время клонирования, указаны в круглых скобках.
На фиг.2 представлена ДНК и экспериментально установленные аминокислотные последовательности уриказы Pig-KS-ΔN (SEQ ID № 9 и SEQ ID № 7, соответственно). Нумерация аминокислот на фиг.2 относительно полной последовательности уриказы свиньи. После инициирующего остатка метионина аспарагиновая кислота в положении 7 аминокислотной последовательности уриказы свиньи заменена на треонин. Обозначены сайты рестрикции, которые используются на различных этапах субклонирования, 3'-нетранслируемая последовательность обозначена строчными буквами. Стоп-кодон трансляции обозначен звездочкой.
На фиг.3 представлено взаимное выравнивание выведенных аминокислотных последовательностей различных последовательностей рекомбинантных уриказ свиньи (SEQ ID № 11), PBC-ΔNC (SEQ ID № 12) и Pig-KS-ΔN (SEQ ID № 7). Звездочками обозначены положения, в которых существуют отличия аминокислот в Pig-KS-ΔN по сравнению с опубликованной последовательностью уриказы свиньи; кружочками обозначены положения, в которых существуют различия аминокислот в Pig-KS-ΔN по сравнению с PBC-ΔN. Пунктирные линии обозначают делеции аминокислот.
На фиг.4 представлен SDS-PAGE уриказы свиньи и вариантов высокоочищенной уриказы, полученных в соответствии с примерами 1-3. Дата производства (месяц/год) и соответствующий номер линии для каждого образца указаны в пояснении к фигуре, ниже. Ось Y обозначает массы маркеров молекулярного веса, и верхняя часть данной фигуры обозначает номера линий. Данные линии означают следующее: Линия 1 - маркеры молекулярного веса; Линия 2 - Pig KS-ΔN (7/98); Линия 3 - Pig (9/98); Линия 4 - Pig KS (6/99); Линия 5 - Pig KS (6/99); Линия 6 - Pig-ΔN (6/99); Линия 7 - Pig KS-ΔN (7/99); Линия 8 - Pig KS-ΔN (8/99).
На фиг.5 представлены фармакокинетические профили пегилированной уриказы (9×10 кД) Pig-KS-ΔN у крыс после в/м (внутримышечной), п/к (подкожной) и в/в (внутривенной) инъекций, установленные в результате мониторинга ферментативной активности в образцах крови. Активность уриказы в образцах плазмы, которые были собраны в определенные моменты времени, определена с помощью колориметрического анализа. Значения активности (mAU = миллиединицы абсобции) означают скорость ферментативной реакции на 1 мкл образца плазмы. Биологическую доступность (количество лекарственного средства, которое попадает в системный кровоток после в/в инъекции) введенной уриказы вычисляли по площади под кривой.
На фиг.6 представлены фармакокинетические профили пегилированной (9×10 кД) уриказы Pig-KS-ΔN у кроликов после в/м (внутримышечной), п/к (подкожной) и в/в (внутривенной) инъекций, установленные в результате мониторинга ферментативной активности в образцах крови. Активность уриказы в образцах плазмы, которые были собраны в определенные моменты времени, определена с помощью колориметрического анализа. Значения активности (mAU = миллиединицы абсобции) означают скорость ферментативной реакции на 1 мкл образца плазмы. Биологическую доступность (количество лекарственного средства, которое попадает в системный кровоток после в/в инъекции) введенной уриказы вычисляли по площади под кривой.
На фиг.7 представлены фармакокинетические профили пегилированной (9×10 кД) уриказы Pig-KS-ΔN у собак после в/м (внутримышечной), п/к (подкожной) и в/в (внутривенной) инъекций, установленные в результате мониторинга ферментативной активности в образцах крови. Активность уриказы в образцах плазмы, которые были собраны в определенные моменты времени, определена с помощью колориметрического анализа. Значения активности (mAU = миллиединицы абсобции) означают скорость ферментативной реакции на 1 мкл образца плазмы. Биологическую доступность (количество лекарственного средства, которое попадает в системный кровоток после в/в инъекции) введенной уриказы вычисляли по площади под кривой.
На фиг.8 представлены фармакокинетические профили пегилированной (9×10 кД) уриказы Pig-KS-ΔN у свиней после в/м (внутримышечной), п/к (подкожной) и в/в (внутривенной) инъекций, установленные в результате мониторинга ферментативной активности в образцах крови. Активность уриказы в образцах плазмы, которые были собраны в определенные моменты времени, определена с помощью колориметрического анализа. Значения активности (mAU = миллиединицы абсобции) означают скорость ферментативной реакции на 1 мкл образца плазмы. Биологическую доступность (количество лекарственного средства, которое попадает в системный кровоток после в/в инъекции) введенной уриказы, вычисляли по площади под кривой.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Предшествующие исследования показали, что если значительное снижение иммуногенности и/или антигенности уриказы достигнуто в результате пегилирования, это неизменно связано с существенной потерей уриколитической активности. Снижение их активности и, как результат, необходимость увеличения вводимой дозы неблагоприятно влияют на безопасность, удобство и рентабельность биофармацевтических препаратов. Таким образом, существует необходимость в безопасных и эффективных альтернативных средствах снижения повышенных уровней мочевой кислоты в жидкостях организма, в том числе в крови. Настоящее изобретение обеспечивает мутантную рекомбинантную уриказу, где уриказа укорочена на 1-20 аминокислот либо на аминоконце, либо на карбокси-конце, либо на обоих, и по существу сохраняет уриколитическую активность природной уриказы.
Уриказа, как используется в настоящем описании, включает отдельные субъединицы, а также тетрамер, если не указано иначе.
Мутантная уриказа, как используется в настоящем описании, относится к молекулам уриказы, имеющей аминокислоты, замененные на другие аминокислоты.
Консервативная мутация, как используется в настоящем описании, представляет собой мутацию одной или нескольких аминокислот, в положении или около положения, которое по существу не изменяет свойства белка. В предпочтительном варианте осуществления уриказа, содержащая, по меньшей мере, одну консервативную мутацию, имеет такую же уриказную активность, как уриказа, не имеющая такой мутации. В альтернативных вариантах осуществления уриказа, содержащая, по меньшей мере, одну консервативную мутацию, имеет по существу такую же уриказную активность, в пределах 5% активности, в пределах 10% активности или в пределах 30% активности уриказа без такой мутации.
Консервативная аминокислотная замена определяется как изменение аминокислотного состава посредством изменения аминокислот пептида, полипептида или белка, или его фрагмента. В конкретных вариантах осуществления в уриказе присутствуют одна, две, три или четыре консервативные мутации. Данной заменой являются аминокислоты, имеющие, как правило, аналогичные свойства (например, кислотность, основность, ароматичность, размер, положительный или отрицательный заряд, полярность, неполярность), таким образом, что данные замены по существу не изменяют свойства пептида, полипептида или белка (например, заряд, изоэлектрическое фокусирование, аффинность, авидность, конформация, растворимость) или активность. Типичные замены, которые могут быть осуществлены для такой консервативной аминокислотной замены, могут входить в следующие группы аминокислот:
глицин (G), аланин (A), валин (V), лейцин (L) и изолейцин (I)
аспарагиновая кислота (D) и глутаминовая кислота (E)
аланин (A), серин (S) и треонин (T)
гистидин (H), лизин (K) и аргинин (R)
аспарагин (N) и глутамин (Q)
фенилаланин (F), тирозин (Y) и триптофан (W)
Белок, несущий одну или несколько консервативных замен, сохраняет свою структурную стабильность и может катализировать реакцию, даже если последовательность его ДНК отличается от последовательности исходного белка.
Укороченная уриказа, как используется в настоящем описании, относится к молекулам уриказы, имеющим укороченные первичные амикнокислотные последовательности. Среди возможных укорочений имеют место укорочения на или около амино- и/или карбоксиконца. Специфические укорочения такого типа могут быть такими, что крайние аминокислоты (те, которые находятся на амино- и/или карбоксиконце) природного белка присутствуют в укороченном белке. Укорочение аминоконца может начинаться с положения 1, 2, 3, 4, 5 или 6. Предпочтительно, укорочения аминоконца начинаются с положения 2, оставляя аминоконцевой метионин. Этот метионин может быть удален в результате посттрансляционной модификации. В конкретных вариантах осуществления аминоконцевой метионин удален после продуцирования уриказы. В определенном варианте осуществления данный метионин удален с помощью эндогенной бактериальной аминопептидазы.
Укороченная уриказа, по отношению к последовательности полной длины, имеет одну или несколько исключенных аминокислотных последовательностей. Белок, содержащий укороченную уриказу, может включать любую аминокислотную последовательность в дополнение к последовательности укороченной уриказы, за исключением белка, включающего последовательность уриказы, содержащей любую непрерывную аминокислотную последовательность дикого типа. Другими словами, белок, содержащий укороченную уриказу, где данное укорочение начинается в положении 6 (то есть укороченная уриказа начинается с положения 7), не имеет, сразу же в 3'-5' направлении от укороченной уриказы, какую либо аминокислоту, которая в уриказе дикого типа находится в положении 6.
Если не обозначено иначе посредством специфической ссылки на другую последовательность или конкретную последовательность SEQ ID №, ссылка на пронумерованные положения аминокислот уриказы, описанной в настоящем описании, сделана относительно нумерации аминокислот в последовательности уриказы свиньи. Аминокислотная последовательность уриказы свиньи и пронумерованные положения аминокислот, имеющие эту последовательность, представлены на фиг.3. Используемая в настоящем описании ссылка на аминокислоты или нуклеиновые кислоты «от положения Х до положения Y» означает непрерывную последовательность, начинающуюся в положении Х и заканчивающуюся в положении Y, включая аминокислоты или нуклеиновые кислоты в обоих положениях Х и Y.
Гены уриказы и белки были определены для нескольких видов млекопитающих, например, свиньи, бабуина, крысы, кролика, мыши и макак-резус. Последовательности различных белков уриказы описаны в настоящем описании посредством ссылки на их инвентарные номера в доступных для общего пользования базах данных, как указано далее: gi|50403728|sp|P25689; gi|20513634|dbj|BAB91555.1; gi|176610|gb|AAA35395.1; gi|20513654|dbj|BAB91557.1; gi|47523606|ref|NP_999435.1; gi|6678509|ref|NP_033500.1; gi|57463|emb|CAA31490.1; gi|20127395|ref|NP_446220.1; gi|137107|sp|P11645; gi|51458661|ref|XP_497688.1; gi|207619|gb|AAA42318.1; gi|26340770|dbj|BAC34047.1 и gi|57459|emb|CAA30378.1. Каждая из этих последовательностей и примечаний к ним в доступных для общего пользования базах данных, открытых для доступа через National Center for Biotechnology Information (NCBI), включена посредством ссылки в полном объеме.
В одном варианте осуществления данного изобретения уриказа укорочена на 4-13 аминокислот на ее аминоконце. В одном варианте осуществления данного изобретения уриказа укорочена на 4-13 аминокислот на ее карбоксиконце. В одном варианте осуществления данного изобретения уриказа укорочена на 4-13 аминокислот и на карбокси-, и на аминоконце.
В одном варианте осуществления данного изобретения уриказа укорочена на 6 аминокислот на ее аминоконце. В одном варианте осуществления данного изобретения уриказа укорочена на 6 аминокислот на ее карбоксиконце. В одном варианте осуществления данного изобретения уриказа укорочена на 6 аминокислот и на карбокси-, и на аминоконце.
В определенном варианте осуществления белок уриказы содержит аминокислотную последовательность от положения 13 до положения 292 аминокислотной последовательности уриказы свиньи (SEQ ID № 11). В определенном варианте осуществления белок уриказы содержит аминокислотную последовательность от положения 8 до положения 287 аминокислотной последовательности PBC-ΔNC (SEQ ID № 12). В определенном варианте осуществления белок уриказы содержит аминокислотную последовательность от положения 8 до положения 287 аминокислотной последовательности Pig-KS-ΔN (SEQ ID № 7).
В другом варианте осуществления белок уриказы содержит аминокислотную последовательность от положения 44 до положения 56 аминокислотной последовательности Pig-KS-ΔN (SEQ ID № 14). Эта область уриказы обладает гомологией с последовательностями в пределах домена тоннельной укладки («T-fold») уриказы и имеет в его пределах мутацию в положении 46 по отношению к последовательности природной уриказы свиньи. Удивительно, что данная мутация существенно не изменяет уриказную активность данного белка.
В одном варианте данного изобретения аминокислоты в положении или вблизи положения любой из аминокислот 7, 46 и 291, и 301 являются мутантными. В предпочтительном варианте осуществления данного изобретения мутированы непосредственно аминокислоты 7, 46 и 291, и 301.
В определенных вариантах осуществления белок кодируется нуклеиновой кислотой, которая кодирует N-концевой метионин. Предпочтительно, за N-концевым метионином следует кодон, который делает возможным удаление этого N-концевого метионина посредством бактериальной метионин-аминопептидазы (MAP). (Ben-Bassat and Bauer (1987) Nature 326:315 включено в настоящее описание посредством ссылки в полном объеме). Аминокислотами, которые делают возможным наиболее полное удаление N-концевого метионина, являются аланин, глицин, пролин, серин и треонин.
В одном варианте осуществления данного изобретения аминокислоты в положении или вблизи положения 7 и/или 46 замещены треонином. Удивительно, что ферментативная активность укороченных уриказ, имеющих эти мутации, аналогична ферментативной активности неукороченного фермента. В еще одном варианте осуществления данного изобретения мутации аминокислот включают треонин, треонин, лизин и серин в положениях 7, 46, 291 и 301, соответственно.
Укороченные уриказы млекопитающих, раскрытые в настоящем описании, могут дополнительно содержать метионин на аминоконце. Предпоследняя аминокислота может быть одной из тех, которые делают возможным удаление N-концевого метионина посредством бактериальной метионин-аминопептидазы (MAP). Аминокислотами, которые делают возможным наиболее полное удаление N-концевого метионина, являются аланин, глицин, пролин, серин и треонин. В определенном варианте осуществления уриказа содержит две аминоконцевых аминокислоты, где эти две аминокислоты являются метионином, за которым следует аминокислота, выбранная из группы, состоящей из аланина, глицина, пролина, серина и треонина.
В другом варианте осуществления данного изобретения замещенные аминокислоты заменены на треонин.
В одном варианте осуществления данного изобретения уриказа является уриказой млекопитающего.
В одном варианте осуществления данного изобретения уриказа млекопитающего содержит последовательность уриказы печени свиньи, быка, овцы и бабуина.
В одном варианте осуществления данного изобретения уриказа является химерной уриказой двух или нескольких млекопитающих.
В одном варианте осуществления данного изобретения данные уриказы млекопитающих выбраны из уриказ печени свиньи, быка, овцы или бабуина.
В одном варианте осуществления данного изобретения уриказа содержит последовательность SEQ ID № 8.
В другом варианте осуществления данного изобретения уриказа содержит последовательность SEQ ID № 13.
Данное изобретение обеспечивает уриказу, кодируемую нуклеиновыми кислотами, содержащими последовательность SEQ ID № 10.
В одном варианте данного изобретения уриказа содержит грибковую или бактериальную уриказу.
В одном варианте данного изобретения данной грибковой или бактериальной уриказой является уриказа Aspergillus flavus, Arthrobacter globiformis или Candida utilis.
В одном варианте данного изобретения уриказа включает уриказу беспозвоночного животного.
В одном варианте данного изобретения уриказой беспозвоночного животного является уриказа Drosophila melanogaster или Drosophila pseudoobscura.
В одном варианте данного изобретения уриказа включает уриказу растительного происхождения.
В одном варианте данного изобретения уриказой растительного происхождения является уриказа Glycine max корневых клубеньков.
Данное изобретение обеспечивает последовательность нуклеиновой кислоты, кодирующую уриказу.
Данное изобретение обеспечивает вектор, включающий данную последовательность нуклеиновой кислоты.
В определенном варианте осуществления уриказа выделена. В определенном варианте осуществления уриказа очищена. В определенных вариантах осуществления уриказа выделена и очищена.
Данное изобретение обеспечивает клетку-хозяина, содержащую вектор.
Данное изобретение обеспечивает способ получения последовательности нуклеиновой кислоты, включающий модификацию с помощью методов ПЦР (полимеразной цепной реакции) последовательности нуклеиновой кислоты, кодирующей неукороченную уриказу. Специалисту в данной области известно, что требуемая последовательность нуклеиновой кислоты получена посредством ПЦР с помощью синтетических олигонуклеотидных праймеров, которые комплиментарны областям амплифицируемой ДНК-мишени (один для каждой цепи). Данные праймеры добавлены к ДНК-мишени (которой нет необходимости быть очищенной) в присутствии избытка дезоксинуклеотидов и Taq-полимеразы, устойчивой к нагреванию ДНК-полимеразы. В серии (обычно 30) температурных циклов ДНК-мишень многократно денатурируется (приблизительно при 90°С), отжигается с праймерами (приблизительно при 50-60°С), и дочерняя цепь удлиняется от праймеров (приблизительно при 72°С). Поскольку данные дочерние нити сами по себе выступают в роли матрицы в последующих циклах, фрагменты ДНК, соответствующие обоим праймерам, амплифицируются экспоненциально, а не линейно.
Данное изобретение обеспечивает способ получения мутантной рекомбинантной уриказы, включающий трансфекцию клетки-хозяина вектором, где клетка-хозяин экспрессирует уриказу, выделение мутантной рекомбинантной уриказы из клетки-хозяина, выделение и очистку мутантной рекомбинантной уриказы с использованием, например, хроматографических методов, и очистку мутантной рекомбинантной уриказы. Например, уриказа может быть получена в соответствии с методами, описанными в Международной Патентной Публикации № WO 00/08196, включенной в настоящее описание посредством ссылки в полном объеме.
Уриказа может быть выделена и/или очищена с помощью любого способа, известного специалисту в данной области. Экспрессируемые полипетиды по данному изобретению в основном выделяют в, по существу, чистой форме. Предпочтительно, данные полипептиды выделены с чистотой, по меньшей мере, 80% по весу, более предпочтительно с чистотой, по меньшей мере, 95% по весу и наиболее предпочтительно с чистотой, по меньшей мере, 99% по весу. В большинстве случаев такую очистку можно обеспечить, используя, например, стандартные методики фракционирования сульфатом аммония, электрофореза в SDS-ПААГ и аффинной хроматографии. Уриказа предпочтительно выделена с использованием катионного поверхностно-активного вещества, например хлорида цетилпиридиния (СРС), согласно способу, описанному в находящейся одновременно на рассмотрении патентной заявке США, зарегистрированной 11 апреля 2005 г., имеющей № заявки 60/670520 и номер в досье поверенного 103864.146644, называемой «Очистка белков с помощью катионного поверхностно-активного вещества», которая включена в настоящее описание посредством ссылки в полном объеме.
В предпочтительном варианте осуществления клетку-хозяина обрабатывают для того, чтобы вызывать экспрессию мутанта рекомбинантной уриказы. Специалисту в данной области известно, что трансфекция клетки вектором обычно достигается с помощью ДНК, осажденной с ионами кальция, хотя можно использовать различные другие способы (например, электропорацию).
В одном варианте осуществления данного изобретения вектор находится под контролем промотора, чувствительного к осмотическому давлению. Промотор представляет собой участок ДНК, с которым РНК-полимераза связывается перед началом транскрипции ДНК в РНК. Промотор, чувствительный к осмотическому давлению, запускает транскрипцию в результате повышенного осмотического давления, которое воспринимается данной клеткой.
В одном варианте осуществления данного изобретения промотор представляет собой модифицированный промотор osmB.
В определенных вариантах осуществления уриказа по данному изобретению конъюгирована с полимером.
В одном варианте осуществления данного изобретения обеспечена фармацевтическая композиция, содержащая уриказу. В одном варианте осуществления композиция представляет собой раствор уриказы. В предпочтительном варианте осуществления раствор является стерильным и пригодным для инъекции. В одном варианте осуществления такая композиция содержит уриказу в виде раствора в забуференном фосфатом физиологическом растворе. В одном варианте осуществления композиция содержится во флаконе, который при желании имеет резиновый ограничитель введения. В конкретных вариантах осуществления композиция содержит уриказу в растворе в концентрации от 2 до 16 миллиграмм уриказы на миллилитр раствора, от 4 до 12 миллиграмм на миллилитр или от 6 до 10 миллиграмм на миллилитр. В предпочтительном варианте осуществления композиция содержит уриказу в концентрации 8 миллиграмм на миллилитр. Предпочтительно, масса уриказы вычисляется относительно массы белка.
Эффективные схемы введения композиций по данному изобретению могут быть определены специалистом в данной области. Соответствующие показатели для оценки эффективности выбранной схемы известны специалисту в данной области. Примеры таких показателей включают нормализацию или снижение уровней мочевой кислоты в плазме крови (PUA) и снижение или поддержание PUA на уровне 6,8 мг/дл или ниже, предпочтительно 6 мг/дл или ниже. В предпочтительном варианте осуществления человек, подвергающийся лечению композицией по данному изобретению, имеет уровень PUA 6 мг/мл или ниже в течение, по меньшей мере, 70%, по меньшей мере, 80% или, по меньшей мере, 90% общего периода лечения. Например, для периода лечения 24 недели, человек имеет уровень PUA 6 мг/мл или менее, в течение, по меньшей мере, 80% этого 24-недельного периода лечения, то есть, по меньшей мере, в течение времени, эквивалентного времени 134,4 дня (24 недели × 7 дней/неделя × 0,8 = 134,4 дня).
В определенных вариантах осуществления от 0,5 до 24 мг уриказы в растворе вводят один раз каждые 2-4 недели. Уриказа может быть введена в организм любым путем, известным специалисту в данной области, например внутривенно, внутримышечно или подкожно. Предпочтительно, в случае внутривенного применения, вводится от 0,5 до 12 мг уриказы. Предпочтительно, в случае подкожного применения, вводится от 4 до 24 мг уриказы. В предпочтительном варианте осуществления уриказу вводят в организм посредством внутривенного вливания в течение периода времени от 30 до 240 минут. В одном варианте осуществления 8 мг уриказы вводят один раз каждые две недели. В определенных вариантах осуществления данное вливание можно осуществить, используя от 100 до 500 мл физиологического раствора. В предпочтительном варианте осуществления 8 мг уриказы в растворе вводят в течение 120 минут один раз каждые 2 недели или один раз каждые 4 недели; предпочтительно, уриказа растворена в 250 мл физиологического раствора для вливания. В определенных вариантах осуществления уриказу применяют в течение периода лечения 3 месяца, 6 месяцев, 8 месяцев или 12 месяцев. В других вариантах осуществления период лечения составляет 12 недель, 24 недели, 36 недель или 48 недель. В определенном варианте осуществления период лечения является продолжительным периодом времени, например 2 года или более, вплоть до конца жизни человека, получающего лечение. Кроме того, можно применять серии периодов лечения, чередуя с периодами времени без лечения, например 6 месяцев лечения, за которыми следуют 3 месяца без лечения, за которыми следуют 6 дополнительных месяцев лечения, и так далее.
В некоторых вариантах осуществления профилактически могут использоваться противовоспалительные соединения, для устранения или снижения возникновения инфузионных реакций в результате применения уриказы. В одном варианте осуществления совместно применяются, по меньшей мере, один кортикостероид, по меньшей мере, один антигистаминный препарат, по меньшей мере, одно NSAID (НПВС) или их комбинации. Пригодные кортикостероиды включают бетаметазон, будесонид, кортизон, дексаметазон, гидрокортизон, метилпреднизолон, преднизолон, преднизон и триамцинолон. Пригодные NSAID включают ибупрофен, индометацин, напроксен, аспирин, ацетоминофен, целекоксиб и валдекоксиб. Пригодные антигистаминные средства включают азатадин, бромфенирамин, цетиризин, хлорфенирамин, клемастин, ципрогептадин, деслоратадин, дексхлорфенирамин, дименгидринат, дифенгидрамин, доксиламин, фексофенадин, гидроксизин, лоратадин и фениндамин.
В предпочтительном варианте осуществления антигистаминным средством является фексофенадин, NSAID является ацетаминофен, и кортикостероидом является гидрокортизон и/или преднизон. Предпочтительно, комбинация всех трех (не обязательно сопутствующая) применяется перед вливанием раствора уриказы. В предпочтительном варианте осуществления данные NSAID и антигистаминное средство применяют перорально за 1-4 часа до вливания уриказы. Подходящая доза фексофенадина включает приблизительно от 30 приблизительно до 180 мг, приблизительно от 40 приблизительно до 150 мг, приблизительно от 50 приблизительно до 120 мг, приблизительно от 60 приблизительно до 90 мг, приблизительно 60 мг, предпочтительно 60 мг. Подходящая доза ацетаминофена включает приблизительно от 500 приблизительно до 1500 мг, приблизительно от 700 приблизительно до 1200 мг, приблизительно от 800 приблизительно до 1100 мг, приблизительно 1000 мг, предпочтительно 1000 мг. Подходящая доза гидрокортизона включает приблизительно от 100 приблизительно до 500 мг, приблизительно от 150 приблизительно до 300 мг, приблизительно 200 мг, предпочтительно 200 мг. В одном варианте осуществления антигистаминное средство не является дифенгидрамином. В другом варианте осуществления NSAID не является ацетаминофеном. В предпочтительном варианте осуществления 60 мг фексофенадина применяют перорально на ночь перед инфузией уриказы; 60 мг фексофенадина и 1000 мг ацетаминофена применяют на следующее утро, и, в заключение, 200 мг гидрокортизона применяют перед самой инфузией раствора уриказы. В одном варианте осуществления преднизон применяют в день, предпочтительно вечером, перед применением уриказы. Подходящая доза преднизона включает от 5 до 50 мг, предпочтительно 20 мг. В некоторых вариантах осуществления эти профилактические методы лечения для устранения или уменьшения возникновения инфузионных реакций применяют у людей, получающих или собирающихся получить уриказу, в том числе пегилированную уриказу и непегилированную уриказу. В определенных вариантах осуществления эти профилактические методы лечения применяют у людей, получающих или собирающихся получить терапевтические пептиды, отличные от уриказы, где эти другие терапевтические пептиды являются пегилированными или непегилированными.
В одном варианте осуществления данного изобретения фармацевтическая композиция содержит уриказу, которая модифицирована посредством конъюгирования с полимером, и модифицированная уриказа сохраняет уриколитическое действие. В определенном варианте осуществления конъюгаты полимер-уриказы получены, как описано в международной публикации патентной заявки № WO 01/59078 и заявке США № 09/501730, включенных в настоящее описание посредством ссылки в полном объеме.
В одном варианте осуществления данного изобретения полимер выбран из группы, содержащей полиэтиленгликоль, декстран, полипропиленгликоль, гидроксипропилметилцеллюлозу, карбоксиметилцеллюлозу, поливинилпирролидон и поливиниловый спирт.
В одном варианте осуществления данного изобретения композиция содержит 2-12 молекул полимера на каждой субъединице уриказы, предпочтительно от 3 до 10 молекул полимера на субъединицу уриказы.
В одном варианте осуществления данного изобретения каждая молекула полимера имеет молекулярную массу от приблизительно 1 кД и до приблизительно 100 кД.
В другом варианте осуществления данного изобретения каждая молекула полимера имеет молекулярную массу от приблизительно 1 кД до приблизительно 50 кД. В предпочтительном варианте осуществления данного изобретения каждая молекула полимера имеет молекулярную массу от приблизительно 5 кД до приблизительно 20 кД, от приблизительно 8 кД до приблизительно 15 кД, от приблизительно 10 кД до приблизительно 12 кД, предпочтительно приблизительно 10 кД. В предпочтительном варианте осуществления каждая молекула полимера имеет молекулярную массу от приблизительно 5 кД до приблизительно 20 кД. В особенно предпочтительном варианте осуществления каждая молекула полимера имеет молекулярную массу 10 кД. Также предусмотрены смеси молекул с различной массой. В одном варианте осуществления данного изобретения композиция является композицией, пригодной для повторного введения.
В определенном варианте осуществления конъюгирование уриказы с полимером содержит связи, выбранные из группы, включающей уретановые связи, связи вторичных аминов и амидные связи.
Настоящее изобретение обеспечивает клетку, способную вырабатывать уриказу, имеющую аминокислотную последовательность рекомбинантной уриказы, где уриказа укорочена на 1-20 аминокислот и имеет мутантные аминокислоты и уриколитическую активность.
Данное изобретение обеспечивает средства для метаболизирования мочевой кислоты с использованием уриказы.
Данное изобретение обеспечивает применение композиции уриказы для снижения уровней мочевой кислоты в биологической жидкости.
В одном варианте осуществления данного изобретения композиция уриказы используется для снижения уровня мочевой кислоты в биологической жидкости, в том числе в крови.
Также обеспечены новые молекулы нуклеиновой кислоты, кодирующие полипептиды уриказы. Манипуляции, приводящие к их получению, хорошо известны специалисту в данной области. Например, последовательности нуклеиновой кислоты уриказы могут быть модифицированы посредством любой из многочисленных стратегий, известных из уровня техники (Maniatis, T., 1990, Molecular Cloning, A Laboratory Manual, 2d ed., Cold Spring Harbor Laboratory, Cold Spring Harbor, N.Y.). Последовательность может быть расщеплена в соответствующих сайтах с помощью эндонуклеазы (эндонуклеаз) рестрикции, при необходимости, с последующей дальнейшей ферментативной модификацией, выделена и лигирована in vitro. При получении гена, кодирующего уриказу, необходимо проявить осторожность, для гарантии того, что модифицированный ген остается в пределах соответствующей трансляционной рамки считывания и не прерван трансляционными стоп-сигналами. Дополнительно, последовательность нуклеиновой кислоты, кодирующая уриказу, может быть мутирована in vitro или in vivo для создания/разрушения трансляционной последовательности, последовательности инициации и/или терминационной последовательности, или для создания вариантов в кодирующих областях, и/или формирования новых сайтов для эндонуклеаз рестрикции, или разрушения существовавших ранее для облегчения дальнейшей модификации in vitro. Могут быть использованы любые технологии мутагенеза, известные из уровня техники, в том числе, но не ограничиваясь, сайт-специфический мутагенез in vitro (Hutchinson, C, et al., 1978, J. Biol. Chem 253: 6551), использованием линкеров TAB® (Pharmacia) и тому подобное.
Нуклеотидная последовательность, кодирующая белок уриказы, может быть встроена в соответствующий экспрессирующий вектор, а именно вектор, который содержит необходимые элементы для транскрипции и трансляции данной встроенной последовательности, кодирующей белок. Для экспрессии данной последовательности, кодирующей белок, могут быть использованы различные системы хозяин-вектор. В том числе, но не ограничиваясь, клеточные системы млекопитающих, зараженные вирусом (например, вирусом коровьей оспы, аденовирусом и тому подобным), клеточные системы насекомых, зараженные вирусом (например, бакуловирусом), микроорганизмы, такие как дрожжи, содержащие векторы дрожжей, или бактерии, трансформированные ДНК бактериофага, плазмидной ДНК, или космидной ДНК. Элементы экспрессии этих векторов различаются по их силе и специфичности. В зависимости от используемой системы хозяин-вектор, может быть использован любой из подходящих элементов транскрипции и трансляции.
Любой из известных способов встраивания фрагментов ДНК в вектор можно использовать для конструирования экспрессирующих векторов, содержащих химерные гены, включающие соответствующие сигналы транскрипции/трансляции и кодирующие последовательности белка. Эти способы могут включать технологии рекомбинантных ДНК и синтетические методы in vitro и рекомбинации in vivo (генетическая рекомбинация). Экспрессию последовательности нуклеиновой кислоты, кодирующей белок уриказы, можно регулировать с помощью второй последовательности нуклеиновой кислоты, так чтобы белок уриказы экспрессировался хозяином, трансформированным молекулой рекомбинантной ДНК. Например, экспрессию уриказы можно контролировать с помощью любого промоторного/энхансерного элемента, известного из уровня техники. Промоторы, которые можно использовать для контроля экспрессии уриказы, включают, но не ограничиваются, область раннего промотора SV40 (Bernoist and Chambon, 1981, Nature 290: 304-310), промотор, содержащий на 3'-конце длинный концевой повтор вируса саркомы Рауса (Yamamoto, et al., 1980, Cell 22: 787-797), промотор тимидинкиназы вируса герпеса (Wagner et al., 1981, Proc. Natl. Acad. Sci. U.S.A. 78: 144-1445), регуляторные последовательности гена металлотионина (Brinster et al., 1982, Nature 296: 39-42), прокариотные экспрессирующие векторы, например промотор β-лактамазы (Villa-Kamaroff, et al., 1978, Proc. Natl. Acad. Sci. U.S.A. 75:3727-3731), tac-промотор (DeBoer, et al., 1983, Proc. Natl. Acad. Sci. U.S.A. 80:21-25), и промотор osmB. В определенных вариантах осуществления нуклеиновая кислота содержит последовательность нуклеиновой кислоты, кодирующую уриказу, функционально связанную с гетерологичным промотором.
После того, как определенная молекула рекомбинантной ДНК, содержащая последовательность кодирующей нуклеиновой кислоты, получена и выделена, можно использовать несколько способов, известных из уровня техники, для ее размножения. После того, как установлены подходящие система хозяина и условия роста, рекомбинантный экспрессирующий вектор может быть размножен и получен в большом количестве. Как описано ранее, экспрессирующие векторы, которые могут быть использованы, включают, но не ограничиваются, следующие векторы или их производные: вирусы человека или животных, такие как вирус коровьей оспы или аденовирус; вирусы насекомых, такие как бакуловирус; векторы дрожжей; векторы на основе бактериофага (например, лямбда), и векторы плазмидной и космидной ДНК, но немногие.
Кроме того, может быть выбран штамм клетки-хозяина, который модулирует экспрессию встроенных последовательностей или модифицирует и производит генный продукт специфическим необходимым способом. Экспрессию от некоторых промоторов можно усилить в присутствии некоторых индуцирующих факторов; следовательно, можно контролировать экспрессию белка уриказы, созданной методами генетической инженерии. Более того, различные клетки-хозяева имеют характерные и специфические механизмы трансляционного и посттрансляционного процессинга и модификации белков (например, гликозилирование, расщепление). Соответствующие клеточные линии или системы хозяина могут быть выбраны для гарантии необходимой модификации и процессинга экспрессированного чужеродного белка. Различные экспрессирующие системы вектор/хозяин могут действовать на реакции процессинга, такие как протеолитическое расщепление до различных диапазонов.
В определенных вариантах осуществления данного изобретения экспрессию уриказы в E.coli предпочтительно осуществляют, используя векторы, которые содержат промотор osmB.
ПРИМЕРЫ
Пример 1. Конструкция гена и экспрессирующей плазмиды для экспрессии уриказы
Рекомбинанатная уриказа свиньи (уратоксидаза), Pig-KS-ΔN (укороченный с аминоконца белок уриказы свиньи, с заменой аминокислот в положении 291 и 301 на лизин и серин, соответственно), была экспрессирована штаммом W3110 F- E.Сoli K-12. Конструировали ряд плазмид, завершившийся плазмидой pOUR-P-ΔN-ks-1, которая после трансформации клеток-хозяев E.Coli была способна направлять эффективную экспрессию уриказы.
Выделение и субклонирование кДНК уриказы из печени свиньи и бабуина
Получали кДНК уриказы из печеней свиньи и бабуина посредством выделения и субклонирования соответствующей РНК. Общую клеточную РНК выделяли из печеней свиньи и бабуина (Erlich, H.A. (1989). PCR Technology; Principles and Application for DNA Amplification; Sambrook, J., et al. (1989). Molecular Cloning: A Laboratory Manual, 2nd edition; Ausubel, F. M. et al. (1998). Current protocols in molecular Biology), затем проводили обратное считывание с использованием набора First-Strand cDNA Synthesis (Pharmacia Biotech). ПЦР-амплификацию проводили с использованием Taq ДНК-полимеразы (Gibco BRL, Life Technologies).
Синтетические олигонуклеотидные праймеры, используемые для ПЦР-амплификации уратоксидаз (уриказ) свиньи и бабуина, представлены в таблице 1.
прямой 5' gcgcgaattccATGGCTCATTACCGTAATGACTACA 3' (SEQ ID № 1)
обратный 5' gcgctctagaagcttccatggTCACAGCCTTGAAGTCAGC 3' (SEQ ID № 2)
Уриказа печени бабуина (D3H):
прямой 5' gcgcgaattccATGGCCCACTACCATAACAACTAT 3' (SEQ ID № 3)
обратный 5' gcgcccatggtctagaTCACAGTCTTGAAGACAACTTCCT 3' (SEQ ID № 4)
Последовательностями рестрикционных ферментов, включенных в окончания праймеров и обозначенных прописными буквами в Таблице 1, были прямые EcoRI и NcoI (для свиньи и бабуина) и обратные NcoI, HindIII и XbaI (свинья), XbaI и NcoI (бабуин). В прямом праймере для последовательности уриказы бабуина третий кодон GAC (аспарагиновая кислота), представленный в уриказе бабуина, был замещен на кодон САС (гистидин), который находится в этом положении в кодирующей последовательности псевдогена уратоксидазы человека. Данная конструкция рекомбинантной уриказы бабуина, созданная с использованием этих праймеров, называется D3H уриказа бабуина.
ПЦР продукт уриказы свиньи расщепляли с помощью EcoRI и HindIII и клонировали в pUC18 для создания конструкции pUC18-уриказа свиньи. ПЦР продукт D3H уриказы бабуина напрямую клонировали в вектор pCR™II, используя TA Cloning™ (Invitrogen, Carlsbad, CA), для создания конструкции pCR™II-D3H уриказа бабуина.
Лигированные кДНК использовали для трансформации штамма XL1-Blue E.Coli (Stratagene, La Jolla, CA). Получали плазмидную ДНК, содержащую клонированную кДНК уриказы, и отбирали и изолировали клоны, которые имеют опубликованные кодирующие последовательности ДНК уриказы (за исключением замены D3H в уриказе бабуина, представленной в таблице 1). В выбранном клоне pCR™II-D3H уриказа бабуина последовательности pCR™II следовали за стоп-кодоном уриказы, полученным в результате удаления последовательностей, встроенных посредством ПЦР. Вследствие этого сайты рестрикции для XbaI и NcoI были удалены из 3'-нетранслируемой области, таким образом делая возможным прямое клонирование с использованием NcoI на 5'-конце ПЦР-продукта, и BamHI, который происходит из вектора pCR™II.
Субклонирование кДНК уриказы в экспрессирующие векторы pET
Субклонирование уриказы бабуина
кДНК бабуина D3H, содержащую полноразмерную кодирующую последовательность уриказы, встраивали в экспрессирующий вектор pET-3d (Novagen, Madison, WI). Конструкцию pCR(TM)II-D3H уриказа бабуина расщепляли с помощью NcoI и BamHI и выделяли фрагмент длиной 960 п.о. Экспрессирующую плазмиду pET-3d расщепляли с помощью NcoI и BamHI и выделяли фрагмент длиной 4600 п.о. Лигировали два данных фрагмента для создания конструкции pET-3d-D3H-бабуина.
Субклонирование уриказы химеры свинья-бабуин
Уриказу химеры свинья-бабуин (РВС) конструировали для получения более высокой экспрессии, стабильности и активности данного рекомбинантного гена. PBC конструировали посредством выделения фрагмента NcoI-ApaI длиной 4936 п.о. из клона pET-3d-D3H-бабуина и лигирования данного изолированного фрагмента с фрагментом NcoI-ApaI длиной 624 п.о., выделенного из pUCl 8-уриказа свиньи, что приводит к образованию pET-3d-PBC. кДНК уриказы PBC содержит кодоны 1-225 уриказы свиньи, соединенные внутри рамки считывания с кодонами 226-304 уриказы бабуина.
Субклонирование уриказы Pig-KS
Уриказу Pig-KS конструировали для добавления одного остатка лизина, чтобы создать дополнительный сайт пегилирования. KS означает вставку в уриказу свиньи аминокислоты лизин в положение 291, вместо аргинина (R291K). Кроме того, треонин в положении 301 заменен на серин (T301S). Плазмиду уриказы PigKS конструировали, изолируя фрагмент NcoI-NdeI длиной 4696 п.о. из pET-3d-D3H-бабуин и затем лигируя его с фрагментом NcoI-NdeI, длиной 864 п.о., который был изолирован из pUC18-уриказа свиньи, что приводит к формированию pET-3d-PigKS. Последовательность полученной уриказы PigKS содержит кодоны 1-288 уриказы свиньи, соединенные в пределах рамки считывания с кодонами 289-304 уриказы бабуина.
Субклонирование последовательности уриказы под контролем промотора osmB
Ген уриказы субклонировали в экспрессирующий вектор, который содержит промотор osmB (следуя рекомендациям патента США № 5795776, включенного в настоящее описание в качестве ссылки в полном объеме). Этот вектор делает возможным индукцию экспрессии белка в ответ на высокое осмотическое давление или старение культуры. Экспрессирующая плазмида pMFOA-18 содержит промотор osmB, последовательность рибосомного участка связывания (rbs) и последовательность терминатора транскрипции (ter). Она придает устойчивость к пенициллину (AmpR) и экспрессирует рекомбинантную ацетилхолинэстеразу человека (AChE).
Субклонирование D3H-уриказа бабуина
Плазмиду pMFOA-18 расщепляли с помощью NcoI и BamHI и изолировали крупный фрагмент. Конструкцию pET-3d-D3H-бабуин расщепляли с помощью NcoI и BamHI и изолировали фрагмент длиной 960 п.о., который включает ген уриказы бабуина D3H. Эти два фрагмента лигировали для создания pMFOU18.
Экспрессирующая плазмида pMFXT133 содержит промотор osmB, rbs (deo оперон E. coli), ter (TrypA E. coli), полипептид ингибитора рекомбинантного фактора Ха (Fxal) и обеспечивает ген устойчивости к тетрациклину (TetR). Данный ген уриказы бабуина встраивали в эту плазмиду для обмена генами устойчивости к антибиотикам. Плазмиду pMFОU18 расщепляли с помощью NcoI, нагружали, затем ее расщепляли с помощью XhoI и изолировали фрагмент длиной 1030 п.о. Плазмиду pMFXT133 расщепляли с помощью NdeI, нагружали, затем ее расщепляли с помощью XhoI и изолировали крупный фрагмент. Эти два фрагмента лигировали для создания вектора, экспрессирующего уриказу бабуина, pURBA16.
Субклонирование уриказы химеры свинья-бабуин
Плазмиду pURBA16 расщепляли с помощью ApaI и AIwNI и изолировали фрагмент длиной 2320 п.о. Плазмиду pMFXT133 расщепляли с помощью NdeI, нагружали, затем ее расщепляли с помощью AlwNI и изолировали фрагмент длиной 620 п.о. Конструкцию pET-3d-PBC расщепляли с помощью XbaI, нагружали, затем ее расщепляли с помощью Apal и изолировали фрагмент длиной 710 п.о. Эти три фрагмента лигировали для создания pUR-PB, плазмиды, которая экспрессирует уриказу PBC под контролем промотора osmB и rbs, а также T7 rbs, который был получен из вектора pET-3d.
T7 rbs удаляли на дополнительном этапе. pUR-PB расщепляли с помощью NcoI, нагружали, затем ее расщепляли с помощью AlwNI и изолировали фрагмент длиной 3000 п.о. Плазмиду pMFXT133 расщепляли с помощью NdeI, нагружали, затем ее расщепляли с помощью AlwNI и изолировали фрагмент длиной 620 п.о. Эти два фрагмента лигировали для создания pDUR-PB, которая экспрессирует PBC под контролем промотора osmB.
Конструирование pOUR-PB-ΔNC
В кДНК уриказы были внесены некоторые изменения, что привело к значительному увеличению стабильности рекомбинантного фермента. Конструировали плазмиду pOUR-PBC-ΔNC, в которой были удалены и N-концевой пептид созревания, состоящий из шести остатков, и С-концевой три-пептид, которые действуют in vivo как пероксисомный нацеливающий сигнал. Это осуществляли, используя последовательность РВС в плазмиде pDUR-PB и специфические олигонуклеотидные праймеры, указанные в Таблице 2, с помощью ПЦР-амплификации.
Прямой
5' gcgcatATGACTTACAAAAAGAATGATGAGGTAGAG 3' (SEQ ID № 5)
Обратный
5' ccgtctagaTTAAGACAACTTCCTCTTGACTGTACCAGTAATTTTTCCGTATGG 3' (SEQ ID № 6)
Последовательности ферментов рестрикции, встроенные на концах данных праймеров, обозначены полужирным шрифтом, и некодирующие области обозначены строчными буквами в Таблице 2. NdeI является прямым, а XbaI является обратным. Обратный праймер также использовали для удаления внутреннего сайта рестрикции для NdeI с помощью введения точковой мутации (подчеркнута), которая не влияет на аминокислотную последовательность и, таким образом, облегчая субклонирование с использованием NdeI.
Фрагмент длиной 900 пар оснований, образованный в результате ПЦР-амплификации плазмиды pDUR-PB, расщепляли с помощью NdeI и XbaI и изолировали. Полученный фрагмент затем встраивали в deo экспрессирующую плазмиду pDB AST-RAT-N, которая несет промотор deo-P1P2 и rbs, полученные из E. Coli, и конститутивно экспрессирует предшественник рекомбинантного инсулина человека. Данную плазмиду расщепляли с помощью NdeI и XbaI, изолировали фрагмент длиной 4035 п.о. и лигировали в ПЦР-продукт PBC-уриказа. Полученную конструкцию, pDUR-PB-ΔNC, использовали для трансформации E. coli K-12 S[Φ]733 (F-cytR strA), который экспрессирует высокий уровень активной укороченной уриказы.
Последовательность двусторонне укороченной PBC-ΔNC также экспрессировали под контролем промотора osmB. Плазмиду pDUR-PB-ΔNC расщепляли с помощью AlwNI-Ndel и изолировали фрагмент длиной 3459 п.о. Плазмиду pMFXT133, описанную выше, расщепляли с помощью Ndel-AlwNI и изолировали фрагмент длиной 660 п.о. Данные фрагменты затем лигировали для создания pOUR-PB-ΔNC, которая была встроена в штамм W3110 F- E. coli K-12 и экспрессировала высокие уровни активной укороченной уриказы.
Конструирование экспрессирующей уриказу плазмиды pOUR-P-ΔN-ks-1
Эту плазмиду конструировали для повышения активности и стабильности данного рекомбинантного фермента. Уриказа Pig-KS-ΔN была укорочена только на N-конце (ΔN), где был удален N-концевой пептид созревания, состоящий из шести остатков, и содержала мутации S46T, R291K и T301S. В положении 46 остаток серина был заменен на треонин вследствие консервативной мутации, произошедшей в течение ПЦР-амплификации и клонирования. В положении 291 аргинин заменен на лизин, и в положении 301 серин вставлен вместо треонина. Обе происходят из последовательности уриказы бабуина. Перестройки R291K и T301S обозначены как KS и обсуждены выше. Дополнительный остаток лизина обеспечивает дополнительный потенциальный сайт пегилирования.
Для конструирования pOUR-P-ΔN-ks-1 (фиг.1) плазмиду pOUR-PB-ΔNC расщепляли с помощью ApaI-XbaI и изолировали фрагмент длиной 3873 п.о. Плазмиду pET-3d-PKS (конструкция показана на Фигуре 4) расщепляли с помощью ApaI-SpeI и изолировали фрагмент длиной 270 п.о. Расщепление с помощью SpeI оставляет 5'-удлиняющий сегмент CTAG, который был успешно лигирован с фрагментами ДНК, полученными с помощью XbaI. Эти два фрагмента лигировали для создания pOUR-P-ΔN-ks-1. После лигирования участки распознавания для SpeI и XbaI были утеряны (их сайт указан в круглых скобках на фиг.9). Конструкцию pOUR-P-ΔN-ks-1 встраивали в штамм W3110 F- E. coli K-12, прототрофный, ATCC # 27325. Полученная уриказа Pig-KS-ΔN, экспрессируемая под контролем промотора osmB, вырабатывалась с высокими уровнями рекомбинантного фермента, имеющего превосходящую активность и стабильность.
На фиг.1 представлена структура плазмиды pOUR-P-ΔN-ks-1. Номера после сайтов рестрикции указывают положение нуклеотида относительно сайта HaeII, обозначенный 1; сайты рестрикции, которые были утеряны в процессе клонирования, указаны в круглых скобках. Плазмида pOUR-P-ΔN-ks-1, кодирующая уриказу Pig-KS-ΔN, имеет длину 4143 пар оснований (п.о.) и содержит следующие элементы:
1. Фрагмент ДНК длиной 113 п.о., охватывающий область от нуклеотида номер 1 до сайта NdeI (в положении 113), который включает промотор osmB и рибосомный участок связывания (rbs).
2. Фрагмент ДНК длиной 932 п.о., охватывающий область от NdeI (в положении 113) до участка соединения SpeI/XbaI (в положении 1045), который включает: кодирующую область Pig-KS-ΔN длиной 900 п.о. (последовательность нуклеиновой кислоты белка укороченной на аминоконце уриказы свиньи, в которой аминокислоты в положения 291 и 301 заменены на лизин и серин, соответственно) и фланкирующую последовательность длиной 32 п.о., полученную из pCR™II, от TA участка клонирования в положении 3'-5' до участка рестрикции SpeI/XbaI.
3. Последовательность множественных участков клонирования (MCS) длиной 25 п.о. от участка соединения SpeI/XbaI (в положении 1045) до HindIII (в положении 1070).
4. Синтетический олигонуклеотид длиной 40 п.о., содержащий TrpA терминатор транскрипции (ter) с HindIII (в положении 1070) и AatII (в положении 1110) концами.
5. Фрагмент ДНК длиной 1519 п.о., охватывающий область от сайта AatII (в положении 1110) до сайта MscI/ScaI (в положении 2629) на pBR322, которая включает ген устойчивости к тетрациклину (TetR).
6. Фрагмент ДНК длиной 1514 п.о., охватывающий область от сайта SсaI (в положении 2629) до сайта HaeII (в положении 4143) на pBR322, которая включает точку инициации репликации ДНК.
На фиг.2 представлена ДНК и установленные аминокислотные последовательности уриказы Pig-KS-ΔN. На этой фигуре нумерация аминокислот соответствует последовательности полной уриказы свиньи. После инициирующего остатка метионина в последовательности уриказы свиньи вместо аспарагиновой кислоты встроен остаток треонина. Этот остаток треонина делает возможным удаление метионина с помощью бактериальной аминопептидазы. Разрыв в аминокислотной последовательности обозначает делетированный N-концевой пептид созревания. Обозначены сайты рестрикции, которые использовали на различных этапах субклонирования различных последовательностей уриказ (ApaI, NdeI, BamHI, EcoRI и SpeI). 3'-нетранслируемая последовательность, обозначенная строчными буквами, была получена из последовательности pCR™II. Стоп-кодон трансляции обозначен звездочкой.
На фиг.3 представлено выравнивание аминокислотных последовательностей различных последовательностей рекомбинантных уриказ. Верхний ряд представляет собой последовательность уриказы свиньи, которая включает полную аминокислотную последовательность. Второй ряд представляет собой последовательность двусторонне укороченной уриказы химеры свинья-бабуин (PBC-ΔNC). Третий ряд представляет собой последовательность уриказы Pig-KS-ΔN, которая укорочена только на N-конце и содержит мутацию S46T и аминокислотные замены R291K и T301S, обе затрагивающие карбоксиконец кодирующей последовательности уриказы, происходящей от бабуина. Звездочками обозначены положения, в которых существуют различия аминокислот в Pig-KS-ΔN по сравнению с опубликованной последовательностью уриказы свиньи; кружочками обозначены положения, в которых существуют различия аминокислот в Pig-KS-ΔN по сравнению с PBC-ΔN, химерой свинья-бабуин; и пунктирными линиями обозначена делеция аминокислот.
кДНК нативных уриказ бабуина, свиньи, уриказы кролика с мутацией Y97H и химеры свинья-бабуин (РВС) были сконструированы для клонирования в E. coli. Клоны, экспрессирующие высокие уровни вариантов уриказы, были конструированы и отобраны так, что все являлись W3110 F- E. coli, и экспрессия регулировалась посредством osmB. Изолировали плазмидные ДНК, определяли посредством секвенирования ДНК и рестрикционного анализа и клетки культивировали.
Конструирование укороченных уриказ, в том числе pig-ΔN и Pig-KS-ΔN, проводили посредством перекрестного лигирования между PBC-ΔNC и Pig-KS, после расщепления с помощью эндонуклеаз рестрикции ApaI и XbaI и ApaI плюс SpeI, соответственно. Можно сказать с достаточной уверенностью, что эти укороченные мутанты сохраняют активность, поскольку шесть N-концевых остатков, «пептид созревания» (1-2), и С-концевой три-пептид, «пероксисомный нацеливающий сигнал» (3-5), не обладают функциями, которые значительно действуют на ферментативную активность, и, возможно, что эти последовательности могут быть иммуногенными. Были отобраны клоны, экспрессирующие очень высокие уровни вариантов уриказ.
Пример 2. Трансформация экспрессирующей плазмиды в бактериальную клетку-хозяина
Экспрессирующая плазмида, pOUR-P-ΔN-ks-1, была встроена в штамм W3110 F- E. coli K-12. Бактериальные клетки подготавливали для трансформации включающей рост до середины логарифмической фазы роста в питательной среде Луриа (LB), затем клетки собирали посредством центрифугирования, промывали в холодной воде и суспендировали в 10% глицерине, в воде, при концентрации приблизительно 3×1010 клеток на мл. Хранили аликвоты данных клеток при -70°С. Плазмидную ДНК осаждали этиловым спиртом и растворяли в воде.
Бактериальные клетки и плазмидную ДНК смешивали, и проводили трансформацию методом высоковольтной электропорации с использованием Gene Pulser II фирмы BIO-RAD (Trevors et al (1992). Electrotransformation of bacteria by plasmid DNA, in Guide to Electroporation and Electrofusion (D. C. Chang, B. M. Chassy, J. A. Saunders and A. E. Sowers, eds.), pp. 265-290, Academic Press Inc., San Diego, Hanahan et al (1991) Meth. Enzymol., 204, 63-113). Трансформированные клетки суспендировали в среде SOC (2% триптон, 0,5% дрожжевой экстракт, 10 мM NaCl, 2,5 мM KCl, 10 мM MgCl2, 10 мM MgSO4, 20 мM глюкоза), инкубировали при 37°C в течение 1 часа и отбирали по устойчивости к тетрациклину. Был отобран высокоэкспрессирующий клон.
Пример 3. Получение рекомбинантной уриказы
Бактерии типа трансформированных (смотри выше) культивировали в среде, содержащей глюкозу; значение pH поддерживали на уровне 7,2±0,2, приблизительно при 37°C.
На последних 5-6 часах культивирования данная среда была дополнена KCl до конечной концентрации 0,3 M. Культивирование продолжали, чтобы обеспечить возможность накопления уриказы.
Рекомбинантная уриказа накапливалась в бактериальных клетках в виде нерастворимого осадка, сходного с внутриклеточными тельцами (IB). Данную клеточную суспензию отмывали посредством центрифугирования и суспендировали в 50 мМ Трис буфере, pH 8,0 и 10 мM ЭДТА и доводили до конечного объема, разводя исходную сухую клеточную массу приблизительно в 40 раз.
IB, содержащие рекомбинантную уриказу, изолировали посредством центрифугирования после разрушения клеточных стенок с использованием лизоцима и высокого давления. Обработку с помощью лизоцима (2000-3000 единиц/мл) проводили в течение 16-20 часов при рН 8,0 и 7±3°С, при перемешивании. Осадок отмывали водой и хранили при -20°С до использования.
Эти обогащенные IB были дополнительно обработаны после суспендирования в 50 мМ буфере NaHCO3, pH 10,3±0,1. Данную суспензию инкубировали в течение ночи, при комнатной температуре, для обеспечения солюбилизации уриказы, извлеченной из IB, и затем очищали посредством центрифугирования.
Уриказу дополнительно очищали в течение нескольких этапов хроматографирования. Первоначально хроматографию проводили на колонке Q-Sepharose FF. Нагруженную колонку отмывали бикарбонатным буфером, содержащим 150 мM NaCl, и уриказу элюировали с помощью бикарбонатного буфера, содержащего 250 мM NaCl. Затем использовали смолу Ксантин-агароза (Sigma) для удаления незначительных примесей из препарата уриказы. Элюат с колонки Q-Sepharose FF разбавляли с помощью 50 мM глицинового буфера, pH 10,3±0,1, до концентрации белка приблизительно 0,25 мг/мл и нагружали. Данную колонку отмывали с помощью бикарбонатного буфера, pH 10,3±0,1, содержащего 100 мM NaCl, и уриказу элюировали с использованием того же буфера, дополненного 60 мкМ ксантина. На этом этапе уриказа была повторно очищена посредством хроматографии на Q-Sepharose для удаления агрегированных форм.
Чистота каждого препарата уриказы составляет более 95%, что определено посредством гель-хроматографии. Используя колонку Superdex 200, менее чем 0,5% агрегированных форм выявлено в каждом препарате.
В таблице 3 подведен итог очистки уриказы Pig-KSΔN из IB, полученных из 2 л среды для культивирования.
Пример 4. Свойства рекомбинантных уриказ
SDS-PAGE
Анализ вариантов высокоочищенной уриказы в SDS-PAGE (фиг.4) выявил довольно характерную картину. Данные образцы хранили при 4°С, в карбонатном буфере, рН 10,3, вплоть до нескольких месяцев. Полноразмерные варианты, Pig, Pig-KS и PBC, показывают накопление двух основных продукта деградации, имеющих молекулярную массу около 20 и 15 кД. Это наблюдение показывает, что, по меньшей мере, один участок расщепляет молекулу субъединицы уриказы. Другой характер деградации выявлен у клонов, укороченных на аминоконце, причем в уриказе кролика, но в меньших количествах. Аминоконец уриказы кролика напоминает таковой укороченных клонов. Были определены амино-терминальные последовательности фрагментов уриказы, полученных в процессе очистки и хранения.
Определение последовательности пептида
Определение последовательности N-конца большого количества препаратов уриказы проведено с помощью метода расщепления белков по Эдману. Провели десять циклов. Рекомбинантная уриказа свиньи (полноразмерный клон) образовывала большое изобилие фрагментов деградации по сравнению с Pig-KS-ΔN. Установленные сайты расщепления, приводящие к образованию фрагментов деградации, следующие:
1) главный сайт в положении 168, имеющий последовательность:
-QSG↓FEGFI-
2) второстепенный сайт в положении 142, имеющий последовательность:
-IRN↓GPPVI-
Вышеуказанные последовательности не предполагают никакого известного протеолитического расщепления. Тем не менее, расщепление может быть обусловлено либо протеолизом, либо какой-либо химической реакцией. Уриказы, укороченные с аминоконца, на удивление более стабильны, чем уриказы, неукороченные с аминоконца. PBC-ΔNC также имеет стабильность, схожую с молекулами другой ΔN и меньшую, по сравнению с РВС, неукороченной с аминоконца.
Активность
Активность уриказы определяли посредством УФ-способа. Скорость ферментативной реакции определяли, измеряя снижение поглощения при 292 нм, которое обусловлено окислением мочевой кислоты до аллантоина. Одна единица активности определена как количество уриказы, необходимое для окисления одного мкмоль мочевой кислоты в минуту, при 25°С, при указанных условиях. Активность уриказы выражена в единицах активности на мг белка (Ед/мг).
Коэффициент экстинкции 1 мМ мочевой кислоты при 292 нм составляет 12,2 мМ-1см-1. Таким образом, окисление 1 мкмоль мочевой кислоты на мл реакционной смеси приводит к снижению поглощения 12,2 мА292. Изменение поглощения с течением времени (ΔA292 в минуту) получено из линейного участка данной кривой.
Концентрацию белка определяли, используя модифицированный метод Брэдфорда (Macart and Gerbaut (1982) Clin Chim Acta 122: 93-101). Специфическую активность (активность) уриказы рассчитывали, деля данную активность в Ед/мл на концентрацию белка в мг/мл. Эффекты ферментативной активности различных рекомбинантных уриказ сведены в таблице 4. Эффекты коммерческих препаратов включены в эту таблицу в качестве эталонных значений. Исходя из этих результатов очевидно, что укорочение белков уриказ не имеет значительного влияния на их ферментативную активность.
Пояснения к таблице 4:
(1) концентрацию белка определяли, измеряя поглощение при 278 нм, используя коэффициент экстинкции 11,3 для 10 мг/мл раствора уриказы (Mahler, 1963).
(2) 1 единица активности уриказы определена как количество фермента, который окисляет 1 мкмоль мочевой кислоты до аллантоина в минуту при 25°С.
(3) значения специфической активности получены из графика Лайнуивера-Берка, при концентрации субстрата, эквивалентной 60 мкМ.
(4) реакционные смеси состояли из различных комбинаций следующих исходных растворов:
100 мМ натриево-боратный буфер, рН 9,2;
300 мкM мочевая кислота в 50 мM натриево-боратном буфере, pH 9,2;
1 мг/мл BSA в 50 мM натриево-боратном буфере, pH 9,2.
(5) Kcat высчитывали, деля Vmax (рассчитан по соответствующему графику Лайнуивера-Берка) на концентрацию уриказы в реакционной смеси (выражена в моль-эквивалентах, исходя из молекулярной массы тетрамера уриказ).
Пример 5. Конъюгация уриказы с m-PEG (пегилирование)
Уриказу Pig-KS-ΔN конъюгировали, используя m-PEG-NPC (монометокси-поли(этиленгликоль)-нитрофенил карбонат). Были определены условия, приводящие к образованию 2-12 цепей 5, 10, или 20 кД PEG на субъединицу уриказы. Постепенно к белковому раствору добавляли m-PEG-NPC. После окончания добавления PEG реакционную смесь уриказа/m-PEG-NPC инкубировали при 2-8°C в течение 16-18 часов, до тех пор, пока максимальное количество свободных цепей m-PEG не свяжутся с уриказой.
Количество цепей PEG на мономер PEG-уриказа определяли посредством супероза 6 гель-хроматографии (SEC), используя стандарты PEG и уриказы. Количество связанных цепей PEG на субъединицу вычисляли по следующему уравнению:
цепи/субъединица=
Концентрацию PEG и белковых молекул в образце PEG-уриказы определяли посредством (SEC), используя ультрафиолетовый (УФ) детектор и детектор показателя преломления (RI), расположенные последовательно (как сконструировано Kunitani, et al., 1991). Получили три калибровочные кривые: калибровочная кривая для белка (поглощение измерено при 220 нм); калибровочная кривая для белка (измерено посредством RI); и калибровочная кривая для PEG (измерено посредством RI). Затем анализировали образцы PEG-уриказа, используя ту же систему. Полученные значения площадей пиков УФ и RI для экспериментальных образцов использовали для вычисления концентраций PEG и белка относительно калибровочных кривых. Индекс 3,42 представляет собой соотношение между молекулярной массой мономера уриказы (34192 Дальтона) и молекулярной массой 10 кД PEG.
Присоединенный PEG улучшает растворимость уриказы в растворах, имеющих физиологические значения рН. В таблице 5 представлены признаки вариабельности между сериями пегилированного продукта уриказы Pig-KS-ΔN. В большинстве случаев существует обратная зависимость между числом присоединенных цепей PEG и сохраненной специфической активностью (SA) данного фермента.
Пример 6. Пегилирование уриказы с помощью 1000 Д и 100000 Д PEG
Уриказу Pig-KS-ΔN конъюгировали с использованием 1000 Д и 100000 Д m-PEG-NPC, как описано в примере 5. Использовали условия, приводящие к присоединению 2-11 цепей PEG на субъединицу уриказы. После окончания добавления PEG реакционную смесь уриказа/m-PEG-NPC инкубировали при 2-8°С в течение 16-18 часов до тех пор, пока максимальное количество свободных цепей m-PEG не свяжется с уриказой.
Количество цепей PEG на мономер PEG-уриказа определяли, как описано выше.
Присоединенный PEG улучшает растворимость уриказы в растворах, имеющих физиологические значения рН.
Пример 7. Фармакокинетика уриказы Pig-KS-ΔN, конъюгированной с PEG
Были проведены биологические эксперименты для определения оптимальной степени и величины пегилирования, необходимых для обеспечения терапевтической пользы.
При изучении фармакокинетики на крысах использование в/в инъекций неизмененной уриказы 0,4 мг (2 Ед) на кг массы тела, введенных в день 1 и день 8, привело к времени полужизни в кровотоке приблизительно 10 минут. Тем не менее, изучения у крыс почечного клиренса 2-11×10 кД PEG-Pig-KS-ΔN уриказы, после целых 9 еженедельных инъекций, показали, что клиренс не зависел от числа цепей PEG (в пределах этого диапазона) и оставался относительно постоянным на протяжении всего периода изучения (см. таблицу 6; время полужизни приблизительно 30 часов). Различия между неделями находятся в пределах экспериментальной ошибки. Такая же картина очевидна после девяти инъекций конъюгатов 10×5 кД PEG- и 10×20 кД PEG-уриказа. Эти результаты показали, что независимо от степени пегилирования уриказы в этом диапазоне наблюдали схожие биологические эффекты в экспериментальной модели на крысах.
Примечания к таблице 6: результаты представлены в часах ± стандартная средняя ошибка. Числа в круглых скобках обозначают количество изученных животных.
Крысы еженедельно получали инъекции 0,4 мг на кг массы тела уриказы Pig-KS-ΔN, модифицированной как указано в таблице. Изначально в каждой группе было по 15 крыс, которым поочередно проводили кровопускание в подгруппах по 5 особей. Несколько крыс погибло во время исследования вследствие анестезии. Время полужизни определяли, измеряя активность уриказы (колориметрический анализ) в образцах плазмы, собранных через 5 минут и 6, 24 и 48 часов после инъекции.
В таблице 5 описаны серии пегилированных уриказ, используемых в данном исследовании.
Исследования биодоступности с использованием 6×5 кД PEG- Pig-KS-ΔN уриказы у кроликов показали, что после первой инъекции время полужизни в кровотоке составляет 98,2±1,8 часа (в/в), а биодоступность после в/м и подкожных (п/к) инъекций составляла 71% и 52%, соответственно. Тем не менее, значительные титры антител к уриказе были выявлены после второй в/м и п/к инъекции у всех кроликов, и клиренс был ускорен после последующих инъекций. Инъекции крысам того же конъюгата привели к времени полужизни, равному 26±1,6 часа (в/в), и биодоступность после в/м и п/к инъекций составляла 33% и 22%, соответственно.
Исследования на крысах 9x10 кД PEG-Pig-KS-ΔN уриказы показали, что время полужизни в кровотоке после первой инъекции составляло 42,4 часа (в/в), а биодоступность после в/м и п/к инъекций составляла 28,9% и 14,5%, соответственно (см. фиг.5 и таблицу 7). После четвертой инъекции время полужизни в кровотоке составляло 32,1±2,4 часа, и биодоступность после в/м и п/к инъекций составляла 26,1% и 14,9%, соответственно.
Подобные фармакокинетические исследования на кроликах с использованием 9×10 кД PEG-Pig-KS-ΔN уриказы показали, что не обнаружено ускорение клиренса после инъекции этого конъюгата (проводили 4 двухнедельные инъекции). У этих животных время полужизни в кровотоке после первой инъекции составляло 88,5 часов (в/в), и биодоступность после в/м и п/к инъекций составляла 98,3% и 84,4%, соответственно (см. фиг.6 и таблицу 7). После четвертой инъекции время полужизни в кровотоке составляло 141,1±15,4 часа, и биодоступность после в/м и п/к инъекций составляла 85% и 83%, соответственно.
Подобные исследования с использованием 9×10 кД PEG-Pig-KS-ΔN провели для оценки биодоступности у биглей (2 кобеля и 2 суки в каждой группе). Время полужизни в кровотоке, равное 70±11,7 часов, было зарегистрировано после первой в/в инъекции, биодоступность после в/м и п/к инъекций составляла 69,5% и 50,4%, соответственно (см. фиг.7 и таблицу 7).
Исследования 9×10 кД PEG-Pig-KS-ΔN препаратов провели на свиньях. Использовали трех животных на группу для применения посредством в/в, п/к и в/м пути введения. Время полужизни в кровотоке, равное 178±24 часа, было зарегистрировано после первой в/в инъекции, биодоступность после в/м и п/к инъекций составляла 71,6% и 76,8%, соответственно (см. фиг.8 и таблицу 7).
Исследования поглощения, распределения, метаболизма и выведения (ADME) проводили после мечения йодом 9x10 кД PEG-Pig-KS-ΔN уриказы, используя способ Болтона-Хантера с 125I. Данные меченые конъюгаты были введены в 7 группах по 4 крысы каждая (2 самца и 2 самки). Распределение радиоактивности анализировали через 1 час и каждые 24 часа в течение 7 дней (за исключением дня 5). Каждую группу, в свою очередь, умерщвляли, выделяли различные органы и анализировали. Животных из седьмой группы содержали в метаболической клетке, из которой собирали всю мочу и фекалии. Распределение вещества в организме животного оценивали, измеряя общую радиоактивность в каждом органе и во фракциях (почки, печень, легкие и селезенка), доступных для осаждения с помощью ТХУ (то есть связанный белок, приведенный к размеру органа). Среди выделенных органов ни один не имел более высокую радиоактивность, чем другие, таким образом, не обнаружили значительного накопления, например, в печени или почках. 70% радиоактивности вывелось через на 7 день.
Пример 8. Результаты клинического испытания
Рандомизированное, открытое, мультицентровое исследование в параллельных группах провели для оценки воздействия на соль мочевой кислоты и фармакокинетики, и безопасных режимов применения pEG-уриказы (Puricase®, Savient Pharmaceuticals) у людей, имеющих гиперурикемию и тяжелую подагру, которые не реагировали или не переносили стандартную терапию. Средняя продолжительность заболевания составляла 14 лет, и 70 процентов из обследованных имели один или несколько подагрических узлов.
В данном исследовании 41 больной (средний возраст составлял 58,1 год) были случайным образом отобраны для получения в течение 12 недель внутривенных инъекций PEG-уриказы в одном из четырех режимов дозирования: 4 мг каждые две недели (7 пациентов); 8 мг каждые две недели (8 пациентов); 8 мг каждые четыре недели (13 пациентов) или 12 мг каждые четыре недели (13 пациентов). Активность уриказы и уровни соли мочевой кислоты в плазме крови определяли через определенные промежутки времени. Фармакокинетические параметры, средняя концентрация соли мочевой кислоты в плазме крови и процент времени, в течение которого концентрация соли мочевой кислоты в плазме крови составляла менее или была равной 6 мг/дл, были получены в ходе анализа активностей уриказы и уровней соли мочевой кислоты.
Пациенты, которые получали 8 мг PEG-уриказы каждые две недели, имели наибольшее снижение PUA до уровней ниже 6 мг/дл в течение 92 процентов времени лечения (концентрация соли мочевой кислоты в плазме крови до лечения 9,1 мг/дл против средней концентрации соли мочевой кислоты в плазме крови 1,4 мг/дл через 12 недель).
Существенное и устойчивое снижение уровней соли мочевой кислоты в плазме крови также наблюдали в группах, получавших другие режимы дозировки PEG-уриказы: PUA ниже 6 мг/мл в течение 86 процентов времени лечения в группе, получавшей 8 мг каждые четыре недели (концентрация соли мочевой кислоты в плазме крови до лечения 9,1 мг/дл против средней концентрации соли мочевой кислоты в плазме крови 2,6 мг/дл через 12 недель); PUA ниже 6 мг/мл в течение 84 процента времени лечения в группе, получавшей 12 мг каждые четыре недели (концентрация соли мочевой кислоты в плазме крови до лечения 8,5 мг/дл против средней концентрации соли мочевой кислоты в плазме крови 2,6 мг/дл через 12 недель); и PUA ниже 6 мг/мл в течение 73 процента времени лечения в группе, получавшей 4 мг каждые две недели (концентрация соли мочевой кислоты в плазме крови до лечения 7,6 мг/дл против средней концентрации соли мочевой кислоты в плазме крови 4,2 мг/дл через 12 недель).
Максимальный процент снижения концентрации мочевой кислоты в плазме крови от исходного уровня в течение первых 24 часов применения PEG-уриказы составлял 72% для пациентов, получавших 4 мг/2 недели (p равно 0,0002); 94% для пациентов, получавших 8 мг/2 недели (p меньше, чем 0,0001); 87% для пациентов, получавших 8 мг/4 недели (p меньше, чем 0,0001); и 93% для пациентов, получавших 12 мг/4 недель (p меньше, чем 0,0001).
Процент снижения уровня мочевой кислоты в плазме крови от исходного уровня в течение 12-недельного периода лечения составил 38% у пациентов, получавших 4 мг/2 недели (р равно 0,0002); 86% у пациентов, получавших 8 мг/2 недели (р меньше, чем 0,0001); 58% у пациентов, получавших 8 мг/4 недели (р равно 0,0003); и 67% у пациентов, получавших 12 мг/4 недели (р меньше, чем 0,0001).
Как ни удивительно, но некоторые пациенты, получавшие PEG-уриказу, испытывали неблагоприятное действие, связанное с вливанием, а именно инфузионную реакцию. Эти реакции развились в 14% всех вливаний.
Все процитированные ссылки включены в настоящее описание посредством ссылки в полном их объеме и для всех целей в той же мере, как каждая индивидуальная публикация или патент, или патентная заявка была бы указана включенной в качестве ссылки в полном объеме для всех целей.
Можно осуществить множество модификаций и изменений настоящего изобретения, не отступая от его сущности и объема, что будет очевидно специалисту в уровне техники. Конкретные варианты осуществления, описанные здесь, предлагаются только в качестве примера, и данное изобретение ограничено только терминами прикрепленной формулы изобретения наряду с полным диапазоном эквивалентов, на которые дает право формула изобретения.












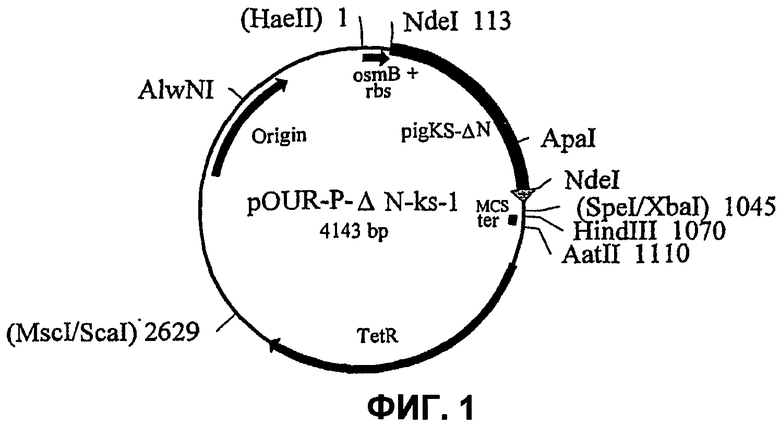


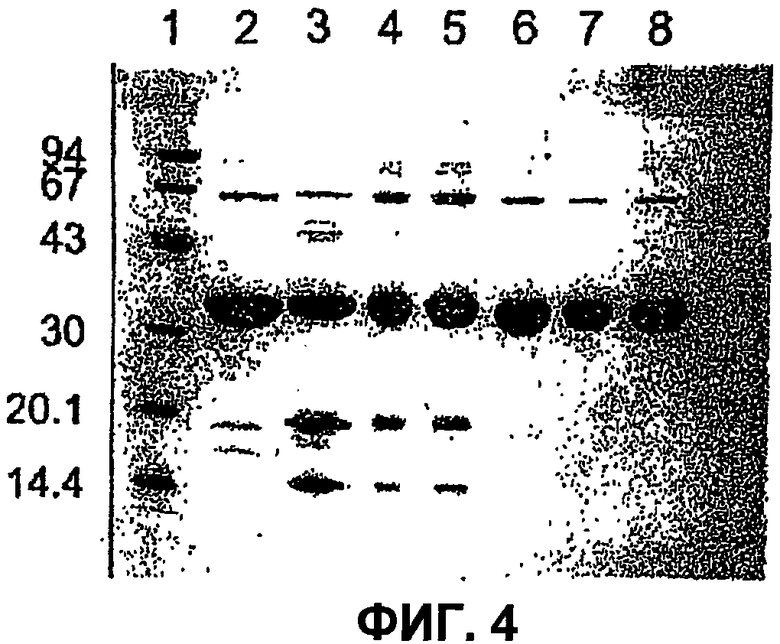
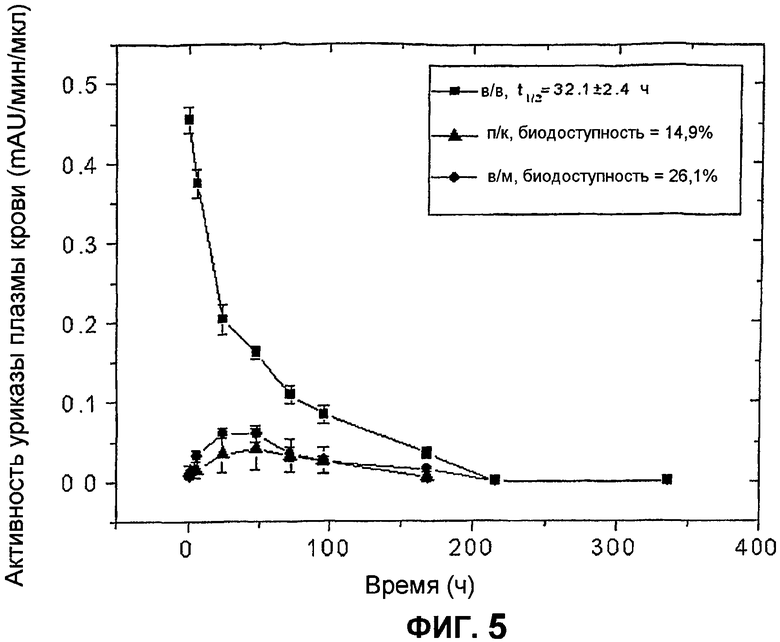
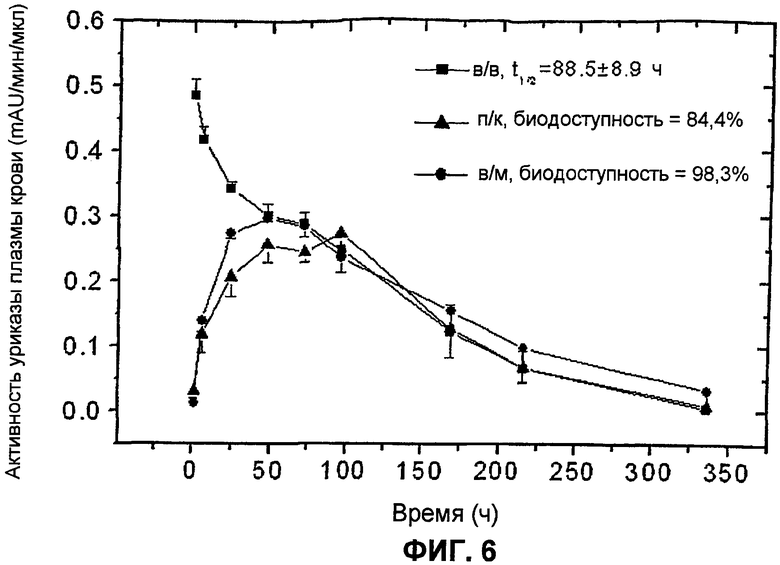
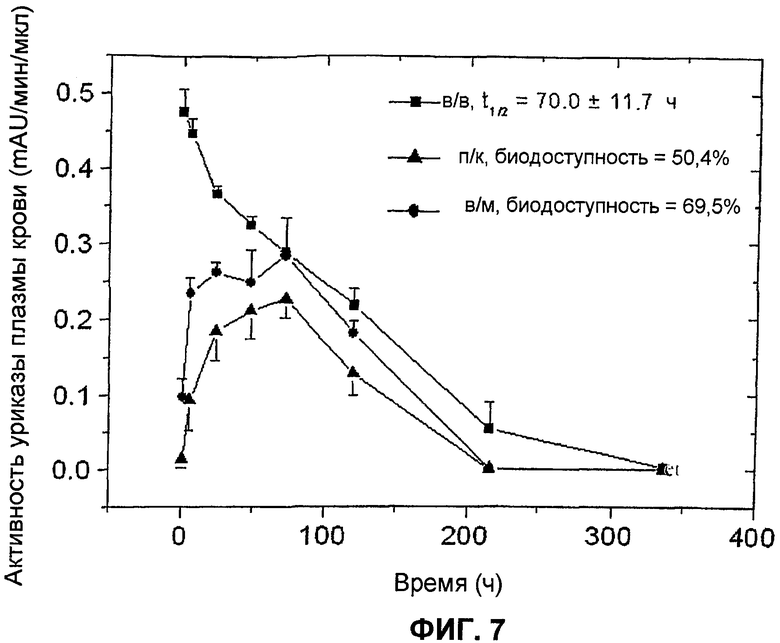
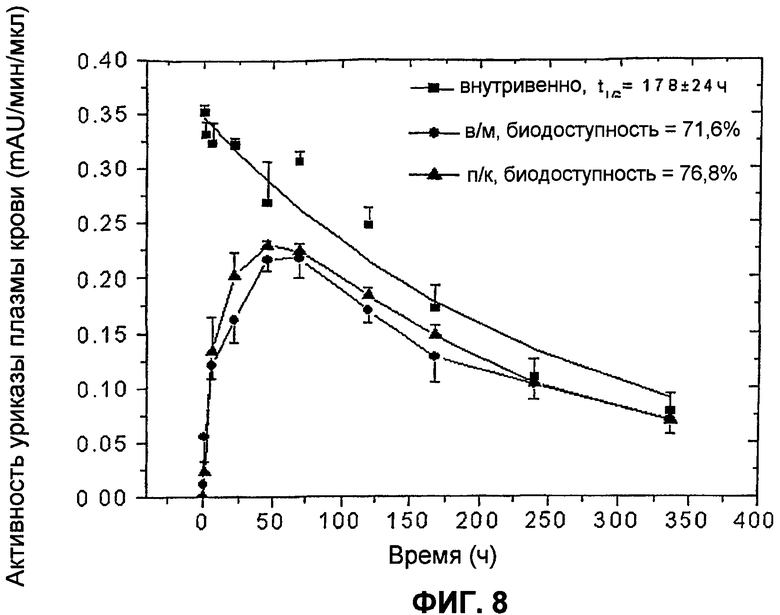
Настоящее изобретение относится к области генетической и белковой инженерии и может быть использовано в медико-биологической промышленности при изготовлении лекарственных препаратов для лечения патологических состояний, связанных с гиперурикемией. Предложен активный рекомбинантный белок уриказы, который представляет собой укороченную с N-конца на 6 аминокислотных остатков мутантную форму уриказы млекопитающего, которая содержит замены S46T, D7T, R291K и T301S. Укороченная уриказа по изобретению характеризуется пониженным уровнем иммуногенности и увеличенной структурной стабильностью. 5 з.п. ф-лы, 8 ил., 7 табл.
1. Изолированная укороченная уриказа млекопитающего, которая укорочена с аминоконца на 6 аминокислот и дополнительно содержит аминокислотную замену на треонин в положении 46 (S46T), аминокислотную замену на треонин в положении 7 (D7T), аминокислотную замену на лизин в положении 291 (R291K) и аминокислотную замену на серин в положении 301 (T301S), где указанное укорочение и аминокислотная замена относятся к неукороченной уриказе свиньи, имеющей аминокислотную последовательность SEQ ID NO:11.
2. Изолированная укороченная уриказа млекопитающего по п.1, дополнительно содержащая аминоконцевую аминокислоту, где данной аминоконцевой аминокислотой является аланин, глицин, пролин, серин или треонин.
3. Изолированная укороченная уриказа млекопитающего по п.2, где аминоконцевой аминокислотой является треонин.
4. Изолированная укороченная уриказа млекопитающего по п.1, состоящая из аминокислотной последовательности SEQ ID NO:8.
5. Изолированная укороченная уриказа млекопитающего по п.4, дополнительно содержащая N-концевую аминокислоту, где N-концевой аминокислотой является метионин.
6. Изолированная укороченная уриказа млекопитающего по п.5, состоящая из аминокислотной последовательности SEQ ID NO:7.
| WO 00/0007629 А2, 17.02.2000 | |||
| RU 2001103131 A, 10.04.2003 | |||
| TSUNASAWA ET AL., J.Biol | |||
| Chem., 1985, v.260, 5382-5391. |
Авторы
Даты
2012-05-20—Публикация
2006-04-11—Подача