Данное изобретение относится к производным 5-(гидроксиметилен- и аминометилен)пиримидина, обладающим ингибирующими репликацию ВИЧ (вирус иммунодефицита человека) свойствами, к их получению и к фармацевтическим композициям, содержащим эти соединения.
Резистентность вируса ВИЧ против доступных в настоящее время лекарственных средств для лечения ВИЧ продолжает оставаться главной причиной неблагоприятного исхода терапии. Это привело к введению комбинированной терапии из двух или более анти-ВИЧ-агентов, обычно имеющих различный профиль активности. Значительный прогресс сделан при введении HAART-терапии (высокоактивная антиретровирусная терапия), которая в результате приводит к значительному снижению заболеваемости и смертности у популяций пациентов с ВИЧ, подвергаемых лечению посредством этой терапии. HAART-терапия включает различные комбинации нуклеозидных ингибиторов обратной транскриптазы (NRTI), ненуклеозидных ингибиторов обратной транскриптазы (NNRTI) и ингибиторов протеазы (PI). Но даже эти множественные лекарственные терапии не полностью устраняют ВИЧ и длительное лечение часто приводит к множественной лекарственной устойчивости. Во многих случаях резистентный вирус переносится на вновь инфицированных индивидуумов, приводя в результате к ограниченным вариантам терапии для этих не подвергающихся воздействию лекарственных средств пациентов.
Следовательно, сохраняется необходимость в новых комбинациях активных ингредиентов, которые эффективны против ВИЧ. Новые типы анти-ВИЧ-агентов, различающихся по химической структуре и профилю активности, пригодны в новых видах комбинированной терапии. Обнаружение таких активных ингредиентов, следовательно, является крайне желательной для достижения целью.
Настоящее изобретение относится к получению конкретных новых серий производных пиримидина, обладающих ингибирующими репликацию ВИЧ свойствами. В WO 99/50250, WO 00/27825 и WO 01/85700 раскрываются некоторые замещенные аминопиримидины, обладающие ингибирующими репликацию ВИЧ свойствами.
Соединения согласно данному изобретению отличаются от соединений известного уровня техники их химической структурой, а также по их фармакологическому профилю. Найдено, что введение определенных заместителей в положение 5 конкретно замещенных пиримидинов приводит, в результате, к соединениям, не только благоприятно воздействующим с точки зрения их способности к ингибированию репликации вируса иммунодефицита человека (ВИЧ), но также к их улучшенной способности ингибировать репликацию мутантных штаммов, в особенности штаммов, которые становятся резистентными по отношению к одному или более известным NNRTI-лекарственным средствам, причем эти штаммы относятся к ВИЧ-штаммам, резистентным по отношению к лекарственным или множественным лекарственным средствам.
Таким образом, в одном аспекте настоящее изобретение относится к соединениям формулы (I):
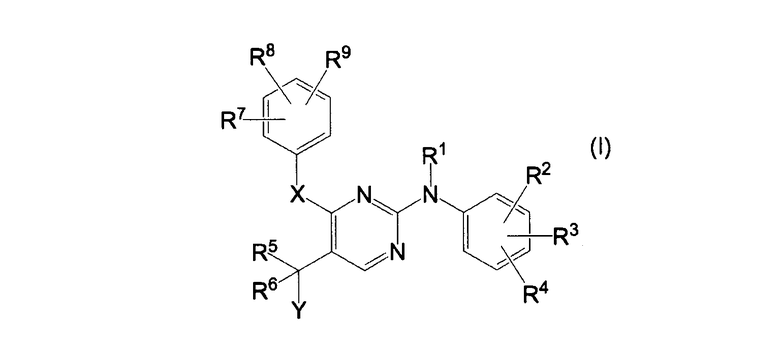
их стереохимически изомерным формам, их фармацевтически приемлемым аддитивным солям, их фармацевтически приемлемым гидратам или сольватам, их N-оксидам, где
каждый R 1 независимо означает водород; арил; формил; С1-6-алкилкарбонил; С1-6-алкил; С1-6-алкилоксикарбонил;
R 2, R 3, R 7 и R 8 независимо означают водород; гидрокси; галоген; С3-7-циклоалкил; С1-6-алкилокси; карбоксил; С1-6-алкилоксикарбонил; циано; нитро; амино; моно- или ди(С1-6-алкил)амино; полигалоген-С1-6-алкил; полигалоген-С1-6-алкилокси; -С(=О)R10; С1-6-алкил, необязательно замещенный галогеном, циано или -С(=О)R10; С2-6-алкенил, необязательно замещенный галогеном, циано или -С(=О)R10; С2-6-алкинил, необязательно замещенный галогеном, циано или -С(=О)R10;
R 4 и R 9 независимо означают гидрокси; галоген; С3-7-циклоалкил; С1-6-алкилокси; карбоксил; С1-6-алкилоксикарбонил; формил; циано; нитро; амино; моно- или ди(С1-6-алкил)амино; полигалоген-С1-6-алкил; полигалоген-С1-6-алкилокси; -С(=О)R10; циано; -S(=O)rR10; -NH-S(=O)rR10; -NHC(=O)H; -C(=O)NHNH2; -NHC(=O)R10; Het; -Y-Het; С1-12-алкил, необязательно замещенный галогеном, циано, амино, моно- или ди(С1-6-алкил)амино, -С(=О)R10, Het или С1-6-алкилокси; С2-12-алкенил, необязательно замещенный галогеном, циано, амино, моно- или ди(С1-6-алкил)амино, -С(=О)R10, Het или С1-6-алкилокси; С2-12-алкинил, необязательно замещенный галогеном, циано, амино, моно- или ди(С1-6-алкил)амино, -С(=О)R10, Het или С1-6-алкилокси;
R 5 означает С1-6-алкил, необязательно замещенный Ar или Het; С2-6-алкенил, необязательно замещенный Ar или Het; С2-6-алкинил, необязательно замещенный Ar или Het; С3-7-циклоалкил; Ar; Het;
R 6 означает водород, С1-6-алкил, Het;
Y означает -OR11, -NR12R13;
каждый R 10 независимо означает С1-6-алкил, амино, моно- или ди(С1-6-алкил)амино или полигалоген-С1-6-алкил;
R 11 означает водород или С1-6-алкил, необязательно замещенный гидрокси, С1-6-алкилокси, фенилом или пиридилом;
R 12 означает водород или С1-6-алкил;
R 13 означает водород или С1-6-алкил; или R 12 и R 13 вместе с атомом азота, заместителями которого они являются, образуют пирролидинил; пиперидинил; морфолинил; пиперазинил; пиперазинил, необязательно замещенный С1-6-алкилом или С1-6-алкилкарбонилом; имидазолил;
Х означает -NR1-, -O-, -C(=O)-, -CH2-, -CHOH-, -S-, -S(=O)r-;
каждый Y независимо означает -NR1-, -O-, -C(=O)-, -S-, -S(=O)r-;
каждый r независимо означает 1 или 2;
Het означает 5- или 6-членный полностью ненасыщенный цикл, где один, два, три или четыре члена цикла являются гетероатомами, причем каждый независимо выбирают из азота, кислорода и серы, и где остающиеся члены цикла являются атомами углерода; и где, возможно, любой член гетероцикла с гетероатомом азота может быть необязательно замещен С1-6-алкилом; причем 5- или 6-членный цикл может быть необязательно аннелирован с бензольным, тиофеновым или пиридиновым циклом; и где любой атом углерода цикла, включая любой атом углерода необязательно аннелированного бензольного, тиофенового или пиридинового цикла, каждый независимо, необязательно может быть замещен заместителем, выбираемым из группы, состоящей из галогена, гидрокси, меркапто, циано, С1-6-алкила, гидрокси-С1-4-алкила, карбокси-С1-4-алкила, С1-4-алкилокси-С1-4-алкила, С1-4-алкилоксикарбонил-С1-4-алкила, циано-С1-4-алкила, моно- и ди(С1-4-алкил)амино-С1-4-алкила, Het1-С1-4-алкила, арил-С1-4-алкила, полигалоген-С1-4-алкила, С3-7-циклоалкила, С2-6-алкенила, С2-6-алкинила, арил-С2-4-алкенила, С1-4-алкилокси, -ОСОNH2, полигалоген-С1-4-алкилокси, арилокси, амино, моно- и ди-С1-4-алкиламино, пирролидинила, пиперидинила, морфолинила, пиперазинила, 4-С1-6-алкилпиперазинила, С1-4-алкилкарбониламино, формила, С1-4-алкилкарбонила, С1-4-алкилоксикарбонила, аминокарбонила, моно- и ди-С1-4-алкиламинокарбонила, арила, Het1;
Het 1 означает пиридил, тиенил, фуранил, оксазолил, изоксазолил, имидазолил, пиразолил, тиазолил, тиадиазолил, оксадиазолил, хинолинил, бензотиенил, бензофуранил; причем каждый может быть необязательно замещен одним или двумя С1-4-алкилами;
каждый арил независимо означает фенил или фенил, замещенный одним, двумя, тремя, четырьмя или пятью заместителями, причем каждый независимо выбирают из группы, состоящей из галогена, гидрокси, меркапто, С1-6-алкила, С2-6-алкенила, С2-6-алкинила, гидрокси-С1-6-алкила, амино-С1-6-алкила, моно- и ди(С1-6-алкил)амино-С1-6-алкила, С1-6-алкилкарбонила, С3-7-циклоалкила, С1-6-алкилокси, фенил-С1-6-алкилокси, С1-6-алкилоксикарбонила, аминосульфонила, С1-6-алкилтио, циано, нитро, полигалоген-С1-6-алкила, полигалоген-С1-6-алкилокси, аминокарбонила, фенила, Het и -Y-Het.
Het представляет собой полностью ненасыщенный цикл, означающий, что цикл содержит максимальное количество двойных связей. Один тип циклов Het представляет собой ароматические гетероциклы. В одном воплощении Het в полном виде, т.е. включающий необязательно аннелированный бензольный, тиофеновый или пиридиновый цикл, может быть необязательно замещен одним, двумя или тремя заместителями, указанными выше или в дальнейшем. В частности, Het содержит не более чем два атома кислорода или серы в цикле, в особенности не более чем один атом кислорода или серы в цикле.
В одном воплощении каждый из Het независимо означает пиридил, тиенил, фуранил, оксазолил, изоксазолил, имидазолил, пиразолил, тиазолил, тиадиазолил, оксадиазолил, хинолинил, бензотиенил, бензофуранил, бензоксазолил, бензотиазолил, имидазотиазолил; каждый из которых может быть необязательно замещен одним или двумя заместителями, независимо выбираемыми из С1-6-алкила; галогена; гидрокси; циано; С1-6-алкилокси; С2-12-алкенила, замещенного галогеном, гидрокси или циано.
Как используется выше или в дальнейшем, С1-4-алкил, в качестве группы или части группы, представляет собой насыщенные углеводородные радикалы с линейной или разветвленной цепью, имеющие 1-4 атома углерода, такие как метил, этил, 1-пропил, 2-пропил, 1-бутил, 2-бутил, 2-метилпропил, трет-бутил; С1-6-алкил, в качестве группы или части группы, представляет собой насыщенные углеводородные радикалы с линейной или разветвленной цепью, имеющие 1-6 атомов углерода, такие как группа, указанная в случае С1-4-алкила, и 1-пентил, 2-пентил, 1-гексил, 2-гексил, 3-гексил, 2-метилбутил, 3-метилпентил и т.п.; С1-2-алкил означает метил или этил; С3-7-циклоалкил означает циклопропил, циклобутил, циклопентил, циклогексил и циклогептил. Предпочтительными среди С1-6-алкилов являются С1-4-алкил или С1-2-алкил. Предпочтительными среди С3-7-циклоалкилов являются циклопентил и циклогексил.
Термин «С2-6-алкенил», в качестве группы или части группы, означает углеводородные радикалы с линейной или разветвленной цепью, имеющие насыщенные связи углерод-углерод и, по меньшей мере, одну двойную связь и имеющие 2-6 атомов углерода, такие как, например, этенил (или винил), 1-пропенил, 2-пропенил (или аллил), 1-бутенил, 2-бутенил, 3-бутенил, 2-метил-2-пропенил, 1-пентенил, 2-пентенил, 3-пентенил, 2-метил-1-бутенил, 1-гексенил, 2-гексенил, 3-гексенил, 4-гексенил, 2-метил-2-пентенил, 1,2-диметил-1-бутенил и т.п. Предпочтительными являются С2-6-алкенилы, имеющие одну двойную связь. Представляющими интерес среди С2-6-алкенильных радикалов являются С2-4-алкильные радикалы. Термин «С3-6-алкенил» имеет такое же значение, как С2-6-алкенил, но ограничен по ненасыщенным углеводородным радикалам, имеющим 3-6 атомов углерода. В случаях, где С3-6-алкенил связан с гетероатомом, атом углерода, связанный с гетероатомом, предпочтительно является насыщенным. Термин «С2-12-алкенил» означает С2-6-алкенил, но имеет 2-12 атомов углерода и включает С2-6-алкенильные радикалы и высшие гомологи, такие как 1-гептенил, 2-гептенил, 3-гептенил, 1-метил-1-гексенил, 1,2-диметил-1-пентенил, 2-метил-1-гексенил, 2-этил-2-пентенил, 3-пропил-2-гексенил, 1-октенил, 2-октенил, 1-ноненил, 1-деценил, 1-ундеценил, 1-додеценил и т.п. Предпочтительными среди С2-12-алкенилов являются С2-6-алкенилы.
Термин «С2-6-алкинил», в качестве группы или части группы, представляет собой углеводородные радикалы с линейной или разветвленной цепью, имеющие насыщенные связи углерод-углерод и, по меньшей мере, одну тройную связь и имеющие 2-6 атомов углерода, такие как, например, этинил, 1-пропинил, 2-пропинил, 1-бутинил, 2-бутинил, 3-бутинил, 2-метил-2-пропинил, 2-пентинил, 3-пентинил, 2-гексинил, 3-гексинил, 4-гексинил, 2-метил-2-бутинил, 2-метил-2-пентинил и т.п. Предпочтительными являются С2-6-алкинилы, имеющие одну тройную связь. Представляющими интерес среди С2-6-алкинильных радикалов являются С2-4-алкильные радикалы. Термин «С3-6-алкинил» означает С2-6-алкинил, но ограничен по ненасыщенным углеводородным радикалам, имеющим 3-6 атомов углерода. В случае, где С3-6-алкинил связан с гетероатомом, атом углерода, связанный с гетероатомом, предпочтительно является насыщенным. Термин «С2-12-алкинил» имеет такое же значение, как С2-6-алкинил, но имеет 2-12 атомов углерода и включает С2-6-алкинильные радикалы и высшие гомологи, как, например, 1-гептинил, 2-гептинил, 1-октинил, 2-октинил, 1-нонинил, 1-децинил, 1-ундецинил, 1-додецинил и т.п. Предпочтительными среди С2-12-алкинилов являются С2-6-алкинилы.
Как используется в данном контексте ранее, элемент (=О) образует карбонильную группу, когда присоединен к атому углерода, сульфоксидную группу, когда присоединен к атому серы, и сульфонильную группу, когда два из вышеуказанных элементов присоединены к атому серы.
Термины «карбоксил», «карбокси» или «гидроксикарбонил» относятся к группе СООН.
Термин «галоген» означает фтор, хлор, бром или йод.
Термин «полигалоген-С1-6-алкил», в качестве группы или части группы, например в полигалоген-С1-6-алкокси, означает моно- или полигалогензамещенный С1-6-алкил, в частности С1-6-алкил, замещенный количеством вплоть до одного, двух, трех, четырех, пяти, шести или более атомов галогена, такой как метил или этил с одним или более атомами фтора, например дифторметил, трифторметил, трифторэтил. Предпочтительным является трифторметил. Также сюда входят перфтор-С1-6-алкильные группы, которые являются С1-6-алкильными группами, где все атомы водорода замещены атомами фтора, например пентафторэтил. В случае, где более чем один атом галогена присоединен к алкильной группе в пределах определения полигалоген-С1-6-алкила, атомы галогена могут быть одинаковыми или различными.
Подразумевают, что любой из гетероциклов, указанных в определениях Het, включает любой изомер, как, например, оксадиазол, который может представлять собой 1,2,4-оксадиазол, 1,3,4-оксадиазол или 1,2,3-оксадиазол; подобное относится к тиадиазолу, который может быть 1,2,4-тиадиазолом, 1,3,4-тиадиазолом или 1,2,3-тиадиазолом; подобным образом имидазол может быть 1Н-имидазолом или 3Н-имидазолом.
Когда же радикал встречается в определении соединений формулы (I) или в любой из подгрупп, описанных в данном контексте, вышеуказанный радикал независимо имеет значение, как указанное выше в определении соединений формулы (I) или в более ограниченных определениях, как указано в дальнейшем.
Также нужно обратить внимание на то, что положения радикала в любом молекулярном остатке, используемом в определениях, может быть где угодно в таком остатке, пока он является химически стабильным. Например, пиридин включает 2-пиридин, 3-пиридин и 4-пиридин; пентил включает 1-пентил, 2-пентил и 3-пентил.
Когда любая переменная (например, галоген, С1-6-алкил, арил, Het и т.д.) встречается более чем один раз в любом остатке, каждое определение является независимым.
Подразумевают, что любые ограниченные определения радикалов, указанные в данном контексте, являются пригодными для группы соединений формулы (I), а также для любой подгруппы, описанной или указанной в данном контексте.
Линии, идущие от заместителей в циклических системах, указывают на то, что связь может быть присоединена к любому из подходящих атомов цикла.
Подразумевают, что термин «соединения формулы (I)» или любые подобные термины, такие как «соединения согласно данному изобретению» и т.п., также включает любые N-оксидные формы соединений формулы (I), которые являются соединениями формулы (I), где один или несколько атомов азота окислены до N-оксидной формы.
Фармацевтически приемлемые аддитивные соли, которые способны образовывать соединения согласно настоящему изобретению, можно без труда получать, используя соответствующие кислоты, такие как, например, неорганические кислоты, как, например, галогенводородные кислоты, например, соляная или бромистоводородная кислота, серная кислота, гемисерная кислота, азотная кислота, фосфорная кислота и т.п. кислоты; или органические кислоты, такие как, например, уксусная кислота, аспарагиновая кислота, додецилсерная кислота, гептановая кислота, гексановая кислота, никотиновая кислота, пропановая кислота, гидроксиуксусная кислота, молочная кислота, пировиноградная кислота, щавелевая кислота, малоновая кислота, янтарная кислота, малеиновая кислота, фумаровая кислота, яблочная кислота, винная кислота, лимонная кислота, метансульфоновая кислота, этансульфоновая кислота, бензолсульфоновая кислота, п-толуолсульфоновая кислота, цикламеновая кислота, салициловая кислота, парааминосалициловая кислота, памовая кислота и т.п. кислоты. Наоборот, вышеуказанные аддитивные солевые формы кислот могут быть превращены в свободную основную форму путем обработки соответствующим основанием.
Соединения формулы (I), содержащие кислые протоны, можно превращать в их фармацевтически приемлемые аддитивные солевые формы с металлом или амином путем обработки соответствующими органическими или неорганическими основаниями. Соответствующие основные солевые формы включают, например, соли аммония, соли щелочных и щелочноземельных металлов, например соли лития, натрия, калия, магния, кальция и т.п., соли с органическими основаниями, например, с первичными, вторичными и третичными алифатическими и ароматическими аминами, такие как соли метиламина, этиламина, пропиламина, изопропиламина, четырех изомеров бутиламина, диметиламина, диэтиламина, диэтаноламина, дипропиламина, диизопропиламина, ди-н-бутиламина, пирролидина, пиперидина, морфолина, триметиламина, триэтиламина, трипропиламина, хинуклидина, пиридина, хинолина и изохинолина, бензатина, N-метил-D-глюкамина, 2-амино-2-(гидроксиметил)-1,3-пропандиола, гидрабамина, и соли с аминокислотами, такими как, например, аргинин, лизин и т.п. Наоборот, солевая форма может быть превращена в свободную кислотную форму путем обработки кислотой.
Данное изобретение также включает гидраты и аддитивные формы с растворителем, которые способны образовывать соединения формулы (I). Примерами таких форм являются, например, гидраты, алкоголяты и т.п.
Следует принимать во внимание, что некоторые из соединений формулы (I) и их аддитивных солей могут включать один или более центров хиральности и существовать в виде стереохимически изомерных форм. Особый интерес представляют такие соединения формулы (I), которые являются стереохимическими чистыми.
Термин «стереохимически изомерные формы», как используется выше, означает все возможные стереоизомерные формы, которые могут иметь соединения формулы (I) и их аддитивные соли. За исключением иначе указанного или упомянутого, химическое название соединений означает смесь всех возможных стереохимически изомерных форм, причем вышеуказанные смеси содержат все диастереомеры и энантиомеры основной молекулярной структуры, а также каждую из отдельных изомерных форм формулы (I) и их солей или сольватов, по существу, свободную, т.е. связанную с менее чем 10%, предпочтительно менее чем 5%, в особенности менее чем 2% и более предпочтительно менее чем 1% других изомеров. Таким образом, когда соединение формулы (I) обозначают, например, как (Е), это означает, что соединение по существу не содержит (Z)-изомера. В частности, стереогенные центры могут иметь R- или S-конфигурацию; заместители у двухвалентных циклических (частично) насыщенных радикалов могут иметь или цис- или трансконфигурацию.
Соединения, имеющие двойные связи, могут иметь Е (против)- или Z (вместе)-стереохимию по вышеуказанной двойной связи. Термины «цис», «транс», «R», «S», «Е» и «Z» хорошо известны квалифицированному специалисту в данной области.
Некоторые из соединений формулы (I) также могут существовать в их таутомерной форме. Подразумевают, что такие формы, хотя и не указаны подробно в вышеприведенной формуле, входят в рамки настоящего изобретения.
Подразумевают, что настоящее изобретение также включает любые изотопы атомов, присутствующих в соединениях согласно данному изобретению. Например, изотопы атома водорода включают тритий и дейтерий, а изотопы атома углерода включают С-13 и С-14.
Как используется выше или в дальнейшем, подразумевают, что термины «соединения формулы (I)», «соединения настоящего изобретения», «соединения согласно настоящему изобретению» или любые эквивалентные термины и подобно термины «подгруппы соединений формулы (I)», «подгруппы соединений настоящего изобретения», «подгруппы соединений согласно настоящему изобретению» или любые эквивалентные термины включают соединения общей формулы (I) или подгруппы соединений общей формулы (I), а также их соли и стереоизомеры.
Когда же, выше или в дальнейшем, указывается, что заместители, каждый независимо, могут быть выбраны из перечня определений, таких как, например, для R8 и R9, подразумевают, что включаются любые возможные комбинации, которые химически возможны или которые приводят к молекулам такой химической стабильности, что они могут быть получены с помощью стандартных фармацевтических способов.
Воплощение А настоящего изобретения включает такие соединения формулы (I) или любую из подгрупп соединений формулы (I), где R1 означает водород.
Воплощение В настоящего изобретения включает такие соединения формулы (I) или любую из подгрупп соединений формулы (I), как таковые в случае воплощения А,
где
(а) R2, R3, R7 и R8 независимо означают водород; гидрокси; галоген; С1-6-алкил; С3-7-циклоалкил; С1-6-алкилокси; карбоксил; С1-6-алкилоксикарбонил; циано; нитро; амино; моно- или ди(С1-6-алкил)амино; полигалоген-С1-6-алкил; полигалоген-С1-6-алкилокси; -С(=О)R10;
(b) R2, R3, R7 и R8 независимо означают водород; гидрокси; галоген; С1-6-алкил; С1-6-алкилокси; карбоксил; С1-6-алкилоксикарбонил; циано; нитро; амино; моно- или ди(С1-6-алкил)амино; полигалоген-С1-6-алкил; -С(=О)R10;
(с) R2, R3, R7 и R8 независимо означают водород; гидрокси; галоген; С1-6-алкил; С1-6-алкилокси; циано; амино; моно- или ди(С1-6-алкил)амино; полигалоген-С1-6-алкил;
(d) R2, R3, R7 и R8 независимо означают водород; галоген; С1-6-алкил; циано;
(е) R2, R3, R7 и R8 независимо означают водород; галоген; С1-6-алкил; циано;
(f) R2 и R3 означают водород, а R7 и R8 независимо означают водород, галоген, циано.
Воплощение С настоящего изобретения включает такие соединения формулы (I) или любую из подгрупп соединений формулы (I), как таковые в случае воплощений А или В,
где
(а) R4 и R9 независимо означают гидрокси; галоген; С1-6-алкилокси; карбоксил; С1-6-алкилоксикарбонил; формил; циано; амино; моно- или ди(С1-6-алкил)амино; полигалоген-С1-6-алкил; -С(=О)R10; Het; -Y-Het; С1-12-алкил, необязательно замещенный галогеном, циано, амино, моно- или ди(С1-6-алкил)амино, -С(=О)R10, Het; С2-12-алкенил, необязательно замещенный галогеном, циано, амино, моно- или ди(С1-6-алкил)амино, -С(=О)R10, Het; С2-12-алкинил, необязательно замещенный галогеном, циано, амино, моно- и ди(С1-6-алкил)амино, -С(=О)R10, Het;
(b) R4 и R9 независимо означают гидрокси; галоген; С1-6-алкилокси; карбоксил; С1-6-алкилоксикарбонил; формил; циано; амино; моно- или ди(С1-6-алкил)амино; полигалоген-С1-6-алкил; -С(=О)R10; Het; -Y-Het; С1-12-алкил, необязательно замещенный галогеном, циано, амино, моно- и ди(С1-6-алкил)амино, -С(=О)R10, Het; С2-12-алкенил, необязательно замещенный галогеном, циано, амино, моно- или ди(С1-6-алкил)амино, -С(=О)R10, Het; С2-12-алкинил, необязательно замещенный галогеном, циано, амино, моно- или ди(С1-6-алкил)амино, -С(=О)R10, Het; и где каждый Het, в особенности, независимо выбирают из тиенила, фуранила, оксазолила, тиазолила, необязательно замещенных галогеном, С1-6-алкилом, циано, карбоксилом, -С(=О)R10;
(с) R4 и R9 независимо означают гидрокси; галоген; С1-6-алкилокси; карбоксил; С1-6-алкилоксикарбонил; циано; амино; моно- или ди(С1-6-алкил)амино; -С(=О)R10; Het; -Y-Het; С1-6-алкил, необязательно замещенный циано, -С(=О)R10, Het; С2-6-алкенил, необязательно замещенный циано, -С(=О)R10, Het; С2-6-алкинил, необязательно замещенный циано, -С(=О)R10, Het; и где каждый Het, в частности, независимо выбирают из тиенила, фуранила, оксазолила, тиазолила, необязательно замещенных галогеном, С1-6-алкилом, циано, карбоксилом, -С(=О)R10;
(d) R4 и R9 независимо означают галоген; карбоксил; С1-6-алкилоксикарбонил; циано; -С(=О)R10; Het; -Y-Het; С1-6-алкил, необязательно замещенный циано, -С(=О)R10, Het; С2-12-алкенил, необязательно замещенный циано, -С(=О)R10, Het; и где каждый Het, в частности, независимо выбирают из тиенила, фуранила, оксазолила, тиазолила, необязательно замещенных галогеном, С1-6-алкилом, циано, карбоксилом, -С(=О)R10;
(е) R4 и R9 независимо означают циано; -С(=О)R10; Het; С1-6-алкил, необязательно замещенный циано, -С(=О)R10, Het; С2-6-алкенил, необязательно замещенный циано, -С(=О)R10, Het; и где каждый Het, в частности, независимо означает тиенил или фуранил, причем каждый необязательно замещен циано, -С(=О)R10;
(f) R4 и R9 независимо означают циано; С1-6-алкил, замещенный циано; С2-6-алкенил, замещенный циано.
Воплощение D настоящего изобретения включает такие соединения формулы (I) или любую из подгрупп соединений формулы (I), как таковые в случае воплощений А, В или С,
где
(а) R5 означает С1-6-алкил, замещенный Ar или Het, С2-6-алкенил, С2-6-алкинил, необязательно замещенный Het, С3-7-циклоалкил, Ar, Het;
R6 означает водород, С1-6-алкил, Het;
Y означает OR11, NR12R13;
R11 означает водород или С1-6-алкил, необязательно замещенный гидрокси, С1-6-алкилокси, фенилом или пиридилом;
R12 означает водород или С1-6-алкил;
R13 означает водород или С1-6-алкил; или R12 и R13 вместе с атомом азота, заместителями которого они являются, образуют имидазолил;
(b) R5 означает С2-6-алкенил, С2-6-алкинил, замещенный Het, Ar, Het;
R6 означает водород, С1-6-алкил, Het;
Y означает OR11, NR12R13;
R11 означает водород или С1-6-алкил, необязательно замещенный гидрокси, С1-6-алкилокси;
R12 означает водород или С1-6-алкил;
R13 означает водород;
где в (а) или (b) Ar и Het могут иметь значения, как описано для соединений формулы (I) или формулы (I'), или любой их подгруппы или, в частности, еще
Ar означает фенил, необязательно замещенный С1-6-алкилокси; и/или
(i) Het означает пиридил, тиазолил, имидазолил, бензотиазолил, имидазотиазолил, причем каждый необязательно замещен С1-6-алкилом, галогеном; или еще, в частности,
(ii) Het означает пиридил, тиазолил, имидазолил, причем каждый необязательно замещен С1-6-алкилом, галогеном; или еще, в частности,
(iii) Het означает пиридил, тиазолил, причем последний необязательно замещен С1-6-алкилом.
Особый интерес представляют соединения формулы (I) или любая из подгрупп соединений формулы (I), где радикал:
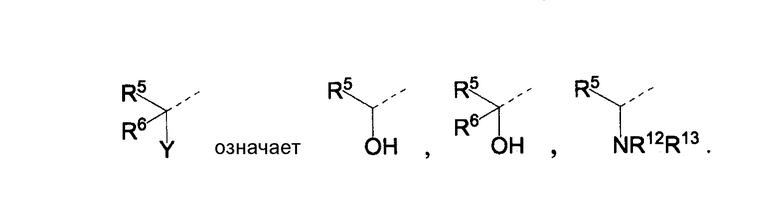
Воплощение Е настоящего изобретения включает такие соединения формулы (I) или любую из подгрупп соединений формулы (I), как таковые в случае воплощений А, В, С или D,
где
каждый из R10 независимо означает С1-6-алкил, амино, моно- или ди(С1-6-алкил)амино.
Воплощение F настоящего изобретения включает такие соединения формулы (I) или любую из подгрупп соединений формулы (I), как таковые в случае воплощений А, В, С, D или Е,
где
Х означает -NR1-, -O-, -S-, -S(=O)r-;
Х означает -NR1-, -O-;
Х означает -NR1-;
Х означает -NН-.
Воплощение G настоящего изобретения включает такие соединения формулы (I) или любую из подгрупп соединений формулы (I), как таковые в случае воплощений А, В, С, D, Е или F,
где
каждый Y независимо означает -NR1-, -O-, -S-, -S(=O)r- или каждый Y независимо означает -NR1-.
Воплощение Н настоящего изобретения включает такие соединения формулы (I) или любую из подгрупп соединений формулы (I), как таковые в случае воплощений А, В, С, D, Е, F или G, где каждый r независимо означает 2.
Воплощение I настоящего изобретения включает такие соединения формулы (I) или любую из подгрупп соединений формулы (I), как таковые в случае воплощений А, В, С, D, Е, F, G и Н, где каждый Het независимо означает пиридил, тиенил, фуранил, оксазолил, изоксазолил, имидазолил, пиразолил, тиазолил, тиадиазолил, оксадиазолил, хинолинил, бензотиенил, бензофуранил; каждый из которых может быть необязательно замещен одним или двумя заместителями, причем каждый независимо выбирают из группы, состоящей из С1-6-алкила, галогена, гидрокси, циано, С1-6-алкилокси, С2-12-алкенила, замещенного галогеном, гидрокси или циано.
Воплощение J настоящего изобретения включает такие соединения формулы (I) или любую из подгрупп соединений формулы (I), как таковые в случае воплощений А, В, С, D, Е, F, G, Н и I, где каждый арил независимо означает фенил или фенил, замещенный одним, двумя или тремя заместителями, причем каждый независимо выбирают из таковых, указанных выше, или, в частности, из
(а) галогена, гидрокси, С1-6-алкила, С2-6-алкенила, С2-6-алкинила, гидрокси-С1-6-алкила, амино-С1-6-алкила, моно- или ди(С1-6-алкил)амино-С1-6-алкила, С1-6-алкилкарбонила, С3-7-циклоалкила, С1-6-алкилокси, фенил-С1-6-алкилокси, С1-6-алкилоксикарбонила, аминосульфонила, циано, нитро, полигалоген-С1-6-алкила, полигалоген-С1-6-алкилокси, аминокарбонила, фенила, Het и -Y-Het; или
(b) галогена, гидрокси, С1-6-алкила, гидрокси-С1-6-алкила, амино-С1-6-алкила, моно- или ди(С1-6-алкил)амино-С1-6-алкила, С1-6-алкилокси, фенил-С1-6-алкилокси, С1-6-алкилоксикарбонила, циано, полигалоген-С1-6-алкила, аминокарбонила.
Одно воплощение настоящего изобретения относится к соединениям формулы:
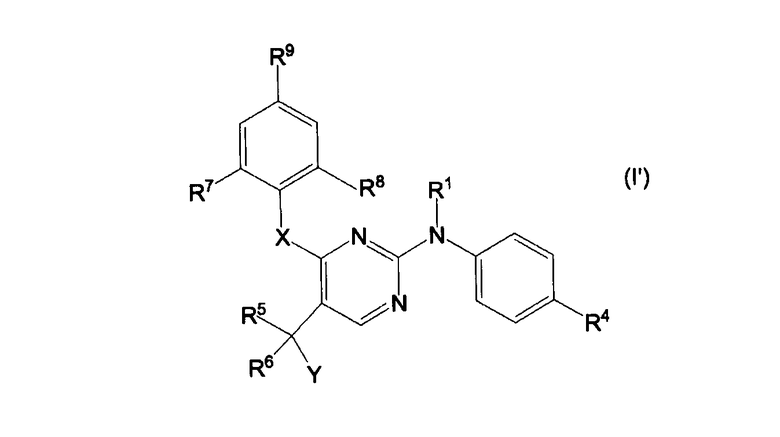
к их фармацевтически приемлемым аддитивным солям или их стереохимически изомерным формам, где Х, Y, R1, R4, R5, R6, R7, R8 и R9 имеют значения, как описано выше.
В конкретном воплощении, R9 в соединениях формулы (I) или формулы (I'), или любой их подгруппе означает -СН2-СН2-CN, -СН=СН-CN или -С≡С-CN. Интерес представляют такие соединения, где R9 является (Е)-изомером -СН=СН-CN.
Другое воплощение относится к таким соединениям формулы (I) или формулы (I'), или любой их подгруппе, где используют одно или более из следующих ограничений:
(i) каждый из R1 независимо означает водород, арил, формил, С1-6-алкилкарбонил, С1-6-алкил, С1-6-алкилоксикарбонил;
(ii) R4 означает гидрокси, галоген, С1-6-алкил, карбоксил, циано, -С(=О)R10, нитро, амино, моно- или ди(С1-6-алкил)амино, полигалогенметил;
(iii) Х означает -NR1-, -O-, -S-, -S(=O)r-;
(iv) R7 означает водород, С1-6-алкил, галоген;
(v) R8 означает водород, С1-6-алкил, галоген;
(vi) R5 означает С1-6-алкил, замещенный Ar или Het; С2-6-алкенил; С2-6-алкинил, необязательно замещенный Het; С3-7-циклоалкил; Ar; Het;
R6 означает водород, С1-6-алкил, Het;
Y означает -OR11, -NR12R13;
R11 означает водород или С1-6-алкил, необязательно замещенный гидрокси, С1-6-алкилокси, фенилом или пиридилом;
R12 означает водород или С1-6-алкил;
R13 означает водород или С1-6-алкил; или R12 и R13 вместе с атомом азота, заместителями которого они являются, образуют имидазолил;
(vii) каждый арил означает фенил или фенил, замещенный одним, двумя, тремя, четырьмя или пятью заместителями, причем каждый независимо выбирают из галогена, гидрокси, меркапто, С1-6-алкила, гидрокси-С1-6-алкила, амино-С1-6-алкила, моно- и ди(С1-6-алкил)амино-С1-6-алкила, С1-6-алкилкарбонила, С3-7-циклоалкила, С1-6-алкилокси, С1-6-алкилоксикарбонила, С1-6-алкилтио, циано, нитро, полигалоген-С1-6-алкила, полигалоген-С1-6-алкилокси, аминокарбонила.
Другое воплощение относится к таким соединениям формулы (I) или формулы (I'), или любой их подгруппе, где используют одно или более из следующих ограничений:
(i) R9 означает -СН2-СН2-CN или -СН=СН-CN; в особенности, где R9 означает -СН=СН-CN;
(ii) R1 означает водород, формил, С1-6-алкилкарбонил, С1-6-алкил, С1-6-алкилоксикарбонил;
(ii-a) R1 означает водород, С1-6-алкил;
(ii-b) R1 означает водород, метил;
(ii-c) R1 означает водород;
(iii) R4 означает циано, аминокарбонил; или где (iii-a) R2 означает циано;
(iv) Х означает -NR1-, -О-;
(iv-a) Х означает -NR1-;
(iv-b) Х означает -NН-, -N(С1-4-алкил)-, -О-;
(iv-c) Х означает -NН-;
(v) R7 означает водород, С1-6-алкил, галоген; (v-a) R7 означает водород, С1-4-алкил, галоген; (v-b) R7 означает С1-4-алкил;
(vi) R8 означает водород, С1-6-алкил, галоген; (v-a) R8 означает водород, С1-4-алкил, галоген; (v-b) R8 означает С1-4-алкил;
(vii) R5 означает С2-6-алкенил, С2-6-алкинил, замещенный Het; Ar, Het;
R6 означает водород, С1-6-алкил, Het;
Y означает OR11, NR12R13;
R11 означает водород или С1-6-алкил, необязательно замещенный гидрокси, С1-6-алкилокси;
R12 означает водород или С1-6-алкил;
R13 означает водород.
Еще другие подгруппы соединений формулы (I) или формулы (I') являются такими соединениями формулы (I) или формулы (I') или любой их подгруппы, где
(а) R10 означает водород, С1-4-алкил; или где (b) R10 означает водород или С1-2-алкил.
Другие подгруппы соединений формулы (I) или формулы (I') являются такими соединениями формулы (I) или формулы (I') или любой их подгруппы, где
(а) арил означает фенил или фенил, замещенный одним, двумя или тремя заместителями, причем каждый независимо выбирают из галогена, гидрокси, меркапто, С1-6-алкила, гидрокси-С1-6-алкила, амино-С1-6-алкила, моно- и ди(С1-6-алкил)амино-С1-6-алкила, С1-6-алкилкарбонила, С3-7-циклоалкила, С1-6-алкилокси, С1-6-алкилоксикарбонила, С1-6-алкилтио, циано, нитро, полигалоген-С1-6-алкила, полигалоген-С1-6-алкилокси, аминокарбонила;
(b) арил означает фенил или фенил, замещенный одним, двумя или тремя заместителями, причем каждый независимо выбирают из галогена, гидрокси, меркапто, С1-6-алкила, гидрокси-С1-6-алкила, амино-С1-6-алкила, моно- или ди(С1-6-алкил)амино-С1-6-алкила, С1-6-алкилкарбонила, С1-6-алкилокси, С1-6-алкилоксикарбонила, С1-6-алкилтио, циано, нитро, трифторметила, трифторметокси, аминокарбонила;
(с) арил означает фенил или фенил, замещенный одним, двумя или тремя заместителями, причем каждый независимо выбирают из галогена, гидрокси, С1-6-алкила, гидрокси-С1-6-алкила, амино-С1-6-алкила, моно- или ди(С1-6-алкил)амино-С1-6-алкила, С1-6-алкилкарбонила, С1-6-алкилокси, С1-6-алкилоксикарбонила, циано, нитро, трифторметила;
(d) арил означает фенил или фенил, замещенный одним, двумя или тремя заместителями, причем каждый независимо выбирают из галогена, гидрокси, С1-6-алкила, С1-6-алкилокси, циано, нитро, трифторметила.
Соединения формулы (I-a), которые являются соединениями формулы (I), где Y означает ОН, а R6 означает водород, можно получать путем взаимодействия пиримидинальдегида формулы (II) с металлоорганическим соединением (М-R5). Таким образом полученные соединения формулы (I-a) можно превращать в соответствующие соединения формулы (I-b), которые являются соединениями формулы (I), где Y означает OR11, где R11 имеет другое значение, чем водород. Группу R11 можно вводить путем реакции образования простого эфира, такой как реакция О-алкилирования, с реагентом W1-R11, где W1 представляет собой удаляемую группу, такую как галоген, в частности хлор, бром или йод, или сульфат или азид. М в М-R5 означает металл, такой как щелочной металл, в частности Li, Na или K, или производное магния, такое как типа реактива Гриньяра (М-R5 означает галоген-Mg-R5). Эти взаимодействия обычно проводят в инертном в условиях реакции растворителе, таком как простой эфир (ТГФ, диэтиловый эфир, диоксан) или галогенированный углеводород (СН2Сl2, CHCl3).
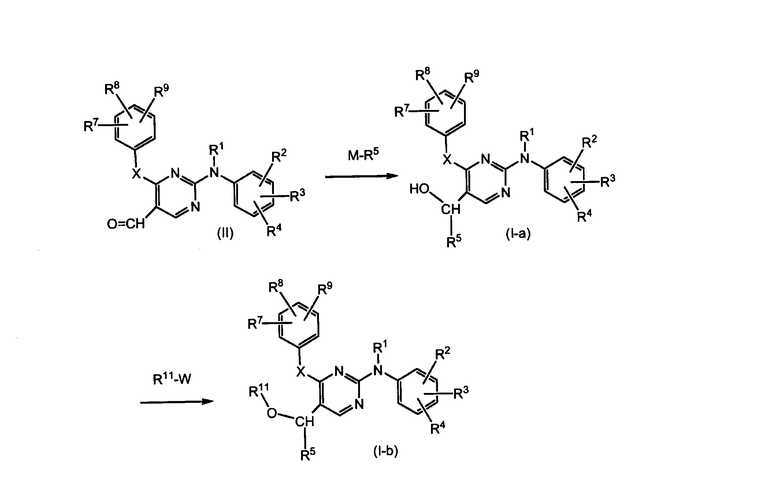
Соединения формулы (I), где Y означает OR11, а R5 и R6 имеют одинаковое значение, можно получать путем взаимодействия эфира пиримидинкарбоновой кислоты формулы (III) с металлоорганическим соединением (М-R5, который имеет значение, как описано выше), таким образом получая соединения формулы (I-c), которые являются соединениями формулы (I), где Y означает OН, а R5 и R6 имеют одинаковое значение. Эфир карбоновой кислоты в случае формулы (III), т.е. группа -СООR, может быть С1-6-алкиловым эфиром, например, метиловым, этиловым или пропиловым эфиром. Соединения формулы (I-c) можно превращать в соответствующие соединения формулы (I-d), которые являются соединениями формулы (I), где Y означает OR11, где R11 имеет другое значение, чем водород, а R5 и R6 имеют одинаковое значение, путем реакции образования простого эфира, как описано выше. Эти взаимодействия обычно осуществляют в инертном в условиях реакции растворителе, таком как растворители, указанные в связи с получением (I-a) и (I-b).
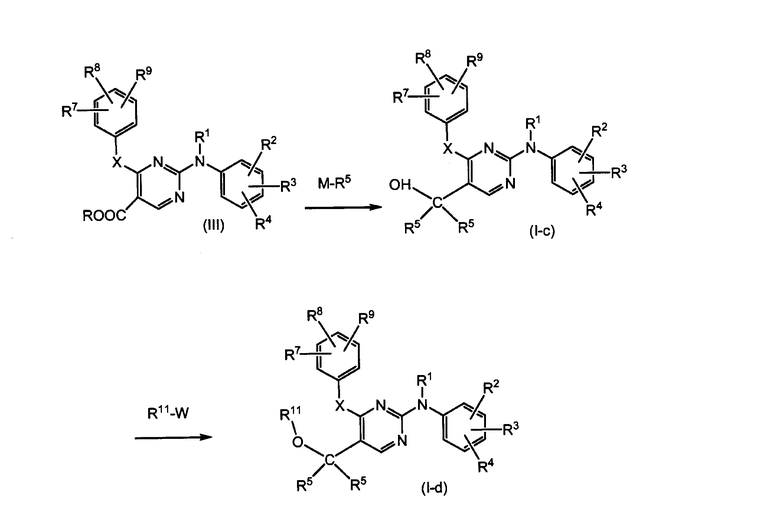
Соединения формулы (I), где Y означает ОН (в дальнейшем обозначают (I-e)) можно получать из кетопроизводного (IV) путем введения во взаимодействие с металлоорганическим соединением (М-R6), как описано выше, при превращении соединения (III) в соединение (I-c). Кетопроизводное (IV) получают из соединения (I-a) путем реакции окисления, в частности, при использовании слабого окислителя, такого как MnO2. Соединения (I-e) превращают в соединения (I-f), которые являются соединениями формулы (I), где Y означает OR11, и где R11 имеет другое значение, чем водород, путем реакции образования простого эфира, как описано выше. Также эти взаимодействия обычно проводят в инертном в условиях реакции растворителе (например, как растворители, указанные выше).
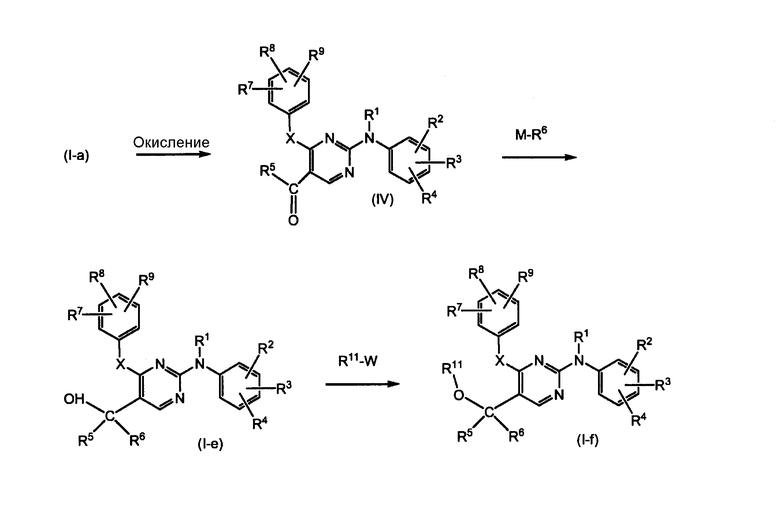
Промежуточные продукты формулы (IV), их соли и возможные стереоизомеры являются новыми соединениями и составляют следующий аспект настоящего изобретения. Соли промежуточных продуктов (IV), в частности, являются аддитивными солями кислот, еще, в частности, фармацевтически приемлемыми аддитивными солями кислот, такими как соли, указанные выше в связи с соединениями формулы (I).
Соединения формулы (I), где Y означает NR11R12, в данном контексте представленные формулой (I-g), можно получать путем взаимодействия соединения формулы (I-c) с агентом, вводящим удаляемую группу, таким как РОСl3 или SOCl2, таким образом получая промежуточные продукты (V), которые превращают в соответствующие амины с R11R12NH. Группа W в соединении (IV) представляет собой удаляемую группу, которая, в частности, означает галоген, предпочтительно хлор или бром, или тозил, мезил или подобное. Также эти взаимодействия обычно проводят в инертном в условиях реакции растворителе (например, как растворители, указанные выше).
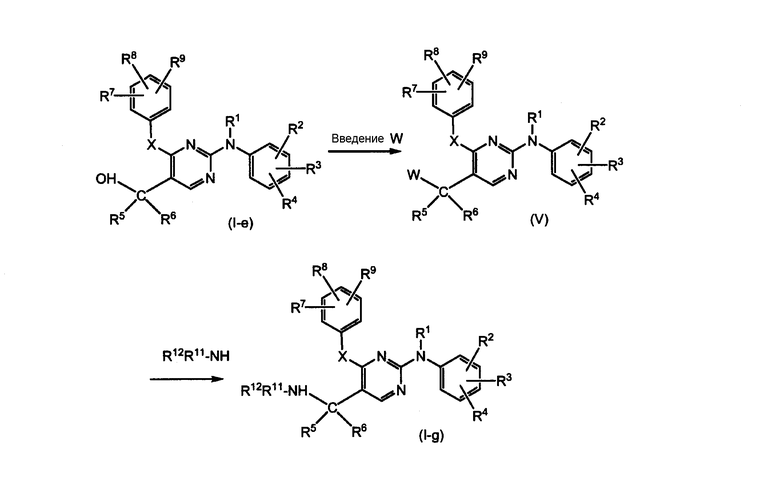
Промежуточные продукты формулы (II) получают сначала галогенированием исходного вещества формулы (VI), которое можно получать, как описано в WO-03/016306. Другие удаляемые группы можно вводить путем замещения галогеновой группы, используя подходящие реагенты. Таким образом полученные промежуточные продукты формулы (VII) затем превращают в соответствующие промежуточные продукты формулы (II), которые имеют группу -СНО в положении 5 пиримидинового остатка, путем введения во взаимодействие соединения (VII) с находящимся под давлением газообразным СО, в присутствии формиата натрия и подходящего катализатора, как, например, дихлорбис(трифенилфосфин)палладий(II).
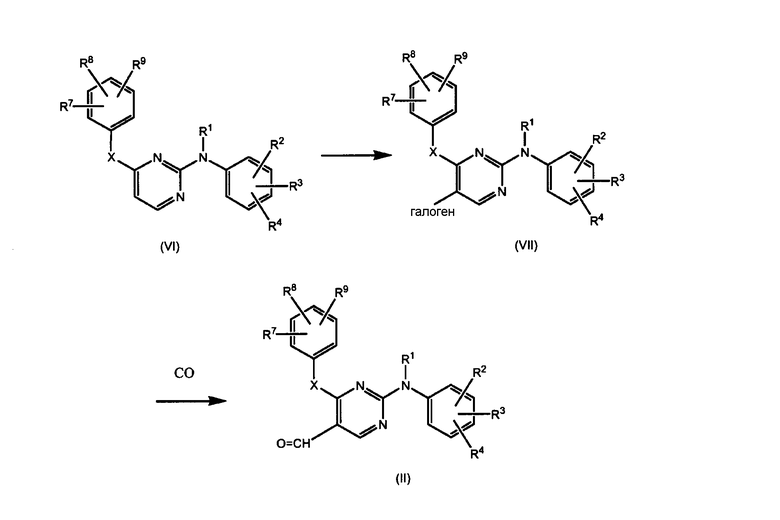
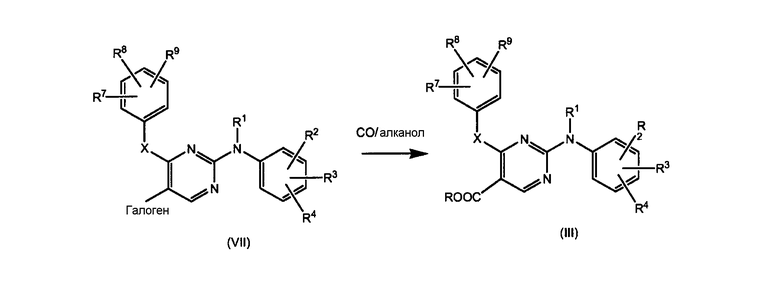
Промежуточные сложные эфиры формулы (III) можно получать сначала путем введения во взаимодействие промежуточных продуктов формулы (VII) с находящимся под давлением газообразным СО, в присутствии этанола или подобного низшего алканола и подходящего катализатора, как, например, дихлорбис(трифенилфосфин)палладий(II).
Соединения формулы (I) можно превращать в соответствующие N-оксидные формы путем следующих известных в уровне техники способов превращения третичного азота в его N-оксидную форму. Вышеуказанную реакцию N-окисления, как правило, можно осуществлять путем введения во взаимодействие исходного вещества формулы (I) с соответствующим органическим или неорганическим пероксидом. Соответствующие неорганические пероксиды включают, например, пероксид водорода, пероксиды щелочных или щелочноземельных металлов, например пероксид натрия, пероксид калия; соответствующие органические пероксиды могут включать надкислоты, как, например, бензолнадкарбоновая кислота или галогензамещенная бензолнадкарбоновая кислота, например 3-хлорбензолнадкарбоновая кислота, алканнадкарбоновые кислоты, например надуксусная кислота, алкилгидропероксиды, например трет-бутилгидропероксид. Подходящими растворителями являются, например, вода, низшие спирты, например этанол и т.п., углеводороды, например толуол, кетоны, например 2-бутанон, галогенированные углеводороды, например дихлорметан, и смеси таких растворителей.
Соединения формулы (I) далее можно превращать друг в друга, используя известные в уровне техники реакции превращения функциональных групп. Соединения формулы (I), где R2 или R3 означает водород, можно превращать в соединения формулы (I), где один или более из R2, R3, R7 или R8 означают галоген, путем введения во взаимодействие с подходящим, вводящим галоген агентом, как, например, N-хлорсукцинимид или N-бромсукцинимид, в присутствии подходящего растворителя, например уксусной кислоты. Соединения формулы (I), где R1 означает С1-6-алкилоксикарбонил, можно превращать в соединение формулы (I), где R1 означает водород, путем введения во взаимодействие с подходящим основанием, таким как, например, гидроксид натрия или метоксид натрия. Там, где R1 означает трет-бутилоксикарбонил, соответствующие соединения, где R1 означает водород, получают путем обработки трифторуксусной кислотой.
Некоторые из соединений формулы (I) и некоторые из промежуточных продуктов согласно настоящему изобретению могут содержать асимметрический атом углерода. Стереохимически чистые изомерные формы вышеуказанных соединений и вышеуказанных промежуточных продуктов можно получать при использовании известных в уровне техники способов. Например, диастереоизомеры можно разделять физическими методами, такими как селективная кристаллизация или хроматографические способы, например противоточная распределительная хроматография, жидкостная хроматография и т.п. способы. Энантиомеры можно получать из рацемических смесей сначала путем превращения вышеуказанных рацемических смесей с помощью подходящих растворяющих агентов, таких как, например, хиральные кислоты, в смеси диастереомерных солей или соединений; затем путем физического разделения вышеуказанных смесей диастереомерных солей или соединений, например, с помощью селективной кристаллизации или хроматографических способов, как, например, жидкостная хроматография и т.п. способы; и, наконец, путем превращения вышеуказанных разделенных диастереомерных солей или соединений в соответствующие энантиомеры. Стереохимически чистые изомерные формы также можно получать из стереохимически чистых изомерных форм соответствующих промежуточных продуктов и исходных веществ при условии, что промежуточные реакции протекают стереоспецифически.
Альтернативный способ разделения энантиомерных форм соединений формулы (I) и промежуточных продуктов включает жидкостную хроматографию, в частности жидкостную хроматографию с использованием хиральной стационарной фазы.
Соединения формулы (I) обладают антиретровирусными свойствами (ингибирующие обратную транскриптазу свойства), в частности, против вируса иммунодефицита человека (ВИЧ), который является этиологическим агентом синдрома приобретенного иммунодефицита (СПИД), у людей. Вирус ВИЧ преимущественно инфицирует человеческие Т-4 клетки и разрушает их или изменяет их нормальную функцию, в особенности координирование иммунной системы. В результате, инфицированный пациент имеет всегда сниженное количество Т-4 клеток, которые, кроме того, ведут себя анормально. Следовательно, иммунологическая защитная система не способна бороться с инфекциями и новообразованиями, и ВИЧ-инфицированный субъект обычно умирает от вызываемых условно-патогенными микроорганизмами инфекций, таких как пневмония, или от раковых заболеваний. Другие состояния, связанные с ВИЧ-инфекцией, включают тромбоцитопению, саркому Капоши и инфекцию центральной нервной системы, характеризующуюся прогрессирующей демиелинизацией, в результате приводящей к деменции и симптомам, таким как прогрессирующая дизартрия, атаксия и дезориентация. ВИЧ-инфекция также далее связана с периферической невропатией, прогрессирующей генерализованной лимфаденопатией (PGL) и СПИД-ассоциированным комплексом (ARC).
Соединения согласно настоящему изобретению также проявляют активность против ВИЧ-штаммов, резистентных к (множественным) лекарственным средствам, в частности ВИЧ-1-штаммов, резистентных к множественным лекарственным средствам, в частности, соединения согласно настоящему изобретению проявляют активность даже против ВИЧ-штаммов, особенно против ВИЧ-1-штаммов, которые обладают приобретенной резистентностью по отношению к одному или более известным в уровне техники ненуклеозидным ингибиторам обратной транскриптазы. Известные в уровне техники ненуклеозидные ингибиторы обратной транскриптазы являются ненуклеозидными ингибиторами обратной транскриптазы, другими, чем соединения согласно настоящему изобретению, и известны квалифицированному специалисту в данной области, в частности коммерчески доступные ненуклеозидные ингибиторы обратной транскриптазы. Соединения согласно настоящему изобретению также обладают небольшой или несвязывающей аффинностью по отношению к человеческому α-1-кислому гликопротеину, причем человеческий α-1-кислый гликопротеин не влияет или только слабо влияет на анти-ВИЧ-активность соединений согласно настоящему изобретению.
Вследствие их антиретровирусных свойств, в частности их анти-ВИЧ-свойств, особенно их анти-ВИЧ-1-активности, соединения формулы (I), их фармацевтически приемлемые аддитивные соли и их стереохимически изомерные формы пригодны для лечения индивидуумов, инфицированных ВИЧ, и для профилактики этих инфекций. Вообще, соединения согласно настоящему изобретению могут быть пригодны для лечения теплокровных животных, инфицированных вирусами, существование которых опосредуется или зависит от фермента обратной транскриптазы. Состояния, которые можно предотвращать или лечить с помощью соединений согласно настоящему изобретению, особенно состояния, связанные с ВИЧ и другими патогенными ретровирусами, включают СПИД, СПИД-ассоциированный комплекс (ARC), прогрессирующую генерализованную лимфаденопатию (PGL), а также хронические заболевания центральной нервной системы, вызванные ретровирусами, такие как, например, ВИЧ-опосредованная деменция и рассеянный склероз.
Соединения согласно настоящему изобретению, следовательно, можно применять в качестве лекарственных средств против вышеуказанных состояний. Вышеуказанное применение в качестве лекарственного средства или способ лечения включает введение ВИЧ-инфицированным субъектам эффективного количества соединения для борьбы с состояниями, связанными с ВИЧ и другими патогенными ретровирусами, особенно с ВИЧ-1. В особенности, соединения формулы (I) можно применять при получении лекарственного средства для лечения или предупреждения ВИЧ-инфекций.
В дальнейшем аспекте данное изобретение относится к способу лечения теплокровных животных, включая людей, страдающих от состояний, связанных с вирусной инфекцией, в частности с ВИЧ-инфекцией, причем вышеуказанный способ включает введение вышеуказанным теплокровным животным, включая людей, антивирусного эффективного количества соединения формулы (I), как описано в данном контексте. Кроме того, оно относится к способу предупреждения развития состояний, связанных с вирусной инфекцией, в частности с ВИЧ-инфекцией, у теплокровных животных, включая людей, причем вышеуказанный способ включает введение вышеуказанным теплокровным животным, включая людей, антивирусного эффективного количества соединения формулы (I), как описано в данном контексте.
Настоящее изобретение также относится к композициям для лечения вирусных инфекций, содержащим терапевтически эффективное количество соединения формулы (I) и фармацевтически приемлемый носитель или разбавитель.
Соединения согласно настоящему изобретению могут быть использованы для получения различных фармацевтических форм в зависимости от пути введения. В качестве подходящих композиций можно назвать все композиции, обычно применяемые для систематического введения лекарственных средств. Для получения фармацевтических композиций согласно данному изобретению эффективное количество конкретного соединения, необязательно в форме аддитивной соли, в качестве активного ингредиента, объединяют путем тщательного смешивания с фармацевтически приемлемым носителем, причем носитель можно выбирать из широкого разнообразия форм в зависимости от формы препарата, желательной для введения. Эти фармацевтические композиции желательны в стандартной лекарственной форме, пригодной, в особенности, для перорального, ректального, подкожного введения или путем парентеральной инъекции. Например, при получении композиций в пероральной лекарственной форме можно использовать любую из обычных фармацевтических сред, такую как, например, вода, гликоли, масла, спирты и т.п., в случае пероральных жидких готовых лекарственных форм, таких как суспензии, сиропы, эликсиры, эмульсии и растворы; или твердые носители, такие как крахмал, сахара, каолин, разбавители, смазочные вещества, связующие вещества, дезинтегрирующие агенты и т.п., в случае порошков, пилюль, капсул и таблеток. Вследствие легкости их введения таблетки и капсулы представляют собой наиболее преимущественные пероральные стандартные лекарственные формы, в случае которых используют твердые фармацевтические носители. В случае парентеральных композиций, носитель обычно включает стерильную воду, по меньшей мере, большей частью, хотя могут быть включены и другие ингредиенты, например, для способствования растворимости. Могут быть получены, например, инъецируемые растворы, в которых носитель включает физиологический раствор, раствор глюкозы или смесь физиологического раствора и раствора глюкозы. Также могут быть получены инъецируемые суспензии, в случае которых могут быть использованы соответствующие жидкие носители, суспендирующие агенты и т.п. Также включаются препараты в твердой форме, которые предназначены для превращения, незадолго до использования, в препараты в жидкой форме. В композициях, пригодных для подкожного введения, носитель необязательно включает усиливающий пенетрацию агент и/или пригодный смачиватель, необязательно комбинированный с подходящими добавками любой природы в незначительных пропорциях, причем добавки не оказывают вредного воздействия на кожу. Вышеуказанные добавки могут облегчать введение через кожу и/или могут быть полезны для получения желательных композиций. Эти композиции можно вводить различными путями, например в виде трансдермального пластыря, в виде капель, в виде мази.
Соединения согласно настоящему изобретению также можно вводить путем ингаляции или инсуффляции при использовании способов и готовых лекарственных форм, используемых в уровне техники для введения этим путем. Таким образом, вообще, соединения согласно настоящему изобретению можно вводить в легкие в форме раствора, суспензии или сухого порошка. Любая система, разработанная для доставки растворов, суспензий или сухого порошка посредством пероральной или назальной ингаляции или инсуффляции, пригодна для введения соединений согласно настоящему изобретению.
Для улучшения растворимости соединений формулы (I) можно включать в композиции подходящие ингредиенты, например циклодекстрины. Соответствующими циклодекстринами являются α-, β-, γ-циклодекстрины или их простые эфиры или их смешанные простые эфиры, где одна или более гидроксильных групп ангидроглюкозных единиц циклодекстрина замещены С1-6-алкилом, в частности метилом, этилом или изопропилом, например метилированный по случаю β-CD; гидрокси-С1-6-алкилом, особенно гидроксиэтилом, гидроксипропилом или гидроксибутилом; карбокси-С1-6-алкилом, в частности карбоксиметилом или карбоксиэтилом; С1-6-алкилкарбонилом, в частности ацетилом. Особенно заслуживающими внимания в качестве комплексообразователей и/или солюбилизаторов являются β-CD, метилированный по случаю β-CD, 2,6-диметил-β-CD, 2-гидроксиэтил-β-CD, 2-гидроксипропил-β-CD и (2-карбоксиметокси)пропил-β-CD, в особенности 2-гидроксипропил-β-CD (2-НР-β-CD).
Термин «смешанный простой эфир» означает производные циклодекстрина, где, по меньшей мере, две циклодекстриновые гидроксильные группы превращены в простой эфир с помощью различных групп, таких как, например, гидроксипропил и гидроксиэтил.
Среднее молярное замещение (M.S.) используют как меру среднего числа молей алкоксильных групп на моль ангидроглюкозы. Степень среднего замещения (D.S.) относится к среднему числу замещенных гидроксильных групп на единицу ангидроглюкозы. Значения M.S. и D.S. могут быть определены различными аналитическими методами, такими как ядерный магнитный резонанс (ЯМР), масс-спектрометрия (МС) и инфракрасная спектроскопия (ИК). В зависимости от используемого метода, могут быть получены слегка различающиеся значения для одного данного производного циклодекстрина. Предпочтительно, как измеряемые путем масс-спектрометрии, M.S. находятся в диапазоне 0,125-10, а D.S. в диапазоне 0,125-3.
Другие пригодные композиции для перорального или ректального введения включают частицы, состоящие из твердой дисперсии, включающей соединение формулы (I) и один или более соответствующих фармацевтически приемлемых водорастворимых полимеров.
Термин «твердая дисперсия», как используется в дальнейшем, описывает систему в твердом состоянии (в качестве противоположного жидкому или газообразному состоянию), содержащую, по меньшей мере, два компонента, при случае, соединение формулы (I) и водорастворимый полимер, где один компонент более или менее равномерно диспергирован в другом компоненте или компонентах (при случае, включают дополнительные фармацевтически приемлемые агенты для получения готовой лекарственной формы, обычно известные в уровне техники, такие как пластификаторы, консерванты и т.п.). Когда вышеуказанная дисперсия компонентов является такой, что система химически и физически однородна или гомогенна или состоит из одной фазы, как описано в термодинамике, такую твердую дисперсию называют «твердым раствором». Твердые растворы являются предпочтительными физическими системами, так как компоненты в них обычно без труда биодоступны организмам, в которые их вводят. Это преимущество, вероятно, можно объяснить легкостью, с которой вышеуказанные твердые растворы могут образовывать жидкие растворы, когда происходит контакт с жидкой средой, такой как желудочно-кишечные соки. Легкость растворения можно приписывать, по меньшей мере частично, тому факту, что энергии, необходимой для растворения компонентов из твердого раствора, нужно меньше, чем энергии, необходимой для растворения компонентов из кристаллической или микрокристаллической твердой фазы.
Термин «твердая дисперсия» также относится к дисперсиям, которые менее гомогенны, чем твердые растворы. Такие дисперсии не являются химически и физически однородными или содержат более чем одну фазу. Например, термин «твердая дисперсия» также относится к системе, имеющей зоны или небольшие участки, где аморфное, микрокристаллическое или кристаллическое соединение формулы (I), или аморфный, микрокристаллический или кристаллический водорастворимый полимер, или оба более или менее однородно диспергированы в другой фазе, включающей водорастворимый полимер, или соединение формулы (I), или твердый раствор, содержащий соединение формулы (I) и водорастворимый полимер. Вышеуказанные зоны являются областями в твердой дисперсии, отчетливо заметными по некоторому физическому признаку (свойству), небольшими по размеру и равномерно и в случайном порядке распределенными по твердой дисперсии.
Существуют различные способы получения твердых дисперсий, включая экструзию из расплава, сушку распылением и выпаривание раствора.
Способ выпаривания раствора включает следующие стадии:
а) растворение соединения формулы (I) и водорастворимого полимера в соответствующем растворителе, необязательно при повышенных температурах;
b) нагревание раствора, полученного в пункте а), необязательно в вакууме, вплоть до выпаривания растворителя. Раствор также можно выливать на большую поверхность так, чтобы образовалась тонкая пленка, и из нее выпаривать растворитель.
Согласно способу сушки распылением, два компонента также растворяют в соответствующем растворителе и полученный раствор затем распыляют через сопло для сушки распылением с последующим выпариванием растворителя из полученных капелек при повышенных температурах.
Предпочтительным способом получения твердых дисперсий является способ экструзии из расплава, включающий следующие стадии:
а) смешивание соединения формулы (I) и соответствующего водорастворимого полимера,
b) необязательно смешивание добавок с таким образом полученной смесью,
с) нагревание и компаундирование таким образом полученной смеси до получения гомогенного расплава,
d) экструзия таким образом полученного расплава через одно или более сопл и
е) охлаждение расплава до его затвердевания.
Подразумевают, что термины «расплав» и «плавление» относятся не только к переходу от твердого состояния к жидкому состоянию, но также относятся к переходу в стеклообразное состояние или каучукообразное состояние, при котором возможно, что один компонент смеси оказывается более или менее гомогенно включенным в другой. В частных случаях, один компонент расплавляется, а другой(ие) компонент(ы) растворяется(ются) в расплаве, таким образом образуя раствор, который после охлаждения может образовывать твердый раствор, обладающий благоприятными свойствами в отношении растворения.
После получения твердых дисперсий, как описано выше, полученные продукты можно необязательно измельчать и просеивать. Продукт в виде твердой дисперсии можно измельчать или размалывать до частиц, имеющих размер частиц менее чем 600 мкм, предпочтительно менее чем 400 мкм, наиболее предпочтительно менее чем 125 мкм.
Частицы, полученные, как описано выше, можно затем с помощью стандартных способов использовать для получения фармацевтических лекарственных форм, таких как таблетки и капсулы.
Водорастворимые полимеры в частицах являются полимерами, которые имеют кажущуюся вязкость, когда растворены при температуре 20°С в водном растворе при концентрации 2% масс./об., равную 1-5000 мПа·с, более предпочтительно 1-700 мПа·с, наиболее предпочтительно 1-100 мПа·с. Например, пригодные водорастворимые полимеры включают алкилцеллюлозы, гидроксиалкилцеллюлозы, гидроксиалкилалкилцеллюлозы, карбоксиалкилцеллюлозы, соли щелочных металлов карбоксиалкилцеллюлозы, карбоксиалкилалкилцеллюлозы, сложные эфиры карбоксиалкилцеллюлозы, крахмалы, пектины, производные хитина, ди-, олиго- и полисахариды, такие как трегалоза, альгиновая кислота или их соли щелочных металлов и аммония, каррагенаны, галактоманнаны, трагакант, агар-агар, гуммиарабик, гуаровая камедь и ксантановая смола, полиакриловые кислоты и их соли, полиметакриловые кислоты и их соли, сополимеры метакрилата, поливиниловый спирт, поливинилпирролидон, сополимеры поливинилпирролидона с винилацетатом, комбинации поливинилового спирта и поливинилпирролидона, полиалкиленоксиды и сополимеры этиленоксида и пропиленоксида. Предпочтительными водорастворимыми полимерами являются гидроксипропилметилцеллюлозы.
Также можно использовать один или более циклодекстринов в качестве водорастворимого полимера при получении вышеуказанных частиц, как описано в WO 97/18839. Вышеуказанные циклодекстрины включают фармацевтически приемлемые незамещенные и замещенные циклодекстрины, известные в уровне техники, в особенности α-, β- или γ-циклодекстрины или их фармацевтически приемлемые производные.
Замещенные циклодекстрины, которые можно использовать для получения вышеописанных частиц, включают простые полиэфиры, описанные в патенте США 3459731. Далее, замещенные циклодекстрины являются простыми эфирами, где водород одной или более циклодекстриновых гидроксильных групп заменен С1-6-алкилом, гидрокси-С1-6-алкилом, карбокси-С1-6-алкилом или С1-6-алкилоксикарбонил-С1-6-алкилом, или их смешанными простыми эфирами. В особенности, такие замещенные циклодекстрины являются простыми эфирами, где водород одной или более циклодекстриновых гидроксильных групп заменен С1-3-алкилом, гидрокси-С2-4-алкилом или карбокси-С1-2-алкилом, или, в особенности, метилом, этилом, гидроксиэтилом, гидроксипропилом, гидроксибутилом, карбоксиметилом или карбоксиэтилом.
Особенно пригодными являются простые эфиры β-циклодекстрина, например диметил-β-циклодекстрин, как описано M. Nogradi в Drugs of the Future, том 9, № 8, сс.577-578 (1984), и простые полиэфиры, например гидроксипропил-β-циклодекстрин и гидроксиэтил-β-циклодекстрин, в качестве примеров. Такой простой алкиловый эфир может быть простым метиловым эфиром со степенью замещения примерно 0,125-3, например примерно 0,3-2. Такой гидроксипропилциклодекстрин, например, может быть получен путем введения во взаимодействие β-циклодекстрина с пропиленоксидом и может иметь значение M.S., равное примерно 0,125-10, например примерно 0,3-3. Другим типом замещенных циклодекстринов, которые можно использовать, являются сульфобутилциклодекстрины.
Соотношение соединения формулы (I) к водорастворимому полимеру можно широко варьировать. Например, можно использовать соотношения от 1/100 до 100/1. Представляющие интерес соотношения соединения формулы (I) и циклодекстрина находятся в диапазоне от примерно 1/10 до 10/1. Представляющие больший интерес соотношения находятся в диапазоне примерно от 1/5 до 5/1.
Далее, может быть пригодным использование соединений формулы (I) в форме наночастиц, которые имеют модификатор поверхности, адсорбированный на их поверхности, в количестве, достаточном для поддержания эффективного среднего размера частиц, менее чем 1000 нм. Полагают, что пригодные модификаторы поверхности включают таковые, которые физически прилипают к поверхности соединения формулы (I), но химически не связываются с вышеуказанным соединением. Пригодные модификаторы поверхности можно предпочтительно выбирать из известных органических и неорганических фармацевтических эксципиентов. Такие эксципиенты включают различные полимеры, низкомолекулярные олигомеры, природные продукты и поверхностно-активные вещества. Предпочтительные модификаторы поверхности включают неионогенные и анионогенные поверхностно-активные вещества.
Еще другой путь использования соединений формулы (I) для получения готовых лекарственных форм включает фармацевтическую композицию, где соединения формулы (I) включены в гидрофильные полимеры, и эту смесь используют в качестве пленочного покрытия для множества маленьких шариков, таким образом, получая композицию, которую можно без труда перерабатывать и которая пригодна для получения фармацевтических лекарственных форм для перорального введения. Эти шарики включают центральное закругленное или сферическое ядро, пленочное покрытие из гидрофильного полимера и соединение формулы (I), и, необязательно, изолирующий покровный слой. Материалом, пригодным для использования в качестве ядер в шариках, является манифолд, при условии, что вышеуказанные материалы являются фармацевтически приемлемыми и имеют соответствующие размеры и твердость. Примерами таких материалов являются полимеры, неорганические вещества, органические вещества и сахариды, и их производные.
Это является особенно благоприятным для получения вышеуказанных фармацевтических композиций в стандартной лекарственной форме в отношении легкости их введения и единообразия дозировок. Стандартная лекарственная форма, как используется в данном контексте, относится к физически дискретным единицам, пригодным в качестве унитарных доз, причем каждая единица содержит заранее определенное количество активного ингредиента, рассчитанное для получения желательного терапевтического эффекта, в сочетании с необходимым фармацевтическим носителем. Примерами таких стандартных лекарственных форм являются таблетки (включая таблетки с насечкой или таблетки с покрытием), капсулы, пилюли, пакетированные порошки, облатки, суппозитории, инъецируемые растворы или суспензии и т.п., и их сегрегированные многократные формы.
Квалифицированный специалист при лечении ВИЧ-инфекции может определять эффективное суточное количество по результатам тестирования, представленным в данном контексте. Вообще, предполагают, что эффективное суточное количество должно составлять от 0,01 мг/кг до 50 мг/кг массы тела, более предпочтительно от 0,1 мг/кг до 10 мг/кг массы тела. Для введения может быть назначена необходимая доза в виде двух, трех, четырех или более субдоз через соответствующие интервалы в течение суток. Вышеуказанные субдозы можно получать в виде стандартных лекарственных форм, например, содержащих 1-1000 мг, в особенности 5-200 мг, активного ингредиента на стандартную лекарственную форму.
Точная дозировка и частота введения зависит от используемого конкретного соединения формулы (I), подвергаемого лечению конкретного состояния, тяжести подвергаемого лечению состояния, возраста, массы тела и общего физического состояния конкретного пациента, а также индивидууму может быть назначено другое лекарственное средство, как хорошо известно квалифицированному специалисту в данной области. Кроме того, очевидно, что вышеуказанное эффективное суточное количество можно уменьшать или увеличивать в зависимости от ответной реакции подвергаемого лечению субъекта и/или в зависимости от оценки лечащим врачом, назначающим соединения согласно настоящему изобретению. Эффективное суточное количество в диапазоне, указанном выше, является, следовательно, только рекомендованным и не подразумевают, что оно в какой-либо мере ограничивает рамки или применение данного изобретения.
Соединения формулы (I) можно применять отдельно или в комбинации с другими терапевтическими агентами, такими как противовирусные агенты, антибиотики, иммуномодуляторы или вакцины для лечения вирусных инфекций. Их можно также применять отдельно или в комбинации с другими профилактическими агентами для предупреждения вирусных инфекций. Соединения согласно настоящему изобретению можно применять в вакцинах и способах защиты индивидуумов против вирусных инфекций в течение длительного периода времени. Соединения можно применять в таких вакцинах или отдельно, или вместе с другими соединениями согласно данному изобретению, или вместе с другими противовирусными агентами при способе, совместимом с обычным использованием ингибиторов обратной транскриптазы в вакцинах. Таким образом, соединения согласно настоящему изобретению можно комбинировать с фармацевтически приемлемыми вспомогательными средствами, обычно применяемыми в вакцинах, и вводить в профилактически эффективных количествах для защиты индивидуумов в течение длительного периода времени против ВИЧ-инфекции.
Также можно использовать комбинацию одного или более дополнительных антиретровирусных соединений и соединения формулы (I) в качестве лекарственного средства. Таким образом, настоящее изобретение также относится к продукту, содержащему (а) соединение формулы (I) и (b) одно или более дополнительных антиретровирусных соединений, в виде комбинированного готового лекарственного средства для одновременного, раздельного или последовательного использования при анти-ВИЧ-лечении. Различные лекарственные средства можно комбинировать в отдельном готовом лекарственном средстве вместе с фармацевтически приемлемыми носителями. Вышеуказанные другие антиретровирусные соединения могут быть любыми известными антиретровирусными соединениями, такими как сурамин, пентамидин, тимопентин, кастаноспермин, декстран (декстрансульфат), фоскарнет-натрий (тринатрийфосфоноформиат); нуклеозидными ингибиторами обратной транскриптазы (NRTIs), например зидовудин (AZT), диданозин (ddI), залцитабин (ddС), ламивудин (3ТС), ставудин (d4T), эмтрицитабин (FTC), абакавир (АВС), амдоксовир (DAPD), элвуцитабин (АСН-126,443), AVX 754 ((-)-dOTC), фозивудинтидоксил (FZT), фосфазид, HDP-990003, KP-1461, MIV-210, рацивир (PSI-5004), UC-781 и т.п.; ненуклеозидными ингибиторами обратной транскриптазы (NNRTIs), такими как делавирдин (DLV), эфавиренз (EFV), невирапин (NVP), дапивирин (ТМС120), этравирин (ТМС125), рилпивирин (ТМС278), DPC-082, (+)-каланолид А, BILR-355 и т.п.; нуклеотидными ингибиторами обратной транскриптазы (NtRTIs), например тенофовир ((R)-PMPA) и тенофовирдизопроксилфумарат (TDF) и т.п.; конкурирующими нуклеотидными ингибиторами обратной транскриптазы (NcRTIs), например NcRTI-1 и т.п.; ингибиторами трансактивирующих белков, такими как ТАТ-ингибиторы, например RO-5-3335, BI-201 и т.п.; REV-ингибиторами; ингибиторами протеазы, например ритонавир (RTV), саквинавир (SQV), лопинавир (АВТ-378 или LPV), индинавир (IDV), ампренавир (VX-478), ТМС126, нелфинавир (AG-1343), атазанавир (BMS 232,632), дарунавир (ТМС114), фозампренавир (GW433908 или VX-175), бреканавир (GW-640385, VX-385), Р-1946, PL-337, PL-100, типранавир (PNU-140690), AG-1859, AG-1776, Ro-0334649 и т.п.; ингибиторами «входа», которые включают ингибиторы гибридизации (например, энфувиртид (Т-20)), ингибиторы присоединения и ингибиторы ко-рецептора, причем последние включают ССR5-антагонисты (например, анкривирок, ССR5mAb004, маравирок (UK-427,857), PRO-140, TAK-220, TAK-652, викривирок (SCH-D, SCH-417,690) и CXR4-антагонисты (например, AMD-070, KRH-27315); примерами ингибиторов «входа» являются PRO-542, TNX-355, BMS-488,043, BlockAide/CR™, FP 21399, hNM01, нонакин, VGV-1; ингибитор созревания представляет собой, например, РА-457; ингибиторами вирусной интегразы, например МК-0518, JTK-303 (GS-9137), BMS-538,158; рибозимами; иммуномодуляторами; моноклональными антителами; агентами генной терапии; вакцинами; siРНК; антисмысловыми РНК; бактерицидными веществами; ингибиторами белков «с цинковыми пальцами».
Соединения согласно настоящему изобретению также можно вводить в комбинации с иммуномодуляторами (например, бропиримин, антитело против человеческого альфа-интерферона, IL-2, метионинэнкефалин, интерферон-альфа и налтрексон), с антибиотиками (например, пентамидинизотиорат), с цитокинами (например, Th2), модуляторами цитокинов, хемокинами или модуляторами хемокинов, рецепторами хемокинов (например, CCR5, CXCR4), модуляторами рецепторов хемокинов или гормонами (например, гормон роста) для улучшения, борьбы или устранения ВИЧ-инфекции и ее симптомов. Такую комбинированную терапию при использовании различных готовых лекарственных форм можно проводить одновременно, последовательно или независимо друг от друга. Альтернативно, такую комбинацию можно вводить в виде одной готовой лекарственной формы, где активные ингредиенты высвобождаются из готовой лекарственной формы одновременно или раздельно.
Соединения согласно настоящему изобретению также можно вводить в комбинации с модуляторами метаболизма с последующим применением лекарственного средства для индивидуума. Эти модуляторы включают соединения, которые интерферируют с метаболизмом цитохромов, таких как цитохром Р450. Известно, что существуют некоторые изоферменты цитохрома Р450, один из которых является цитохромом Р450 3А4. Ритонавир представляет собой пример модулятора метаболизма через цитохром Р450. Такую комбинированную терапию при использовании различных готовых лекарственных форм можно проводить одновременно, последовательно или независимо друг от друга. Альтернативно, такую комбинацию можно вводить в виде одной готовой лекарственной формы, где активные ингредиенты высвобождаются из готовой лекарственной формы одновременно или раздельно. Такой модулятор можно вводить в таком же или другом соотношении, как соединение согласно настоящему изобретению. Предпочтительно массовое соотношение такого модулятора по отношению к соединению согласно настоящему изобретению (модулятор:соединение согласно настоящему изобретению) составляет 1:1 или ниже, более предпочтительно соотношение составляет 1:3 или ниже, подходящим образом соотношение составляет 1:10 или ниже, более подходящим образом соотношение составляет 1:30 или ниже.
Хотя настоящее изобретение направлено на применении соединений согласно настоящему изобретению для предупреждения или лечения ВИЧ-инфекций, соединения согласно настоящему изобретению также можно применять в качестве ингибирующих агентов для других вирусов, которые зависят от подобных обратных транскриптаз в отношении обязательных событий в их жизненном цикле.
Следующие примеры предназначены для иллюстрации настоящего изобретения и не ограничивают рамок данного изобретения.
ПРИМЕРЫ
Пример 1
Получение соединения 1
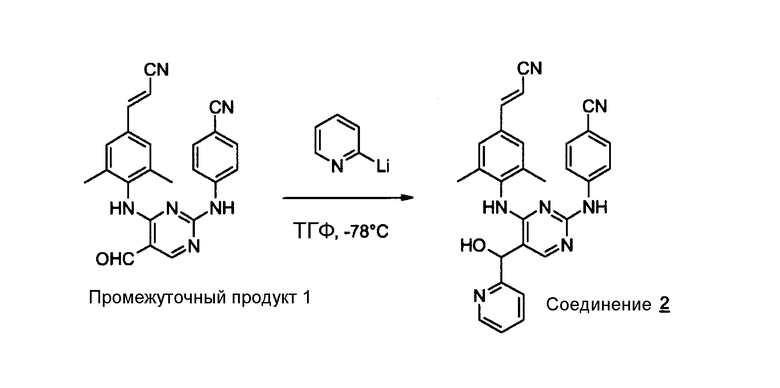
1,6 М раствор n-BuLi (н-бутиллития) (3,04 ммоль) по каплям добавляют к раствору 2-бромпиридина (3,04 ммоль) в ТГФ (5 мл) при температуре -78°С. Смесь перемешивают при температуре -78°С в течение 1 часа. Затем по каплям добавляют промежуточный продукт 1 (0,761 ммоль) при температуре -78°С и эту смесь перемешивают при температуре -78°С в течение 1 часа и при комнатной температуре в течение ночи. Добавляют воду и смесь экстрагируют этилацетатом. Органический слой сушат над сульфатом магния, отфильтровывают и растворитель выпаривают. Остаток очищают с помощью колоночной хроматографии на силикагеле (элюент: от CH2Cl2/MeOH/NH4OН = 98/2/0,1 до CH2Cl2/MeOH/NH4OН = 92/8/0,4; Kromasil, 5 мкм). Чистые фракции собирают и растворитель выпаривают. Выход: 0,085 г соединения 2 (17%, температура плавления: 244°С).
Таблица 1
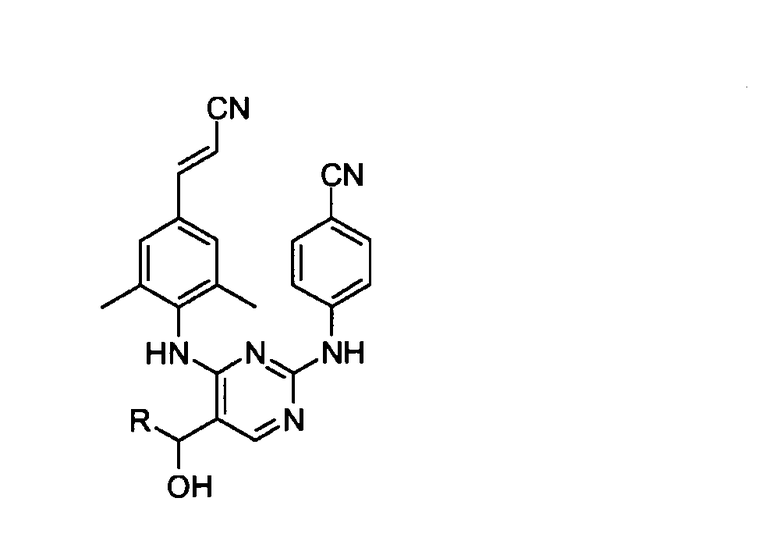
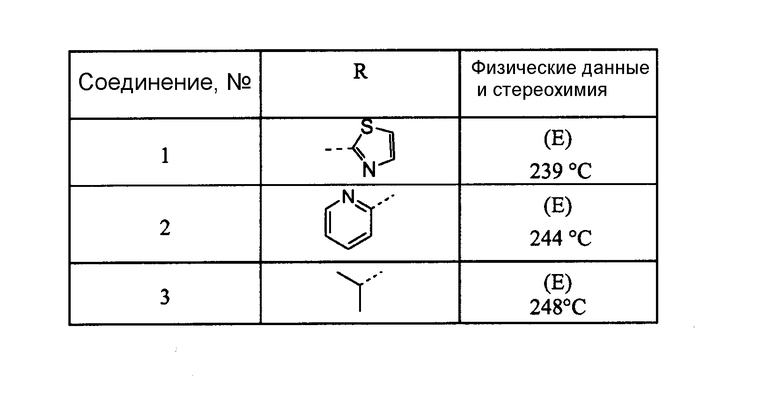
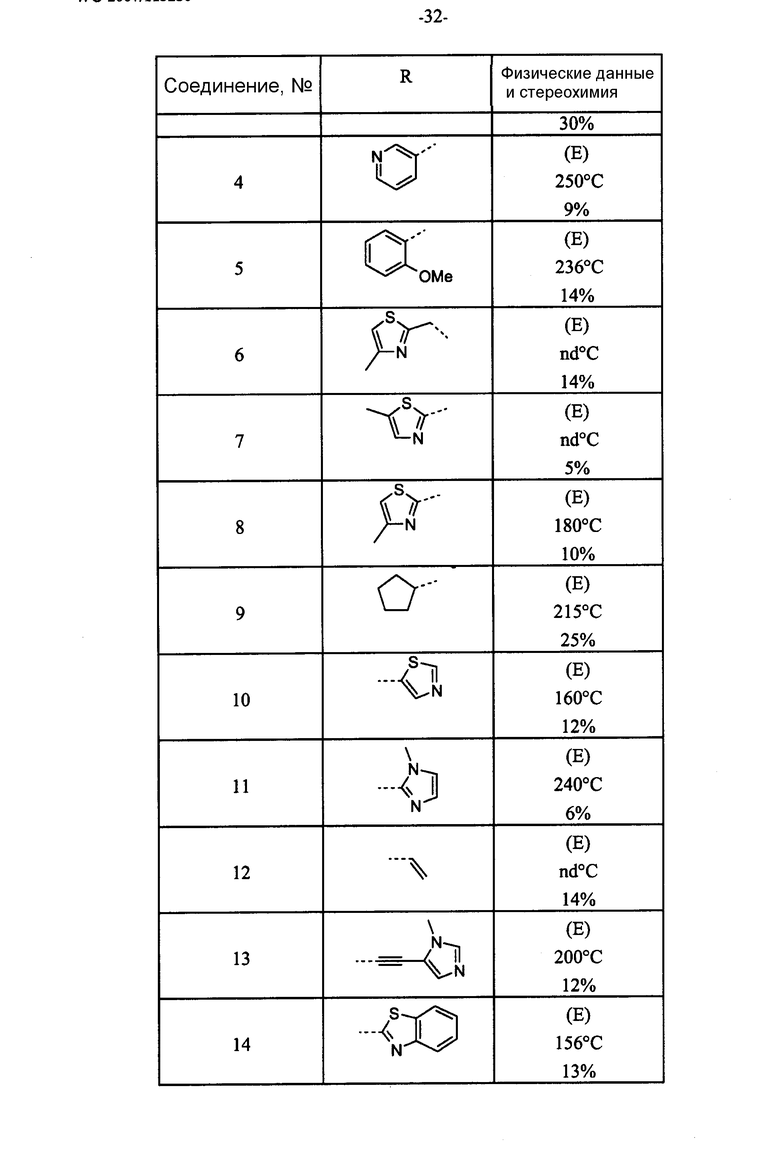
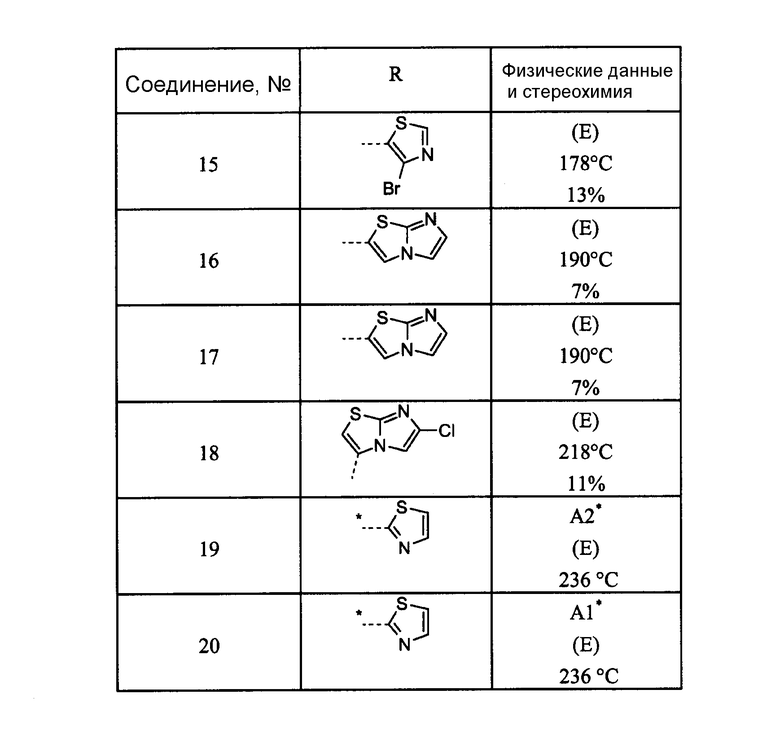
*Разделение энантиомеров с помощью хиральной хроматографии.
Пример 2
Получение промежуточного продукта 2
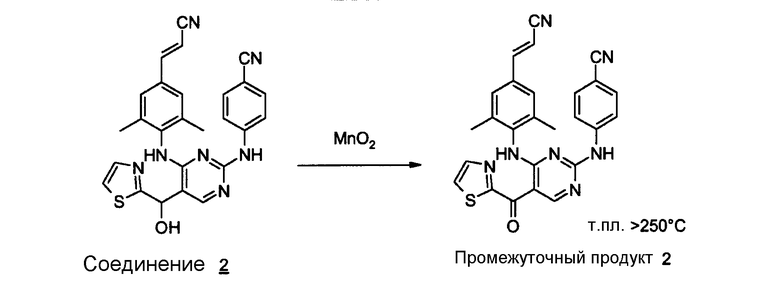
Диоксид марганца (0,012 моль) добавляют к раствору соединения 2 (0,00062 моль) в СН2Сl2 (20 мл) и смесь перемешивают при комнатной температуре в течение 24 часов, затем отфильтровывают через целит. Целит промывают смесью СН2Сl2/МеОН/ТГФ и фильтрат выпаривают. Остаток очищают с помощью колоночной хроматографии на силикагеле (элюент: СН2Сl2/МеОН = 99/1, SiO2, 10 мкм). Чистые фракции собирают и растворитель выпаривают. Выход: 0,060 г промежуточного продукта 2 (20%, температура плавления: >250°С).
Пример 3
Получение третичных спиртов
Способ А
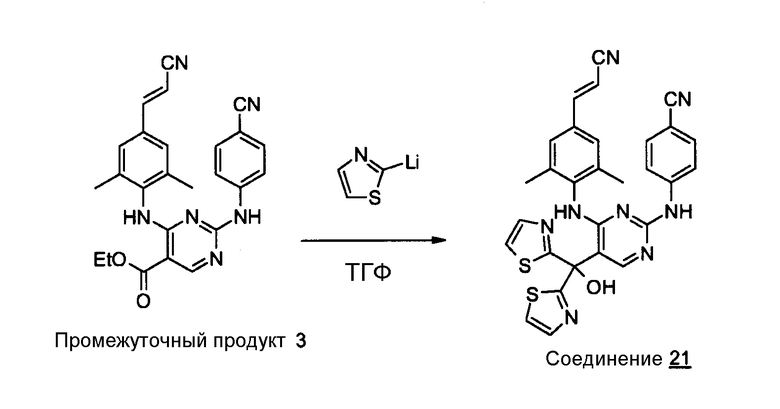
1,6 М раствор n-BuLi (3,08 ммоль) по каплям добавляют к раствору тиазола (3,08 ммоль) в ТГФ (5 мл) при температуре -78°С. Смесь перемешивают при температуре -78°С в течение 1 часа. Затем по каплям добавляют промежуточный продукт 2 (0,761 ммоль) при температуре -78°С, затем смесь перемешивают при температуре -78°С в течение 1 часа и при комнатной температуре в течение ночи. Добавляют воду и 10%-ный раствор NH4Cl и смесь экстрагируют с помощью СН2Сl2/ТГФ. Органический слой сушат над сульфатом магния, отфильтровывают и растворитель выпаривают. Остаток очищают с помощью колоночной хроматографии на силикагеле (элюент: от CH2Cl2/MeOH/NH4OН = 99/1/0,1 до CH2Cl2/MeOH/NH4OН = 95/5/0,5; Kromasil, 5 мкм). Чистые фракции собирают и растворитель выпаривают. Выход: 0,044 г соединения 5 (11%).
Способ В:
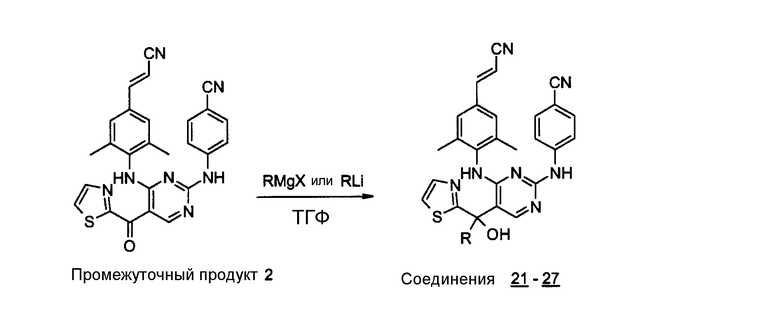
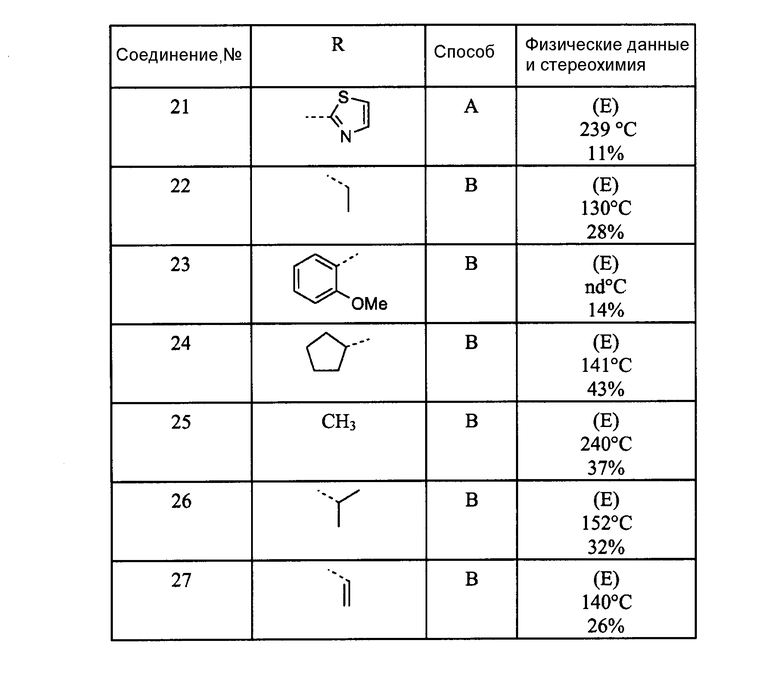
Коммерчески доступный магнийсодержащий реагент (3,5 экв.) добавляют к раствору промежуточного продукта 2 (1 экв.) в ТГФ (15 мл) при температуре 0°С, смесь перемешивают в течение 1 часа при температуре 0°С и затем при комнатной температуре в течение ночи. Добавляют воду и 10%-ный раствор NH4Cl и смесь экстрагируют с помощью СН2Сl2/ТГФ. Органический слой сушат над сульфатом магния, отфильтровывают и растворитель выпаривают. Остаток очищают с помощью колоночной хроматографии на силикагеле. Чистые фракции собирают и растворитель выпаривают, получая соединения 21-27.
Пример 4
Получение производных тиазола
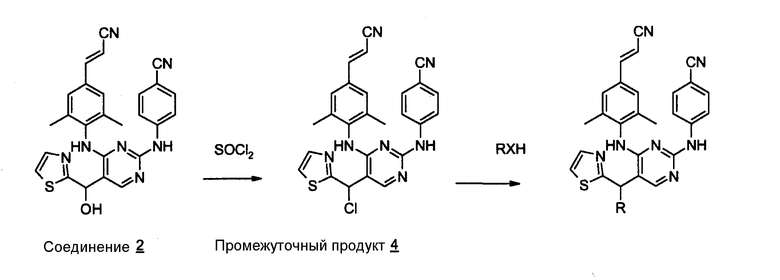
Тионилхлорид (1 мл) по каплям добавляют к раствору соединения 2 (0,60 ммоль) в СН2Сl2 (5 мл) при температуре 0°С. Смесь перемешивают при температуре 0°С в течение 3 часов и затем при комнатной температуре в течение ночи. Смесь выпаривают досуха и полученное твердое вещество (промежуточный продукт 4) отфильтровывают и промывают с помощью Et2O. Этот промежуточный продукт используют в следующих реакциях без дальнейшей очистки.
Способ А
Морфолин (1,2 мл) по каплям добавляют к раствору промежуточного продукта 4 (0,30 ммоль) в ТГФ (15 мл) при комнатной температуре. Смесь перемешивают при комнатной температуре в течение ночи. Смесь выливают в воду и 10%-ный раствор K2СО3 и экстрагируют смесью СН2Сl2/МеОН/ТГФ. Органический слой сушат над сульфатом магния, отфильтровывают и растворитель выпаривают. Остаток очищают с помощью колоночной хроматографии на силикагеле (элюент: от СН2Сl2/МеОН/NH4OH = 98/2/0,2 до СН2Сl2/МеОН/NH4OH = 94/6/0,6; Kromasil, 5 мкм). Чистые фракции собирают и растворитель выпаривают. Остаток кристаллизуют из Et2O. Выход: 0,047 г соединения 29 (28%, температура плавления: 220°С).
Способ В
Смесь соединения 2 (0,00028 моль, 1 экв.), 1,1'-карбонилбисимидазола (0,0031 моль, 1,5 экв.) и метиламина (0,0031 моль, 1,5 экв.) в ТГФ (2 мл) перемешивают в течение 18 часов. Эту смесь выливают в воду и 10%-ный раствор K2СО3 и экстрагируют смесью СН2Сl2/МеОН/ТГФ. Органический слой сушат над сульфатом магния, отфильтровывают и растворитель выпаривают. Остаток очищают с помощью колоночной хроматографии на силикагеле (элюент: от СН2Сl2/МеОН/NH4OH = 99/1/0,1 до СН2Сl2/МеОН/NH4OH = 94/6/0,6; Kromasil, 5 мкм). Чистые фракции собирают и растворитель выпаривают. Остаток кристаллизуют из iPr2O. Выход: 0,040 г соединения 30 (36%, температура плавления: 165°С).
Способ С
1,2-Этандиол (8,02 ммоль, 2 экв.) по каплям добавляют к раствору соединения 6 (4,01 ммоль, 1 экв.) и триэтиламина (8,02 ммоль, 2 экв.) в ТГФ (4 мл) при комнатной температуре. Смесь перемешивают при комнатной температуре в течение ночи, затем кипятят с обратным холодильником в течение 24 часов. Смесь выливают в воду и 10%-ный раствор K2СО3 и экстрагируют смесью СН2Сl2/МеОН/ТГФ. Органический слой сушат над сульфатом магния, отфильтровывают и растворитель выпаривают. Остаток очищают с помощью колоночной хроматографии на силикагеле (элюент: от СН2Сl2/МеОН/NH4OH = 99/1/0,1 до СН2Сl2/МеОН/NH4OH = 95/5/0,5; Kromasil, 5 мкм). Чистые фракции собирают и растворитель выпаривают. Остаток кристаллизуют из iPr2O. Выход: 0,048 г соединения 31 (22%, температура плавления: 120°С).
В следующей таблице перечислены соединения, которые получают в соответствии со способами, описанными в вышеуказанном примере.
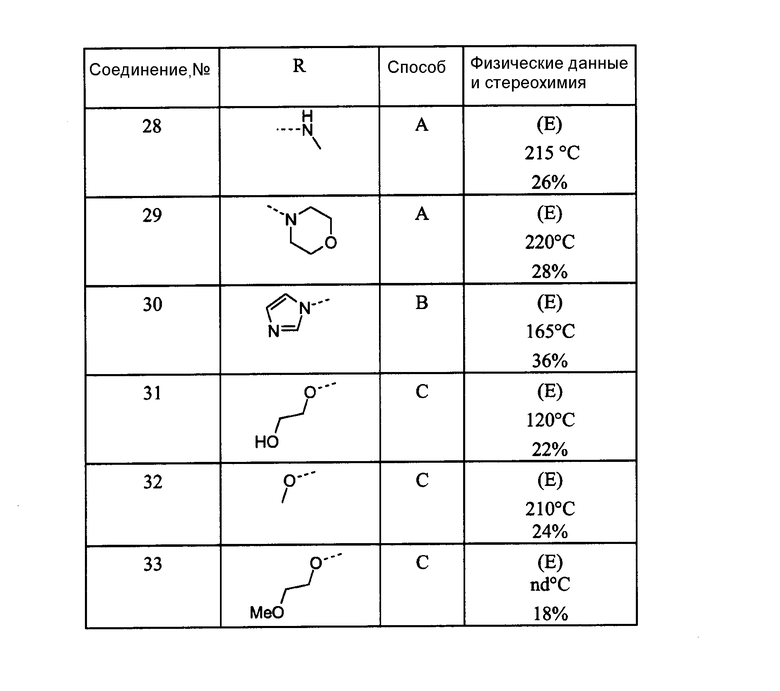
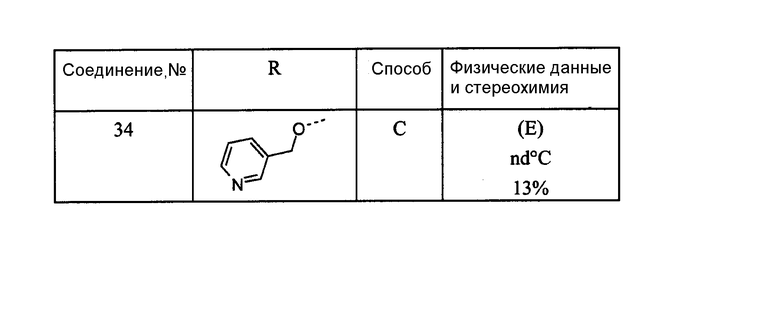
nd означает не установлена.
Примеры получения готовой лекарственной формы
Капсулы
Соединение формулы (I) растворяют в органическом растворителе, таком как этанол, метанол или метиленхлорид, предпочтительно в смеси этанола и метиленхлорида. Полимеры, такие как сополимер поливинилпирролидона с винилацетатом (PVP-VA) или гидроксипропилметилцеллюлоза (НРМС), обычно, вплоть до вязкости 5 мПа·с, растворяют в органических растворителях, таких как этанол, метанол, метиленхлорид. Подходящим образом, полимер растворяют в этаноле. Растворы полимера и соединения смешивают и потом подвергают сушке распылением. Соотношение соединение/полимер выбирают от 1/1 до 1/6. Промежуточное соотношение может составлять 1/1,5 и 1/3. Подходящее соотношение может быть 1/6. Высушенным путем распылительной сушки порошком, твердой дисперсией потом заполняют капсулы для введения. Лекарственным средством заполняют одну капсулу в диапазоне 50-100 мг, в зависимости от используемого размера капсулы.
Таблетки с пленочным покрытием
Получение ядра таблетки
Смесь из 100 г соединения формулы (I), 570 г лактозы и 200 г крахмала тщательно перемешивают и после этого увлажняют раствором 5 г додецилсульфата натрия и 10 г поливинилпирролидона в примерно 200 мл воды. Влажную порошкообразную смесь просеивают, сушат и снова просеивают. Затем добавляют 100 г микрокристаллической целлюлозы и 15 г гидрогенизированного растительного масла. Все это тщательно перемешивают и прессуют в таблетки, получая 10000 таблеток, каждая из которых содержит 10 мг активного ингредиента.
Покрытие
К раствору 10 г метилцеллюлозы в 75 мл денатурированного этанола добавляют раствор 5 г этилцеллюлозы в 150 мл дихлорметана. Затем добавляют 75 мл дихлорметана и 2,5 мл 1,2,3-пропантриола. 10 г полиэтиленгликоля расплавляют и растворяют в 75 мл дихлорметана. Последний раствор добавляют к первому и затем туда добавляют 2,5 г октадеканоата магния, 5 г поливинилпирролидона и 30 мл концентрированной суспензии красящего вещества и все это гомогенизируют. На ядра таблеток наносят покрытие с помощью таким образом полученной смеси в глазировочном аппарате.
Антивирусный спектр
Вследствие увеличивающегося появления резистентных к лекарственным средствам ВИЧ-штаммов, соединения согласно настоящему изобретению тестировали на их эффективность в отношении клинически изолированных ВИЧ-штаммов, обладающих некоторыми мутациями. Эти мутации связаны с резистентностью по отношению к ингибиторам обратной транскриптазы и приводят к вирусам, которые проявляют различные степени фенотипической перекрестной резистентности по отношению к коммерчески доступным в настоящее время лекарственным средствам, таким как, например, AZT и делавирдин.
Антивирусную активность соединений согласно настоящему изобретению оценивали в присутствии ВИЧ дикого типа и ВИЧ-мутантов, несущих мутации в гене обратной транскриптазы. Активность соединений оценивали, используя клеточный анализ, который выполняли в соответствии со следующей методикой.
Человеческую Т-клеточную линию МТ4 конструировали с флуоресцирующим зеленым белком (GFP) и ВИЧ-специфическим промотором, длинным концевым повтором ВИЧ-1 (LTR-последовательность). Эту клеточную линию обозначали МТ4 LTR-EGFP, и ее можно использовать при in vitro оценке анти-ВИЧ-активности исследуемых соединений. В инфицированных ВИЧ-1 клетках продуцируется Tat-белок, который активирует LTR-промотор и, в конце концов, приводит к стимуляции продуцирования GFP-репортера, позволяя измерять продолжающуюся ВИЧ-инфекцию флуорометрически.
Аналогично, МТ4-клетки конструировали с GFP и конституциональным промотором цитомегаловируса (CMV). Эту клеточную линию обозначали МТ4 CMV-EGFP, и ее можно использовать при in vitro оценке цитотоксичности исследуемых соединений. В этой клеточной линии уровни GFP сравнимы с таковыми инфицированных клеток МТ4 LTR-EGFP. Цитотоксические исследуемые соединения снижают уровни GFP мнимоинфицированных клеток МТ4 CMV-EGFP.
Определяли значения эффективной концентрации, такой как 50%-ная эффективная концентрация (ЕС50), и, как правило, выражали в мкМ. Значение ЕС50 определяли как концентрацию тестируемого соединения, которая уменьшает флуоресценцию ВИЧ-инфицированных клеток на 50%. Концентрацию в отношении цитотоксичности на 50% (СС50 в мкМ) определяли как концентрацию тестируемого соединения, которая уменьшает флуоресценцию мнимоинфицированных клеток на 50%. Соотношение СС50 к ЕС50 определяли как индекс селективности (SI), и он является показателем селективности анти-ВИЧ-активности ингибитора. Осуществляли конечный мониторинг ВИЧ-1-инфекции и цитотоксичности, используя сканирующий микроскоп. Анализ «по образу» позволяет осуществлять очень чувствительное детектированию вирусной инфекции. Измерения проводили перед некрозом клеток, который обычно имеет место спустя примерно пять дней после инфицекции, в частности измерения осуществляли спустя три дня после инфекции.
В колонках IIIB, L100I и т.п., в таблице, перечислены значения рЕС50 против различных штаммов IIIB, L100I и т.п.
Штамм IIIB представляет собой ВИЧ-штамм дикого типа.
«MDR» относится к штамму, который содержит мутации L100I, K103N, Y181C, E138G, V179I, L2214F, V278V/I и A327A/V в обратной транскриптазе при ВИЧ.
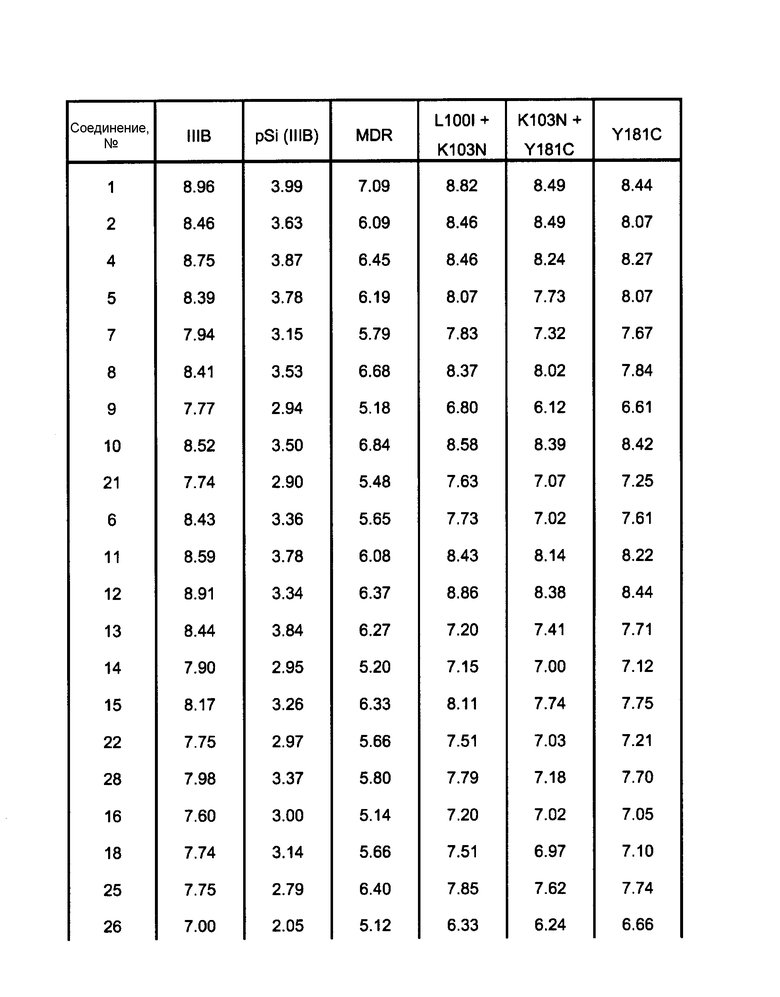
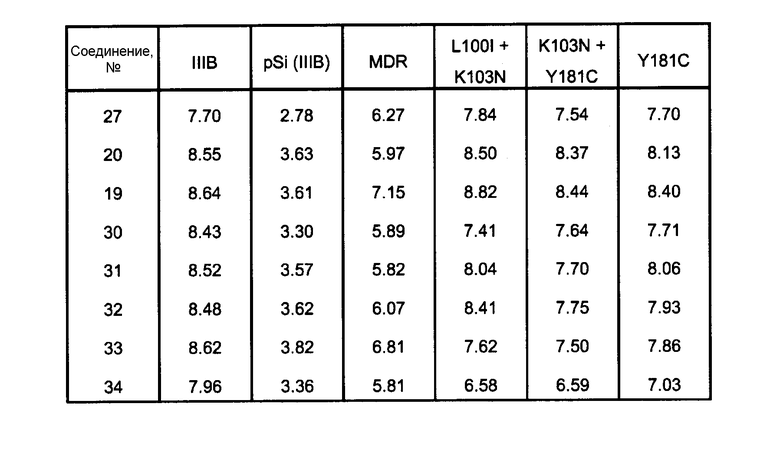
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНГИБИТОРЫ ВЗАИМОДЕЙСТВИЯ МЕЖДУ MDM2 И P53 | 2008 |
|
RU2477724C2 |
| 5-ЗАМЕЩЕННЫЕ ПИРИМИДИНЫ, ИНГИБИРУЮЩИЕ ВИЧ | 2005 |
|
RU2410379C2 |
| ПРОИЗВОДНЫЕ 1,10b-ДИГИДРО-2-(АМИНОКАРБОНИЛФЕНИЛ)-5Н-ПИРАЗОЛО[1,5-c][1,3]БЕНЗОКСАЗИН-5-ИЛ)ФЕНИЛМЕТАНОНА В КАЧЕСТВЕ ИНГИБИТОРОВ РЕПЛИКАЦИИ ВИЧ ВИРУСА | 2005 |
|
RU2382789C2 |
| 5-АМИДО-ЗАМЕЩЕННЫЕ ПИРИМИДИНЫ, ИНГИБИРУЮЩИЕ ВИЧ | 2007 |
|
RU2480464C2 |
| ЗАМЕЩЕННЫЕ ТИАЗОЛИЛЬНЫЕ И ЗАМЕЩЕННЫЕ ПИРИДИНИЛЬНЫЕ ПРОИЗВОДНЫЕ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ КИСЛОТНО-АДДИТИВНЫЕ СОЛИ, СПОСОБ ИХ ПОЛУЧЕНИЯ И КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ АНТИАЛЛЕРГИЧЕСКОЙ АКТИВНОСТЬЮ | 1991 |
|
RU2067978C1 |
| АНТИБАКТЕРИАЛЬНЫЕ ПРОИЗВОДНЫЕ ХИНОЛИНА | 2007 |
|
RU2446159C2 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ КАРБОНОВЫХ КИСЛОТ, ИМЕЮЩИЕ 2,5-ЗАМЕЩЕННОЕ ОКСАЗОЛОПИРИМИДИНОВОЕ КОЛЬЦО | 2011 |
|
RU2559896C2 |
| АНТИБАКТЕРИАЛЬНЫЕ ХИНОЛИНОВЫЕ ПРОИЗВОДНЫЕ | 2007 |
|
RU2439058C2 |
| ВИЧ-ИНГИБИРУЮЩИЕ 5-КАРБО- ИЛИ ГЕТЕРОЦИКЛИЧЕСКИЕ ЗАМЕЩЕННЫЕ ПИРИМИДИНЫ | 2005 |
|
RU2403244C2 |
| МАКРОЦИКЛИЧЕСКИЕ ИНГИБИТОРЫ ВИРУСА ГЕПАТИТА С | 2006 |
|
RU2486189C2 |
Изобретение относится к новым замещенным производным пиримидина, обладающим свойствами ингибитора репликации HIV, или их фармацевтически приемлемым солям. В формуле (I):
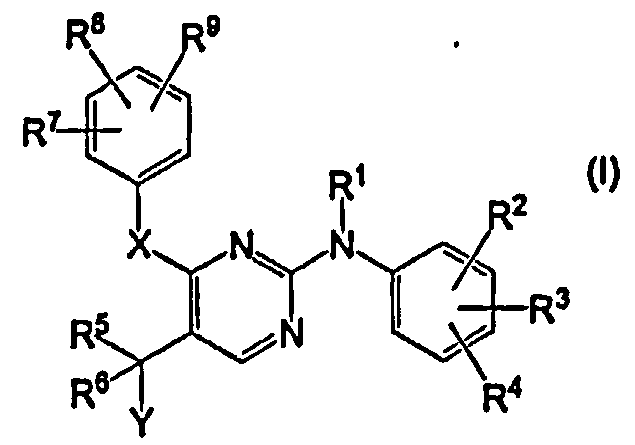
R1 означает водород; R2 и R3 независимо означают водород; R7 и R8 означают C1-6алкил; R4 означает циано; R9 означает C1-6алкил, необязательно замещенный циано, С2-6алкенил, замещенный циано, С2-6алкинил, необязательно замещенный циано; R5 означает C1-6алкил, необязательно замещенный Аr или Het; С2-6алкенил, необязательно замещенный Аr или Het; С2-6алкинил, необязательно замещенный Аr или Het; С3-7циклоалкил; Аr; Het; R6 означает Н, Het; Y означает -OR11, -NR12R13; R11 означает водород или C1-6алкил, необязательно замещенный гидрокси, C1-6алкокси или пиридил; R12 означает водород или C1-6алкил; R13 означает водород или C1-6алкил; или R12 и R13 вместе с атомом азота, заместителями которого они являются, образуют морфолинил; имидазолил; Х представляет собой -NR1-; Het означает 5- или 6-членный полностью ненасыщенный цикл, где один или два члена цикла являются гетероатомами, причем каждый независимо выбирают из азота и серы, и где остальные члены цикла являются атомами углерода; и где, возможно, любой член гетероцикла с гетероатомом азота необязательно может быть замещен C1-6алкилом; где 5- или 6-членный цикл может быть необязательно аннелирован с бензольным, тиофеновым циклом; каждый арил независимо означает фенил или фенил, замещенный одним заместителем, выбранным из С1-6алкокси. Изобретение также относится к фармацевтической композиции, содержащей указанные соединения. 2 н. и 5 з.п. ф-лы, 4 пр., 1 табл.
1. Соединение формулы (I):
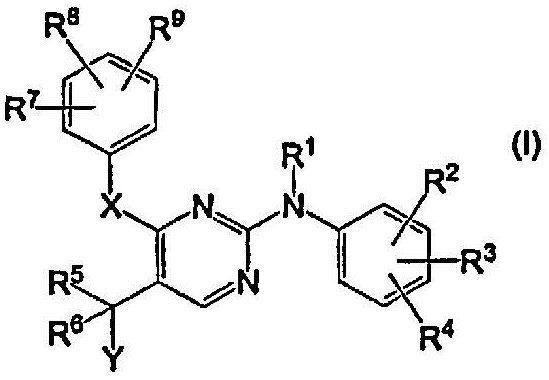
или его фармацевтически приемлемая аддитивная соль, где
R1 означает водород;
R2 и R3 независимо означают водород;
R7 и R8 означают C1-6алкил;
R4 означает циано;
R9 означает C1-6алкил, необязательно замещенный циано, С2-6алкенил, замещенный циано, С2-6алкинил, необязательно замещенный циано;
R5 означает С1-6алкил, необязательно замещенный Аr или Het; С2-6алкенил, необязательно замещенный Аr или Het; С2-6алкинил, необязательно замещенный Аr или Het; С3-7циклоалкил; Аr; Het; R6 означает Н, Het;
Y означает -OR11, -NR12R13;
R11 означает водород или C1-6алкил, необязательно замещенный гидрокси, C1-6алкокси или пиридил;
R12 означает водород или C1-6алкил;
R13 означает водород или C1-6алкил;
или R12 и R13 вместе с атомом азота, заместителями которого они являются, образуют морфолинил; имидазолил;
Х представляет собой -NR1-;
Het означает 5- или 6-членный полностью ненасыщенный цикл, где один или два члена цикла являются гетероатомами, причем каждый независимо выбирают из азота и серы, и где остальные члены цикла являются атомами углерода; и где, возможно, любой член гетероцикла с гетероатомом азота необязательно может быть замещен C1-6алкилом; где 5- или 6-членный цикл может быть необязательно аннелирован с бензольным, тиофеновым циклом; каждый арил независимо означает фенил или фенил, замещенный одним заместителем, выбранным из С1-6алкокси.
2. Соединение по п.1, где соединение отвечает формуле (I'):
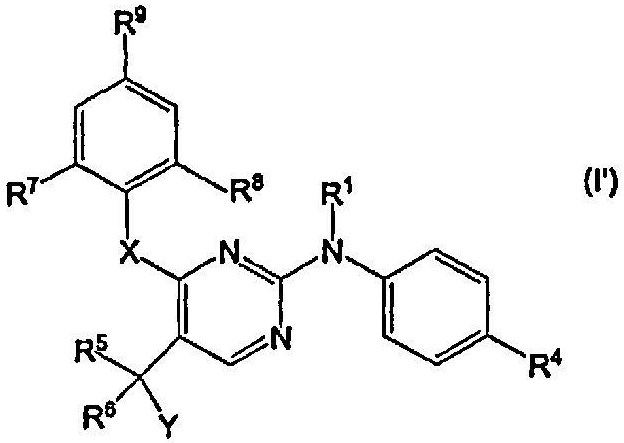
где X, Y, R1, R4, R5, R6, R7, R8 и R9 имеют значения, как описано в п.1.
3. Соединение по п.1, где R4 независимо означает циано; и R9 независимо означает C1-6алкил, замещенный циано; С2-6алкенил, замещенный циано.
4. Соединение по любому из пп.1-3, где R5 означает C1-6алкил, замещенный Аr или Het, С2-6алкенил, С2-6алкинил, необязательно замещенный Het, С3-7циклоалкил, Аr, Het;
R13 означает водород или C1-6алкил; или R12 и R13 вместе с атомом азота, заместителями которого они являются, образуют имидазолил.
5. Соединение по любому из пп.1-4, где R5 означает С2-6алкенил, С2-6алкинил, необязательно замещенный Het; Аr, Het;
R11 означает водород или C1-6алкил, необязательно замещенный гидрокси, C1-6алкилокси;
R12 означает C1-6алкил;
R13 означает водород.
6. Соединение по любому из пп.1-5, где каждый Het независимо означает пиридил, тиенил, тиазолил, каждый из которых может быть необязательно замещен радикалом, выбираемым из C1-6алкила.
7. Фармацевтическая композиция, обладающая свойствами ингибитора репликации HIV, содержащая фармацевтически приемлемый носитель и, в качестве активного ингредиента, терапевтически эффективное количество соединения по любому из пп.1-6.
| LUDOVICI D.W | |||
| "Evolution of Anti-HIV Drug Candidates | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Chem Letters, 11, pp.2235-2239 | |||
| US 20030171374 A1, 11.09.2003 | |||
| WO 2004065378 A1, 05.08.2004 | |||
| WO 2004069812 A1, 19.08.2004 | |||
| Прибор для измерения и масштабного вычерчивания линий и углов и для вычерчивания дуг круга | 1925 |
|
SU2973A1 |
Авторы
Даты
2012-06-10—Публикация
2007-03-30—Подача