Настоящее изобретение относится к производным пиримидина, обладающим ингибирующими репликацию ВИЧ (вирус иммунодефицита человека) свойствами. Кроме того, данное изобретение относится к способам их получения и содержащим их фармацевтическим композициям. Данное изобретение также относится к применению вышеуказанных соединений для профилактики или лечения ВИЧ-инфекции.
Резистентность вируса ВИЧ к доступным в настоящее время лекарственным средствам против ВИЧ продолжает оставаться основной причиной недостатка терапии. Это приводит к введению комбинированной терапии при использовании двух или более анти-ВИЧ-агентов, как правило, имеющих различный профиль активности. Значительный прогресс достигается за счет введения HAART-терапии (высокоактивная антиретровирусная терапия), которая приводит к существенному снижению заболеваемости и смертности в случае подвергаемых с ее помощью лечению ВИЧ-пациентов. HAART-терапия включает различные комбинации ингибиторов нуклеозидной обратной транскриптазы (NRTIs), ингибиторов ненуклеозидной обратной транскриптазы (NNRTIs) и ингибиторов протеазы (PIs). Современные методические рекомендации в отношении антиретровирусной терапии включают такую тройную комбинированную схему лечения для первоначальной терапии. Однако эти мультилекарственные терапии не полностью уничтожают ВИЧ, а длительное лечение, как правило, приводит к резистентности ко многим лекарственным средствам. В частности, половина пациентов, подвергаемых комбинированной анти-ВИЧ-терапии, совершенно не поддается лечению, главным образом, вследствие резистентности вируса к одному или более используемым лекарственным средствам. Также показано, что резистентный вирус переносится на вновь инфицируемых индивидуумов, что приводит к выбору строго ограниченной терапии для этих не поддающихся воздействию лекарственных средств пациентов.
Следовательно, существует постоянная потребность в новых комбинациях активных ингредиентов, которые эффективны против ВИЧ. Новые типы активных ингредиентов эффективных против ВИЧ, различающиеся по химической структуре и профилю активности, пригодны в новых видах комбинированной терапии. Обнаружение таких активных ингредиентов, следовательно, является очень желательной достигаемой целью.
Настоящее изобретение относится к получению конкретного нового ряда производных пиримидина, обладающих ингибирующими репликацию ВИЧ свойствами. В WO-99/50250, WO-00/27825 и WO-01/85700 раскрываются некоторые замещенные аминопиримидины, а в WO-99/50256 и ЕР-834507 раскрываются аминотриазины, обладающие ингибирующими репликацию ВИЧ свойствами.
Соединения согласно данному изобретению отличаются от известных в данной области соединений по структуре, фармакологической активности и/или фармакологической эффективности. Найдено, что введение определенных заместителей в положение 5 особым образом замещенных пиримидинов приводит к соединениям, не только благоприятно действующим с точки зрения их способности ингибировать репликацию вируса иммунодефицита человека (ВИЧ), но также к их улучшенной способности ингибировать репликацию мутантных штаммов, в частности штаммов, которые становятся резистентными к одному или более известным NNRTI-лекарственным средствам (лекарственные средства, ингибирующие ненуклеозидную обратную транскриптазу), штаммов, которые относят к резистентным к лекарственному средству или многим лекарственным средствам штаммам ВИЧ.
Таким образом, в одном аспекте, настоящее изобретение относится к соединениям формулы (I)
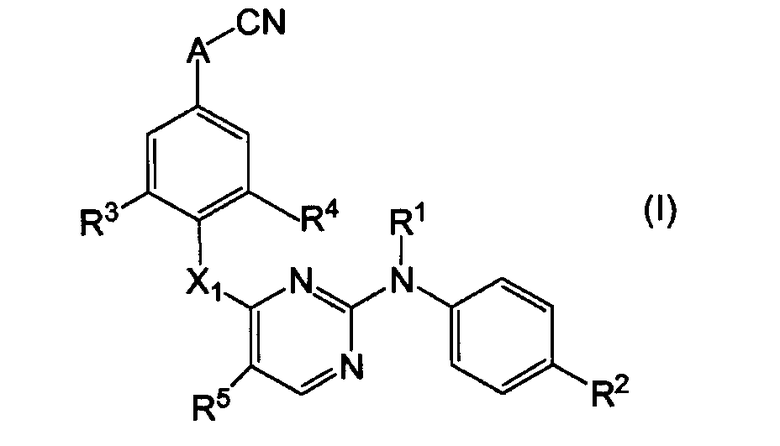
их N-оксидам, фармацевтически приемлемым аддитивным солям, четвертичным аминам или стереохимически изомерным формам, где
А означает -СН2-СН2-, -СН=СН-, -С≡С-;
каждый из R1 независимо означает водород, арил, формил, С1-6-алкилкарбонил, С1-6-алкил, С1-6-алкилоксикарбонил;
R2 означает гидрокси, галоген, С1-6-алкил, карбоксил, циано, -С(=О)R6, нитро, амино, моно- или ди(С1-6-алкил)амино, полигалогенметил;
Х1 означает -NR1-, -О-, -S-, -S(=O)p-;
R3 означает Н, С1-6-алкил, галоген;
R4 означает Н, С1-6-алкил, галоген;
R5 означает нитро, амино, моно- и ди(С1-4-алкил)амино, арил, галоген, -СО-Н, -СО-R6, -COOR7, -NH-С(=О)Н, -NH-С(=О)R6, -СН=N-О-R8;
R6 означает С1-4-алкил, амино, моно- или ди(С1-4-алкил)амино или полигалоген-С1-4-алкил;
R7 означает водород, С1-6-алкил, арил-С1-6-алкил;
R8 означает водород, С1-6-алкил, арил;
каждый р означает 1 или 2;
каждый арил означает фенил или фенил, замещенный одним, двумя, тремя, четырьмя или пятью заместителями, каждый из которых независимо выбирают из галогена, гидрокси, меркапто,
С1-6-алкила, гидрокси-С1-6-алкила, амино-С1-6-алкила, моно- или ди(С1-6-алкил)амино-С1-6-алкила, С1-6-алкилкарбонила, С3-7-циклоалкила, С1-6-алкилокси, С1-6-алкилоксикарбонила, С1-6-алкилтио, циано, нитро, полигалоген-С1-6-алкила, полигалоген-С1-6-алкилокси, аминокарбонила.
Как используется выше или в дальнейшем, термин «С1-4-алкил» в качестве группы или части группы означает насыщенные углеводородные радикалы с линейной или разветвленной цепью, имеющие 1-4 атома углерода, такие как метил, этил, пропил, 1-метилэтил, бутил; термин «С1-6-алкил» в качестве группы или части группы означает насыщенные углеводородные радикалы с линейной или разветвленной цепью, имеющие 1-6 атомов углерода, такие как группа, определенная для С1-4-алкила, и пентил, гексил, 2-метилбутил и тому подобное; термин «С1-2-алкил» означает метил или этил; термин «С3-7-циклоалкил» является общим для циклопропила, циклобутила, циклопентила, циклогексила и циклогептила. Наиболее предпочтительными среди С1-6-алкилов являются С1-4-алкил или С1-2-алкил.
Как указано выше, радикал «(=О)» образует карбонильный остаток, когда присоединен к атому углерода, сульфоксидный остаток, когда присоединен к атому серы, и сульфонильный остаток, когда два вышеуказанных радикала присоединены к атому серы.
Термины «карбоксил», «карбокси» или «гидроксикарбонил» относятся к группе -СООН.
Термин «галоген» характерен для фтора, хлора, брома и иода. Как используется в данном контексте выше и в дальнейшем, термин «полигалогенметил» в качестве группы или части группы означает моно- или полигалогензамещенный метил, в частности метил с одним или более атомами фтора, например фторметил, дифторметил или трифторметил; термин «полигалоген-С1-4-алкил» или «полигалоген-С1-6-алкил» в качестве группы или части группы означает моно- или полигалогензамещенный С1-4-алкил или С1-6-алкил, например группы, определенные в случае галогенметила, 1,1-дифторэтил, 2,2,2-трифторэтил, пентафторэтил и тому подобное. В случае, когда более чем один атомов галогена присоединены к алкильной группе, то в рамках определения «полигалогенметил», «полигалоген-С1-4-алкил» или «полигалоген-С1-6-алкил» они могут быть одинаковыми или различными.
Когда он встречается в определении соединений формулы (I) или любой из указанных в данном контексте подгрупп, каждый арил независимо имеет значение, как указанное выше в определении соединений формулы (I) или в более ограниченных определениях арила, указанных в описании.
Когда любая переменная встречается более чем один раз в любом радикале, каждое значение такой переменной является независимым.
Подразумевают, что любое из ограничений в определениях радикалов, согласно данному контексту, применимо к группе соединений формулы (I), а также к любой определенной или указанной в данном контексте подгруппе.
Проведенные линии от заместителей к циклическим системам указывают, что связь может быть присоединена к любому из подходящих атомов цикла.
Для терапевтического применения соли соединений формулы (I) являются таковыми, где противоион является фармацевтически приемлемым. Однако соли кислот и оснований, которые являются фармацевтически неприемлемыми, также могут находить применение, например, при получении или очистке фармацевтически приемлемого соединения. Все соли, являются ли они фармацевтически приемлемыми или нет, входят в рамки настоящего изобретения.
Подразумевают, что фармацевтически приемлемые аддитивные соли, как указанные выше, включают терапевтически активные, нетоксичные, аддитивные солевые формы с кислотами, которые способны образовывать соединения формулы (I). Последние пригодным образом могут быть получены путем обработки основной формы такими подходящими кислотами, как неорганические кислоты, например галогенводородные кислоты, как, например, соляная кислота, бромистоводородная кислота и тому подобное; серная кислота; азотная кислота; фосфорная кислота и тому подобное; или органические кислоты, как, например, уксусная кислота, пропановая кислота, гидроксиуксусная кислота, 2-гидроксипропановая кислота, 2-оксопропановая кислота, щавелевая кислота, малоновая кислота, янтарная кислота, малеиновая кислота, фумаровая кислота, яблочная кислота, винная кислота, 2-гидрокси-1,2,3-пропантрикарбоновая кислота, метансульфоновая кислота, этансульфоновая кислота, бензолсульфоновая кислота, 4-метилбензолсульфоновая кислота, циклогексансульфаминовая кислота, 2-гидроксибензойная кислота, 4-амино-2-гидроксибензойная кислота и тому подобные кислоты. И наоборот, солевая форма может быть превращена в форму свободного основания путем обработки щелочью.
Соединения формулы (I), содержащие кислотные протоны, можно превращать в их терапевтически активные, нетоксичные, аддитивные солевые формы с металлом или амином путем обработки соответствующими органическими или неорганическими основаниями. Соответствующие основные солевые формы включают, например, аммониевые соли; соли щелочных и щелочноземельных металлов, например соли лития, натрия, калия, магния, кальция, и тому подобное; соли с органическими основаниями, например с первичными, вторичными и третичными алифатическими и ароматическими аминами, такими как метиламин, этиламин, пропиламин, изопропиламин, четыре изомера бутиламина, диметиламин, диэтиламин, диэтаноламин, дипропиламин, диизопропиламин, ди-н-бутиламин, пирролидин, пиперидин, морфолин, триметиламин, триэтиламин, трипропиламин, хинуклидин, пиридин, хинолин или изохинолин, бензатин, N-метил-D-глюкамин, 2-амино-2-(гидроксиметил)-1,3-пропандиол, гидрабаминовые соли; и соли с аминокислотами, такими как, например, аргинин, лизин и тому подобное. И наоборот, солевая форма может быть превращена в форму свободной кислоты путем обработки кислотой.
Термин «аддитивная соль» также включает гидраты и аддитивные формы с растворителями, которые способны образовывать соединения формулы (I). Примерами таких форм являются, например, гидраты, алкоголяты и тому подобное.
Термин «четвертичный амин», как используется в данном контексте выше, означает четвертичные аммониевые соли, которые способны образовывать соединения формулы (I) путем взаимодействия между основным азотом соединения формулы (I) и подходящим кватернизующим агентом, таким как, например, необязательно замещенный алкилгалогенид, арилгалогенид или арилалкилгалогенид, например метилиодид или бензилиодид. Также можно использовать другие реагенты с пригодным образом удаляемыми группами, такие как алкилтрифторметансульфонаты, алкилметансульфонаты и алкил-п-толуолсульфонаты. Четвертичный амин содержит положительно заряженный атом азота.
Фармацевтически приемлемые противоионы включают хлор, бром, иод, трифторацетат и ацетат. Выбранный противоион можно вводить, используя ионообменные смолы.
Подразумевают, что N-оксидные формы соединений согласно настоящему изобретению включают соединения формулы (I), где один или несколько третичных атомов азота окислены до так называемых N-оксидов.
Следует принимать во внимание, что некоторые из соединений формулы (I) и их N-оксиды, аддитивные соли, четвертичные амины и стереохимически изомерные формы могут содержать один или более хиральных центров и существуют в виде стереохимически изомерных форм.
Термин «стереохимически изомерные формы», как используется в данном контексте выше, включают все возможные стереоизомерные формы, которые могут иметь соединения формулы (I) и их N-оксиды, аддитивные соли, четвертичные амины или физиологически функциональные производные. За исключением иначе указанного или определенного, химическое название соединений означает смесь всех возможных стереохимически изомерных форм, причем вышеуказанные смеси содержат все диастереомеры и энантиомеры основной молекулярной структуры, а также каждую из индивидуальных изомерных форм соединений формулы (I) и их N-оксидов, солей, сольватов или четвертичных аминов, по существу, свободных, т.е. ассоциированных с менее чем 10%, предпочтительно, менее чем 5%, в частности, менее чем 2%, и, в высшей степени предпочтительно, менее чем 1% других изомеров. Таким образом, когда соединение формулы (I), например, указано в виде (Е), это означает, что соединение является, по существу, свободным от (Z)-изомера. В частности, стереогенные центры могут иметь R- или S-конфигурацию; заместители двухвалентных циклических (частично) насыщенных радикалов могут иметь или цис-, или транс-конфигурацию.
Соединения, имеющие двойные связи, могут иметь Е(«против»)- или Z(«вместе»)-стереохимию по вышеуказанной двойной связи. Термины «цис», «транс», «R», «S», «E» и «Z» хорошо известны квалифицированному специалисту в данной области.
Стереохимически изомерные формы соединений формулы (I) входят в рамки данного изобретения.
Некоторые из соединений формулы (I) также могут существовать в их таутомерной форме. Подразумевают, что такие формы, хотя и точно не указаны в вышеприведенной формуле, входят в рамки настоящего изобретения.
Когда бы ни использовался в дальнейшем, подразумевают, что термин «соединения формулы (I)» также включает их N-оксидные формы, их соли, их четвертичные амины и их стереохимически изомерные формы. Особый интерес представляют такие соединения формулы (I), которые являются стереохимически чистыми.
Отдельные подгруппы соединений формулы (I) или любая из подгрупп соединений формулы (I), указанных в данном контексте, являются несолевыми формами, солями, N-оксидными формами и стереохимически изомерными формами. Среди них интерес представляют несолевые формы, соли и стереохимически изомерные формы. Как используется в данном контексте, термин «несолевая форма» относится к форме соединения, которое не является солью, но которое, в большинстве случаев, может быть в форме свободного основания.
Когда бы ни упоминалось выше или в дальнейшем, заместители могут быть выбраны, каждый независимо, из перечня многочисленных значений, таких как, например, для R9 и R10, подразумевая все возможные комбинации, которые химически возможны или которые приводят к химически стабильным молекулам.
Должно быть понятно, что подразумевают, что любые из подгрупп соединений формулы (I), как указано в данном контексте, также включают любые пролекарственные формы, N-оксиды, аддитивные соли, четвертичные амины, комплексы с металлами и стереохимически изомерные формы таких соединений.
Отдельные подгруппы соединений формулы (I) являются таковыми соединений формулы (I) или любой подгруппой соединений формулы (I), указанных в данном контексте, где
(а) А означает -СН2-СН2- или -СН=СН-; или где
(b) А означает -СН=СН-.
Кроме того, подгруппы соединений формулы (I) являются таковыми соединений формулы (I) или любой подгруппой соединений формулы (I), указанных в данном контексте, где
(а) R1 означает водород, формил, С1-6-алкилкарбонил, С1-6-алкил, С1-6-алкилоксикарбонил;
(b) R1 означает водород, С1-6-алкил;
(с) R1 означает водород, метил;
(d) R1 означает водород.
Кроме того, подгруппы соединений формулы (I) являются таковыми соединений формулы (I) или любой подгруппой соединений формулы (I), указанных в данном контексте, где
(а) R2 означает циано, аминокарбонил; или где
(b) R2 означает циано.
Кроме того, подгруппы соединений формулы (I) являются таковыми соединений формулы (I) или любой подгруппой соединений формулы (I), указанных в данном контексте, где
(а) Х1 означает -NR1-, -О-;
(b) Х1 означает -NR1-;
(с) Х1 означает -NH-, -N(C1-4-алкил)-, -О-;
(d) Х1 означает -NH-, -N(CH3)-, -О-;
(е) Х1 означает -NH-, -N(C1-4-алкил)-;
(f) Х1 означает -NH-, -N(CH3)- или
(g) Х1 означает -NH-.
Другие подгруппы соединений формулы (I) являются подгруппами соединений формулы (I) или любой подгруппой соединений формулы (I), указанных в данном контексте, где
(а) R3 означает Н, C1-6-алкил, галоген;
(b) R3 означает Н, C1-4-алкил, галоген;
(с) R3 означает Н, фтор, хлор, бром, метил;
(d) R3 означает Н, метил; или где
(е) R3 означает метил.
Еще другие подгруппы соединений формулы (I) являются таковыми соединений формулы (I) или любой подгруппой соединений формулы (I), указанных в данном контексте, где
(а) R4 означает Н, C1-6-алкил, галоген;
(b) R4 означает Н, C1-4-алкил, галоген;
(с) R4 означает Н, фтор, хлор, бром, метил;
(d) R4 означает Н, метил;
(е) R4 означает метил.
Еще другие подгруппы соединений формулы (I) являются таковыми соединений формулы (I) или любой подгруппой соединений формулы (I), указанных в данном контексте, где
(а) R5 означает нитро;
(b) R5 означает амино, моно- и ди(С1-4-алкил)амино, -NH-С(=О)Н, -NH-С(=О)R6;
(с) R5 означает амино, моно- и ди(С1-4-алкил)амино;
(d) R5 означает арил;
(е) R5 означает галоген;
(f) R5 означает -СО-Н-, -СО-R6, -COOR7;
(g) R5 означает -СО-Н-;
(h) R5 означает -СО-R6;
(i) R5 означает -COOR7;
(j) R5 означает -СН=N-О-R8.
Еще другие подгруппы соединений формулы (I) являются таковыми соединений формулы (I) или любой подгруппой соединений формулы (I), указанных в данном контексте, где
(а) R6 означает C1-4-алкил, амино, моно- или ди(С1-4-алкил)амино;
(b) R6 означает C1-4-алкил, амино или диметиламино;
(с) R6 означает метил, амино, моно- или диметиламино;
(d) R6 означает амино или диметиламино;
(е) R6 означает метил, амино или моно- или диметиламино, полигалогенметил.
Еще другие подгруппы соединений формулы (I) являются таковыми соединений формулы (I) или любой подгруппой соединений формулы (I), указанных в данном контексте, где
(а) R7 означает водород, C1-4-алкил; или где
(b) R7 означает водород или C1-2-алкил.
Еще другие подгруппы соединений формулы (I) являются таковыми соединений формулы (I) или любой подгруппой соединений формулы (I), указанных в данном контексте, где
(а) R8 означает водород, C1-4-алкил; или где
(b) R8 означает водород или C1-2-алкил.
Еще другие подгруппы соединений формулы (I) являются таковыми соединений формулы (I) или любой подгруппой соединений формулы (I), указанных в данном контексте, где
(а) арил означает фенил или фенил, замещенный одним, двумя или тремя заместителями, каждый из которых независимо выбирают из группы, состоящей из галогена, гидрокси, меркапто, С1-6-алкила, гидрокси-С1-6-алкила, амино-С1-6-алкила, моно- или ди(С1-6-алкил)амино-С1-6-алкила, С1-6-алкилкарбонила, С3-7-циклоалкила,
С1-6-алкилокси, С1-6-алкилоксикарбонила, С1-6-алкилтио, циано, нитро, полигалоген-С1-6-алкила, полигалоген-С1-6-алкилокси, аминокарбонила;
(b) арил означает фенил или фенил, замещенный одним, двумя или тремя заместителями, каждый из которых независимо выбирают из группы, состоящей из галогена, гидрокси, меркапто, С1-6-алкила, гидрокси-С1-6-алкила, амино-С1-6-алкила, моно- или ди(С1-6-алкил)амино-С1-6-алкила, С1-6-алкилкарбонила, С1-6-алкилокси, С1-6-алкилоксикарбонила, С1-6-алкилтио, циано, нитро, трифторметила, трифторметокси, аминокарбонила;
(с) арил означает фенил или фенил, замещенный одним, двумя или тремя заместителями, каждый из которых независимо выбирают из группы, состоящей из галогена, гидрокси, С1-6-алкила, гидрокси-С1-6-алкила, амино-С1-6-алкила, моно- или ди(С1-6-алкил)амино-С1-6-алкила, С1-6-алкилкарбонила, С1-6-алкилокси, С1-6-алкилоксикарбонила, циано, нитро, трифторметила;
(d) арил означает фенил или фенил, замещенный одним, двумя или тремя заместителями, каждый из которых независимо выбирают из группы, состоящей из галогена, гидрокси, С1-6-алкила, С1-6-алкилокси, циано, нитро, трифторметила.
Особый интерес представляют такие соединения формулы (I) или любая из подгрупп соединений формулы (I), где А означает -СН=СН- и где заместители А находятся в Е-конфигурации (т.е., так называемые «Е»-изомеры).
Соединения формулы (I) можно получать путем взаимодействия промежуточных продуктов формулы (II), где W1 означает подходящую удаляемую группу, такую как, например, галоген, например хлор, бром, тозил, мезил и тому подобные группы, с промежуточным продуктом формулы (III).
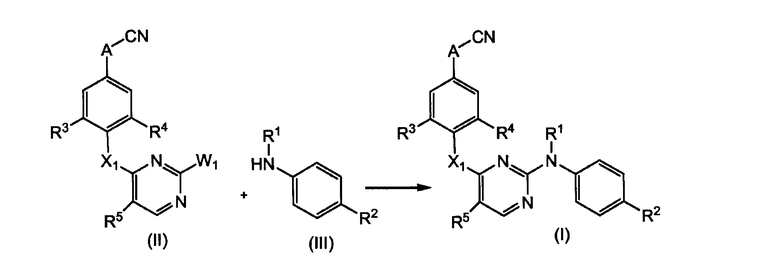
Взаимодействие производного пиримидина (II) с амином (III) обычно проводят в присутствии подходящего растворителя. Подходящими растворителями являются, например, спирт, такой как, например, этанол, 2-пропанол; биполярный апротонный растворитель, такой как ацетонитрил, N,N-диметилформамид, N,N-диметилацетамид, 1-метил-2-пирролидинон; простой эфир, такой как тетрагидрофуран, 1,4-диоксан, монометиловый эфир пропиленгликоля. Взаимодействие можно проводить в кислой среде, получаемой за счет добавляемых количеств подходящей кислоты, такой как, например, камфорсульфокислота, или за счет использования протонных растворителей, например раствора хлороводорода в алканоле, таком как 1- или 2-пропанол.
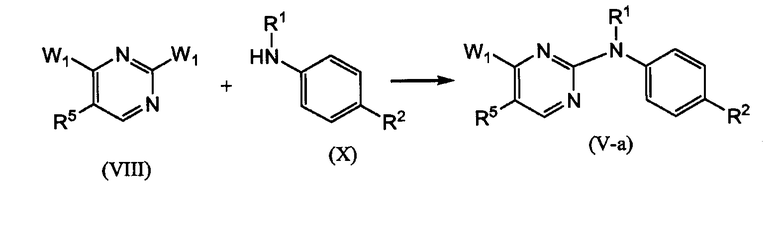
Соединения формулы (I) также можно получать путем образования Х1-связи или путем взаимодействия соединения (IV-a) c соединением (V-a) или соединения (IV-b) c соединением (V-b), как представлено на следующей схеме.
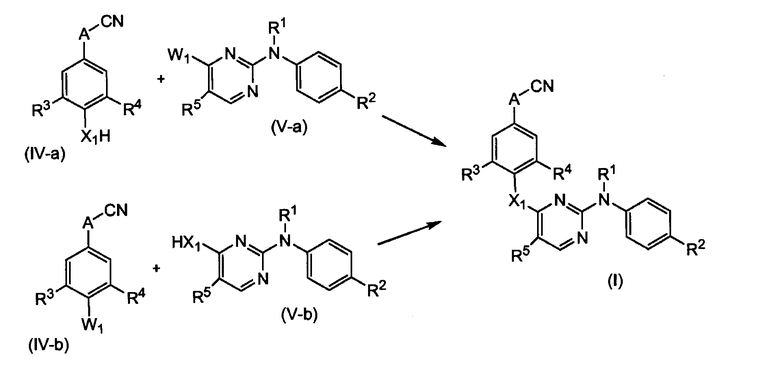
На этой реакционной схеме W1 означает подходящую удаляемую группу, которая, в частности, имеет значение, как указано выше.
В частности, соединения формулы (I), где Х1 означает NR1, вышеуказанные соединения, представленные формулой (I-a), можно получать путем взаимодействия промежуточного продукта формулы (IV-c), где W1 означает подходящую удаляемую группу, например хлор или бром, с промежуточным продуктом формулы (V-c). Удаляемую группу W1 также можно вводить in situ, например, путем превращения соответствующей гидроксильной группы в удаляемую группу, например, с помощью POCl3. Реакцию соединения (IV-c) с соединением (V-c) предпочтительно осуществляют в подходящем растворителе, в присутствии основания, например триэтиламина. Подходящими растворителями являются, например, ацетонитрил, спирты, такие как, например, этанол, 2-пропанол, этиленгликоль, пропиленгликоль, полярные апротонные растворители, такие как N,N-диметилформамид, N,N-диметилацетамид, диметилсульфоксид, 1-метил-2-пирролидинон, [bmim]PF5; простые эфиры, такие как 1,4-диоксан, монометиловый эфир пропиленгликоля.
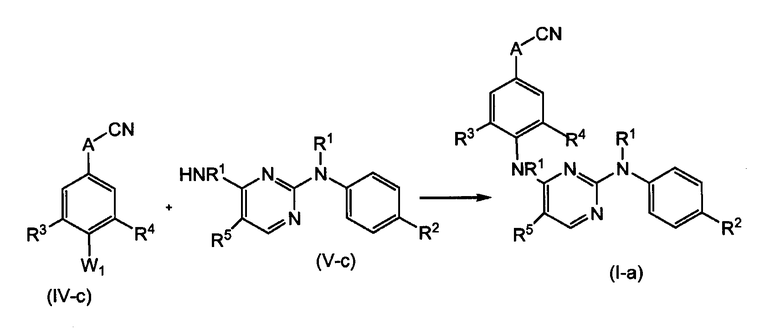
Реакция соединения (IV-а) или соединения (IV-b) с соединением (V-a) или соединением (V-b) также пригодна в случае, где Х1 означает -О- или -S-. В частности, соединения формулы (I), где Х1 означает О, вышеуказанные соединения, которые представлены формулой (I-b), можно получать путем взаимодействия промежуточного продукта формулы (VI), где W1 означает подходящую удаляемую группу, такую как, например, галоген, например хлор, и тому подобное, с промежуточным продуктом формулы (VII), в присутствии подходящего основания, такого как, например, K2CO3 или трет-бутоксид калия (трет-BuOK), и подходящего растворителя, такого как, например, ацетон или тетрагидрофуран. При конкретном осуществлении промежуточный продукт формулы (VII) сначала вводят во взаимодействие, при перемешивании и при комнатной температуре, с подходящим гидридом металла в органическом растворителе. Затем добавляют промежуточный продукт формулы (VI), где W1 означает подходящую удаляемую группу или предшественник удаляемой группы.
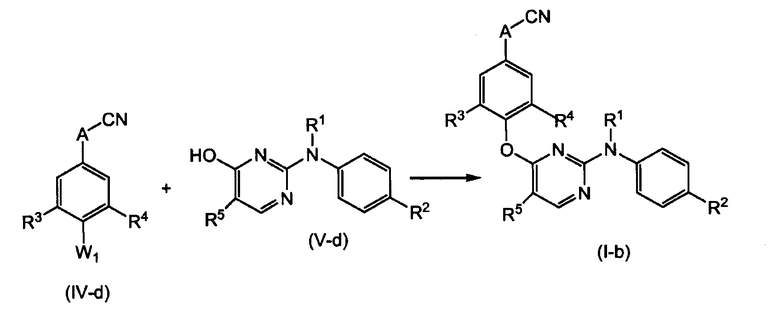
Соединения формулы (I-b) также можно получать путем взаимодействия промежуточного продукта формулы (IV-е) с промежуточным продуктом формулы (V-d), в присутствии POCl3, подходящего основания, такого как, например, K2CO3 или трет-бутоксид калия (трет-BuOK), и подходящего растворителя, такого как, например, ацетон или тетрагидрофуран.
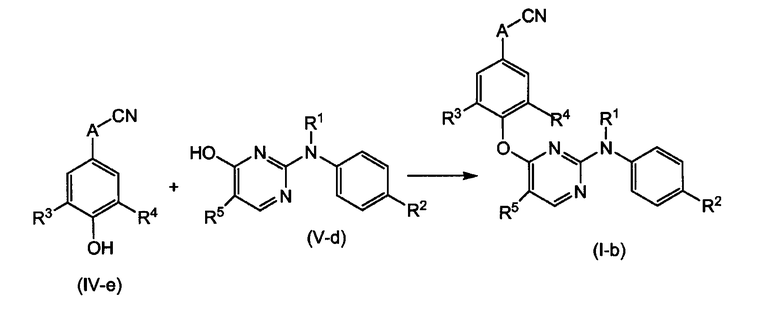
Тиосоединения (Х1 означает -S-) можно получать подобным образом и можно пригодным образом превращать в соответствующий сульфоксид или сульфон, используя известные в уровне техники способы окисления.
Соединения формулы (I-c), которые являются соединениями формулы (I), где R5 означает арил, также можно получать путем взаимодействия соединения (I-d), где W1 означает подходящую удаляемую группу, такую как, например, галоген, например хлор, бром, с арильным радикалом с особыми группами, такими как бороновая кислота (т.е. -В(ОН)2) или эфиры бороновой кислоты (т.е. -В(OR)2, где R означает алкил или алкилен, например R означает метил, этил или этилен). Этот тип реакции обычно можно осуществлять в присутствии соли меди, в частности ацетата меди (II), и к реакционной смеси может быть добавлен подходящий для прекращения реакции продукт, подобный пиридину.
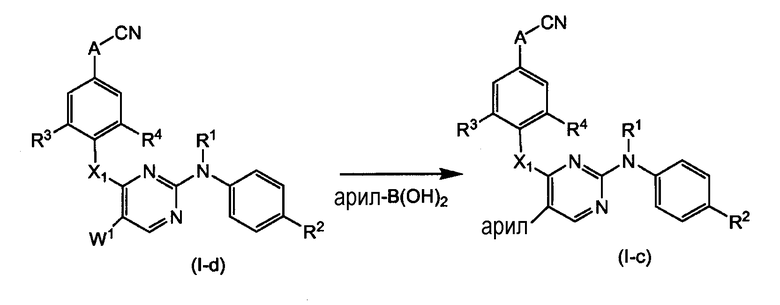
Соединения (I-d-1), которые являются соединениями формулы (I-d), где W1 означает галоген, получают, например, путем галогенирования соответствующего исходного соединения формулы (VI), которое можно получать, как описано в WO-03/016306. Другие удаляемые группы можно вводить путем замещения галоген-группы, используя подходящие реагенты.
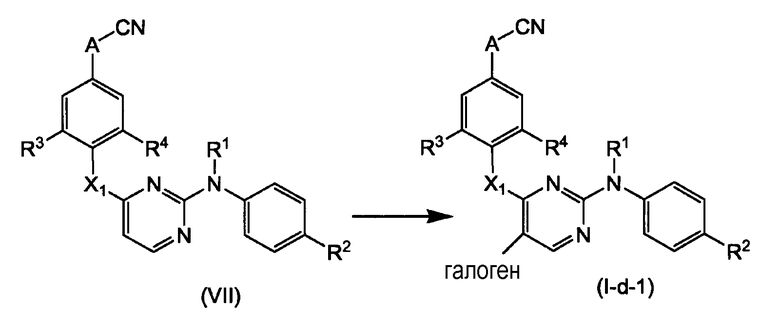
Соединения (I-d-1) можно превращать в соответствующие соединения (I-e), которые имеют группу -COOR в положении 5 пиримидинового остатка. Соединения (I-e), в свою очередь, можно превращать в соответствующие амиды (I-f).
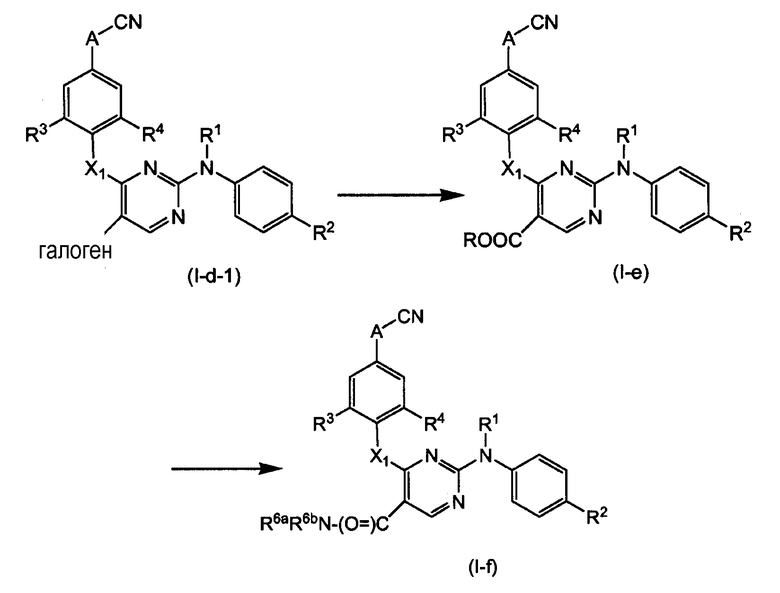
Соединения (I-g), которые являются соединениями формулы (I), где R5 означает нитрогруппу, можно превращать путем восстановления нитрогруппы до аминогруппы в соответствующие соединения (I-h), которые содержат аминогруппу в положении 5 пиримидинового остатка. Соединения (I-h), в свою очередь, можно превращать в соответствующие амиды (I-i), используя соответствующую реакцию ацилирования.
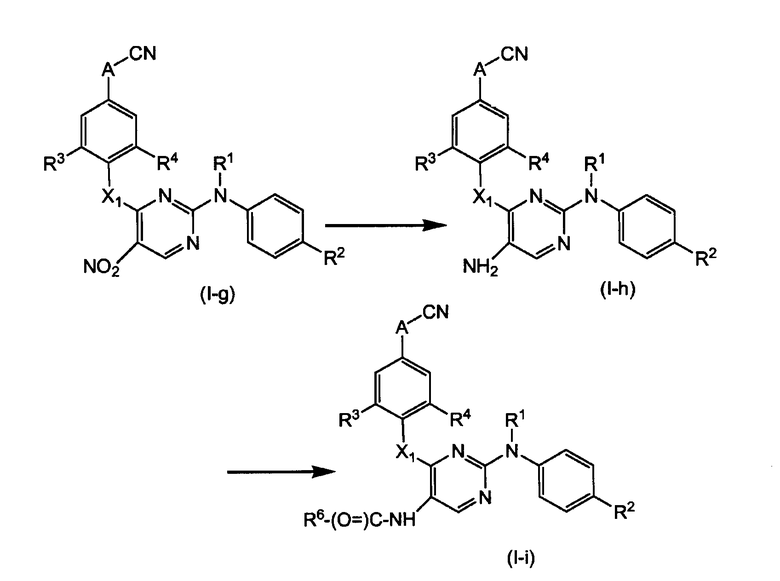
Соединения формулы (I-j), которые являются соединениями формулы (I), где R5 означает -СНО, можно получать путем взаимодействия соединений (I-d-1) с находящимся под повышенным давлением газообразным СО, в присутствии формиата натрия и подходящего катализатора, например, дихлорбис(трифенилфосфин)-палладия (II).
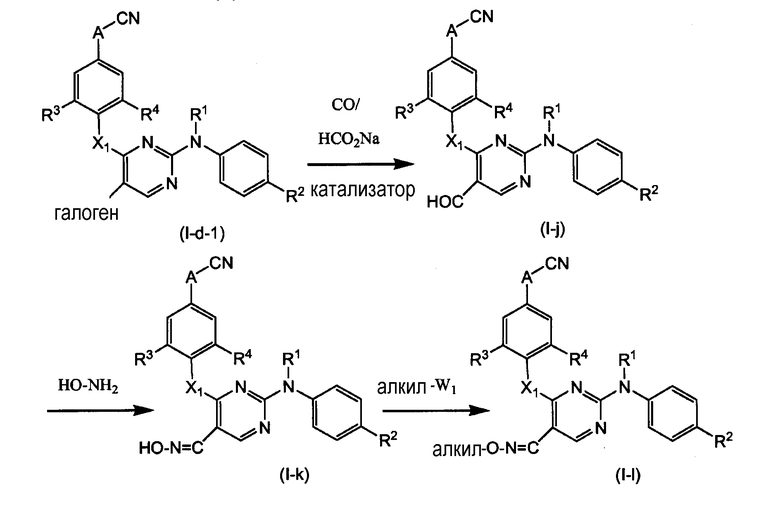
Соединения (I-j) могут быть введены во взаимодействие с гидроксиламином для получения соединений (I-k), которые, в свою очередь, можно алкилировать для получения соединений (I-l), где R5 означает алкилированный оксим. Соединения (I-j) также можно превращать непосредственно в соединения (I-l) путем взаимодействия исходных соединений (I-j) с алкилгидроксиламином.
Соединения формулы (I), далее, можно получать путем превращения соединений формулы (I) в любые другие, в соответствии с известными из уровня техники реакциями превращения групп.
Соединения формулы (I) можно превращать в соответствующие N-оксидные формы, следуя известным из уровня техники способам превращения третичного азота в его N-оксидную форму. Вышеуказанную реакцию N-окисления обычно можно осуществлять путем взаимодействия исходного соединения формулы (I) с соответствующим органическим или неорганическим пероксидом. Соответствующие неорганические пероксиды включают, например, пероксид водорода, пероксиды щелочных или щелочноземельных металлов, например пероксид натрия, пероксид калия; соответствующие органические пероксиды могут включать надкислоты, такие как, например, бензолпероксокарбоновая кислота или галогензамещенная бензолпероксокарбоновая кислота, например 3-хлорбензолпероксокарбоновая кислота; пероксоалкановые кислоты, например пероксоуксусная кислота; алкилгидропероксиды, например трет-бутилгидропероксид. Подходящими растворителями являются, например, вода, низшие спирты, например этанол, и тому подобное; углеводороды, например толуол; кетоны, например 2-бутанон; галогенированные углеводороды, например дихлорметан; и смеси таких растворителей.
Соединения формулы (I), где R3 или R4 означает водород, можно превращать в соединения формулы (I), где R3 или R4 означает галоген, путем взаимодействия с подходящим, вводящим галоген агентом, таким как, например, N-хлорсукцинимид, или N-боросукцинимид, или их комбинация, в присутствии подходящего растворителя, такого как, например, уксусная кислота.
Соединения формулы (I), где R1 означает С1-6-алкилоксикарбонил, можно превращать в соединения формулы (I), где R1 означает водород, путем взаимодействия с подходящим основанием, таким как, например, гидроксид или метоксид натрия. Там, где R1 означает трет-бутилоксикарбонил, соответствующие соединения, где R1 означает водород, можно получать путем обработки трифторуксусной кислотой.
Некоторые из соединений формулы (I) и некоторые из промежуточных продуктов согласно настоящему изобретению могут содержать асимметричный атом углерода. Стереохимически чистые изомерные формы вышеуказанных соединений и вышеуказанных промежуточных продуктов можно получать путем использования известных из уровня техники способов. Например, диастереоизомеры можно разделять физическими методами, такими как селективная кристаллизация или хроматографические способы, например противоточное распределение, жидкостная хроматография и тому подобные способы. Энантиомеры можно получать из рацемических смесей путем превращения сначала вышеуказанных рацемических смесей с помощью подходящих расщепляющих агентов, таких, как, например, хиральные кислоты, в смеси диастереомерных солей или соединений; затем путем физического разделения вышеуказанных смесей диастереомерных солей или соединений, например, с помощью селективной кристаллизации или хроматографических способов, например жидкостной хроматографии и тому подобных методов; и, наконец, путем превращения вышеуказанных разделенных диастереомерных солей или соединений в соответствующие энантиомеры. Стереохимически чистые изомерные формы также можно получать из стереохимически чистых изомерных форм соответствующих промежуточных продуктов и исходных веществ, при условии, что осуществляющиеся реакции протекают стереоспецифически.
Альтернативный способ разделения энантиомерных форм соединений формулы (I) и промежуточных продуктов включает жидкостную хроматографию, в частности жидкостную хроматографию с использованием хиральной неподвижной фазы.
Некоторые из промежуточных продуктов и исходных веществ являются известными соединениями и могут быть коммерчески доступны или их можно получать в соответствии с известными из уровня техники способами.
Промежуточные соединения формулы (II) можно получать путем взаимодействия промежуточного продукта формулы (VIII), где W1 имеет значение, как описано выше, с промежуточным продуктом формулы (IX), в присутствии подходящего растворителя, такого как, например, тетрагидрофуран, и, необязательно, в присутствии подходящего основания, такого как, например, Na2CO3.
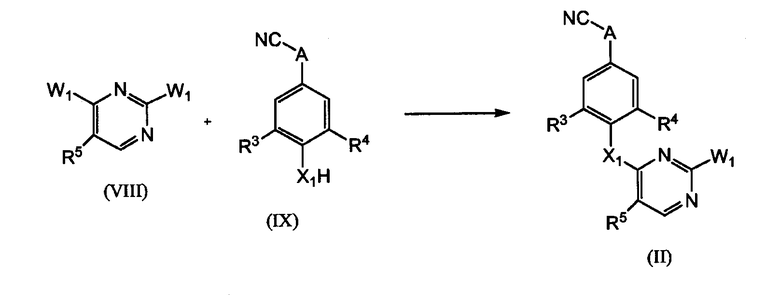
Промежуточные продукты формулы (VIII) можно получать в соответствии с известными из уровня техники способами.
Промежуточные продукты формулы (V-a) и формулы (V-b) можно получать следующим образом:
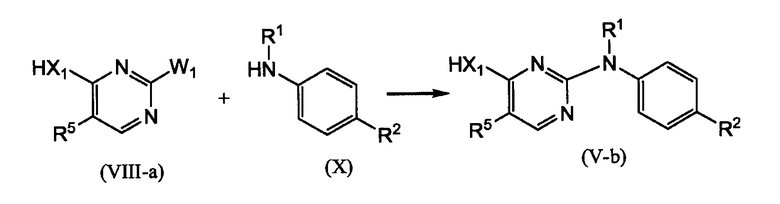
Промежуточные продукты формулы (III) или формулы (IV-а), где R1 означает водород или Х1 означает NH, вышеуказанные промежуточные продукты, представленные формулами (III-а) и (IV-а-1), можно получать путем взаимодействия промежуточного продукта формулы (XI) или формулы (XII) с подходящим восстановителем, таким как Fe, в присутствии NH4Cl и подходящего растворителя, такого как, например, тетрагидрофуран, Н2О и спирт, например метанол, и тому подобное.
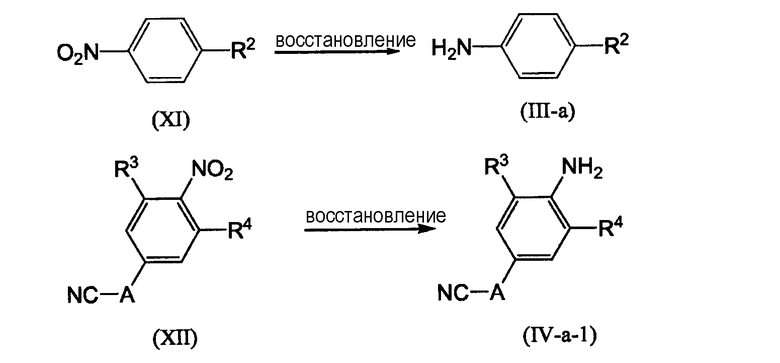
Промежуточные продукты формулы (III-а), где А означает -СН2-СН2-, вышеуказанные промежуточные продукты, представленные формулой (III-а-1), можно получать путем взаимодействия промежуточного продукта формулы (XII-а) с Pd/C, в присутствии подходящего растворителя, такого как, например, спирт, например этанол, и тому подобное.
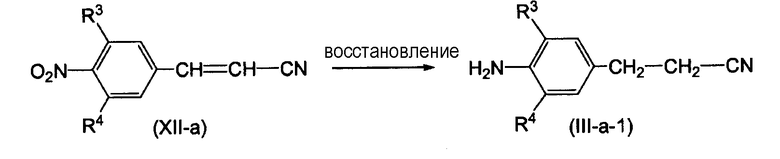
Промежуточные продукты формулы (XII-а) можно получать путем взаимодействия промежуточного продукта формулы (XIII) с диэтилцианометилфосфонатом в присутствии подходящего основания, такого как, например, NaOCH3, и подходящего растворителя, такого как, например, тетрагидрофуран.
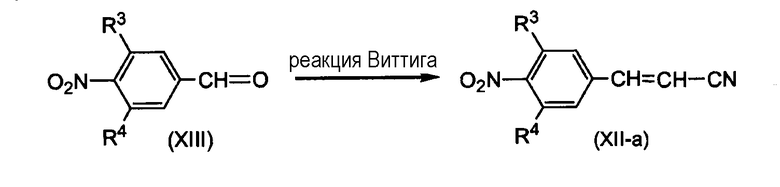
Промежуточные продукты формулы (XIII) можно получать путем взаимодействия промежуточного продукта формулы (XIV) с подходящим окислителем, таким как, например, MnO2, в присутствии подходящего растворителя, такого как, например, ацетон.
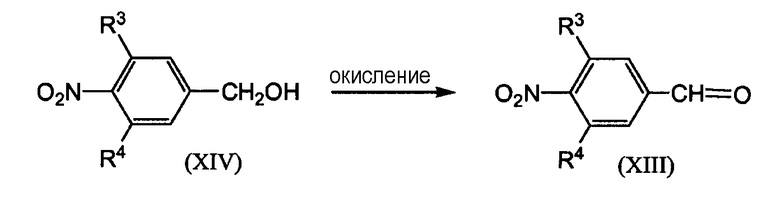
Промежуточные продукты формулы (XIV) можно получать путем взаимодействия промежуточного продукта формулы (XV) с NaBH4 в присутствии этилхлорформиата, подходящего основания, такого как, например, N,N-диэтилэтанамин, подходящего растворителя, такого как, например, тетрагидрофуран.
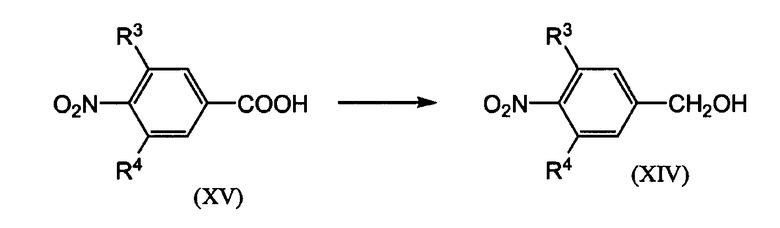
Промежуточные продукты формулы (XI) и формулы (XII) можно получать путем взаимодействия промежуточного продукта формулы (XVI) соответственно, формулы (XVII), с HNO3, NaNO3 или KNO3, в присутствии H2SO4, AcOH или CH3SO3H.
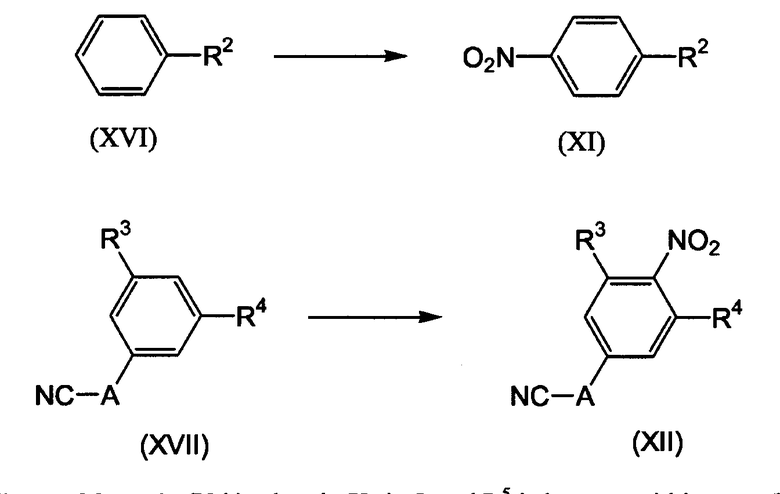
Промежуточные продукты формулы (V-b), где Х1 означает О и R5 означает бром, вышеуказанные промежуточные продукты, представленные формулой (V-b-1), можно получать из промежуточных продуктов формулы (XVIII) путем взаимодействия с Br2, в присутствии подходящего основания, такого как, например, N,N-диэтилэтанамин, и подходящего растворителя, такого как, например, диметилсульфоксид.
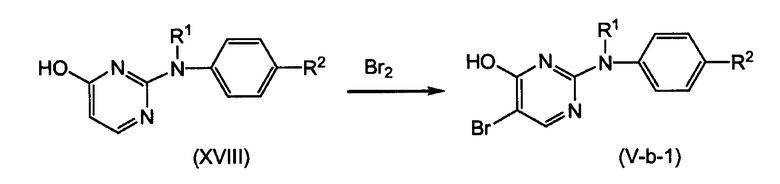
Промежуточные продукты формулы (V-b-1) можно превращать в промежуточные продукты формулы (V-а), где R5 и W1 означают хлор, вышеуказанные промежуточные продукты, представленные формулой (V-а-1), путем взаимодействия с POCl3.
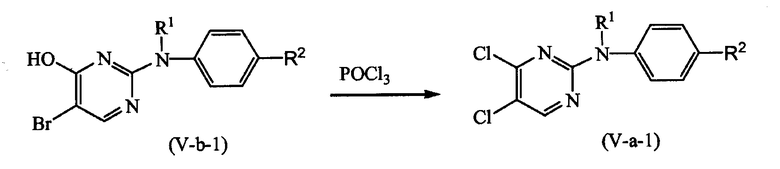
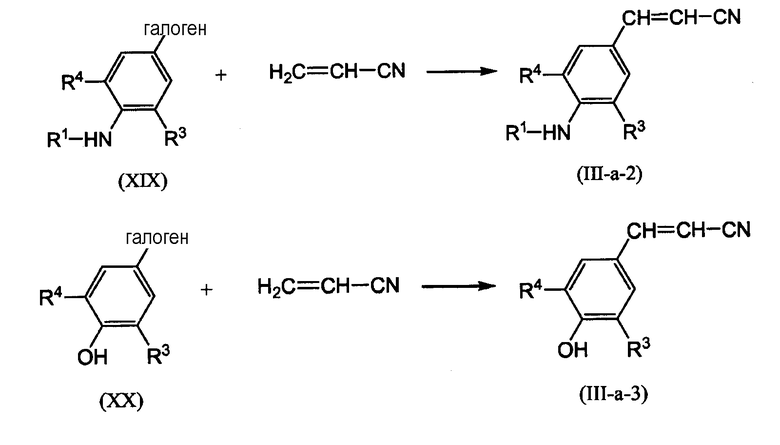
Промежуточные продукты формулы (III-a), где А означает -СН=СН- и Х1 означает NH или О, вышеуказанные промежуточные продукты, представленные формулой (III-a-2) соответственно, формулой (III-a-3), также можно получать из промежуточных продуктов формулы (XIX) соответственно формулы (ХХ), путем взаимодействия с Н2С=СН-CN в присутствии Pd(OAc)2, P(o-Tol)3, подходящего основания, такого как, например, N,N-диэтилэтанамин, и подходящего растворителя, такого как, например, СН3-CN.
Соединения формулы (I) проявляют антиретровирусные свойства (ингибирующие обратную транскриптазу свойства), в частности, против вируса иммунодефицита человека (ВИЧ), который является этиологическим агентом синдрома приобретенного иммунодефицита (СПИД) у людей. Вирус ВИЧ предпочтительно инфицирует человеческие Т-4-клетки и разрушает их или изменяет их нормальную функцию, в особенности координацию иммунной системы. В результате инфицированный пациент всегда имеет уменьшающееся количество Т-4-клеток, которые, кроме того, ведут себя аномально. Следовательно, иммунологическая защитная система неспособна бороться с инфекциями и новообразованиями, и ВИЧ-инфицированный субъект обычно умирает от инфекций, вызываемых условно-патогенными микроорганизмами, таких как пневмония, или от раковых заболеваний. Другие состояния, связанные с ВИЧ-инфекцией, включают тромбоцитопению, саркому Капоши и инфекцию центральной нервной системы, характеризующуюся прогрессирующей демиелинизацией, которая приводит, в результате, к деменции и симптомам, таким как прогрессирующая дизартрия, атаксия и дезориентация. ВИЧ-инфекция, далее, также ассоциируется с периферической невропатией, прогрессирующей генерализованной лимфаденопатией (PGL) и СПИД-связанным комплексом (ARC).
Соединения согласно настоящему изобретению также проявляют активность против резистентных ко многим лекарственным средствам штаммов ВИЧ, в частности, резистентных ко многим лекарственным средствам штаммам ВИЧ-1, более того, в особенности, соединения согласно настоящему изобретению проявляют активность против штаммов ВИЧ, главным образом, штаммов ВИЧ-1, которые обладают приобретенной резистентностью к одному или более, известным из уровня техники, ингибиторам ненуклеозидной обратной транскриптазы. Известные в данной области ингибиторы ненуклеозидной обратной транскриптазы являются ингибиторами ненуклеозидной обратной транскриптазы, другими, чем соединения согласно настоящему изобретению, и известны квалифицированному специалисту в данной области, в частности, как коммерчески доступные ингибиторы ненуклеозидной обратной транскриптазы. Соединения согласно настоящему изобретению также обладают незначительной или «не связующей» аффинностью к человеческому α-1-кислотному гликопротеину; человеческий α-1-кислотный гликопротеин не подвергается или только слабо подвергается воздействию анти-ВИЧ-активности соединений согласно настоящему изобретению.
Вследствие их антиретровирусных свойств, особенно их анти-ВИЧ-свойств, главным образом, их анти-ВИЧ-1-активности, соединения формулы (I), их N-оксиды, фармацевтически приемлемые аддитивные соли, четвертичные амины и стереохимически изомерные формы, пригодны при лечении индивидуумов, инфицированных ВИЧ, и для профилактики этих инфекций. Обычно соединения согласно настоящему изобретению могут быть пригодны при лечении теплокровных животных, инфицированных вирусами, чье существование опосредовано или зависит от фермента, обратной транскриптазы. Состояния, которые можно предотвращать или лечить с помощью соединений согласно настоящему изобретению, главным образом, являются состояниями, связанными с ВИЧ и другими патогенными ретровирусами, включая СПИД, связанный со СПИДом комплекс (ARC), прогрессирующую генерализованную лимфаденопатию (PGL), а также хронические заболевания центральной нервной системы, вызванные ретровирусами, такие как, например, опосредуемая ВИЧ деменция и рассеянный склероз.
Соединения согласно настоящему изобретению или любую их подгруппу, следовательно, можно использовать в качестве лекарственных средств против вышеуказанных состояний. Вышеуказанное использование в качестве лекарственного средства или способ лечения включает введение ВИЧ-инфицированным субъектам эффективного количества соединений для борьбы с состояниями, связанными с ВИЧ и другими патогенными ретровирусами, главным образом с ВИЧ-1. В частности, соединения формулы (I) можно использовать для получения лекарственного средства в целях лечения или предотвращения ВИЧ-инфекций.
С точки зрения полезности соединений формулы (I) предусматривают способ лечения теплокровных животных, включая людей, страдающих от вирусных инфекций, или способ предохранения теплокровных животных, включая людей, от страдания от вирусных инфекций, главным образом от ВИЧ-инфекций. Вышеуказанный способ включает введение, предпочтительно, пероральное введение, эффективного количества соединения формулы (I), его N-оксидной формы, фармацевтически приемлемой аддитивной соли, четвертичного амина или возможной стереоизомерной формы, теплокровным животным, включая людей.
Настоящее изобретение также относится к композициям для лечения вирусных инфекций, содержащим терапевтически эффективное количество соединения формулы (I) и фармацевтически приемлемый носитель или разбавитель.
Соединения согласно настоящему изобретению или их любая подгруппа могут быть использованы для получения различных фармацевтических форм для целей введения. В качестве подходящих композиций можно назвать все композиции, обычно применяемые для систематически вводимых лекарственных средств. Для получения фармацевтических композиций согласно данному изобретению эффективное количество конкретного соединения, необязательно в форме аддитивной соли, в качестве активного ингредиента, комбинируют, при тщательном смешении, с фармацевтически приемлемым носителем, который может иметь большое разнообразие форм в зависимости от готовой лекарственной формы, желательной для введения. Эти фармацевтические композиции желательны в унифицированной лекарственной форме, пригодной, в особенности, для перорального введения, ректального введения, чрескожного введения или парентеральной инъекции. Например, при получении композиций в виде пероральной лекарственной формы можно использовать любую из обычных фармацевтических сред, такую как, например, вода, гликоли, масла, спирты и тому подобное, в случае пероральных жидких готовых лекарственных форм, таких как суспензии, сиропы, эликсиры, эмульсии и растворы; или твердые носители, такие как крахмалы, сахара, каолин, разбавители, смазочные вещества, связующие вещества, дезинтегрирующие агенты и тому подобное, в случае порошков, пилюль, капсул и таблеток.
Вследствие легкости их введения таблетки и капсулы представляют собой наиболее выгодные пероральные унифицированные лекарственные формы, в случае которых обычно используют твердые фармацевтические носители. В случае парентеральных композиций носитель обычно включает стерильную воду, по меньшей мере, большей частью, несмотря на то, что могут быть включены другие ингредиенты, например, для способствования растворимости. Могут быть получены инъецируемые растворы, в которых носитель включает насыщенный солевой раствор, раствор глюкозы или смесь насыщенного солевого раствора и раствора глюкозы. Также могут быть получены инъецируемые суспензии, в случае которых могут быть использованы подходящие жидкие носители, суспендирующие агенты и тому подобное. Также сюда входят твердые готовые лекарственные формы, которые предназначены для превращения, незадолго до использования, в жидкие готовые лекарственные формы. В композициях, пригодных для чрескожного введения, носитель необязательно включает улучшающий пенетрацию агент и/или пригодное смачивающее вещество, необязательно комбинированное с пригодными добавками любой природы в небольших количествах, причем добавки не оказывают значительного пагубного воздействия на кожу. Вышеуказанные добавки могут облегчать введение в кожу и/или могут быть полезны для получения желательных композиций. Эти композиции можно вводить различными путями, например в виде трансдермального пластыря, в виде притирания, в виде мази. Соединения согласно настоящему изобретению также можно вводить путем ингаляции или инсуффляции посредством способов и при использовании готовых лекарственных форм, применяемых в данной области для введения этим путем. Таким образом, обычно, соединения согласно настоящему изобретению можно вводить в легкие в форме раствора, суспензии или сухого порошка. Любая система, разработанная для доставки растворов, суспензий или сухих порошков посредством пероральной или назальной ингаляции или инсуффляции, пригодна для введения соединений согласно настоящему изобретению.
Для способствования растворимости соединений формулы (I) в композиции можно включать подходящие ингредиенты, например циклодекстрины. Соответствующими циклодекстринами являются α-, β-, γ-циклодекстрины или их простые эфиры и смешанные простые эфиры, где одна или более гидроксильных групп ангидроглюкозных звеньев циклодекстрина замещены С1-6-алкилом, особенно метилом, этилом или изопропилом, как, например, статистически метилированный β-CD; гидрокси-С1-6-алкилом, особенно гидроксиэтилом, гидроксипропилом или гидроксибутилом; карбокси-С1-6-алкилом, особенно карбоксиметилом или карбоксиэтилом; С1-6-алкилкарбонилом, особенно ацетилом. В особенности, заслуживающими внимания в качестве комплексообразователей и/или солюбилизаторов являются β-CD, статистически метилированный β-CD, 2,6-диметил-β-CD, 2-гидроксиэтил-β-CD, 2-гидроксипропил-β-CD и (2-карбоксиметокси)пропил-β-CD, и, в частности, 2-гидроксипропил-β-CD (2-НР-β-CD).
Термин «смешанный простой эфир» означает производные циклодекстрина, где, по меньшей мере, две гидроксильные группы циклодекстрина превращены в простые эфиры с разными группами, такими как, например, гидроксипропил и гидроксиэтил.
Среднее молярное замещение (M.S.) используют в качестве меры среднего числа молей алкоксильных единиц на моль ангидроглюкозы. Средняя степень замещения (D.S.) относится к среднему числу замещенных гидроксильных групп на единицу ангидроглюкозы. Значения М.S. и D.S. могут быть определены различными аналитическими методами, такими как ядерный магнитный резонанс (ЯМР), масс-спектрометрия (МС) и инфракрасная спектроскопия (ИК). В зависимости от используемого метода могут быть получены незначительно различающиеся значения для одного данного производного циклодекстрина. Предпочтительно, при измерении с помощью масс-спектрометрии, М.S. колеблется в пределах от 0,125 до 10, а D.S. колеблется в пределах от 0,125 до 3.
Другие пригодные композиции для перорального или ректального введения включают частицы, состоящие из твердой дисперсии, содержащей соединение формулы (I) и один или более подходящих, фармацевтически приемлемых, растворимых в воде полимеров.
Термин «твердая дисперсия», используемый в дальнейшем, относится к системе в твердом состоянии (в отличие от жидкого или газообразного состояния), включающей, по меньшей мере, два компонента, например соединение формулы (I) и растворимый в воде полимер, где один компонент более или менее равномерно диспергирован в другом компоненте или компонентах (когда включают дополнительные, фармацевтически приемлемые агенты для получения готовой лекарственной формы, как правило, известные в данной области, такие как пластификаторы, консерванты и тому подобное). Когда вышеуказанная дисперсия компонентов является такой, что система химически и физически совершенно однородна или гомогенна или состоит из одной фазы, как определено в термодинамике, такую твердую дисперсию можно назвать «твердым раствором». Твердые растворы являются предпочтительными физическими системами, так как компоненты в них обычно без труда биодоступны организмам, в которые они введены. Это преимущество можно, вероятно, объяснить легкостью, с которой вышеуказанные твердые растворы могут образовывать жидкие растворы, когда происходит контакт с жидкой средой, такой как желудочно-кишечный сок. Легкость растворения можно приписать, по меньшей мере, отчасти тому факту, что энергия, необходимая для растворения компонентов из твердого раствора, меньше, чем таковая, необходимая для растворения компонентов из кристаллической или микрокристаллической твердой фазы.
Термин «твердая дисперсия» также включает дисперсии, которые являются во всех отношениях менее гомогенными, чем твердые растворы. Такие дисперсии не являются химически и физически совершенно однородными по всей фазе или включают более чем одну фазу. Например, термин «твердая дисперсия» также относится к системе, имеющей области или небольшие зоны, где аморфное, микрокристаллическое или кристаллическое соединение формулы (I), или аморфный, микрокристаллический или кристаллический водорастворимый полимер, или они оба, более или менее равномерно диспергированы в другой фазе, включающей растворимый в воде полимер или соединение формулы (I) или твердый раствор, содержащий соединение формулы (I) и растворимый в воде полимер. Вышеуказанные области являются зонами твердой дисперсии, отчетливо заметными за счет физической особенности: малые по размеру и по случаю и статистически распределенные в твердой дисперсии.
Существуют различные способы получения твердых дисперсий, включающие экструзию из расплава, сушку распылением и растворение-выпаривание.
Способ растворения-выпаривания включает следующие стадии:
а) растворение соединения формулы (I) и водорастворимого полимера в подходящем растворителе, необязательно при повышенных температурах;
b) нагревание раствора, полученного согласно пункту а), необязательно в вакууме, вплоть до испарения растворителя. Раствор также можно выливать на большую поверхность для образования тонкой пленки и оттуда выпаривать растворитель.
В случае способа сушки распылением два компонента также растворяют в подходящем растворителе и полученный раствор затем распыляют через насадку распылительной сушилки с последующим испарением растворителя из полученных капель при повышенных температурах.
Предпочтительным способом получения твердых дисперсий является процесс экструзии из расплава, включающий следующие стадии:
а) смешение соединения формулы (I) и соответствующего растворимого в воде полимера;
b) необязательно смешение добавок с полученной таким образом смесью;
с) нагревание и компаундирование таким образом полученной смеси вплоть до получения гомогенного расплава;
d) продавливание таким образом полученного расплава через одну или более насадок; и
е) охлаждение расплава вплоть до его отверждения.
Термины «расплав» и «плавление» могут быть широко интерпретированы. Эти термины означают не только изменение от твердого состояния до жидкого состояния, но также могут относиться к переходу в стекловидное состояние или каучукообразное состояние, при котором возможно включение одного компонента смеси более или менее гомогенно в другой компонент. В отдельных случаях, один компонент расплавляется, а другой(ие) компонент(ы) растворяется(ются) в расплаве, таким образом, образуя раствор, который после охлаждения может давать твердый раствор, обладающий благоприятными в отношении растворения свойствами.
После образования твердых дисперсий, как раскрыто выше, полученные продукты необязательно можно измельчать и отфильтровывать.
Продукт в виде твердой дисперсии можно измельчать или размалывать до частиц, имеющих размер менее чем 600 мкм, предпочтительно, менее чем 400 мкм, и, наиболее предпочтительно, менее чем 125 мкм.
Частицы, полученные, как описано выше, можно затем использовать для получения обычными способами фармацевтических лекарственных форм, таких как таблетки и капсулы.
Следует принимать во внимание, что квалифицированный специалист в данной области способен оптимизировать параметры способов получения твердой дисперсии, как описано выше, такие как наиболее подходящий растворитель, рабочая температура, тип используемой аппаратуры, скорость сушки распылением, пропускная способность экструдера для расплава.
Водорастворимые полимеры в частицах представляют собой полимеры, которые имеют кажущуюся вязкость, когда растворены при температуре 20°С в водном растворе с концентрацией 2% (мас./об.), составляющую 1-5000 мПа·с, более предпочтительно, 1-700 мПа·с, и, наиболее предпочтительно, 1-100 мПа·с. Например, пригодные водорастворимые полимеры включают алкилцеллюлозы, гидроксиалкилцеллюлозы, гидроксиалкилалкилцеллюлозы, карбоксиалкилцеллюлозы, соли щелочных металлов карбоксиалкилцеллюлоз, карбоксиалкилалкилцеллюлозы, сложные эфиры карбоксиалкилцеллюлозы, крахмалы, пектины, производные хитина, ди-, олиго- и полисахариды, такие как трегалоза, альгиновая кислота или их соли щелочных металлов или аммониевые соли, каррагенаны, галактоманнаны, трагакант, агар-агар, гуммиарабик, гуаровая смола и гуммиксантан, полиакриловые кислоты и их соли, полиметакриловые кислоты и их соли, сополимеры на основе метакрилатов, поливиниловый спирт, поливинилпирролидон, сополимеры поливинилпирролидона с винилацетатом, комбинации поливинилового спирта и поливинилпирролидона, полиалкиленоксиды и сополимеры этиленоксида и пропиленоксида. Предпочтительными растворимыми в воде полимерами являются гидроксипропилметилцеллюлозы.
Также один или более циклодекстринов можно использовать в качестве растворимого(ых) в воде полимера(ов) при получении вышеуказанных частиц, как описано в WO-97/18839. Вышеуказанные циклодекстрины включают фармацевтически приемлемые незамещенные и замещенные циклодекстрины, известные в данной области, более предпочтительно, α-, β- или γ-циклодекстрины, или их фармацевтически приемлемые производные.
Замещенные циклодекстрины, которые можно использовать для получения вышеописанных частиц, включают простые полиэфиры, описанные в патенте США 3459731. Далее, замещенные циклодекстрины являются простыми эфирами, где водород одной или более гидроксильных групп циклодекстрина замещен С1-6-алкилом, гидрокси-С1-6-алкилом, карбокси-С1-6-алкилом или С1-6-алкилоксикарбонил-С1-6-алкилом или их смешанными простыми эфирами. В частности, такие замещенные циклодекстрины являются простыми эфирами, где водород одной или более гидроксильных групп циклодекстрина замещен С1-3-алкилом, гидрокси-С2-4-алкилом или карбокси-С1-2-алкилом, или еще, в частности, метилом, этилом, гидроксиэтилом, гидроксипропилом, гидроксибутилом, карбоксиметилом или карбоксиэтилом.
В особенности пригодными являются простые эфиры β-циклодекстрина, например диметил-β-циклодекстрин, как описано M. Nogradi в Drugs of the Future, том 9, № 8, сс.577-578 (1984), и простые полиэфиры, например гидроксипропил-β-циклодекстрин и гидроксиэтил-β-циклодекстрин. Таким простым алкиловым эфиром может быть метиловый эфир со степенью замещения от примерно 0,125 до 3, например от примерно 0,3 до 2. Такой гидроксипропилциклодекстрин, например, может образоваться при взаимодействии β-циклодекстрина с пропиленоксидом и может иметь значение MS от примерно 0,125 до 10, например от примерно 0,3 до 3.
Другим типом замещенных циклодекстринов являются сульфобутилциклодекстрины.
Соотношение соединения формулы (I) к растворимому в воде полимеру можно широко варьировать. Например, можно использовать соотношения от 1/100 до 100/1. Представляющие интерес соотношения соединения формулы (I) к циклодекстрину составляют от примерно 1/10 до 10/1. Представляющие больший интерес соотношения составляют от примерно 1/5 до 5/1.
Далее, может быть пригодно получение соединений формулы (I) в форме наночастиц, которые включают модификатор поверхности, адсорбированный на их поверхности, в количестве, достаточном для поддержания эффективного среднего размера частиц менее чем 1000 нм. Подразумевают, что пригодные модификаторы поверхности включают таковые, которые физически сцепляются с поверхностью соединения формулы (I), но не за счет химической связи с вышеуказанным соединением.
Пригодные модификаторы поверхности предпочтительно могут быть выбраны из известных органических и неорганических фармацевтических эксципиентов. Такие эксципиенты включают различные полимеры, олигомеры с низкой молекулярной массой, натуральные продукты и поверхностно-активные вещества. Предпочтительные модификаторы поверхности включают неионные и анионные поверхностно-активные вещества.
Еще другой представляющий интерес путь использования соединений формулы (I) для получения готовых лекарственных форм включает фармацевтическую композицию, где соединения формулы (I) внедрены в гидрофильные полимеры, и применение этой смеси в качестве покровной пленки для множества маленьких гранул, таким образом, получая композицию, которую можно без труда перерабатывать и которая пригодна для получения фармацевтических лекарственных форм для перорального введения.
Такие гранулы обладают центральным, округленным или сферическим ядром, покровной пленкой из гидрофильного полимера и соединения формулы (I) и, необязательно, герметизирующим покровным слоем.
Вещества, пригодные для использования в качестве ядер в гранулах, разнообразны, при условии, что вышеуказанные вещества являются фармацевтически приемлемыми и имеют подходящие размеры и плотность. Примерами таких веществ являются полимеры, неорганические вещества, органические вещества и сахариды и их производные.
Особенно выгодным является приготовление вышеуказанных фармацевтических композиций в унифицированной лекарственной форме для легкости введения и единообразия дозировки. Унифицированная лекарственная форма, как используется в данном контексте, относится к физически дискретным единицам, пригодным в качестве унифицированных доз, причем каждая унифицированная доза содержит предопределенное количество активного ингредиента, рассчитанное для достижения желательного терапевтического эффекта, в сочетании с требующимся фармацевтическим носителем. Примерами таких унифицированных лекарственных форм являются таблетки (включая таблетки с насечкой или с нанесенным покрытием), капсулы, пилюли, пакетированные порошки, облатки, суппозитории, инъецируемые растворы или суспензии и тому подобное и их отдельные вариации.
Специалист в данной области при лечении ВИЧ-инфекции может определить эффективное суточное количество из результатов теста, представленных в данном контексте. Обычно предполагают, что эффективное суточное количество составляет от 0,01 мг/кг до 50 мг/кг массы тела, более предпочтительно, от 0,1 мг/кг до 10 мг/кг массы тела. Оно может быть подходящим для введения требуемой дозы в виде двух, трех, четырех или более субдоз через соответствующие интервалы в течение суток. Вышеуказанные субдозы можно приготовлять в виде унифицированных лекарственных форм, например, содержащих 1-1000 мг, и, в особенности, 5-200 мг активного ингредиента на унифицированную лекарственную форму.
Точная дозировка и частота введения зависят от используемого конкретного соединения формулы (I), конкретного излечиваемого состояния, тяжести излечиваемого состояния, возраста, массы и общего физического состояния конкретного пациента, а также использования другой лекарственной терапии для индивидуума, которая хорошо известна квалифицированному специалисту в данной области. Кроме того, очевидно, что вышеуказанное эффективное суточное количество может быть уменьшено или увеличено в зависимости от ответной реакции подвергаемого лечению субъекта и/или в зависимости от оценки врача, назначающего прием соединений согласно настоящему изобретению. Указанные выше диапазоны эффективного суточного количества, следовательно, являются только рекомендуемыми и не предназначены для ограничения рамок настоящего изобретения или использования данного изобретения в любом объеме.
Соединения формулы (I) согласно настоящему изобретению можно использовать отдельно или в комбинации с другими терапевтическими агентами, такими как противовирусные средства, антибиотики, иммуномодуляторы или вакцины для лечения вирусных инфекций. Их можно также использовать отдельно или в комбинации с другими профилактическими агентами для предотвращения вирусных инфекций. Соединения согласно настоящему изобретению можно использовать в вакцинах и способах защиты индивидуумов против вирусных инфекций на длительный период времени. Соединения можно использовать в таких вакцинах или отдельно, или совместно с другими соединениями согласно данному изобретению, или совместно с другими противовирусными агентами, до известной степени совместимыми со стандартным применением ингибиторов обратной транскриптазы в вакцинах. Таким образом, соединения согласно настоящему изобретению можно комбинировать с фармацевтически приемлемыми вспомогательными средствами, обычно применяемыми в вакцинах, и вводить в профилактически эффективных количествах для защиты индивидуумов на длительный период времени против ВИЧ-инфекций.
Также комбинации одного или более дополнительных антиретровирусных соединений и соединения формулы (I) можно использовать в качестве лекарственного средства. Таким образом, настоящее изобретение также относится к продукту, содержащему (а) соединение формулы (I) и (b) одно или более дополнительных антиретровирусных соединений, в качестве комбинированного препарата для одновременного, раздельного или последовательного использования при анти-ВИЧ-лечении. Различные лекарственные средства можно комбинировать в одном препарате вместе с фармацевтически приемлемыми носителями. Вышеуказанные другие антиретровирусные соединения могут быть известными антиретровирусными соединениями, такими как сурамин, пентамидин, тимопентин, кастаноспермин, декстран (декстрансульфат), фоскарнет-натрий (тринатрийфосфоноформиат); ингибиторы нуклеозидной обратной транскриптазы, например, зидовудин (3'-азидо-3'-дезокситимидин, AZT), диданозин (2',3'-дидезоксиинозин; ddI), залцитабин (дидезоксицитидин, ddC) или ламивудин (2',3'-дидезокси-3'-тиацитидин, 3ТС), ставудин (2',3'-дидегидро-3'-дезокситимидин, d4T), абакавир и тому подобное; ингибиторы ненуклеозидной обратной транскриптазы, такие как невирапин (11-циклопропил-5,11-дигидро-4-метил-6Н-дипиридо[3,2-b:2',3'-e][1,4]диазепин-6-он), эфавиренц, делавирдин, ТМС-120, ТМС-125 и тому подобное; ингибиторы фосфонатной обратной транскриптазы, например, тенофовир и тому подобное; соединения типа TIBO (тетрагидроимидазо[4,5,1-jk][1,4]бензодиазепин-2(1Н)-он и тион), например (S)-8-хлор-4,5,6,7-тетрагидро-5-метил-6-(3-метил-2-бутенил)имидазо[4,5,1-jk][1,4]бензодиазепин-2(1Н)-тион; соединения типа α-АРА (α-анилинофенилацетамид), например α-[(2-нитрофенил)амино]-2,6-дихлорбензолацетамид и тому подобное; ингибиторы транс-активирующих белков, такие как ТАТ-ингибиторы, например, RO-5-3335, или REV-ингибиторы и тому подобное; ингибиторы протеазы, например, индинавир, ритонавир, саквинавир, лопинавир (АВТ-378), нелфинавир, ампренавир, ТМС-126, BMS-232632, VX-175, и тому подобное; ингибиторы слияния, например, Т-20, Т-1249 и тому подобное; антагонисты CXCR4-рецептора, например, AMD-3100 и тому подобное; ингибиторы вирусной интегразы; ингибиторы нуклеотидподобной обратной транскриптазы, например тенофовир и тому подобное; ингибиторы рибонуклеотидной редуктазы, например гидроксимочевина и тому подобное.
При введении соединений согласно настоящему изобретению с другими противовирусными агентами, которые нацелены на другие события в вирусном жизненном цикле, может быть усилен терапевтический эффект этих соединений. Комбинированные терапии, как описано выше, оказывают синергическое действие на ингибирование ВИЧ-репликации, так как каждый компонент комбинации действует на другой участок ВИЧ-репликации. Использование таких комбинаций может снижать дозировку данного стандартного антиретровирусного агента, которая требуется для желательного терапевтического или профилактического эффекта, по сравнению с той, когда агент вводят в качестве монотерапии. Эти комбинации могут снижать или исключать побочные эффекты стандартной антиретровирусной монотерапии, когда нет взаимного влияния противовирусной активности агентов. Эти комбинации снижают потенциал резистентности к терапиям с использованием одного агента, в то время как происходит минимизация любой связанной с этим токсичности. Эти комбинации также могут повышать эффективность стандартного агента без увеличения связанной с этим токсичности.
Соединения согласно настоящему изобретению также можно вводить в комбинации с иммуномодулирующими агентами, как, например, левамизол, бропиримин, антитело против человеческого альфа-интерферона, альфа-интерферон, интерлейкин-2, метионинэнкефалин, диэтилдитиокарбамат, фактор некроза опухоли, налтрексон и тому подобное; антибиотиками, как, например, пентамидинизетиорат и тому подобное; холинергическими агентами, как, например, такрин, ривастигмин, донепезил, галантамин и тому подобное; блокаторами NMDA-канала, как, например, мемантин; для предотвращения или борьбы с инфекцией и заболеваниями или симптомами заболеваний, связанными с ВИЧ-инфекциями, такими как СПИД и ARC, как, например деменция. Соединение формулы (I) также можно комбинировать с другим соединением формулы (I).
Несмотря на то, что настоящее изобретение направлено в основном на использование соединений согласно настоящему изобретению для предотвращения или лечения ВИЧ-инфекций, соединения согласно настоящему изобретению также можно использовать в качестве ингибирующих агентов для других вирусов, которые зависят от подобных обратных транскриптаз в обязательных событиях их жизненного цикла.
Следующие примеры предназначены для пояснения настоящего изобретения.
ПРИМЕРЫ
В дальнейшем, «ДМСО» означает диметилсульфоксид, «ТФУК» означает трифторуксусную кислоту, «ДМФА» означает N,N-диметилформамид и «ТГФ» означает тетрагидрофуран.
Пример 1
Получение соединения 1
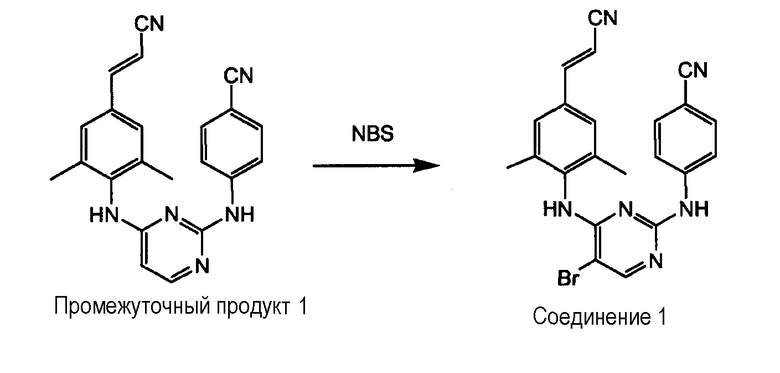
N-Бромсукцинимид (0,0393 моль) порциями добавляют, при комнатной температуре, к промежуточному продукту 1 (0,0327 моль), получение которого описано в WO-03/016306, в CH3CN (100 мл). Смесь перемешивают при комнатной температуре в течение 4 часов. Осадок отфильтровывают, промывают с помощью CH3CN и высушивают, получая 10,08 г желательного конечного продукта. Фильтрат выпаривают и очищают с помощью колоночной хроматографии (элюент: CH2Cl2 - 100; 35-70 мкм). Чистые фракции собирают, растворитель выпаривают и остаток кристаллизуют из CH3CN. Выход: 2,4 г соединения 1. Собирают вторые фракции. Выход: 12,48 г соединения 1 (86%, температура плавления: >250°С).
Пример 2
Получение соединения 2
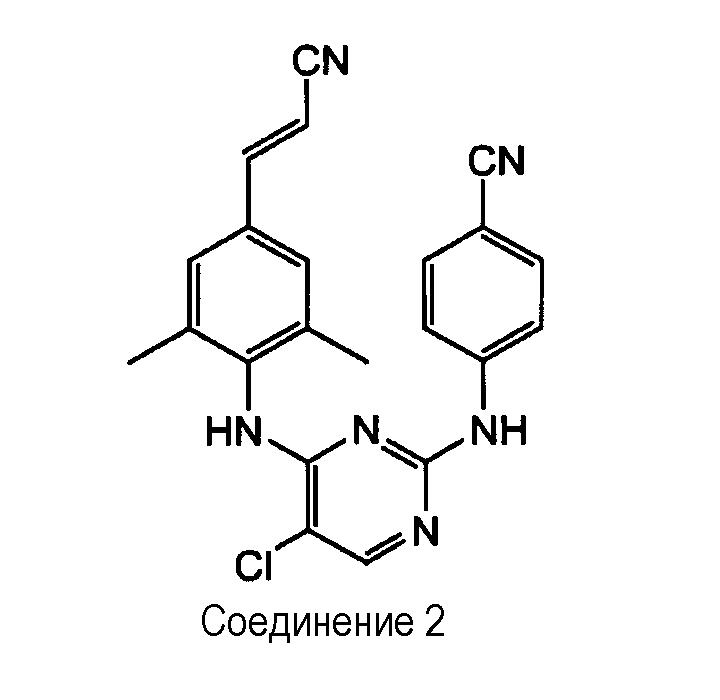
N-Хлорсукцинимид (0,000327 моль) порциями добавляют, при комнатной температуре, к соединению 1 (0,000273 моль) в CH3CN (5 мл). Смесь перемешивают при комнатной температуре в течение 4 часов. Осадок отфильтровывают, промывают с помощью CH3CN и высушивают. Выход: 0,065 г (59%, температура плавления: >250°С).
Пример 3
Получение соединения 3
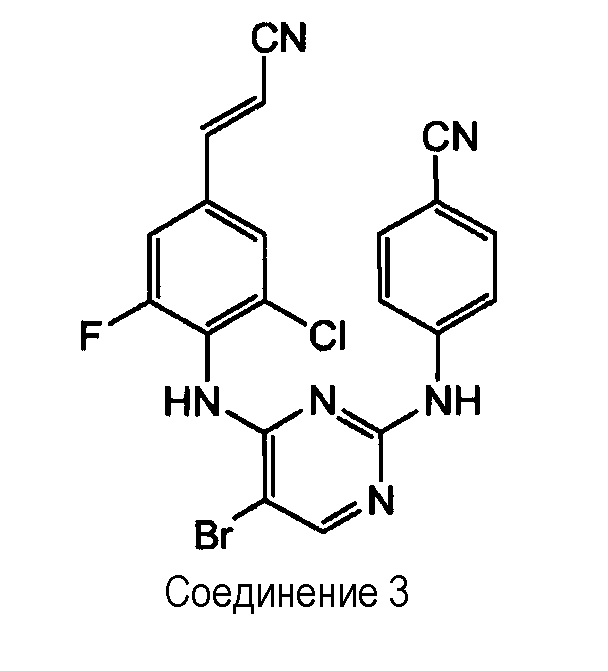
Используют такую же методику, как в примере 1, исходя из 2-фтор-6-хлор-аналога промежуточного продукта 1 (0,000128 моль) и N-бромсукцинимида (0,000154 моль) в CH3CN (5 мл), получая 0,037 г соединения 3 (62%, температура плавления: 236°С).
Пример 4
Получение соединения 4
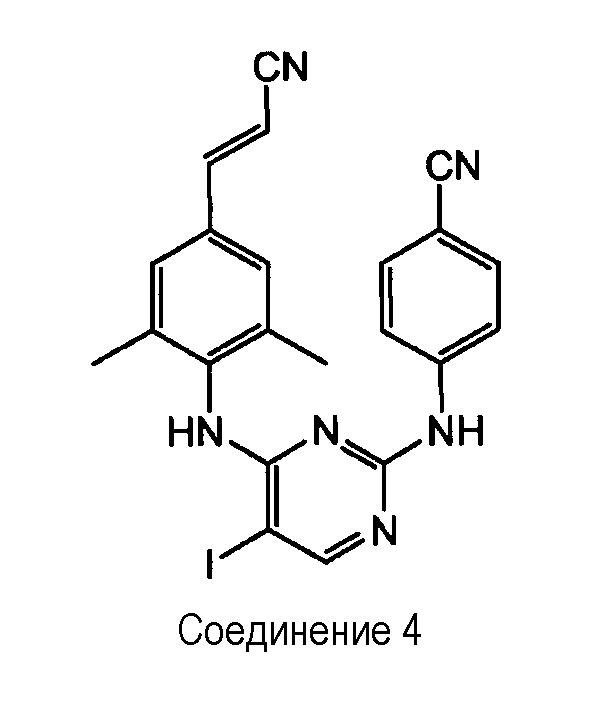
Суспензию СаСО3 (1,64 г) в воде (30 мл) добавляют к суспензии промежуточного продукта 1 (0,0273 моль) в EtOH (180 мл). Добавляют по каплям хлористый иод (ICl) в CH2Cl2 (1 н. раствор, 22,5 мл). Смесь перемешивают при комнатной температуре в течение 24 часов, затем охлаждают до температуры 0°С и отфильтровывают. Фильтрат высушивают в вакууме, затем обрабатывают EtOH (180 мл), отфильтровывают, промывают EtOH и CH3CN и высушивают. Выход: 8,5 г. Часть фильтрата выпаривают. Остаток кристаллизуют из горячего CH3CN. Осадок отфильтровывают и высушивают. Выход: 1,54 г (общий выход - 78%).
Пример 5
Получение соединений 5 и 6
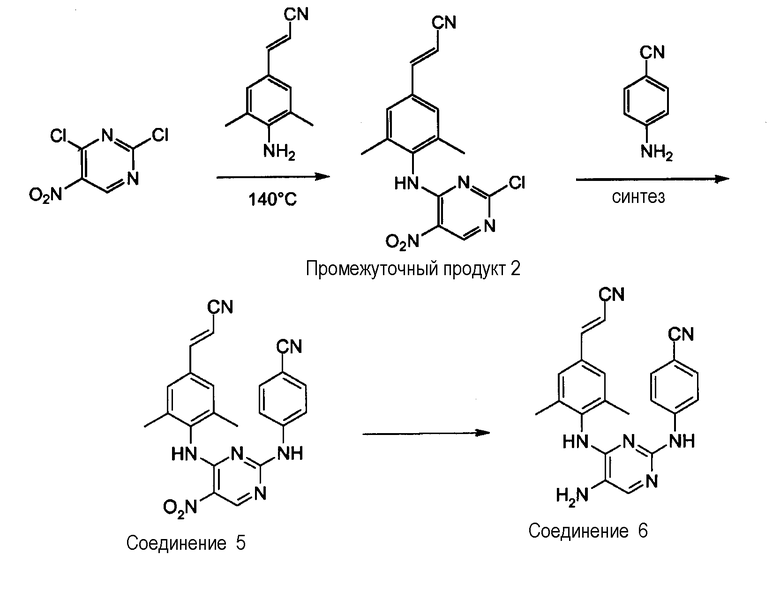
Смесь 2,4-дихлор-5-нитропиримидина (0,0516 моль) и 4-(2-цианоэтенил)-2,6-диметилфениламина (0,0516 моль) перемешивают при температуре 140°С на масляной бане в течение 45 минут, затем выливают в смесь воды и 10% К2СО3. Осадок отфильтровывают и фильтрат экстрагируют с помощью CH2Cl2. Органический слой сушат над сульфатом магния, отфильтровывают и растворитель выпаривают. Остаток очищают с помощью колоночной хроматографии на силикагеле (элюент: CH2Cl2 - 100; 35-70 мкм). Чистые фракции собирают и растворитель выпаривают, получая 6,0 г промежуточного продукта 2 (выход 35%, температура плавления: >250°С).
Получение соединения 5
Смесь промежуточного продукта 2 (0,0182 моль) и 4-цианоанилина (0,0182 моль) нагревают при плавлении в течение 5 минут, затем выливают в смесь воды и 10% К2СО3. Добавляют CH2Cl2 и небольшое количество МеОН и осадок отфильтровывают и высушивают. Выход: 7,4 г соединения 5 (95%, температура плавления: >250°С).
Получение соединения 6
Смесь соединения 5 (0,0180 моль) и дигидрата хлорида олова-(II) (0,125 моль) в этаноле (100 мл) перемешивают при температуре 70°С в течение ночи, затем выливают в смесь воды и 10% К2СО3. Осадок отфильтровывают через целит. Фильтрат удаляют и осадок промывают с помощью CH2Cl2 и ТГФ. Растворитель выпаривают. Выход: 6,0 г соединения 6 (87%, температура плавления: >250°С).
Пример 6
Получение 2-фтор-6-хлорфенил-аналогов соединений 5 и 6
Смесь 2,4-дихлор-5-нитропиримидина (0,0153 моль) и 4-(2-цианоэтенил)-2-фтор-6-хлорфениламина (0,0153 моль) нагревают при плавлении в течение 5 минут, затем выливают в смесь воды и 10% К2СО3 и экстрагируют с помощью CH2Cl2. Органический слой сушат над сульфатом магния, отфильтровывают и растворитель выпаривают. Остаток очищают с помощью колоночной хроматографии на силикагеле (элюент: CH2Cl2 - 100; 35-70 мкм). Чистые фракции собирают и растворитель выпаривают. Выход: 1,9 г 2-хлор-4-[4-(2-цианоэтенил)-2-фтор-6-хлорфениламино]-5-нитропиримидина, промежуточный продукт 3 (35%, температура плавления: 217°С).
Смесь промежуточного продукта 3 (0,000424 моль) и 4-цианоанилина (0,000424 моль) нагревают при плавлении в течение 5 минут, затем выливают в смесь воды и 10% К2СО3. Добавляют CH2Cl2 и небольшое количество МеОН и осадок отфильтровывают и высушивают. Выход: 1,34 г 4-[4-[4-(2-цианоэтенил)-2-фтор-6-хлорфениламино]-5-нитропиримидин]амино]бензонитрила, соединение 7 (73%, температура плавления: >250°С).
Смесь соединения 7 (0,00306 моль) и дигидрата хлорида олова-(II) (0,0214 моль) в этаноле (20 мл) перемешивают при температуре 70°С в течение ночи, затем выливают в смесь воды и 10% К2СО3. Осадок отфильтровывают через целит. Фильтрат удаляют и осадок промывают с помощью CH2Cl2 и ТГФ. Растворитель выпаривают. Выход: 1,1 г 4-[4-[4-(2-цианоэтенил)-2-фтор-6-хлорфениламино]-5-аминопиримидин]амино]бензонитрила, соединение 8 (89%, температура плавления: >250°С).
Пример 7
Получение соединения 9
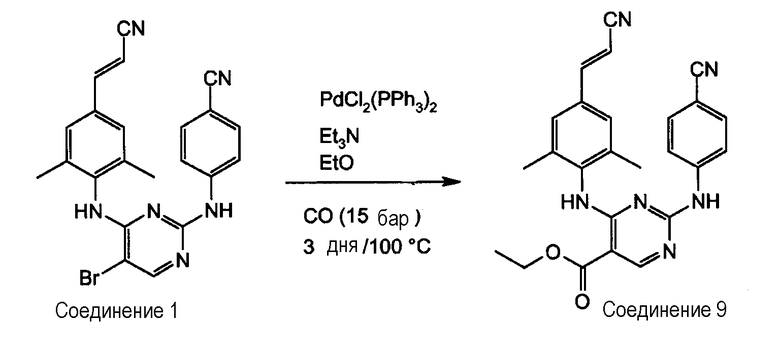
Смесь соединения 1 (0,0247 моль), дихлорбис(трифенилфосфин)палладия (II) (0,00494 моль) и триэтиламина (0,107 моль) в этаноле (100 мл) перемешивают при температуре 100°С в течение 72 часов, при давлении монооксида углерода в 15 бар. Смесь выливают в воду. Осадок отфильтровывают. Выход: 6 г. Фильтрат экстрагируют с помощью CH2Cl2. Органический слой сушат над сульфатом магния, отфильтровывают и растворитель выпаривают. Остаток очищают с помощью колоночной хроматографии на силикагеле (элюент: CH2Cl2/МеОН=99,5/0,5; 15-40 мкм). Чистые фракции собирают и растворитель выпаривают. Выход: 1,9 г. Собирают вторые фракции. Общий выход: 7,9 г соединения 9 (73%, температура плавления:>250°С).
Соединение 26 получают из соединения 3, используя ту же самую методику.
Пример 8
Получение соединения 10
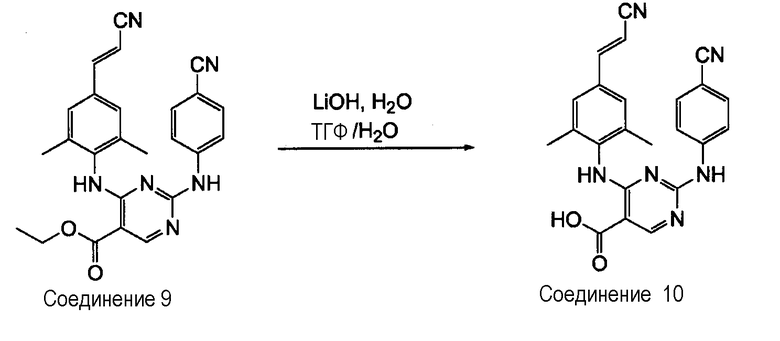
Смесь соединения 9 (0,00456 моль), моногидрата гидроксида лития (0,0137 моль) в ТГФ (20 мл) и воде (7 мл) перемешивают при температуре 50°С в течение ночи. ТГФ выпаривают. Остаток разбавляют водой и добавляют 3 н. раствор HCl до тех пор, пока значение рН не станет равным 2-3. Осадок отфильтровывают, промывают водой и высушивают. Выход: 1,78 г соединения 10 (95%, температура плавления: >250°С).
Пример 9
Получение соединения 11
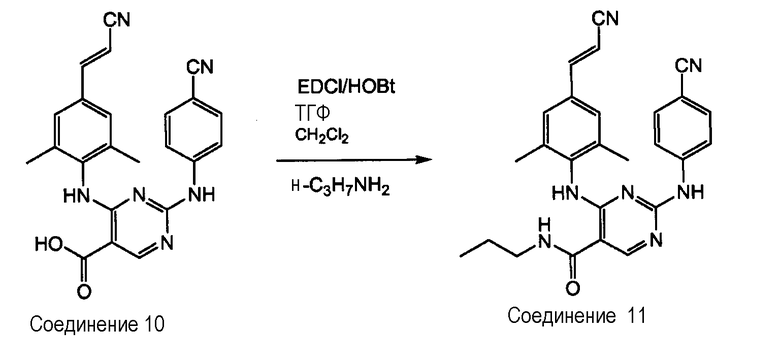
1-Гидроксибензотриазол (0,548 ммоль) добавляют к смеси соединения 10 (0,365 ммоль) в ТГФ (3 мл). К смеси последовательно добавляют дихлорметан (3 мл) и 1-(3-диметиламинопропил)-3-этилкарбодиимидгидрохлорид (0,548 ммоль). К этому раствору добавляют 1-пропиламин (0,548 ммоль). Смесь перемешивают при комнатной температуре в течение 24 часов, затем выливают в смесь воды и 10% К2СО3 и экстрагируют смесью CH2Cl2 и метанола (90/10). Органический слой промывают насыщенным солевым раствором, сушат над сульфатом магния, отфильтровывают и растворитель выпаривают. Остаток очищают с помощью колоночной хроматографии на силикагеле (элюент:от CH2Cl2=100 до CH2Cl2/МеОН = 95/5; Kromasil, 5 мкм). Выход: 0,116 г соединения 11 (70%, температура плавления: >250°С).
Соединение 30 получают, используя ту же самую методику, исходя из соединения 3.
Пример 10
Получение соединения 12
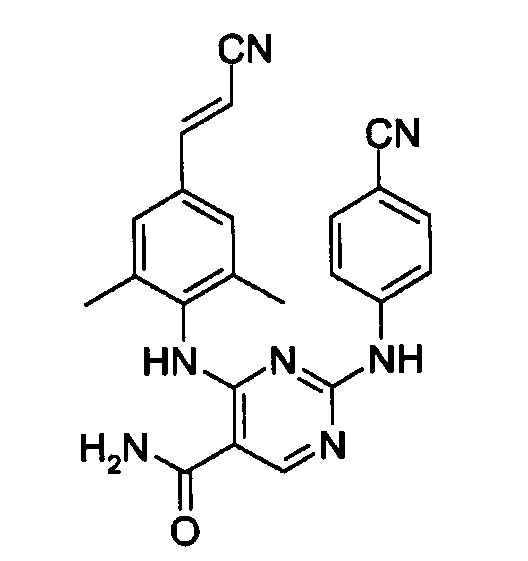
Тионилхлорид (5 мл) добавляют к соединению 10 (0,000365 моль) и смесь кипятят с обратным холодильником в течение 1 часа. Тионилхлорид удаляют в вакууме и остаток разбавляют с помощью CH2Cl2 (5 мл). Смесь охлаждают до температуры 0°С и по каплям добавляют 30%-ный раствор аммиака (2 мл). Смесь перемешивают при температуре 0°С, по меньшей мере, в течение 1 часа, и осадок отфильтровывают, промывают водой и диизопропилэтиловым эфиром и высушивают. Остаток очищают с помощью колоночной хроматографии на силикагеле (элюент: CH2Cl2/МеОН/NH4OH=95/5/0,1; 35-70 мкм). Чистые фракции собирают и растворитель выпаривают. Выход: 0,071 г соединения 12 (47%, температура плавления: >250°С).
Пример 11
Получение соединений 13, 14 и 15
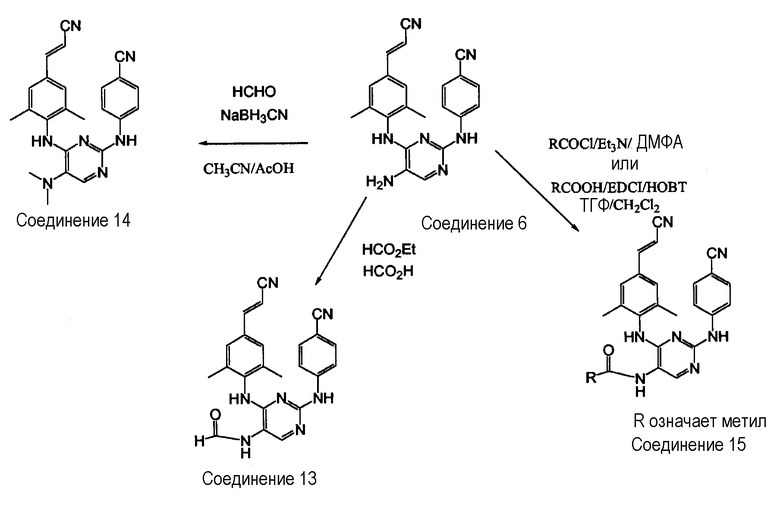
Муравьиную кислоту (10 мл) добавляют, при комнатной температуре, к соединению 6 (0,00215 моль) в этилформиате (30 мл). Смесь перемешивают при температуре кипения с обратным холодильником в течение 4 часов. Смесь выпаривают досуха, затем вносят в смесь воды и 10% К2СО3 и экстрагируют смесью CH2Cl2 и МеОН. Органический слой сушат над сульфатом магния, отфильтровывают и растворитель выпаривают. Остаток кристаллизуют из CH2Cl2 и МеОН. Выход: 0,48 г соединения 13 (55%, температура плавления: >250°С).
Получение соединения 14
Цианоборгидрид натрия (0,00262 моль) добавляют, при комнатной температуре, к смеси соединения 6 (0,000524 моль) и параформальдегида (0,00524 моль) в ацетонитриле (10 мл). Добавляют несколько капель уксусной кислоты и смесь перемешивают при комнатной температуре в течение 2 часов. Эту смесь выливают в смесь воды и 10% К2СО3 и экстрагируют с помощью CH2Cl2. Органический слой сушат над сульфатом магния, отфильтровывают и растворитель выпаривают. Остаток очищают с помощью колоночной хроматографии на силикагеле (элюент: от CH2Cl2=100 до CH2Cl2/МеОН=99/1; 10 мкм). Чистые фракции собирают и растворитель выпаривают. Выход: 0,070 г. Эту фракцию кристаллизуют из смеси диизопропилового эфира и диэтилового эфира. Осадок отфильтровывают и высушивают. Выход: 0,059 г соединения 14 (27%, температура плавления: >250°С).
Получение соединения 15
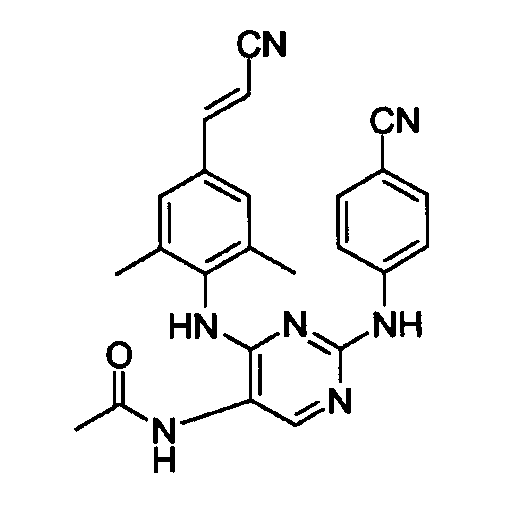
Ацетилхлорид (0,000315 моль) по каплям добавляют, при комнатной температуре, к смеси соединения 6 (0,000262 моль) и триэтиламина (0,000524 моль) в CH2Cl2 (2 мл) и ТГФ (2 мл). Смесь перемешивают при комнатной температуре в течение 4 часов, затем выливают в смесь воды и 10% К2СО3 и экстрагируют с помощью CH2Cl2. Органический слой сушат над сульфатом магния, отфильтровывают и растворитель выпаривают. Остаток очищают с помощью колоночной хроматографии на силикагеле (элюент: CH2Cl2/МеОН/NH4OH=95/5/0,1; 35-70 мкм). Чистые фракции собирают и растворитель выпаривают. Выход: 0,061 г соединения 15 (55%, температура плавления: >250оС).
Соединение 28 получают, используя ту же самую методику, исходя из соединения 8.
Пример 12
Получение 5-арилзамещенных соединений
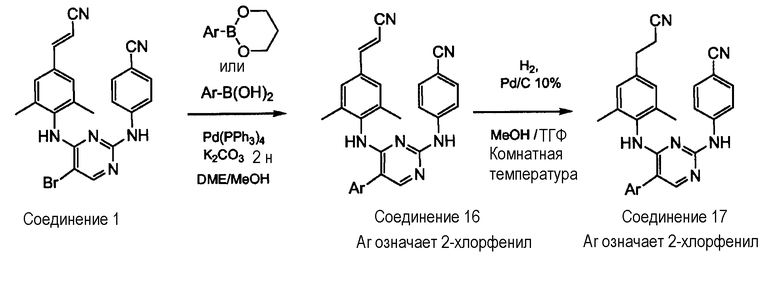
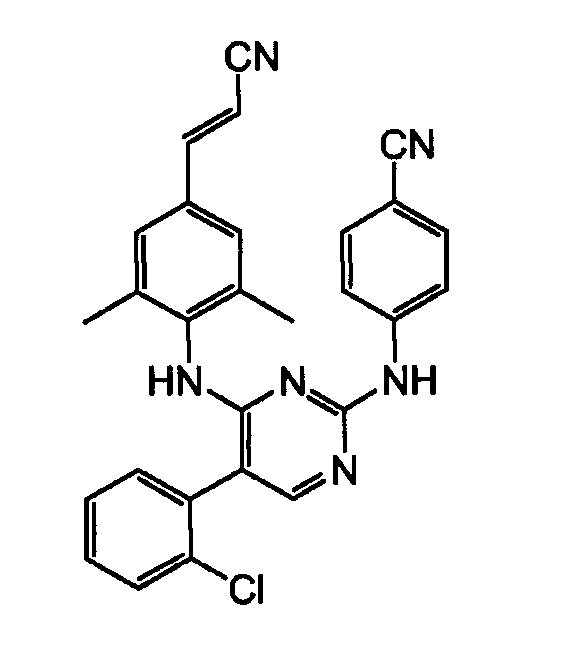
Соединение 1 (0,449 ммоль) добавляют к раствору тетракис(трифенилфосфин)палладия (0) (0,0449 ммоль) в 1,2-диметоксиэтане при комнатной температуре. Добавляют раствор 2-хлорфенилборной кислоты (0,135 ммоль) в метаноле (3 мл) при комнатной температуре. Смесь перемешивают при температуре 95°С в течение 24 часов и затем выливают в воду, экстрагируют этилацетатом. Органический слой промывают насыщенным солевым раствором и сушат над сульфатом магния, отфильтровывают и выпаривают. Остаток очищают с помощью колоночной хроматографии на силикагеле (элюент: CH2Cl2/МеОН=99/1; Kromasil Si, 10 мкм). Чистые фракции собирают и растворитель выпаривают. Выход: 0,130 г соединения 16 (60%, температура плавления:168-170°С).
Соединение 17 получают путем взаимодействия соединения 16 с водородом, в присутствии Pd/C, в смеси метанол/ТГФ.
Пример 13
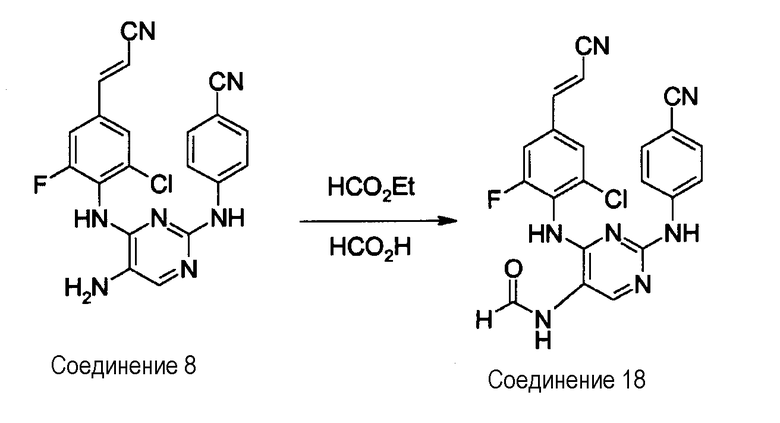
Получение соединения 18
Муравьиную кислоту (2 мл) добавляют, при комнатной температуре, к соединению 8 (0,000370 моль) в этилформиате (6 мл). Смесь перемешивают при температуре кипения с обратным холодильником в течение 3 часов. Смесь выливают в смесь воды и 10% К2СО3. Осадок отфильтровывают, промывают смесью диизопропилового эфира и диэтилового эфира и высушивают. Остаток кристаллизуют из CH2Cl2 и МеОН. Выход: 0,72 г соединения 18 (45%, температура плавления: 250°С).
Пример 14
Получение соединения 19
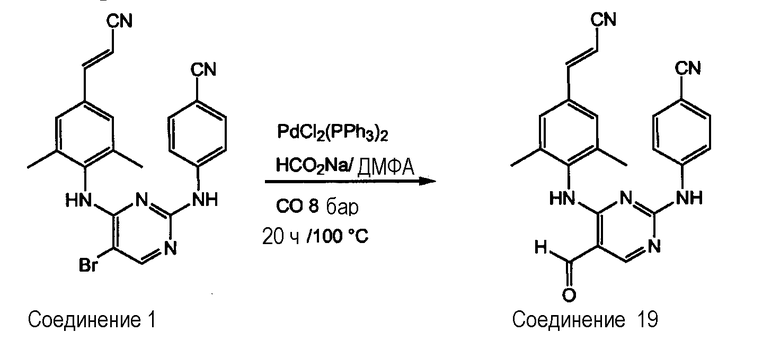
Смесь соединения 1 (0,0112 моль), дихлорбис(трифенилфосфин)палладия (II) (0,00228 моль), формиата натрия (0,0336 моль) и сульфата магния (1 г) в ДМФА (50 мл) перемешивают при температуре 100°С в течение 20 часов при давлении монооксида углерода 8 бар. Смесь отфильтровывают через целит и выливают в воду. Осадок отфильтровывают, промывают водой и Et2O, и сушат. Выход: 2,9 г соединения 19 (65%, температура плавления: >250°С).
Пример 15
Получение соединения 20
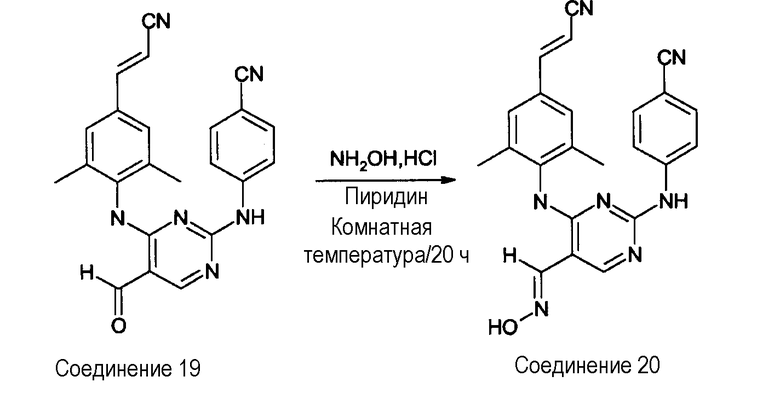
Смесь соединения 19 (0,000254 моль) и гидроксиламингидрохлорида (0,000380 моль) в пиридине (3 мл) перемешивают при комнатной температуре в течение 20 часов, затем выливают в воду. Осадок отфильтровывают, промывают водой и Et2O, и сушат. Выход: 0,048 г соединения 20 (39%, температура плавления: >250°С).
Пример 16
Получение соединения 31
Суспензию соединения 19 (0,0003 моль) и метоксиамингидрохлорида (0,0004 моль) в пиридине (4 мл) перемешивают при комнатной температуре в течение ночи, выливают в воду, отфильтровывают, промывают водой и высушивают при температуре 85єС в вакууме. Остаток (0,128 г) очищают с помощью колоночной хроматографии при использовании кромасила (элюент: CH2Cl2/СН3ОН=от 100/0 до 95/5; 5 мкм). Чистые фракции собирают и растворитель выпаривают, получая 0,065 г (46%) соединения 31 (температура плавления: >250°С).
Пример 17
Получение соединения 26
Смесь соединения 12 (0,0001 моль) и 10%-ного Pd/C (0,1 г) в ТГФ (5 мл) и МеОН (5 мл) гидрируют при комнатной температуре в течение ночи, при давлении 3 бар, затем отфильтровывают через целит. Фильтрат выпаривают. Остаток кристаллизуют из DIPE. Осадок отфильтровывают и высушивают, получая 0,065 г (81%) соединения 26 (температура плавления: 180°С).
Пример 18
Получение соединения 33
Смесь соединения 6 (0,0005 моль) и 10%-ного Pd/C (0,2 г) в ТГФ (8 мл) и МеОН (6 мл) гидрируют при комнатной температуре в течение ночи при давлении 3 бар, затем отфильтровывают через целит. Фильтрат выпаривают. Эту фракцию очищают с помощью колоночной хроматографии на силикагеле (элюент: CH2Cl2/СН3ОН= 95/5; 35-70 мкм). Чистые фракции собирают и растворитель выпаривают. Выход: 0,071 г (35%, температура плавления: 180°С).
В следующих таблицах перечислены соединения, которые уже получены или которые можно получать в соответствии с методиками, описанными в вышеприведенных примерах.
Таблица 1
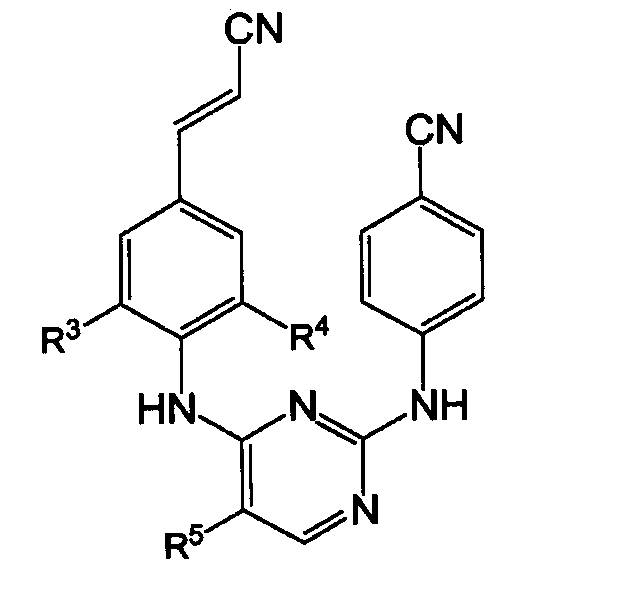
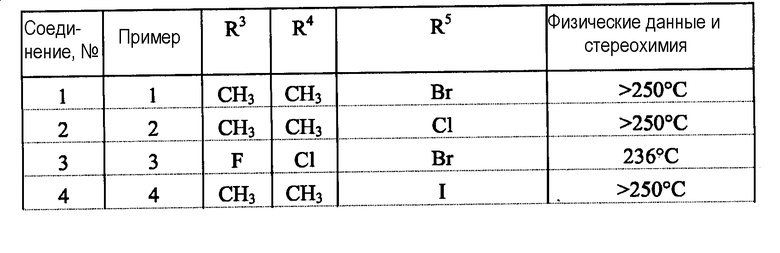
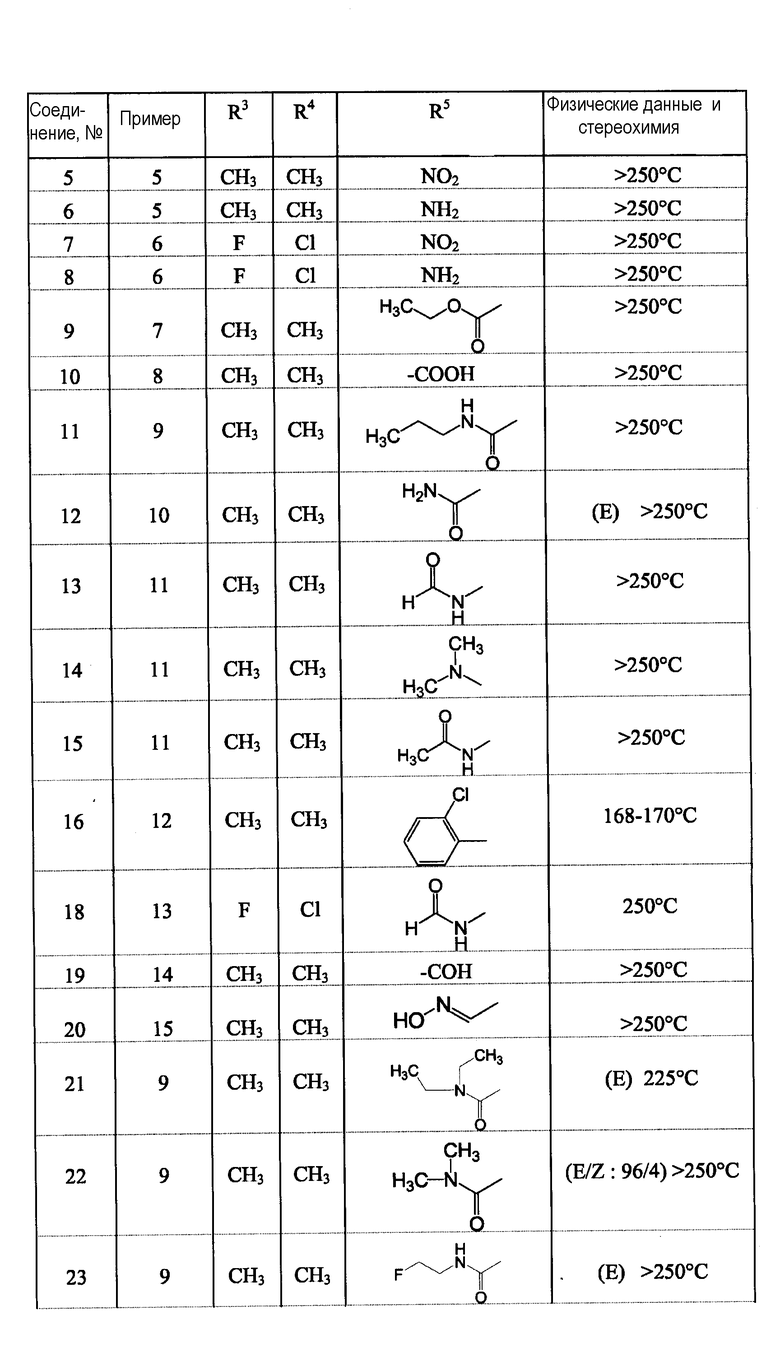
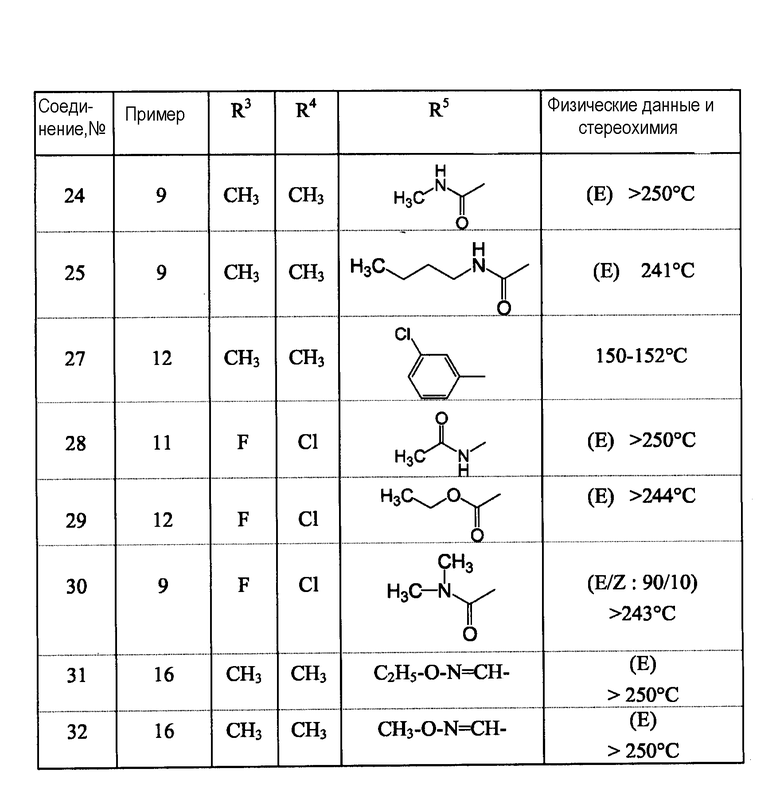
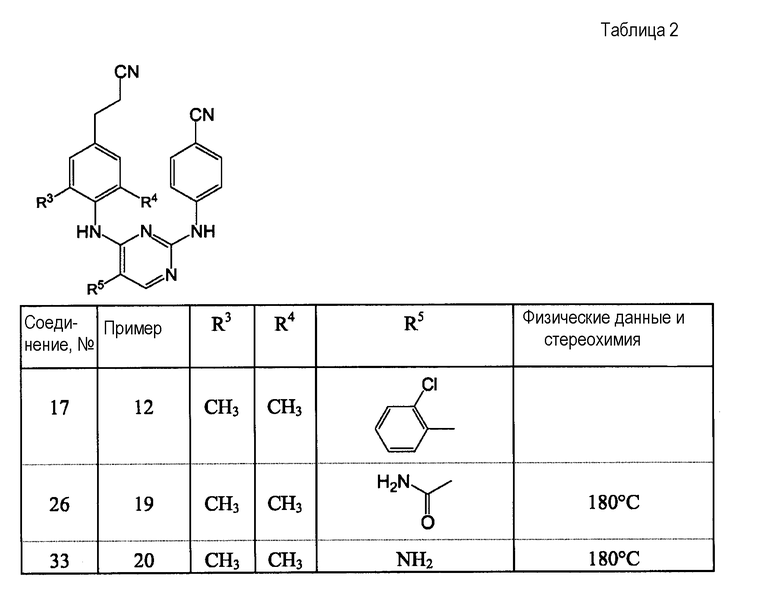
Примеры получения готовых лекарственных форм
Капсулы
Соединение формулы (I) растворяют в органическом растворителе, таком как этанол, метанол или метиленхлорид, предпочтительно, смесь этанола и метиленхлорида. Полимеры, такие как сополимер винилпирролидона и винилацетата (PVP-VA) или гидроксилпропилметилцеллюлоза (НРМС), обычно с вязкостью 5 мПа·с, растворяют в органических растворителях, таких как этанол, метанол и метиленхлорид. Пригодным образом, полимер растворяют в этаноле. Растворы полимера и соединения смешивают и затем подвергают сушке распылением. Соотношение соединение/полимер выбирают в диапазоне от 1/1 до 1/6. Промежуточные диапазоны могут составлять 1/1,5 и 1/3. Подходящим соотношением может быть 1/6. Порошком, полученным сушкой распылением, твердой дисперсией, затем заполняют капсулы для введения. Количество лекарственного средства, содержащееся в одной капсуле, составляет 50-100 мг, в зависимости от используемого размера капсулы.
Таблетки с пленочным покрытием
Получение ядра таблетки
Смесь 100 г соединения формулы (I), 570 г лактозы и 200 г крахмала тщательно перемешивают и затем увлажняют раствором из 5 г додецилсульфата натрия и 10 г поливинилпирролидона в примерно 200 мл воды. Влажную порошковую смесь просеивают, высушивают и снова просеивают. Затем добавляют 100 г микрокристаллической целлюлозы и 15 г гидрированного растительного масла. Все это тщательно перемешивают и прессуют в таблетки, получая 10000 таблеток, каждая из которых содержит 10 мг активного ингредиента.
Покрытие
К раствору 10 г метилцеллюлозы в 75 мл денатурированного этанола добавляют раствор из 5 г этилцеллюлозы в 150 мл дихлорметана. Затем добавляют 75 мл дихлорметана и 2,5 мл 1,2,3-пропантриола. 10 г полиэтиленгликоля расплавляют и растворяют в 75 мл дихлорметана. Последний раствор добавляют к предшествующему и затем добавляют 2,5 г октадеканоата магния, 5 г поливинилпирролидона и 30 мл концентрированной суспензии красящего вещества и все это вместе гомогенизируют. Ядра таблеток покрывают таким образом полученной смесью в глазировочном аппарате.
Антивирусный спектр
Вследствие увеличивающегося появления резистентных к лекарственным средствам штаммов ВИЧ, соединения согласно настоящему изобретению были тестированы в отношении их эффективности против клинически выделенных штаммов ВИЧ, обладающих некоторыми мутациями. Эти мутации связаны с резистентностью к ингибиторам обратной транскриптазы и приводят к вирусам, которые проявляют различные степени фенотипической перекрестной резистентности к коммерчески доступным в настоящее время лекарственным средствам, таким как, например, AZT и делавирдин.
Антивирусную активность соединения согласно настоящему изобретению оценивали в присутствии ВИЧ дикого типа и ВИЧ-мутантов, обладающих мутациями в гене обратной транскриптазы. Активность соединений оценивали, используя цитологический анализ, и остаточную активность выражали в значениях рЕС50. В таблице 3, в колонках IIIB и A-G, перечислены значения рЕС50 против различных штаммов IIIB, A-G.
Штамм IIIB представляет собой штамм ВИЧ-LAI дикого типа;
Штамм А содержит мутацию Y181C в обратной транскриптазе ВИЧ;
Штамм В содержит мутацию K103N в обратной транскриптазе ВИЧ;
Штамм С содержит мутацию L100I в обратной транскриптазе ВИЧ;
Штамм D содержит мутацию Y188L в обратной транскриптазе ВИЧ;
Штамм Е содержит мутации L100I и K103N в обратной транскриптазе ВИЧ;
Штамм F содержит мутации K103N и Y181C в обратной транскриптазе ВИЧ;
Штамм G содержит мутации L100I, K103N, Y181C, V179I, Y181C, E138G, V179I, L2214F, V278V/I и A327A/V в обратной транскриптазе ВИЧ.
| название | год | авторы | номер документа |
|---|---|---|---|
| 5-(ГИДРОКСИМЕТИЛЕН- И АМИНОМЕТИЛЕН)ЗАМЕЩЕННЫЕ ПИРИМИДИНЫ, ИНГИБИРУЮЩИЕ ВИЧ | 2007 |
|
RU2452737C2 |
| ВИЧ-ИНГИБИРУЮЩИЕ 5-КАРБО- ИЛИ ГЕТЕРОЦИКЛИЧЕСКИЕ ЗАМЕЩЕННЫЕ ПИРИМИДИНЫ | 2005 |
|
RU2403244C2 |
| ИНГИБИРУЮЩИЕ ВИЧ 2-(4-ЦИАНОФЕНИЛ)-6-ГИДРОКСИЛАМИНОПИРИМИДИНЫ | 2006 |
|
RU2401261C2 |
| БИЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ ПИРИМИДИНА, ИНГИБИРУЮЩИЕ ВИЧ | 2005 |
|
RU2403254C2 |
| 5-ГЕТЕРОЦИКЛИЛПИРИМИДИНЫ, ИНГИБИРУЮЩИЕ ВИЧ | 2005 |
|
RU2405778C2 |
| ИНГИБИРУЮЩИЕ ВИЧ ПРОИЗВОДНЫЕ 2-(4-ЦИАНОФЕНИЛАМИНО)ПИРИМИДИНА | 2006 |
|
RU2403245C2 |
| ИНГИБИРУЮЩИЕ ВИЧ ПРОИЗВОДНЫЕ 2-(4-ЦИАНОФЕНИЛАМИНО)-ПИРИМИДИН-ОКСИДА | 2006 |
|
RU2398768C2 |
| 5-АМИДО-ЗАМЕЩЕННЫЕ ПИРИМИДИНЫ, ИНГИБИРУЮЩИЕ ВИЧ | 2007 |
|
RU2480464C2 |
| ПРОИЗВОДНЫЕ 1, 2, 4-ТРИАЗИН-6-ОНА, ИНГИБИРУЮЩИЕ ВИЧ | 2005 |
|
RU2401833C2 |
| ПРОИЗВОДНЫЕ 1,10b-ДИГИДРО-2-(АМИНОКАРБОНИЛФЕНИЛ)-5Н-ПИРАЗОЛО[1,5-c][1,3]БЕНЗОКСАЗИН-5-ИЛ)ФЕНИЛМЕТАНОНА В КАЧЕСТВЕ ИНГИБИТОРОВ РЕПЛИКАЦИИ ВИЧ ВИРУСА | 2005 |
|
RU2382789C2 |
Изобретение относится к новым 5-замещенным пиримидинам общей формулы (I), их фармацевтически приемлемым аддитивным солям, возможно, в виде их стереохимически изомерной формы, обладающих антивирусной активностью в отношении ВИЧ инфекции. В общей формуле (I)
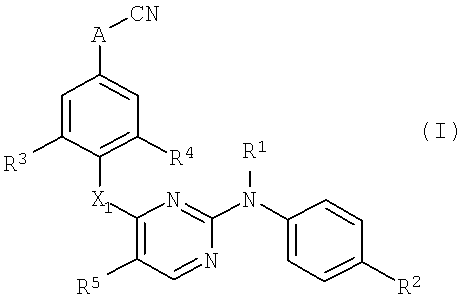
А означает -СН2-СН2-, -СН=СН-; каждый из R1 независимо означает водород; R2 означает циано; X1 означает -NR1-; R3 означает Н, С1-6-алкил, галоген; R4 означает Н, С1-6-алкил, галоген; R5 означает нитро, амино, моно- и ди(С1-4-алкил)амино, фенил, возможно замещенный галогеном, галоген, -СО-Н-, -COOR7, -NH-C(=O)H, -NH-C(=O)R6, -CH=N-O-R8; R6 означает С1-4-алкил, амино, моно- или ди(С1-4-алкил)амино или полигалоген-C1-4-алкил; R7 означает водород, С1-6-алкил; R8 означает водород, С1-6-алкил. Изобретение также относится к фармацевтической композиции на основе новых соединений. 2 н. и 5 з.п. ф-лы, 3 табл.
1. Соединение формулы

его фармацевтически приемлемая аддитивная соль или стереохимически изомерная форма, где:
А означает -СН2-СН2-, -СН=СН-;
каждый из R1 независимо означает водород;
R2 означает циано;
X1 означает -NR1-;
R3 означает Н, С1-6-алкил, галоген;
R4 означает Н, C1-6-алкил, галоген;
R5 означает нитро, амино, моно- и ди(С1-4-алкил)амино, фенил, возможно замещенный галогеном, галоген, -СО-Н-, -COOR7, -NH-C(=O)H, -NH-C(=O)R6, -CH=N-O-R8;
R6 означает С1-4-алкил, амино, моно- или ди(С1-4-алкил)амино или полигалоген-С1-4-алкил;
R7 означает водород, С1-6-алкил;
R8 означает водород, C1-6-алкил.
2. Соединение по п.1, где А означает -СН=СН-; X1 означает -NH-; R3 означает метил или галоген; R4 означает метил или галоген; R6 означает амино или диметиламино.
3. Соединение по п.1, где
R5 означает нитро или
R5 означает амино, моно- и ди(С1-4-алкил)амино, -NH-C(=O)H, -NH-C(=O)R6.
4. Соединение по п.1, где
R5 означает фенил, возможно замещенный галогеном; или
R5 означает галоген.
5. Соединение по п.1, где
R5 означает -СО-Н-, -COOR7.
6. Соединение по п.1, где
R5 означает -CH=N-O-R8.
7. Фармацевтическая композиция, обладающая антивирусной активностью в отношении ВИЧ-инфекции, содержащая фармацевтически приемлемый носитель и в качестве активного ингредиента терапевтически эффективное количество соединения по любому из пп.1-6.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Приспособление для спуска затвора Фотографической камеры | 1931 |
|
SU27825A1 |
| ПРОИЗВОДНЫЕ 2-АНИЛИНО-ПИРИМИДИНА ИЛИ ИХ СОЛИ, ПРОЯВЛЯЮЩИЕ ФУНГИЦИДНУЮ АКТИВНОСТЬ | 1992 |
|
RU2045520C1 |
Авторы
Даты
2011-01-27—Публикация
2005-09-29—Подача