Изобретение относится к области медицинской диагностики, может быть использовано для прогнозирования нарушения маточно-плацентарного и плодово-плацентарного кровотока как на этапе планирования, так и во время беременности.
В процессе эмбрио- и фетогенеза огромную роль играет новая функциональная система мать-плацента-плод, в которой одновременно формируется плодово-плацентарное и маточно-плацентарное кровообращение [1]. Выраженные гемодинамические сдвиги в этой системе являются ведущим патогенетическим механизмом нарушения состояния и развития плода [2, 3]. Оценку маточно-плацентарного и плодово-плацентарного кровообращения путем прямых и неинвазивных измерений проводят методом ультразвуковой доплерометрии. При динамическом наблюдении отмечено отсутствие нормализации или улучшения показателей гемодинамики при 1А, 2 и 3 степени нарушения маточно-плацентарно-плодового кровотока. Установлена нормализация плодово-плацентарного кровотока только при 1Б степени [4].
Беременность воздействует на все факторы организма, лежащие в основе регуляции сосудов, в результате чего происходит снижение вазореактивности, что имеет значение для поддержания низкого сосудистого сопротивления и, в свою очередь, состояний, способствующих высокому кровотоку к маточно-плацентарному сосудистому руслу [5]. Сосуды миометрия, хорионические сосуды плаценты и пуповины особенно чувствительны к ангиотензину II и реагируют на него сильнее, чем на другие вазоактивные вещества [6]. Действие ангиотензина II на клеточном уровне опосредуется четырьмя типами мембранных рецепторов - AT1-АТ4. Влияние ангиотензина II на рецепторы ангиотензина 1 типа (AT1) приводит к вазоконстрикции, стимуляции высвобождения вазопрессина, пролиферации гладкомышечных клеток сосудистой стенки, повышению чувствительности барорецепторов и др. [7, 8, 9]. При нормально протекающей беременности имеет место стимуляция работы ренин-ангиотензиновой системы [10], в то время как при преэклампсии, когда уровень ангиотензина II (AT II) относительно снижен, происходит гиперстимуляция AT1-рецепторов посредством агонистически действующих аутоантител к ним [11].
Известны способы прогнозирования и диагностики фетоплацентарной недостаточности, описанные в патентах РФ. Например, в патенте РФ №2130185 (опубл. 10.05.1999 г.) способ прогнозирования компенсированной и субкомпенсированной форм хронической фетоплацентарной недостаточности во второй половине беременности основан на исследовании цервикальной слизи в сроке беременности 28-30 недель. Недостатком этого способа является поздний срок прогнозирования.
Известен способ выявления доклинических лабораторных иммунологических признаков, характерных для развития фетоплацентарной недостаточности, путем вычисления диагностического индекса по данным о концентрации С-реактивного белка, β2-микроглобулина, гаптоглобитна и церулоплазмина, полученным по результатам анализа сыворотки крови беременной (патент РФ №2300770, опубл. 10.06.2007).
Известен также способ прогнозирования предрасположенности к плацентарной недостаточности, заключающийся в заборе крови в 1-й и 21-й дни цикла, анализе крови, определении противосвертывающих и антифибринолитических параметров крови, а решение о предрасположенности или отсутствии предрасположенности к плацентарной недостаточности принимают на основании рассчитанного по формуле индивидуального показателя динамики депрессии антиоксидантного показателя крови или индивидуального показателя динамики депрессии противосвертывающей системы крови. Данный способ позволяет осуществлять прогнозирование предрасположенности к плацентарной недостаточности уже на этапе планирования беременности. Недостатком является необходимость неоднократного забора крови и соблюдения установленных сроков этого забора, а также длительный срок и потребность в проведении большого количества анализов с использованием дорогостоящих реактивов (патент РФ №2180756, опубл. 20.03.2002).
Современный уровень техники позволяет установить связь различных нарушений деятельности человеческого организма с его генетическими особенностями.
К настоящему времени изучены ассоциации различных генетических полиморфизмов с состоянием маточно-плодово-плацентарного кровотока у беременных [12, 13, 14]. Среди этих генетических маркеров важное место отводится полиморфизмам генов ренин-ангиотензиновой системы (РАС) [15, 16, 17, 18, 19, 20]. При этом не известно влияние генотипов локуса -1166 А/С рецептора ангиотензина II 1-го типа на состояние маточно-плацентарного и плодово-плацентарного кровотока у беременных.
Задачей изобретения является расширение арсенала способов прогнозирования состояния маточно-плодово-плацентарного кровотока у беременных на основе данных о генотипах локуса -1166 А/С рецептора ангиотензина II 1-го типа.
Технический результат использования изобретения - сокращение сроков определения риска развития нарушения маточно-плодово-плацентарного кровотока как на стадии планирования, так и при наступлении беременности и возможность разработать на этой основе индивидуальные профилактические мероприятия (динамическое наблюдение, назначение лекарственных препаратов, улучшающих МППК).
В соответствии с поставленной задачей был разработан способ оценки состояния маточно-плодово-плацентарного кровотока на основе анализа полиморфизма гена рецептора ангиотензина II 1-го типа, включающий:
1) забор периферической венозной крови;
2) выделение ДНК из периферической венозной крови;
3) анализ генотипов локуса -1166 А/С рецептора ангиотензина II 1-го типа путем определения единичных нуклеотидных замен в гене, которые вызывают изменения уровня продукции рецептора ангиотензина II 1-го типа;
4) прогнозирование состояния маточно-плодово-плацентарного кровотока при разных генотипах локуса -1166 А/С рецептора ангиотензина II 1-го типа, а именно:
- прогнозирование высокого риска развития нарушения МППК при генотипе -1166 СС ATIIR1;
- прогнозирование низкого риска развития нарушения МППК при генотипе -1166 АА и -1166 AC ATIIR1.
Таким образом, осуществление предлагаемого изобретения позволяет разработать индивидуальные профилактические мероприятия на стадии планирования и при наступлении беременности, например, в случае выявления генотипа -1166 СС рецептора ангиотензина II 1-го типа, проведение терапии, направленной на улучшение маточно-плодово-плацентарного кровотока при наступлении беременности и осуществление регулярного наблюдения состояния маточно-плодово-плацентарного кровотока.
Новизна и изобретательский уровень заключаются в том, что в настоящее время не известна возможность прогнозирования состояния маточно-плацентарного и плодово-плацентарного кровотока на стадии планирования и при наступлении беременности на основе данных о генотипе СС локуса -1166 А/С рецептора ангиотензина II 1-го типа.
Способ характеризуется следующими графическими материалами.
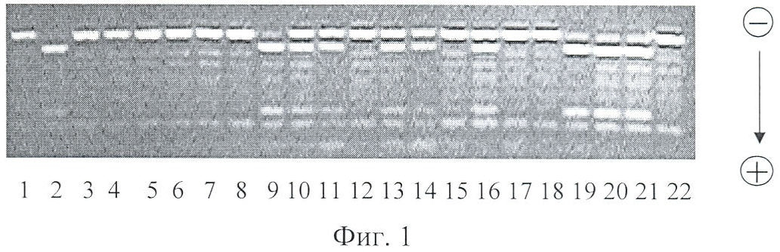
Фиг.1 - электрофоретическое разделение продуктов рестрикции гена рецептора ангиотензина II 1-го типа.
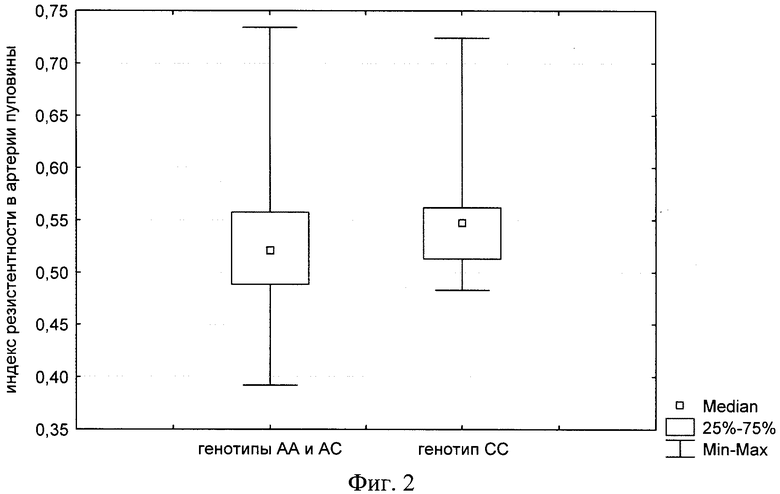
Фиг.2 - ассоциации -1166А/С полиморфизма ATIIR1 с показателем индекса резистентности в артерии пуповины у беременных.
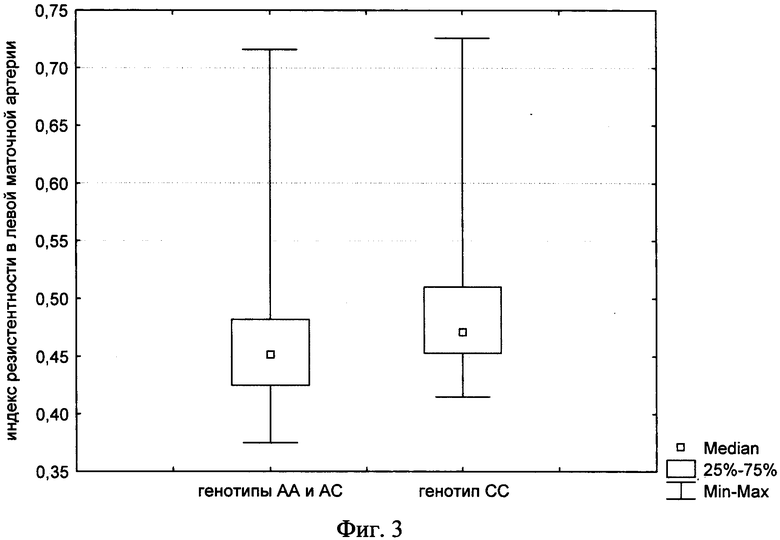
Фиг.3 - ассоциации -1166А/С полиморфизма рецептора ангиотензина II 1-го типа с показателем индекса резистентности в левой маточной артерии у беременных.
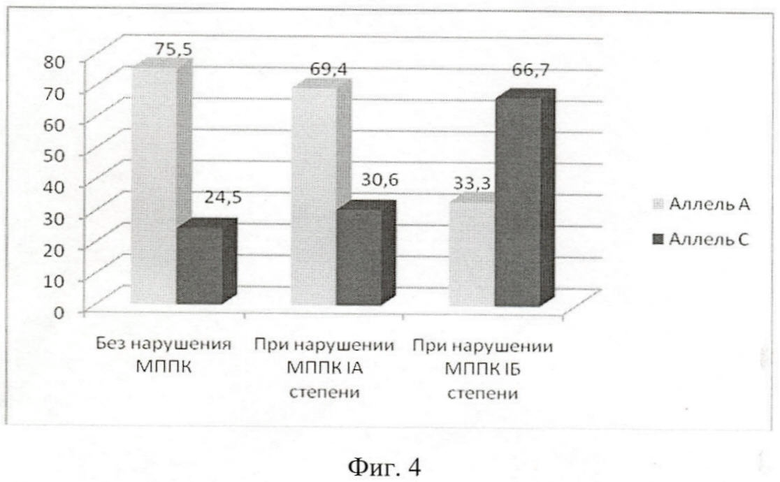
Фиг.4 - частота аллелей локуса -1166 А/С рецептора ангиотензина II 1-го типа у беременных с преэклампсией в зависимости от степени нарушения маточно-плодово-плацентарного кровотока.
Способ осуществляют следующим образом
Осуществляют забор периферической венозной крови, выделяют ДНК, проводят анализ генотипов локуса -1166 А/С рецептора ангиотензина II 1-го типа.
ДНК выделяют из образцов периферической венозной крови беременных в 2 этапа. На первом этапе к 4 мл крови добавляют 25 мл лизирующего буфера, содержащего 320 мМ сахарозы, 1% тритон Х-100, 5 мМ MgCl2, 10 мМ трис-HCl (рН 7,6). Полученную смесь перемешивают и центрифугируют при 4°С, 4000 об/мин в течение 20 минут. После центрифугирования надосадочную жидкость сливают, к осадку добавляют 4 мл раствора, содержащего 25 мМ ЭДТА (рН 8,0) и 75 мМ NaCl, ресуспензируют. Затем прибавляют 0,4 мл 10% SDS, 35 мкл протеиназы К (10 мг/мл) и инкубируют образец при 37°С в течение 16 часов.
На втором этапе из полученного лизата последовательно проводят экстракцию ДНК равными объемами фенола, фенол-хлороформа (1:1) и хлороформа с центрифугированием при 4000 об/мин в течение 10 минут. После каждого центрифугирования производят отбор водной фазы. ДНК осаждают из раствора двумя объемами охлажденного 96% этанола. Сформированную ДНК растворяют в бидистиллированной, деионизованной воде и хранят при -20°С.
Анализ локуса рецептора ангиотензина II 1-го типа проводят методом полимеразной цепной реакции синтеза ДНК с использованием стандартных олигонуклеотидных праймеров (см. таблицу).
Реакцию осуществляют в 12,5 мкл общего объема смеси, содержащей 33,5 мМ трис-HCl (рН 8,8), 1,25 мМ MgCl2, 0,5 мкг геномной ДНК, по 5 пМ каждого праймера, по 100 мкМ dATP, dGTP, dCTP, dTTP и 1 единицу активной Taq-полимеразы. После денатурации (5 мин при 95°С) выполняют 34 цикла амплификации по схеме: денатурация - 1 мин при 95°С; отжиг праймеров - 1 мин при 59°С; элонгация - 1 мин при 72°С. Затем пробы выдерживают 6 мин при 72°С и охлаждают. Продукты амплификации визуализируют в 2%-ном агарозном геле, приготовленном на основе ТВЕ-буфера, окрашенном раствором бромистого этидия (0,01%), в течение 20 минут при 200 V. В качестве электрофорезного буфера используют 1xTAE (трис-ацетатный буфер). Затем пробы идентифицируют в проходящем УФ-свете.
Амплификат, наработанный при ПЦР, подвергают рестрикции (ПДРФ-анализ) путем добавления к 12,5 мкл амплификата 5 ед. активности эндонуклеазы рестрикции DdeI (BstDE I) "СибЭнзим"и инкубируют в термостате при температуре 37°С в течение 16 часов.
Продукты ПДРФ-анализа оценивают путем разделения при помощи электрофореза в 3%-ном агарозном геле, в течение 30 мин при 150 V. Визуализацию фореграмм осуществляют в темном боксе с трансиллюминатором фирмы UVP (Швеция). Аллелю -1166А соответствуют фрагменты длиной 536 п.н. и 90 п.н. Фрагменты длиной 119 п.н., 417 п.н. и 90 п.н. соответствуют аллелю -1166С (фиг.1).
Формирование базы данных и статистические расчеты осуществляют с использованием программы «STATISTICA 6.0». Сравнивается степень нарушения состояния маточно-плацентарного и плодово-плацентарного кровотока у беременных с различными генотипами по локусу -1166 А/С ATIIR1.
В качестве конкретного примера представлен анализ результатов наблюдений 241 беременной: с неосложненной беременностью (109 индивидуумов) и с развившейся преэклампсией (132 женщины). Пациенты включались в группу обследования только после установления состояния маточно-плацентарного и плодово-плацентарного кровотока, подтвержденного с помощью клинико-инструментальных методов обследования. Исследование маточно-плодово-плацентарного кровотока проводили на аппарате Aloka α 10 с режимами двухмерного сканирования, цветового доплеровского сканирования и импульсной доплерографии. Использовали конвексный датчик с частотой 2-5 МГц. Кровоток в сосудах плода регистрировали в условиях двигательного покоя плода при ритмичной частоте его колебаний. Для оценки состояния кровообращения использовали уголнезависимый показатель индекса резистентности, характеризующий периферическое сосудистое сопротивление и зависящий от сократительной способности сердца, эластичности стенки исследуемого сосуда и объема периферического сосудистого русла, находящегося дистальнее исследуемого сосуда.
Проведено изучение индекса резистентности артерии пуповины (РА пуп), правой (РМА пр) и левой маточной артерии (РМА лев) в зависимости от генотипов локуса -1166 А/С рецептора ангиотензина II 1-го типа. Характер распределения данных количественных признаков не соответствует закону нормального распределения, о чем свидетельствуют значения критерия Шапиро-Уилка W=0,83-0,91 с уровнем их статистической значимости р<0,001. Поэтому для сравнительного анализа состояния маточно-плацентарного и плодово-плацентарного кровотока у пациенток с разными генотипами по изучаемому молекулярно-генетическому маркеру использовали непараметрические методы (критерий Манна-Уитни).
Установлено, что у гомозигот по аллелю С (генотип СС) индекс резистентности артерии пуповины (медиана 0,55, интерквартильный размах 0,51-0,56) (фиг.2) и левой маточной артерии (медиана 0,47, нижний квартиль - 0,45, верхний квартиль - 0,51) (фиг.3) был выше (р=0,04 и р=0,02, соответственно) в сравнении с таковым у женщин с генотипами АА и АС (медиана 0,52, интерквартильный размах 0,49-0,56 и медиана 0,45, нижний квартиль - 0,42, верхний квартиль - 0,48, соответственно).
Выявлена значительно более высокая частота аллеля -1166 С полиморфизма гена рецептора ангиотензина II 1-го типа у женщин с преэклампсией при нарушении МППК 1Б степени (66,7%) в сравнении с беременными без нарушения МППК (24,5%) (фиг.4) (OR=6,15, р=0,005).
Таким образом, полученные данные свидетельствуют о статистически значимых ассоциациях генетического полиморфизма -1166 А/С ATIIR1 с нарушением МППК: у беременных с генотипом -1166 СС ATIIR1 чаще наблюдаются нарушения маточно-плодово-плацентарного кровотока (повышение индекса резистентности артерий пуповины и левой маточной артерии, нарушения МППК 1Б степени).
Использование предложенного способа позволит прогнозировать развитие нарушения маточно-плодово-плацентарного кровотока на ранних стадиях беременности, что даст возможность на доклиническом этапе осуществить профилактику нарушения маточно-плодово-плацентарного кровотока (выбрать наиболее адекватную медикаментозную терапию для конкретной беременной с учетом ее генотипа) и поможет снизить перинатальную заболеваемость и смертность.
Литература
1. Функция эндотелия и маточно-плодово-плацентарный кровоток у беременных с артериальной гипертонией / Р.И.Стрюк [и др.] // Кардиология. - 2010. - №4. - С.18-22.
2. Сидорова И.С. Руководство по акушерству / И.С.Сидорова, В.И.Кулаков, И.О.Макаров. - М.: Медицина, 2006. - 848 с.
3. Агеева М.И. Диагностическое значение доплерографии в оценке функционального состояния плода // Автореферат дис. на соискание уч. ст. д.м.н. - Москва. - 2008. - 45 с.
4. Клиническое руководство по ультразвуковой диагностике [Электронный ресурс], Т.21. Под ред. Митькова В.В. - Электрон, дан. - М.: Издательский дом ВИДАР-М, 2001. - Эл. опт. диск (CD-ROM): цв. ил, рис., табл., фото. цв.: цв. + Прил.: Руководство пользователя (1 с.).
5. Савельева Г.М. Акушерство / Под ред. Г.М.Савельевой. - М.: Медицина, 2000. - 816 с.
6. Ордынский В.Ф. Особенности кровотока в артериальных сосудах системы мать-плацента-плод у беременных с сахарным диабетом при гестозе. К вопросу об этиопатогензе гестоза / В.Ф.Ордынский, Н.А.Постникова // Ультразвуковая и функциональная диагностика. - 2005. - №1. - С.23-37.
7. Мамедов М.Н. Почему ингибиторы ангиотензинпревращающего фермента считаются препаратом выбора у больных с артериальной гипертонией и метаболическим синдромом: метаанализ клинических исследований по эффективности хинаприла / М.Н.Мамедов // Consilium Medicum. - 2007. - Т.9, №5. - С.54-57.
8. Кобалава Ж.Д. Антагонисты рецепторов ангиотензина II в кардиологической практике: современный взгляд на проблему / Ж.Д.Кобалава, Е.К.Шаварова // Русский медицинский журнал. - 2008. - Т.16, №11. - С.1609-1616.
9. Осадчий К.К. Блокаторы AT1-ангиотензиновых рецепторов в лечении артериальной гипертензии: фокус на валсартан / К.К.Осадчий, В.И.Подзолков // Русский медицинский журнал. - 2009. - Т.17, №8. - С.582-589.
10. Блощинская И.А. Роль основных вазоактивных факторов сосудистого эндотелия в развитии гестоза / И.А.Блощинская // Рос. вест. акушера-гинеколога. - 2003. - №4. - С.7-10.
11. The detrimental role of angiotensin receptor agonistic autoantibodies in intrauterine growth restriction seen in preeclampsia / R.A.Irani [et al.] // J. Exp. Med. - 2009. - V.206, №12. - P.2809-2822.
12. Polymorphisms in the ACE and PAI-1 genes are associated with recurrent spontaneous miscarriages / T.Buchholz [et al.] // Human Reproduction. - 2003. - V.18, №11. - P.2473-2477.
13. An A>G polymorphism at position -670 in the Fas (TNFRSF6) gene in pregnant women with pre-eclampsia and intrauterine growth restriction / I.Sziller [et al.] // Molecular Human Reproduction. - 2005. - V.11, №3. - P.207-210.
14. Matrix Metalloproteinase 9 (MMP9) Expression in Preeclamptic Decidua and MMP9 Induction by Tumor Necrosis Factor Alpha and Interleukin 1 Beta in Human First Trimester Decidual Cells / С.J.Lockwood [et al.] // Biology of Reproduction. - 2008. - V.78, №6. - P.1064-1072.
15. Maternal-Fetal Flow, Negative Events, and Preeclampsia. Role of ACE I/D Polymorphism / G.Mello [et al.] // Hypertension. - 2003. - №41. - P.932-937.
16. Low-Molecular-Weight Heparin Lowers the Recurrence Rate of Preeclampsia and Restores the Physiological Vascular Changes in Angiotensin-Converting Enzyme DD Women / G.Mello [et al.] // Hypertension. - 2005. - №45. - P.86-91.
17. Differential Roles of Renin and Angiotensinogen in the Feto-Maternal Interface in the Development of Complications of Pregnancy / E.Takimoto-Ohnishi [et al.] // Molecular Endocrinology. - 2005. - №19. - P.1361-1372.
18. Кварацхелия E.E. Генетическая и приобретенная тромбофилии у пациенток с хронической гипертензией и метаболическим синдромом / Кварацхелия Е.Е // Журнал Российского общества акушеров-гинекологов. - 2006. - №4. - С.16-19.
19. Correlation of angiotensin converting enzyme activity and the genotypes of the I/D polymorphism in the ACE gene with preterm birth and birth weight / R.Uma [et al] // Eur J Obstet Gynecol Reprod Biol. - 2008. - V.141, №1. - P.27-30.
20. Association of angiotensin-converting enzyme intron 16 insertion/deletion polymorphism with history of foetal loss / L.Bukreeva [et al.] // Reproductive Sciences. - 2009. - V.16, №12. - P.1144-1152.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ прогнозирования риска развития преэклампсии у женщин с учетом генетических маркеров | 2022 |
|
RU2795660C1 |
| Способ прогнозирования риска развития задержки роста плода | 2021 |
|
RU2775435C1 |
| Способ прогнозирования риска развития задержки роста плода с учетом эпистатических взаимодействий полиморфных локусов менархе | 2021 |
|
RU2775432C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА НЕВЫНАШИВАНИЯ ПЕРВОЙ ПОЛОВИНЫ БЕРЕМЕННОСТИ | 2014 |
|
RU2566728C2 |
| Способ прогнозирования риска развития синдрома задержки роста плода у женщин с отягощенным семейным анамнезом | 2021 |
|
RU2770869C1 |
| Прогнозирование плацентарной преэклампсии по данным плацентометрии в сроки гестации 19-21 неделя у пациентов группы низкого риска | 2021 |
|
RU2771762C1 |
| Способ прогнозирования риска развития преэклампсии у женщин с хронической артериальной гипертензией | 2018 |
|
RU2699974C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ПЛОЩАДИ МИОМАТОЗНЫХ УЗЛОВ ПРИ МИОМЕ МАТКИ | 2010 |
|
RU2433402C1 |
| Способ прогнозирования развития коморбидной формы артериальной гипертензии и хронической обструктивной болезни легких | 2016 |
|
RU2620566C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ УРОВНЯ АРТЕРИАЛЬНОГО ДАВЛЕНИЯ У ЖЕНЩИН НА СРОКЕ РОДОРАЗРЕШЕНИЯ С ИСПОЛЬЗОВАНИЕМ ГЕНЕТИЧЕСКОГО ПОЛИМОРФИЗМА 4a/4b eNOS | 2014 |
|
RU2565405C1 |
Изобретение относится к области медицинской диагностики, может быть использовано для прогнозирования нарушения маточно-плодово-плацентарного кровотока. Способ включает выделение ДНК из периферической венозной крови и анализ генотипов локуса -1166 А/С рецептора ангиотензина II 1-го типа. Прогноз низкого риска развития нарушения маточно-плодово-плацентарного кровотока делают при выявлении генотипов -1166 АА и -1166 AC ATIIR1; высокий риск развития нарушения маточно-плодово-плацентарного кровотока - при выявлении генотипа -1166 СС ATIIR1. Использование способа позволяет прогнозировать нарушения маточно-плацентарного и плодово-плацентарного кровотока у беременных на ранних стадиях в короткие сроки, что дает возможность осуществить своевременную индивидуальную профилактику, а также снизить перинатальную заболеваемость и смертность. 1 табл., 4 ил.
Способ прогнозирования нарушения маточно-плодово-плацентарного кровотока, включающий забор и анализ периферической венозной крови, прогнозирование риска развития нарушения маточно-плодово-плацентарного кровотока, отличающийся тем, что из периферической венозной крови выделяют ДНК и проводят анализ генотипов локуса -1166 А/С рецептора ангиотензина II 1-го типа, прогнозируют повышенный риск развития нарушения маточно-плодово-плацентарного кровотока при выявлении генотипа -1166 СС ATIIR1, при выявлении генотипов -1166 АА и -1166 АС ATIIR1 - сниженный риск развития нарушения маточно-плодово-плацентарного кровотока.
| СПОСОБ ПРОГНОЗИРОВАНИЯ ПРЕДРАСПОЛОЖЕННОСТИ К ПЛАЦЕНТАРНОЙ НЕДОСТАТОЧНОСТИ (ВАРИАНТЫ) | 2000 |
|
RU2180756C1 |
| Способ изготовления шипов | 1929 |
|
SU23073A1 |
| АБАЕВА И.Ш | |||
| и др | |||
| Роль провоспалительных цитокинов в патогенезе синдрома потери плода // Материалы IV съезда акушеров-гинекологов России | |||
| Москва, 2008, 618 с | |||
| Найдено из БД Google, http://www.mediexpo.ru/fileadmin/user_upload/content/pdf/thesis/md08.pdf | |||
| BIANCHI D.W | |||
| Circulating fetal DNA: its | |||
Авторы
Даты
2012-07-20—Публикация
2011-04-04—Подача