Изобретение относится к области медицинской диагностики, может быть использовано для прогнозирования риска развития синдрома задержки роста плода у женщин с отягощенным семейным анамнезом.
В структуре осложнений беременности значимое место занимает задержка роста плода (далее ЗРП) [Devaskar S.U., Chu A. Intrauterine growth restriction: hungry for an answer. Physiology (Bethesda). 2016;31(2):131–46]. При недостаточном достижении плодом показателей массы и роста в соответствии с гестационным сроком с учетом пола и этнической принадлежности можно говорить о задержке роста плода [Intrauterine Growth Restriction: Antenatal and Postnatal Aspects [Text]. Sharma D, Shastri S, Sharma P. Clinical Medicine Insights: Pediatrics. 2016;10:67-83]. Среди всех беременностей встречаемость ЗРП может достигать 8-10%. ЗРП имеет неблагоприятные последствия как для перинатального периода (повышает риски асфиксии, аспирации меконием, респираторного дистресс-синдрома, и других заболеваний, а также смертности в этот период), так и для взрослого возраста (увеличивает риски возникновения сердечно-сосудистой патологии, метаболических расстройств и др. [Malhotra A., Allison B.J., Castillo-Melendez M. et al. Neonatal morbidities of fetal growth restriction: pathophysiology and impact. Front Endocrinol (Lausanne). 2019;10:55].
ЗРП имеет гетерогенную природу и может являться результатом воздействия целого ряда различных факторов плацентарного (морфофункциональные и эпигенетические нарушения в плаценте и др.), плодного (генетически детерминированные дефекты) и материнского (заболевания сердца и сосудов, дефицит и дисбаланс питания, гипоксические воздействия, влияние токсических веществ и др.) происхождения. В настоящее время не вызывает сомнений значимая роль наследственных факторов среди причин ЗРП и в том числе генетических факторов материнского организма [Ефремова О.А. Изучение ассоциации полиморфных локусов генов фолатного цикла с развитием синдрома задержки роста плода 2-3 степени. Научные результаты биомедицинских исследований. 2020;6(1):37-50]. По современным данным вес новорожденного на 40% связан с наследственными факторами [Golovchenko O, Abramova M, Ponomarenko I, et al. Functionally significant polymorphisms of ESR1and PGR and risk of intrauterine growth restriction in population of Central Russia. Eur J Obstet Gynecol Reprod Biol. 2020;253:52-57]. Однако следует отметить, что имеющиеся молекулярно-генетические исследования не дают однозначного ответа о роли конкретных полиморфных локусов различных групп генов в формировании ЗРП. Поэтому остается актуальным поиск генетических маркеров для ранней диагностики данного осложнения беременности.
Ген EGF (хромосомная локализация 4q25, HGNC ID: 3229) относится к суперсемейству генов эпидермальных факторов роста, а из кодируемого им препропротеина, вследствие протеолитической трансформации, образуется пептид - эпидермальный фактор роста (состоит из 53-аминокислот и имеет молекулярную массу 6,0 kD, OMIM 131530). Этот белок действует как мощный митогенный фактор, который играет важную роль в росте, пролиферации и дифференцировке многочисленных типов клеток (эктодермального и мезодермального происхождения). Биологические эффекты эпидермального фактора роста реализуются за счет его связывания со своим специфическим рецептором (рецептор эпидермального фактора роста, EGFR), расположенным на клеточной мембране [Zeng F, Harris RC. Epidermal growth factor, from gene organization to bedside. Semin Cell Dev Biol. 2014;28:2-11]. Как митогенный фактор роста, EGF играет важную роль в развитии эмбриона уже с момента предимплантации [Wei Z, Park KW, Day BN, Prather RS. Effect of epidermal growth factor on preimplantation development and its receptor expression in porcine embryos. Mol Reprod Dev. 2001]. Было показано, что EGF способствует предимплантационному росту эмбрионов, а также инвазии трофобластов и постимплантационному росту эмбрионов [Dadi TD, Li MW, Lloyd KC. EGF and TGF-alpha supplementation enhances development of cloned mouse embryos. Cloning Stem Cells. 2007;9:315–326]. Исследований, направленных на изучение вовлеченности локуса rs4444903 гена EGF в формирование осложнений беременности в доступной литературе обнаружено не было.
В Российской Федерации исследования вовлеченности гена эпидермального фактора роста (EGF) в формирование предрасположенности к развитию синдрома задержки роста плода немногочисленны, а данные о роли полиморфного локуса rs4444903 гена EGF в формировании синдрома задержки роста плода у беременных с отягощенным семейным анамнезом отсутствуют.
В изученной научно-медицинской и доступной патентной литературе авторами не было обнаружено способа прогнозирования риска развития синдрома задержки роста плода у беременных, имеющих отягощенный семейный анамнез задержке роста плода, на основе данных о полиморфизме rs4444903 гена EGF.
Из области техники известен патент № 2646505 «Способ выявления наследственной предрасположенности к развитию задержки роста плода у курящих женщин» по заявке № 2017115003 от 27.04.2017. Способ представляет собой исследование периферической венозной крови, включающий выделение ДНК, проведение полимеразной цепной реакции и анализ полиморфизма генов женщин, отличающийся тем, что проводят анализ полиморфизма гена IL-10 G-1082A и при выявлении генотипов IL-10-1082А/А или IL-70-1082G/A делают вывод о наличии наследственной предрасположенности к задержке роста плода у курящих женщин. Недостатком указанного способа является возможность прогнозирования риска развития задержки роста плода только в ограниченной группе беременных, а именно, только у курящих женщин.
За прототип взят патент № 2540928 по заявке № 2013148878/15 от 31.10.2013 г. «Способ прогнозирования риска развития плацентарной недостаточности с синдромом задержки роста плода 2-3-ей степени у беременных», включающий забор периферической венозной крови, и отличающийся тем, что после выделения ДНК проводят анализ полиморфизмов генов факторов коагуляции 20210G/A FII, 1691G/A FV, 10976G/A FVII и прогнозируют повышенный риск развития плацентарной недостаточности с синдромом задержки роста плода 2-3-ей степени у беременных в случае выявления аллеля 10976G FVII и генотипа 10976GG FVII, а низкий риск прогнозируют при наличии следующих комбинаций: генотипа 20210GG FII и аллеля 10976А FVII; аллелей 20210G FII, 10976А FVII с генотипом 1691GG FV; аллелей 20210G FII и 10976А FVII. Методическая сложность: выделение ДНК и анализ нескольких генов факторов коагуляции. Для их изучения необходима современная генетическая лаборатория. Недостатками данного способа являются методическая сложность и многокомпонентность исследования. Кроме того, не проведены аналогичные аналитические исследования у женщин с плацентарной недостаточностью, но без формирования синдрома ЗРП.
Задачей настоящего исследования является расширение арсенала способов диагностики, а именно создание способа прогнозирования риска развития синдрома задержки роста плода у беременных русской национальности, являющихся уроженками Центрального Черноземья, и имеющих отягощенный семейный анамнез по задержке роста плода, на основе данных о полиморфном локусе rs4444903 гена эпидермального фактора роста EGF.
Технический результат использования изобретения – получение критериев оценки риска развития синдрома задержки роста плода у беременных, русской национальности, являющихся уроженками Центрального Черноземья и имеющих отягощенный семейный анамнез по ЗРП, на основе данных о полиморфном локусе rs4444903 гена эпидермального фактора роста EGF, включающий:
- выделение ДНК из периферической венозной крови;
- анализ полиморфизма гена эпидермального фактора роста rs4444903 EGF;
- прогнозирование высокого риска развития синдрома задержки роста плода у беременных с отягощенным семейным анамнезом по ЗРП при выявлении в генотипе аллеля G полиморфного локуса роста rs4444903 гена EGF.
Новизна и изобретательский уровень заключаются в том, что из уровня техники не известна возможность прогноза развития синдрома задержки роста плода у беременных, русской национальности, являющихся уроженками Центрального Черноземья и имеющих отягощенный семейный анамнез по ЗРП на основе данных о полиморфном локусе rs4444903 гена эпидермального фактора роста (EGF);
Выделение геномной ДНК из периферической крови осуществляют методом фенольно-хлороформной экстракции (Mathew, 1984) в два этапа. На первом этапе к 4 мл крови с ЭДТА добавляют 25 мл лизирующего буфера, содержащего 320мМ сахарозы, 1% тритон Х-100, 5мМ MgCl2, 10 мМ трис-HCl (pH=7,6). Полученную смесь перемешивают и центрифугируют при 4°С, 4000 об/мин в течение 20 минут. После центрифугирования надосадочную жидкость сливают, к осадку добавляют 4 мл раствора, содержащего 25 мМ ЭДТА (рН=8,0) и 75 мМ NaCl, ресуспензируют. Затем прибавляют 0,4 мл 10% SDS, 35 мкл протеиназы К (10мг/мл) и инкубируют образец при 37ºС в течение 16 часов.
На втором этапе из полученного лизата последовательно проводят экстракцию ДНК равными объемами фенола, фенол-хлороформа (1:1) и хлороформа с центрифугированием при 4000 об/мин в течение 10 минут. После каждого центрифугирования производят отбор водной фазы. ДНК осаждают из раствора двумя объемами охлажденного 96% этанола. После лиофилизации полученную ДНК растворяют в бидистиллированной, деионизованной воде и хранят при -20°С. Выделенную ДНК используют для проведения полимеразной цепной реакции синтеза ДНК.
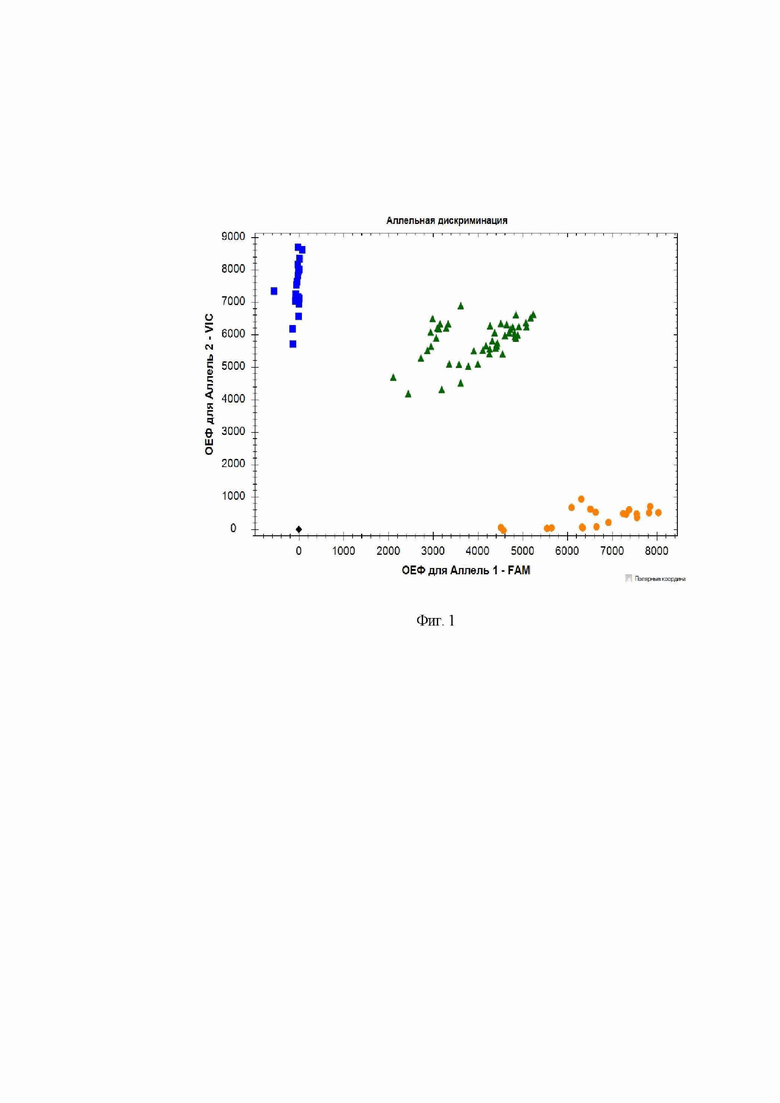
Анализ полиморфизма rs4444903 гена EGF проводят методом ПЦР-синтеза ДНК на амплификаторе СFX96 (Bio-Rad) с использованием стандартных олигонуклеотидных праймеров и зондов с последующим анализом полиморфизма методом дискриминации аллелей. Реакционная смесь объемом 10 мкл включает: 67 мМ трис-HCl (pH=8,8), 2,5мМ MgCl2, 0,1 мкг геномной ДНК, по 10 пМ каждого праймера, по 5 пкмоль каждого зонда, по 200 мкМ dATP, dGTP, dCTP, dTTP и 1 единицу активной Taq-полимеразы. После денатурации (2 мин при 95°С) выполняют 40 циклов амплификации по схеме: отжиг праймеров – 30 сек при t=60°С; денатурация – 10 сек при t=94°С. При проведении ПЦР в амплификаторе (CFX96) с флюоресцентной детекцией генотипирование осуществляют методом Tag Man зондов по данным величин ОЕФ (относительные единицы флуоресценции). Для rs4444903 EGF зонд с флуоресцентным красителем VIC соответствует аллелю A, зонд с красителем FAM – аллелю G (фиг.1).
Изобретение характеризуется фигурами.
Фиг. 1. Дискриминации аллелей методом детекции TaqMan зондов по данным величин ОЕФ (относительные единицы флуоресценции) каждого зонда на амплификаторе CFX96 c детектирующей системой в режиме реального времени полиморфизма ITGB3 (rs5918):  - AA,
- AA,  - GG,
- GG,  - AG, ♦ - отрицательный контроль.
- AG, ♦ - отрицательный контроль.
Для анализа ассоциации изучаемого полиморфного локуса с риском развития синдрома задержки роста плода у беременных с отягощенным семейным анамнезом по ЗРП проведен расчет показателей отношения шансов (ОШ) и их 95% доверительного интервала (95% ДИ). Вычисления выполнялись методом логистической регрессии в статистическом пакете программы PLINK (размещен на электронном ресурсе http://zzz.bwh.harvard.edu/plink/) согласно четырех генетических моделей (аллельная, аддитивная, рецессивная, доминантная) с введением поправок на ковариаты (возраст и индекс массы тела женщины до беременности) и множественные сравнения (применялся адаптивный пермутационный тест). В качестве статистически значимого уровня использовали значение pperm<0,05.
Возможность использования предложенного способа для оценки риска развития синдрома задержки роста плода у беременных с задержкой роста плода подтверждает анализ результатов наблюдений 196 беременных с ЗРП и 324 беременных контрольной группы. Показатели среднего возраста женщин с ЗРП (26,63±4,41 лет) и женщин контрольной группы с физиологическим течением гестации (26,17 ±4,98 лет) были сопоставимы (р > 0,05). Основанием для диагностики ЗРП являлось наличие несоответствия показателя расчетного веса плода (при отклонении более 10-го процентиля) в сравнении с нормативным для данного возраста гестации. Оценка антропометрических характеристик новорожденного использовалась для подтверждения наличия ЗРП. Выборки для исследования формировались в профильных отделениях перинатального центра Белгородской ОКБ Святителя Иоасафа в период 2008–2015 гг. Основанием для включения в основную группу было наличие у беременной изолированной ЗРП, контрольная группа была сформирована из беременных с физиологической гестацией. Критерии исключения: срок гестации <37 нед. и >40 нед., многоплодная беременность, наличие другой патологии беременности (преэклампсия, аномалии прикрепления и расположения плаценты, наличие резус-конфликта), ВПР у плода, доброкачественные пролиферативные заболевания матки (миома матки) и ее аномалии развития, тяжелая соматическая патология, отказ женщины от участия в настоящем исследовании.
Настоящее исследование выполнено по стандартам надлежащей клинической практики и в соответствии с принципами Хельсинской декларации. Данная работа была одобрена этическим комитетом медицинского института НИУ БелГУ (протокол №2 от 13.02.2008) и выполнялась при письменном добровольном информированном согласии всех обследованных женщин.
Обследование беременных выполнялись на сроке родоразрешения и включало: общеклинический анализ крови и мочи, биохимический анализ крови, коагулограмму, определение уровня белка в суточной моче. Выполнялись КТГ, УЗИ плода, доплерометрия с оценкой кровотока в сосудах пуповины и матки. Для исследования использовался биохимический анализатор Architect c4000 (Abbotte, США). Ультразвуковая фетометрия проводилась на ультразвуковом аппарате экспертного класса TOSHIBA XARIO SSA-660A (Toshiba, Япония). При диагностике ЗРП осуществлялась оценка различий между полученными фетометрическими показателями и номограммами F. Hadlock. Соматометрия новорожденного проводилась стандартным методом.
Выявлено, что аллель G полиморфного локуса rs4444903 гена EGF ассоциирован с высоким риском развития задержки роста плода в рамках следующих генетических моделей взаимодействия аллелей: аддитивной (ОШ=1,33, 95%ДИ 1,02-1,75, р=0,038, pperm=0,039, осуществлено 512 пермутационных процедур) и доминантной (ОШ=1,62, 95%ДИ 1,06-2,47, р=0,026, pperm=0,031, проведено 655 пермутационных процедур). Результаты приведены в таблице 1.
Таблица 1
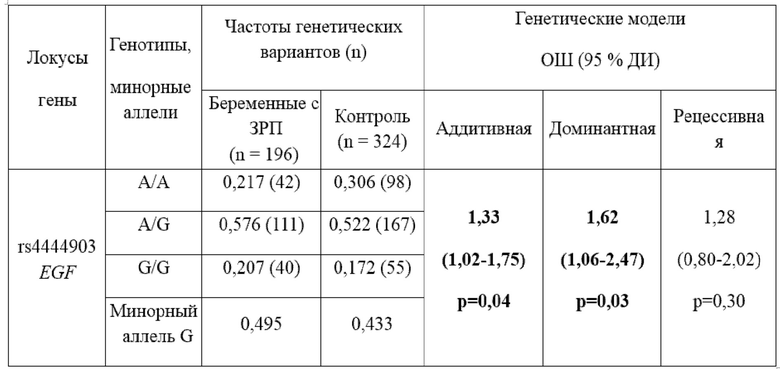
Таким образом, полученные данные свидетельствуют о том, что аллельный вариант G полиморфного локуса rs4444903 гена EGF является фактором риска развития синдрома задержки роста плода у беременных с отягощенным семейным анамнезом по ЗРП.
Примеры конкретного выполнения
У беременной женщины К., уроженки Центрального Черноземья русской национальности, имеющей отягощенный семейный анамнез, на ранних сроках беременности была взята венозная кровь, при генотипировании ДНК-маркеров был выявлен аллель G в генотипе AG полиморфного локуса rs4444903 гена EGF, что позволило отнести ее в группу беременных с высоким риском развития СЗРП. Это подтвердило дальнейшее наблюдение: на сроке 30 недель установлен диагноз задержка роста плода I степени.
У беременной женщины Ж., уроженки Центрального Черноземья русской национальности, имеющей отягощенный семейный анамнез, на ранних сроках беременности была взята венозная кровь, при генотипировании ДНК-маркеров был выявлено отсутствие аллеля G, генотип AА, полиморфного локуса rs4444903 гена EGF, что позволило отнести ее в группу беременных с низким риском развития СЗРП. Это подтвердило дальнейшее наблюдение: в течение беременности и после родов не было выявлено признаков СЗРП.
У беременной женщины М., уроженки Центрального Черноземья русской национальности, имеющей отягощенный семейный анамнез, на этапе прегравидарной подготовки была взята венозная кровь, при генотипировании ДНК-маркеров был выявлен аллель G в генотипе GG полиморфного локуса rs4444903 гена EGF, что позволило отнести ее в группу беременных с высоким риском развития СЗРП. Это подтвердило дальнейшее наблюдение: при наступлении беременности на сроке 30 недель установлен диагноз задержка роста плода II степени.
У беременной женщины Д., уроженки Центрального Черноземья русской национальности, имеющей отягощенный семейный анамнез, на этапе прегравидарной подготовки была взята венозная кровь, при генотипировании ДНК-маркеров был выявлено отсутствие аллеля G, генотип AА, полиморфного локуса rs4444903 гена EGF, что позволило отнести ее в группу беременных с низким риском развития СЗРП. Это подтвердило дальнейшее наблюдение после наступлении беременности: в течение беременности и после родов не было выявлено признаков СЗРП.
Таким образом, предложенный способ дает возможность прогнозирования риска развития синдрома задержки роста плода у беременных русской национальности, являющихся уроженками Центрального Черноземья России и имеющих отягощенный семейный анамнез по ЗРП, с учетом полиморфизма rs4444903 гена эпидермального фактора роста (EGF).
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ прогнозирования риска развития преэклампсии у беременных с синдромом задержки роста плода | 2021 |
|
RU2754956C1 |
| Способ прогнозирования веса новорожденного у беременных с преэклампсией в сочетании с синдромом задержки роста плода | 2020 |
|
RU2741861C1 |
| Способ прогнозирования риска развития синдрома задержки роста плода у женщин без отягощенного семейного анамнеза с использованием молекулярно-генетических данных | 2020 |
|
RU2738680C1 |
| Способ прогнозирования веса новорожденного у беременных с преэклампсией и отягощенным семейным анамнезом по преэклампсии | 2020 |
|
RU2738685C1 |
| Способ прогнозирования роста новорожденных с использованием данных о генетическом полиморфизме матерей | 2023 |
|
RU2820498C1 |
| Способ прогнозирования риска развития преэклампсии у женщин без отягощенного семейного анамнеза с учетом генетических факторов | 2020 |
|
RU2738675C1 |
| Способ прогнозирования риска развития задержки роста плода с учетом эпистатических взаимодействий полиморфных локусов менархе | 2021 |
|
RU2775432C1 |
| Способ прогнозирования риска развития задержки роста плода | 2021 |
|
RU2775435C1 |
| Способ прогнозирования веса новорожденного с учетом полиморфного локуса гексокиназы 2, дифференциально экспрессирующегося в плаценте | 2021 |
|
RU2786313C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ВЕСА НОВОРОЖДЕННОГО С УЧЕТОМ ПОЛИМОРФНЫХ ВАРИАНТОВ ЛОКУСА 10976 G/AFVII | 2014 |
|
RU2557952C1 |
Изобретение относится к области биотехнологии. Предложен способ прогнозирования риска развития синдрома задержки роста плода у беременных, являющихся уроженками Центрального Черноземья русской национальности, имеющих отягощенный семейный анамнез по задержке роста плода. Данный способ включает выделение ДНК из периферической венозной крови и анализ полиморфизма гена эпидермального фактора роста (EGF). 1 ил., 1 табл., 4 пр.
Способ прогнозирования риска развития синдрома задержки роста плода у беременных, являющихся уроженками Центрального Черноземья русской национальности и имеющих отягощенный семейный анамнез по задержке роста плода, включающий выделение ДНК из периферической венозной крови и анализ полиморфизма гена эпидермального фактора роста EGF, высокий риск развития синдрома задержки роста плода у беременных с отягощенным семейным анамнезом определяется при выявлении аллеля G полиморфного локуса rs4444903 гена EGF.
| Abd-Rabou A | |||
| A | |||
| R | |||
| S | |||
| Molecular genetic studies in pregnancies affected by preeclampsia and intrauterine growth restriction, University of Nottingham, 2011, докторская диссертация | |||
| А | |||
| Теремов, Р | |||
| Петросова, Биология | |||
| Биологические системы и процессы, стр | |||
| Машина для добывания торфа и т.п. | 1922 |
|
SU22A1 |
| Н.А | |||
| КУРНОСОВА, М.А | |||
| СЕМЕНОВА, Основы генетики, Ульяновский Государственный Университет, | |||
Авторы
Даты
2022-04-22—Публикация
2021-04-28—Подача