Изобретение относится к области устройств для биомиметической нейростимуляции.
Альтернативным лечением неврологических нарушений является нейростимулирующая терапия. Такая терапия применяет электрические или магнитные стимулы на нервную ткань посредством внешних или имплантированных устройств. Устройство биомиметической нейростимуляции описано Berger et аl., Proc. IEEE, Vol. 89, #7, июль 2001, с.993-1012. Этот документ описывает электронную модель трансформации ввода-вывода гиппокампом.
Задачей настоящего изобретения является обеспечение адаптивного и гибкого устройства для биомиметической нейростимуляции.
Задачи и преимущества будут очевидны по прочтении нижеследующих описания и формулы изобретения. Из следующего описания будет очевидно, что более адаптивное и гибкое устройство может быть использовано в качестве протеза для поврежденной ткани и включает в себя по меньшей мере один блок обработки сигналов, который включает в себя канал прямой связи и канал модуляции. Канал прямой связи симулирует обработку неврологических сигналов между областями, афферентной и эфферентной к подозрительной области. Канал модуляции информирует канал прямой связи в ответ на сигналы, принятые из другого места. Канал модуляции может подавать обратно сигналы даже более эфферентные, чем выходной сигнал канала прямой связи.
Нарушения, потенциально излечимые этой терапией, включают двигательные нарушения, когнитивные нарушения или повреждение. Особенно есть надежда, что такое более адаптивное и гибкое устройство было бы полезно при неврологических нарушениях, таких как болезнь Паркинсона. Другие примеры неврологических нарушений, потенциально излечимых таким устройством, включают в себя рассеянный склероз, эпилепсию, боль и другие когнитивные нарушения, такие как болезнь Альцгеймера, депрессия, биполярное расстройство, синдром навязчивых состояний, зависимость и даже, возможно, ожирение. Более того, лечение может быть использовано в реабилитационной терапии, следующей после инсульта или травматического повреждения головного мозга.
Аспекты изобретения теперь будут описаны посредством неограничивающего примера со ссылкой на следующие фигуры:
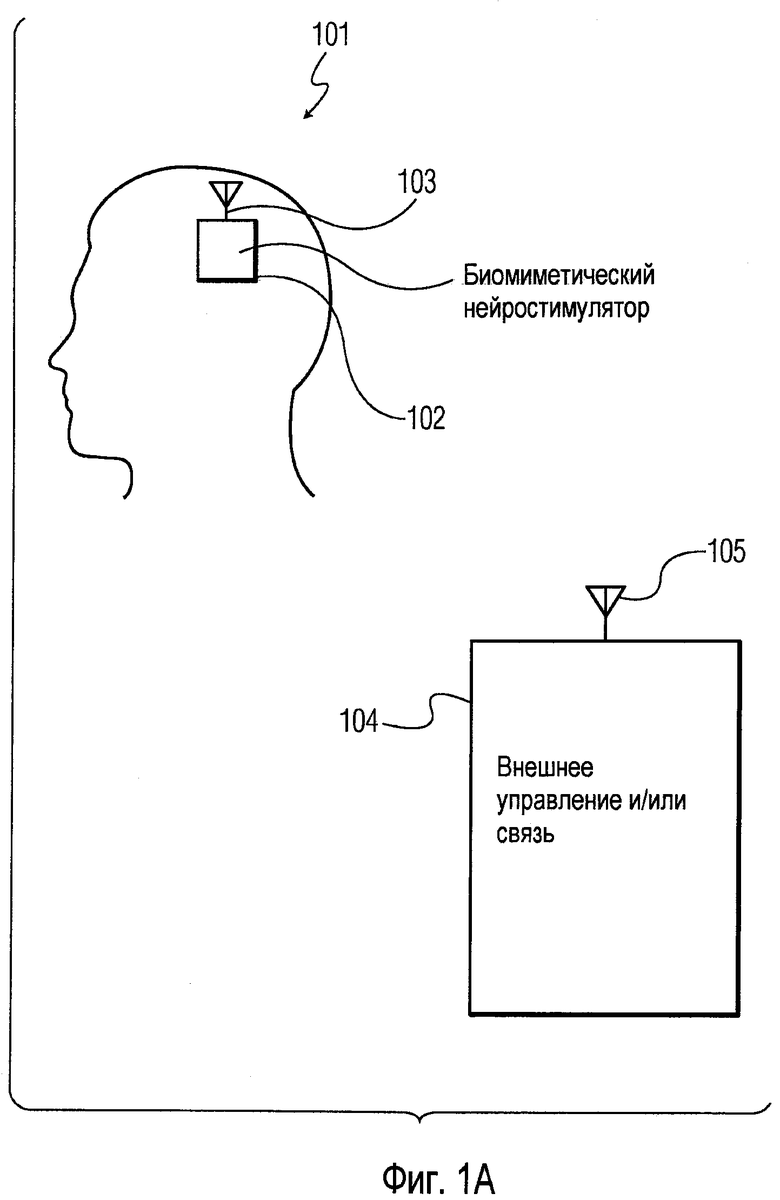
Фиг.1А - схема устройства для биомиметической стимуляции в голове пациента и внешняя система управления.
Фиг.1В - схематизированный вид подобного цепи функционирования участка головного мозга.
Фиг.2 - более детальная схема части Фиг.1В.
Фиг.3 показывает схему биомиметического нейростимулятора, имплантированного в головной мозг или нервный путь.
Фиг.4 - блок-схема последовательности операций работы устройства Фиг.3.
Фиг.5 иллюстрирует функцию передачи.
Фиг.6 иллюстрирует функцию преобразования частоты.
Фиг.7 иллюстрирует последовательность импульсов.
Фиг.8 показывает альтернативный вариант осуществления Фиг.3.
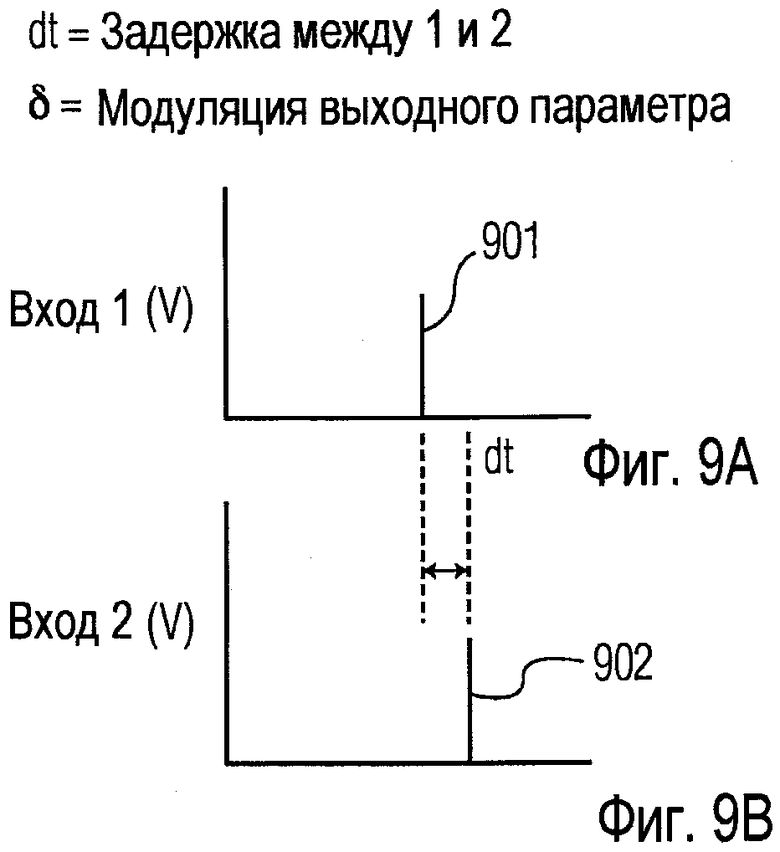
Фиг.9А показывает входной сигнал.
Фиг.9В показывает другой входной сигнал, отсроченный относительно первого входного сигнала.
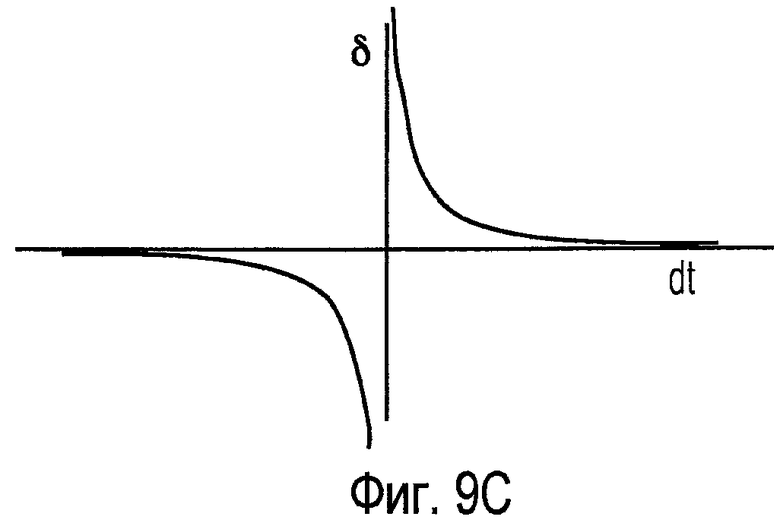
Фиг.9С показывает выход нейростимулятора.
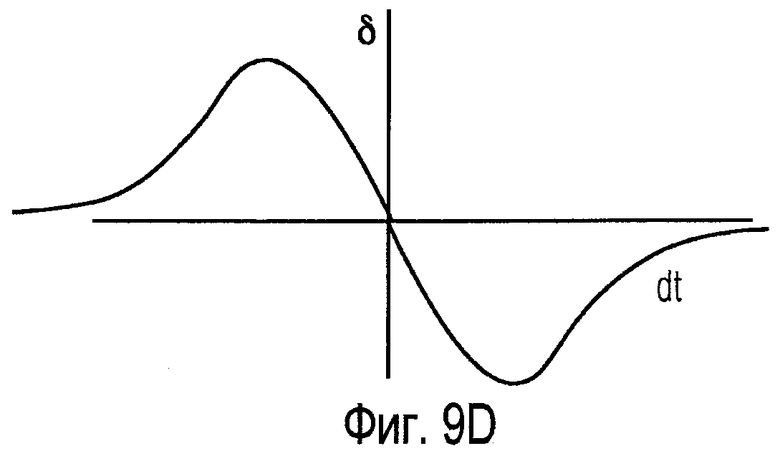
Фиг.9D показывает альтернативный выход нейростимулятора.
Следующие дополнительные документы патента включены здесь ссылкой: US 5,913,882; WO 2005053787A1 и US 20050113744A1.
Фиг.1А - схема головы пациента 101, включающая в себя устройство 102 для биомиметической стимуляции, снабженное необязательной антенной 103 (показанной схематически) для внешней связи. Могли быть возможны другие типы внешней связи, такие как отведение, соединенное с внешней поверхностью черепа пациента. Устройство 102 показано внутри головного мозга, но оно могло бы быть помещено в другие нервные проводящие пути, такие как позвоночник.
Необязательная внешняя система 104 сообщается с устройством 102 посредством антенны 105. Внешняя система 104 обеспечивает данные устройству 102, например, когда медицинский работник определяет прогрессирование нарушения или от какого-либо сенсора. Внешняя система 104 может дополнительно или альтернативно обеспечивать вспомогательную обработку или управление для 102.
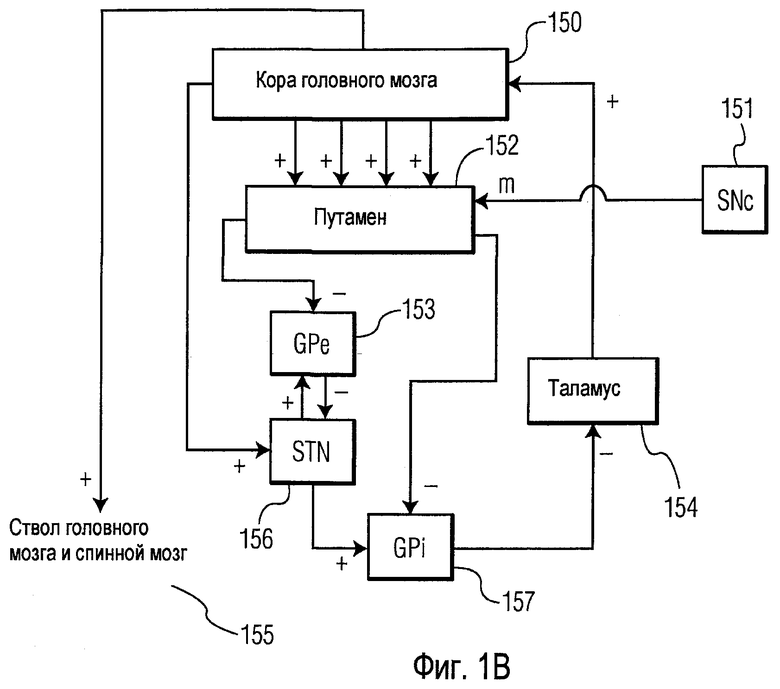
Как пример типичных цепей головного мозга, Фиг.1В показывает схематическое изображение цепей ганглии-таламокортикальных двигательных нервов (Y. Temel et al., Progress in Neurobiology volume 76, с. 393-413 (2005)). Эта фигура показывает кору 150 головного мозга, компактную часть 151 черного вещества (SNc), путамен 152, внешний сегмент 153 «бледного шара» (GPe), таламус 154, ствол головного мозга и спинной мозг 155, гипоталамическое ядро (STN) 156 и внутренний сегмент 157 «бледного шара» (GPi). Возбуждающие связи обозначены «+», ингибирующие связи обозначены «-» и модулирующие связи обозначены «m». Физиологические функции, схематизированные в этой цепи, поражены при заболеваниях двигательных нервов типа болезни Паркинсона, эссенциального тремора и дистонии, например. Предложенное устройство для биомиметической нейростимуляции хорошо адаптировано для коррекции патологических сигналов в таких цепях головного мозга.
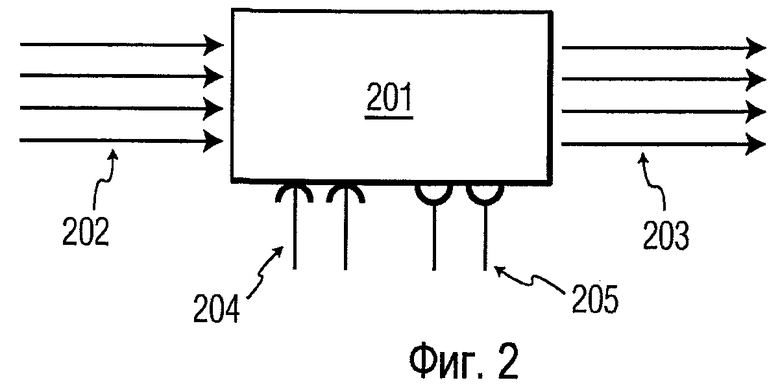
Фиг.2 - более подробная схема подраздела цепи головного мозга, как показано на Фиг.1В. Изображенная область неврологической системы показывает поток сигналов преимущественно в одном направлении. Некоторые области регуляции моторики особенно способны иметь поток такого сорта. В общем поток будет переходить из афферентной (вверх по потоку) области к эфферентной (вниз по потоку) области. Подраздел цепи принимает афферентные сигналы 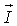 на его (синаптических) входах 202 и вырабатывает неврологические сигналы
на его (синаптических) входах 202 и вырабатывает неврологические сигналы 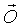 на его выходах 203. Четыре линии показаны в качестве входов 202 и в качестве выходов 203. Четыре - это произвольное число. Фактически сигналы из других областей головного мозга или других нервных проводящих путей типично модулируют афферентные сигналы в соответствии с очень высокоразмерной функцией ввода-вывода
на его выходах 203. Четыре линии показаны в качестве входов 202 и в качестве выходов 203. Четыре - это произвольное число. Фактически сигналы из других областей головного мозга или других нервных проводящих путей типично модулируют афферентные сигналы в соответствии с очень высокоразмерной функцией ввода-вывода 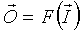 . В дополнение размер O и размер I в основном будут различны. Модулирующие сигналы могут быть ингибирующими 204 и/или возбуждающими 205 и в основном включают в себя сигналы как прямой связи, так и обратной связи. Как афферентные входные сигналы, так и модуляторные сигналы по сущности нестационарные, таким образом, выходной сигнал будет высоко динамичным. Обратите внимание, что как показано на Фиг.1В, двусторонний поток сигналов между областями (либо прямой, или через большие цепи) представляет собой другую общую тему в неврологических системах. Функционирование таких цепей может быть описано подобным образом.
. В дополнение размер O и размер I в основном будут различны. Модулирующие сигналы могут быть ингибирующими 204 и/или возбуждающими 205 и в основном включают в себя сигналы как прямой связи, так и обратной связи. Как афферентные входные сигналы, так и модуляторные сигналы по сущности нестационарные, таким образом, выходной сигнал будет высоко динамичным. Обратите внимание, что как показано на Фиг.1В, двусторонний поток сигналов между областями (либо прямой, или через большие цепи) представляет собой другую общую тему в неврологических системах. Функционирование таких цепей может быть описано подобным образом.
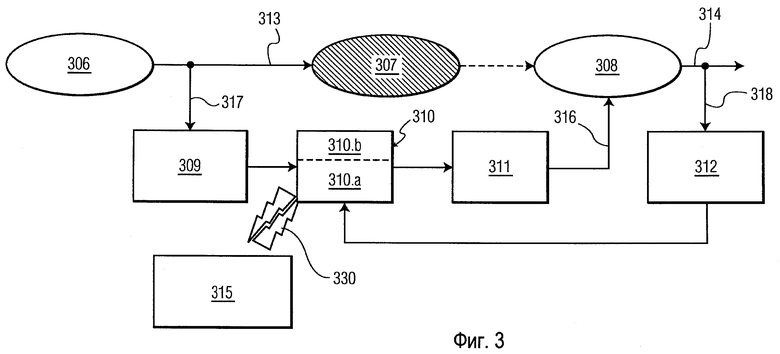
Фиг.3 показывает схему биомиметического нейростимулятора, имплантированного в головной мозг или нервный проводящий путь. Проводящий путь включает в себя три области 306, 307 и 308. Предполагается, что области 306 и 308 остаются здоровыми, в то время как область 307 либо повреждена или может стать поврежденной. Предполагается, что согласно Фиг.2, первичный поток нервных сигналов идет в одном направлении, например от 306 к 307, к 308. Предполагаемая дисфункция 307 иллюстрирована иллюстрацией сигналов 325, вытекающих из нее, в виде пунктирной линии.
Имплантированный нейростимулятор включает в себя первый сенсор 309; процессор 310, включающий в себя процесс 310а обучения/записи и установившийся процесс 310b; генератор 311 стимулов, и второй сенсор 312. Первый сенсор 309 получает афферентный сигнал 313 от поврежденной области.
Генератор стимулов 311 является, например, генератором электрических импульсов. Генератор стимулов 311 обеспечивает имитированный ответ для области 308. Второй сенсор 312 получает эфферентный сигнал 314 от области 308.
Необязательный внешний узел или узлы 315 сообщаются (по беспроводной связи или иначе) с процессором. Внешний узел или узлы 315 могут иметь множество необязательных свойств, таких как дополнительный сенсор, который считывает некоторый входной сигнал, отличный от нервной активности (например, мышечную активность, движение, пищеварение, или некоторые другие физиологические или нефизиологические параметры), или дополнительный процессор, в случае некоторой функции, особенно обучения, требует еще процессор.
Элемент 316 является выходом нейромиметического протезного устройства, в то время как элементы 317 и 318 являются входами.
Сенсоры 309 и 312 могут быть многих типов, включая: электрические, оптические, химические, биохимические, электрохимические, магнитные или их комбинацию. Генератор 311 стимулов может излучать стимулы многих типов, включая электрические, магнитные, оптические, химические, биохимические или их комбинацию. Несмотря на то, что нарисован только один сенсор на позициях 309 и на 312, может быть использован более чем один сенсор. Несмотря на то, что нарисован только один генератор 311 стимулов, может быть использован более чем один генератор. Более того, мог бы также использоваться более чем один процессор 310 с более чем двумя подпроцессами.
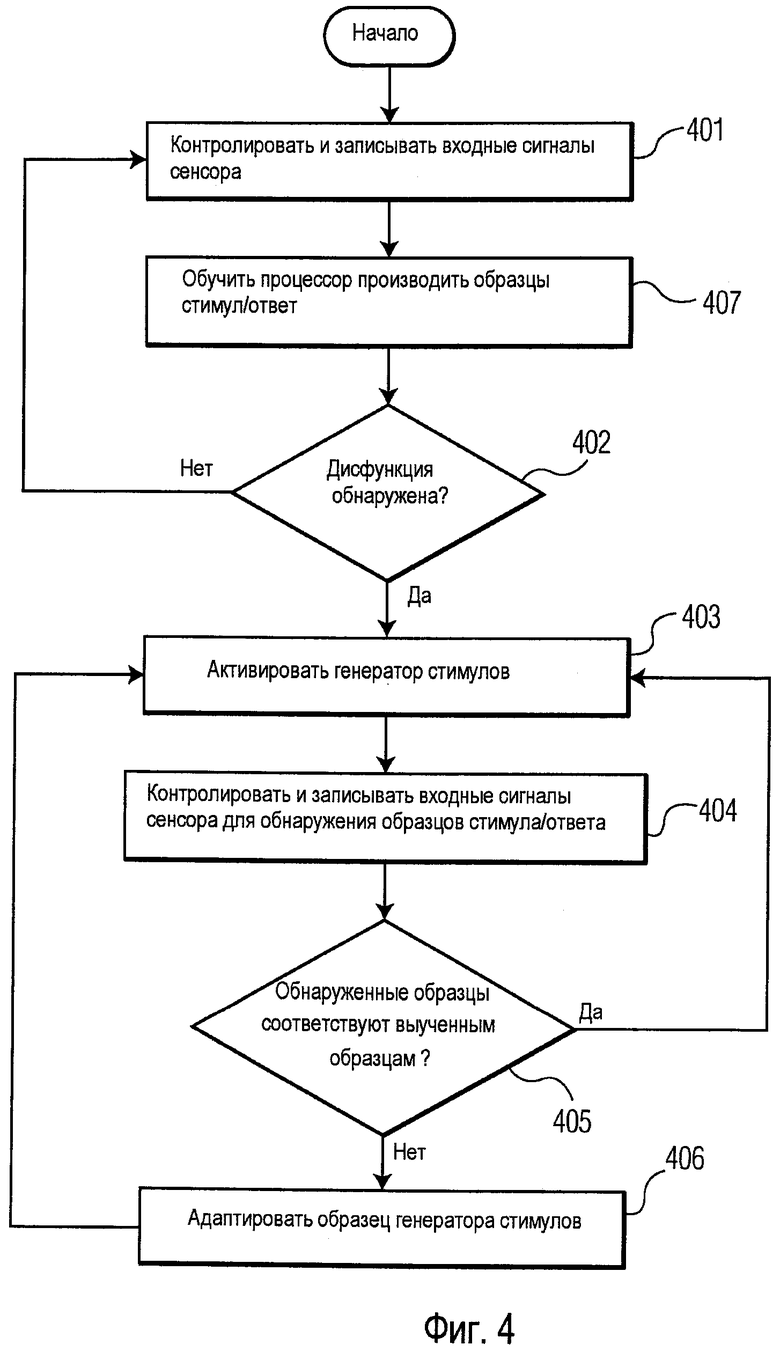
В другом примерном варианте осуществления процессор 310 сконструирован таким образом, что он проходит через две стадии обучения, как показано на блок-схеме Фиг.4.
На первой стадии предполагается, что область 307 функционирует по меньшей мере до некоторой степени. В течение первой стадии процесс 310а просто контролирует сигналы 313 и 314 на этапе 401 и обучает себя на этапе 407 по образцу стимул/ответ реагирования областей 307 и 308 на сигналы на 313. Затем процессор 310 обнаруживает на этапе 402, что область 307 стала так повреждена, что ее функционирование должно быть заменено. Такое обнаружение может осуществляться в ответ на наблюдения изменений в эфферентном сигнале 314. Альтернативно такое обнаружение может осуществляться в ответ на сигнал 330 от внешнего узла 315, например, если доктор диагностирует достаточное ухудшение, требующее активацию протезного устройства.
На второй стадии обучения процесс 310b продолжает контролировать сигналы 313 и 314; однако, на этапе 403, он теперь активирует блок 311 генератора стимулов, предписывая ему обеспечить некоторую стимуляцию 316 области 308. Затем, на этапе 405, процессор сравнивает сигналы 313 и 314, следуют ли они образцам стимул/ответ, записанным в течение первой стадии обучения. Если наблюдаемые образцы отличаются от заученных образцов, на этапе 406 процессор должен адаптировать образцы 316 генератора стимулов, вернуться к этапу 403, контролировать еще на этапе 404 и затем на этапе 405 сравнить сигналы 313 и 314 снова.
Вторая стадия обучения может продолжаться неопределенно долго, продолжая адаптировать излучаемый стимул к продолжающемуся ухудшению области 307.
Альтернативно протезное устройство использует только вторую стадию обучения, со ссылкой на базу данных образцов стимул/ответ. Такое устройство хорошо подходит для применения следующему, например, при инсульте или травматическом повреждении головного мозга, где в отличие от постепенной деградации, обусловленной прогрессирующей болезнью, произошла внезапная деградация функции головного мозга.
Аспекты обучения процесса Фиг.4 могут быть представлены под управлением необязательного внешнего устройства 315. Благоприятно, если процесс обучения требует большого объема вычислений и требует больше средств, чем было бы легко вставить в имплантированное устройство.
Необязательно пациента можно попросить выполнить задания в течение первой и/или второй стадии обучения.
Процессор 310 включает функцию, которая позволяет извлекать из считанных сигналов выходной сигнал, который передается генератору 311 стимулов (например, генератору импульсов). Этот выходной сигнал может привести, например, к амплитудной, или частотной, или фазовой модуляции электрического стимула, генерируемого генератором стимулов 311. Функция, реализованная в 310, может быть усложнена, как, например, описано в статье Бергера. Альтернативно процессор может иметь более простые функции, такие как функцию передачи или функцию преобразования частоты.
Средства для считывания и анализа обнаруженных нервных сигналов хорошо известны в области техники. Например, путем использования алгоритмов обнаружения спайков (см., например, Zumsteg et al., IEEE Transactions on Neural Systems and Rehabilitation Engineering, 2005, Книга 13, стр. 272-279) можно определять наличие нервных сигналов спайков, обнаруженных чувствительным элементом(ами). Из этого может быть получена временная последовательность потенциалов действия, которая может дополнительно обрабатываться, например, для задавания частоты.
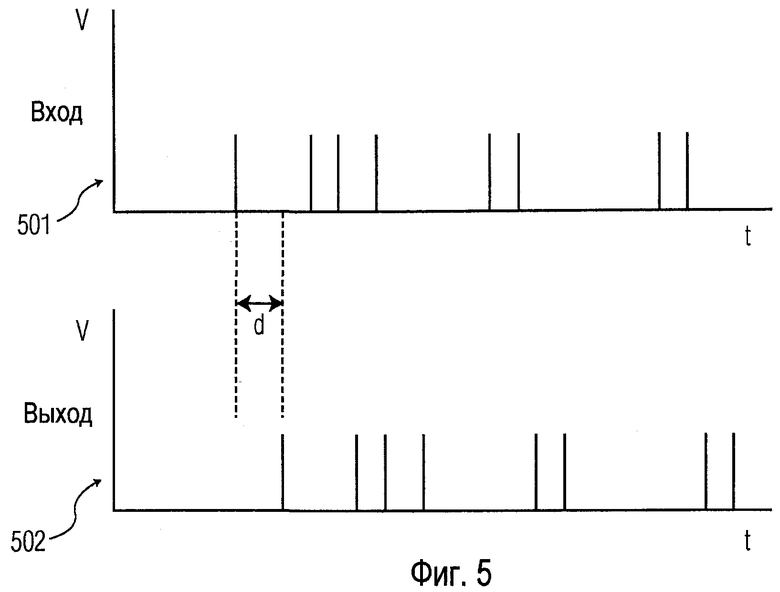
Фиг.5 иллюстрирует функцию передачи, подходящую для использования процессором 310. Эта фигура показывает считанный нервный сигнал 501 и выходной сигнал 502 стимула, имеющий фиксированную задержку в отношении считанного нервного сигнала. После того как нервный сигнал обнаружен (например, используя вышеупомянутые способы сортировки спайков), стимулятором генерируется выброс стимулов после заданной задержки. Оба сигнала иллюстрированы по величине напряжения в зависимости от времени. Типичная величина d задержки составляет 0,1-10 мс. Особая последовательность импульсов является только примерной иллюстрацией. Могут быть использованы другие последовательности. Могут быть использованы модулирующие входные сигналы, чтобы увеличить/уменьшить эту задержку d.
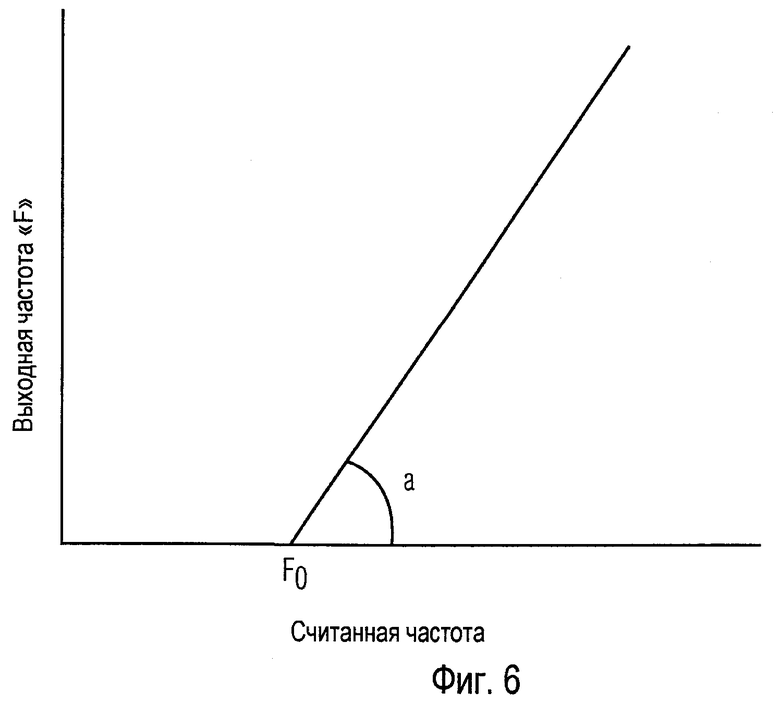
Фиг.6 иллюстрирует функцию преобразования частоты альтернативно подходящей для использования процессором 310. На этой фигуре частота считанного сигнала (действие-потенциал-серия, или потенциал поля), показанная на горизонтальной оси, соединена с частотой выходной серии импульсов, показанной на вертикальной оси. На этой фигуре F0 показывает пересечение с горизонтальной осью и «а» показывает угол, с которым функция пересекает горизонтальную ось. «F0» и «а» могут быть модулированы другими входными сигналами, например, сигналами обратной связи, или другими сигналами. Функция показана здесь как линейная, но может принимать другие формы.
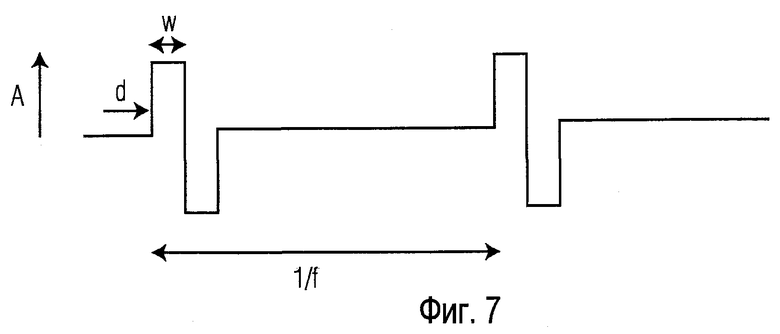
Фиг.7 иллюстрирует серию импульсов, производимых генератором стимулов 311. Фигура показывает импульсное напряжение или ток в зависимости от времени. Фигура показывает выброс амплитуды А, задержку d' и ширину w. Типичными пределами является амплитуда от 0,1 до 4 Вольт (или 0,1-4 мА, в зависимости от сопротивления электрода) и длительность импульса 10-1000 мкс.
Особенно предполагается, что дискинезия, особенно та, что связана с болезнью Паркинсона, будет реагировать на протез вида, иллюстрированного на Фиг.3, потому что полагается, что дискинезия обусловлена избыточной стимуляцией, некомпенсированной обратной связью, и не настроена на точное намерение прямой связью.
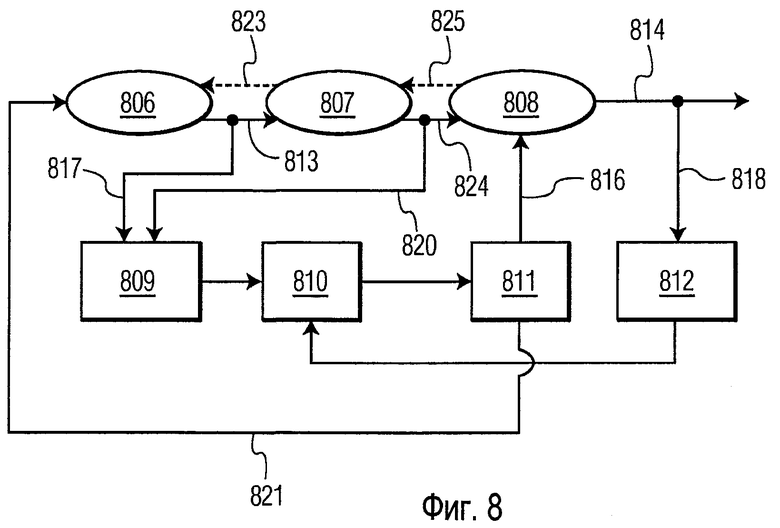
Фиг.8 показывает альтернативный вариант осуществления Фиг.3. На Фиг.8 последние два числа в номерах позиций в клетках и эллипсах показывают соотношение с теми клетками и эллипсами, имеющими те же самые последние два числа на Фиг.3. В варианте осуществления Фиг.8 пораженная область 807 имеет двусторонний поток сигналов 813, 823, 824, 825 с афферентными и эфферентными областями. Выходные сигналы 823 и 825 от 807 снова проиллюстрированы пунктирными линиями, показывающими, что они подразумеваются нарушенными, когда область 807 становится нарушенной. Фиг.8 включает два дополнительных канала 820 и 821 обратной связи, неиллюстрированных на Фиг.3.
Фиг.9А-D иллюстрируют вариант осуществления модуляции выходного сигнала нейростимулятора, основанной на считываемых сигналах. Фиг.9А и 9В показывают два считанных сигнала, вход 1 и вход 2. Каждый считанный сигнал включает в себя входной импульс 901 и 902, соответственно. Здесь выходная характеристика модулирована в соответствии со считанными сигналами от двух сенсоров. Амплитуда модуляции на временной шаг обозначена как δ, и в этом примере она связана с временной задержкой dt между обнаруженными сигналами на сенсорах 1 и 2. Модулируемый выходной сигнал может быть например непрерывной серией импульсов, как показано на Фиг.7, модуляция которой применена к одному или более параметрам (например, амплитуда импульсов, ширина импульсов или частота импульсов). Величина и знак δ в этом примере зависят от dt, как показано на двух эскизах Фиг.9С и Фиг.9D. В первом случае (Фиг.9С) для небольшой положительной dt модуляция строго положительна и опускается для более положительных величин dt; для небольшой отрицательной dt модуляция строго отрицательна, становясь менее отрицательной для более отрицательных величин dt. Второй пример (Фиг.9D) показывает альтернативную зависимость модуляции от dt; она близка к нулю для небольших величин dt и имеет строго положительную (отрицательную) величину около специфической отрицательной (положительной) величины dt и снова снижается до нуля для больших отрицательных и положительных величин dt. В конечном итоге модуляция, использованию которой обучается биомиметический протез, будет зависеть от того, какую неврологическую функцию следует заменить.
В основном функция, выполняемая процессорами 310 и 810, большей частью будет изучена на основе экспериментальных данных и поэтому не обязательно является предсказуемой заранее.
Из настоящего раскрытия специалистам в данной области техники будут очевидны другие модификации. Такие модификации могут включать в себя другие свойства, которые уже известны в разработке, производстве и используют неврологические протезные устройства и которые могут быть использованы вместо или в дополнение к свойствам, уже описанным здесь. Хотя формула изобретения была сформулирована в этой заявке в особенных комбинациях свойств, следует понимать, что область раскрытия настоящей заявки также включает любое новое свойство или новую комбинацию свойств, разглашенных здесь либо прямо или косвенно, или любое обобщение этого, не зависимо от того, уменьшает ли оно какую-либо или все одинаковые технические проблемы, как осуществляется в настоящем изобретении. Заявители таким образом уведомляют, что к таким свойствам может быть сформулирована новая формула изобретения в течение рассмотрения настоящей заявки или какой-либо дальнейшей заявке, производной от этой.
Используемые здесь слова «включающий», «включают» или «включает» не следует рассматривать как исключающие дополнительные элементы. Используемое здесь единственное число не следует рассматривать как исключение наличия множества элементов.
| название | год | авторы | номер документа |
|---|---|---|---|
| СИСТЕМА СТИМУЛЯЦИИ ФУНКЦИОНИРОВАНИЯ ОРГАНОВ | 2009 |
|
RU2401137C1 |
| СПОСОБ ЛЕЧЕНИЯ РАССТРОЙСТВ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ ПОСРЕДСТВОМ УСТРОЙСТВА ДЛЯ НЕЙРОСТИМУЛЯЦИИ | 2006 |
|
RU2491104C2 |
| СПОСОБ ЭЛЕКТРОСТИМУЛЯЦИИ И ПРИБОР ДЛЯ ЭЛЕКТРОСТИМУЛЯЦИИ | 2018 |
|
RU2771207C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ФУНКЦИОНАЛЬНОГО СОСТОЯНИЯ ЭМОЦИОГЕННЫХ ЦЕРЕБРАЛЬНЫХ СИСТЕМ ЧЕЛОВЕКА | 2007 |
|
RU2336016C1 |
| СПОСОБ ИНВАЗИВНОЙ ЭЛЕКТРОСТИМУЛЯЦИИ СПИННОГО МОЗГА МОДУЛИРОВАННЫМИ ЭЛЕКТРИЧЕСКИМИ ИМПУЛЬСАМИ | 2016 |
|
RU2618206C1 |
| СПОСОБ ЛЕЧЕНИЯ БОЛЕЗНИ АУРИКУЛЯРНОЙ АНЕСТЕЗИЕЙ ЧЕРЕПНЫХ НЕРВОВ | 2016 |
|
RU2701548C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СКОРОСТИ ФОРМИРОВАНИЯ МОТОРНЫХ ПРОГРАММ В ЦЕНТРАЛЬНОЙ НЕРВНОЙ СИСТЕМЕ ЧЕЛОВЕКА | 2007 |
|
RU2340281C2 |
| СПОСОБ ФОРМИРОВАНИЯ СИСТЕМЫ УПРАВЛЕНИЯ МОЗГ-КОМПЬЮТЕР | 2019 |
|
RU2704497C1 |
| СПОСОБ ИССЛЕДОВАНИЯ НЕЙРОПСИХОЛОГИЧЕСКИХ МЕХАНИЗМОВ СТАНОВЛЕНИЯ ПРОСТРАНСТВЕННОГО СЛУХА У ДЕТЕЙ РАННЕГО ДОШКОЛЬНОГО ВОЗРАСТА | 2011 |
|
RU2454933C1 |
| Модуль популяции нейронов | 1989 |
|
SU1732356A1 |
Изобретение относится к медицинской технике, а именно к способам и устройствам для нейростимулирующей терапии. Нейромиметическое устройство включает первый и второй входы, выполненные с возможностью принимать нервные сигналы, при этом первый вход принимает сигналы, афферентные к подозрительной области, а второй вход - отличной от подозрительной области. Выход, выполненный с возможностью излучать нервные совместимые сигналы, эфферентные к подозрительной области. Блок обработки сигналов содержит канал прямой связи, расположенный между первым входом и выходом и канал модуляции, выполненный с возможностью принимать сигналы от второго входа и обеспечивать модулирующий сигнал в канал прямой связи. Канал прямой связи включает первый сенсор, процессор, выполненный с возможностью обучения и имитации функций подозрительной области, которая является второй нервной областью, и генератор стимулов, выполненный с возможностью подавать сигналы к эфферентной третьей нервной области, предполагаемой здоровой. Способ замены функционирования подозрительной нервной ткани содержит этапы имплантации нейромиметического устройства, излучения по меньшей мере одного стимула, основанного на функции обработки, контроля сигналов, принятых от первого и второго входов, сравнения образцов сигналов, принятых на первом и втором входах, и адаптации образца излучения на основе результата сравнения. Использование изобретения позволяет повысить адаптивность и гибкость при диагностике и лечении нейромоторных исходов, таких как болезнь Паркинсона. 2 н. и 10 з.п. ф-лы, 9 ил.
1. Нейромиметическое устройство, включающее:
по меньшей мере первый и второй входы (317, 318), выполненные с возможностью принимать нервные сигналы, при этом первый вход (317) выполнен с возможностью принимать сигналы, афферентные к подозрительной области (307), а второй вход (318) выполнен с возможностью принимать сигналы от нервной области (308), отличной от подозрительной области;
по меньшей мере, один выход (316), выполненный с возможностью
излучать нервные совместимые сигналы, эфферентные к подозрительной области; и
по меньшей мере, один блок обработки сигналов, содержащий канал (309, 310, 311) прямой связи, расположенный между первым входом и выходом, и канал (312) модуляции, выполненный с возможностью принимать сигналы от второго входа и обеспечивать модулирующий сигнал в канал прямой связи,
причем канал прямой связи включает в себя:
первый сенсор (309), выполненный с возможностью принимать первые сигналы, выходящие от афферентной первой нервной области (306), предполагаемой здоровой;
процессор (310), выполненный с возможностью обучения и имитации функций подозрительной области (307), которая является второй нервной областью; и
генератор (311) стимулов, выполненный с возможностью подавать сигналы к эфферентной третьей нервной области (308), предполагаемой здоровой.
2. Устройство п.1, в котором второй вход (318) выполнен с возможностью принимать сигналы от нервной области (308), эфферентной к подозрительной области (307).
3. Устройство п.1, в котором канал прямой связи включает в себя, по меньшей мере, один процессор для выполнения операций, при этом операции включают в себя:
контролирование (401) сигналов, принятых от первого и второго входов в течение первого периода времени;
обучение (407) процессора в течение первого периода времени производить функции обработки, чтобы производить сигналы, принимаемые от второго входа, в ответ на сигналы, принятые от первого входа; обнаружение (402), что подозрительная область стала дисфункциональной после первого периода времени;
выполнение (403) заученных функций обработки в течение второго периода времени;
контролирование (404) сигналов, принятых от первого и второго входов в течение второго периода времени; и
изменение (406) функций обработки в течение второго периода времени в ответ на определение (405), что сигналы, принятые на втором входе, не согласуются с сигналами, заученными в течение процесса обучения.
4. Устройство п.3, дополнительно включающее в себя, по меньшей мере, один третий вход (330) для приема сигналов, сгенерированных извне (315), к телу пациента, и при этом обнаружение осуществляется в ответ на сигналы, принятые на третьем входе.
5. Устройство п.1, в котором канал прямой связи включает в себя узел генератора стимулов, соединенный с выходом.
6. Устройство п.1, в котором второй вход выполнен с возможностью принимать сигналы, эфферентные к выходу, и при этом модуляция включает в себя обратную связь, осуществляемую в ответ на эти эфферентные сигналы.
7. Устройство п.1, дополнительно включающее в себя, по меньшей мере, один третий вход (330) для приема сигналов, сгенерированных извне (315), к телу пациента.
8. Устройство п.1, в котором канал модуляции включает в себя второй сенсор (312), выполненный с возможностью принимать сигналы от четвертой области, эфферентной к выходу генератора (311) стимулов, и подавать модулирующий сигнал на процессор (310).
9. Устройство п.1, в котором:
подозрительная область (807) сообщается двунаправлено (813, 823, 824, 825) с первой и третьей нервными областями (806, 808);
первый сенсор (809) дополнительно выполнен с возможностью приема вторых сигналов, эфферентных к подозрительной области, но афферентных к выходу (816) узла (811) генератора стимулов; и
устройство дополнительно включает в себя канал (821) обратной связи от узла (811) генератора стимулов к зоне, афферентной к первому входу, к первому сенсору.
10. Устройство п.1, в котором предполагается, что подозрительная область (807) сообщается двунаправлено (813, 823, 824, 825) с прилежащей тканью, и устройство дополнительно включает в себя:
первое соединение (820) с первым сенсором (809) от области, расположенной между подозрительной областью и выходом узла генератора стимулов; и
второе соединение (821) с первой нервной областью (806) от узла генератора стимулов.
11. Способ замены функционирования подозрительной нервной ткани, при этом способ содержит этапы, на которых:
имплантируют нейромиметическое устройство, при этом устройство включает в себя, по меньшей мере, один выход (316), выполненный с возможностью излучать нервные совместимые сигналы, эфферентные к подозрительной области (307), по меньшей мере первый (317) и второй (318) входы выполнены с возможностью принимать нервные сигналы, первый вход (317) выполнен с возможностью принимать сигналы, афферентные к подозрительной области (307), и второй вход выполнен с возможностью принимать сигналы, эфферентные к выходу (316), и по меньшей мере один блок обработки сигналов содержит канал (309, 310, 311) прямой связи, соединяющий первый вход и выход, и канал (312) обратной связи, выполненный с возможностью принимать сигналы от второго входа и обеспечивать сигнал обратной связи в канал прямой связи, причем канал прямой связи включает в себя:
первый сенсор (309), выполненный с возможностью принимать первые сигналы, выходящие от афферентной первой нервной области (306), предполагаемой здоровой;
процессор (310), выполненный с возможностью обучения и имитации функций подозрительной области (307), которая является второй нервной областью; и
генератор (311) стимулов, выполненный с возможностью подавать сигналы к эфферентной третьей нервной области (308), предполагаемой здоровой;
излучают (403) по меньшей мере один стимул, основанный на функции обработки;
контролируют (404) сигналы, принятые от первого и второго входов;
сравнивают (405) образцы сигналов, принятых на первом и втором входах; и
адаптируют (406) образец излучения на основе результата сравнения.
12. Способ п.11, дополнительно содержащий этапы, на которых:
принимают (401) сигналы, принятые от первого и второго входов в течение первого периода времени;
обучают (407) функциям обработки в течение первого периода времени, чтобы обеспечивать сигналы, принимаемые на втором входе (318), в ответ на сигналы, принятые на первом входе (317);
обнаруживают (402), что подозрительная область стала дисфункциональной после первого периода времени; и выполняют этапы излучения (403), контролирования (404), сравнения (405) и адаптации (406) в течение второго периода времени.
| BERGER W.T | |||
| et al | |||
| "Brain-Implantable Biomimetic Electronics as the Next Era in Neural Prosthetics", PROCEEDINGS OF THE IEEE, vol.89, №7, July 2001, p.p.993-1012 | |||
| WENTAI LIU et al | |||
| "Implantable biomimetic microelectronic systems design" | |||
| Engineering in Medicine and Biology Society, v.24, Issue 5, p.p.66-74, 26.09.2005, реферат | |||
| WO 2005053787 |
Авторы
Даты
2012-09-20—Публикация
2007-12-18—Подача