Изобретение относится к медицинской технике и может быть использовано при производстве имплантатов и костных шурупов, а также в стоматологии при операциях имплантации, в травматологии при остеосинтезе.
Известен способ изготовления стоматологического имплантата с многослойным биоактивным покрытием (патент РФ 2146535). Данный способ включает предварительную пескоструйную обработку имплантата для получения шероховатости поверхности и плазменное напыление, которое позволяет обеспечить адгезионную прочность, однако не создает поверхностной упорядоченной пористости покрытия, в результате чего снижается уровень его остеоинтеграции.
Известен способ (патент РФ 2386454) покрытия на титане и его сплавах, который содержит оксиды титана и меди в определенном количественном соотношении и лантан. Формирование покрытия осуществляют электрохимическим путем в двух электролитах. Способ позволяет получить оксидное покрытие, обладающее бактерицидными и антикоагулянтными свойствами. Недостатками данного способа являются содержащиеся в поверхности включения меди, которая отрицательно влияет на остеоинтеграцию. Данный способ не позволяет получить упорядоченной пористости покрытия (наноструктуры) с биоинертными свойствами оксида титана.
Известен способ нанесения покрытия на имплантат из титана и его сплавов, взятый за прототип (патент РФ 2154463), заключающийся в анодировании титана и его сплавов. Данный способ не позволяет получить достаточную поверхностную пористость покрытия, что снижает его остеоинтеграционные свойства. Известные из уровня техники включения в состав покрытия оксидов меди, гидроксиаппатитов, фосфора и кальция нарушают сплошность оксидной пленки из TiO2, могут приводить к сколам, что отрицательно влияет на остеоинтеграцию.
Известно, что наиболее предсказуемым методом является двухэтапная внутрикостная имплантация, при которой используют разборные имплантаты. Наличие внутренней резьбы и посадочной поверхности для соединения с внекостными частями значительно ослабляют конструкцию имплантата, что особенно критично при малых диаметрах имплантата.
Имплантаты для стоматологии в настоящее время производят из технически чистого титана (Grade 1-4 ASTM, ISO) или ВТ 1-0 по ГОСТ, предел прочности составляет 300-550 МПа. По механическим свойствам он уступает сплавам титана марки Ti6Al4V (ВТ-6), предел прочности которого - 850-1000 МПа.
Сплав Ti6Al4V (ВТ6) также используется для производства имплантатов и костных шурупов, но не может считаться оптимальным, так как увеличение прочности в сплаве достигается за счет введения в его состав алюминия и ванадия. Установлено, что добавки алюминия снижают коррозионную стойкость титана в активном и пассивном состояниях.
Используемые в медицине свойства чистого титана - биоинертность, способность к интеграции в костной ткани без воспалительной инкапсуляции, присущи титану благодаря образующейся на его поверхности пленке оксида титана.
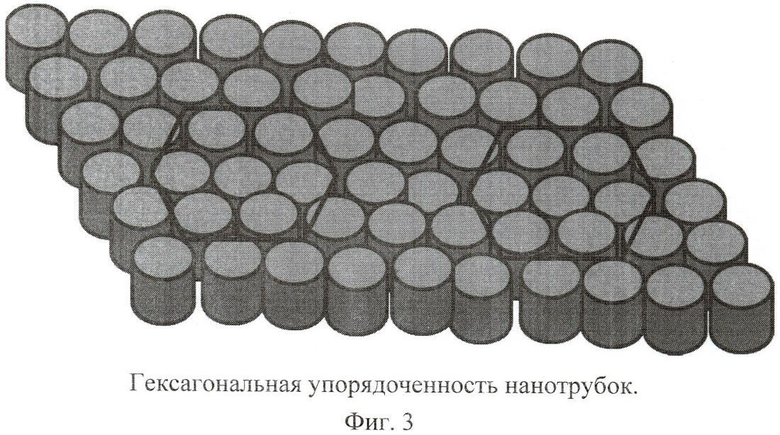
Задачей предлагаемого изобретения является получение на поверхности имплантатов (костных шурупов), изготовленных из титана и сплавов титана, наноструктурной ориентированной пористой поверхности, состоящей из открытых нанотрубок оксида титана TiO2 или (и) Ti2O3 гексагональной и тетрагональной сингонии (упорядоченности).
Задачей предлагаемого изобретения также является получение на имплантатах, изготовленных из сплавов титана (ВТ16, ВТ-6, BT6-ELI, ВТ-5, ВТ14, Ti15Mo, α-татановые, α/β-титановые и β-титановые сплавы и др.), биоинертной оксидной пленки, сходной по структуре и остеоинтеграционным свойствам с оксидной пленкой, образующейся на технически чистом титане.
Задачей предлагаемого изобретения также является создание имплантатов для стоматологии и травматологии с наноструктурированной пористой поверхностью с повышенными биоинертными и остеоинтеграционными свойствами.
Поставленная задача решается следующей совокупностью существенных признаков.
Для создания наноструктурной пористой поверхности, состоящей из ориентированных нанотрубок оксида титана TiO2 и (или) Ti2O3 гексагональной упорядоченности заданной толщины, поверхность имплантата (титана) после пескоструйной обработки подвергают травлению в растворе HF (2-3% масс.), или HF (2-3% масс.) + HNO3 (5-30% масс.), или HNO3 + HCl (10-30% масс.), после чего проводят обжиг - дегазацию в вакууме при температуре 300-770°C, затем проводят электрохимическое оксидирование (анодирование) постоянным или импульсным (0,5 Гц) током в растворе электролита, при формирующем напряжении 25-130 В (время выдержки от 0,1 сек до 100 сек, в зависимости от силы (плотности) тока), после которого проводят отжиг в печи при температуре 300-550°С в вакууме.
Последовательность существенных признаков - пескоструйная обработка для придания шероховатости, травление в кислотах для удаления примесей и получения на поверхности чистого титана, обжиг - дегазация в вакууме для удаления растворенных газов и снятия напряжений, анодирование (однофазное или двухфазное) при формирующем напряжении 25-130 В, отжиг в печи до 300-550°C для структурирования оксидной пленки и удаления связанной воды из пор поверхности.
Техническим результатом данного изобретения является получение структуры биосовместимого (биоинертного) нанопокрытия на имплантатах, состоящего из открытых нанотрубок оксида титана, расположенных перпендикулярно поверхности, с размерами пор 40-140 нм, что повышает смачиваемость, повышает всасывающую способность и позволяет внедряться в них молекулам. Техническим результатом данного изобретения является также создание имплантатов из высокопрочных сплавов титана, покрытых биоинертнертной оксидной пленкой, сходной по составу, структуре и остеоинтеграционным свойствам с оксидной пленкой, образующейся на технически чистом титане, что увеличит возможности дентальной имплантологии и травматологии за счет применения более прочных имплантатов и костных шурупов.
Заявляемый способ позволяет получить оксидную пленку на поверхности титана и его сплавов, состоящую из нанотрубок оксида титана, ориентированных перпендикулярно металлической основе, диаметр которых можно изменять в пределах нескольких десятков нанометров в зависимости от напряжения и состава электролита. Важным преимуществом открытых нанотрубок оксида титана является их пористость и высокая удельная площадь поверхности.
Предлагаемый способ осуществляется следующим образом.
Имплантаты, после пескоструйной обработки, подвергали травлению в растворе HF (2-3% масс.), или HF (2-3% масс.) + HNO3 (5-30% масс.), или HNO3 + HCl (10-30% масс.), после чего в печи проводили обжиг - дегазацию в вакууме при температуре от 300-770°C, затем проводили однофазное или двухфазное электрохимическое оксидирование (анодирование) в водном растворе щавелевой кислоты, обычно 5-20%, при формирующем напряжении 25-130 В (время выдержки от 0,1 сек до 100 сек, в зависимости от силы (плотности) тока). В результате образуется пористая поверхность, состоящая из нанотрубок оксида титана TiO2, толщиной от 1 до 10 мкм в зависимости от параметров тока. Для удаления связанной воды, остающейся в порах, снятия напряжения оксидной пленки и кристаллизации оксида титана повторно проводили отжиг в печи (преимущественно в вакууме) при температуре 300-550°C, в результате чего происходит кристаллизация оксида титана в форме анатаза.
В зависимости от сплава оксидирование может выполняться двухфазным способом: т.е. проводят предварительное оксидирование при напряжении 30-90 В, затем полученную оксидную пленку удаляют травлением в специальном растворе, обычно используют HF (2-3% масс.), или HF (2-3% масс.) + HNO3 (5-30% масс.), или HNO3 + HCl (10-30% масс.), тем самым получают структурированную поверхность чистого титана, после чего повторно проводят электрохимическое оксидирование при формирующем напряжении 30-130 В, создавая структурированную поверхность открытых нанотрубок оксида титана. В качестве электролита для анодирования в способе могут использоваться растворы кислот - ортофосфорной, лимонной, серной и др., обычно используют раствор щавелевой кислоты различной концетрации, или р-р сульфосалициловой (или салициловой к-ты), или их смесь в соотношении от 1:1 до 1:10. Концетрация подбирается в зависимости от обрабатываемого сплава титана.
Заданную толщину оксидной пленки обычно от 1 до 7 мкм формируют путем изменения напряжения тока. Чем выше напряжения, тем большую толщину получают при оксидировании. При большей толщине оксидной пленки (>10 мкм) происходит слипание - «закрытие» верхних концов нанотрубок.
Заявленный способ был определен путем проведения испытаний по электрохимическому оксидированию титановых образцов из различных сплавов и их исследований путем электронной микроскопии (РЭМ).
Образцы, окисленные при напряжениях 50-110 В, обладают открытой пористостью. Внутренний диаметр пор линейно зависит от напряжения и изменяется в пределах от 40 до 140 нм.
При малых радиусах пор механические напряжения могут приводить к сжатию трубок и закрытию ее концов.
Образцы имплантатов, которые подвергали электрохимическому окислению при напряжениях до 20 В, образуют тетрагональное упорядочение пор. При напряжениях 30-110 B поры оксидной пленки образует гексогональную кристаллическую структуру. При применении сплавов титана, содержащих различные химические примеси, также происходило «закрытие» концов напотрубок.
При использовании двухстадйного окисления (т.е. предварительное окисление с удалением пленки TiO2 для получения структурированной поверхности металлического титана и второе окисление для формирования упорядоченной структуры нанотрубок) получен оксид открытых нанотрубок оксида титана с «открытым» гексагональным упорядочением нанопор.
Оксид титана с гексогональной сингонией Фиг.3 (сходноугольность, группировка, ориентация, упорядоченность) нанотрубок является более плотной структурой с повышенной площадью пористости по сравнению с тетрагональной сингонией. Преимуществом данного изобретения является также создание имплантатов и костных шурупов с высокими остеоинтеграционными свойствами, что способствует сокращению сроков лечения методом стоматологической имплантации, а также повышает эффективность при сращивании костей, дистракционном остеосинтезе в стоматологии и травматологии.
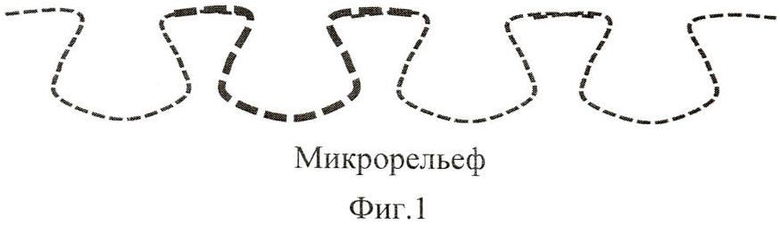
Таким образом, кроме известных из уровня техники способов обработки имплантатов - создание «макрорельефа» - форма, резьба имплантата и «микрорельефа» Фиг.1 - пескоструйная обработка, травление в кислотах, предложен способ создания «нанорельефа» Фиг.2 - структурированных нанопор - нанотрубок оксида титана в «микрорельефе» покрытия имплантата.
Имплантаты из титана и его сплавов с покрытием, полученным заявленным способом, прошли токсикологические испытания на биосовместимость и биоинертность. В качестве контроля использовали имплантаты, изготовленные из технически чистого титана ВТ1-0, с пескоструйной обработкой поверхности.
Были проведены технические испытания на прочность покрытия имплантатов, подвергнутых напряжениям сжатия и растяжения.
Также были проведены испытания на прочность покрытия в агрессивных средах путем погружения образцов из сплава ВТ-6 в 10%-ный водный раствор HCl. В результате проведенных испытаний было установлено, что наноструктурная окисная пленка TiO2, сформированной двухфазным анодированием, абсолютно биоинертна, аналогично имплантатам из ВТ1-0, полностью защищает поверхность от растравливания, выдерживает напряжения, по силе превосходящие физиологические нагрузки в 2,-3 раза.
Источники информации
1. Грилихес С.Я. Обезжиривание, травление и полирование металлов. - Л.: Машиностроение, 1983, 102 с.
2. Патент РФ №2159094, 2000. Способ нанесения покрытия на имплантат из титана и его сплавов.
3. Патент РФ №2154463, 2000. Покрытие на имплантат из титана и его сплавов и способ его нанесения.
4. Rouquerol J., Recommendations for the characterization of porous solids. Pure Appl. Chem. vol. 66, 1994, pp.1739-1758.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ФОРМИРОВАНИЯ НАНОСТРУКТУРИРОВАННОГО БИОИНЕРТНОГО ПОКРЫТИЯ НА ТИТАНОВЫХ ИМПЛАНТАТАХ | 2015 |
|
RU2604085C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ МИКРО-НАНОСТРУКТУРИРОВАННОГО ПОРИСТОГО СЛОЯ НА ПОВЕРХНОСТИ ТИТАНОВЫХ ИМПЛАНТАТОВ | 2018 |
|
RU2677271C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ВНУТРИКОСТНОГО ИМПЛАНТАТА | 2018 |
|
RU2687792C1 |
| ПОКРЫТИЕ НА ИМПЛАНТАТ ИЗ ТИТАНА И ЕГО СПЛАВОВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2008 |
|
RU2361623C1 |
| ДЕНТАЛЬНЫЙ ИМПЛАНТАТ (ВАРИАНТЫ) И СПОСОБ ВНУТРИКОСТНОЙ ИМПЛАНТАЦИИ | 2003 |
|
RU2273464C2 |
| Способ формирования нанопористого оксида на поверхности имплантата из порошкового ниобия | 2015 |
|
RU2633143C2 |
| СТОМАТОЛОГИЧЕСКИЙ ИМПЛАНТАТ | 2002 |
|
RU2202984C1 |
| ПОКРЫТИЕ НА ИМПЛАНТ ИЗ ТИТАНА И ЕГО СПЛАВОВ И СПОСОБ ЕГО ПРИГОТОВЛЕНИЯ | 2012 |
|
RU2502526C1 |
| Способ получения фотокатализатора на основе нанотубулярного диоксида титана | 2019 |
|
RU2732130C1 |
| ОКСИДНОЕ ПОКРЫТИЕ НА ЧРЕСКОСТНЫЕ ОРТОПЕДИЧЕСКИЕ ИМПЛАНТАТЫ ИЗ НЕРЖАВЕЮЩЕЙ СТАЛИ | 2011 |
|
RU2465015C1 |

Изобретение относится к способу создания наноструктурной пористой поверхности имплантатов из титана и сплавов титана. Заявленный способ включает пескоструйную обработку для придания шероховатости, травление в кислотах для удаления примесей и получения на поверхности чистого титана, обжиг - дегазацию для удаления растворенных газов и снятия напряжений, однофазное или двухфазное анодирование (электрохимическое оксидирование) и обжиг в печи для структурирования кристаллов и удаления связанной воды из пор поверхности. Обжиг - дегазацию проводят в вакууме при температуре 300-770°C, анодирование проводят постоянным или импульсным током (0,5 Гц) в растворе электролита при формирующем напряжении 25-130 В, а отжиг в печи проводят при температуре 300-550°C. Заявленный способ позволяет получить пористую наноструктурированную оксидную пленку толщиной 1-10 мкм, которая состоит из открытых нанотрубок оксидов титана с размерами пор 40-140 нм гексагональной или тетрагональной упорядоченности. 5 з.п. ф-лы, 3 ил.
1. Способ создания наноструктурированной (наноструктурной) пористой поверхности имплантатов из титана и сплавов титана, включающий пескоструйную обработку, травление в растворах кислот и анодирование, отличающийся тем, что поверхность имплантата (титана) после пескоструйной обработки подвергают травлению для получения поверхности чистого титана, после чего проводят обжиг - дегазацию в вакууме при температуре 300-770°C, затем проводят однофазное или двухфазное электрохимическое оксидирование (анодирование) постоянным или импульсным (0,5 Гц) током в растворе электролита при формирующем напряжении 25-130 В, после которого проводят отжиг в печи при температуре 300-550°C, в результате чего формируется пористая наноструктурированная оксидная пленка толщиной 1-10 мкм, состоящая из открытых нанотрубок оксида титана TiO2 и/или Ti2O3 с размерами пор от 40 до 140 нм гексагональной или тетрагональной упорядоченности.
2. Способ создания наноструктурированной пористой поверхности имплантатов из титана и сплавов титана по п.1, отличающийся тем, что поверхность имплантата (титана) после пескоструйной обработки подвергают травлению в растворе HF (2-3 мас.%), или HF (2-3 мас.%) + HNO3 (5-30 мас.%), или HNO3 + HCl (10-30 мас.%).
3. Способ создания наноструктурированной пористой поверхности имплантатов из титана и сплавов титана по п.1, отличающийся тем, что оксидирование проводится двухфазным способом: вначале проводят предварительное оксидирование при напряжении 30-90 В, затем полученную оксидную пленку удаляют травлением в растворе HF (2-20 мас.%) или HF (2-3 мас.%) + HNO3 (5-30 мас.%), тем самым получают структурированную поверхность чистого титана, после чего повторно проводят электрохимическое оксидирование при формирующем напряжении 30-130 В, создавая структурированную поверхность открытых нанотрубок оксида титана.
4. Способ создания наноструктурированной пористой поверхности имплантатов из титана и сплавов титана по п.1, отличающийся тем, что в качестве электролита для анодирования используют 5-20%-ный водный раствор щавелевой кислоты.
5. Способ создания наноструктурированной пористой поверхности имплантатов из титана и сплавов титана по п.1, отличающийся тем, что в качестве электролита для анодирования используют раствор сульфосалициловой кислоты.
6. Способ создания наноструктурированной пористой поверхности имплантатов из титана и сплавов титана по п.1, отличающийся тем, что указанный имплантат является двухэтапным стоматологическим винтовым имплантатом.
| ПОКРЫТИЕ НА ИМПЛАНТАТ ИЗ ТИТАНА И ЕГО СПЛАВОВ И СПОСОБ ЕГО НАНЕСЕНИЯ | 1999 |
|
RU2154463C1 |
| KR 1020070011200 A, 24.01.2007 | |||
| БИОАКТИВНОЕ ПОКРЫТИЕ НА ИМПЛАНТАТЕ ИЗ ТИТАНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2008 |
|
RU2385740C1 |
| НИТРОЦЕЛЛЮЛОЗНАЯ ЭМАЛЬ | 1999 |
|
RU2168527C1 |
| СПОСОБ НАНЕСЕНИЯ ПОКРЫТИЯ НА ИМПЛАНТАТ ИЗ ТИТАНА И ЕГО СПЛАВОВ | 1999 |
|
RU2159094C1 |
| CN 0101518467 A, 02.09.2009. | |||
Авторы
Даты
2012-12-20—Публикация
2011-06-30—Подача