Изобретение относится к медицине, а именно к лучевой терапии в офтальмологии, и может быть использовано для расчета распределения дозных нагрузок на структуры орбиты при проведении брахитерапии опухолей орбиты.
Превышение толерантных значений доз ионизирующего излучения для структур орбиты при проведении лучевой терапии опасно развитием необратимых осложнений, приводящих к снижению функций органа зрения и неудовлетворительным косметическим результатам лечения. Кумуляция тумороцидной дозы в опухолевом очаге с минимальным облучением окружающих здоровых структур является одной из главных задач при проведении лучевой терапии. Моделирование клинических ситуаций опухолей орбиты и разработка схем облучения методом брахитерапии на доклиническом этапе предназначено для решения поставленной задачи.
Авторам не известны способы моделирования постоперационной брахитерапии опухолей орбиты.
Задачей изобретения является моделирование имплантационно-расчетного этапа брахитерапии опухолей орбиты.
Техническим результатом является разработка схем размещения радиоактивных источников в зависимости от локализации и объема ложа удаленной опухоли (ЛУО), что позволит уменьшить дозные нагрузки на здоровые структуры орбиты и снизить риск лучевых осложнений.
Технический результат достигается тем, что в способе моделирования постоперационной брахитерапии опухолей орбиты создают модель орбиты человека в масштабе 1:1, содержащую рентгеноконтрастные модели структур орбиты, включающие глазное яблоко, зрительный нерв, прямые мышцы, ЛУО, и заполняют тканеэквивалентным материалом; выполняют компьютерную томографию (КТ) модели орбиты, получают серии сканов во фронтальной и сагиттальной плоскостях с изображениями структур модели орбиты; на передней поверхности модели орбиты маркируют квадрант локализации модели ЛУО; создают макеты радиоактивных источников (МРИ) йод-125 в масштабе 1:1 и размещают их в носителе цепочкой вплотную друг за другом либо на расстоянии до 7 мм друг от друга по 1-5 МРИ, который представляет собой полую гибкую полимерную трубочку диаметром, соответствующим диаметру МРИ; носители с МРИ равномерно размещают в ЛУО параллельно друг другу на расстоянии 4-6 мм; проводят контрольную КТ модели орбиты и получают серии сканов во фронтальной и сагиттальной плоскостях с изображениями структур орбиты и МРИ; с помощью программы для планирования брахитерапии Permanent Seed Implant Dosimetry (PSID 4.5) и серии сканов КТ выполняют расчет доз ионизирующего излучения на структуры модели орбиты и подбирают параметры облучения, при которых распределение дозных нагрузок будет соответствовать максимуму в ЛУО и минимуму на структуры орбиты.
Предлагаемый способ осуществляется следующим образом. Создают модель орбиты человека в масштабе 1:1, содержащую модели глазного яблока, зрительного нерва, прямых мышц и ЛУО, заполняют орбиту тканеэквивалентным материалом. Модели структур орбиты и ЛУО выполнены из эластичного материала, содержащего рентгенконтрастные включения. Форма, размер и локализация модели ЛУО зависит от моделируемой клинической ситуации. Выполняют КТ модели орбиты, получают серии сканов во фронтальной и сагиттальной плоскостях с изображениями структур модели орбиты. На передней поверхности модели орбиты маркируют квадрант локализации модели ЛУО. Создают МРИ йод-125, имеющие форму и размеры, идентичные самому радиоактивному источнику (капсулы длиной 4,5 мм и диаметром 0,8 мм) и выполненные из металла, и размещают их в носителях цепочкой вплотную друг за другом либо на расстоянии до 7 мм друг от друга по 1-5 МРИ. Носитель представляет собой полую гибкую полимерную трубочку, внутренним диаметром 0,9 мм, наружным диаметром 1,5 мм и длиной 4-5 см в зависимости от глубины нахождения ЛУО. Равномерно и параллельно относительно друг друга носители с МРИ размещают в ЛУО в модели орбиты на расстоянии 4-6 мм друг от друга с помощью жесткого проводника (разрезанной иглы). Проводят контрольную КТ модели орбиты и получают серии сканов во фронтальной и сагиттальной плоскостях с изображениями структур орбиты и МРИ. С помощью программы для планирования брахитерапии PSID 4.5 проводят графическое обозначение контуров структур орбиты и облучаемого объема тканей орбиты, включающего ЛУО и 3 мм окружающих тканей орбиты. На основании известной величины суммарной очаговой дозы в облучаемом объеме тканей орбиты, активности и количества МРИ методом последовательного подбора с помощью численных алгоритмов выполняют расчет доз ионизирующего излучения на структуры орбиты и необходимой длительности экспозиции источников и подбирают параметры (время экспозиции и пространственное распределение макетов источников), при которых распределение дозных нагрузок будет соответствовать максимуму в облучаемом объеме тканей орбиты и минимуму на структуры орбиты.
Пример
Способ моделирования постоперационной брахитерапии опухолей орбиты представлен на примере удаленной опухоли слезной железы. В модель орбиты человека помещают модели глазного яблока, зрительного нерва и прямых мышц. В передний верхне-латеральный отдел орбиты помещают модель ЛУО, которая по форме сходна со слезной железой и имеет размеры 8/15/3 мм.
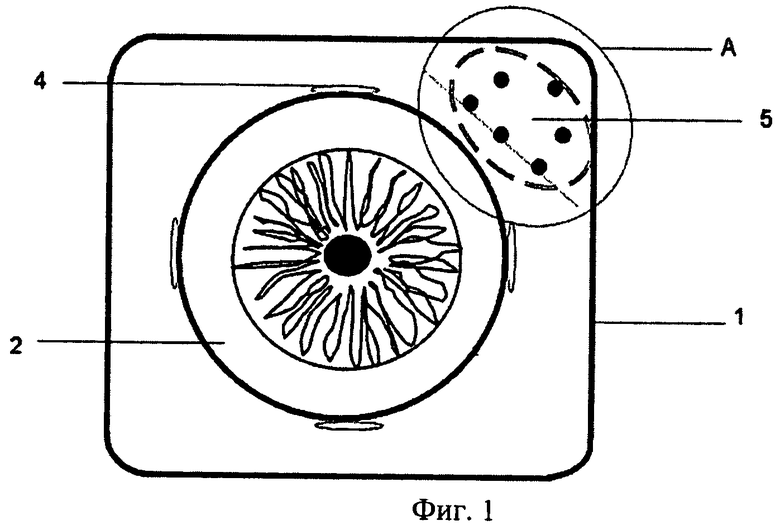
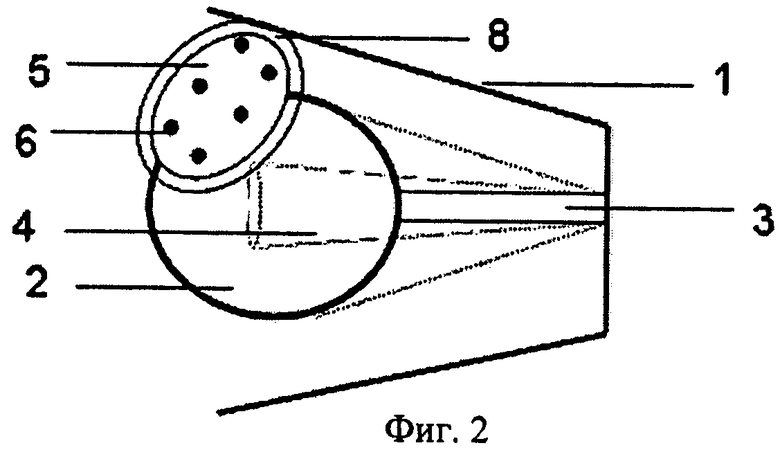
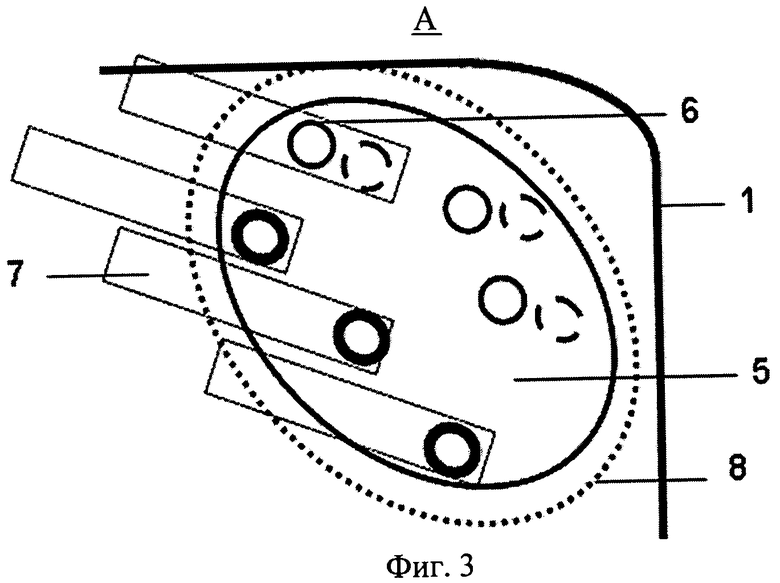
Изобретение поясняется фиг.1-3. На фиг.1 представлен общий вид модели орбиты с моделями структур орбиты, вид прямо; на фиг.2 - общий вид модели орбиты с моделями структур орбиты, вид сбоку. На фиг.3 представлен вид А с фиг.1., на которой изображена схема размещения МРИ в ЛУО. Позицией 1 обозначена модель орбиты человека, позицией 2 - модель глазного яблока, позицией 3 - модель зрительного нерва, позицией 4 - модели четырех прямых мышц, позицией 5 - модель ложа удаленной опухоли (ЛУО), позицией 6 - макеты радиоактивных источников (МРИ), позицией 7 - носители макетов радиоактивных источников, позицией 8 - облучаемый объем тканей орбиты.
В модель орбиты человека 1 помещали модели глазного яблока 2, зрительного нерва 3 и прямых мышц 4. В передний верхне-латеральный отдел орбиты помещали модель ЛУО 5, которая имеет овальную форму. Заполняли орбиту тканеэквивалентным материалом. Проводили КТ модели орбиты и получали информацию о топографических особенностях структур модели орбиты 1. На передней поверхности модели орбиты 1 маркировали квадрант локализации модели ЛУО 5. Девять МРИ 6 размещали в шести носителях 7. Носители 7 с МРИ 6 размещали в ЛУО 5 в три параллельных ряда, расположенных по касательной к глазу (фиг.3): в первом ряду три носителя 7, содержащие по одному МРИ 6, носители 7 располагали на одной линии на расстоянии 6 мм друг от друга; во втором ряду два носителя 7, содержащих по два один за другим МРИ 6, располагали на расстоянии 10 мм друг от друга на одной линии; в третьем ряду один носитель 7, содержащий два МРИ 6, расположенных вплотную один за другим. Расстояние между тремя параллельными рядами носителей 7-3 мм. Далее проводили контрольную КТ модели орбиты 1. На полученных изображениях с помощью программы для планирования брахитерапии PSID 4.5 проводили графическое обозначение контуров структур модели орбиты 1 и облучаемого объема тканей орбиты 8, определяли положение МРИ 6. Суммарная доза ионизирующего излучения в облучаемом объеме тканей орбиты 8 составила 50 Гр. Активность одного МРИ 4,5 мКи, всего использовано девять МРИ. Далее с помощью численных алгоритмов выполняли расчет доз ионизирующего излучения на структуры орбиты. Получили, что необходимое время экспозиции источников составляет 7,3 суток, при этом на наружную прямую мышцу приходилось 11,1 Гр, на зрительный нерв 5,5 Гр, на заднюю поверхность глаза 6,4 Гр, на переднюю поверхность глаза 3,2 Гр.
Таким образом, при заданных параметрах и предложенной схеме расстановки МРИ возможно провести облучение без превышения толерантных значений для структур орбиты и подвести тумороцидную дозу к облучаемому объему тканей орбиты.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛУЧЕВОЙ ТЕРАПИИ ГЛАЗНЫХ ОПУХОЛЕЙ | 1990 |
|
RU2021793C1 |
| Способ оперативного формирования распределенной поглощенной дозы протонов в облучаемом объекте при проведении операций лучевой терапии | 2024 |
|
RU2823897C1 |
| Способ формирования распределений поглощенной дозы протонов в облучаемом объекте при проведении операций лучевой терапии | 2024 |
|
RU2837979C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ПОВРЕЖДАЮЩЕГО ДЕЙСТВИЯ ИОНИЗИРУЮЩЕГО ИЗЛУЧЕНИЯ НА ТВЕРДЫЕ ТКАНИ ЗУБА ЧЕЛОВЕКА | 2011 |
|
RU2462282C1 |
| СПОСОБ ДОЗИМЕТРИЧЕСКОГО ПЛАНИРОВАНИЯ ВНУТРИПОЛОСТНОЙ БРАХИТЕРАПИИ РАКА ШЕЙКИ МАТКИ | 2005 |
|
RU2299080C2 |
| ЗАКРЫТЫЙ ИСТОЧНИК ИОНИЗИРУЮЩЕГО ИЗЛУЧЕНИЯ (ВАРИАНТЫ) | 2002 |
|
RU2238121C2 |
| СПОСОБ ПРЕДЛУЧЕВОЙ ПОДГОТОВКИ БОЛЬНЫХ С ОПУХОЛЯМИ В ЗОНЕ ПРЕЦЕНТРАЛЬНОЙ ИЗВИЛИНЫ ГОЛОВНОГО МОЗГА | 2016 |
|
RU2632539C1 |
| Закрытый источник ионизирующего излучения и способ его подготовки к использованию | 2016 |
|
RU2621666C1 |
| СПОСОБ ЛЕЧЕНИЯ РАКА ПОЛОВОГО ЧЛЕНА И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2010 |
|
RU2459645C1 |
| Способ ультразвуковой диагностики инвазии юкстапапиллярной увеальной меланомы (УМ) в интрабульбарную часть зрительного нерва | 2023 |
|
RU2807527C1 |
Изобретение относится к медицине, а именно к лучевой терапии в офтальмологии. Создают модель орбиты человека в масштабе 1:1, содержащую рентгеноконтрастные модели структур. орбиты и заполняют тканеэквивалентным материалом; выполняют компьютерную томографию (КТ) модели орбиты, получают серии сканов во фронтальной и сагиттальной плоскостях. На передней поверхности модели орбиты маркируют квадрант локализации модели ложа удаленной опухоли (ЛУО); создают макеты радиоактивных источников (МРИ) йод-125 в масштабе 1:1 и размещают их цепочкой вплотную друг за другом, либо на расстоянии до 7 мм друг от друга по 1-5 МРИ в носителе, носители с МРИ равномерно размещают в ЛУО параллельно друг другу на расстоянии 3-10 мм; проводят контрольную КТ модели орбиты и получают серии сканов во фронтальной и сагиттальной плоскостях с изображениями структур орбиты и МРИ; с помощью программы для планирования брахитерапии Permanent Seed проводят графическое обозначение контуров структур орбиты и облучаемого объема тканей орбиты, включающее ЛУО и 3 мм окружающих тканей орбиты, и выполняют расчет доз ионизирующего излучения. Способ позволяет уменьшить дозные нагрузки на здоровые ткани орбиты и снизить риск лучевых осложнений. 3 ил., 1 пр.
Способ моделирования постоперационной брахитерапии опухолей орбиты, заключающийся в том, что создают модель орбиты человека в масштабе 1:1, содержащую рентгеноконтрастные модели структур орбиты, включающие глазное яблоко, зрительный нерв, прямые мышцы, ложе удаленной опухоли (ЛУО), и заполняют тканеэквивалентным материалом; выполняют компьютерную томографию (КТ) модели орбиты, получают серии сканов во фронтальной и сагиттальной плоскостях с изображениями структур модели орбиты; на передней поверхности модели орбиты маркируют квадрант локализации модели ЛУО; создают макеты радиоактивных источников (МРИ) йод-125 в масштабе 1:1 и размещают их в носителе цепочкой вплотную друг за другом, либо на расстоянии до 7 мм друг от друга по 1-5 МРИ, который представляет собой полую гибкую полимерную трубочку диаметром, соответствующим диаметру МРИ; носители с МРИ равномерно размещают в ЛУО параллельно друг от другу на расстоянии 3-10 мм; проводят контрольную КТ модели орбиты и получают серии сканов во фронтальной и сагиттальной плоскостях с изображениями структур орбиты и МРИ; с помощью программы для планирования брахитерапии Permanent Seed Implant Dosimetry проводят графическое обозначение контуров структур орбиты и облучаемого объема тканей орбиты, включающее ЛУО и 3 мм окружающих тканей орбиты, и выполняют расчет доз ионизирующего излучения на структуры модели орбиты, подбирают параметры облучения, при которых распределение дозных нагрузок будет соответствовать максимуму в облучаемом объеме тканей орбиты и минимуму на структуры орбиты.
| СПОСОБ ЛЕЧЕНИЯ ВНУТРИГЛАЗНЫХ ОПУХОЛЕЙ | 2005 |
|
RU2295944C1 |
| СПОСОБ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ЗЛОКАЧЕСТВЕННЫХ ЛИМФОМ КОНЪЮНКТИВЫ С ПОМОЩЬЮ БЕТА-АППЛИКАЦИОННОЙ ТЕРАПИИ | 2000 |
|
RU2164161C1 |
| Бровкина А.Ф., Зарубей Г.Д | |||
| Об эффективности брахитерапии при увеальных меланомах | |||
| - Офтальмологический журнал, 1993, №1, с.1-4 | |||
| МЕЕРОВИЧ Г.А | |||
| и др | |||
| Лазерно-спектроскопический комплекс для флуоресцентной диагностики и фотодинамической терапии заболеваний сетчатой и сосудистой оболочек глаза | |||
| - Квантовая электроника, 2002, №11, с.959-962. | |||
Авторы
Даты
2012-12-27—Публикация
2011-11-16—Подача