Изобретение относится к области медицинской радиологии и предназначено для проведения дистанционной фотонной терапии новообразований органа зрения и его придатков.
Известны способы терапии опухолей глаза и его придатков с помощью облучения бета-частицами, при этом источниками излучения являются глазные аппликаторы на мягкой и жесткой основах с использованием радионуклидов с прометием-147, таллием-204, фосфором-32 и некоторыми другими.
Наиболее подходящим является офтальмоаппликатор с радионуклидом 90Sr + 90Y. Офтальмоаппликаторы для лучевой терапии представляют собой устройства сложной формы (по ферме и размеру глазного яблока), размещаемые на наружной поверхности глаза, т.е. контактно (см. фиг. 1).
Существует и дистанционный способ облучения в офтальмологии с использованием бета-излучения выше указанных радионуклидов. Дистанционная бета-терапия осуществляется с помощью аппарата типа АБЕТ-1 с набором цилиндрических коллиматоров из алюминия, железа и меди различных диаметров.
Применение данных способов терапии новообразований органа зрения и его придатков ограничено по следующим причинам: максимальная энегия бета-излучения используемых радионуклидов составляет Eβмакс = 0,225-2,3 МэВ, при этом максимальный пробег бета-частиц в мягкой биологической ткани равен 0,5-11 мм, слой половинного ослабления Δ1/2 = 0,15-1,8 мм соответственно и, следовательно, интенсивно облучаются ткани до глубины 5 мм; подвергаются лучевой нагрузке критический орган глаза - хрусталик, роговица и окружающие новообразование здоровые ткани; кроме того, контакт бета-аппликаторов (как инородных тел) с глазным яблоком и другими тканями органа зрения не желателен с клинической точки зрения.
Однако в офтальмологии необходима лучевая терапия внутриглазных новообразований и опухолей орбиты глаза, залегающих на глубинах от 10 до 40 мм от переднего отдела глазного яблока.
Для этого возможно применение фотонного излучения (гамма и рентгеновского) четко определенной энергии, Для терапии новообразований, залегающих на глубине 10-25 мм, оптимальным является использование фотонного излучения с энергией 25-40 кэВ, а для опухолей орбиты глаза на глубине 25-40 мм - с энергией 50-100 кэВ соответственно.
Выбор такого диапазона оптимальных энергий фотонного излучения соответствует нескольким физическим критериям, основным из которых является слой половинного ослабления (Δ1/2) фотонного излучения в мягкой биологической ткани (Н2О).
В мягкой биологической ткани Δ1/2 для энергии Е = 25-40 кэВ соответствует 14-18 мм, а для Е = 50-100 кэВ равен 30-40 мм. Кроме того, необходимо сконцентрировать пучок фотонного излучения в центр новообразования таким образом, чтобы мощность дозного поля составила 100-90% максимальной мощности дозы испускаемого фотонного излучения при минимальной лучевой нагрузке на роговицу глаза, критический орган - хрусталик и подлежащие здоровые ткани.
В настоящее время дистанционная лучевая терапия новообразований глаза и его придатков, залегающих на глубине 10-40 мм от переднего отдела глазного яблока, в офтальмоонкологии не проводится.
Решением, наиболее близким к предлагаемому способу, является дистанционная гамма-терапия злокачественных опухолей спинного мозга путем его облучения пучком гамма-излучения через два поля, при которой для уменьшения объема облучаемых здоровых тканей облучение проводят через позитивную сфокусированную вольфрамовую решетку с полей, расположенных на расстоянии 0,5-1,0 см под углом 20-30о к вертикали. Недостатком известного способа является использование фотонного излучения с энергиями более 150 кэВ, при которых невозможно формирование дозного поля фотонного излучения с определенными характерными размерами для терапии новообразований органа зрения и его придатков без травмирования тканей глаза.
Целью изобретения является уменьшение лучевой нагрузки на здоровые ткани при облучении опухолей.
Способ лучевой терапии в офтальмоонкологии состоит в следующем. Для дистанционной терапии опухолей заднего отдела глазного яблока с толщиной 3-5 мм и длиной 5-10 мм, залегающих на глубине 10-25 мм от переднего отдела глаза, которые наблюдают в клинической офтальмоонкологической практике, используют коллимирова- нное (F = 30 мм) фотонное излучение, например, радионуклида 125I с энергией  =28.4 (2) кэВ(2) кэВ, Σ Iγ+kx≃ 148 %. Учитывая эти исходные данные, коллиматор с помощью геометрических размеров каналов и их ориентации формирует дозное поле (100± 10)% с характерными размерами - диаметр пятна в сагиттальном сечении фокальной плоскости равен 3 мм, а во фронтальном сечении по оси коллиматора в фокусе образуемое дозное поле составляет 6 мм. В пределах этих размеров дозное поле считается равномерным и составляет 100-90% максимальной мощности дозы испускаемого фотонного излучения.
=28.4 (2) кэВ(2) кэВ, Σ Iγ+kx≃ 148 %. Учитывая эти исходные данные, коллиматор с помощью геометрических размеров каналов и их ориентации формирует дозное поле (100± 10)% с характерными размерами - диаметр пятна в сагиттальном сечении фокальной плоскости равен 3 мм, а во фронтальном сечении по оси коллиматора в фокусе образуемое дозное поле составляет 6 мм. В пределах этих размеров дозное поле считается равномерным и составляет 100-90% максимальной мощности дозы испускаемого фотонного излучения.
Для дистанционной терапии новообразований орбиты глаза с толщиной 3-5 и длиной 10-20 мм, залегающих на глубине 25-40 мм от переднего отдела глаза, которые наблюдают в клинической офтальмологической практике, используют коллимирован- ное F= 40 мм фотонное излучение, например, радионуклида 169Yb с энергиями  = 92.8 (8) кэВ (8) кэВ, Σ Iγ+kx≃ 328 %. Учитывая эти исходные данные, коллиматор с помощью геометрических размеров каналов и их ориентации формирует дозное поле (100 ± 10)% с характерными размерами - диаметр пятна в сагиттальном сечении фокальной плоскости 2 мм, а во фронтальном сечении по оси коллиматора в фокусе высотой 10 мм соответственно.
= 92.8 (8) кэВ (8) кэВ, Σ Iγ+kx≃ 328 %. Учитывая эти исходные данные, коллиматор с помощью геометрических размеров каналов и их ориентации формирует дозное поле (100 ± 10)% с характерными размерами - диаметр пятна в сагиттальном сечении фокальной плоскости 2 мм, а во фронтальном сечении по оси коллиматора в фокусе высотой 10 мм соответственно.
На фиг. 1 показана схема облучения внутриглазной опухоли бета-аппликатором с радионуклидом 90Sr + 90Y. Доза в контакте с передним отделом глазного яблока принята за 100%. На фиг. 1 даны следующие обозначения: 1 - бета-аппликатор, 2 - опухоль, 3 - хрусталик, 4 - глазное яблоко, 5 - зрительный нерв.
На фиг. 2 и 3 показана схема облучения опухолей внутриглазной и орбиты соответственно с помощью коллимированного фотонного излучения, где даны следующие обозначения: 1 - пучок излучения, 2 - источник фотонного излучения (125I, 57Со), 3а - девятиканальный коллиматор, 3б - 32-канальный коллиматор, 4 - хрусталик, 5 - глазное яблоко, 6 - орбита глаза, 7а - внутриглазная опухоль, 7б - опухоль орбиты глаза, 8 - зрительный нерв, 9 - мягкая ткань. Доза в центре опухоли принята за 100%.
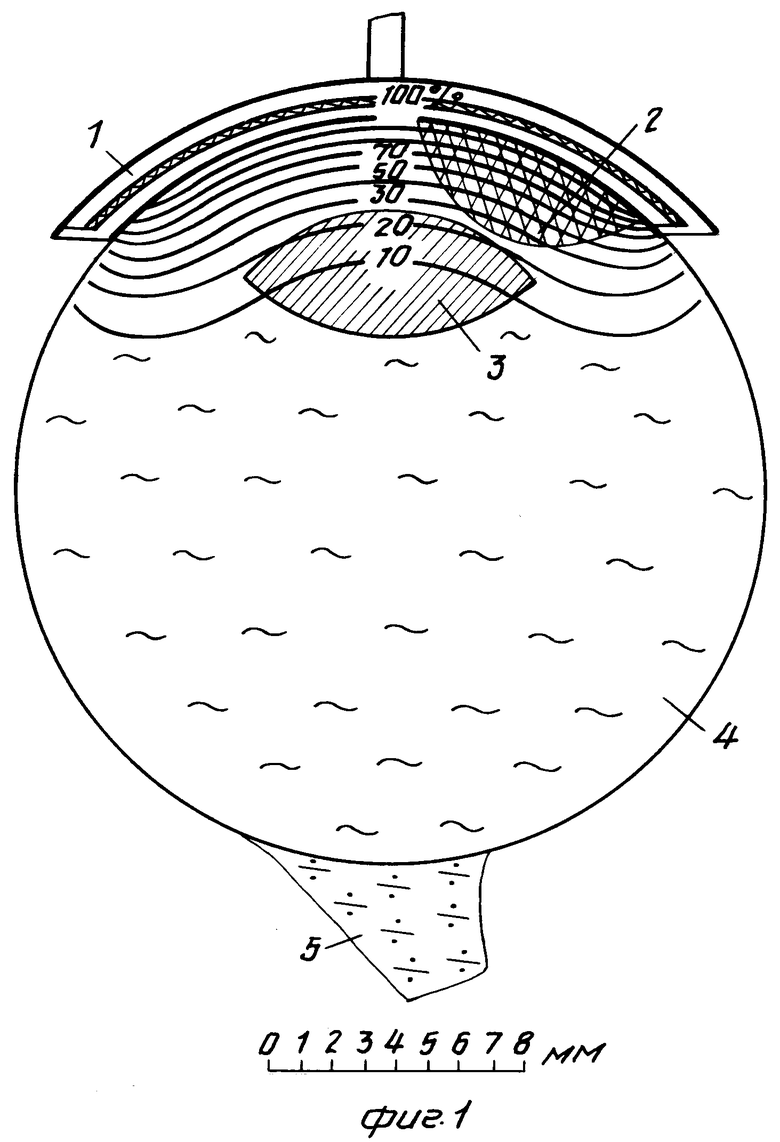
П р и м е р 1. На фиг. 2 представлено полученное экспериментально на фантоме схематическое изображение облучения внутриглазной опухоли толщиной 4 мм, длиной 8 мм, расположенной в заднем отделе глазного яблока на глубине 27 мм. В качестве источника фотонного излучения использовали радионуклид 125I с 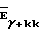 =28.4 (2) кэВ (2) кэВ, Σ Iγ+kx≃ 148 %.
=28.4 (2) кэВ (2) кэВ, Σ Iγ+kx≃ 148 %.
Как видно на фиг. 2, 9-канальным фокусирующим коллиматором с F = 30 мм 100-90% дозное поле формируется на расстоянии 27 мм, а 30% и 20% дозное поле - на расстоянии 6 мм и 9 мм от торца коллиматора соответственно. За счет выбора энергии фотонного излучения радионуклида 125I и соответствующей коллимации его глубже 27 мм в биологической ткани дозное поле составляет 20% на расстоянии 36 мм и благодаря своей конфигурации практически не создает лучевой нагрузки на критический орган зрения - хрусталик, роговицу, большую часть окружающих опухоль тканей и зрительный нерв.
П р и м е р 2. На фиг. 3 представлено полученное экспериментально на фантоме схематическое изображение облучения опухоли орбиты глаза толщиной 3 мм и длиной 15 мм, расположенной на внутренней стороне орбиты на глубине 38 мм. В качестве источника фотонного излучения использовали радионуклид 169Yb с  =92.8 (8) кэВ, Σ Iγ+kx≃ 328 % .
=92.8 (8) кэВ, Σ Iγ+kx≃ 328 % .
Как видно на фиг. 3, 32-канальным фокусирующим коллиматором с F = 40 мм 100-90% дозное поле формируется на расстоянии 38 мм, а дозное поле 30% и 20% на расстоянии 7 мм и 12 мм от торца коллиматора соответственно.
За счет выбора энергии фотонного излучения радионуклида 169Yb и соответствующей коллимации его глубже 38 мм в биологической ткани дозное поле составляет 20% на расстоянии 50 мм и благодаря своей конфигурации практически не создает лучевой нагрузки на хрусталик, роговицу и большую часть окружающих опухоль тканей и зрительный нерв.
На фиг. 1 для сравнения с заявленным способом, представлено схематическое изображение лучевой терапии внутриглазной опухоли толщиной 3 мм и протяженностью 8 мм, расположенной в переднем отделе глазного яблока на глубине 3 мм, с помощью бета-аппликатора 90Sr + 90Y 90Sr + 90Y  = 928 (1) кэВ (1) кэВ и Eβмакс = 2274 кэВ.
= 928 (1) кэВ (1) кэВ и Eβмакс = 2274 кэВ.
Из рисунка видно, что 100% дозное поле, создаваемое бета-частицами, формируется в контакте с передним отделом глазного яблока, а 10% дозное поле на глубине 5 мм. Из-за своей конфигурации дозное поле создает лучевую нагрузку, как на опухоль, так и на роговицу, частично (30%-5%) на критический орган глаза - хрусталик, а также на большую часть окружающих опухоль тканей до глубины 11 мм.
Сравнивая изображенные на фиг. 1 и фиг. 2-3 способы лучевой терапии опухолей в офтальмологии, можно сделать следующий вывод.
С помощью заявленного способа дистанционной фотонной терапии возможно эффективно проводить терапию внутриглазных опухолей, расположенных на расстоянии 10-25 мм, и опухолей орбиты, залегающих на глубинах 25-40 мм от переднего отдела глазного яблока. Кроме того, возможна и эффективная терапия внутриглазных опухолей, располо- женных в переднем отделе глазного яблока 1-10 мм.
За счет выбора источника энергии фотонного излучения и соответствующей коллимации излучения создается такая конфигурация дозного поля, которая значительно уменьшает лучевую нагрузку на роговицу, критический орган глаза - хрусталик и окружающие новообразование здоровые ткани, по сравнению со способами бета-лучевой терапии, применяемыми в офтальмоонкологии.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ЗЛОКАЧЕСТВЕННЫХ ЛИМФОМ КОНЪЮНКТИВЫ С ПОМОЩЬЮ БЕТА-АППЛИКАЦИОННОЙ ТЕРАПИИ | 2000 |
|
RU2164161C1 |
| СПОСОБ ЛЕЧЕНИЯ ЛИМФОМ ОРГАНА ЗРЕНИЯ | 2013 |
|
RU2514638C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ПОСТОПЕРАЦИОННОЙ БРАХИТЕРАПИИ ОПУХОЛЕЙ ОРБИТЫ | 2011 |
|
RU2470615C1 |
| Способ проведения анестезии перед лучевой дистанционной терапией внутриглазных новообразований | 2023 |
|
RU2811663C1 |
| МНОГОФУНКЦИОНАЛЬНЫЙ КОМПЛЕКС ДЛЯ ДИАГНОСТИКИ, ДИСТАНЦИОННОЙ СТЕРЕОТАКСИЧЕСКОЙ РАДИОХИРУРГИИ И РАДИОТЕРАПИИ | 2019 |
|
RU2712303C1 |
| СПОСОБ КОМБИНИРОВАННОГО ОРГАНОСОХРАНЯЮЩЕГО ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ ОРБИТЫ | 2005 |
|
RU2286187C1 |
| Способ лечения злокачественных новообразований кожи век и конъюнктивы | 1987 |
|
SU1556673A1 |
| СПОСОБ СОЧЕТАННОЙ ФОТОННО-НЕЙТРОННОЙ ТЕРАПИИ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ | 2009 |
|
RU2428227C2 |
| Способ протонной лучевой терапии внутриглазных злокачественных новообразований | 2015 |
|
RU2680208C2 |
| СПОСОБ ОРГАНОСОХРАНЯЮЩЕГО ЛЕЧЕНИЯ ВНУТРИГЛАЗНЫХ ОПУХОЛЕЙ | 2010 |
|
RU2452444C1 |


Использование: в области медицинской радиологии и предназначено для проведения дистанционной фотонной терапии новообразований органа зрения и его придатков. Сущность изобретения: способ лучевой терапии глазных опухолей, включающий дистанционное сфокусированное фотонное облучение на глубине 10 - 40 мм, облучение осуществляют радионуклидами, испускающими фотонное излучение с энергией 20 - 100 кэВ через многоканальные коллиматоры с фокусным расстоянием 25 - 45 мм. При облучении очага поражения заднего отдела глазного яблока на глубине 10 - 25 мм формируют однородное дозное поле радионуклидами, испускающими фотонное излучение с энергией 25 - 40 кэВ через многоканальный фокусирующий коллиматор с фокусным расстоянием 25 - 30 мм. При облучении очага поражения орбиты глаза на глубине 25 - 40 мм формируют однородное дозное поле радионуклидами, испускающими фотонное излучение с энергией 50 - 100 кэВ через многоканальный фокусирующий коллиматор с фокусным расстоянием 40 - 45 мм. 2 з.п.ф-лы, 3 ил.
| Способ дистанционной гамма-терапии злокачественных опухолей спинного мозга | 1974 |
|
SU495859A1 |
| Устройство для сортировки каменного угля | 1921 |
|
SU61A1 |
Авторы
Даты
1994-10-30—Публикация
1990-03-30—Подача