Изобретение относится к области медицины и биологии, в частности к исследованиям веществ, модифицирующих апоптоз у населения, проживающего в районах экологического неблагополучия, и может быть использовано для диагностики токсического действия органических низкомолекулярных соединений на иммунную систему для тестирования ранних нарушений состояния здоровья как в скрининговых, так и мониторинговых исследованиях.
Для понимания сути вопроса, следует пояснить следующее. Постоянное многокомпонентное воздействие техногенных химических факторов в промышленно развитых регионах оказывает негативное влияние на здоровье населения. Ряд известных исследований посвящены изучению влияния антропогенной нагрузки на здоровье работающих на производстве людей. Однако несомненный интерес также представляет изучение состояния иммунной системы у людей, постоянно проживающих в непосредственной близости к источникам выбросов и сбросов промышленных отходов.
Апоптоз - генетическая запрограммированная форма клеточной гибели, определяемая на основе характерных морфологических изменений умирающих клеток. Данный процесс является одним из ключевых процессов, определяющих формирование антигенспецифической составляющей иммунной системы и в значительной степени реализацию ее эффекторных функций. Однако известны патологические состояния, при которых механизм запрограммированной клеточной гибели оказывается заблокированным либо активированным, что приводит либо к неконтролируемой клеточной пролиферации, не сдерживаемой конкурирующим процессом апоптоза, либо к ускоренной клеточной гибели и снижению их иммунокомпетентности. При этом экотоксиканты химического производства, в частности органические низкомолекулярные соединения, способны нарушать регуляторные функции иммунной системы, что может способствовать снижению адаптационных возможностей организма, возникновению онкологических, аутоиммунных и иммунодефицитных состояний. Этим и обусловлена потребность в получении количественной оценки апоптоза, модифицированного органическими низкомолекулярными соединениями.
Из уровня техники известен ряд способов, при реализации которых оценивают апоптоз у биологических объектов, а именно:
- «Способ определения тяжести заболевания и эффективности лечения у больных бронхолегочными заболеваниями (заявка на изобретение №2009101693, от 2009 г.). Согласно указанному известному решению производят отбор исследуемого материала, выделение из него клеточной субстанции, подготовку ее к исследованию, определение величины альтерации клеток путем оценки их апоптоза, при этом в качестве исследуемого материала используют индуцированную мокроту больного и здорового человека, в клеточной субстанции дополнительно определяют величину альтерации клеток путем некроза, при этом показатели апоптоза и некроза определяют при двух и более обследованиях с интервалом в 1-3 суток, полученные показатели выражают в виде апоптотического индекса (АИ) и индекса некроза (ИН), рассчитывают индекс альтерации клеток (ИАК) по формуле: ИАК=ИН/АИ, где ИН - индекс некроза; АИ - апоптотический индекс; при этом тяжесть заболевания определяют путем сравнения показателя индекса альтерации клеток больного с показателем индекса альтерации клеток здоровых лиц, и диагностируют легкое течение бронхолегочного заболевания при показателях ИАК более 1,5, среднее до 1,0 и тяжелое менее 1,0, а эффективность лечения определяют путем сравнения начальных показателей индекса альтерации клеток больного с показателем индекса альтерации после лечения и диагностируют положительную динамику лечения при увеличении ИАК до значений для здоровых лиц 2,0.
Предлагаемый способ отличается от указанного известного тем, что оценивается не степень тяжести патологии, а идентифицируется этиологический фактор (химический), инициирующий процесс апоптоза, а также степень вызываемых исключительно этим фактором отклонений по данному критерию. Кроме того, в качестве показателя гибели используется критерий только апоптоз (некроз, как в известном способе, не учитывается), что позволяет анализировать ранние нарушения состояния запрограммированного процесса клеточной гибели.
- «Функциональный иммуноанализ in vitro» (патент РФ №2416797 от 2005), согласно которому производят выделение клеток, первичную инкубацию из крови, сыворотки или плазмы пациента клеток с исследуемым веществом, получение супернатанта или смеси из клеток и супернатанта первичной инкубации, вторичную инкубацию клеток-мишеней с супернатантом или смесью из клеток и супернатанта и анализ клеток-мишеней. При этом в случае выделенных клеток речь идет о первичной инкубации эффекторных клеток иммунной системы. В случае клеток-мишеней вторичной инкубации речь идет о клетках человека или клетках высших млекопитающих. Указанный способ принимается за наиболее близкий аналог - прототип.
Предлагаемый способ повторяет два первых этапа известного способа, однако отличается тем, что преследует цель определить уровень опасности уже имеющейся экспозиции вещества по критерию апоптоза для дальнейшего ограничения поступления и форсированной элиминации. В известном же способе вещество используется как лекарственное преиммобилизационное средство, измененные клетки и супернатант после экспозиции которого будут применяться для апоптоза опухолевых клеток.
Технический результат, достигаемый предлагаемым изобретением, заключается в обеспечении высокой точности количественной оценки апоптоза, модифицированного органическими низкомолекулярными соединениями, с обеспечением возможности в последующем судить об иммунодефицитных состояниях населения.
Указанный технический результат достигается предлагаемым способом количественной оценки апоптоза, модифицированного органическими низкомолекулярными соединениями, включающим отбор пробы крови у пациента, выделение из пробы мононуклеарных клеток и инкубацию клеток с исследуемым соединением, при этом, согласно изобретению, выделение из пробы мононуклеарных клеток производят путем введения в пробу этилендиаминтетраацетата, разведения ее водным раствором хлорида натрия, наслоения на 3 мл фиколла-урографина с градиентом плотности 1,077 г/мл, с последующим центрифугированием в течение 30 мин при 1500 об/мин и отбором мононуклеарных клеток, затем производят двукратный отмыв выделенных клеток раствором хлорида натрия и проводят ресуспендирование указанных клеток в рабочем растворе буфера для окрашивания 1X Annexin V Binding Buffer до концентрации 1×106 клеток/мл, при этом рабочий раствор буфера для окрашивания 1X Annexin V Binding Buffer представляет собой смесь концентрированного буфера для окрашивания 10Х Annexin V Binding Buffer с дистиллированной водой в объемном соотношении 1:9 соответственно, затем осуществляют инкубацию полученных клеток с исследуемым органическим низкомолекулярным соединением, получая опытный образец, и осуществляют инкубацию полученных клеток без добавления указанного соединения, получая контрольный образец, при этом инкубацию полученных клеток с исследуемым органическим низкомолекулярным соединением и без него проводят в течение 1 часа при температуре 37°С, после инкубации в опытный и контрольный образцы вводят реагенты аннексии V и йодид пропидия, образцы вновь инкубируют в темноте при комнатной температуре в течение 15 мин, добавляют рабочий раствор буфера для окрашивания 1X Annexin V Binding Buffer и осуществляют цитометрический анализ полученных образцов с определением содержания в них аннексина V, сравнивают численные величины содержания аннексина V в контрольном и опытном образцах и по соотношению большего числа содержания аннексина V к меньшему количественно оценивают апоптоз, модифицированный органическим низкомолекулярным соединением, причем при указанном соотношении, равном 1,5 и более, судят об апоптозе - критическом состоянии запрограммированной клеточной гибели в связи с влиянием указанного органического соединения.
В качестве водного раствора хлорида натрия используют раствор с концентрацией 9 г/л и рН 7,2.
При наслоении на 3 мл градиента плотности фиколла-урографина концентрация фиколла составляет 9 об.%, а плотность градиента - 1,077 г/мл.
Указанный технический результат достигается за счет следующего.
Благодаря тому что выделение из пробы мононуклеарных клеток производят путем введения в пробу этилендиаминтетраацетата (ЭДТА), разведения ее водным раствором хлорида натрия, наслоения на 3 мл фиколла-урографина с градиентом плотности 1,077 г/мл с последующим центрифугированием в течение 30 мин при 1500 об/мин, обеспечиваются оптимальные условия для получения чистой культуры специфических клеток (мононуклеаров).
Осуществление двукратного отмыва выделенных клеток раствором хлорида натрия необходимо для максимального освобождения культуры мононуклеаров от тканевых «примесей».
Последующее их ресуспендирование в рабочем растворе буфера для окрашивания 1X Annexin V Binding Buffer до концентрации 1×106 клеток/мл обеспечивает необходимый количественный стандарт мононуклеаров. Использование при этой операции рабочего раствора буфера для окрашивания 1X Annexin V Binding Buffer, представляющего смесь концентрированного буфера для окрашивания 10Х Annexin V Binding Buffer с дистиллированной водой в объемном соотношении 1:9 соответственно, необходимо для подготовки смеси мононуклеаров к дальнейшему внесению красителей (аннексина V и йодида пропидия).
Проведение цитометрического анализа после добавления в образцы реагентов аннексина V и йодида пропидия является традиционным.
Однако как показали наши исследования, точность предлагаемого способа в установлении факта критического состояния запрограммированной клеточной гибели в связи с воздействием на организм человека низкомолекулярного органического соединения обеспечивается и тем, что экспериментально установлен соответствующий этому состоянию конкретный численный показатель 1,5 и более через соотношение большего числа содержания аннексина V к меньшему числу его содержания в контрольном или опытном образцах. Благодаря этому в дальнейшем можно говорить либо о формировании иммунодефицитного состояния (если содержание аннексина V в опытном образце превосходит его содержание в контрольном образце), либо о старении клетки (если содержание аннексина V в контрольном образце превосходит его содержание в опытном образце).
По указанному установленному предлагаемым способом показателю в дальнейшем можно судить о нарушении состояния здоровья, связанном с воздействием анализируемого низкомолекулярного органического соединения, при одновременном обнаружении этого соединения в пробе крови в концентрации, превышающей референтную.
Предлагаемый способ реализуется следующим образом.
В процессе испытаний была исследована кровь у 12 пациентов. Исследования проводили следующим образом. Для исследования кровь с ЭДТА разводили в два раза раствором хлорида натрия (9 г/л, рН 7,2), наслаивали на 3 мл градиента плотности фиколла-урографина (концентрация фиколла составляла 9%, плотность градиента - 1,077 г/мл) и центрифугировали 30 мин при 1500 об/мин.
Образовавшееся в интерфазе «кольцо» мононуклеарных клеток отбирали пипеткой, полученную клеточную взвесь дважды отмывали раствором хлорида натрия (9 г/л, рН 7,2).
Полученную взвесь мононуклеаров ресуспендировали в рабочем растворе буфера для окрашивания (1X Annexin V Binding Buffer) до концентрации 1×106 клеток/мл. Причем рабочий раствор буфера для окрашивания 1X Annexin V Binding Buffer представлял собой смесь концентрированного буфера для окрашивания 10Х Annexin V Binding Buffer (компонент No. 51-66121E из набора Cat. No. 556570, производство фирмы Бектон Дикинсон) с дистиллированной водой в объемном соотношении 1:9. В состав концентрированного буфера для окрашивания 10Х Annexin V Binding Buffer входила смесь солей: хлорида натрия, хлорида кальция, Hepes/NaOH, с рН=7,4.
В процессе конкретных исследований на этих 12 пациентах оценивали влияние хлороформа (это вещество относится к органическому низкомолекулярному соединению) на включение клеток в апоптоз. Для этого 100 мкл суспензии ранее подготовленных мононуклеарных клеток (1×106 клеток/мл) инкубировали с референтной концентрацией хлороформа (0,017 мкг/см3) в течение 1 часа при 37°С. Хлороформ доводили до нужной концентрации путем разведения в отмывочном растворе в соотношении 20 мкл хлороформа к 10 мл раствора хлорида натрия (9 г/л, рН 7,2). В качестве контроля 100 мкл мононуклеарных клеток без добавления хлороформа инкубировалось при таких же условиях.
После инкубации переносили 100 мкл клеточной суспензии в пробирку емкостью 5 мл, добавляли 5 мкл Annexin V-FITC и 5 мкл Propidium Iodide (PI). После этого содержимое пробирки аккуратно перемешивали и инкубировали 15 мин при комнатной температуре в темноте. Далее в каждую пробирку добавляли 400 мкл рабочего раствора буфера для окрашивания 1X Annexin V Binding Buffer. Анализировали на проточном цитометре в течение часа после окрашивания. Таким образом, для каждого пациента анализировалось 2 пробы - опытная (с добавлением референтной дозы хлороформа) и контрольная (без нее).
Цитометрический анализ мононуклеарных клеток проводили на проточном цитофлуориметре FACSCalibur фирмы «Becton Dickinson» с использованием универсальной программы CellQuest.PrO. Накопление производили до 10000 событий в лимфоцитарной области. Для настройки режимов компенсации и установки границ квадрантов использовали следующие контроли: неокрашенные клетки, клетки, окрашенные только Annexin V-FITC (без PI), клетки, окрашенные только Propidium Iodide (без Annexin V-FITC).
В образце оценивали показатели прямого (FSC) и бокового (SSC) светорассеяния клеток, интенсивность флуоресценции Annexin V-FITC (FL1) и Propidium Iodide (FL3). После исключения дебриса (по показателям прямого и бокового светорассеяния) и выделения лимфоцитарного гейта определяли количество Annexin+- и Рi+-клеток в режиме DotPlot (двумерная гистограмма). Количество апоптотических Annexin+-клеток определяли в нижнем правом квадранте, клетки в позднем апоптозе (Annexin+PI+-клетки) оценивали в верхнем правом квадранте гистограммы. Данные, полученные в ходе испытаний, приведены в таблице.
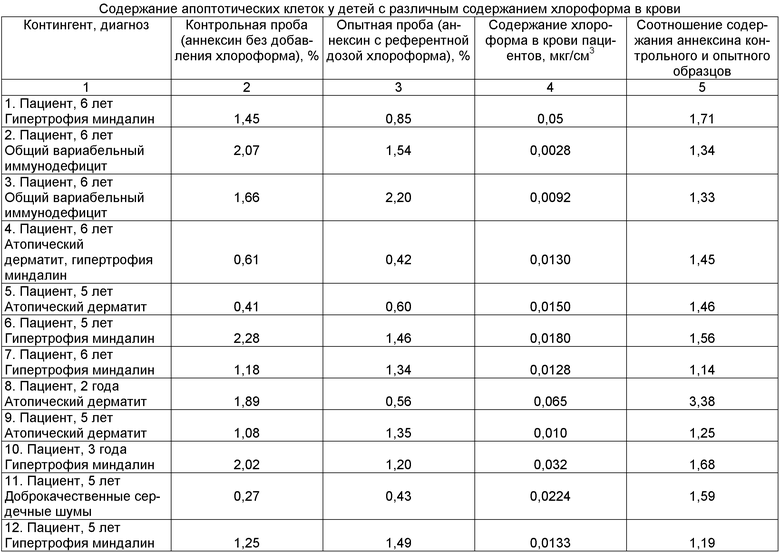
Данные, приведенные в таблице, показывают, что добавление референтной концентрации хлороформа в взвесь мононуклеаров модифицирует апоптоз (графа 3). Причем степень отклонения показателя, фиксируемая по величине соотношения содержания аннексина в контрольных и опытных образцах (графа 5), зависит от базового уровня содержания органического соединения в крови пациента (графа 4). Чем выше концентрация хлороформа в крови, тем больше соотношение содержания аннексина контрольной и опытной проб. Так, пациенты под номерами 1, 6, 8, 10 характеризуются снижением содержания аннексина после инкубации с референтной концентрацией хлороформа более чем в 1,5 раза по отношению к контрольной пробе. При этом базовое содержание хлороформа в крови у данных пациентов превышало референтную концентрацию. Пациент под номером 11 характеризуется повышением содержания аннексина после инкубации с референтной концентрацией хлороформа более чем в 1,5 раза по отношению к контрольной пробе. При этом базовое содержание хлороформа в крови у данного пациента также превышало референтную концентрацию.
Подобные опыты были проведены с исследованием влияния фенола на апоптоз клеток. В качестве референтной концентрации фенола использовали концентрацию 0,05 мкг/см3. Результаты были аналогичны предыдущим исследованиям.
Ускорение аннексин-индуцированного апоптоза ведет к дефициту иммуноцитов, замедлению иммуноопосредованных реакций, снижению функционального резерва и клеточной компетенции специфических лимфоцитарных фенотипов.
Замедление аннексин-индуцированного апоптоза снижает готовность к клеточной гибели в условиях контаминантной нагрузки и может служить отправной точкой инициации иммунопролиферативных состояний и снижения компетенции иммунной системы, ведет к ускоренному старению и онкогенной преформированности клетки.
Нагрузка с референтной концентрацией органического токсиканта, в зависимости от исходного его содержания в крови, может приводить либо к ускорению (опыты 1, 6, 8 и 10), либо к замедлению (опыт 11) клеточной гибели. И тот, и другой процесс являются негативными и изменение относительного количества апоптотических клеток в 1,5 и более раз свидетельствует о критическом состоянии процесса запрограммированной клеточной гибели в связи с экспозицией конкретного техногенного химического фактора и сдвиге его за границы диапазона оптимума с формированием либо иммунодефицитного состояния, либо старения клетки.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ оценки у детей влияния стронция на апоптоз, ассоциированный с аллельными вариантами гена FAS | 2016 |
|
RU2621155C1 |
| Способ оценки влияния нитрозаминов на апоптоз у детей, проживающих в неблагоприятных условиях среды обитания | 2016 |
|
RU2626516C1 |
| СПОСОБ ДИАГНОСТИКИ НАРУШЕНИЙ КЛЕТОЧНОГО ИММУНИТЕТА У РАБОТНИКОВ ХИМИЧЕСКИХ ПРОИЗВОДСТВ ПРИ ВОЗДЕЙСТВИИ ФОРМАЛЬДЕГИДА | 2014 |
|
RU2539391C1 |
| Способ оценки влияния алюминия на иммунный статус | 2016 |
|
RU2629597C1 |
| СПОСОБ ОЦЕНКИ ВЛИЯНИЯ МЕТАНОЛА НА ИММУННЫЙ СТАТУС РАБОТНИКОВ ХИМИЧЕСКОГО ПРОИЗВОДСТВА | 2014 |
|
RU2546524C1 |
| СПОСОБ ОЦЕНКИ НАРУШЕНИЙ КЛЕТОЧНОГО ИММУНИТЕТА ПРИ ВОЗДЕЙСТВИИ ФЕНОЛА | 2013 |
|
RU2523418C1 |
| СПОСОБ ДИАГНОСТИКИ ВТОРИЧНЫХ ИММУНОДЕФИЦИТНЫХ СОСТОЯНИЙ ЧЕЛОВЕКА, СВЯЗАННЫХ С ХИМИЧЕСКИМ КОНТАМИНАНТОМ | 2011 |
|
RU2452963C1 |
| СПОСОБ ДИАГНОСТИКИ СНИЖЕНИЯ ПОСТВАКЦИНАЛЬНОГО ИММУНИТЕТА К КОКЛЮШУ У ДЕТЕЙ, ПРОЖИВАЮЩИХ В УСЛОВИЯХ ВОЗДЕЙСТВИЯ ВРЕДНЫХ ХИМИЧЕСКИХ ФАКТОРОВ СРЕДЫ ОБИТАНИЯ | 2013 |
|
RU2538676C1 |
| СПОСОБ ДИАГНОСТИКИ СНИЖЕНИЯ ПОСТВАКЦИНАЛЬНОГО ИММУНИТЕТА К ДИФТЕРИИ У ДЕТЕЙ, ПРОЖИВАЮЩИХ В УСЛОВИЯХ ВОЗДЕЙСТВИЯ ВРЕДНЫХ ХИМИЧЕСКИХ ФАКТОРОВ СРЕДЫ ОБИТАНИЯ | 2013 |
|
RU2524636C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ТОКСИЧНОСТИ ДЕЙСТВИЯ МАРГАНЦА НА ОРГАНИЗМ ДЕТЕЙ, ПРОЖИВАЮЩИХ В УСЛОВИЯХ ТЕХНОГЕННОЙ НАГРУЗКИ СРЕДЫ ОБИТАНИЯ | 2010 |
|
RU2437095C1 |
Изобретение относится к области медицины и описывает способ количественной оценки апоптоза, модифицированного органическими низкомолекулярными соединениями, включающий отбор пробы крови у пациента, выделение из пробы мононуклеарных клеток и инкубацию клеток с исследуемым соединением, где выделение из пробы мононуклеарных клеток производят путем введения в пробу этилендиаминтетраацетата, разведения ее водным раствором хлорида натрия, наслоения на 3 мл фиколла-урографина с градиентом плотности 1,077 г/мл, с последующим центрифугированием в течение 30 мин при 1500 об/мин и отбором мононуклеарных клеток, затем производят двукратный отмыв выделенных клеток раствором хлорида натрия и проводят ресуспендирование указанных клеток в рабочем растворе буфера для окрашивания 1X Annexin V Binding Buffer до концентрации 1×106 клеток/мл, при этом рабочий раствор буфера для окрашивания 1X Annexin V Binding Buffer представляет собой смесь концентрированного буфера для окрашивания 10Х Annexin V Binding Buffer с дистиллированной водой в объемном соотношении 1:9 соответственно, затем осуществляют инкубацию полученных клеток с исследуемым органическим низкомолекулярным соединением, получая опытный образец, и осуществляют инкубацию полученных клеток без добавления указанного соединения, получая контрольный образец, при этом инкубацию полученных клеток с исследуемым органическим низкомолекулярным соединением и без него проводят в течение 1 часа при температуре 37°С, после инкубации в опытный и контрольный образцы вводят реагенты аннексии V и йодид пропидия, образцы вновь инкубируют в темноте при комнатной температуре в течение 15 мин, добавляют рабочий раствор буфера для окрашивания 1X Annexin V Binding Buffer и осуществляют цитометрический анализ полученных образцов с определением содержания в них аннексина V, сравнивают численные величины содержания аннексина V в контрольном и опытном образцах и по соотношению большего числа содержания аннексина V к меньшему количественно оценивают апоптоз, модифицированный органическим низкомолекулярным соединением, причем при указанном соотношении, равном 1,5 и более, судят об апоптозе - критическом состоянии запрограммированной клеточной гибели в связи с влиянием указанного органического соединения. Способ обеспечивает высокую точность количественной оценки апоптоза, модифицированного органическими низкомолекулярными соединениями, с обеспечением возможности в последующем судить об иммунодефицитных состояниях населения. 2 з.п. ф-лы, 1 табл., 1 пр.
1. Способ количественной оценки апоптоза, модифицированного органическими низкомолекулярными соединениями, включающий отбор пробы крови у пациента, выделение из пробы мононуклеарных клеток и инкубацию клеток с исследуемым соединением, отличающийся тем, что выделение из пробы мононуклеарных клеток производят путем введения в пробу этилендиаминтетраацетата, разведения ее водным раствором хлорида натрия, наслоения на 3 мл фиколла-урографина с градиентом плотности 1,077 г/мл, с последующим центрифугированием в течение 30 мин при 1500 об/мин и отбором мононуклеарных клеток, затем производят двукратный отмыв выделенных клеток раствором хлорида натрия и проводят ресуспендирование указанных клеток в рабочем растворе буфера для окрашивания 1X Annexin V Binding Buffer до концентрации 1×106 клеток/мл, при этом рабочий раствор буфера для окрашивания 1X Annexin V Binding Buffer представляет собой смесь концентрированного буфера для окрашивания 10Х Annexin V Binding Buffer с дистиллированной водой в объемном соотношении 1:9 соответственно, затем осуществляют инкубацию полученных клеток с исследуемым органическим низкомолекулярным соединением, получая опытный образец, и осуществляют инкубацию полученных клеток без добавления указанного соединения, получая контрольный образец, при этом инкубацию полученных клеток с исследуемым органическим низкомолекулярным соединением и без него проводят в течение 1 ч при температуре 37°С, после инкубации в опытный и контрольный образцы вводят реагенты аннексии V и йодид пропидия, образцы вновь инкубируют в темноте при комнатной температуре в течение 15 мин, добавляют рабочий раствор буфера для окрашивания 1X Annexin V Binding Buffer и осуществляют цитометрический анализ полученных образцов с определением содержания в них аннексина V, сравнивают численные величины содержания аннексина V в контрольном и опытном образцах и по соотношению большего числа содержания аннексина V к меньшему количественно оценивают апоптоз, модифицированный органическим низкомолекулярным соединением, причем при указанном соотношении, равном 1,5 и более, судят об апоптозе - критическом состоянии запрограммированной клеточной гибели в связи с влиянием указанного органического соединения.
2. Способ по п.1, отличающийся тем, что в качестве водного раствора хлорида натрия используют раствор с концентрацией 9 г/л и рН 7,2.
3. Способ по п.1, отличающийся тем, что при наслоении на 3 мл градиента плотности фиколла-урографина концентрация фиколла составляет 9 об.%, а плотность градиента 1,077 г/мл.
| ФУНКЦИОНАЛЬНЫЙ ИММУНОАНАЛИЗ in vitro | 2006 |
|
RU2416797C2 |
| RU 2009101693 A, 27.07.2010 | |||
| KLEIN J.B | |||
| et al | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| ЩИТОВОЙ ДЛЯ ВОДОЕМОВ ЗАТВОР | 1922 |
|
SU2000A1 |
| DEROUET M | |||
| et al | |||
| Granulocyte macrophage colony-stimulating | |||
Авторы
Даты
2012-12-27—Публикация
2011-10-03—Подача