1. Медицинские и технические предпосылки
Многие заболевания не поражают весь организм, а затрагивают определенные виды тканей, зачастую до весьма ограниченных отдельных участков тканей или органов. Примерами тому являются опухолевые заболевания, заболевания суставов и сосудов, в частности солидные опухоли и заболевания артериальных сосудов.
Фармакотерапия таких заболеваний, как правило, заключается в пероральном или внутривенном введении лекарственных веществ, которые разносятся по всему организму и во многих случаях именно в результате нежелательных воздействий приводят к серьезным заболеваниям здоровых тканей и органов, что ограничивает их применение. Селективная терапия больных тканей происходит путем специфического связывания лекарственных веществ (например, антител) с больной тканью, при этом способ применения не меняется, или путем селективного введения, например, путем введения непосредственно в больную ткань, или путем доставки лекарственных веществ с помощью катетера в пораженные кровеносные сосуды. В случае селективного введения возникают проблемы, связанные, как правило, с коротким временем действия и инвазивными способами введения лекарственного вещества, поскольку любое повторное введение невозможно.
Проблемы фармакотерапии возникают из-за специфического способа введения и необходимости достижения существенного профилактического или терапевтического эффекта за одно применение. За последние 10 лет были достигнуты значительные успехи в лечении атеросклеротических изменений сосудов. Такие изменения часто носят локальный характер. Они являются причиной сужения или блокирования некоторых участков сосудов, что приводит к уменьшению или прекращению кровоснабжения нижележащих тканей, поражая в первую очередь сердце, кости, мозг, почки и хирургически измененные сосуды, такие как, например, диализные шунты. Такие сужения можно лечить путем чрескожного введения катетеров, которые благодаря небольшому диаметру можно вводить в пораженные кровеносные сосуды без нанесения больших повреждений. Как правило, в их дистальной части находится растягиваемый с помощью жидкости баллон, сложенный в виде складок вокруг стержня катетера. В сложенном состоянии этот баллон вводят в зауженное место кровеносного сосуда и там расширяют за короткий промежуток времени (секунды - несколько минут) таким образом, чтобы восстановился исходный просвет сосуда, и кровь снова могла проходить через суженный участок. Для того чтобы просвет сосуда оставался открытым, также можно ввести трубчатую металлическую сетку (опору для сосудов, стент), которая устанавливается либо в сложенном баллоне, либо высвобождается с помощью специального катетера в виде эластичного самораскрывающегося стента.
Хотя первоначальный процент успеха по увеличению просвета сосудов до размера, соответствующего примерно размеру до начала сужения, составлял около 90%, у многих пациентов через несколько месяцев после лечения происходило повторное сужение сосудов (рестеноз). Одной из наиболее важных причин является чрезмерная пролиферация клеток стенок сосудов, вызванная повреждением стенок при насильственном растяжении, в частности гладкой мускулатуры, которая не прекращается даже после заживления первоначального повреждения. Этот процесс можно полностью подавить, если покрыть стенты для коронарных артерий эффективным антипролиферативным лекарственным средством. Одним из требований является медленное высвобождение лекарственного средства из полимерного матрикса, т.е. высвобождение в течение нескольких дней или недель. Недостатком покрытия стента является замедление процесса заживления. При установке стента в случае если он находится в непосредственном контакте с кровью, может образоваться тромб. Тромбы могут приводить к внезапным и полным закупоркам сосудов, инфаркту и смерти. Такие опоры должны быстро и надолго врасти в эндотелиальный слой. Этому препятствует продолжительное высвобождение активного вещества, оказывающего ингибирующее влияние на размножение клеток.
Для периферических артерий отсутствуют какие-либо достоверные исследования, демонстрирующие эффективную профилактику рестеноза путем покрытия стентов лекарственными средствами. Однако, по-видимому, самораскрывающиеся нитиноловые стенты каким-то образом уменьшают процент рестеноза без необходимого покрытия их лекарственным средством (Schillinger M, Sabeti S, Loewe C et al. Balloon angioplasty versus implantation of nitinol stents in the superficial femoral artery. J N Engl J Med 2006; 30 354: 1879-88).
В патенте ЕР EP 1372737 A в основных чертах описано нанесение покрытия на баллоны. Такое активное вещество наносится, например, путем погружения баллона в раствор с активным веществом. В патенте WO 2004/028582 A описан вариант нанесения покрытия на баллоны на разных стадиях, а также на стадиях, предшествующих складыванию баллона.
Суженные артерии, часто связанные с массивным обызвествлением, могут быть снова расширены до своего первоначального просвета только с помощью повышенного давления (8-20 атм). Это достигается с помощью баллонов высокого давления, диаметр которых существенно не изменяется с увеличением внутреннего давления. Такие баллоны формируют под давлением жесткий цилиндр, который плотно прилегает к стенке сосуда, поскольку диаметр просвета сосуда до расширения баллона был меньше диаметра баллона. Нанесенное снаружи активное вещество прижимается к растянутой стенке сосуда соответствующим высоким давлением.
Также может возникнуть потребность в применении местной терапии лекарственными средствами без расширения просвета сосудов. Примером является лечение артерий после удаления материала бляшек механическим (например, с помощью катетера для атерэктомии) или тепловым (например, с помощью лазера) способом либо также лечение не приводящих к стенозу изменений стенок сосудов, препятствующих кровотоку (например, уязвимые бляшки, слоистые тромбы). В таких случаях нежелательно растяжение и повреждение сосудов. Выбирают обычный ангиопластический баллон с диаметром, который не приводит к какому-либо растяжению сосудов, мембрана такого баллона местами прилегает к неровной стенке сосуда и в эти места транспортирует лекарственное вещество.
2. Область техники, к которой относится изобретение
В WO 02/076509 A впервые было обнаружено, что контакт с пораженной стенкой сосудов в течение нескольких секунд является достаточным для подавления рестеноза, развивающегося в течение нескольких недель. Также описаны баллонные катетеры, покрытые лекарственным средством, активное вещество которого при контакте со стенкой сосуда высвобождается сразу в биодоступной форме.
В некоторых ранее и недавно опубликованных заявках на патент описан процесс нанесения лекарственных средств на баллонные катетеры, при этом, однако, всегда предпринималась попытка получения постоянного уровня активного вещества путем замедленного высвобождения несмотря на короткое время контакта ангиопластического баллона со стенкой сосуда. При таких способах нанесения покрытия все описанные изделия имеют существенные качественные недостатки и/или процесс их изготовления является трудоемким и дорогостоящим.
Липофильные, малорастворимые в воде, активные вещества являются более предпочтительными по сравнению с гидрофильными активными веществами, поскольку липофильные вещества с органическими летучими растворителями легко наносятся и, таким образом, во время применения и в крови легко преждевременно смываются с поверхности баллона, быстрее усваиваются клетками и дольше там остаются. В отдельных случаях для подавления рестеноза при гиперплазии неоинтимы на стентах применяются гидрофильные активные вещества, такие как метотрексат или триоксид арсения (US 20060348947; Yang W, Ge J, Liu H et al. Cardiovascular Research 2006;72:483-493). Активные вещества помещают в нерастворимый в воде полимер, из которого они медленно высвобождаются. Этот способ предотвращает преждевременную потерю активного вещества. Он также пригоден для применения гидрофильного цитостатического средства для антимикробного покрытия, наносимого на катетеры длительного использования и другие импланты (WO 03099346).
Фактически, только известные покрытия катетеров, описанные в WO 02/076509 A и WO 2004/028582 A, дают в результате эффективные изделия, которые уменьшают размер и частоту появления рестеноза после дилатации сосудов у больных (Scheller B, Hehrlein C, Bocksch W, Rutsch W, Haghi D, Dietz U, Böhm M, Speck U. Treatment of Coronary In-stent Restenosis with a Paclitaxel-coated Balloon Catheter. N Engl J Med 2006; 255: 2113-2124, Tepe G, Zeller T, Albrecht T, Heller S, Schwarzwälder U, Beregi J-P, Claussen CD, Oldenburg A, Scheller B, Speck U. Local - delivery of paclitaxel to inhibit restenosis during angioplasty of the leg. New Engl J Med 2008; 358:689-699).
Из документов предшествующего уровня техники известно множество активных веществ и матриксных веществ, пригодных для покрытия: указанные активные вещества предпочтительно представляют собой вещества, которые подавляют клеточную пролиферацию, имеют противовоспалительное и антикоагулирующее действие.
Среди адъювантов можно упомянуть следующие: контрастное вещество, матричное или гелеобразующее вспомогательное вещество, например липиды или применяемые в фармацевтике полимеры, гепарин, касторовое масло (WO 02/076509) или матриксное вещество массой 5000 дальтон, гидрофильные, красители, такие как, например, индоцианин зеленый, флуоресцин, метиленовый синий, сахар, производные сахара, низкомолекулярные ПЭГ (полиэтиленгликоли), соли органических и неорганических кислот, бензоаты, салицилаты (WO 2004/028582), полимеры, а также оболочки для лекарственных веществ (EP 0519063; US 5102402).
Также можно упомянуть полимеры, такие как сахара, желатин, ПЭГ, альбумин, хитозан, β-циклодекстрины, гидроксиэтиленцеллюлоза, а также липиды, амфифильные фосфолипиды и рентгеноконтрастные вещества, включая амфифильную йод-оксаминовую кислоту (DE 102004046244), вещества, которые повышают клеточную проницаемость, такие как линолевая кислота, линоленовая кислота, олеиновая кислота, стеариновая кислота, фенилсалицилат; антиоксиданты, такие как витамин Е, токотриенол, токоферол, а также нитрофенилоктиловый эфир, бис-этилгексил себакат, диизододецилфталат, N-метилпирролидон, бутилгидроксианизол, бутилгидрокситолуол, фосфорилхолин и полимеры (WO 2004/022124); масла, жирные кислоты, сложные эфиры жирных кислот, производные контрастных веществ, аминокислоты, пептиды, витамины, о-фосфосерин, нейтральные или заряженные амфифильные вещества, соли (WO 2007090385); амфифильные вещества, такие как сложные эфиры полиэтиленгликоля, сложные эфиры сахара и жирной кислоты, сложные эфиры полиглицерил-6 и жирной кислоты, сложные эфиры полиглицерил-10 и жирной кислоты, монопальмитат сахарозы, поверхностно-активные вещества с липидной основой, включенные в липидную мембрану, заряженные и незаряженные детергенты, вещества с более чем четырьмя гидроксил-, карбоксил- или аминогруппами, сложные эфиры жирной кислоты и сорбитана, вещества с фенольным кольцом, холат натрия, таурохолат натрия; также витамины и их производные, полиэтиленгликоль в виде добавки к суспензии, состоящей из органических кислот и частиц лекарственного вещества, соли, ангидриды, аминокислоты и пептиды, протеины, включая фибриноген, большое количество веществ с определенными функциональными свойствами и покрытия (US 2008/0118544). Только некоторые из указанных адъювантов являются действительно пригодными и часто только для определенных активных веществ и покрытий. Многие из указанных выше адъювантов воздействуют на клеточные мембраны, повреждая их (детергенты, амфифильные вещества), препятствуют быстрому внедрению активных веществ в клетки или являются нестабильными. Для специалиста в данной области техники является очевидным, какой адъювант является пригодным, в какой дозе и с каким активным веществом.
Подробно описаны способы замедленного высвобождения активного вещества. С другой стороны, мало внимания уделено способам нанесения покрытия на баллоны, хотя они являются очень важными с точки зрения требований, относящихся к получению воспроизводимого изготовления медицинского изделия и введению эффективной дозы в целевую ткань за несколько секунд - максимум несколько минут.
На сегодняшний день описаны следующие способы нанесения покрытия на баллоны.
В WO 92/11890 A описан способ применения микрокапсул в качестве переносчиков лекарственного вещества, которые гарантируют замедленное высвобождение активного вещества. Покрытие наносится методом распыления или погружения. Кроме описания углублений на мембране баллона отсутствуют какие-либо указания на то, каким образом в эти места на баллоне доставляется специфическое активное вещество так, чтобы оно прочно удерживалось во время введения баллона и в условиях быстро текущей крови и полностью высвобождалось при расширении баллона.
В описанном в WO 2004/006976 A способе активное вещество наносят путем погружения, абсорбции или распыления на шероховатую или структурированную поверхность баллона, причем баллон находится в расширенном состоянии. Гидрофильный слой, находящийся между мембраной баллона и липофильным лекарственным средством, облегчает отделение активного вещества.
В WO 00/21584 A описано нанесение на баллон нерастворимого в воде лекарственного вещества путем погружения, распыления или капельного нанесения с помощью пипетки. Баллон покрывают полимером, который содержит активное вещество. Высвобождение, длящееся от нескольких минут до нескольких часов, является неполным.
В WO 2007090385 с использованием различных примеров подробно описано требуемое размещение покрытия в продольных складках баллонного катетера. Композиции, содержащие активное вещество, доставляются в складки с помощью пипетки, шприца или путем распыления. При нанесении тонкого покрытия примеры демонстрируют высокий разброс дозировок.
В US 2003/064965 A заявлено быстрое высвобождение лекарственного средства из баллонного катетера, причем сами препараты гарантируют контролируемое (задержанное) высвобождение. С этой целью активные вещества применяются в капсулированном виде, например в виде липосом, коллоидов, микрочастиц, агрегатов или коагулятов. В качестве матрицы используется фибрин или гидрогель, а также глюкоза. Пористый слой должен защищать покрытие. В US 2006/002973 A описана мягкая защитная трубка, расположенная над покрытием. Препараты наносятся на мембрану баллона методом распыления, погружения, нанесения с помощью валика, щетки, нанесение с использованием растворителей или адгезивных веществ.
В нижеприведенных документах также раскрыты дополнительные способы нанесения покрытия: распыление в вакууме с использованием суспензии или эмульсии (DE 102004048265 A), использование жиров и масел (US 2004/224003 A, WO 2003/039612 A), применение веществ или условий, способствующих высвобождению лекарственного вещества (WO 96/39949 A), применение липофильных ингибиторов гидратации (WO 2005/089855 A), покрытие баллонов заранее установленными стентами (например, DE 102004046244 A; US 2005/0033417 A) и защита покрытых баллонов оболочками, которые легко удаляются перед расширением баллона.
В EP 1 372 737 A и WO 2004/028582 A раскрыты способы, в которых в том числе описано покрытие баллонных катетеров липофильными биосовместимыми активными веществами сразу после расширения баллона. Нанесение покрытия осуществляется методом погружения, намазывания, распыления или с помощью волюметрического устройства.
С точки зрения равномерности нанесения покрытия на поверхность в WO 2004/006976 A покрытие наносится на баллон в расширенном состоянии с учетом однородности открытой внешней поверхности, в WO 2001/052772 A во время нанесения покрытия на различные изделия используется вибрационное устройство.
До настоящего времени, за исключением покрытых баллонов, соответствующих описанным в EP 1372737 A и WO 2004/028582 A, не доказана эффективность описанных баллонных катетеров с точки зрения улучшения клинических результатов или также в экспериментах на животных с точки зрения достижения желаемых биологических и терапевтических целей. Способы покрытия описаны очень неопределенно, либо в результате описанных способов получаются изделия с существенными недостатками.
Несмотря на хорошую эффективность описанные в патентных документах EP 1372737 A и WO 2004/028582 A баллоны имеют недостатки, нежелательные для фармацевтических изделий. Многие активные вещества во всех вышеуказанных патентах можно вводить с помощью катетера, который покрывается соответствующим образом указанными способами, совсем не приводящими или приводящими к совершенно неудовлетворительному результату в месте воздействия, или, в любом случае, не раскрывается способ, согласно которому специалист может получить пригодное и соответствующее данному уровню техники изделие. Раскрытые на сегодняшний день способы нанесения лекарственных средств на баллонные катетеры являются, среди прочего, либо неудовлетворительными, либо недостаточно эффективными, поскольку лекарственные вещества распределяются неравномерно, очень прочно или слишком прочно прикрепляются к мембране баллона, быстро или медленно растворяются или содержат адъюванты, которые, со своей стороны, повреждают стенку сосуда или образуют ненужные комплексы, что приводит к недостаткам с точки зрения изготовления, воспроизводимости, стабильности и применения.
До сих пор не описаны баллонные катетеры для доставки активного вещества в стенки сосудов, которые бы при этом не растягивали и не повреждали стенки. Предпочтительны обычные ангиопластические баллоны с любым диаметром, которые не приводят к растяжению сосудов, прилегают мембраной к стенке сосудов только в тех местах, где она неравномерна, и только в эти места доставляют лекарственное вещество.
Определения
Медицинское изделие представляет собой изделие для лечения или профилактики заболеваний, при необходимости, подкрепленной фармакологически активным веществом.
Баллонный катетер представляет собой катетер с расширяемым дистальным сегментом
Мембраной баллона - мембраной или мембраной баллона называется наружная оболочка баллона катетера, которая соприкасается со стенкой сосуда; предпочтительными являются гладкие мембраны или мембраны, которые покрываются в сложенном состоянии; обычные баллонные катетеры имеют гладкие мембраны баллонов. Для придания мембранам баллонов некой структуры или шероховатости требуются особые процедуры при изготовлении.
Стент представляет собой трубчатую структуру для установки в полостях или тканях (опору для сосудов).
Активное вещество представляет собой биологическое или эффективное вещество; предпочтительными являются лекарственные вещества, т.е. одобренные лекарственные средства, содержащие активные вещества.
Адъювант представляет собой вещество без какого-либо специального биологического эффекта.
Матриксное вещество представляет собой вещество, которое включает или каким-либо иным способом удерживает активное вещество; сам матрикс может выступать в качестве активного вещества.
Липофильное вещество представляет собой вещество, имеющее сродство к жирам, измеряемое в виде коэффициента распределения между жирорастворимым и водорастворимым растворителями.
Гидрофильное вещество представляет собой вещество, имеющее сродство к воде, измеряемое в виде коэффициента распределения между жирорастворимым и водорастворимым растворителями.
Водорастворимые и/или гидрофильные активные вещества представляют собой биологически активные вещества, которые непосредственно сами или в виде любой соли растворяются в воде или другой растворимой в воде среде, такой как плазма или кровь, до по меньшей мере 1 мг/мл (предпочтительно до 5 мг/мл, более предпочтительно до 20 мг/мл) или имеют показатель коэффициента распределения бутанол/вода не ниже 0,5.
Труднорастворимый в воде - термин “труднорастворимый в воде” означает растворимость вещества в воде менее 5 мг/мл, предпочтительно менее 1 мг/мл.
Гидрофильные растворители представляют собой растворители, в которых при комнатной температуре растворяется 1 об.% воды, предпочтительно 10 об.%
Мгновенная биодоступность означает перенос активного вещества в ткани за короткое время дилатации баллона без растворения активного вещества или его замедленного высвобождения в ткани с помощью специальных средств, таких как инкапсуляция.
Немедленное высвобождение означает, что эффективная доза активного вещества переносится в среду при расширении баллона максимум за одну минуту. Активное вещество может доставляться, например, в особом виде и во время растворения быть дольше эффективным.
Низкомолекулярный относится к веществам с молекулярной массой меньше 5000 дальтон, предпочтительно меньше 2000 дальтон, более предпочтительно меньше 1000 дальтон.
Гидрофильная/гидрофилизированная мембрана баллона представляет собой гидрофильную мембрану, состоящую из смачиваемых водой или гидрофильными растворителями материалов; гидрофилизированные мембраны баллонов представляют собой мембраны, изготовленные, например, из нейлона, поверхность которых изменяется при их последующей обработке в смоченном водой или другим гидрофильным растворителем состоянии. Гидрофильные и/или гидрофилизированные мембраны не следует путать с мембранами, которые обеспечивают дополнительный гидрофильный слой.
Мембрана баллона с гидрофильным покрытием представляет собой мембрану, содержащую дополнительный нанесенный слой, который смачивается водой.
Открытый на поверхности относится к лекарственным веществам или адъювантам, которые не включены в мембрану баллона или в покрытие, прочно прикрепленное к мембране баллона, например в полимерное, нерастворимое в воде покрытие, каким, в частности, является неотслаивающийся гидрогель. Открытый на поверхности включает покрытия, которые в сложенном состоянии закрыты складками мембраны баллона.
Прочное прикрепление - сложенные баллонные катетеры (Orbus IX, Bavaria Medizin Technologie, Oberpfaffenhofen, Deutschland, SeQent, BBraun, Melsungen, изготовленные в Германии баллоны диаметром 3,5 мм, длиной 20 мм, или аналогичные продукты других производителей) покрывают в сложенном состоянии активным веществом в количестве не менее 3 мкг/1 мм2, как описано ниже. Высушенные баллоны расширяют и встряхивают в стакане в течение 5 сек: более 75% дозы остается прикрепленной к баллону.
Летучий относится к растворителям с температурой кипения ниже 300°C, предпочтительно ниже 160°C, более предпочтительно ниже 100°C.
Описание изобретения
Задачей изобретения является предоставление улучшенных медицинских изделий, например баллонных катетеров, которые способствуют надежному локальному лечению пораженных тканей, раскрывают новые применения и способствуют использованию гидрофильных, хорошо растворимых в воде, активных веществ в качестве компонентов покрытия.
В частности, задачей настоящего изобретения является изготовление баллонных катетеров, которые не приводят к удлинению или растяжению сосудов и при этом высвобождают активные вещества в количестве, достаточном для лечения или профилактики пораженных стенок сосудов.
Эта задача решается с помощью независимых пунктов формулы настоящего изобретения. Дополнительные предпочтительные варианты осуществления даны в виде примеров и зависимых пунктов формулы изобретения. Кроме того, достаточно подробно раскрыта новая конструкция специфического баллонного катетера и способы нанесения покрытия на баллонные катетеры. Кроме того, согласно изобретению можно использовать нижеприведенные активные вещества и адъюванты.
Активные вещества и адъюванты
В качестве активных веществ предпочтительны антипролиферативные, противоопухолевые, противовоспалительные вещества, вещества с антигиперпластическим эффектом, антинеопластические, антимитотические, цитостатические, цитотоксические, антиангиогенные, антирестенотические вещества, вещества, ингибирующие образование микротрубочек, антитромботические вещества.
Примерами антипролиферативных, противоопухолевых, противовоспалительных веществ, веществ с антигиперпластическим эффектом, антинеопластических, антимитотических, цитостатических, цитотоксических, антиангиогенных, антирестенотических веществ, веществ, ингибирующих образование микротрубочек, антимиграционных и антитромботических веществ являются:
абциксимаб, ацеметацин, ацетилвизмион B, акларубицин, адементионин, адриамицин, аэсцин, афромозон, акагерин, альдеслейкин, амидорон, аминоглутетемид, амсакрин, анакинра, анастрозол, анемонин, аноптерин, антимикотики, антитромботики, апоцимарин, аргатробан, аристолактам-AII, аристоловая кислота, арсентриоксид и другие соединения мышьяка, аскомицин, аспарагиназа, аспирин, аторвастин, ауранофин, азатиоприн, азитромицин, баккатин, бафиломицин, базиликсимаб, бендамустин, бензокаин, берберин, бетулин, бетулиновая кислота, билобол, биолимус, биспартенолидин, блеомицин, бомбрестатин, босвелиновые кислоты и их производные, бруцеанол A, B и C, бриофиллин A, бузулфан, антитромбин, бивалирудин, кадгерин, камптотецин, капецитабин, o-карбамоилфеноксиуксусная кислота, карбоплатин, кармустин, целекоксиб, цефарантин, церивастатин, CETP-ингибиторы, хлорамбуцил, хлорохин фосфат, циктоксин, ципрофлоксацин, цисплатин, кладрибин, кларитромицин, колхицин, конканамицин, кумадин, натрийуретический пептид C-типа (CNP), изофлавон A кудрании (Cudraisoflavon), куркумин, циклофосфамид, циклоспорин A, цитарабин, дакарбазин, даклизумаб, дактиномицин, дапсон, даунорубицин, диклофенак, 1,11-диметоксикантин-6-он, доцетаксель, доксорубицин, дунаимицин, эпирубицин, эпотилон A и B, эритромицин, эстрамустин, этобозид, эверолимус, филграстим, флуробластин, флувастатин, флударабин, флударабин-5'-дигидрогенфосфат, флюороурацил, фолимицин, фосфестрол, гемцитабин, галакинозид, гинкгол, гинкголовая кислота, гликозид 1a, 4-гидроксиоксициклофосфамид, идарубицин, ифосфамид, джозамицин, лапахол, ломустин, ловастатин, мелфалан, мидекамицин, митоксантрон, нимустин, питавастатин, правастатин, прокарбазин, митомицин, метотрексат, меркаптопурин, тиогуанин, оксалиплатин, висмут и соединения висмута или хелаты, иринотекан, топотекан, гидроксикарбамид, милтефозин, пентостатин, пегаспараза, эксеместан, летрозол, форместан, ингибитор пролиферации SMC типа 2ω, митоксантрон, микофенолат мофетил, c-myc-антисмысловой, b-myc-антисмысловой, β-лапахон, подофилотоксин, подофиловой кислоты 2-этилгидразид, молграмостим (rhuGM-CSF), пегинтерферон α-2b, ленограстим (r-HuG-CSF), макрогол, селектин (антагонист цитокинов), ингибиторы цитокинов, COX-2-ингибитор, NFkB, ангиопептин, моноклональные антитела, которые ингибируют пролиферацию мышечных клеток, антагонисты bFGF, пробукол, простагландин, 1-гидрокси-11-метоксикантин-6-он, скополетин, доноры NO, пентаэритритилтетранитрат, синднонимин, S-нитрозопроизводные, тамоксифен, стауроспорин, β-эстрадиол, α-эстрадиол, эстриол, эстрон, этинилэстрадиол, медроксипрогестерон, эстрадиола ципионат, эстрадиола бензоат, траниласт, камебакаурин и другие терпеноиды, которые применяются при лечении рака, верапамил, ингибиторы тирозинкиназы (тирфостин), паклитаксел, производные паклитаксела, 6-α-гидрокси-паклитаксел, 2'-сукцинилпаклитаксел, 2'-сукцинилпаклитаксел-триэтаноламин, 2'-глутарилпаклитаксел, 2'- глутарилпаклитаксел-триэтаноламин, 2'-О-сложный эфир паклитаксела с N-(диметиламиноэтил)глутамидом, 2'-О-сложный эфир паклитаксела с N-(диметиламиноэтил)глутамидгидрохлоридом, таксотер, субоксиды углерода (MCS), макроциклические олигомеры субоксида углерода, мофебутазон, лоназолак, лидокаин, кетопрофен, мефенаминовые кислоты, пироксикам, мелоксикам, пеницилламин, гидроксихлорохин, натрия ауротиомалат, оксацепрол, β-ситостерин, миртекаин, полидоканол, нонивамид, левоментол, эллиптицин, D-24851 (кальбиохем), колцемид, цитохалазин A-E, инданоцин, нокадазол, белок S-100, бацитрацин, антагонисты рецептора витронектина, азеластин, стимулятор гуанидилциклазы, тканевый ингибитор металлопротеиназы-1 и -2, свободные нуклеиновые кислоты, нуклеиновые кислоты, встроенные в вирусные трансмиттеры, фрагменты ДНК и РНК, ингибитор активатора плазминогена 1 типа, ингибитор активатора плазминогена 2 типа, антисмысловые олигонуклеотиды, ингибиторы VEGF (васкулоэндотелиального фактора роста), активные вещества, выбранные из группы антибиотиков, такие как цефадроксил, цефазолин, цефаклор, цефотаксим, тобрамицин, гентамицин, пенициллины, такие как диклоксациллин, оксациллин, сульфонамиды, метронидазол, эноксапарин, десульфатированный и N-реацетилированный гепарин, тромбоцитарный мембранный рецептор GpIIb/IIIa, антитело-ингибитор фактора Ха, гепарин, гирудин, r-гирудин, PPACK (D-фенилаланин-L-пролин-L-аргинин хлорметилкетон), протамин, проурокиназа, стрептокиназа, варфарин, урокиназа, вазодилататоры, такие как дипирамидолтрапидил, нитропруссиды, антагонисты PDGF (тромбоцитарного фактора роста), такие как триазолопиримидин и серамин, ингибиторы АСЕ (ангиотензин-конвертирующего фермента), такие как каптоприл, цилазаприл, лизиноприл, эналаприл, лозартан, ингибиторы тиопротеазы, простациклин, вапипрост, интерферон α, β и γ, антагонисты гистамина, блокаторы серотонина, ингибиторы апоптоза, регуляторы апоптоза, такие как р65 NF-kB или Bcl-xL антисмысловые олигонуклеотиды, галофугинон, нифедипин, токоферол, траниласт, молсидомин, полифенолы чая, эпикатехина галлат, эпигаллокатехина галлат, лефлуномид, этанерцепт, сульфасалазин, этопозид, диклоксациллин, тетрациклин, триамцинолон, мутамицин, прокаинамид, ретиноевая кислота, хинидин, дизопиримид, флекаинид, пропафенон, соталол, природные и синтетические стероиды, такие как инотодиол, махирозид А, галакинозид, мансонин, стреблозид, гидрокортизон, бетаметазон, дексаметазон, нестероидные вещества (NSAIDS (нестероидные противовоспалительные препараты)), такие как фенопрофен, ибупрофен, индометацин, напроксен, фенилбутазон, и другие противовирусные вещества, такие как ацикловир, ганцикловир и зидовудин, клотримазол, флуцитозин, гризеофульвин, кетоконазол, миконазол, нистатин, тербинафин, противопротозойные вещества, такие как хлорохин, мефлохин, хинин, а также природные терпеноиды, такие как гиппоцескулин, баррингтогенол-C21-ангелат, 14-дегидроангростистахин, агроскерин, агростистахин, 17-гидроксиангростистахин, оватодиолиды, 4,7-оксициклоанизомелиновая кислота, бакхариноиды В1, В2, B3 и В7, тубеимозид, бруцеатинозид С, яданзиозиды N и Р, изодезоксиэлефантопин, томенфантопин А и В, коронарин А, В, С и D, урсоловая кислота, гиптатовая кислота А, изоиридогерманал, майтенфолиол, эффусантин А, эксцисанин А и В, лонгикаурин В, скульпонеатин С, камебаунин, лейкаменин А и В, 13,18-дегидро-6-альфа-сенециоилоксичапаррин, таксамаирин А и В, регенилол, триптолид, цимарин, гидроксианоптерин, протоанемонин, челибурина хлорид, синококулин А и В, дигидронитидин, нитидина хлорид, 12-бета-гидроксипрегнадиен 3,20-дион, геленалин, индицин, индицин-N-оксид, лазиокарпин, инотодиол, подофиллотоксин, джустицидин А и В, ларреатин, маллотерин, маллотохроманол, изобутирилмаллотохроманол, махирозид А, марчантин А, майтанзин, ликоридицин, маргетин, панкратистатин, лириоденин, биспартенолидин, оксоушинсунин, периплокозид А, урсолиевая кислота, дезоксипсороспермин, психорубин, рицин А, сангвинарин, кислота Manwuweiz, метилсорбифолин, сфателиахромен, стизофиллин, мансонин, стреблозид, дигидроусамбаренсин, гидроксиусамбарин, стрихнопентамин, стрихнофиллин, усамбарин, усамбарензин, лириоденин, оксоушинсунин, дафноретин, ларицирезинол, метоксиларицирезинол, сирингарезинол, сиролимус (рапамицин), рапамицин в комбинации с мышьяком или соединениями мышьяка или комплексен, соматостатин, такролимус, рокситромицин, тролеандомицин, симвастатин, росувастатин, винбластин, винкристин, виндезин, талидомид, тенипозид, винорелбин, трофосфамид, треосульфан, тремозоломид, тиотепа, третоноин, спирамицин, умбеллиферон, дезацетилвисмион А, висмион А и В, зеорин, фасудил.
Предпочтительными активными веществами, которые наносятся на баллон катетера, являются паклитаксел и другие таксаны, рапамицин и другие ингибиторы mTOR (мишени рапамицина у млекопитающих), метотрексат, мышьяк или соединения мышьяка, висмут или соединения висмута или талидомид.
В других предпочтительных вариантах осуществления по меньшей мере одно активное вещество находится в виде труднорастворимого в воде нейтрального вещества, труднорастворимой в воде соли, труднорастворимой в воде кислоты или труднорастворимого в воде основания.
В качестве гидрофильного адъюванта предпочтительно использовать летучие гидрофильные растворители или смеси гидрофильных растворителей, а также нелетучие вещества без какого-либо биологического эффекта при их применении, такие как сахара, сахарные спирты, аминокислоты, жиры, неорганические или органические соли и/или контрастные вещества, пригодные для внутрисосудистого введения, или красители. Предпочтительными адъювантами являются аскорбиновая кислота, мочевина, полиэтиленгликоль 8000, а также несмотря на низкую растворимость в воде триглицериды, в частности твердые при комнатной температуре триглицериды, такие как тримиристин.
Покрытие для баллонного катетера
В вышеупомянутых патентах описаны обычные баллонные катетеры с ровными стенками для чрескожной транслюминальной ангиопластики, состоящие из различных материалов, таких как, например, нейлон, PEBAX, полиэтилен и различные другие материалы, которые описаны в патенте DE 10 2004 046 244 и других патентах, баллонные катетеры со складками или порами, в которых находятся активные вещества, или баллонные катетеры со структурированной или шероховатой мембраной. Целью структурных изменений, с точки зрения увеличения поверхности, является увеличение ее загрузки активными веществами или адгезии активных веществ к баллонам. В WO 2004/006976 описаны также баллоны с дополнительным гидрофильным слоем. Баллоны таких катетеров расширяются до заданного размера, устойчивы к давлению и в стенозированных артериях снова расширяются до своего первоначального диаметра.
Однако структурирование поверхности имеет некоторые недостатки, заключающиеся в замедлении доставки активного вещества при расширении баллона в сосуде. В расширенном состоянии баллон полностью блокирует ток крови через предназначенный для лечения сосуд. Блокирование тока крови, в частности, в коронарных артериях допускается только на очень короткий промежуток времени. В течение этого времени должна высвободиться эффективная доза. Любая задержка при отделении от мембраны баллона по меньшей мере одного активного вещества является недостатком.
Неожиданным оказался тот факт, что гидрофильные или гидрофилизованные мембраны баллона можно воспроизводимо и равномерно покрывать активным веществом, кроме того, доступным является широкий спектр используемых для покрытия растворителей, и по меньшей мере одно активное вещество хорошо прикрепляется к мембране баллона. В частности, это справедливо и для случаев, когда необходимо покрывать баллоны в уже сложенном состоянии. Гидрофильные мембраны баллонов хорошо известны и используются для уменьшения слипания катетера до расширения баллона.
Таким образом, настоящее изобретение относится к баллонному катетеру, содержащему баллон с мембраной, причем мембрана баллона является гидрофильной или гидрофилизованной, и/или поверхность мембраны баллона имеет гидрофильное покрытие. Предпочтительно гидрофильное покрытие прочно прикреплено к поверхности баллона, т.е. прочно соединено с поверхностью баллона и не отделяется при расширении баллона катетера.
Настоящее изобретение также относится к баллонному катетеру, содержащему баллон с гидрофильной или гидрофилизованной мембраной, причем мембрана баллона покрыта по меньшей мере одним находящимся на открытой поверхности активным веществом, таким образом, что по меньшей мере одно активное вещество высвобождается сразу при расширении баллона катетера. Более того, баллон катетера дополнительно может быть покрыт адъювантами.
Гидрофильную поверхность баллона, или поверхность баллона с гидрофильным покрытием, или поверхность баллона, имеющую прочно прикрепленное гидрофильное покрытие на мембране баллона, предпочтительно покрывают по меньшей мере одним гидрофильным активным веществом или по меньшей мере одним гидрофильным активным веществом вместе с по меньшей мере одним гидрофильным адъювантом.
Предпочтительные по изобретению баллоны катетеров характеризуются двумя покрытиями, нижним прочно прикрепленным гидрофильным покрытием и внешним удаляемым покрытием, содержащим активное вещество или композицию, содержащую по меньшей мере одно активное вещество.
При этом предпочтительной является обработка, как правило, липофильной поверхности баллона активированным кислородом для придания ей гидрофильности. Гидрофильная мембрана баллона или, более конкретно, гидрофильная поверхность указанной мембраны баллона, т.е. гидрофильная поверхность баллона, может быть изготовлена путем нанесения гидрофильного покрытия на липофильную мембрану баллона и/или поверхность баллона или, что предпочтительнее с точки зрения нанесения покрытия, путем изменения липофильной мембраны химическим способом (например, реакцией с активированным кислородом).
Гидрофильные баллоны катетеров могут быть покрыты предназначенными для покрытия композициями с помощью простых хорошо воспроизводимых способов, таких как погружение, таким образом, чтобы содержание активного вещества на баллоне катетера, покрытого по меньшей мере одним активным веществом, имело стандартное отклонение от средней величины, не превышающее 20%, предпочтительно менее 15%, более предпочтительно менее 10% и наиболее предпочтительно менее 5%.
В другом предпочтительном варианте осуществления мембрану баллона, или гидрофильную мембрану, или мембрану баллона с гидрофильным покрытием покрывают по меньшей мере одним активным веществом, которое необязательно находится в смеси с по меньшей мере одним малорастворимым в воде адъювантом. Такое конструктивное решение имеет преимущество, заключающееся в том, что малорастворимый в воде адъювант препятствует преждевременному отделению активного вещества.
При покрытии активными веществами или адъювантом может исчезнуть улучшенная сопротивляемость гидрофильных баллонов склеиванию, во всяком случае, когда покрытие также находится снаружи нерасширенного баллона. Недостатком гидрофильных баллонов является то, что при расширении в зауженных артериях они легко сползают из нужного положения. По наблюдениям авторов этот недостаток легко устраняется путем покрытия лекарственными и матричными веществами, поскольку первое покрытие не растворяется в окружающей среде и повышает трение между баллоном и стенками артерии.
Как правило, ангиопластические баллоны не должны сильно растягиваться. Следовательно, при низком давлении они достигают некоторого диаметра, который при повышении давлении сильно не увеличивается.
Другая полезная модификация мембраны баллона касается ее механических свойств: для переноса лекарственного вещества на стенку сосуда без растяжения стенки выбирают мембраны, которые являются гибкими (эластичными) и растяжимыми при низком давлении или существенно превышают диаметр сосуда. Существенное превышение означает, что диаметр баллона превышает исходный диаметр сосуда по меньшей мере на 20%, предпочтительно превышает более чем на 30%, и баллон может растягиваться до максимально возможной степени при давлении не выше чем примерно 2000 гПа. Такие баллоны не предназначены для существенного расширения просвета сосуда путем оказания давления на его стенки. Существенным расширением просвета, в частности, является устранение закупорки или сильного стеноза или расширение просвета более чем на 30% от исходного диаметра сосуда. Специалист в данной области может получить такие характеристики мембраны путем выбора состава мембраны и/или толщины стенки и складок. Баллоны могут иметь сравнительно небольшое давление разрыва, например, равное или ниже 10000 гПа (9,87 атм; [1 атм =1013 гПа]), предпочтительно равное или ниже 5000 гПа (4,93 атм), поскольку их не расширяют при высоком давлении. Как правило, давление расширения предпочтительно не превышает 4000 гПа (3,95 атм), более предпочтительно находится ниже 2000 гПа (1,97 атм) и более предпочтительно ниже 1000 гПа (0,97 атм) от нормального. Практически предпочтительным является давление, находящееся в пределах от 2000 гПа (1,97 атм) до 200 гПа (0,20 атм) от нормального. Для лечения артерий, вен или гемодиализных шунтов предпочтительными являются катетеры с размером баллонов, у которых отношение диаметра к длине не превышает значения 0,2 или более предпочтительно отношение диаметра к длине ниже 0,1.
Описанные баллоны не следует путать с баллонами, которые состоят, например, из силикона или латекса, являются в основном круглыми и используются для фиксации катетеров в полостях, таких как мочевой пузырь, и не заполняют полностью указанную полость.
Согласно изобретению предпочтительными также являются баллонные катетеры, которые достигают своего максимального диаметра в расширенном состоянии даже при низком давлении и все еще обладают некоторой пластичностью для адаптации к неровной стенке сосуда. Следовательно, предпочтительным является, когда радиус баллона катетера после полного его расширения при повышенном давлении увеличивается более чем на 15%, предпочтительно более чем на 30% и особенно предпочтительно более чем на 60%. Увеличение давления обычно происходит при введении внутрь баллона катетера газа (например, углекислого газа) или жидкости, такой как, например, контрастирующее средство.
Более предпочтительными являются баллонные катетеры, у которых радиус баллона после полного расширения с помощью повышенного давления внутри баллона катетера увеличивается более чем на 15%, предпочтительно более чем на 30% и особенно предпочтительно более чем на 60%.
Другой вариант осуществления настоящего изобретения относится к баллонному катетеру с по меньшей мере одним находящимся на открытой поверхности активным веществом, которое сразу высвобождается при расширении баллона, причем радиус баллона после полного расширения с помощью повышенного давления внутри указанного баллона увеличивается более чем на 15%, предпочтительно более чем на 30%, и особенно предпочтительно более чем на 60%.
Активное вещество или несколько активных веществ и при необходимости дополнительные адъюванты прикреплены к мембране баллона и/или защищены структурой или складками готового к применению баллона, несмотря на низкую прочность мембраны, неожиданно хорошую для преждевременного отделения. Структура мембраны баллона в сложенном состоянии или состоянии хранения, т.е. не в расширенном состоянии баллона, может содержать ниши, углубления и выпуклости, складки любой формы, которые сами по себе являются гладкими при расширении пластичной и эластичной мембраны при низком давлении. Такие баллоны применимы предпочтительно для лечения сосудистых изменений, которые существенно не сокращают кровоток, т.е. которые сужают свободный просвет сосуда менее чем на 50%. Они позволяют лечить сосуды с низким сопротивлением к давлению, поскольку они применяются в сосудах с низким давлением и неровной стенкой. В частности, такие баллонные катетеры по изобретению являются подходящими для местного лечения и профилактики больных сосудов и, в частности, для лечения воспалительных изменений сосудов, уязвимых бляшек, участков сосудов, которые ранее подвергались механическому или хирургическому лечению, обширных поражений без необходимости (повторного) растяжения, а также небольших сосудов, которые недоступны для стента.
Баллонные катетеры по изобретению являются особенно подходящими для лечения изменений стенок сосудов, которые существенно не ограничивают кровоток.
Нанесение покрытия
Одной из нерешенных проблем является предоставление в достаточной мере точной дозы активного вещества, достаточной для равномерного распределения на поверхности баллона. Для введения лекарственных веществ установлены жесткие требования, относящиеся к дозированию лекарственной формы, которая в данном случае наносится на баллон. Несмотря на известность способов точного дозирования для большинства фармацевтических применений отсутствует необходимость в равномерном распределении активного вещества на поверхности. Кроме того, обычные дозаторы в области фармацевтики и биохимии, как правило, работают с водными растворами, давление пара которых при комнатной температуре не влияет существенным образом на дозирование.
В приведенных ниже патентах можно найти некоторые неявные ссылки на аналогичную требующую решения проблему, однако смысл проблемы не определен, к тому же не описаны какие-либо процедуры, которые могли бы позволить специалисту осуществить покрытие баллона экономичным и воспроизводимым способом таким образом, чтобы полученные изделия быстро и полностью высвобождали лекарственное вещество в нужном месте и были надежными и эффективными. Раскрытый в EP 1372737 A и WO 2004/028582 A способ нанесения покрытия путем многократного погружения обычного, готового к применению сложенного баллона в слабовязкие растворы липофильных лекарственных веществ и подходящих адъювантов дает в результате прежде всего достаточно воспроизводимую дозу на баллоне для медицинского применения. Важным открытием было то, что несмотря на обусловленное складками неоднородное распределение активного вещества в радиальном направлении баллонов при их расширении распределение по меньшей мере активного вещества на стенках сосуда было равномерным (Scheller B, Bacon U, Böhm M. Prevention OF restenosis - is angioplasty to who? Heart 2007; 93: 539-541). Тем не менее, при обычном применении этого способа в производстве очевиден ряд недостатков. Способ является неудобным и дорогостоящим, поскольку он требует нескольких погружений с процессом сушки между ними. Количество активного вещества, прикрепляемого к баллону, определяется неполностью контролируемыми факторами. Хотя достаточно однородные баллоны из одной партии могут быть покрыты с удовлетворительной воспроизводимостью, это не всегда верно для партий разных производственных циклов. Другой трудной для решения проблемой, возникающей при использовании метода погружения, является продольное распределение активного вещества. В частности, существует вероятность того, что проксимальный участок баллона не будет погружен должным образом. И, наконец, в вышеуказанном способе являются необходимыми соответствующие меры, которые предотвращают проникновение слабовязкого раствора в центральный просвет катетера.
Другие ранее известные способы нанесения покрытия приводят к более неблагоприятным результатам: после нанесения покрытия на расширенные баллоны баллоны с покрытием должны быть сложены. Это можно сделать без существенных потерь, с точки зрения нанесенной дозы, только в случае прочно прикрепленного покрытия. Прикрепленное покрытие высвобождается не в достаточной степени за время кратковременного контакта между мембраной баллона и стенкой сосуда. При нанесении покрытия на сложенные баллоны методом распыления активное вещество находится только сверху на баллоне, что приводит к увеличению потерь во время введения баллонного катетера в сосуд, направления катетера и его продвижения по сосуду против кровотока. Распыление, намазывание и нанесение с помощью пипетки не гарантирует ни воспроизводимой, точно заданной дозы, ни равномерного распределения на катетере по меньшей мере одного активного вещества. С помощью обычной пипетки трудно получить как точную величину требуемого очень небольшого объема предпочтительных летучих растворителей, так и равномерного распределения раствора на баллоне. Преимущество способа, описанного в WO 2007/090385, заключается в распределении активных веществ в складках баллонов.
Способ по изобретению для нанесения покрытия на медицинские изделия или их компоненты, такие как баллоны, расположенные на дистальном конце катетеров, включает в себя следующие этапы, на которых:
а) готовят баллонный катетер;
в) готовят микродозатор, содержащий предназначенную для покрытия композицию, которая не находится в контакте с газовой фазой;
с) равномерно без потерь покрывают баллон катетера предназначенной для покрытия композицией, используя микродозатор.
При нанесении покрытия обычно применяется раствор или жидкость для покрытия, но также может применяться гель или суспензия, эмульсия, дисперсия или взвесь.
При нанесении покрытия важно, чтобы предназначенный для покрытия растворитель не испарился до его нанесения на баллон. Следовательно, растворитель не должен находиться в контакте с газовой фазой, объем которой может влиять на выдаваемую дозу.
Во время нанесения покрытия баллонный катетер обычно располагают горизонтально и вращают вокруг продольной оси, при этом микродозатор движется взад и вперед вдоль продольной оси баллона катетера, гарантируя при этом полное покрытие сложенного или неполное покрытие несложенного баллона катетера.
В качестве микродозатора можно использовать шприц (Фиг.3), канюлю, трубку или другое устройство, которое является достаточно точным для доставки требуемых небольших количеств на баллон катетера и при нанесении покрытия не повреждает и предпочтительно не касается баллона катетера.
Подходящими растворителями для предназначенной для покрытия композиции предпочтительно являются летучие растворители или соединения хлора или фтора с температурой кипения ниже 300°C, предпочтительно ниже 100°C. Кроме того, можно применять гидрофильные растворители или смеси по меньшей мере одного растворителя или гидрофильного растворителя с водой.
Баллоны предпочтительно покрывают в сложенном виде, но их также можно покрывать в любом виде с помощью устройств, подобранных соответствующим образом.
Для достижения равномерного покрытия мембрану баллона одновременно полностью смачивают, от дистального конца до проксимального конца, включая все складки, предназначенной для покрытия композицией во время нанесения покрытия, но так, чтобы не было стекающих капель.
В качестве предназначенной для покрытия композиции можно использовать гель. При этом по меньшей мере одно активное вещество может служить в качестве гелеобразующего вещества или может принимать участие в образовании геля. В отсутствие других гелеобразующих веществ активное вещество само действует в качестве гелеобразующего вещества для получения гелеобразной предназначенной для покрытия композиции.
Кроме того, предпочтительным является, если на баллон катетера наносится по меньшей мере одно активное вещество в труднорастворимой в воде форме.
В качестве альтернативы, по меньшей мере одно активное вещество, которое может быть хорошо растворимым в воде, т.е. гидрофильным, для нанесения на баллон катетера может быть переведено в труднорастворимую в воде форму. Это может произойти, например, путем образования комплекса с циклодекстрином или образования соли. Получение труднорастворимых в воде солей, так же как выбор противоиона или комплексообразующего вещества, хорошо известно специалистам в данной области и может быть выполнено путем обычного определения растворимости.
Ниже описан предпочтительный вариант осуществления способа для нанесения покрытия по изобретению, который включает следующие этапы:
А) Приготовление:
1) определенный баллонный катетер или более подходящие компоненты, содержащие баллон, причем баллон предпочтительно находится в сложенном состоянии или в состоянии с предварительно сформированными, но не окончательно плотно уложенными складками;
2) поддерживающее баллон устройство предпочтительно в горизонтальном положении, причем в предпочтительном варианте осуществления баллон может вращаться вокруг своей продольной оси;
3) волюметрическое устройство для микрообъемов для подачи раствора, предпочтительно содержащего летучий органический растворитель, в котором подаваемый объем не находится в контакте с газовой фазой, объем которой может влиять на подаваемую дозу;
4) передаточный элемент для передачи жидкости из волюметрического устройства для микрообъемов в баллон;
5) раствор с по меньшей мере одним активным веществом и необязательно одним или несколькими адъювантами.
В) Этапы выполнения:
1) вычисляют объем растворителя, необходимый для нужной предназначенной для нанесения дозы, используя известную площадь поверхности баллона в мм2 и концентрацию активного вещества в растворителе;
2) вставляют катетер или компоненты катетера, содержащие баллон, в поддерживающее устройство;
3) калибруют волюметрическое устройство на рассчитанный объем применяемого раствора;
4) заполняют волюметрическое устройство предназначенным для покрытия раствором так, чтобы не образовывались пузырьки газа;
5) медленно непрерывно вращают баллон вокруг своей оси;
6) устанавливают передаточный элемент с отверстием, через которое выходит раствор, на баллон, или непосредственно над баллоном, или непосредственно под баллоном, или сбоку;
7) переносят заданный объем предназначенного для покрытия раствора на баллон посредством передаточного элемента с равномерной скоростью на цилиндрическую часть баллона в направлении продольной оси, перемещая вперед и назад. Скорость подачи раствора предпочтительно регулируют таким образом, чтобы все части баллона были смочены жидкостью одновременно без образования на баллоне стекающих капель.
Хотя волюметрическое устройство гарантированно выдает точную рассчитанную для баллона дозу независимо от материала баллона, структуры его поверхности (гладкая или структурированная, готовая к применению или свободно сложенная или частично или полностью раскрытая), размера и свойств баллона, а также отдельных партий баллонов, движение баллона и передаточного элемента, имеющее отношение к полному смачиванию баллона предназначенным для покрытия раствором, приводит к неожиданно равномерному его распределению на растянутом в длину баллоне.
После нанесения покрытия готовые баллоны складывают и/или сушат в подходящих условиях, могут быть установлены стенты, и катетеры упаковывают и стерилизуют обычным способом.
Вышеописанный способ для нанесения покрытия может быть реализован специалистами в данной области техники с помощью объектов и устройств разного типа и разными способами и может быть приспособлен к объектам, на которые необходимо нанести покрытие. Он характеризуется точностью дозирования и размещения, равномерностью распределения покрытия на поверхности предназначенной для покрытия области, включая проникновение в складки и другие труднодоступные структуры. Он является несложным и экономичным в применении, поскольку требуется минимальное количество материала и времени, а процесс является легко контролируемым и поддающимся автоматизации. В частности, исключается потеря предназначенной для покрытия композиции в контейнере и нежелательное распределение композиции на медицинские изделия или их окружение. Исключено какое-либо изменение предназначенной для покрытия композиции до момента ее нанесения на медицинское изделие в результате преждевременного испарения летучего растворителя.
Ускоренное расплавление и растворение липофильного активного вещества
В EP 1372737 A и WO 2004/028582 A, в патенте США № 6306166 и других патентных документах описано несколько растворителей, подходящих для покрытия медицинских изделий лекарственными средствами. Неожиданно было обнаружено, что липофильные лекарственные средства, такие как паклитаксел и другие таксаны, а также рапамицин и родственные соединения, в водной среде, крови или ткани особенно хорошо отделяются от поверхности баллона и переходят в раствор, когда медицинские изделия покрыты растворами этих соединений в хлороформе, или дихлорметане, или других летучих соединениях хлора или фтора, или их смесях.
Другие способы ускорения отделения липофильного и/или труднорастворимого в воде активного вещества представляют собой применение гидрофильных летучих органических растворителей, в частности метанола, этанола, пропанола, муравьиной кислоты, уксусной кислоты, тетрагидрофурана (ТГФ), ацетона, бутанола, 3-пентанола, сложных эфиров карбоновых кислот, в частности метилформиата, этилформиата, метилацетата, этилацетата и т.д. и их смесей с водой. При особенно предпочтительном типе покрытия, например, паклитакселем отсутствуют какие-либо дополнительные покрытия мембраны баллона другими полимерами, гидрогелями или другими слоями, несущими лекарственные вещества, все добавки и сложные смеси растворителей. До настоящего времени такие покрытия считались очень неэффективными (Scheller B, Speck U, Abramjuk C, Bernhardt U, Böhm M, Nickenig G: Paclitaxel balloon coating - a novel method for prevention and therapy of restenosis. Circulation 2004; 110: 810-814, WO 2004/028582, Beispiel 7; Cremers B, Biedermann M, Mahnkopf D, Böhm M, Scheller B. Paclitaxel-beschichtete PTCA-Katheter: Gibt es Unterschiede? Einfluss von PACCOCATH® - und DIOR®-Ballonkathetern auf die Neointimaproliferation an Schweinekoronarien. Clin Res Cardiol 2008; 97 - Suppl 1: V1742).
Неожиданным оказалось то, что кристаллическую структуру и адгезию паклитаксела к мембране баллона можно очень точно регулировать небольшим количеством воды в растворе паклитаксела, например в изопропаноле, тетрагидрофуране, диметилформамиде или уксусной кислоте или смеси этих растворителей. Предпочтительными являются растворители, которые (а) приводят к очень прочной адгезии паклитаксела к мембране баллона и (в) в которых при комнатной температуре растворяется по меньшей мере один объемный процент воды. Из этих обычных смесей растворителей без каких-либо технических усилий образуются кристаллы активного вещества, в данном случае паклитаксела, который прочно прикрепляется к сложенному баллону и при расширении баллона, например, в зауженной артерии быстро полностью отделяется и почти полностью переходит в ткань. Происходит медленное растворение кристаллов, как это известно в фармацевтике, и таким образом обеспечивается эффективное количество лекарственного средства в течение определенного времени. Как описано в WO 2007/090385, дозирование осуществляется значительно проще и, что касается дозы, то она определяется более точно. Отсутствие матриксного материала дает большое преимущество, поскольку отсутствует необходимость в оценке совместимости с активным веществом, стабильности матрикса в течение длительного промежутка времени, влияния на мембрану баллона и биологической активности. Адъюванты могут оказывать влияние на адгезию заранее установленных стентов, например при уменьшении адгезии стенты отделяются раньше времени, либо при увеличении адгезии стенты не отделяются после расширения баллона, что в обоих случаях наносит вред здоровью пациента. Уменьшение загрузки баллонов путем отказа от адъювантов также дает преимущество, поскольку дополнительно наносимые вещества усложняют требуемую плотную упаковку баллона. Для того чтобы баллоны могли проходить через узкие просветы сосудов, необходимо, чтобы они имели небольшой наружный диаметр.
Другие варианты изобретения относятся к баллону катетера, имеющего мембрану с гладкими стенками, покрытому активным веществом, растворенным в органическом растворителе, содержащем по меньшей мере 1%, предпочтительно по меньшей мере 10% воды, высушенному и стерилизованному, причем активное вещество находится в кристаллическом виде. Предпочтительным является, если баллоны катетеров с мембраной, имеющей гладкую стенку, покрывают в сложенном состоянии.
Другой предпочтительный вариант настоящего изобретения относится к баллонному катетеру, у которого мембрана баллона, т.е. баллон этого баллонного катетера, покрыта активным веществом, растворенным в органическом растворителе, содержащем по меньшей мере 1%, предпочтительно 10% воды, высушена и стерилизована, причем активное вещество на мембране баллона находится в кристаллическом виде.
Другой предпочтительный вариант настоящего изобретения также относится к баллонному катетеру, причем мембрана баллона указанного баллонного катетера имеет гладкую стенку и покрыта лежащими на открытой поверхности кристаллами паклитаксела без добавок так, чтобы при введении сложенного баллона в артерию оставалось по меньшей мере 70%, предпочтительно по меньшей мере 80% и более предпочтительно по меньшей мере 90% прикрепленного паклитаксела, который сразу высвобождается при расширении баллонного катетера в зауженной артерии.
Жидкие лекарственные средства для покрытия могут добавляться в виде известных растворимых, водорастворимых или микрокорпускулярных матриксных веществ, причем микрокорпускулярные матриксные вещества также могут представлять собой активное вещество. Выбор подходящих адъювантов, как правило, зависит от активного вещества, растворителя и поверхности баллона. Примеры подходящих способствующих отделению адъювантов представляют собой аскорбиновую кислоту, мочевину и полиэтиленгликоль предпочтительно с молекулярной массой в пределах от примерно 5000 до 20000 дальтон. Из-за неблагоприятного влияния загрузки баллона на диаметр и эластичность покрытых баллонов общая загрузка (активное вещество и адъюванты) баллонов, т.е. общая нанесенная на мембрану баллона доза всех нелетучих компонентов, должна предпочтительно составлять менее 10 мкг/мм2, более предпочтительно менее 5 мкг на 1 мм2 поверхности баллона (в расширенном состоянии), доза адъювантов не должна превышать 1 мкг на 1 мм2 поверхности баллона, особенно предпочтительно 0,3 мкг/мм2.
Более того, настоящее изобретение относится к баллонному катетеру, причем мембрана указанного баллона катетера покрыта находящимся на открытой поверхности активным веществом и либо аскорбиновой кислотой, либо мочевиной, либо твердым при комнатной температуре триглицеридом, таким как тримиристин, либо полиэтиленгликолем с молекулярной массой от 8000 до 20000 дальтон, либо любой их смесью способом, при котором при расширении баллона катетера по меньшей мере одно активное вещество немедленно высвобождается.
Водорастворимые и гидрофильные вещества
На сегодняшний день различают два класса соединений, применяемых для местной профилактики и лечения артериальных заболеваний: "… гидрофобные лекарственные вещества, которые остаются внутри ткани и обладают сильным действием, и гидрофильные лекарственные вещества, которые быстро вымываются и являются неэффективными” (Levin AD, Vukmirovic N, Hwang C-W, Edelman ER. Specific binding to intracellular proteins determines arterial transport properties for rapamycin and paclitaxel. PNAS 2004; 101:9463-9467). В US 6306166 для покрытия выбрано очень хорошо растворимое в воде активное вещество. Например, показано, что покрытие стента не в достаточной степени липофильными веществами для профилактики рестеноза является неэффективным (Muni N. I. et al. Am Heart J 2005;149:415-433; Kiesz RS et al. Circulation 2001;103:26-31; Kutryk MJB et al. J Am Coll Cardiol 2002; 39:281-7). Huang Y и др. (Am J Cardiol.) сообщают о слабом ингибировании пролиферации неоинтимы в случае применения стентов, которые покрыты метатрексатом и которые медленно высвобождают из полимера активное вещество. Метатрексат сложно использовать для покрытия баллонов катетеров, поскольку указанное водорастворимое активное вещество быстро растворяется еще до достижения баллоном стеноза на кровеносном сосуде. Также описана эффективность триоксида мышьяка во время медленного высвобождения из полимерного матрикса (Yang W, Ge J, Liu H et al. Cardiovascular Research 2006; 72:483-493). Ограничение лекарственных веществ липофильными веществами нежелательным образом сокращает выбор с точки зрения эффективности, профиля действия и доступности. Было найдено, что приведенные ниже водорастворимые и слаболипофильные вещества являются очень эффективными лекарственными веществами. Неожиданно было обнаружено, что водорастворимые и/или гидрофильные активные вещества несмотря на полностью отличающиеся физико-химические и фармакологические характеристики при однократном кратковременном контакте с клетками способны оказывать такое же продолжительное действие, как и липофильные лекарственные вещества. Неожиданно отпала необходимость в компенсации быстрой растворимости этих веществ длительным высвобождением из резервуара, имплантированного на длительный срок.
В случае применения гидрофильных, как правило, хорошо растворимых в воде лекарственных веществ для введения с помощью покрытых медицинских изделий, в частности баллонных катетеров, возникают следующие требующие решения проблемы: хотя труднорастворимые вещества, такие как паклитаксел и рапамицин и их производные, при введении в сосуд, направлении катетера и в крови в значительной степени остаются прикрепленными на поверхности покрытых медицинских изделий и отделяются только во время механической нагрузки, например, при расширении баллона и его трении о стенки сосудов и, при необходимости, растворяются при наличии белков и мембранных липидов, гидрофильные вещества, как правило, растворяются при первом контакте с водой и/или кровью и большая их часть теряется по дороге еще до достижения цели. Следовательно, как правило, для гидрофильных активных веществ требуются меры защиты с тем, чтобы во время использования предотвратить их отделение в течение короткого промежутка времени, начиная с первого контакта стерильного покрытого медицинского изделия с водными растворами, например кровью, до момента достижения цели и при достижении цели. Эти меры не следует путать с композициями, которые вызывают замедленное высвобождение активного вещества в месте назначения для обеспечения продолжительного эффекта. Высвобождение гидрофильного, водорастворимого активного вещества должно быть немедленным при достижении медицинским изделием места воздействия, однако не раньше.
Неожиданным свойством обладает триоксид мышьяка несмотря на его гидрофильный характер. Он может быть нанесен на поверхность баллона в виде раствора, тем не менее прочно прикрепляется к мембране после высушивания и при расширении баллона практически полностью отделяется.
Проблемы, связанные с гидрофильными и/или водорастворимыми активными веществами, возникают с момента их нанесения на поверхность медицинских изделий. Многие из этих поверхностей, в частности обычный катетер, не могут быть смочены равномерно или вовсе не смачиваются водными или другими гидрофильными растворителями или смачиваются очень неравномерно. Другой существенной характеристикой является адгезия покрытия к поверхности медицинского изделия или, в частности, к мембране баллона. Неожиданно выяснилось, что на равномерность распределения покрытия и свойство адгезии хорошо влияет небольшая модификация поверхности. Так, поверхности, обработанные активированным кислородом ('плазмой'), дают не только равномерное распределение, но также, в частности, показывают хорошую адгезию покрытия на сложенной мембране и отделение его при расширении баллона. Аналогичные результаты получены с гидрофилизированными или покрытыми мембранами.
В качестве растворителей для слоя гидрофильных и/или водорастворимых активных веществ относительно пригодна только вода. Предпочтительным является смешиваемый с водой, относительно гидрофильный органический растворитель такой, как метанол, этанол, пропанол, изопропанол, диметилсульфоксид, ацетон, муравьиная кислота, уксусная кислота, аммиак, тетрагидрофуран, диметилацетамид и т.д., их смеси между собой и с водой, причем рН раствора можно регулировать с помощью кислоты или основания. Перед применением медицинских изделий растворители выпаривают насколько это возможно и необходимо и при необходимости при высокой температуре и повышенном давлении.
Гидрофильные и/или водорастворимые активные вещества могут растворяться в том виде, в каком они находятся, или в виде соли. Что касается антрациклинов, в частности доксорубицина, то он может быть приготовлен путем подбора соответствующим образом концентрации и концентрации ионов, в частности концентрации ионов натрия, и рН вязких растворов в воде (Hayakawa E, Furuya K, Kuroda T, Moriyama M, Kondo A. Viscosity study on the self-association of doxorubicin in aqueous solution. Chem. Pharm Bull 1991; 39:1282-1286), которые удивительно хорошо подходят для покрытия поверхностей. Хотя эти растворы могут содержать только воду в качестве растворителя, они могут обеспечивать равномерное покрытие, даже если мембраны являются более липофильными, как у традиционных баллонных катетеров.
Все вышеуказанные покрытия наносят обычными методами погружения, распыления, нанесения покрытия или с использованием волюметрического устройства предпочтительно вышеописанным способом с использованием волюметрического устройства. В случае баллонного катетера покрытие можно наносить на баллон в расширенном или сложенном состоянии или в промежуточном состоянии.
Другой вариант нанесения покрытия с гидрофильными и/или водорастворимыми веществами связан с тем фактом, что эти вещества не наносятся на поверхности в растворенном состоянии. Гидрофильные и/или водорастворимые вещества, например твердые вещества, могут содержаться в жидкости в виде микро- или наночастиц, при этом они могут быть малорастворимыми или могут осаждаться из раствора, в котором они растворены. Это позволяет применять липофильные органические растворители и добавлять липофильные адъюванты в комбинацию с гидрофильными и/или водорастворимыми веществами. Покрытие поверхности образованными частицами и возможность добавления липофильных адъювантов в липофильные растворители предотвращает преждевременное отделение покрытия.
Многие гидрофильные и/или водорастворимые вещества содержат функциональные группы, которые могут быть заряжены. Они могут быть растворимыми в электрически неизмененном состоянии в органических растворителях и в таком виде использоваться для покрытия. Они могут образовывать хорошо растворимые или труднорастворимые соли. Предпочтительным вариантом покрытия медицинских изделий является применение труднорастворимых солей гидрофильных и/или водорастворимых веществ. Это позволяет избежать отделения после контакта, например, с физиологическими растворами, такими как растворы, применяемые для смачивания катетера, или с кровью при введении в сосуд, направлении катетера или непосредственно в кровотоке. Эффективность лекарственного средства не снижается во время образования нерастворимых солей. Труднорастворимая соль после отделения от медицинского изделия неизмененного лекарственного вещества становится снова свободной, что является совершенно достаточным при чрезвычайно малом количестве лекарственного вещества, необходимом для хорошей эффективности при местном введении. Такой же принцип может быть использован для гидрофильных, водорастворимых адъювантов. Превращение в труднорастворимую соль формирует труднорастворимую матриксную структуру, которая защищает гидрофильные и/или водорастворимые активные вещества от преждевременного отделения в течение некоторого времени, например на время манипуляции, производимой с баллонным катетером, до, по сути, расширения сосуда.
Для применения гидрофильных и/или водорастворимых веществ можно получать их нерастворимые соли для нанесения на медицинские изделия и затем использовать в виде суспензий с подходящими жидкостями-носителями. Предпочтительным способом является покрытие медицинских изделий растворимой формой в водном растворе, или содержащем воду органическом растворителе, или относительно гидрофильном органическом растворителе, или смеси растворителей, выпаривание растворителя и последующая обработка покрытой поверхности осаждающим веществом для гидрофильных и/или водорастворимых веществ и, таким образом, последующее превращение их в нерастворимую соль или нерастворимую незаряженную форму. Осаждающее вещество может быть нанесено любым способом, например погружением, распылением, нанесением или с использованием волюметрического устройства.
Примерами физиологически приемлемых труднорастворимых в воде солей являются соединения кальция, магния, цинка и железа II или железа III, с одной стороны, и фосфаты, сульфаты, оксалаты или также соли ионных рентгеноконтрастных веществ, таких как диатризоат и т.д., с другой стороны.
Таким образом, настоящее изобретение также относится к применению по меньшей мере одного гидрофильного низкомолекулярного активного вещества в виде труднорастворимой в воде соли, или в виде труднорастворимой в воде кислоты, или в виде труднорастворимого в воде основания для лечения и профилактики больных сосудов и для достижения продолжительного эффекта после однократного введения при немедленной биодоступности.
В другом варианте осуществления согласно настоящему изобретению мембрану баллона на баллоне катетера покрывают по меньшей мере одним находящимся на открытой поверхности активным веществом способом, при котором при расширении баллона катетера упомянутое по меньшей мере одно активное вещество немедленно высвобождается, причем упомянутое по меньшей мере одно водорастворимое активное вещество представлено в виде труднорастворимой в воде соли, или труднорастворимой в воде кислоты, или труднорастворимого в воде основания, или труднорастворимого в воде комплексного соединения.
Аналогичный вариант осуществления по настоящему изобретению относится к мембране баллона на баллоне катетера с по меньшей мере одним находящимся на открытой поверхности активным веществом, которая покрыта таким способом, что при расширении баллона катетера упомянутое по меньшей мере одно активное вещество немедленно высвобождается, причем упомянутое по меньшей мере одно активное вещество после нанесения на мембрану баллона, или гидрофильную мембрану баллона, или гидрофильно покрытую мембрану баллона переходит в труднорастворимую в воде форму, в частности в труднорастворимую в воде соль, или труднорастворимую в воде кислоту, или труднорастворимое в воде основание, или труднорастворимое в воде комплексное соединение.
Отделение гидрофильных и/или водорастворимых активных веществ от медицинских изделий во время манипулирования, в частности, при введении в сосуд или направлении катетера к месту лечения также может происходить при нанесении дополнительного покрытия, содержащего мало или медленно растворимые в воде физиологически приемлемые вещества. При этом такие вещества могут иметь нужный фармакологический эффект или служить в качестве адъювантов. Слои могут быть твердыми или, как в случае некоторых липидов, также жидкими. Примерами твердых слоев являются сахар, сахарные спирты, другие органические нейтральные вещества, липофильные аминокислоты, соли органических и неорганических кислот и оснований, в медицине обычные контрастные вещества или красители, ингибиторы коагуляции, такие как гепарин, ингибитор агрегации тромбоцитов, такой как ацетилсалициловая кислота, салициловая кислота и многое другое. В отдельных случаях оценивают степень эффективности защиты покрытия специальным слоем. Защитные слои предпочтительно наносят, используя растворы в растворителях, в которых предназначенное для защиты покрытие не растворяется. Примером является ацетилсалициловая кислота (в качестве защитной оболочки), хорошо растворимая в этилацетате, в котором многие гидрофильные и/или водорастворимые активные вещества растворяются плохо.
Защитная оболочка должна быть тонкой, насколько это возможно. Предпочтительным является слой <30 мкг на 1 мм2 поверхности.
Защитные слои могут наноситься разными способами, причем предпочтительным является распыление и кратковременное погружение.
Таким образом, настоящее изобретение относится к дополнительному предпочтительному варианту осуществления баллонного катетера, который покрывают по меньшей мере одним гидрофильным активным веществом или композицией, содержащей по меньшей мере одно гидрофильное активное вещество, причем на этот слой наносят дополнительный внешний защитный слой в виде мало или медленно растворимых в воде биосовместимых материалов. Таким образом, предпочтительным является баллонный катетер, у которого по меньшей мере одно активное вещество или по меньшей мере одно гидрофильное активное вещество покрыто или пропитано мало или медленно растворимым в воде биосовместимым слоем. Защитный слой может проникать в слой активного вещества. Он может состоять, например, из биологически неэффективных веществ, а также из ацетилсалициловой кислоты или гепарина.
Примеры
Пример 1
Эксперименты № 102/103 и 128/129 по покрытию гидрофильных и негидрофильных катетеров паклитакселем
Раствор для покрытия: 30 мг паклитаксела/мл в растворе ацетона (89%), этанола (9%) и Ультравизите®-370 (Schering AG, Berlin) (2%) для 4 погружений с сушкой между ними:
Заключение: Баллоны с гидрофильной поверхностью являются воспроизводимыми для покрытия.
Пример 2
Нанесение покрытия с помощью микродозирующего устройства, сравнение с покрытием методом погружения
Во время первых серий экспериментов (эксперименты № 323 и 326-329) каждый из 3-х готовых к применению сложенных баллонов погружали по 4 раза в раствор A для покрытия с тщательным высушиванием баллонов между погружениями, либо дважды наносили активное вещество с постоянной скоростью с помощью поршневого шприца Hamilton по 12,5 мкл одного и того же раствора, либо наносили 3 дополнительный раствор для покрытия в летучих органических растворителях.
Дозирование с помощью шприца Hamilton выдавало значительно более точные дозы на баллон.
Также удалось соблюсти величину дозы для баллонов разной величины (эксперименты 390/391), при этом дозы были более точными, чем в случае нанесения покрытия методом погружения (392).
Распределение лекарственного вещества вдоль продольной оси баллона в этом примере исследовали на 3-х участках длиной 100 мм баллонов РТА, имеющих диаметр 5 мм. После нанесения покрытия либо дозированием с помощью шприца Hamilton (Фиг.1), либо методом погружения (Фиг.2) баллоны разрезали на кусочки длиной 10 мм. Содержание активного вещества на этих кусочках измеряли с помощью ВЭЖХ. На графиках линией 1 по оси Y обозначено среднее количество по всей длине, т.е. идеальное равномерное распределение.
Распределение вещества вдоль продольной оси баллона после нанесения дозированием не было менее равномерным, чем после погружения баллонов в раствор (см. Фиг.1 и 2).
Пример 3
Перенос баллона для нанесения предназначенного для покрытия раствора: предпочтительной является игла с узким просветом длиной 2-10 см, на проксимальном конце, соединенная с микродозирующим устройством, закрытая на дистальном конце. Игла имеет боковое отверстие в виде округлого надреза, которое подгоняется под скругление баллона (см. Фиг.3).
Пример 4
Покрытие баллонного катетера метатрексатом
Раствор для покрытия:
30 мг метатрексата+100 мкл бикарбоната натрия (7,5%)+900 мкл метанола (покрытие 2×16 мкл, соответствующее ~4 мкг/мм2 поверхности баллона)
Пример 5
Эффективность и совместимость покрытого баллонного катетера в примере 5 в растянутой коронарной артерии свиньи
Способ: Scheller B, Speck U, Abramjuk C, Bernhardt U, Böhm M, Nickenig G: Paclitaxel balloon coating - a novel method for prevention and therapy of restenosis. Circulation 2004; 110: 810-4.
Свиньям были имплантированы стенты с помощью баллонных катетеров, покрытых или непокрытых (контрольных) метатрексатом. После 4 недель с помощью количественной ангиографии определяли степень сужения просвета в районе стента.
n=9
n=8
Фраза “Последующее уменьшение просвета” означает, что в течение 4 недель в исходном диаметре просвета коронарной перфузируемой кровью артерии избыточный рост клеток в контрольной группе (без метатрексата) снизился на 2,64 и/или 2,41 мм - 1,1 мм, а в группе, обработанной метатрексатом, снизился на 0,67 мм. Следовательно, метатрексат значимо уменьшал нежелательную пролиферацию клеток стенки артерии в суженном просвете (p<0,025).
Пример 6
Покрытие баллонного катетера талидомидом
Falcon Bravo RX 3,5-20 мм, Invatec S.R.L., Roncadelle, Италия, 8 штук
Раствор для покрытия:
диметилформамид +50 мг/мл талидомид.
Каждый баллон покрывали 2 раза по 8 мкл, сушили после каждого нанесения покрытия по меньшей мере 12 часов.
Затем осуществляли кратковременное погружение 4 баллонов в 50 мг тримиристина в 3 мл нагретого этилацетата. Анализировали потери при введении в сосуд, направлении катетера и нахождении его в течение 1 мин в коронарной артерии свиньи (без расширения) и выемке. Анализ проводили с помощью ВЭЖХ, колонка Waters Symmetry, С18, 5 мкм, 25 см×4,6 мм, мобильная фаза: 72 об.% 0,01 М аммоний ацетатного буфера, рН 5,5, и из 28 об.% ацетонитрила, 0,8 мл/мин, детектирование при 300 нм.
За время продвижения в коронарной артерии и выемки баллоны, обработанные тримистатом, в среднем потеряли 28% активного вещества, не обработанные тримистатом баллоны потеряли 95%, т.е. покрытие тримистатом явно улучшает адгезию талидомида к баллону.
Пример 7
Баллонные катетеры, покрытые триоксидом мышьяка
Флакон Bravo RX 3,5-20 мм, Invatec S.R.L., Rocadelle, Италия, 12 штук
Раствор для нанесения покрытия:
50 мг AS2O3 растворяли в 1 мл воды с целью инъекции, раствор растворяли в 3 мл ацетона или метанола.
Покрытие каждого баллона осуществляли 3 раза 25 мкл, после каждого покрытия сушили по меньшей мере 12 часов.
Исследовали потерю при введении в сосуд, направлении катетера и нахождении в течение 1 мин в коронарной артерии свиньи (без расширения) и выемке и/или после расширения в коронарной артерии в течение 1 мин; анализ проводили после озоления методом атомно-абсорбционной спектрометрии.
За время продвижения в коронарной артерии и обратно баллоны потеряли в среднем 25% активного вещества, после расширения в артерии на баллонах осталось в среднем 13% дозы (в каждом случае n=4).
Пример 8а
Управление адгезией только с помощью растворителя (серия 1)
Флакон Bravo RX 3.5 - 20 мм, Invatec S.R.L., Rocadelle, Италия, 12 штук
Каждый баллон покрывали в сложенном состоянии 3-4 мкг/мм2 паклитаксела и тестировали в сухом состоянии, как при оценке потери активного вещества при расширении:
Ацетон 21%,
Диоксан 12%,
Диметилформамид 24%,
Диметилсульфоксид 66%,
Уксусная кислота 4%,
Изопропанол 19%,
Тетрагидрофуран 4%.
Пример 8b
Управление адгезией только с помощью добавления воды до предела растворимости воды в тетрагидрофуране (THF) при комнатной температуре (серия 2)
Тетрагидрофуран 3%,
Тетрагидрофуран с 10 об.% воды 3%,
Тетрагидрофуран с 20 об.% воды 16%,
Тетрагидрофуран с 37,5 об.% воды 37%.
Пример 9
Покрытие баллонного катетера с добавлением мочевины
Флакон Bravo RX 3,5-20 мм, Invatec S.R.L., Rocadelle, Италия, 8 штук
Раствор для покрытия:
70 мг мочевины растворяли в 1 мл воды+9 мл тетрагидрофурана +500 мг паклитаксела.
Баллон покрывали 1 раз единичной дозой (18 мкл), как описано в примере 2.
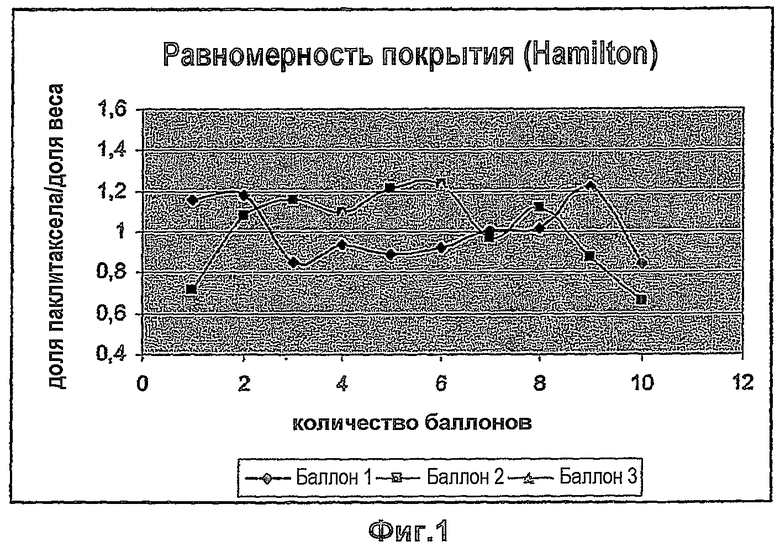
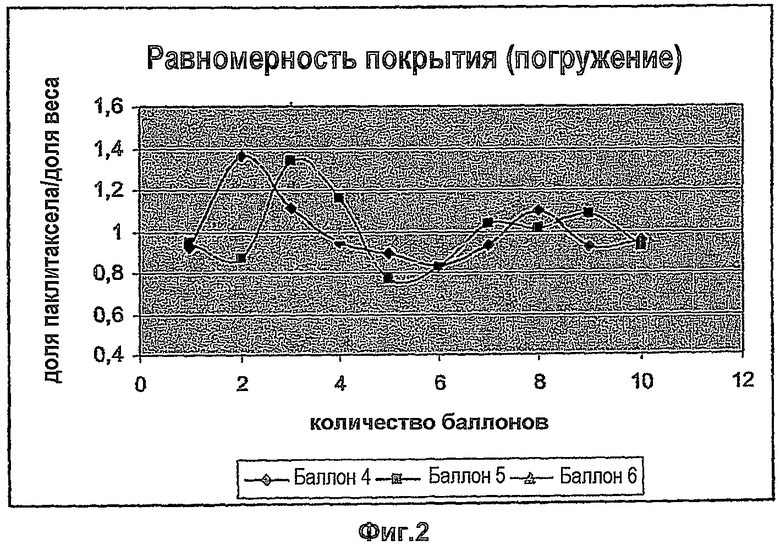
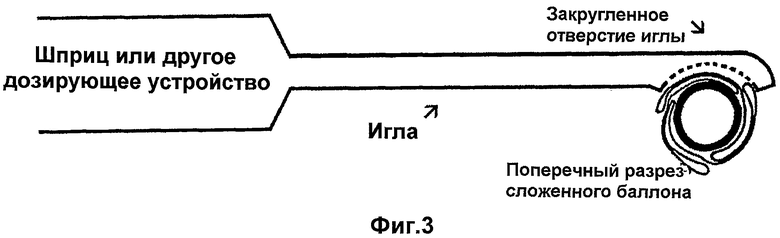
Изобретение относится к новой комбинации баллонного катетера и композиции активного вещества, прикрепленного к поверхности мембраны баллона. Изобретение также относится к способу нанесения покрытия для изготовления баллонного катетера и его использования для лечения и профилактики сосудистых заболеваний. Баллонный катетер не приводит к растяжению сосудов, прилегает мембраной к стенке сосудов только в тех местах, где она неравномерна, и только в эти места доставляют лекарственное вещество. 2 н. и 24 з.п. ф-лы, 3 ил., 4 табл., 9 пр.
1. Баллонный катетер, содержащий баллон катетера с гидрофильной или гидрофилизированной мембраной баллона, пригодной для контакта со стенкой сосуда, причем мембрана баллона покрыта, по меньшей мере, одним активным веществом совместно с, по меньшей мере, одним гидрофильным неактивным веществом, вещества лежат открыто на поверхности мембраны баллона, и причем, по меньшей мере, одно активное вещество немедленно высвобождается, когда баллон катетера расширен.
2. Баллонный катетер по п.1, в котором мембрана баллона баллона катетера обработана активированным кислородом.
3. Баллонный катетер по п.1 или 2, в котором баллон катетера дополнительно покрыт требуемыми неактивными веществами.
4. Баллонный катетер по п.1, причем когда баллон катетера полностью развернут помощью повышенного давления внутри баллона катетера, радиус баллона катетера увеличивается более чем на 15%.
5. Баллонный катетер по п.1, причем баллон катетера имеет давление разрыва ниже 10000 гПа.
6. Баллонный катетер по п.1, в котором баллон катетера имеет диаметр, который по меньшей мере на 20% больше референсного диаметра артерии.
7. Баллонный катетер по п.1, причем мембрана баллона или гидрофильная мембрана баллона или гидрофильно покрытая мембрана баллона баллона катетера покрыта по меньшей мере одним гидрофильным активным веществом или по меньшей мере одним гидрофильным активным веществом вместе с по меньшей мере одним гидрофильным неактивным веществом.
8. Баллонный катетер по п.1, причем мембрана баллона баллона катетера покрыта по меньшей мере одним активным веществом, причем упомянутое вещество лежит на поверхности мембраны баллона открыто, так, что по меньшей мере одно активное вещество при расширении баллона катетера немедленно высвобождается, причем по меньшей мере одно водорастворимое активное вещество представлено в виде труднорастворимой в воде соли, или труднорастворимой в воде кислоты, или труднорастворимого в воде основания, или труднорастворимого в воде комплексного соединения.
9. Баллонный катетер п.1, причем мембрана баллона баллона катетера покрыта по меньшей мере одним активным веществом, причем упомянутое вещество лежит на поверхности мембраны баллона открыто, так, что по меньшей мере одно активное вещество при расширении баллона катетера немедленно высвобождается, причем после нанесения, по меньшей мере, одного активного вещества на мембрану баллона или гидрофильную мембрану баллона или гидрофильно покрытую мембрану баллона, активное вещество переходит в труднорастворимую в воде форму.
10. Баллонный катетер п.1, причем мембрана баллона или гидрофильная мембрана баллона или гидрофильно покрытая мембрана баллона баллона катетера покрыта, по меньшей мере, одним гидрофильным активным веществом, которое находится в смеси с, по меньшей мере, одним малорастворимым в воде неактивным веществом.
11. Баллонный катетер по п.1, в котором, по меньшей мере, одно активное вещество или, по меньшей мере, одно гидрофильное активное вещество покрыто или пропитано мало или медленно растворимым в воде биосовместимым покрытием.
12. Баллонный катетер по п.1, в котором баллон катетера содержит требуемое защитное покрытие.
13. Баллонный катетер по п.1, причем баллон катетера покрыт композицией, содержащей, по меньшей мере, один легколетучий растворитель или по меньшей мере одно соединение хлора или соединение фтора с точкой кипения ниже 300°С.
14. Баллонный катетер по п.1, в котором баллон катетера покрыт гелем, причем, по меньшей мере, одно активное вещество само действует как гелеобразующее вещество или участвует в гелеобразовании.
15. Баллонный катетер по п.1, в котором смесь для покрытия содержит, по меньшей мере, один гидрофильный растворитель или смесь, по меньшей мере, одного гидрофильного растворителя с водой.
16. Баллонный катетер по п.1, причем мембрана баллона баллона катетера покрыта активным веществом, растворенным в органическом растворителе, содержащем по меньшей мере 1%, и затем высушена и стерилизована, и при этом активное вещество находится на мембране баллона в кристаллическом виде.
17. Баллонный катетер по п.1, причем баллон катетера с гладкостенной мембраной баллона покрыт активным веществом, растворенным в органическом растворителе, содержащем, по меньшей мере, 1% воды, и затем высушен и стерилизован, и при этом активное вещество находится на мембране баллона в кристаллическом виде.
18. Баллонный катетер по п.17, причем баллон катетера с гладкостенной мембраной баллона покрывают в сложенном состоянии.
19. Баллонный катетер по п.1, причем мембрана баллона баллона катетера является гладкостенной и покрыта кристаллами паклитаксела без добавки, упомянутое покрытие лежит открыто на поверхности мембраны баллона, таким образом, что при введении сложенного баллона в артерию по меньшей мере 70% паклитаксела продолжает прилегать, и немедленно высвобождается в зауженной артерии при расширении баллона катетера.
20. Баллонный катетер по любому из пп.15-19, причем органический растворитель содержит метанол, этанол, (изо)пропанол, ацетон, тетрагидрофуран, уксусную кислоту, диоксан или диметилформамид.
21. Баллонный катетер по п.1, в котором мембрана баллона баллона катетера покрыта, по меньшей мере, одним активным веществом, которое лежит открыто на поверхности мембраны баллона, и либо аскорбиновой кислотой, либо мочевиной, либо твердым при комнатной температуре триглициридом, таким как тримиристин, либо полиэтиленгликолем с молекулярной массой от 8000 до 20000 дальтон, либо любой требуемой их смесью.
22. Баллонный катетер по п.21, причем общая доза находящаяся на мембране баллона всех нелетучих компонентов ниже 10 мкг/мм2.
23. Баллонный катетер по п.1, содержащий метотрексиновую кислоту, мышьяк или соединения мышьяка, висмут или соединения висмута, или талидомид.
24. Баллонный катетер по п.1, подходящий для местного лечения или профилактики сосудистых заболеваний, и/или для лечения изменения стенок сосудов, которые существенно не ограничивают кровоток.
25. Способ покрытия баллонов катетера баллонного катетера, содержащий этапы, на которых:
а) подготавливают баллонный катетер, имеющий гидрофильную или гидрофилизированную мембрану баллона;
в) подготавливают микродозирующее устройство, содержащее смесь для покрытия, которая не находится в контакте с газовой фазой;
с) равномерно и без потерь покрывают баллон катетера смесью для покрытия, используя микродозирующее устройство.
26. Способ по п.25, причем во время покрытия баллон катетера вращают вокруг своей продольной оси и микродозирующее устройство движется туда и сюда вдоль продольной оси баллона катетера.
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| МИКРОДОЗИРУЮЩЕЕ УСТРОЙСТВО | 1995 |
|
RU2146220C1 |
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| ПОКРЫТЫЙ СТЕНТ, ПОДДАЮЩИЙСЯ РАСШИРЕНИЮ НАДУВНЫМ БАЛЛОНОМ, ВВОДИМЫМ В ПОЛОСТЬ ТРУБЧАТОГО ОРГАНА ТЕЛА, И СПОСОБ РАЗВЕРТЫВАНИЯ СТЕНТА | 1999 |
|
RU2214840C2 |
Авторы
Даты
2013-01-10—Публикация
2008-08-01—Подача