Настоящее изобретение относится к новому пути синтеза акрилонитрила из возобновляемого сырья, и более конкретно его объектом является способ синтеза акрилонитрила из глицерина.
Современное промышленное производство акрилонитрила основано главным образом на способе Sohio, предложенном в 1957 году. Этот способ заключается в каталитическом окислении пропилена в газообразной фазе воздухом в присутствии аммиака, реакция, известная под названием аммоксидирование. Реакция следующая:
CH2=CH-CH3+NH3=3/2O2→CH2=CH-CN+3H2O,
Реакцию проводят в реакторе с псевдоожиженным слоем при температуре главным образом от 400°C до 500°C и, предпочтительно, от 420°C до 450°C при использовании самых современных катализаторов под давлением, которое может составлять от 20 кПа до 300 кПа и обычно от 150 кПа до 300 кПа. Используют различные катализаторы, такие как комплексы на основе висмута, или молибдата висмута, или смешанных молибдатов железа и висмута, или антимоната железа, или фосфомолибдата или комбинаций сурьма-уран. Обычно оптимальный для данного способа катализатор имеет формулу (К,Cs)0,1(Ni,Mg,Mn)7,5(Fe,Cr)2,3Bi0,5Mo12Ox и носитель, содержащий 50 мас.% двуоксида кремния. Таким образом, можно получать примерно от 1 до 1,1 кг акрилонитрила на кг пропилена (см.: "Fundamentals of Industrial Catalytic Processes", C.H.Bartholomew, R.J.Farrauto, 2 Edition, Wiley Interscience, p.604-609). Этот способ тем не менее имеет ряд недостатков:
Акрилонитрил, полученный аммоксидированием пропилена, содержит примеси и побочные продукты, которые следует отделять и которые не всегда можно утилизировать. Основными побочными продуктами, в частности, являются циановодородная кислота (HCN), ацетонитрил (CH3CN) и оксиды углерода. Они получаются в результате разрыва связи C-C пропилена во время реакции аммоксидирования, проводимой при высокой температуре и в присутствии очень активных катализаторов. После экстрагирования и очистки циановодородную кислоту можно, например, использовать в способах синтеза метилметакрилата. Напротив, ацетонитрил с учетом ограниченных видов его применения обычно уничтожают. Таким образом, особый интерес представляет возможность использования другого сырья, которое по своей природе позволяет получать целевой продукт при помощи другого реакционного механизма с образованием меньшего количества побочных продуктов.
Реакция аммоксидирования пропилена является высоко экзотермической и, следовательно, ее проведение требует использования технологичного реактора, позволяющего эффективно выводить теплоту реакции, такого, например, как мультитрубчатые реакторы или псевдоожиженные слои. В связи с наличием высокого риска вспенивания, связанного с экзотермичностью реакции, используются разбавленные потоки, в частности, обычно используют смесь пропилен/воздух/аммиак, в которой пропилен составляет лишь несколько %. При такой конфигурации размер реактора зависит от общего количества газа в установке и, следовательно, является чрезмерным по отношению к количеству реагента пропилена, что приводит к увеличению в отношении реактора.
Стоимость установки, таким образом, пропорциональна количеству теплоты, которая должна обмениваться в ходе способа. Главная задача, таким образом, заключается в минимизации тепловых потерь путем уменьшения размера установок. Наибольшее преимущество заключается в том, чтобы получать акрилонитрил способом, обеспечивающим значительно более высокое частичное давление реагентов и продуктов, чем в традиционном способе аммоксидирования пропилена.
К тому же в современном способе аммоксидирования пропилена в качестве окислителя используют воздух, обеспечивая, таким образом, введение инертных газов (азота), необходимых для осуществления способа. В способе, в котором частичное давление реагентов является более высоким, становится возможным использование в качестве окислителя высоко концентрированного кислорода или воздуха, обогащенного кислородом. Воздух всегда рассматривается как бесплатный реагент, тогда как кислород покупают. Однако воздух для использования должен быть очищен и сжат, что требует не только вложений в компрессор, но и непостоянных затрат на электроэнергию, тогда как продаваемый кислород уже находится под давлением и имеет хорошее качество. Таким образом, использование кислорода может существенно сократить вложения в промышленную установку, а также, в некоторых случаях, расходы на эксплуатацию.
Из уровня техники известны другие пути синтеза акрилонитрила реакцией аммоксидирования, в частности, из альдегидов, более конкретно, из акролеина, из алкана, такого как пропан или из спиртов.
В патенте GB 709337 компании Distillers описан способ получения акрилонитрила путем аммоксидирования акролеина, используемого индивидуально или в смеси с соответствующим спиртом (аллиловый спирт) или соответствующим ацеталем. Предпочтительные катализаторы выбирают из катализаторов на основе молибдена, способных катализировать реакцию окисления бензола до малеинового ангидрида или нафталина до фталевого ангидрида. Получаемые выходы составляют от 25% до 60%.
В своем патенте на усовершенствование GB 897226 компания Distillers получает выход по акрилонитрилу более 70% по отношению к акролеину, используя в качестве катализаторов соединения на основе сурьмы, олова и кислорода. Реакцию можно осуществлять в присутствии инертного газа, такого как азот, водяной пар, углекислый газ или пропан, бутан или изобутан.
В патенте BE 628287 описан способ аммоксидирования акролеина, позволяющий получать выход по акрилонитрилу более 87% с использованием катализатора на основе мышьяка и значительного количества водяного пара в качестве разбавителя.
В патенте EP 558424 описан способ аммоксидирования пропана в присутствии катализатора, содержащего ванадий, сурьму и по меньшей мере один металл, выбираемый из железа, галлия или индия. Селективность по акрилонитрилу может достигать более 70%.
В патенте US 4138430 описано аммоксидирование н-пропанола. Реакцию проводят в присутствии кислорода и аммиака, пропуская газообразный поток последовательно по двум слоям катализатора: первый слой катализатора, состоящий из фосфата бора, двуоксида кремния-оксида алюминия, совместно осажденных, или оксида алюминия-оксида вольфрама, совместно осажденных, в котором происходит реакция дегидратации пропанола до олефина, и второй слой катализатора, в котором происходит реакция аммоксидирования олефина, состоящего из смешанных оксидов Fe, Co, Ni, Bi, P, Mo и K, смешанных оксидов Fe, Co, W, Bi, Mo и Mg, смешанных оксидов Sb и U, молибдата висмута или фосфомолибдата висмута, или смеси этих соединений. Обе стадии способа осуществляют при одинаковой температуре, либо при очень высокой температуре, выше 400°C. Преимущество способа заключается в сочетании эндотермической дегидратации и экзотермического аммоксидирования, что позволяет лучше контролировать температуру. Однако выход акрилонитрила не является очень высоким, и количество побочных продуктов, таких как ацетонитрил, пропионитрил и оксиды углерода, является очень существенным.
Таким образом, реакция аммоксидирования пропилена, альдегидов, таких как акролеин, кетонов или спиртов, таких как пропанол или изопропанол, являлась объектом ряда фундаментальных исследований для определения используемых реакционных механизмов или для изучения действия различных параметров, таких как природа катализатора или присутствие водяного пара в качестве разбавителя.
В частности, можно назвать статью Н.Oka et coll в J. Appl. Chem. Biotehnol (1975), 25, p.663-670, касающуюся аммоксидирования акролеина, в которой делается вывод о том, что эта реакция протекает в 1000 раз быстрее, чем аммоксидирование пропилена, предполагая, что реакция может происходить в химическом режиме при 400°C.
М.Cathala et J.E.Germain в Bull. Chem. Soc. №6, 1971, p.2167-2174 исследовали аммоксидирование акролеина при 460°C с использованием катализатора Bi-Mo-O, которое приводит к селективности по акронитрилу 87%. По мнению авторов, селективность реакции, в которой исходным реагентом является акролеин, выше, чем при использовании пропилена в качестве исходного реагента при тех же катализаторах.
В статье Bull. Soc. Chim. №3-4 (1975), p.731-734, J.E.Germain et coll. сравнивают аммоксидирование пропилена и акролеина с использованием катализатора типа Sn-Sb-Fe-O при температуре около 450°C с водяным паром или без него.
Аммоксидирование спиртов изопропанола и н-пропанола сравнивают в Bull. Soc. Chim. №5-6 (1979), р.173-178. Аммоксидирование изопропанола при 460°C на катализаторе Bi-Mo-O приводит к пропилену в качестве первичного продукта, который при продолжительном контакте дает CO+CO2, ацетонитрил и акрилонитрил. Однако селективность нитрилов очень отличается от селективности, имеющей место при аммоксидировании пропилена, так, максимальное превращение в акрилонитрил, исходя из изопропанола, составляет лишь 17%. При использовании катализатора Sn-Sb-O первичным продуктом является главным образом ацетон, который приводит в основном к ацетонитрилу. При том же катализаторе в случае аммоксидирования н-пропанола, первичным продуктом является н-пропанальдегид, а не ацетон. Существенная разница в этом случае заключается также в отсутствии пропилена. При превращении, близком к 100%, выход акрилонитрила составляет только 7,5%.
В настоящее время заявителем было неожиданно обнаружено, что можно получать акрилонитрил путем аммоксидирования возобновляемого сырья, такого как глицерин.
Глицерин получают в результате метанолиза растительных масел одновременно с метиловыми эфирами, которые используют, в частности, в качестве топлива или горючего в газойле или бытовом жидком топливе (D.Ballerini et G. Hillion, L'actualité chimique-nov-dec.2002-p.64-69). Это натуральный продукт, относящийся к «зеленым», он имеется в большом количестве и его можно хранить и транспортировать без проблем.
Способ получения акрилонитрила непосредственно из глицерина обладает, таким образом, особыми преимуществами, т.к. не зависит от ископаемого сырья, такого как пропилен, а использует возобновляемое сырье. Возобновляемым сырьем являются природные, животные или растительные ресурсы, запас которых может восстанавливаться в течение краткосрочного периода в человеческом масштабе. В частности, нужно, чтобы этот запас мог восстанавливаться также быстро, как расходуется.
Действительно в отличие от материалов, полученных из ископаемого сырья, материалы, полученные из возобновляемого сырья, содержат 14C. Все образцы углерода, полученные из живых организмов (животных или растений), представляют собой смесь трех изотопов: 12C (составляет около 98,892%), 13C (примерно 1,108%) и 14C (следы: 1,2×1012%). Отношение 14C/12C в живых тканях идентично тому же отношению в атмосфере. В окружающей среде 14C существует в двух преобладающих формах: в неорганической форме, т.е. в виде углекислого газа (CO2), и в органической форме, т.е. в виде углерода, интегрированного в органические молекулы.
В живом организме отношение 14C/12C поддерживается постоянным путем метаболизма, т.к. углерод постоянно обменивается с окружающей средой. Поскольку содержание 14C в атмосфере по существу является постоянным, тоже относится и к организму, пока он жив, т.к. он поглощает 14C, также как и 12C. Среднее отношение 14C/12C составляет 1,2×10-12.
12C является стабильным, т.е. число атомов 12C в образце является постоянным во времени. 14C является радиоактивным (каждый грамм углерода живого существа содержит достаточно изотопа 14C для получения 13,6 распадов в минуту) и число таких атомов в образце уменьшается во времени (t) по закону:
n-no exp(-at)
в котором:
- no обозначает исходное число 14C (после гибели животного или растения),
- n обозначает число атомов 14C, оставшихся по истечении времени t,
- 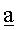 обозначает константу распада (или радиоактивную константу); она связана с периодом полураспада.
обозначает константу распада (или радиоактивную константу); она связана с периодом полураспада.
Период полураспада (или период) - это период времени, по истечении которого какое-либо число радиоактивных ядер или неустойчивых частиц данного вида сведено к половине в результате распада; период полураспада T1/2 связан с константой распада 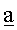 по формуле
по формуле 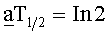 . Период полураспада 14C составляет 5730 лет.
. Период полураспада 14C составляет 5730 лет.
С учетом периода полураспада (T1/2) 14C, содержание 14C является по существу постоянным после экстракции растительного масла, из которого происходит глицерин, до получения акрилонитрила и даже до конца его использования.
Акрилонитрил, полученный из глицерина, состоит из 100% органического углерода, происходящего из возобновляемого сырья, т.е. он содержит порядка 10-10 мас.%. 14C по отношению к общей массе углерода, что может быть подтверждено путем определения содержания 14C одним из методов, описанных в стандарте ASTM D6866-06 или в стандарте ASTM D7026-04, в частности, методами масс-спектрометрии или жидкостной сцинтилляционной спектрометрии, описанными в стандарте ASTM D8866-06. Этими методами измеряют отношение 14C/12C образца и сравнивают его с отношением 14C/12C контрольного образца, имеющего 100% возобновляемое происхождение, для получения относительного процентного содержания С возобновляемого происхождения в образце.
Такой способ соответствует критериям, связанным с новой концепцией «зеленой химии» в более общих рамках долгосрочного развития.
Другое преимущество этого способа заключается в том, что он образует меньше примесей, поскольку механизм аммоксидирования отличается от механизма реакции аммоксидирования пропилена. К тому же, поскольку сырье глицерин является уже частично окисленным, его превращение в акрилонитрил является менее экзотермическим, чем аммоксидирование пропилена, и, следовательно, можно осуществлять синтез в реакторах, имеющих соответствующий размер, при высоких показателях частичного давления реагентов, ограничивая при этом риски, связанные с этим синтезом.
Цель настоящего изобретения заключается, таким образом, в том, чтобы ответить на проблемы долгосрочного развития, устраняя в то же время недостатки современных способов.
Таким образом, целью настоящего изобретения является способ получения акрилонитрила реакцией аммоксидирования глицерина в газообразной фазе.
Реакционный механизм является следующим:
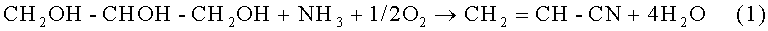
В соответствии с настоящим изобретением глицерин вводят во взаимодействие в газообразной фазе с аммиаком и кислородом в присутствии кислого катализатора в соответствии с одностадийным способом.
Глицерин используют в чистом виде или в виде концентрированного или разбавленного водного раствора. Преимущественно можно использовать водный раствор глицерина в концентрации от 10% до 100 мас.%. Концентрация не должна быть слишком высокой с тем, чтобы избежать побочных реакций, таких как образование простых эфиров глицерина, или реакций между полученным акрилонитрилом и глицерином. К тому же раствор глицерина не должен быть слишком разбавленным в связи с энергетическими затратами, вызванными испарением водного раствора глицерина. Количество водяного пара, выделяющегося из водного раствора глицерина, может изменяться в широких пределах, но для хорошего осуществления способа по изобретению содержание реакционного газа, определяемого как сумма глицерин-аммиак-кислород, составляет предпочтительно менее 2%, более конкретно, менее 4% в смеси, содержащей водяной пар и инертные газы, в том числе азот из воздуха, когда последний используют в качестве окислителя.
Можно использовать разбавляющие газы, инертные в реакционных условиях, такие как гелий, азот или аргон.
В составе реакционного газа соответствующие содержания глицерина, аммиака и кислорода могут изменяться в широких пределах.
Молярное отношение аммиак/глицерин может изменяться от 1 до 1,5 и, предпочтительно, от 1 до 1,2 и молярное отношение кислород/глицерин может изменяться от 0,5 до 10 и, предпочтительно, от 0,5 до 7.
Температура реакции обычно составляет от 280°C до 550°C и, предпочтительно, от 400°C до 500°C.
Общее давление реакционной смеси может быть больше или равно атмосферному давлению. Оно обычно составляет от 1 до 5 бар и предпочтительно от 1 до 4 бар.
Катализатор, используемый в способе аммоксидирования глицерина, является кислым катализатором, который не насыщен аммиаком при температуре реакции. Катализатор может содержать один или несколько смешанных оксидов, выбираемых, например, из молибдена, висмута, железа, олова, ванадия, вольфрама, сурьмы, циркония, титана, хрома, никеля, алюминия, фосфора, галлия.
Специалист может определить компромисс между температурой, расходом газа и точной природой используемого катализатора и другие различные параметры реакции для получения высокой продуктивности.
В соответствии со способом осуществления изобретения реакция протекает в одном реакторе, т.е. происходит прямое аммоксидирование глицерина, все элементарные стадии которого происходят в одном и том же реакторе. Можно использовать любое устройство, пригодное для реакций амоксидирования или окисления в парообразной фазе. Способ может осуществляться непрерывно или периодически с использованием неподвижного слоя, псевдоожиженного слоя, циркулирующего слоя, пластинчатого теплообменника с модульным расположением катализатора, микроструктурированного реактора или миллиструктурированного реактора.
В соответствии со способом осуществления изобретения глицерин предварительно подвергают стадии дегидратации акролеина, при этом механизм реакции включает в себя две следующие последовательные реакции:
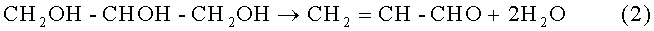
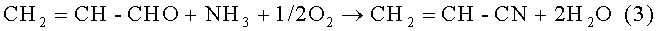
В этом случае реакцию осуществляют с использованием двух последовательных катализаторов, при этом первый кислый катализатор позволяет провести реакцию дегидратации глицерина до акролеина, а второй катализатор служит для аммоксидирования акролеина.
В этом варианте осуществления аммоксидирование акролеина преимущественно осуществляют без промежуточной очистки акролеина и, следовательно, в смеси с побочными продуктами, происходящими со стадии дегидратации глицерина, такими как ацетальдегид или пропанальдегид. Действительно, легкие альдегиды превращаются в нитрилы, предпочтительно ненасыщенные, одновременно на стадии аммоксидирования.
К тому же дегидратация глицерина стехиометрически продуцирует 2 молекулы воды. На самом деле, полученный акролеин естественно разбавляется в водяном паре, тем более, что глицерин разведен в воде. Когда вводят аммиак и кислород, необходимые для проведения реакции аммоксидирования, реакцию можно осуществлять в концентрированной среде реагента, оставаясь за пределами границ воспламеняемости. В этих условиях высококонцентрированной среды можно в целях экономии повторно использовать не вступившие в реакцию или недостаточно преобразованные реагенты.
В соответствии с частным вариантом осуществления изобретения обе стадии способа осуществляются при одной и той же температуре, предпочтительно от 400°C до 500°C.
В соответствии с другим вариантом осуществления обе стадии способа осуществляются при разных температурах, обеспечивая таким образом оптимизацию каждой из двух реакций в отношении эффективности используемого катализатора и ограничения количества побочных продуктов, таких как продукты разложения глицерина при высокой температуре.
Стадия разложения глицерина осуществляется в газообразной фазе в присутствии катализатора при температуре от 150°C до 500°C, предпочтительно, от 250°C до 350°C и под давлением от 1 до 5 бар.
Пригодными катализаторами являются гомогенные или многофазные вещества, нерастворимые в реакционной среде, которые обладают кислотностью по Гаммету, обозначаемой H0, меньше +2. Как указано в патенте US 5387720, в котором делается ссылка на статью К. Tanabe et al., в "Studies in Surface science and Catalysis", vol 51, 1989, chap 1 et 2, кислотность по Гаммету определяется титрованием амина при помощи индикаторов или путем адсорбции основания в газообразной фазе. Катализаторы, обладающие кислотностью H0, меньше +2, можно выбирать из природных или синтезированных силикатных материалов или кислых цеолитов; минеральных носителей, таких как оксиды, покрытые неорганическими кислотами, моно, ди, три или поликислотами; оксидов или смешанных оксидов или гетерополикислот.
Преимущественно, катализаторы выбирают из цеолитов, композитных материалов Nafion® (на основе сульфоновой кислоты фтористых полимеров), хлорированных оксидов алюминия, кислот и солей фосфовольфрамовых и/или силиковольфрамовых кислот и различных твердых веществ типа оксидов металлов, таких как оксид тантала Ta2O5, оксид ниобия Nb2O5, оксид алюминия Al2O3, оксид титана TiO2, двуоксид циркония ZrO2, оксид олова SnO2, двуоксида кремния SiO2 или силико-алюминат SiO2-Al2O3, пропитанных кислотными группами, такими как борат BO3, сульфат SO4, вольфрамат WO3, фосфат PO4, силикат SiO2 или молибдат MoO3. Согласно информации, приведенной в литературе, все эти катализаторы имеют кислотность по Гаммету H0 меньше +2.
Предпочтительными катализаторами являются сульфатированные двуоксиды циркония, фосфатированные двуоксиды циркония, вольфрамированные двуоксиды циркония, кремнийсодержащие двуоксиды циркония, сульфатированные оксиды титана или олова, фосфатированные двуоксиды алюминия или оксиды кремния.
Все эти катализаторы имеют кислотность по Гаммету H0 меньше +2, кислотность Но может варьироваться в широких пределах до значений, которые могут достигать -20 по контрольной шкале показателей Гаммета. Таблица, приведенная на стр.71 публикации, касающейся кислотно-щелочного катализа (С.Marcilly), Том 1 в Editions Technip (№ISBN 2-7108-0841-2), иллюстрирует примеры твердых катализаторов в этом диапазоне кислотности.
Можно вводить молекулярный кислород или газ, содержащий молекулярный кислород на стадии дегидратации глицерина. Количество кислорода предпочтительно выбирают так, чтобы в любой точке установки быть вне области воспламенения. Присутствие кислорода позволяет ограничить дезактивацию катализатора дегидратации путем коксования. К тому же введение кислорода повышает выход реакции при использовании ряда каталитических систем.
Предпочтительно, аммиак вводится только на второй стадии.
Затем осуществляют стадию аммоксидирования акролеина в акрилонитрил на катализаторе аммоксидирования при температуре, главным образом составляющей от 300°C до 550°C и, предпочтительно, от 400°C до 500°C, и под давлением, главным образом, от 1 до 5 бар и, предпочтительно, от 1 до 4 бар.
Состав реакционной смеси акролеин-аммиак-кислород, может изменяться в широких пределах и можно и30спользовать газообразные разбавители, инертные в реакционный условиях, такие как гелий, азот или аргон или азот воздуха, если последний используют в качестве окислителя.
Молярные отношения аммиак/акролеин и кислород/акролеин могут изменяться в широких пределах. Молярное отношение аммиак/акролеин может составлять от 1 до 1,5 и, предпочтительно, от 1 до 1,2, а молярное отношение кислород/акролеин может составлять от 0,5 до 10 и, предпочтительно, от 0,5 до 7.
В качестве катализатора аммоксидирования акролеина используют кислый катализатор, который не насыщен аммиаком при температуре реакции. Катализатор может содержать один или несколько смешанных оксидов, выбираемых, например, из молибдена, висмута, железа, сурьмы, олова, ванадия, вольфрама, сурьмы, циркония, титана, хрома, никеля, алюминия, фосфора, галлия.
В качестве катализаторов аммоксидирования, которые можно использовать, можно назвать, в частности, смешанные оксиды на основе молибдата висмута, смешанные оксиды, содержащие по меньшей мере Fe и Sb, или по меньшей мере U и Sb, или по меньшей мере Sn и Sb, или по меньшей мере Mo и V, и/или W/Nb/Ti/Ta, и/или Te/Sb/Bi, а также оксинитриды, содержащие по меньшей мере Al и P.
Преимущество этого способа осуществления заключается в наилучшем выборе пары катализаторов. Действительно, реакция дегидратации требует кислых катализаторов, которые могут ингибироваться в присутствии аммиака, если они являются слишком кислыми. Разделение двух стадий позволяет индивидуально оптимизировать условия протекания каждой из двух реакций дегидратации и аммоксидирования.
В соответствии с другим предпочтительным вариантом осуществления изобретения, который иллюстрирует в качестве примера прилагаемая фигура, глицерин предварительно проходит стадию дегидратации акролеина, и промежуточно проводят частичную конденсацию воды и тяжелых побочных продуктов стадии дегидратации.
Использование предварительной стадии дегидратации глицерина, применяемого в виде водного раствора, имеет недостаток, заключающийся в образовании потока, содержащего не только полученный акролеин и побочные продукты, но и значительное количество воды, происходящей, с одной стороны, из раствора глицерина, а, с другой стороны, воды, полученной в ходе реакции дегидратации.
Цель стадии частичной конденсации заключается в конденсации части воды и продуктов, точка кипения которых выше, чем акролеина. Таким образом речь идет об упрощенном разделении, образующем два потока, при этом первый содержит акролеин и легкие побочные продукты, такие как ацетальдегид, пропанальдегид, ацетон и возможно инертные газы, CO и CO2, а второй, богатый водой, содержит тяжелые побочные продукты, такие как фенол, гидроксипропанон и продукты присоединения акролеина с глицерином (ацетали), продукты поликонденсации глицерина, циклические или нециклические простые эфиры глицерина, пропионовую кислоту, акриловую кислоту.
Установка для частичной конденсации может представлять собой абсорбционную колонну, соединенную или несоединенную с десорбционной секцией, теплообменником, конденсатором, дефлегматором, а также с любым устройством, хорошо известным специалисту, позволяющим осуществлять частичную конденсацию водного потока. Эту установку к тому же можно использовать для нагревания водного раствора глицерина, оптимизируя таким образом энергетические затраты установки.
После промежуточной стадии конденсации поток, богатый акролеином, направляется на катализатор аммоксидирования, с добавлением аммиака, необходимого для проведения реакции, и с регулировкой частичного давления реагентов акролеина и кислорода и, возможно, с разбавлением реакционного газа инертным газом.
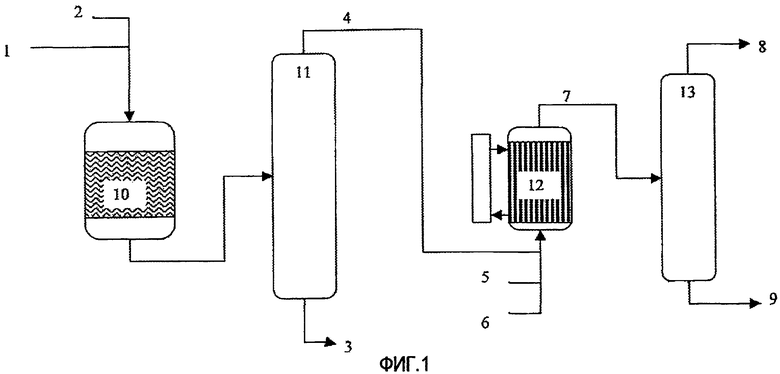
На фиг.1 глицерин в виде водного раствора вводят через (1) в первый реактор (10) дегидратации. Молекулярный кислород (2) также вводят, например, в виде воздуха или воздуха, обогащенного или обедненного молекулярным кислородом. Реакцию дегидратации проводят в газообразной фазе в реакторе (10) в присутствии катализатора дегидратации при температуре от 250°C до 350°C и под давлением от 1 до 5 бар.
На выходе из реактора (10) поток газа состоит из смеси, содержащей акролеин, воду, не превращенный глицерин и побочные продукты. Побочными продуктами, в частности, являются гидроксипропанон, пропанальдегид, ацетальдегид, ацетон, фенол, продукты присоединения акролеина с глицерином, продукты поликонденсации глицерина, циклические или нециклические простые эфиры глицерина.
Этот поток направляют в конденсационную установку (11), которая разделяет, с одной стороны, смесь (3), богатую водой, содержащую тяжелые побочные продукты, и, с другой стороны, поток (4), богатый акролеином, содержащий легкие побочные продукты, такие как ацетальдегид, пропанальдегид, ацетон и, возможно, инертные газы, CO и CO2.
Поток (3) полностью или частично направляют в ректификационную колонну для извлечения легкой фракции, которая может быть абсорбирована этим потоком, или на станцию обработки сточных вод. Его также можно направить в устройство для теплового окисления или часть этого потока можно возвратить для разбавления глицерина до требуемой концентрации.
Поток (4), богатый акролеином и очищенный от тяжелых побочных продуктов и большей части воды, направляют в реактор аммоксидирования (12), содержащий неподвижный слой катализатора аммоксидирования акролеина.
Реакцию проводят в присутствии молекулярного кислорода (6), который может быть в виде воздуха или воздуха, обогащенного или разбавленного молекулярным кислородом, в количестве от 3 до 20 объемных % по отношению к входящему потоку и в присутствии смеси газов (5), содержащей инертные газы и аммиак. Инертные газы, необходимые для осуществления способа, необязательно могут состоять полностью или частично из газа (8), полученного в верхней части абсорбционной колонны (13).
Реакцию аммоксидирования проводят при температуре от 400°C до 500°C и под давлением от 1 до 5 бар.
Газообразные отходы (7), выходящие со стадии аммоксидирования, богатые акролеином, затем очищают в разделительной установке (13) для отделения, с одной стороны, легких продуктов (8) и не преобразованного акролеина, и, с другой стороны, акрилонитрила (9), который еще может содержать следы тяжелых побочных продуктов.
В соответствии с другим вариантом осуществления изобретения, реакцию аммоксидирования глицерина проводят в присутствии газа, содержащего пропилен. Газ, содержащий пропилен, может подаваться вместе с глицерином или может подаваться после реакции дегидратации глицерина.
В соответствии с другим вариантом осуществления изобретения, реакцию аммоксидирования глицерина проводят в присутствии теплового балласта, такого, например, как пропан или газ, содержащий пропан, метан, этан или CO2.
Тепловой балласт представляет собой газообразный теплоноситель, который может служить для доставки тепла, необходимого для реакции дегидратации, а также для вывода тепла, выделяемого в ходе реакции аммоксидирования. Тепловой балласт можно вводить вместе с глицерином или, если стадии дегидратации и аммоксидирования проводят раздельно, его можно вводить между этими стадиями. Тепловой балласт, такой как пропан, возможно, рекуперируют и используют повторно.
Продукты реакции можно рекуперировать из газообразных отходов любым пригодным средством. Например, газообразные отходы могут проходить через конденсатор, содержащий разведенную серную кислоту для нейтрализации не превращенного аммиака. Газы могут затем проходить через охлаждаемую абсорбционную колонну для конденсации акрилонитрила, ацетонитрила и цианистоводородной кислоты. Затем можно выделить из побочных продуктов акрилонитрил путем последующей дистилляции.
Способом по изобретению можно получать акрилонитрил высокой степени очистки с высокой производительностью, уменьшив при этом зависимость от ископаемых ресурсов, таких как пропилен. Акрилонитрил, который можно получать этим способом, содержит 14C, преимущественно, акрилонитрил содержит больше 10-11% 14C по отношению к общему количеству углерода, что можно подтвердить измерением одним из методов, описанных в стандарте ASTM D6866-06.
Акрилонитрил, который можно получить способом по изобретению, используют для получения, в частности, адипонитрила, предшественника нейлона, синтетических полимеров, таких как акриловые волокна, синтетического каучука, эластомеров или смол, таких как сополимеры акрилонитрила, бутадиена и стирола (смолы ABS) или сополимеры стирола и акрилонитрила (смолы SAN). Полученные таким образом продукты содержат органический углерод, происходящий из возобновляемого источника, соответствующего концепции зеленой химии.
Нижеследующие примеры иллюстрируют настоящее изобретение, не ограничивая тем не менее его объем.
ПРИМЕРЫ
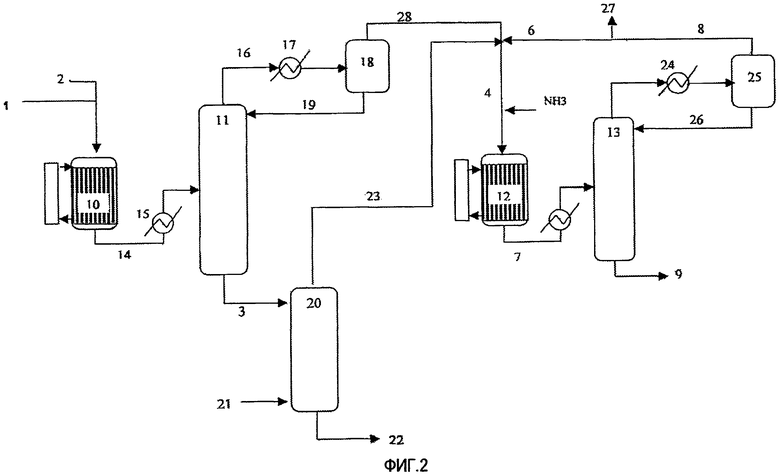
Пример 1 (со ссылкой на фиг.2)
Для иллюстрации способа по изобретению использовали моделирование при помощи программы ASPEN. Величины выражены в кмоль/час. Для ясности указаны только основные компоненты.
Газообразный поток при 331°C под 2,0 барами (188 кмоль/час глицерина, 963 кмоль/час воды, 426 кмоль/час азота, 113 кмоль/час кислорода) вводят в мультитрубчатый реактор с неподвижным слоем (10), содержащим гетерогенный катализатор дегидратации в сочетании с расплавом соли. Из этого реактора выходит газообразный поток (14) при 320°C под давлением 1,7 бар (1336 кмоль/час воды, 426 кмоль/час азота, 78 кмоль/час кислорода, 147 кмоль/час акролеина, 19 кмоль/час ацетальдегида, 25 кмоль/час CO, 13 кмоль/час CO2). Этот поток охлаждают до 151°C в теплообменнике (15) и направляют в основание абсорбционной колонны (11), которая теоретически содержит 4 уровня. Газообразный поток (16), выходящий при 102°C из верхней части этой абсорбционной колонны, направляют в частичный конденсатор (17), который охлаждает его до 79°C, затем в испарительную камеру (18), служащую для отделения газообразной фазы (28) от жидкой фазы (19). Эту жидкую фазу (19) направляют обратно в верхнюю часть абсорбционной колонны (11). Из основания абсорбционной колонны извлекают жидкую фазу (3) при 103°C (1067 кмоль/час воды, 4 кмоль/час уксусной кислоты, 4 кмоль/час муравьиной кислоты). Эту жидкую фазу (3) направляют в верхнюю часть десорбционной колонны (20), содержащей 8 пластин, в основание которой вводят воздух (21) при 90°C под давлением 1,7 бара. Из основания этой десорбционной колонны извлекают водный поток (22) (55°C, 976 кмоль/час воды, 4 кмоль/час уксусной кислоты, 4 кмоль/час муравьиной кислоты). Газообразный поток (23), рекуперируемый в верхней части десорбционной колонны, смешивают с газообразной фазой (24) из описанной выше испарительной камеры (79°C, 426 кмоль/час N2, 145 кмоль/час акролеина, 78 кмоль/час кислорода, 270 кмоль/час воды, 18 кмоль/час ацетальдегида, 25 кмоль/час моноксида углерода, 13 кмоль/час диоксида углерода) и газообразной фазой (6) (923 кмоль/час азота, 38 кмоль/час кислорода, 134 кмоль/час воды, 41 кмоль/час диоксида углерода, 53 кмоль/час моноксида углерода), к которой добавляют поток аммиака (178 кмоль/час). Смесь нагревают до 300°C, затем вводят во второй мультитрубчатый реактор (12), содержащий катализатор аммоксидирования. На выходе из этого реактора получают газообразный поток (7) под давлением 1,4 бара (2030 кмоль/час азота, 830 кмоль/час воды, 118 кмоль/час акрилонитрила, 52 кмоль/час кислорода, 155 кмоль/час диоксида углерода, 85 кмоль/час моноксида кислорода). Этот поток охлаждают до 157°C, затем вводят в основание абсорбционной колонны (13). В верхней части этой колонны газообразный поток частично конденсируется в теплообменнике (24), затем направляется в разделительную камеру (25), в которой получают жидкую фазу (26) и газообразную фазу (8) (азот, кислород, вода, диоксид углерода, моноксид углерода). Жидкую фазу (26) повторно направляют в колонну (13). Газообразную фазу (8) частично направляют в верхнюю часть реактора (12) через поток (6). В основании абсорбционной колонны (13) получают поток с высокой концентрацией акрилонитрила (9) (116 кмоль/час акрилонитрила, 587 кмоль/час воды и другие побочные продукты).
Следует отметить, что способ позволяет устранить из водной фазы (22) некоторые примеси, образовавшиеся в реакторе дегидратации (10): например, расход гидроксипропанона и уксусной кислоты в газообразном потоке, выходящем из реактора дегидратации (10), составляют соответственно 1 и 4 кмоль/час. На входе в реактор окисления (12) они соответственно составляют 0,02 и 0,3 кмоль/час.
В нижеследующих примерах превращение глицерина, селективность по акролеину и выходы различных продуктов определяют следующим образом:
Превращение глицерина (%) = 100-число оставшихся молей глицерина/число введенных молей глицерина.
Выход акролеина (%) = число полученных молей глицерина/число введенных молей глицерина.
Селективность по акролеину (%) = 100*число полученных молей глицерина/число молей глицерина, вступивших в реакцию.
Выход ацетона или гидроксипропанона вычисляют также, как и выход акролеина.
Выход ацетальдегида (%) = 2/3*число полученных молей ацетальдегида/число введенных молей глицерина.
Выход фенола (%) = 2*число полученных молей фенола/число введенных молей глицерина.
Все результаты выражены в молярных процентах по отношению к вводимому глицерину.
Пример 2: Получение акролеина
Используют трубчатый реактор, состоящий из трубы длиной 35 см, имеющей внутренний диаметр 22 мм для проведения реакции дегидратации глицерина в газообразной фазе при атмосферном давлении. Этот реактор помещают в нагреваемую камеру, температура в которой поддерживается на уровне температуры проведения реакции, которая составляет 300°C, если нет других инструкций. Используемый катализатор измельчают и/или таблетируют для получения частиц размером от 0,5 до 1,0 мм. В реактор загружают 10 мл катализатора для образования каталитического слоя длиной 5 см. Последний доводят до температуры реакции в течение 5-10 минут до ввода реагентов. В реактор подают водный раствор, содержащий 20 мас.% глицерина со средним расходом подачи 12 мл/час и с расходом 0,8 л/час молекулярного кислорода в примерах изобретения. В этом случае относительное содержание O2/превращенный в пар глицерин/водяной пар составляет 6/4,5/89,5. Водный раствор глицерина выпаривают в нагреваемой камере, затем пропускают через катализатор. Вычисляемая продолжительность контакта составляет порядка 2,9 сек. По окончании реакции продукты конденсируют в ловушке, охлаждаемой измельченным льдом.
Общая масса продуктов на входе и на выходе измеряется, что позволяет подвести материальный баланс. Также образовавшиеся продукты анализируют хроматографией.
Продуктами, количественный анализ которых таким образом проведен, являются не вступивший во взаимодействие глицерин, образовавшийся акролеин и побочные продукты, такие как гидроксипропанон, ацетальдегид, пропанальдегид, ацетон и фенол.
В этом примере тестируемым катализатором (10 мл) является вольфрамсодержащий двуоксид циркония (90,7% ZrO2 - 9,3% WO3) фирмы Daiichi Kigenso (поставщик обозначен Н1417). Катализатор характеризуется потерей 1,75% при горении при 1000°C и удельной поверхностью 47,4 м2/г (BET, 1 пункт). Результаты приведены в следующей таблице:
Полученный акролеин не содержит ни гидроксипропанона, ни фенола.
Пример 3: Синтез акрилонитрила
В реактор из пирекса вводят слой катализатора. Для удержания катализатора реактор снабжен фриттой. Сначала загружают катализатор окисления пропилена до акролеина массой 6,578 г, выпускаемый Nippon Shokubai под номером ACF4, используемый в этом примере в качестве катализатора аммоксидирования, хотя он не оптимизирован для этой реакции, разведенный 7 мл карбида кремния с гранулометрическим составом 0,125 мм. Затем вводят слои 2 мл карбида кремния с гранулометрическим составом 0,125 мм, затем 7 мл с гранулометрическим составом 0,5 мм. И, наконец, реактор до верха загружают карбидом кремния с гранулометрическим составом 1,19 мм.
После этого реактор присоединяют к установке для проведения испытания. Температура катализатора устанавливается 420°C, и VVH устанавливают 1200 час-1.
В реактор подают газообразную смесь, содержащую 4,5% акролеина/8,7% кислорода/5,4% аммиака/(остаток)гелий-криптон/15% воды. Газообразная смесь гелий/криптон содержит 4,92% криптона, который служит внутренним эталоном. Используют смесь вода-акролеин из примера 2, превращенную в пар в верхней части реактора после концентрации.
Газообразные отходы собирают на выходе из реактора в ловушку, охлаждаемую льдом, а количественный анализ полученного акрилонитрила определяют хроматографией. Выход акрилонитрила составляет 60%.
Изобретение относится к способу получения акрилонитрила из глицерина. Способ включает первую стадию дегидратации глицерина в газовой фазе в присутствии катализатора, который обладает кислотностью по Гаммету, обозначаемой H0, меньше +2, при температуре от 150°C до 500°C и под давлением от 1 до 5 бар, с получением акролеина; вторую стадию аммоксидирования акролеина на катализаторе аммоксидирования при температуре от 300°C до 550°C и под давлением от 1 до 5 бар, с получением акрилонитрила; и промежуточную стадию частичной конденсации воды и тяжелых побочных продуктов, полученных на стадии дегидратации. Изобретение относится также к акрилонитрилу, содержащему 14C порядка 10-10 мас.% по отношению к общей массе углерода, который можно получать указанным выше способом. Предлагаемый способ позволяет оптимизировать стадию аммоксидирования акролеина путем уменьшения количества воды и примесей в потоке, обогащенном акролеином. 2 н. и 1 з.п. ф-лы, 2 ил., 1 табл., 3 пр.
1. Способ получения акрилонитрила из глицерина, включающий:
первую стадию дегидратации глицерина в газовой фазе в присутствии катализатора, который обладает кислотностью по Гаммету, обозначаемой H0, меньше +2, при температуре от 150°C до 500°C и под давлением от 1 до 5 бар, с получением акролеина, и
вторую стадию аммоксидирования акролеина на катализаторе аммоксидирования при температуре от 300°C до 550°C и под давлением от 1 до 5 бар с получением акрилонитрила, и
промежуточную стадию частичной конденсации воды и тяжелых побочных продуктов, полученных на стадии дегидратации.
2. Способ по п.1, отличающийся тем, что используют глицерин в виде водного раствора с концентрацией от 10% до 100%.
3. Акрилонитрил, который можно получать способом по любому из предшествующих пунктов, отличающийся тем, что содержит 14C порядка 10-10 мас.% по отношению к общей массе углерода.
| Е.LEETE et al | |||
| Biosynthesis of Shihunine in Dendrobium pierardii, J | |||
| AMER | |||
| CHEM | |||
| SOC, 1976, vol | |||
| Дорожная спиртовая кухня | 1918 |
|
SU98A1 |
| Инструмент для отделочной обработки криволинейных поверхностей | 1978 |
|
SU709337A2 |
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| US 5387720 A, 07.02.1995 | |||
| СПОСОБ ПАРОФАЗНОГО АММОКСИДИРОВАНИЯ С - С-МОНООЛЕФИНОВ | 1993 |
|
RU2105757C1 |
Авторы
Даты
2013-01-10—Публикация
2008-02-18—Подача