Изобретение относится к медицине, а именно к неврологии, и может быть использовано для выявления аутоиммунного поражения парасимпатического отдела вегетативной нервной системы на ганглионарном уровне.
Известные клинические (дермографизм, пупиллометрия, пиломоторный рефлекс, динамика артериального давления и частоты сердечных сокращений в орто-, клиностатических и рефлекторных пробах с вычислением разнообразных коэффициентов и т.д.) и электрофизиологические (измерение R-R интервала при различных нагрузках, оценка кожно-гальванического рефлекса и др.) способы исследования позволяют установить преобладание симпатического или парасимпатического отдела вегетативной нервной системы (ВНС) при различных патологических состояниях. Способы оценки состояния ВНС с проведением фармакологических проб (адрено- и холиноактивные средства) выявляют наличие вегетативной дисфункции и в ряде случаев локализуют уровень ее поражения, но введение этих (в основном - сильнодействующих группы А) препаратов связано с риском развития выраженных побочных эффектов, особенно у пациентов с органическим поражением жизненно важных структур периферического отдела ВНС (Методы исследования вегетативной нервной системы. В кн. Вегетативные расстройства. Клиника, диагностика, лечение. Под ред. А.М.Вейна. - М.: ООО «Медицинское информационное агентство», 2003, с.44-102). Однако эти методы не позволяют установить причину и уровень поражения ВНС.
Наиболее близким к изобретению является способ диагностики аутоиммунного поражения периферического отдела ВНС путем определения антител к ганглионарной субъединице α3-ацетилхолинового рецептора (α3-АХР) методом радиоиммунопреципитации, где в качестве антигена использовался рецептор, выделенный из культуры клеток нейробластомы и связанный с эпибатидином, меченным изотопом 1-125 (Vemino S., Low P.A., Fealey R.D., Stewart J.D., Farrugia G., Lennon V.A.. Autoantibodies to ganglionic acetylcholine receptors in autoimmune autonomic neuropathies., N. Engl. J. Med., 2000, 343, 847-855).
Данный способ позволяет произвести определение антител в сыворотке крови, установить уровень поражения ВНС, однако он наряду с высокой специфичностью трудоемок в исполнении, так как предполагает работу с радиоактивными изотопами, требует специального оборудования и помещений, является более дорогостоящим.
Предлагаемые нами варианты способов являются более дешевыми и безопасными для определения антител в сыворотке крови по взаимодействию с экстрацеллюлярным доменом α3-АХР методом твердофазного иммуноферментного анализа и Вестерн-Блотинга. Кроме того, данные способы позволяют при той же специфичности более простым и экономичным путем (в частности не требующим мер защиты от радиации) осуществить диагностику аутоиммунного поражения периферического отдела ВНС при нервных и нервно-мышечных заболеваниях.
Это в свою очередь позволяет назначить адекватную терапию пациентам не только неврологических, но и кардиологических, гастроэнтерологических, урологических и офтальмологических клиник.
Указанный технический результат достигается тем, что для диагностики аутоиммунного поражения периферического отдела ВНС проводят в первом случае определение наличия в сыворотке крови антител к α3-АХР, при этом антитела к α3-АХР определяют экспресс-методом Вестерн-Блотинга в сыворотке крови по взаимодействию с экстрацеллюлярным участком α3-субъединицы нейронального АХР, а наличие антител к α3-АХР определяют окрашиванием, используя в качестве хромогена тетраметилбензидин преципитирующий. А во втором случае для диагностики аутоиммунного поражения периферического парасимпатического отдела вегетативной нервной системы проводят определение в сыворотке крови антител к α3-АХР, причем, антитела к α3-АХР определяют методом тИФА в образце сыворотки крови по взаимодействию с экстрацеллюлярным участком α3-субъединицы нейронального АХР, уровень антител к α3-АХР определяют окрашиванием, используя в качестве хромогена тетраметилбензидин, оптическое поглощение света измеряют на ИФА-анализаторе при длине волны 450 нм в единицах оптической плотности (OD) и при повышении уровня антител к α3-АХР более 0,24 OD450HM, относительно контроля диагностируют аутоиммунное поражение периферического отдела ВНС на уровне парасимпатических ганглиев.
Способ осуществляют следующим образом.
Для экспресс-метода Вестерн-Блотинга и тИФА пациенту производят забор крови из кубитальной вены, затем отделяют сыворотку от кровяного сгустка путем центрифугирования в течение 15 минут при 3000 об/мин. Сыворотку тестировали на наличие антител к α3-АХР в ИФА.
В качестве антигена для определения аутоантител методом тИФА использовался экстрацеллюлярный участок α3-субъединицы нейронального АХР, полученный в лаборатории готовых лекарственных форм Центра «Биоинженерия» РАН.
Методом Вестерн-Блотинга было выявлено наличие антител в сыворотке крови больной с аутоиммунной вегетативной ганглиопатией по взаимодействию с экстрацеллюлярным доменом α3-субъединицы нейронального АХР. В качестве контроля была исследована сыворотка крови здорового донора. Вестерн-Блотинг сыворотки крови больного и здорового донора проводили по следующей схеме: нитроцеллюлозную мембрану после электрофореза и электропереноса, содержащую экстрацелюллярный участок α3-субъединицы АХР, инкубировали с сывороткой крови в разведении (1:100) 60 минут при 37°С, с последующим 3-кратным отмыванием (0,2% BSA в PBS/Твин-20) в течение 3-х минут.Затем мембрана была инкубирована с коньюгатом пероксидазы с анти- IgG человека (Sigma) при разведении 1:1000 в течение 60 минут при 37°С, после чего проводили 3-кратное отмывание (0,2% BSA в PBS/Твин-20) в течение 3-х минут. Для окрашивания в качестве хромогена использовали однокомпонентный субстрат тетраметиленбензидин преципитирующий (США).
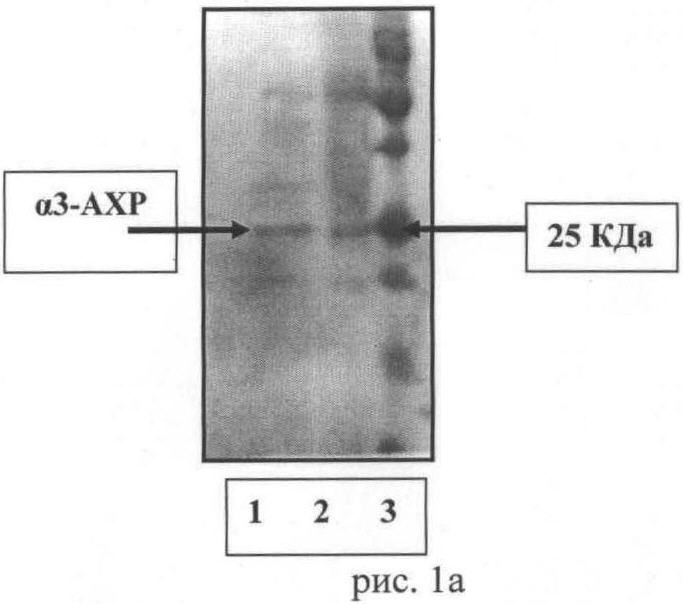
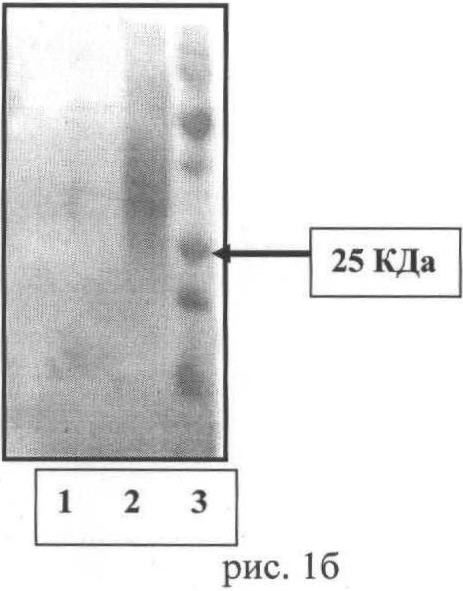
Результаты анализа экспресс-метода Вестерн-Блотинга представлен на рис.1а и 1б.
На рис.1a - Больная П., 54 г., на 2 и 3 дорожках выявлено наличие антител, диагноз: Аутоиммунная автономная ганглиопатия.
На рис.1б - Контроль (сыворотка здорового донора) антитела на 2 и 3 дорожках отсутствуют.
На рисунках: 1-дорожка - экстрацеллюлярный домен α3-АХР
2-дорожка - экстрацеллюлярный домен α3-АХР
3-дорожка - белки-маркеры.
Для количественного определения уровня аутоантител к α3-АХР был проведено следующее исследование с помощью тИФА.
На 96-ти луночные планшеты фирмы «Costar» сорбировали экстрацеллюлярный домен α3 субъединицы нейронального АХР в концентрации 2 мкг/лунку и инкубировали в течение 60 минут при 37°С. Первый ряд лунок оставляли свободным для коньюгатного контроля. Для блокирования неспецифического связывания в лунки вносили 2% раствор BSA (Sigma) в PBS/TBHH-20 по 200 мкл/лунку и инкубировали 60 минут при 37°С. После инкубации во второй ряд вносили сыворотки контрольных доноров, во все последующие ряды вносили сыворотки больных с аутоиммунной вегетативной ганглиопатией, миастенией и миастенией с тимомой в разведении 1:100 и инкубировали 60 мин при 37°С с последующим 3-кратным отмыванием (0,2% BSA в PBS/TBHH-20 по 200 мкл/лунку) в течение 3-х минут. Наличие антител определяли окрашиванием с использованием коньюгата пероксидазы с анти- IgG человека (Sigma), который вносили по 100 мкл/лунку при разведении 1:1000 и инкубировали 60 минут при 37°С, после чего проводили 3-кратное отмывание (0,2% BSA в PBS/Твин-20 по 200 мкл/лунку) в течение 3-х минут. В качестве хромогена использовали тетраметиленбензидин (Sigma): 10 мг растворяли в 5 мл нитратного буфера (рН 4,5) и 15 мкл пероксида водорода и вносили по 100 мкл/лунку. Окрашивание развивалось в течение 20 минут. Торможение реакции осуществляли 0,25 М раствором серной кислоты - 100 мкл/лунку. Измерение оптического поглощения света при длине волны 450 нм проводили на ИФА-анализаторе.
Результаты выражали в единицах оптической плотности (OD). В качестве нормального количества антител к α3-АХР было принято среднее значение содержания антител в контрольной группе - 0,2±0,04 OD.
Предлагаемым способом было обследовано 3 пациента с генерализованной формой миастении, 3 - миастенией с тимомой, 4-аутоиммунной вегетативной ганглиопатией и 10 контрольных здоровых доноров. Во всех случаях показатели уровня антител соответствовали состоянию больных и здоровых доноров.
Таким образом, предложенные способы обладают высокой специфичностью выявления наличия антител к α3-АХР в Вестернт-Блотинге и тИФА и позволяют с высокой точностью обнаруживать как наличие антител (появление темной окрашенной полосы), так и количественный уровень антител, при котором диагностируют аутоиммунное поражение периферического отдела ВНС.
Это обеспечивает своевременное адекватное лечение, направленное на подавление аутоиммунного поражения ВНС и улучшение качества жизни пациентов с периферической вегетативной недостаточностью (ПВН).
Таким образом, способы, предлагаемые нами, отличаются от известного уровня техники следующим:
1) позволяют проводить оценку ВНС путем исследования крови пациентов, разработанным нами методом тИФА в сыворотке крови по взаимодействию с экстрацеллюлярным участком α3-субъединицы нейронального АХР;
2) позволяют оценить уровень поражения ВНС;
3) позволяют отказаться от использования радиоактивных изотопов в качестве реагентов при выполнении методики;
4) позволяют проводить дифференциальную диагностику, объективизировать динамику патологического процесса, а также облегчают выбор адекватной терапии у больных с признаками ПВН;
5) являются более экономичными и не менее чувствительными по сравнению с другими методами;
6) не требуют введения в организм пациентов сильнодействующих лекарственных препаратов, находящихся на специальном учете;
7) один из способов позволяет количественно определять уровень антител к α3-АХР, что может характеризовать в какой-то степени и тяжесть аутоиммунного поражения периферического отдела ВНС на уровне парасимпатических ганглиев.
Примеры реализации способа.
Пример 1. Больная П., 54 лет, наблюдалась в клинике нервных болезней им. Кожевникова I МГМУ им. И.М.Сеченова с признаками периферической вегетативной недостаточности, прогрессирующей в течение 8 лет: синдром Горнера справа, нарушение аккомодации с извращенной реакцией зрачков в пробе с адреналином, обратная реакция артериального давления в клиностатической и ортостатической пробе (повышение в положении лежа и существенное снижение - в положении стоя), отсутствие динамики частоты сердечных сокращений при изменении позы, смена запоров учащенным жидким стулом (до 12-15 раз за ночь), слабость в положении стоя и сидя, невозможность передвигаться без утягивающей одежды, быстрая утомляемость, сухость кожи и слизистых оболочек с проксимальным гипергидрозом. Получала симптоматическую терапию (усиленный водный режим, минералокортикоиды, утягивающую одежду) с незначительным временным эффектом на фоне прогрессирования заболевания. Проведенное исследование сыворотки крови пациентки предлагаемым количественным тИФА способом выявило значительное повышение уровня аутоантител к α3-АХР: 1,78 OD450нм.
На основании анализа был поставлен диагноз аутоиммунной вегетативной ганглиопатии, минералокортикоиды были заменены на глюкокортикоиды, состояние больной постепенно улучшилось на фоне иммуносупрессивной терапии.
Пример 2. Больной Д., 37 лет, наблюдается в НЦ Неврологии РАМН с диагнозом миастения с тимомой (тератома с признаками дермоидной кисты - по МРТ). В клинической картине преобладали симптомы тяжелой миастении: асимметричный динамичный птоз, наружный офтальмопарез с диплопией, выраженный бульбарный синдром (до невозможности глотания и афонии), утомление при жевании, слабость и утомляемость мышц лица, шеи и конечностей, затруднение дыхания вследствие слабости дыхательной мускулатуры. Клинических признаков дисфункции вегетативной нервной системы не выявлено. В таких случаях препаратами первого ряда для лечения миастении являются глюкокортикостероиды. Вместе с тем, проведенное исследование сыворотки крови способом тИФА выявило наличие аутоантител к α3-АХР до 0,45 OD450нм, что позволило назначить адекватную иммунокоррегирующую терапию и избежать выраженных побочных симпатомиметических эффектов глюкокортикоидов (психомоторное возбуждение, тахикардия, повышение АД, нарушение моторики желудочно-кишечного тракта, нарушение потоотделения и др.). Пациенту проведен курс плазмафереза с последующим назначением цитостатиков, при интеркуррентной инфекции - курс в/в нормального человеческого иммуноглобулина с положительным эффектом.
Пример 3.
Больная И., 46 лет, наблюдается в НЦ Неврологии РАМН с диагнозом миастения, генерализованная форма. У больной выявлены симптомы вегетативной дисфункции в виде приступов тахикардии, потливости с сухостью слизистых оболочек, нарушения зрения (помимо диплопии, связанной с миастеническим наружным офтальмопарезом, периодически - «расфокусировка» контуров предметов на среднем расстоянии), помимо слабости и утомляемости произвольных мышц, общая слабость, повышенная утомляемость, не реагирующие на ингибиторы АХЭ. Проведенное исследование сыворотки крови предлагаемым способом не выявило аутоантител в сыворотке крови, что позволило отнести эти нарушения к надсегментарному уровню дисфункции ВИС на фоне дисгормональных нарушений (4 года назад оперирована по поводу рака щитовидной железы, есть нарушения менструального цикла с чередованием маточных кровотечений и длительных периодов аменореи) и позволило скорректировать проводимую терапию.
Таким образом, определение AT к α3-АХР экспресс-методом Вестерн-Блотинга тИФА в сыворотке крови по взаимодействию с экстрацеллюлярным участком α3-субъединицы нейронального АХР - отражает ганглионарный уровень поражения парасимпатического отдела ВНС. Анализ позволяет установить диагноз аутоиммунной вегетативной ганглиопатии, выявить наличие вегетативной недостаточности у больного миастенией с тимомой, а также исключить поражение периферического отдела ВНС у пациентки с миастенией и вегетативной дисфункцией.
Заявляемый экспресс-метод Вестерн-Блотинга и тИФА позволяют добиться улучшения диагностического процесса у больных имеющих признаки периферической вегетативной недостаточности в короткие сроки, проследить динамику патологического процесса и выбрать правильную тактику лечения. При высокой специфичности способы являются более простыми и экономичными и обеспечивают возможность осуществления диагностики аутоиммунного поражения периферического отдела ВНС при нервных и нервно-мышечных заболеваниях.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ДИАГНОСТИКИ АУТОИММУННОГО ПОРАЖЕНИЯ ВЕГЕТАТИВНЫХ СТРУКТУР ЖЕЛУДОЧНО-КИШЕЧНОГО ТРАКТА | 2013 |
|
RU2526812C1 |
| СПОСОБ КОМПЛЕКСНОЙ ОЦЕНКИ РАЗЛИЧНЫХ УРОВНЕЙ ПОРАЖЕНИЯ СТРУКТУР ВЕГЕТАТИВНОЙ НЕРВНОЙ СИСТЕМЫ | 2012 |
|
RU2485518C1 |
| Способ диагностики у детей астено-вегетативного синдрома в условиях экспозиции алюминием | 2018 |
|
RU2687731C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СДВИГА БАЛАНСА ВЕГЕТАТИВНОЙ НЕРВНОЙ СИСТЕМЫ В СТОРОНУ ПАРАСИМПАТИКОТОНИИ | 2008 |
|
RU2368304C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СОСУДОРАСШИРЯЮЩЕЙ РЕАКЦИИ НИТРОГЛИЦЕРИНА У БОЛЬНЫХ ИШЕМИЧЕСКОЙ БОЛЕЗНЬЮ СЕРДЦА | 2010 |
|
RU2444278C2 |
| СПОСОБ ДИАГНОСТИКИ АУТОИММУННОГО ПРОЦЕССА В СУСТАВАХ У БОЛЬНЫХ ОСТЕОАРТРОЗОМ | 2003 |
|
RU2280875C2 |
| СПОСОБ ОЦЕНКИ ЭФФЕКТИВНОСТИ СОСУДИСТОЙ РЕКОНСТРУКЦИИ У БОЛЬНЫХ С КРИТИЧЕСКОЙ ИШЕМИЕЙ НИЖНИХ КОНЕЧНОСТЕЙ | 2006 |
|
RU2310376C1 |
| СПОСОБ ДИАГНОСТИКИ ИНФЕКЦИОННЫХ, АЛЛЕРГИЧЕСКИХ, АУТОИММУННЫХ И ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2018 |
|
RU2702011C1 |
| СПОСОБ ОТБОРА ЛИЦ ДЛЯ МЕДИЦИНСКОГО ОБСЛЕДОВАНИЯ ПРИ КОРОНАРНОЙ ПАТОЛОГИИ | 2010 |
|
RU2465813C2 |
| ПРОГНОЗИРОВАНИЕ ТЕЧЕНИЯ И ИСХОДА КОМЫ И ПОСТКОМАТОЗНЫХ БЕССОЗНАТЕЛЬНЫХ СОСТОЯНИЙ (В ТОМ ЧИСЛЕ ВЕГЕТАТИВНЫХ) С ПОМОЩЬЮ ГЕМОТЕСТОВ | 2016 |
|
RU2648515C1 |
Изобретение относится к медицине, а именно, к вариантам способа лабораторной диагностики аутоиммунных заболеваний вегетативной нервной системы. В первом случае - проводят определение наличия в сыворотке крови антител к α3-АХР, при этом антитела к α3-АХР определяют экспресс-методом Вестерн-Блотинга в сыворотке крови по взаимодействию с экстрацеллюлярным участком α3-субъединицы нейронального АХР, а наличие антител к α3-АХР определяют окрашиванием, используя в качестве хромогена тетраметилбензидин преципитирующий. Во втором случае - проводят определение в сыворотке крови антител к α3-АХР методом тИФА по взаимодействию с экстрацеллюлярным участком α3-субъединицы нейронального АХР, уровень антител к α3-АХР определяют окрашиванием, используя в качестве хромогена тетраметилбензидин, оптическое поглощение света измеряют на ИФА-анализаторе при длине волны 450 нм в единицах оптической плотности (OD), при повышении уровня антител к α3-АХР более 0,24 OD450HM. Изобретение является более дешевыми и безопасными. Кроме того, данные способы позволяют при той же специфичности более простым и экономичным путем (в частности не требующим мер защиты от радиации) осуществить диагностику аутоиммунного поражения периферического отдела ВНС при нервных и нервно-мышечных заболеваниях. 2 н.п. ф-лы, 2 ил.
1. Способ диагностики аутоиммунного поражения периферического парасимпатического отдела вегетативной нервной системы, включающий определение наличия в сыворотке крови антител к α3-АХР, отличающийся тем, что антитела к α3-АХР определяют экспресс-методом Вестерн-Блотинга в сыворотке крови по взаимодействию с экстрацеллюлярным участком α3-субъединицы нейронального АХР, а наличие антител к α3-АХР определяют окрашиванием, используя в качестве хромогена тетраметилбензидин преципитирующий.
2. Способ диагностики аутоиммунного поражения периферического парасимпатического отдела вегетативной нервной системы, включающий определение в сыворотке крови антител к α3-АХР, отличающийся тем, что антитела к α3-АХР определяют методом тИФА в образце сыворотки крови по взаимодействию с экстрацеллюлярным участком α3-субъединицы нейронального АХР, уровень антител к α3-АХР определяют окрашиванием, используя в качестве хромогена тетраметилбензидин, оптическое поглощение света измеряют на ИФА-анализаторе при длине волны 450 нм в единицах оптической плотности (OD) и при повышении уровня антител к α3-АХР более 0,24 OD450HM, относительно контроля диагностируют аутоиммунное поражение периферического отдела ВНС на уровне парасимпатических ганглиев.
| VEMINO S., et al | |||
| Autoantibodies to ganglionic acetylcholinereceptors in autoimmune autonomic neuropathies., N | |||
| Engl | |||
| J | |||
| Med., 2000, 343, 847-855 | |||
| СПОСОБ ОЦЕНКИ ФУНКЦИОНАЛЬНОГО СОСТОЯНИЯ СЕРДЕЧНО-СОСУДИСТОЙ И ВЕГЕТАТИВНОЙ НЕРВНОЙ СИСТЕМ | 1999 |
|
RU2151545C1 |
| KOSEDA-DRAGAN M | |||
| et al | |||
| New diagnostic criteria for the neuropsychiatric form of systemic lupus erythematosus | |||
| Psychiatr Pol | |||
| ЩИТОВОЙ ДЛЯ ВОДОЕМОВ ЗАТВОР | 1922 |
|
SU2000A1 |
| Найдено из PubMed, PMID: 11304890. | |||
Авторы
Даты
2013-04-10—Публикация
2011-12-28—Подача