Изобретение относится к биотехнологии, в частности к культивированию органов и тканей растений, и может быть использовано в цветоводстве для повышения коэффициента размножения, оздоровления посадочного материала, а также в селекционной практике для создания новых улучшенных сортов I.ensata.
Известен способ получения растений-регенерантов I.ensata, согласно которому в качестве эксплантов используют молодые побеги. Их культивируют на среде Мурасиге-Скуга, дополненной гормонами и сахарозой. Наблюдают индукцию двух видов каллуса: зеленого и белого. Из зеленого каллуса были получены побеги. Введение активированного угля в питательную среду положительно влияло на образование корней у этих побегов (Yabuya Т, Ikeda Y., Adachi Т. (1991) In vitro propagation of Japanese garden iris iris ensata Thunb. // Euphytica 57, P.77-82).
Недостатком данного способа (аналога) является следующее. Получение каллусной ткани с последующей индукцией органогенеза или соматического эмбриогенеза не пригодно для использования при микроразмножении сортов растений, так как повышается вероятность сомаклональной изменчивости исходного материала.
Наиболее близким является способ получения растений-регенерантов I.ensata на основе индукции развития почек в эксплантах околоцветник - завязь прямым путем, минуя каллусообразование. Экспланты культивировали на питательных средах Мурасиге-Скуга, дополненных фитогормонами НУК(α-нафтилуксусная кислота) и БАП (6-бензиламинопурин) в количестве 0-5 мг/л. Отмечена высокая способность к побегообразованию у данного типа эксплантов. Укоренить побеги автору не удалось (Kawase К, Mizutani Н, Yoshioka М, Fukuda S (1995) Shoot formation on floral organs of Japanese iris in vitro // Journal of the Japanese Society for Horticultural Science 64, P.143-8).
Недостатками данного способа является отсутствие способности к укоренению у полученных побегов I.ensata.
Наиболее близким является способ прямой регенерации флоральных элементов в ткани трубки околоцветника I.ensata. Бутоны, смоченные в 96% этиловом спирте, обжигали в пламени спиртовки. Следующий этап обеззараживания проводили в 0,1% растворе сульфохлорантина в течение 20 минут. Части цветка делили на фрагменты 3×3 мм. В качестве эксплантов использовали фрагменты трубки околоцветника. Экспланты высаживали на питательные среды на основе MS (по прописи Мурасиге и Скуга), дополненные фитогормонами: 1-нафтилуксусной кислотой (НУК) 3-5 мкМ и 6-бензиламинопурином (БАП) 4-8 мкМ. Данным способом трубка околоцветника I.ensata способна регенерировать флоральные элементы (Тихомирова Л.И. Особенности индукции морфогенеза из различных фрагментов цветка ириса в культуре in vitro // Turczaninowia. 2010. - №13 (3). - C.147-151).
Недостатками данного способа (прототипа) является отсутствие способности к размножению и укоренению полученных флоральных элементов I.ensata, a также отсутствие подтверждения идентичности материнским экземплярам.
Задачей изобретения является создание способа получения растений-регенерантов, идентичных материнским растениям I.ensata, способных к дальнейшему размножению и укоренению.
Сущность изобретения
Способ получения растений-регенерантов I.ensata, заключающийся в том, что образование побегов осуществляется непосредственно из ткани экспланта, минуя стадию каллусообразования, зачатки побегов с флоральными элементами разделяют и пересаживают на питательные среды с БАП 20 мкМ и полноценные вегетативные побеги укореняют на среде с НУК 3 мкМ.
Способ получения растений-регенерантов ириса мечевидного (I.ensata Thunb.) in vitro, заключающийся в том, что бутоны, смоченные в 96% этиловом спирте, обжигают в пламени спиртовки, обеззараживают в 0,1% растворе сульфохлорантина в течение 20 минут, затем части трубки околоцветника делят на фрагменты 3×3 мм и высаживают каждый фрагмент на питательную среду Мурасиге-Скуга, содержащую 3-5 мкМ НУК в сочетании с 4-8 мкМ БАП, затем культивируют и укореняют, а через 30 суток культивирования образовавшиеся зачатки побегов с флоральными элементами пересаживают на питательные среды с БАП 20 мкМ и через 30 суток культивирования побеги укореняют на среде Мурасиге-Скуга с НУК 3 мкМ.
Способ обеспечивает высокий процент выхода генетически стабильных регенерантов. Для подтверждения идентичности материнским экземплярам проводят анализ методом RAPD полногеномной ДНК.
Способ реализуют следующим образом.
Получение растений-регенерантов I.ensata осуществляют в два этапа, в качестве эксплантов используют фрагменты трубки околоцветника.
1 этап. Цветки берут в фазе бутонизации (VII этап органогенеза), когда они плотно закрыты листочками обертки. Стерилизацию материала проводят в условиях ламинар-бокса. Бутоны цветка, смоченные в 96% этиловом спирте, обжигают в пламени спиртовки, далее проводят обеззараживание в 0,1% растворе сульфохлорантина в течение 20 минут. Подобный способ обеспечивает на 100% стерильность и жизнеспособность материала. Части трубки околоцветника делят на фрагменты размером не более 3×3 мм и помещают на питательные среды.
Питательные среды готовят по прописи Мурасиге и Скуга, содержащие 30 г/л сахарозы. В них вводят фитогормоны в разных концентрациях: 3-5 мкМ НУК в сочетании с 4-8 мкМ БАП, всего девять вариантов сред (таблица 1) pH среды доводят до 5,8-5,9 и добавляют 0,6% агара. Среды разливают в пластиковые контейнеры по 30 мл или в культуральные флаконы по 10 мл. Автоклавируют приготовленные питательные среды в течение 20 мин при 120°С. Экспланты культивируют в условиях фотопериода 16/8 часов свет/темнота при 24-26°С.
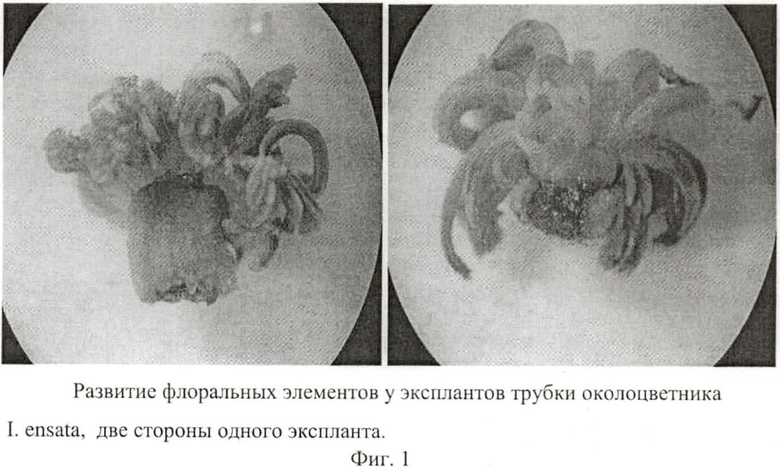
В первые две недели культививования in vitro все экспланты увеличиваются в размерах и приобретают зеленую окраску. Далее еще через две недели в тканях экспланта развиваются зачатки вегетативных побегов, у которых вместо примордиев первых листьев формируются структуры, похожие на доли околоцветника - флоральные элементы. Со временем эти структуры приобретают характерную для цветков данного сорта окраску (Фиг.1).
2 этап. Для получения вегетативных побегов I.ensata из фрагментов трубки околоцветника готовят питательные среды. Зачатки побегов с флоральными элементами пересаживают на питательные среды (используются среды Мурасиге-Скуга или Гамборга B5), содержащие 20 мкМ БАП (таблица 2). Этап, во время которого из эксплантов формируются вегетативные побеги, характеризуется как промежуточный. Через 30 дней регенерируют полноценные побеги с зелеными листьями. В результате данным способом через 60 суток получают полноценные вегетативные побеги I.ensata в количестве 5-8 штук на один эксплант (Фиг.2), которые укореняют на среде Мурасиге-Скуга с НУК 3 мкМ. А после этапа укоренения получают растения-регенеранты, идентичные материнским экземплярам. Для подтверждения идентичности растений-регенерантов и материнских растений I.ensata проводят анализ с помощью ПЦР (Фиг.3).
Необходимым условием клонального микроразмножения является стабильное воспроизводство исходного генотипа. Однако соблюдение этого условия вызывает ряд трудностей, т.к. биологически активные компоненты питательных сред способны вызвать генетические изменения в клетках, что приводит к генетической вариабельности полученных регенерантов. Методом RAPD-анализа полногеномной ДНК отличий между материнскими экземплярами I.ensata и растениями-регенерантами, полученными методом прямой регенерации побегов из ткани экспланта трубки околоцветника, не обнаружено.
Способом получения растений-регенерантов ириса мечевидного (I.ensata Thunb.) in vitro получают побеги в количестве 5-8 штук на один эксплант, способные к дальнейшему размножению и укоренению. Высокий процент укоренения до 100% достигается на средах Мурасиге и Скуга, дополненных 3 мкМ НУК.


Изобретение относится к способу получения растений-регенерантов ириса мечевидного (I.ensata Thunb.) in vitro. Способ включает стерилизацию бутонов при условии, что бутоны, смоченные в 96%-ном этиловом спирте, обжигают в пламени спиртовки, обеззараживают в 0,1%-ном растворе сульфохлорантина в течение 20 минут, затем части трубки околоцветника делят на фрагменты 3×3 мм и высаживают на питательную среду Мурасиге-Скуга, содержащую 3-5 мкМ НУК в сочетании с 4-8 мкМ БАП. Затем культивируют и укореняют. При этом через 30 суток культивирования образовавшиеся зачатки побегов с флоральными элементами пересаживают на питательные среды с БАП 20 мкМ и через 30 суток культивирования побеги укореняют на среде Мурасиге-Скуга с НУК 3 мкМ. Изобретение позволяет получать растения-регенеранты прямым методом, минуя каллусную культуру, с высоким процентом укоренения. 3 ил., 2 табл.
Способ получения растений-регенерантов ириса мечевидного (I.ensata Thunb.) in vitro, включающий стерилизацию бутонов, заключающийся в том, что бутоны, смоченные в 96%-ном этиловом спирте, обжигают в пламени спиртовки, обеззараживают в 0,1%-ном растворе сульфохлорантина в течение 20 минут, затем части трубки околоцветника делят на фрагменты 3×3 мм и высаживают на питательную среду Мурасиге-Скуга, содержащую 3-5 мкМ НУК в сочетании с 4-8 мкМ БАП, затем культивируют и укореняют, отличающийся тем, что через 30 суток культивирования образовавшиеся зачатки побегов с флоральными элементами пересаживают на питательные среды с БАП 20 мкМ и через 30 суток культивирования побеги укореняют на среде Мурасиге-Скуга с НУК 3 мкМ.
| ТИХОМИРОВА Л.И | |||
| Особенности индукции морфогенеза из различных фрагментов цветка ириса в культуре in vitro, Turczaninoia, 2010, 13(3), с.147-151 | |||
| KAWASE К | |||
| et.al | |||
| Shoot formation on floral organs of Japanese iris in vitro J | |||
| Japan | |||
| Soc | |||
| Hort | |||
| Sci | |||
| Нефтяной конвертер | 1922 |
|
SU64A1 |
| Топка с качающимися колосниковыми элементами | 1921 |
|
SU1995A1 |
| ТИХОМИРОВА Л.И | |||
| Получение растений-регенерантов ириса из изолированных зародышей | |||
Авторы
Даты
2013-05-20—Публикация
2011-10-25—Подача