Изобретение относится к медицине и ветеринарии, предназначено для применения в трансплантологии, травматологии, хирургии и онкологии и может быть использовано для замещения костных дефектов.
Известен имплантат, основой которого является титан и его сплавы (никелида титан, титан-тантал-ниобий, титан-кобальд) с нанесенным на него биосовместимым кальций-фосфатным покрытием, обеспечивающим адгезию клеток (патент РФ №2385740). Недостатком такого имплантата является опасность повреждения в зонах крепления к кости из-за различной плотности соприкасающихся поверхностей.
Наиболее близким к заявляемому изобретению (прототипом) является гибридный биоимплантат, выполненный в виде пористой мембраны из политетрафторэтилена с наноструктурированным многофункциональным биосовместимым нерезорбируемым покрытием, на основе элементов M-Ca-P-C-O-N или M-Ca-C-O-N, где М - металл, выбранный из ряда, включающего Ti, Zr, Hf, Nb, Ta, на поверхности которого пассированы аутогенные или аллогенные стромальные клетки, выделенные из жировой ткани или костного мозга (патент РФ №2416434).
Недостатки прототипа: 1) синтетическая основа имплантата не имеет анатомических особенностей, свойственных кости; 2) имплантат колонизируют клетками, коммитированными до стадии преостеобластов (клеток-предшественников костной ткани), не способными сформировать фиксирующую соединительнотканную капсулу и капиллярную сеть для реваскуляризации зоны имплантации; 3) в случае повреждения МБНП политетрафторэтилен не способен обеспечить адгезию клеток на своей поверхности, что ведет к ухудшению функциональных характеристик биоимплантата и развитию местной воспалительной реакции.
Задачей изобретения является создание биоимплантата с многофункциональным биоактивным наноструктурированным покрытием (МБНП), не приводящего к развитию реакции отторжения реципиента, обеспечивающего быструю фиксацию и репарацию тканью реципиента.
Задача решается тем, что в качестве основы биоимплантата используют донорскую кость, деиммунизированную с помощью хлорсодержащих окислителей с МБНП, на основе элементов M-Ca-P-C-O-N или M-Ca-C-O-N, где М - металл, выбранный из ряда, включающего Si, Ti, Zr, Hf, Nb, Та, и колонизированную мезенхимальными стволовыми клетками (МСК) реципиента.
Заявляемый биоимплантат с МБНП получали следующим образом. Мононуклеарные клетки выделяли на градиенте фиколл-урографин (плотность 1,077) центрифугированием при 900g из костного мозга реципиента. Затем клетки дважды отмывали от фиколла, центрифугируя в среде RPMI-1640 при 600 g. Суспензию клеток (концентрация 5-9х106 клеток в 1 мл) культивировали в среде RPMI-1640, содержащей 10% фетальной телячьей сыворотки, L-глутамина 2 мМ, пенициллина G 100 МЕ/мл, стрептомицина 100 мкг/мл, в пластиковых культуральных флаконах при t=37°C и 5% CO2 в течение 2-3 пассажей. МБНП на основе элементов M-Ca-P-C-O-N или M-Ca-C-O-N, где М - металл, выбранный из ряда, включающего Si, Ti, Zr, Hf, Nb, на костную основу наносили способом, описанным в статье D.V.Shtansky; I.V.Batenina; I.A.Yadroitsev; N.S.Ryashin; Ph.V.Kiryukhantsev-Korneev; A.E.Kudryashov; A.N.Sheveyko; I.Y.Zhitnyak; N.A.Gloushankova; I.Y.Smurov; E.A.Levashov «A new combined approach to metal-ceramic implants with controllable surface topography, chemistry, blind porosity, and wettability». Surface & Coatings Technology, Volume 208, Issue (September 15, 2012), p.14-23. На МБНП костной основы, деиммунизированной с помощью хлорсодержащих окислителей, пассировали суспензию МСК, морфологически характеризующихся как фибробластоподобные колониеобразующие клетки с уровнем экспрессии CD271 не ниже 70%, в количестве 500-1000 клеток на 1 см3 для эффективного колониеобразования. Полученный образец инкубировали при t=37°C и 5% CO2 в среде экспансии, содержащей RPMI-1640 и MACS NH Expansion Medium (Milteny Biotec) в соотношении 1:1,10% фетальную телячью сыворотку, L-глутамин 2 мМ, пенициллин G 100 МЕ/мл, стрептомицин 100 мкг/мл до формирования клеточного монослоя.
Изобретение иллюстрируется фигурами 1-8.
Фиг.1. Биоимплантат с МБНП, содержащим Ti-Ca-C-O-N (фрагмент лучевой кости собаки).
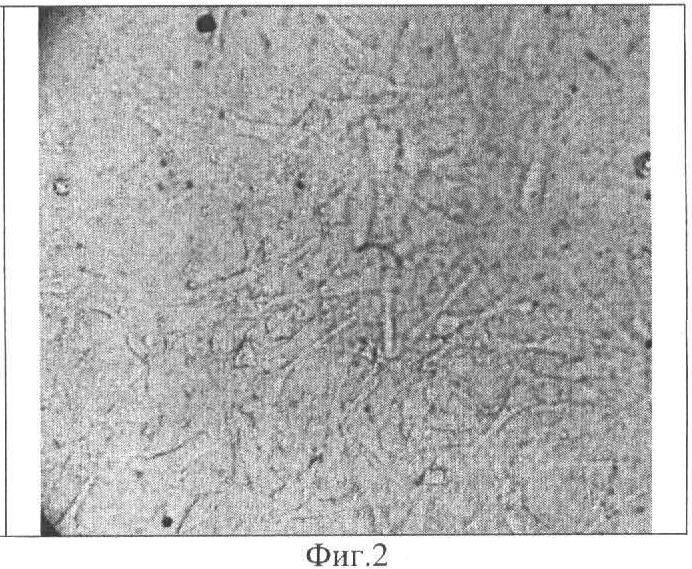
Фиг.2. МБНП биоимплантата, содержащее Ti-Ca-C-O-N, колонизированное МСК реципиента. Ув. 400.
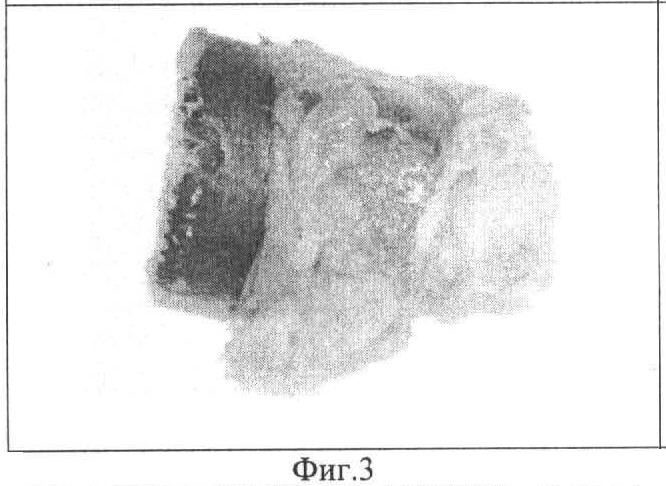
Фиг.3. Биоимплантат с МБНП, содержащим Ti-Ca-C-O-N, с отодвинутой фиброзной капсулой через 3 месяца после гетеротопной трансплантации собаке.
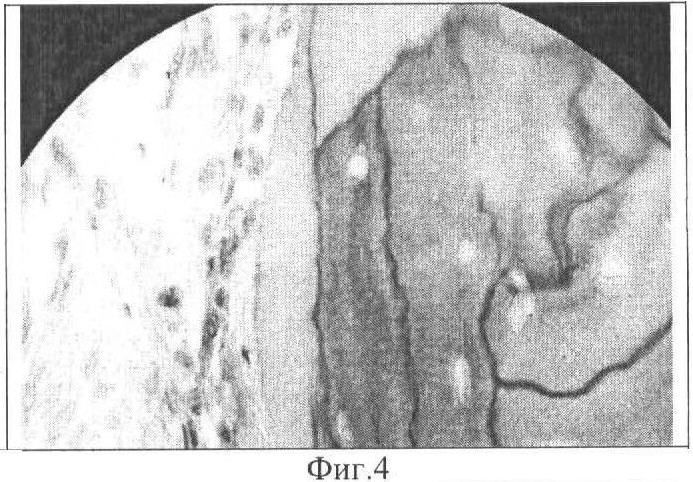
Фиг.4. Поверхностный слой биоимплантата с МБНП, содержащим Ti-Ca-C-O-N, и соединительнотканная капсула через 3 месяца после гетеротопной трансплантации собаке. Окраска гематоксилин-эозином. Ув. 900.
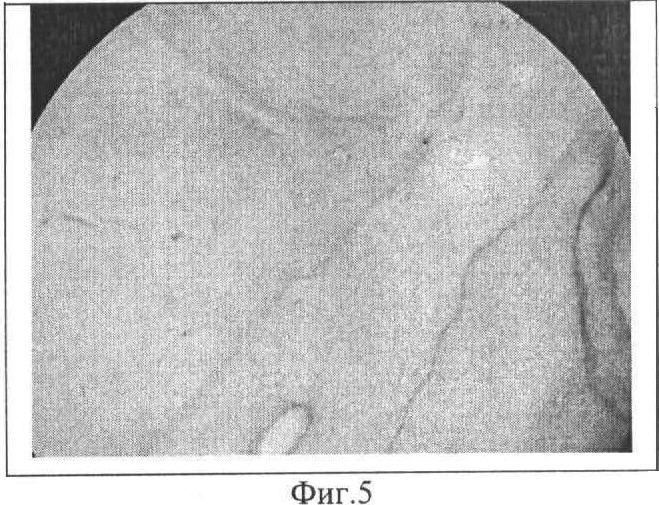
Фиг.5. Межклеточное компактное костное вещество основы биоимплантата с МБНП, содержащим Ti-Ca-C-O-N, через 3 месяца после гетеротопной трансплантации собаке. Окраска гематоксилин-эозином. Ув. 900.
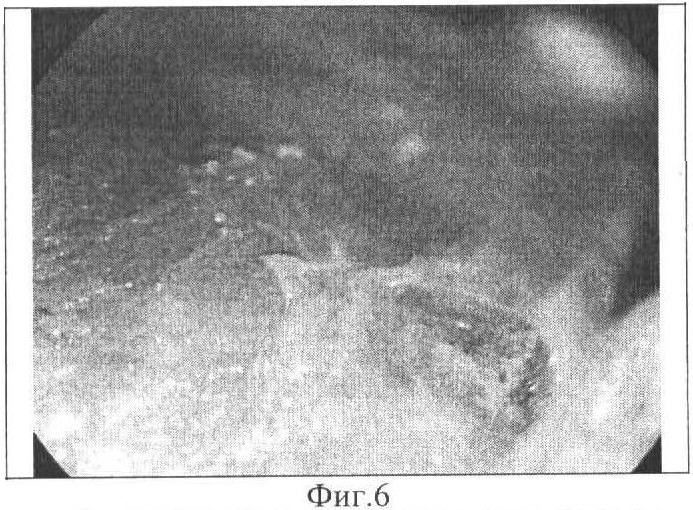
Фиг.6. Соединительнотканная капсула на поверхности биоимплантата с МБНП, содержащим Ti-Ca-C-O-N, сформированная через 3 месяца после гетеротопной трансплантации. Поперечный срез. Ув.80.
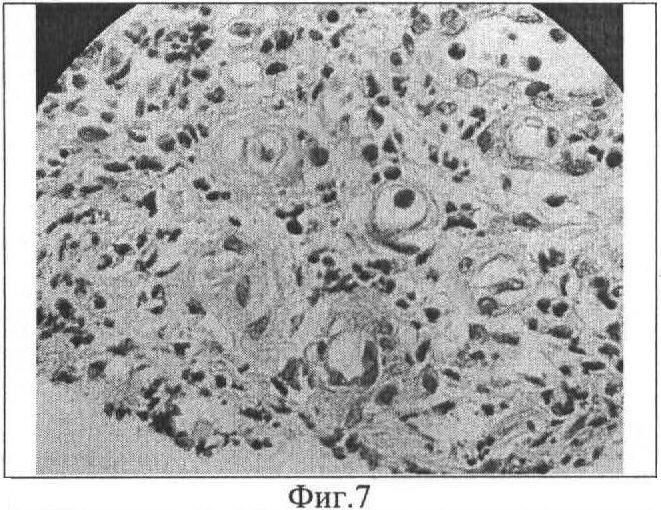
Фиг.7. Формирование сосудистой сети в соединительнотканной капсуле биоимплантата с МБНП, содержащим Ti-Ca-C-O-N, через 3 месяца после гетеротопной трансплантации. Окраска гематоксилин-эозином. Ув. 900.
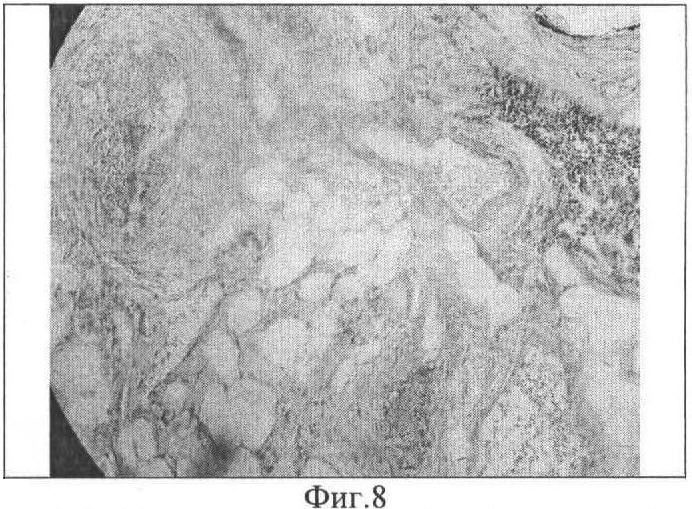
Фиг.8. Прорастание сосудов в костно-мозговой канал биоимплантата и колонизация клетками реципиента. Поперечный срез. Окраска гематоксилин-эозином. Ув. 200.
Изобретение иллюстрируется следующим примером.
Проведена гетеротопная трансплантация собаке биоимплантата из диафизарного отдела лучевой кости длиной 2,8 см и диаметром 1,2 см. На поверхность кости, деиммунизированной с помощью хлорсодержащих окислителей, с МБНП, содержащим Ti-Ca-C-O-N, пассировали суспензию МСК с концентрацией CD271+ клеток - 73,5% (Фиг.1). Полученный образец помещали в среду RPMI-1640, содержащую 10% фетальной телячьей сыворотки, L-глутамина 2 мМ, пенициллина G 100 МЕ/мл, стрептомицина 100 мкг/мл на 4 суток до образования на поверхности клеточного монослоя (Фиг.2). Подготовленный биоимплантат с МБНП имплантировали в паховую складку здоровой беспородной собаки (возраст 3,5 года). Послеоперационный период протекал гладко. Через 3 месяца биоимплантат был извлечен и подвергнут патолого-анатомическому исследованию, при котором не выявлено структурных изменений биоимплантата, МБНП на поверхности кости сохранено (Фиг.1, 3). Скоплений иммунокомпетентных клеток в тканях, прилегающих к поверхности имплантата, не обнаружено. Признаков разрушения структуры межклеточного компактного костного вещества не выявлено (Фиг.4, 5). На поверхности биоимплантата сформирована соединительнотканная капсула, в которой образовалось большое количество замкнутых контуров, выстланных эндотелием (Фиг.6, 7). На срезах костно-мозгового канала обнаружены признаки реколонизации имплантата клетками реципиента с формированием кровеносных сосудов (Фиг.8).
При использовании в МБНП циркония и других металлов, указанных в формуле, были получены результаты, близкие к титану.
Технический результат
Биоимплантат с МБНП, содержащем элементы M-Ca-P-C-O-N или M-Ca-C-O-N, где М - металл, выбранный из ряда, включающего Si, Ti, Zr, Hf, Nb, Ta, основу которого представляет деиммунизированная донорская кость, соответствующая анатомо-морфологическим особенностям замещаемой кости, обеспечивает адгезию клеток, отсутствие реакции отторжения трансплантата, ускоренное формирование соединительной ткани и костной мозоли.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ БИОИНЖЕНЕРНОЙ КОНСТРУКЦИИ ДЛЯ ЗАМЕЩЕНИЯ КОСТНЫХ ДЕФЕКТОВ | 2012 |
|
RU2482881C1 |
| БИОИНЖЕНЕРНАЯ КОНСТРУКЦИЯ ДЛЯ ЗАКРЫТИЯ КОСТНЫХ ДЕФЕКТОВ С ВОССТАНОВЛЕНИЕМ В НИХ КОСТНОЙ ТКАНИ И СПОСОБ ПОЛУЧЕНИЯ УКАЗАННОЙ КОНСТРУКЦИИ | 2009 |
|
RU2416434C1 |
| СПОСОБ УСТРАНЕНИЯ КОСТНЫХ ДЕФЕКТОВ С ВОССТАНОВЛЕНИЕМ В НИХ КОСТНОЙ ТКАНИ | 2009 |
|
RU2449755C2 |
| СПОСОБ ПОЛУЧЕНИЯ ТРАХЕОБРОНХИАЛЬНОГО БИОИМПЛАНТА | 2011 |
|
RU2458635C1 |
| Способ наращивания объема костной ткани гребня альвеолярного отростка челюсти | 2016 |
|
RU2645963C2 |
| БИОТРАНСПЛАНТАТ ДЛЯ ВОССТАНОВЛЕНИЯ ОБЪЕМА КОСТНОЙ ТКАНИ ПРИ ДЕГЕНЕРАТИВНЫХ ЗАБОЛЕВАНИЯХ И ТРАВМАТИЧЕСКИХ ПВОРЕЖДЕНИЯХ КОСТЕЙ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2012 |
|
RU2530622C2 |
| Титановый имплантат с поверхностью, модифицированной для усиления клеточной адгезии, и способ его изготовления | 2021 |
|
RU2779364C1 |
| Способ получения биоимплантата для замещения сегментарных дефектов трахеи | 2015 |
|
RU2612528C1 |
| СПОСОБ ПОЛУЧЕНИЯ МАТРИКСА ТРАХЕИ ДЛЯ АЛЛОГЕННОЙ ТРАНСПЛАНТАЦИИ | 2010 |
|
RU2453291C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИМПЛАНТАЦИОННОГО МАТЕРИАЛА НА ОСНОВЕ ПОРИСТОГО ПОЛИТЕТРАФТОРЭТИЛЕНА И МАТЕРИАЛ, ПОЛУЧЕННЫЙ ЭТИМ СПОСОБОМ | 2007 |
|
RU2325191C1 |

Изобретение относится к медицине и ветеринарии, предназначено для применения в трансплантологии, травматологии, хирургии и онкологии и может быть использовано для замещения костных дефектов. Описан биоимплантат, который представляет собой донорскую кость, деиммунизированную с помощью хлорсодержащих окислителей, на поверхность которой наносят многофункциональное биоактивное наноструктурированное покрытие (МБНП) на основе элементов M-Ca-P-C-O-N или M-Ca-C-O-N, где М - металл, выбранный из ряда, включающего Si, Ti, Zr, Hf, Nb, Ta, и колонизированную мезенхимальными стволовыми клетками (МСК) реципиента. Биоимплантат с МБНП соответствует анатомо-морфологическим особенностям замещаемой кости, обеспечивает адгезию клеток, отсутствие реакции отторжения трансплантата, ускоренное формирование соединительной ткани и костной мозоли. 8 ил., 1 пр.
Биоимплантат с многофункциональным биоактивным наноструктурированным покрытием на основе элементов M-Ca-P-C-O-N или M-Ca-C-O-N, где М - металл, выбранный из ряда, включающего Si, Ti, Zr, Hf, Nb, отличающийся тем, что его основа представляет собой донорскую кость, анатомически соответствующую замещаемой, деиммунизированную с помощью хлорсодержащих окислителей, колонизированную мезенхимальными стволовыми клетками реципиента.
| БИОИНЖЕНЕРНАЯ КОНСТРУКЦИЯ ДЛЯ ЗАКРЫТИЯ КОСТНЫХ ДЕФЕКТОВ С ВОССТАНОВЛЕНИЕМ В НИХ КОСТНОЙ ТКАНИ И СПОСОБ ПОЛУЧЕНИЯ УКАЗАННОЙ КОНСТРУКЦИИ | 2009 |
|
RU2416434C1 |
| БИОАКТИВНОЕ ПОКРЫТИЕ НА ИМПЛАНТАТЕ ИЗ ТИТАНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2008 |
|
RU2385740C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОМАТЕРИАЛОВ ИЗ КОСТНОЙ ТКАНИ И ПОЛУЧЕННЫЙ ЭТИМ СПОСОБОМ МАТЕРИАЛ ДЛЯ ОСТЕОПЛАСТИКИ И ТКАНЕВОЙ ИНЖЕНЕРИИ | 2005 |
|
RU2342162C1 |
Авторы
Даты
2013-05-27—Публикация
2012-03-28—Подача