Изобретение относится к области экспериментальной медицины и может быть использовано для изучения репаративных процессов, протекающих в тканях поврежденного сустава.
Известен способ моделирования процесса репаративной регенерации тканей при повреждениях тазобедренного сустава, предусматривающий нарушение его целостности с последующей репозицией и фиксацией суставных компонентов с помощью аппарата внешней фиксации (Силантьева Т.А. Репаративное костеобразование при заживлении перелома тазовой кости в области суставной (вертлужной) впадины (экспериментально-морфологическое исследование): автореф. дис… канд. биол. наук. РНЦ «ВТО» им. акад. Г.А.Илизарова. Саранск, 2005. 26 с.).
Однако известный способ не предусматривает направленной регуляции реперативных процессов в тканях поврежденного сустава.
Известен способ лечения патологии суставов у животных, предусматривающий иммобилизацию сустава с восстановлением анатомически правильных взаимоотношений его компонентов с помощью аппарата внешней фиксации и введение в суставную полость лекарственных препаратов (Патент РФ №2404726, опубл. 27.11.2010).
Однако данный способ также не предусматривает направленной регуляции репаративных процессов в тканях поврежденного сустава.
Известен способ лечения повреждений сустава, предусматривающий его стабилизацию с помощью аппарата внешней фиксации и введение в полость сустава смеси растворов глюкозы, аскорбиновой кислоты и аутологичной плазмы крови, которые являются дифференцировочными и питательными средами для клеток соединительной и опорных тканей в зоне регенерации (Силантьева Т.А., Краснов В.В., Кирсанова А.Ю. Экспериментальная апробация методики оптимизации репаративного процесса при лечении внутрисуставного перелома / Бюллетень ВСНЦ СО РАМН. 2011. №4. Ч.1. С.278-283).
Однако в известном способе введение указанной смеси в суставную полость производилось для активизации репаративного остеогенеза в зоне регенерации и не преследовало своей целью воздействия на другие ткани поврежденного сустава.
Задачей изобретения является разработка способа, обеспечивающего изучение особенностей репаративной регенерации тканей при внутрисуставных повреждениях, в условиях стимуляции репаративного процесса веществами, являющимися дифференцировочными и питательными средами для клеток соединительной и опорных тканей.
Указанная задача решается тем, что в способе моделирования процесса репаративной регенерации тканей при внутрисуставных повреждениях, включающем восстановление анатомических взаимоотношений в суставе, его стабилизацию с помощью аппарата внешней фиксации, а также введение круглосуточно, капельно в полость сустава раствора или смеси растворов, являющихся дифференцировочными и питательными средами для клеток соединительной и опорных тканей в зоне регенерации, для дифференцировки в остеобластическом направлении и формирования преимущественно костного сращения вводят смесь официнальных растворов глюкозы, аскорбиновой кислоты и аутологичной плазмой крови, взятых в соотношении 1:2:7, в фибробластическом направлении и формирования преимущественно соединительнотканного сращения - смесь растворов глюкозы и аскорбиновой кислоты, взятых в соотношении 1:1; а в хондробластическом направлении и формирования преимущественно хрящевого сращения - изотонический раствор хлорида натрия.
Выполнение способа поясняется описанием, примерами практического использования и иллюстративным материалом, на котором изображено:
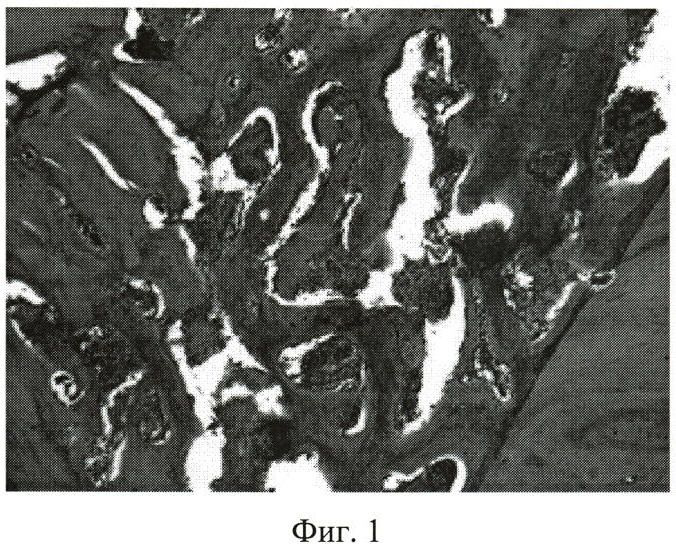
фиг.1 - микрофото зоны сращения отломков вертлужной впадины: костная ткань, прилежащая к раневой поверхности отломка при внутрисуставном введении смеси аскорбиновой кислоты, глюкозы, аутоплазмы крови. Срок эксперимента - 14 суток после операции. Парафиновый срез. Окраска гематоксилином и эозином. Об. 10, ок. 10;
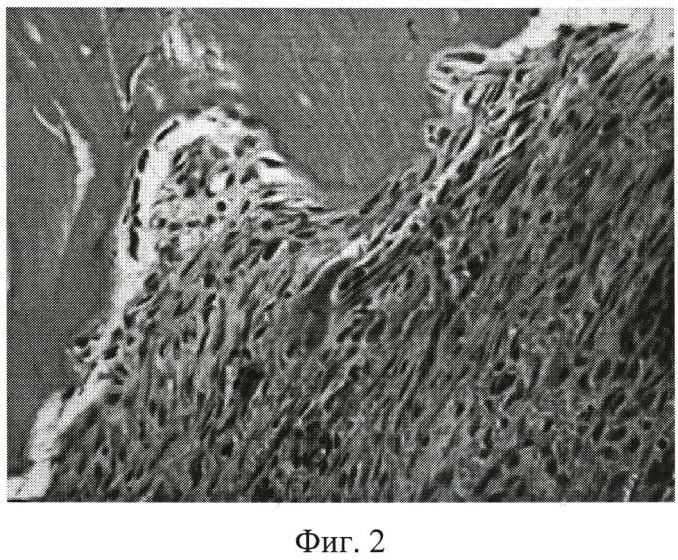
фиг.2 - микрофото зоны сращения отломков вертлужной впадины: соединительная ткань, прилежащая к раневой поверхности отломка при внутрисуставном введении смеси аскорбиновой кислоты и глюкозы. Срок эксперимента - 14 суток после операции. Парафиновый срез. Окраска гематоксилином и эозином. Об. 40, ок. 10;
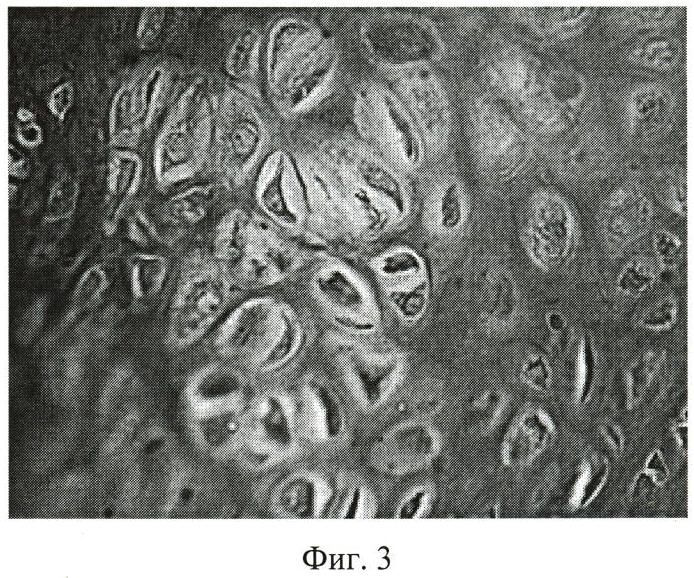
фиг.3 - микрофото зоны сращения отломков вертлужной впадины: хрящевая ткань, прилежащая к раневой поверхности отломка при внутрисуставном введении физиологического раствора. Срок эксперимента - 14 суток после операции. Парафиновый срез. Окраска Шифф-йодной кислотой. Об. 40, ок. 10.
Способ осуществляется следующим образом.
В условиях операционной после анестезии и обработки операционного поля осуществляют воспроизведение модели перелома вертлужной впадины, после чего проводят остеосинтез пораженного сустава аппаратом внешней фиксации. При его выполнении известными приемами фиксирующие элементы - спицы и/или стержни-шурупы, на нескольких уровнях чрескостно проводят (или консольно вводят) в прилежащие к пораженному суставу участки смежных костных сегментов. Свободные концы фиксаторов крепят на устанавливаемых на соответствующем уровне опорах аппарата, которые с помощью резьбовых стержней и шарнирных узлов соединяют между собой с возможностью дозированного разноплоскостного перемещения и разворота. При необходимости смещением опор аппарата и, соответственно, фиксируемых сегментов конечностей или их фрагментов восстанавливают анатомически правильные взаимоотношения компонентов сустава. Одновременно в суставную полость вводят катетер.
В послеоперационном периоде, начиная со вторых суток, через установленный катетер в полость сустава осуществляют круглосуточное капельное введение раствора или смеси растворов, являющихся дифференцировочными и питательными средами для клеток соединительной и опорных тканей в зоне регенерации. При этом, исходя из целей эксперимента, для дифференцировки клеток в остеобластическом направлении вводят приготовленную ex temporae смесь 40% официнального раствора глюкозы, 5% официнального раствора аскорбиновой кислоты и аутологичной плазмы крови, взятых в объемном соотношении 1:2:7; в фибробластическом направлении - приготовленную ех temporae смесь 5% официнального раствора глюкозы и 5% официнального раствора аскорбиновой кислоты, взятых в соотношении 1:1; а в хондробластическом направлении - 0,9% официнальный раствор хлорида натрия.
Указанные растворы вводят в течение 3-5 суток, после чего катетер в стерильных условиях извлекают. В дальнейшем в течение необходимого периода осуществляют стабильную фиксацию сустава, после чего его демонтируют. Животное выводят из опыта, полученный материал обрабатывают и анализируют.
Практическое использование способа иллюстрируют следующие наблюдения.
Пример 1.
Собака, кобель, возраст 3 года. После воспроизведения модели центрального поперечного перелома вертлужной впадины производили остеосинтез спице-стержневым аппаратом внешней фиксации. Перемещением опор аппарата восстановили анатомически правильные взаимоотношения компонентов тазобедренного сустава и в суставную щель чрескожно ввели мягкий катетер. Для пролонгированного управляемого введения дозированных объемов раствора в полость сустава использовали автоматизированный дозатор лекарственных веществ, который закрепляли на опоре аппарата внешней фиксации.
В послеоперационном периоде животному со 2-х по 5-е сутки для моделирования репаративного процесса с преобладанием остеогенеза осуществляли капельное введение приготовленной ex temporae смеси 40% официнального раствора глюкозы, 5% официнального раствора аскорбиновой кислоты и аутологичной плазмы крови, взятых в объемном соотношении 1:2:7.
Через 14 суток после травмы животное вывели из опыта. Проведенное гистологическое исследование зоны повреждения выявляло полное костное сращение отломков, образованное мелкопетлистым губчатым костным веществом (фиг.1). Клеточные элементы в ее составе имели, в зависимости от локализации, фенотип остеобластов либо остеоцитов - базофильную, более или менее развитую отростчатую цитоплазму и эухроматиновое, эксцентрично расположенное ядро с двумя либо одним крупным ядрышком. Рыхлая волокнистая соединительная ткань узких межтрабекулярных пространств отличалась высокой клеточной и сосудистой плотностью. Гемокапилляры, врастающие из губчатой кости отломков, были окружены малодифференцированными фибробластоподобными клетками с крупным, светлым ядром и узкой базофильной цитоплазмой. Вблизи капилляров располагались центры интрамембранозного окостенения.
Соотношение площадей костной ткани трабекул и соединительной ткани межтрабекулярных промежутков в составе губчатого костного вещества зоны сращения отломков составляло 60% и 40% соответственно. Численность костных и фибробластоподобных клеток находилась в соотношении 52% и 48%.
Изложенное позволило констатировать, что введение в полость сустава смеси 40% официнального раствора глюкозы, 5% официнального раствора аскорбиновой кислоты и аутологичной плазмы крови, взятых в объемном соотношении 1:2:7, обеспечивает дифференцировку клеток преимущественно в остеобластическом направлении, что обеспечивает формирование первичного костного сращения отломков и позволяет рассматривать его в качестве средства, стимулирующего репаративный остеогенез.
Пример 2.
Собака, кобель, возраст 2 года. Моделирование центрального поперечного перелома вертлужной впадины, остеосинтез спице-стержневым аппаратом внешней фиксации, установка катетера для внутрисуставного введения растворов.
В послеоперационном периоде животному со 2-х по 5-е сутки для моделирования репаративного процесса с преобладанием фибробластогенеза осуществляли интраартикулярное капельное введение приготовленной ex temporae смеси равных объемов 5% официнального раствора глюкозы и 5% официнального раствора аскорбиновой кислоты.
Через 14 суток после операции сращение отломков вертлужной впадины формировала рыхлая соединительная ткань (фиг.2). Клеточный компонент соединительной ткани зоны сращения был представлен преимущественно фибробластоподобными клетками вытянутой формы с развитой базофильной цитоплазмой, крупным эухроматиновым ядром с 1-2 ядрышками. Кровоснабжение зоны сращения осуществляли узкие полнокровные микрососуды капиллярного типа. Очаги костеобразования не были выявлены ни на поверхности травмированных костных трабекул, ни в толще соединительной ткани.
Соединительная ткань занимала 100% площади зоны сращения отломков, соответственно доля фибробластоподобных клеток (по отношению к костным и хрящевым) также составляла 100%.
Изложенное позволило констатировать, что введение в полость сустава смеси равных объемов 5% официнального раствора глюкозы и 5% официнального раствора аскорбиновой кислоты обеспечивает дифференцировку клеток преимущественно в фибробластическом направлении и способствует формированию соединительнотканного сращения отломков кости, что позволяет рассматривать его в качестве средства стимулирующего репаративный фиброгенез.
Пример 3.
Собака, кобель, возраст 2 года. Моделирование перелома вертлужной впадины, остеосинтез костей таза и внутрисуставное введение растворов производили аналогично примеру 1.
В послеоперационном периоде животному со 2-х по 5-е сутки для моделирования репаративного процесса с преобладанием хондрогенеза осуществляли интраартикулярное капельное введение 0,9% официнального раствора хлорида натрия.
Через 14 суток после выполнения оперативного вмешательства на гистологических препаратах определялось сращение отломков вертлужной впадины с преобладанием хрящевой ткани. Остеогенез наблюдался локально на поверхности поврежденных костных трабекул отломков (фиг.3).
Доля тканевых компонентов в зоне сращения отломков вертлужной впадины составляла 10% - для костной, 56% - для хрящевой и 34% - для соединительной ткани. Соотношение долей костных, хрящевых и фибробластоподобных клеток в зоне сращения составляло 8%, 47% и 45% соответственно. Кровоснабжение зоны сращения осуществляли немногочисленные полнокровные микрососуды капиллярного типа, расположенные в тяжах соединительной ткани, разделяющих поля новообразованного хряща.
Изложенное позволило констатировать, что введение в полость сустава 0,9% официнального раствора хлорида натрия обеспечивает дифференцировку клеток преимущественно в хондробластическом направлении и формирование преимущественно хрящевого сращения отломков кости, что позволяет рассматривать его в качестве средства, стимулирующего репаративный хондрогенез.
Использование способа показало, что его применение для моделирования процессов репаративной регенерации тканей при внутрисуставных повреждениях, обеспечивает изучение особенностей их репарации в условиях воздействия веществами, являющимися дифференцировочными и питательными средами для клеток соединительной и опорных тканей в зоне регенерации.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ СТИМУЛЯЦИИ РЕПАРАТИВНЫХ ПРОЦЕССОВ ПРИ ЛЕЧЕНИИ ВНУТРИСУСТАВНЫХ ПЕРЕЛОМОВ | 2010 |
|
RU2463986C2 |
| СПОСОБ МОДЕЛИРОВАНИЯ ВНУТРИСУСТАВНОГО ПОВРЕЖДЕНИЯ У МЕЛКИХ ЛАБОРАТОРНЫХ ЖИВОТНЫХ | 2011 |
|
RU2470378C1 |
| СПОСОБ ОПТИМИЗАЦИИ РЕПАРАТИВНОГО ОСТЕОГЕНЕЗА | 2006 |
|
RU2315580C2 |
| Способ осуществления прицельного малоинвазивного доступа для клеточных трансплантаций в костный регенерат | 2020 |
|
RU2748544C1 |
| Устройство, комплект и способ для введения трансплантата в костный регенерат | 2020 |
|
RU2741206C1 |
| СПОСОБ ЛЕЧЕНИЯ МНОГООСКОЛЬЧАТЫХ И МНОЖЕСТВЕННЫХ ПЕРЕЛОМОВ ДЛИННЫХ ТРУБЧАТЫХ КОСТЕЙ | 2008 |
|
RU2370227C1 |
| Жидкостный ин виво биореактор для выращивания костной ткани | 2021 |
|
RU2777947C1 |
| СПОСОБ ПОЛУЧЕНИЯ БОГАТОЙ ТРОМБОЦИТАМИ ПЛАЗМЫ И ЕЕ ПРИМЕНЕНИЯ В СОСТАВЕ МАЗИ | 2012 |
|
RU2511737C2 |
| Способ оптимизации репаративного остеогенеза трубчатых костей животных | 2023 |
|
RU2816808C1 |
| СПОСОБ СТИМУЛЯЦИИ РЕПАРАТИВНОГО ОСТЕОГЕНЕЗА | 2008 |
|
RU2373883C1 |
Изобретение относится к экспериментальной медицине и может быть использовано для изучения стимуляции репаративных процессов, протекающих в тканях поврежденного сустава. Для этого моделируют внутрисуставной перелом вертлужной впадины. Стимуляция включает восстановление анатомических взаимоотношений в суставе, его стабилизацию с помощью аппарата внешней фиксации. Далее в полость сустава в течение 3-5 суток, начиная со вторых суток после операции, круглосуточно капельно вводят раствор или смеси растворов. При этом для дифференцировки в остеобластическом направлении и формирования преимущественно костного сращения вводят смесь официнальных растворов 40% глюкозы, 5% аскорбиновой кислоты и аутологичной плазмой крови, взятых в объемном соотношении 1:2:7. Для дифференцировки в фибробластическом направлении и формирования преимущественно соединительнотканного сращения - смесь официнальных растворов 5% глюкозы и 5% аскорбиновой кислоты, взятых в объемном соотношении 1:1. Для дифференцировки в хондробластическом направлении и формирования преимущественно хрящевого сращения - официнальный 0,9% раствор хлорида натрия. Способ обеспечивает направленную регуляцию репаративных процессов в тканях поврежденного сустава. 3 ил., 3 пр.
Способ дифференцированной стимуляции репаративной регенерации тканей при моделировании внутрисуставных переломов вертлужной впадины, включающий восстановление анатомических взаимоотношений в суставе, его стабилизацию с помощью аппарата внешней фиксации, введение в полость сустава в течение 3-5 суток, начиная со вторых суток после операции, круглосуточно, капельно раствора или смеси растворов, являющихся дифференцировочными и питательными средами для клеток соединительной и опорных тканей в зоне регенерации, при этом для дифференцировки в остеобластическом направлении и формирования преимущественно костного сращения вводят смесь официнальных растворов 40% глюкозы, 5% аскорбиновой кислоты и аутологичной плазмы крови, взятых в объемном соотношении 1:2:7, для дифференцировки в фибробластическом направлении и формирования преимущественно соединительнотканного сращения - смесь официнальных растворов 5% глюкозы и 5% аскорбиновой кислоты, взятых в объемном соотношении 1:1; а для дифференцировки в хондробластическом направлении и формирования преимущественно хрящевого сращения - официнальный 0,9% раствор хлорида натрия.
| БОРИСОВ И.В | |||
| Лечение поперечных переломов вертлужной впадины у собак методом чрезкостного остеосинтеза: клинико-экспериментальное обоснование, Курган, 2004, Научная библиотека диссертаций и авторефератов disserCat |
Авторы
Даты
2013-07-20—Публикация
2012-04-02—Подача