Текст описания приведен в факсимильном виде.






























































































































| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ КУЛЬТИВИРОВАНИЯ КЛЕТОК, РАЗМНОЖЕНИЯ И ОЧИСТКИ ВИРУСОВ | 2009 |
|
RU2547587C2 |
| ПОСТОЯННЫЕ ЛИНИИ КЛЕТОК ЧЕЛОВЕКА ДЛЯ ПОЛУЧЕНИЯ ВИРУСОВ ГРИППА | 2011 |
|
RU2565546C2 |
| СПОСОБ КУЛЬТИВИРОВАНИЯ КЛЕТОК БЕЗ КОМПОНЕНТОВ ЖИВОТНОГО ПРОИСХОЖДЕНИЯ | 2004 |
|
RU2369634C2 |
| Бессывороточная питательная среда для культивирования клеток MDCK или Vero или вакцинных штаммов вирусов кори или гриппа | 2018 |
|
RU2703826C1 |
| СПОСОБ РЕПЛИКАЦИИ ВИРУСА В ПТИЧЬИХ ЭМБРИОНАЛЬНЫХ СТВОЛОВЫХ КЛЕТКАХ | 2006 |
|
RU2457253C2 |
| СПОСОБ ПРОДУЦИРОВАНИЯ РЕПЛИКАТИВНОЙ ЧАСТИЦЫ ВИРУСА ГРИППА, КОМПОЗИЦИЯ КЛЕТОК (ВАРИАНТЫ), КОМПОЗИЦИЯ КЛЕТОЧНОЙ КУЛЬТУРЫ И ЕЕ ПРИМЕНЕНИЕ | 2005 |
|
RU2435855C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЖИВОЙ КУЛЬТУРАЛЬНОЙ ВАКЦИНЫ ПРОТИВ ВИРУСА ГРИППА | 2003 |
|
RU2330885C2 |
| ВАРИАНТЫ ГЕМАГГЛЮТИНИНОВ ВИРУСА СВИНОГО ГРИППА | 2010 |
|
RU2560420C2 |
| СПОСОБ ПОЛУЧЕНИЯ РАБОЧЕГО ПОСЕВНОГО МАТЕРИАЛА ВИРУСА ГРИППА, СПОСОБ ПОЛУЧЕНИЯ ВАКЦИНЫ ОТ ГРИППА С ПРИМЕНЕНИЕМ УКАЗАННОГО ПОСЕВНОГО МАТЕРИАЛА И ПОСЕВНОЙ МАТЕРИАЛ ВИРУСА, ПОЛУЧЕННЫЙ УКАЗАННЫМ СПОСОБОМ | 2018 |
|
RU2748577C1 |
| СПОСОБ КУЛЬТИВИРОВАНИЯ АДГЕЗИОННЫХ КЛЕТОК | 2010 |
|
RU2612154C2 |
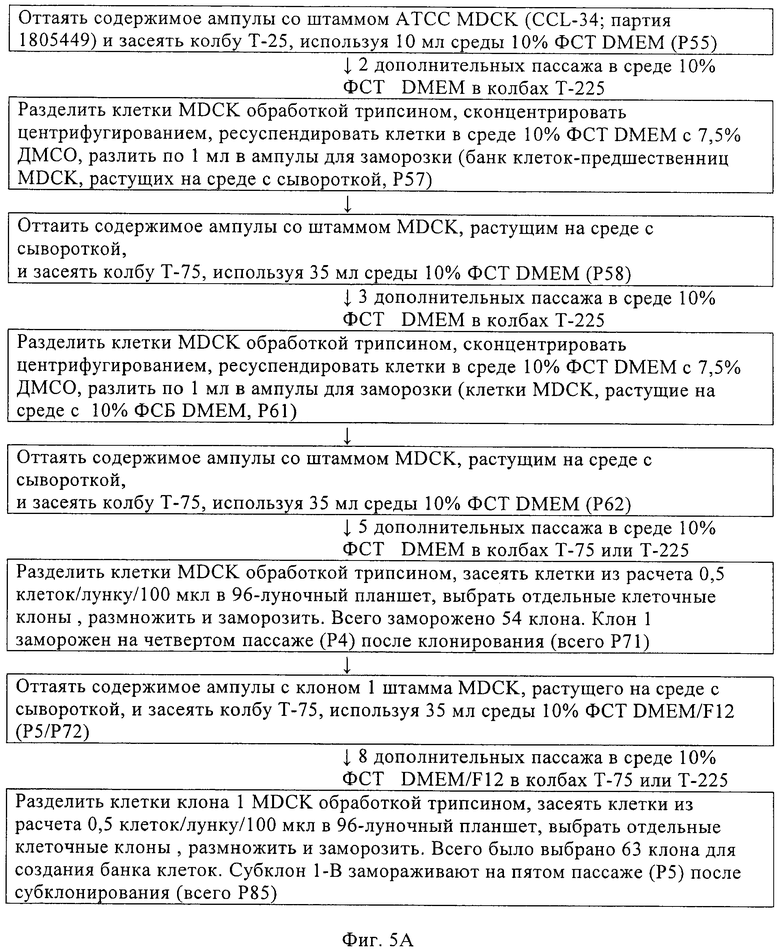

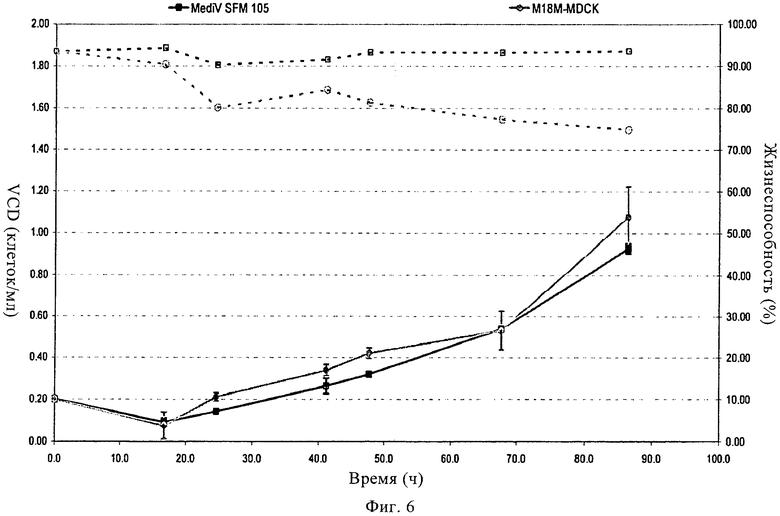
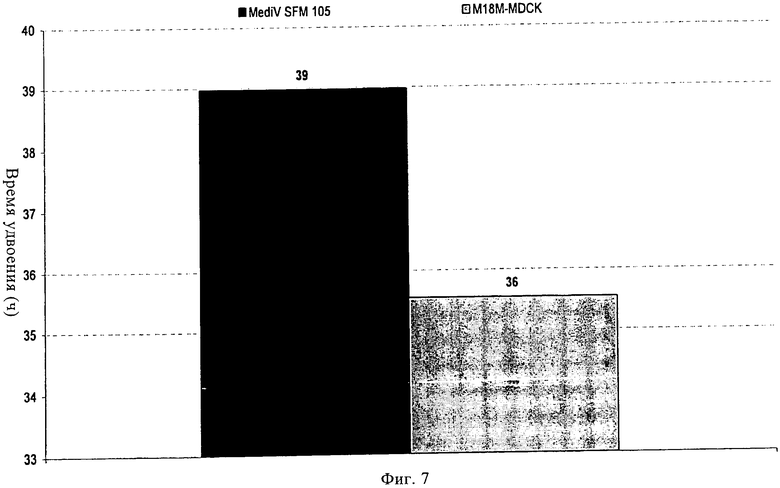
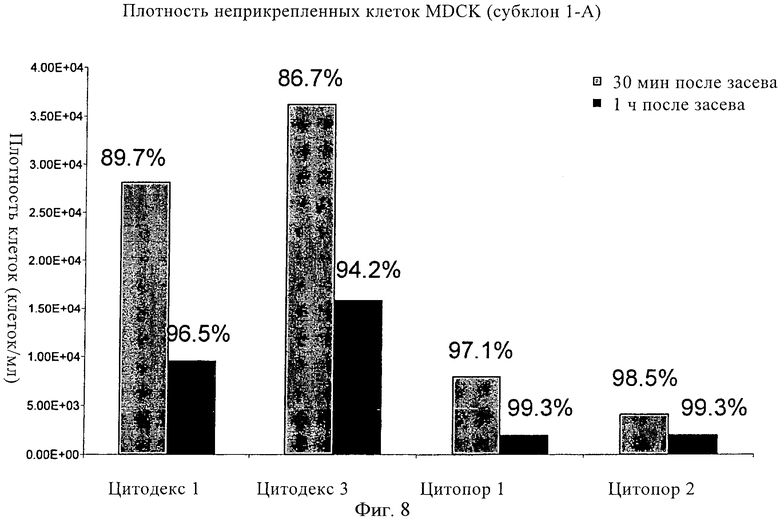
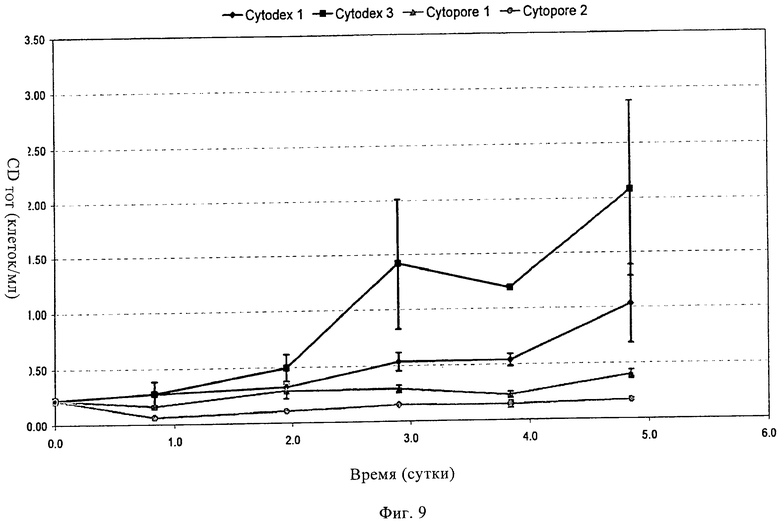
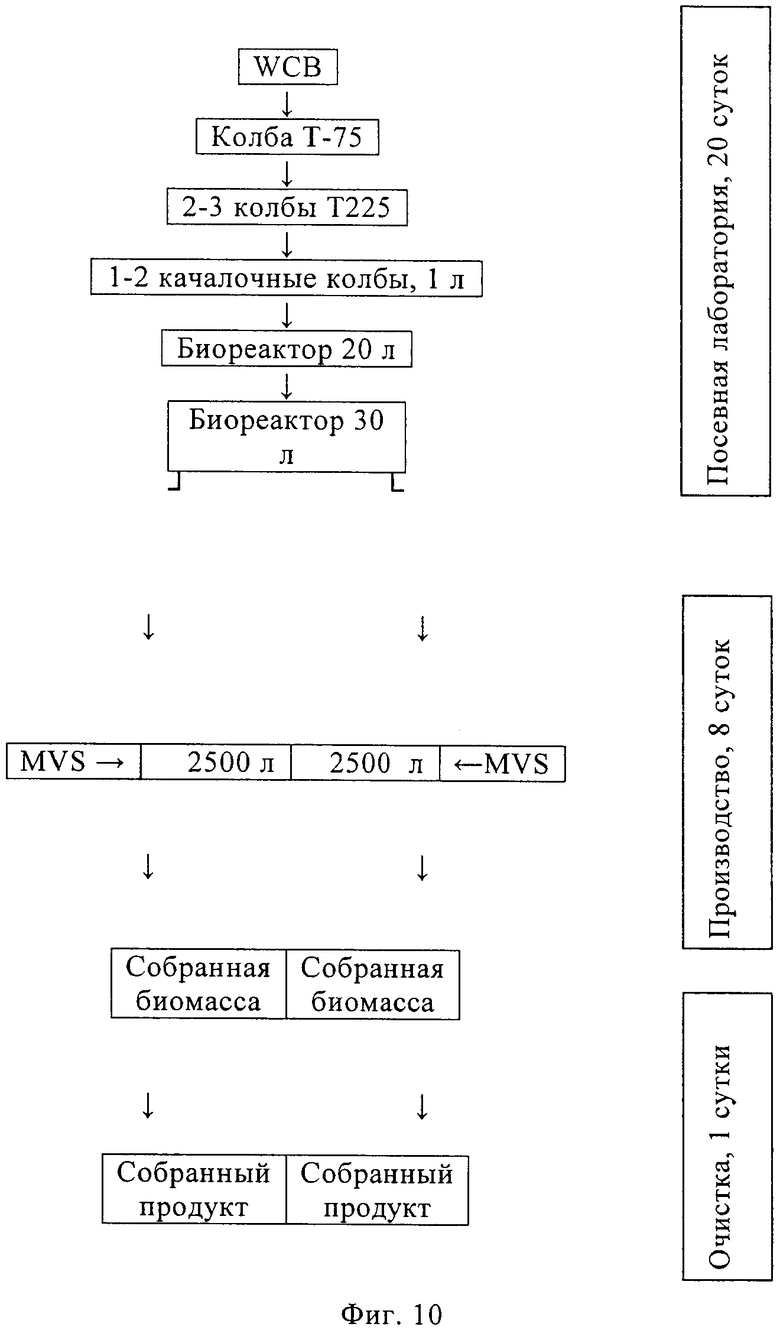

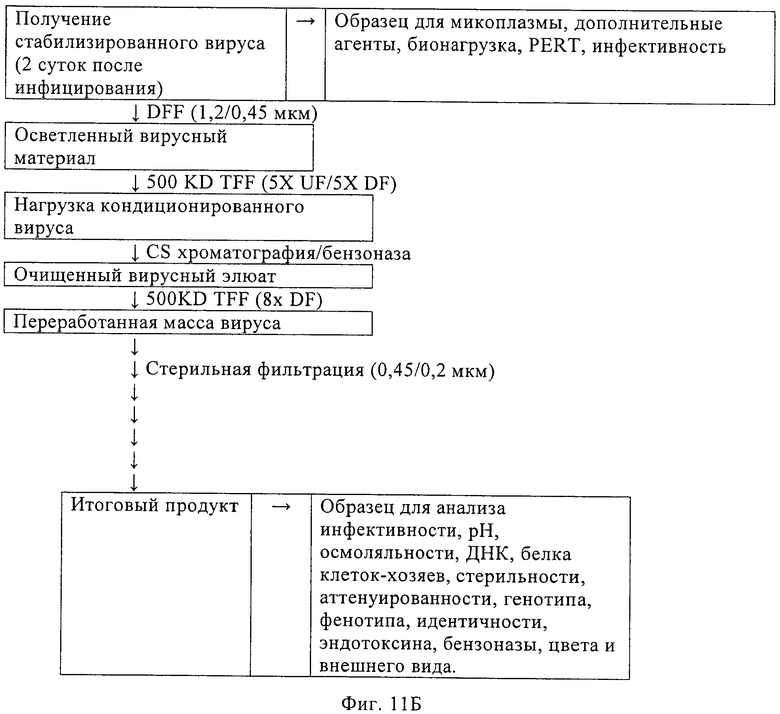
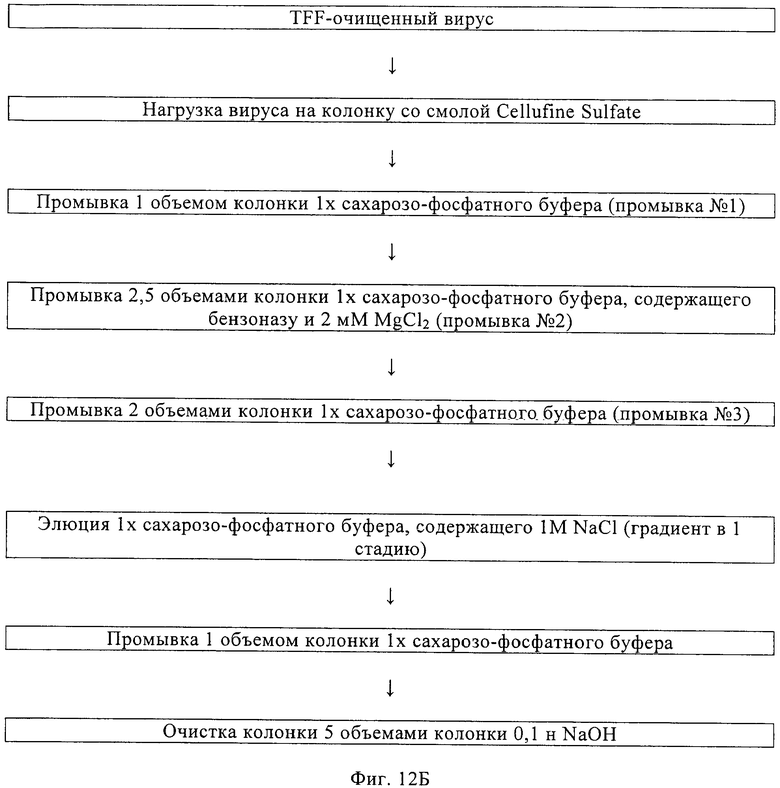
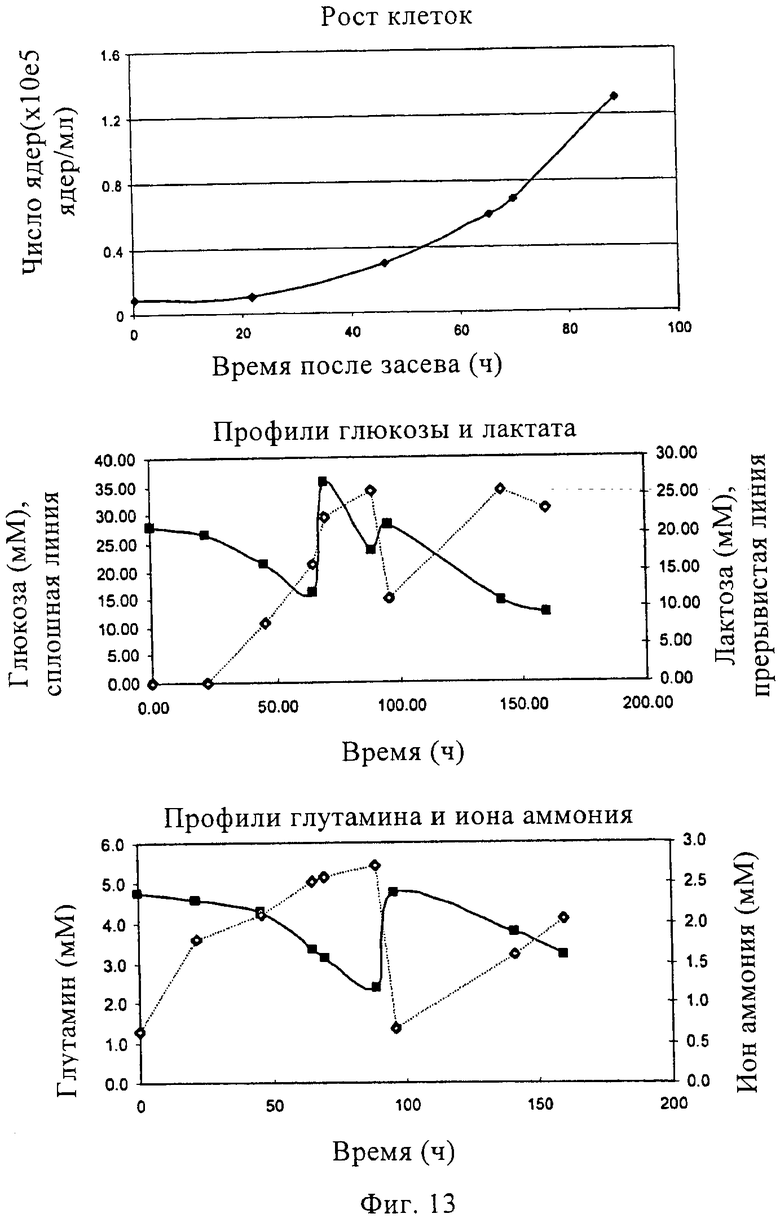
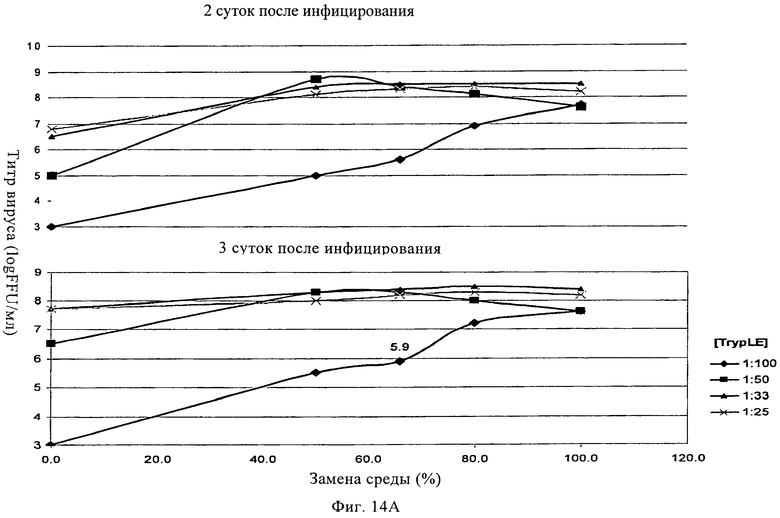
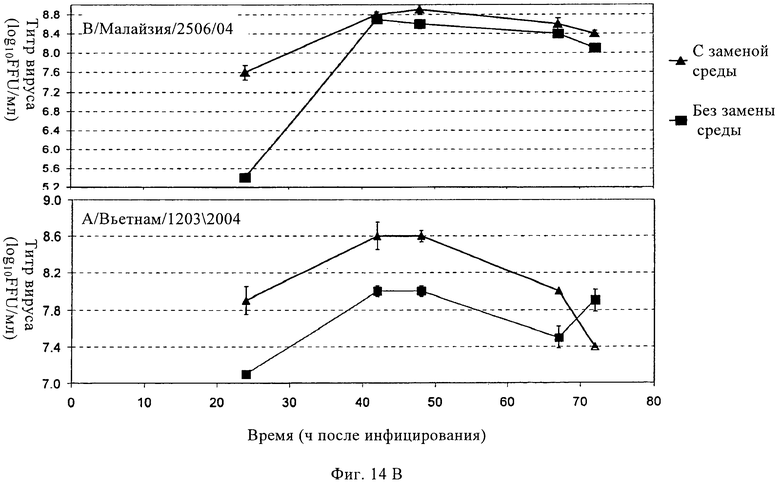
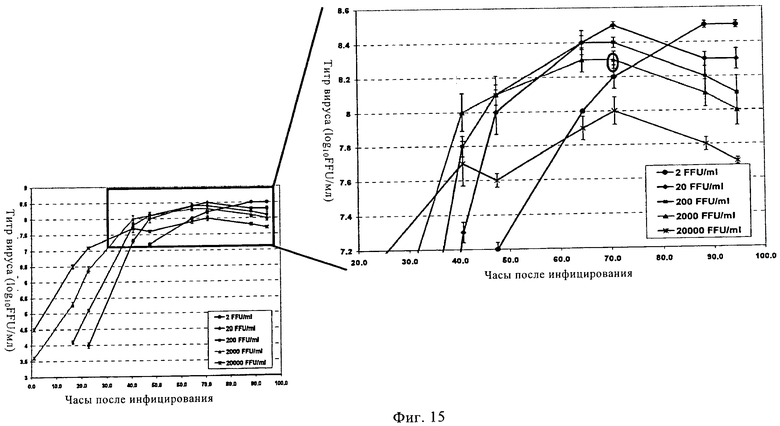
Изобретение относится к области биотехнологии, клеточных технологий и вирусологии. Описаны новые штаммы клеток почки собаки Майдин-Дэрби (MDCK). Штаммы используются для размножения вирусов, в частности вируса гриппа, в культуре клеток до более высокого титра по сравнению с ранее достигавшимися титрами. Клетки MDCK могут быть адаптированы к культуральной среде без сыворотки. Также описан способ получения вирусов гриппа в культуре клеток, в которых используют клетки MDCK по настоящему изобретению. 3 н. и 25 з.п. ф-лы, 20 ил., 20 табл., 14 пр.
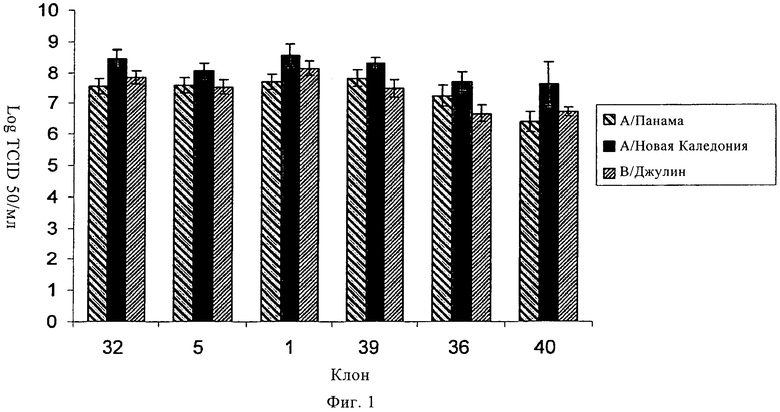
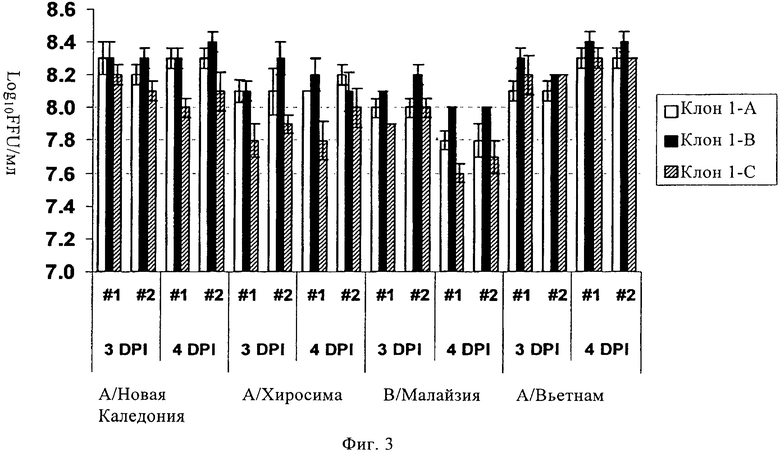
1. Линия клеток почки собаки Майдин-Дэрби (MDCK), депонированная в коллекции АТСС под номером РТА-7909 и поддерживающая репликацию адаптированного к холоду вируса гриппа до выраженной десятичным логарифмом величины средней инфицирующей культуру ткани дозы на миллилитр (log10 TCID50/мл), составляющей по меньшей мере примерно 7,8 или выше, или до выраженного десятичным логарифмом количества единиц флуоресцентного фокусирования на миллилитр (log10 FFU/мл), составляющего по меньшей мере примерно 7,8 или выше; причем композиция культуры клеток этой линии включает множество клеток MDCK и среду для культивирования клеток, которая не содержит сыворотки, выбранную из группы, состоящей из сред MediV-105, MediV-105 с добавлением глюкозы, М-32, М-32 с добавлением глюкозы, MediV-107, MediV-107 с добавлением глюкозы.
2. Линия клеток MDCK по п.1, причем клетки MDCK являются агрегированными, неопухолеродными и/или незлокачественными.
3. Линия клеток MDCK по п.1 или 2, причем вирус гриппа аттенуирован.
4. Линия клеток MDCK по пп.1, 2 или 3, причем вирус гриппа чувствителен к температуре.
5. Линия клеток MDCK по любому из пп.1-4, где вирус гриппа включает один или несколько генных сегментов штаммов вируса гриппа A/Ann Arbor/6/60 или B/Ann Arbor/1/66.
6. Линия клеток по п.1, где средой для культивирования клеток является среда MediV-105 или MediV-105 с добавлением глюкозы.
7. Линия клеток почки собаки Майдин-Дэрби (MDCK), депонированная в коллекции АТСС под номером РТА-7910 и поддерживающая репликацию адаптированного к холоду вируса гриппа до выраженной десятичным логарифмом величины средней инфицирующей культуру ткани дозы на миллилитр (log10 TCID50/мл), составляющей по меньшей мере примерно 7,8 или выше, или до выраженного десятичным логарифмом количества единиц флуоресцентного фокусирования на миллилитр (log10 FFU/мл), составляющего по меньшей мере примерно 7,8 или выше; причем композиция культуры клеток этой линии включает множество клеток MDCK и среду для культивирования клеток, которая не содержит сыворотки, выбранную из группы, состоящей из сред MediV-105, MediV-105 с добавлением глюкозы, М-32, М-32 с добавлением глюкозы, MediV-107, MediV-107 с добавлением глюкозы.
8. Линия клеток MDCK по п.7, причем клетки MDCK являются агрегированными, неопухолеродными и/или незлокачественными.
9. Линия клеток MDCK по п.7 или 8, причем вирус гриппа аттенуирован.
10. Линия клеток MDCK по пп.7, 8 или 9, причем вирус гриппа чувствителен к температуре.
11. Линия клеток MDCK по любому из пп.8-10, где вирус гриппа включает один или несколько генных сегментов штаммов вируса гриппа A/Ann Arbor/6/60 или B/Ann Arbor/1/66.
12. Линия клеток по п.11, где средой для культивирования клеток является среда MediV-105 или MediV-105 с добавлением глюкозы.
13. Способ репликации вируса гриппа в системе биореактора однократного применения (SUB), включающий:
(а) культивирование клеток почки собаки Майдин-Дэрби MDCK по любому из пп.1-5 и 7-11 в системе биореактора однократного применения (SUB) в присутствии микроносителя при культуральных условиях, которые предусматривают перемешивание, и продуцирование, таким образом, культивируемых клеток,
(б) инфицирование клеток вирусом гриппа с получением инфицированных клеток,
(в) инкубирование инфицированных клеток в условиях, допускающих репликацию вируса гриппа.
14. Способ по п.13, причем условия для культивирования не являются бессывороточными.
15. Способ по п.14, в условия культивирования включают среду для культивирования клеток, которая выбрана из группы, состоящей из сред MediV-105, MediV-105 с добавлением глюкозы, М-32, М-32 с добавлением глюкозы, MediV-107, MediV-107 с добавлением глюкозы.
16. Способ по п.15, в котором среда для культивирования клеток включает MediV-105 или MediV-105 с добавлением глюкозы.
17. Способ по любому из пп.13-16, где скорость перемешивания составляет от 80 об/мин до 120 об/мин.
18. Способ по п.17, где скорость перемешивания составляет от 90 об/мин до 100 об/мин.
19. Способ по любому из пп.13-18, в котором свежую среду или дополнительные компоненты среды вносят в культуру клеток до, в течение или после стадии (а).
20. Способ по п.19, в котором свежая среда или дополнительные компоненты среды включают протеазу.
21. Способ по п.20, в котором протеазой является сериновая протеаза.
22. Способ по п.21, где протеазой является трипсин.
23. Способ по любому из пп.13-18, в котором некоторое количество среды для культивирования клеток удаляют или не удаляют, и замещают свежей средой перед стадией (б) или на стадии (б).
24. Способ по любому из пп.13-23, в котором стадию (б) проводят при множественности заражения (МЗ) примерно от 0,00001 до примерно 0,003 FFU/клетку.
25. Способ по п.24, в котором стадию (б) проводят при множественности заражения (МЗ) примерно от 0,001 до примерно 0,003 FFU/клетку.
26. Способ по п.13, где протеазу добавляют в биореактор однократного применения до, одновременно с или после этапа (б).
27. Способ по п.26, в котором протеазой является сериновая протеаза.
28. Способ по п.27, где протеазой является трипсин.
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| US 6726907 В1, 27.04.2004. | |||
Авторы
Даты
2013-07-20—Публикация
2007-09-14—Подача