Изобретение относится к биотехнологии, в частности к генетической инженерии, и может быть использовано в медицине для выявления генетического материала (РНК) вируса Эбола-Заир в клинических или секционных пробах, в образцах внешней среды с целью постановки диагноза или коррекции лечения, а также для решения научно-исследовательских задач по изучению свойств филовирусов, созданию диагностических, профилактических или лечебных препаратов против филовирусов. При помощи набора диагностических праймеров возможно одновременное выявление генетического материала (РЕК) вирусов Эбола-Заир в исследуемом образце.
Вирусы Эбола входят в семейство филовирусов (Filoviridae). Семейство Filoviridae, в соответствии с последними решениями Международного Таксономического Комитета, включает в себя два рода: Marburgvirus и Ebolavirus (http://www.ncbi.nlm.nih.gov/ICTVdb/Ictv/index.htm).
Род Ebolavirus включает в себя 4 вида:
- Эболавирус Рестон (Reston ebolavirus - REBOV);
- Эболавирус Судан (Sudan ebolavirus - SEBOV);
- Эболавирус леса Тай (Tai Forest ebolavirus - TFEBOV);
- Эболавирус Заир (Zaire ebolavirus - ZEBOV).
Заболевания, вызванные вирусом Эбола, протекают с одинаковыми клиническими проявлениями. Необходимость диагностировать филовирусы друг от друга вызвана как минимум двумя причинами. Во-первых, дифференциация геморрагической лихорадки Марбург от геморрагической лихорадки Эбола необходима, потому что для лечения этих заболеваний может использоваться специфический иммуноглобулин. Антигенного перекреста между вирусом Марбург и вирусом Эбола нет, и иммуноглобулины от одного заболевания не помогут при лечении другого. Вторая причина необходимости идентификации вида филовируса связана с тем, что правильное молекулярно-эпидемиологическое заключение необходимо для проведения адекватных и своевременных мероприятий санитарно-эпидемиологического надзора.
Известны праймеры (аналог) для определения генетического материала вирусов Марбург и Эбола [Zhai J., Palacios G., Towner J.S et al Rapid Molecular Strategy for Filovirus Detection and Characterization // J.Clin. Microbiol., 2007, 45(1): 224-6.].
Однако накопление данных по геномному разнообразию филовирусов и детальный анализ этих данных показали, что и этот набор праймеров в ряде случаев может не обеспечить надежной идентификации филовирусов, поскольку были выявлены геноварианты вируса, для которых вышеназванные наборы праймеров не обладают достаточной специфичностью, чтобы обеспечить надежный синтез целевых фрагментов ДНК. Для ПЦР использованы не меченые флюорофором праймеры, и это не позволяет определить количество РНК вируса в анализируемой пробе. Кроме этого, с помощью предложенных праймеров можно провести только один раунд ПЦР, а по данным литературы [Towner J.S., Rollin Р.Е., Bausch D.G. et al. Rapid Diagnosis of Ebola Hemorrhagic Fever by Reverse Transcription-PCR in an Outbreak Setting and Assessment of Patient Viral Load as a Predictor of Outcome // J.Virol., 2004, 78(8): 4330-11] чувствительность тест-систем, использующих однораундовый ПЦР, составляет 100-1000 РНК вируса. Однораундовая тест-система, ввиду низкой чувствительности, может не определить наличие РНК вируса, как например это было в случае туристки из Колорадо (2008 год), у которой после возвращения из Уганды на 10 сут после появления клинических признаков заболевания РНК вируса Марбург определена не была. При перестановке этого же образца двураундовым ПЦР уже через 6 мес (когда ИФА тест показал нарастание антител к вирусу Марбург) РНК вируса Марбург была обнаружена [Fujita N., Miller A., Gershman К. et al. Imported Case of Marburg Hemorrhagic Fever, Colorado, 2008 // JAMA, 2010, 303 (5): 413-5. (Reprinted MMWR. 2009; 58: 1377-1381)].
Наиболее близким аналогом (прототипом) являются семейство-специфичные олигонуклеотидные праймеры, которые позволяют выявить наличие в образце одного из представителей семейства филовирусов методом ПЦР [Grolla A., Lucht A., Dick D., Strong J. Е., Feldmann Н. Laboratory diagnosis of Ebola and Marburg hemorrhagic fever // Bull Soc Pathol Exot, 2005, 98 (3): 205-209].
Однако для проведения ПЦР используются семейство-специфичные праймеры, которые позволяют выявить наличие в образце одного из представителей семейства филовирусов, и не позволяет идентифицировать вид вируса. При лечении больного сывороткой или плазмой важно знать, к какому виду относится вирус, вызвавший заболевание, в противном случае эффективность лечения будет существенно снижена. Кроме этого определение вида филовируса очень важно и для организации противоэпидемических мероприятий.
Техническим результатом заявляемого изобретения является создание более специфичного набора олигонуклеотидных праймеров и зондов для идентификации генетического материала вируса Эбола-Заир в клинических образцах и биологических жидкостях, образцах внешней среды и других вируссодержащих пробах (культуральная вируссодержащая жидкость и т.д) методом мультиплексного ПЦР в режиме реального времени.
Указанный технический результат достигается путем сконструированного набора олигонуклеотидных праймеров и флуоресцентно-меченых зондов (на консервативную область L-гена, кодирующего РНК полимеразу вируса Эбола-Заир для видоспецифичной экспресс-идентификации вируса Эбола методом полимеразной цепной реакции в реальном времени, включающий - последовательности, видоспецифичные для вируса Эбола-Заир:
внешние:
5'→3' 5' CCACTTTTCTCAACCAAAATTATTAGTGA 3'
3'←5' 5' TTCTCTAAATCAGTTACAAARCTACTCCC 3'
внутренние:
5'→3' 5' TGGGATGCAGTHTTYGARCC 3'
3'←5' 5' ACTACCATCATATTGCTAGGAAATGCTT 3'
зонд:
FAM - TACTACCACAATATCGGAACTTTTCTTTCTCATTGAA -BHQ1
На начальном этапе для каждого из вирусов были подобраны и синтезированы пары специфических олигонуклеотидных праймеров и зонды для гибридизационно-флуоресцентной детекции продуктов ПНР.
Для этого в базе данных NCBI Mega BLAST (http://www.ncbi.nlm.nih.gov/) были выбраны наиболее консервативные участки геномов вируса Эбола-Заир. Были проанализированы все имеющиеся в литературе последовательности каждого из вирусов. Для всех филовирусов участки-мишени генома соответствовали L-гену, кодирующему основной компонент РНК-полимеразы. Последовательности праймеров и зондов, температуры их отжига, и размеры продуктов амплификации представлены в таблице 1.
Подбор и анализ свойств олигонуклеотидных праймеров и зондов проводился с использованием программного обеспечения Vector NTI 9.0.0 (InforMax).
Пример 1. Проверка аналитической чувствительности набора праймеров и зондов.
Для контроля амплификации были получены положительные контрольные образцы, представляющие собой рекомбинантные плазмиды, несущие вирусспецифические вставки, являющиеся матрицей для амплификации вирусспецефических ДНК-фрагментов.
Для проведения ПЦР в режиме реального времени в качестве анализируемых образцов использовали рекомбинантную плазмидную ДНК, включающую вставку ДНК, соответствующую детектируемым участкам геномов вируса Эбола-Заир.
Условия проведения амплификации оптимизировались по следующим параметрам: концентрация ионов магния в реакционной смеси; концентрация праймеров и зондов в реакционной смеси; температура отжига праймеров.
Для определения чувствительности набора из концентрированного раствора плазмидной ДНК были приготовлены последовательные 10-кратные разведения. Определение концентрации ДНК в разведениях при исследовании чувствительности праймеров осуществляли при помощи флуориметра QUBIT (Invitrogen, США) и наборов реагентов производителя.
ПЦР в режиме реального времени и регистрацию результатов проводили в приборе Rotor Gene 6000 (Corbett Research, Австралия) по каналам Green (470 nm /510 nm) и Yellow (530 nm/555 nm).
В результате выполненных экспериментов было определено минимальное количество рекомбинантной плазмидной ДНК, содержащей фрагмент генома вируса Эбола-Заир. При использовании внешних праймеров к геному вируса Эбола-Заир - 0.03 плазмидной ДНК.
Для определения аналитической чувствительности моновариантов систем «праймеры-зонд» для детекции каждого вируса из концентрированных растворов положительных контрольных образцов были приготовлены последовательные 10-кратные разведения. Определение концентрации ДНК в разведениях при исследовании чувствительности праймеров осуществляли при помощи коммерческого набора «Quant-iT dsDNA, HS» («Invitrogen», США) и флуориметра QUBIT («Invitrogen», США). Минимальное количество ДНК-матриц, детектируемое с применением заявляемых праймеров и зондов после оптимизации условий проведения реакции, выраженное в ГЭ (геномных эквивалентах) в 30 мкл реакционной смеси, представлено в таблице 2.
Пример 2. Определение РНК вируса Эбола-Заир в вируссодержащих образцах
Оценку эффективности выявления генетического материала вирусов проводили на штамме Mayinga вируса Эбола-Заир. Штаммом вируса Эбола заражали 10 мышей линии BALB/c. На 5 сут у животных забирали кровь и определяли наличие специфической вирусной РНК.
Предварительную инактивацию образцов и выделение РНК проводили в условиях, регламентированных Методическими указаниями МУ 1.3. 2569 -09 «Организация работы лабораторий, использующих методы амплификации нуклеиновых кислот при работе с материалом, содержащим микроорганизмы I-IV групп патогенности».
Процедуру выделения РНК из исследуемого материала проводили с использованием набора «Комплект реагентов для выделения ДНК/РНК из сыворотки или плазмы крови» (НПФ Литех, Россия) в соответствии с инструкцией по применению.
ПЦР в режиме реального времени проводили с праймерами F13060 и R13367, фланкирующими участок ДНК в 307 п.н., в реакционной смеси следующего состава (на 1 исследование):
Реакцию обратной транскрипции проводили с использованием набора реагентов «Реверта-L» (ЦНИИЭ, Россия) в соответствии с инструкцией по применению.
В качестве отрицательного контрольного образца в реакционную смесь добавляли ТЕ-буфер.
ПЦР в режиме реального времени и регистрацию результатов проводили в приборе Rotor Gene 6000 (Corbett Research, Австралия) по следующей программе, приведенной в таблице 3:
Детекцию сигнала флуоресценции осуществляли при шаге циклирования 55 0С на канале Green (470 nm /510 nm) для вирусов Эбола-Заир.
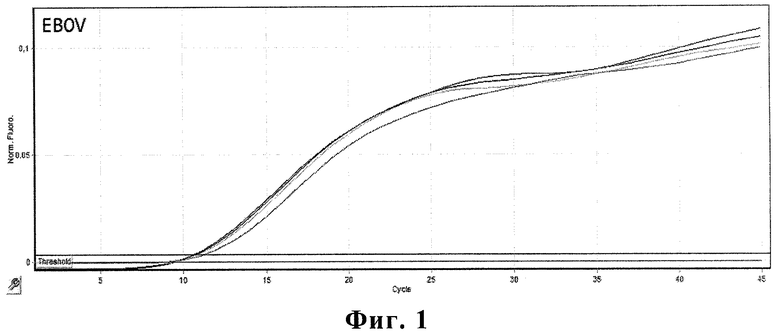
Результаты интерпретировали на основании наличия (или отсутствия) пересечения кривой флуоресценции с установленной на соответствующем уровне пороговой линией, что соответствует наличию (или отсутствию) значения порогового цикла Ct в соответствующей графе в таблице результатов. Результат считали положительным в случае, если кривая накопления флуоресценции для соответствующего образца имела характерную «сигмовидную» форму и пересекала пороговую линию. При этом значение Ct для данного образца было не больше 40 (фиг.1).
На фиг.1 приведены кривые флуоресценции на трех оптических каналах амплификатора Rotor Gene 6000 (Corbett Research, Австралия). Флуоресценция в образцах, содержащих: генетический материал: вируса Эбола-Заир и Эбола-Судан (EBOV) - 4 образца на канале Green.
Таким образом, из вышеприведенных примеров 1 и 2 видно достижение заявляемого технического результата: создан
видоспецифичный набор олигонуклеотидных праймеров и зондов для идентификации генетического материала вируса Эбола-Заир в клинических образцах и биологических жидкостях, образцах внешней среды и других вируссодержащих пробах (культуральная вируссодержащая жидкость и т.д) методом мультиплексного ПЦР в режиме реального времени.
Приложение. Перечень последовательностей
Последовательности, видоспецифичные для вируса Эбола-Заир:
внешние:
5'→3' 5' CCACTTTTCTCAACCAAAATTATTAGTGA 3'
3'←5' 5'TTCTCTAAATCAGTTACAAARCTACTCCC 3'
внутренние:
5'→3' 5' TGGGATGCAGTHTTYGARCC 3'
3'←5' 5' ACTACCATCATATTGCTAGGAAATGCTT 3'
зонд:
FAM - TACTACCACAATATCGGAACTTTTCTTTCTCATTGAA - BHQ1.
Изобретение относится к области биотехнологии и касается набора олигонуклеотидных праймеров и флуоресцентно-меченых зондов для видоспецифичной экспресс-идентификации вируса Эбола-Заир методом полимеразной цепной реакции в реальном времени. Набор включает последовательности, видоспецифичные для вируса Эбола-Заир:
внешние: 5'→5' CCACTTTTCTCAACCAAAATTATTAGTGA 3'
3'←5'5' TTCTCTAAATCAGTTACAAARCTACTCCC 3'
внутренние: 5'→3'5' TGGGATCCAGTHTIYGARCC 3'
3'←5'5' ACTACCATCATATTGCTAGGAAATGCTT 3'
зонд: FAM - TACTACCACAATATCGGAACTTTTCTTTCTCATTGAA - BHQ1.
Представленное изобретение может быть использовано в медицине для быстрого выявления генетического материала (РНК) вируса Эбола-Заир. 1 ил., 3 табл., 2 пр.
Набор олигонуклеотидных праймеров и флуоресцентно-меченых зондов для видоспецифичной экспресс-идентификации вируса Эбола-Заир методом полимеразной цепной реакции в реальном времени, включающий последовательности, видоспецифичные для вируса Эбола-Заир: внешние:
5'→'3'5' CCACTTTTCTCAACCAAAATTATTAGTGA 3'
3'←5'5' TTCTCTAAATCAGTTACAAARCTACTCCC 3'
внутренние:
5'→3'5' TGGGATGCAGTHTTYGARCC 3'
3'←5'5' ACTACCATCATATTGCTAGGAAATGCTT 3'
зонд:
FAM - TACTACCACAATATCGGAACTTTTCTTTCTCATTGAA - BHQ1.
| СПОСОБ ОБНАРУЖЕНИЯ НАЛИЧИЯ МИКРООРГАНИЗМОВ В БИОЛОГИЧЕСКОМ ОБРАЗЦЕ | 2007 |
|
RU2435865C2 |
| JUNHUI ZHAI et al., Rapid Molecular Strategy for Filovirus Detection and Characterization, journal of clinical microbiology, Jan | |||
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
Авторы
Даты
2013-07-20—Публикация
2012-02-08—Подача