Изобретение относится к наборам праймеров и флуоресцентно-меченого зонда для выявления генетического материала (РНК) респираторно-синцитиального вируса человека в клинических образцах, секционных пробах, образцах окружающей среды, культуральных вируссодержащих жидкостях и прочих биопрепаратах с целью постановки диагноза, коррекции лечения, эпидемиологического расследования, а также для решения научно-исследовательских задач по мониторингу и изучению свойств респираторно-синцитиального вируса, созданию диагностических, профилактических и лечебных препаратов и может быть использовано в медицине, биотехнологии и эпидемиологии.
При помощи разработанных диагностических праймеров и флуоресцентно-меченых зондов возможно выявление генетического материала (РНК) респираторно-синцитиального вируса человека.
Метод полимеразной цепной реакции с обратной транскрипцией (ОТ-ПЦР) является наиболее распространенным методом, используемым в лабораторной практике для дифференциальной диагностики инфекционных заболеваний. В основе метода лежат две реакции - обратная транскрипция и полимеразная цепная реакция. В реакции обратной транскрипции на матрице вирусной РНК строится комплиментарная ДНК (кДНК). В следующей за реакцией обратной транскрипции ПЦР происходит многократное избирательное удвоение целевого участка кДНК (амплификация). Амплифицируемый участок кДНК является маркерным, так как строго ограничен последовательностями ДНК-затравок (праймеров), без которых невозможно протекание ПЦР. Для детекции накопления продуктов амплификации в режиме реального времени помимо пары праймеров необходим также флуоресцентно-меченый ДНК-зонд. Сложность выбора праймеров и зонда обусловлена требованием их строгой видоспецифичности. В случае если выбранные олигонуклеотиды не обладают видовой специфичностью к целевому объекту либо не обладают достаточной гомологией к целевой нуклеотидной последовательности, возможны ложноотрицательные результаты исследования. В случае если выбранные праймеры и зонды демонстрируют сродство к нецелевым последовательностям ДНК, то возможны ложноположительные результаты исследования. Правильный выбор сочетания пары праймеров и флуоресцентно-меченого ДНК-зонда позволяет осуществить строго специфическую амплификацию целевого фрагмента кДНК и провести детекцию накопления продуктов ПЦР в режиме реального времени.
Известны зарубежные аналоги олигонуклеотидов, позволяющие производить детекцию респираторно-синцитиального вируса человека. В патенте Китая № CN 1544656, опубл. 2004 г., представлены олигонуклеотидные праймеры и флуорогенные зонды, позволяющие проводить количественную ПЦР в реальном времени. В патенте Канады № СА 2236022, опубл. 1997 г., и заявке США №1182004253582, опубл. 2004 г., представлены олигонуклеотиды, позволяющие произвести детекцию генетического материала (РНК) респираторно-синцитиального вируса человека методом ПЦР в реальном времени. В заявке США №20100221711, опубл. 2010 г., приведен набор реагентов, позволяющих детектировать в клинических образцах от людей и животных респираторно-синцитиальный вирус и произвести оценку вирусной нагрузки, а в заявке США №20040253582, опубл. 2004 г., опубликован набор реагентов, позволяющих детектировать геномную РНК респираторно-синцитиального вируса человека типов A и B в клинических образцах.
Наиболее близким аналогом (прототипом) является набор праймеров для детекции кДНК респираторно-синцитиальный вируса человека методом ПЦР "АмплиСенс®ОРВИ-скрин-FL" (http://www.pacxodka39.ru/product_3056.html ЦНИИ Эпидемиологии, г.Москва). Набор реагентов предназначен для выявления возбудителей острых респираторных вирусных инфекций человека (ОРВИ): РНК респираторно-синцитиального вируса, РНК метапневмовируса, вирусов парагриппа 1-4 типов, коронавирусов, риновирусов, ДНК аденовирусов групп В, С и Е и бокавируса в клиническом материале методом полимеразной цепной реакции (ПЦР) с гибридизационно-флуоресцентной детекцией.
Однако в известных аналогах и прототипе праймеры имеют недостаточный уровень гомологии ко всем циркулирующим в настоящее время респираторно-синцитиальным вирусам человека в природе, а также имеющимся в базе данных геномам метапневмовируса человека, что снижает надежность и достоверность диагностики указанного вируса с использованием заявляемых праймеров.
Техническим результатом заявляемого изобретения является расширение спектра импортозамещающих олигодезоксирибонуклеотидных праймеров и флуоресцентно-меченых зондов, позволяющих идентифицировать РНК респираторно-синцитиального вируса человека методом ПЦР в реальном времени.
Указанный технический результат достигается разработкой набора олигодезоксирибонуклеотидных праймеров и флуоресцентно-меченых зондов для идентификации РНК респираторно-синцитиального вируса человека, содержащего две пары олигонуклеотидных полимера, обладающих активностью прямого и обратного праймеров в полимеразной цепной реакции, а также два флуоресцентно-меченых ДНК-зонда.

В рамках заявляемого технического решения разработанные праймеры и ДНК-зонды обладают высокой степенью гомологии ко всем известным нуклеотидным последовательностям геномов изолятов респираторно-синцитиального вируса человека, доступным в международной базе данных биотехнологической информации GenBank.
Заявляемый набор реагентов обладает рядом значительных преимуществ. За счет внесения «вырожденных» нуклеотидов в последовательность патентуемые праймеры и флуорогенные зонды обладают значительным уровнем гомологии ко всем имеющимся в базе данных геномам респираторно-синцитиального вируса человека. Так как набор представляет собой комплект из четырех праймеров и двух флуорогенных ДНК-зондов, можно провести двухраундовую ПЦР, что увеличивает чувствительность метода на порядки, а также позволяет получить продолжительный продукт ПЦР, нуклеотидную последовательность которого можно определить на автоматическом геномном анализаторе. Это, в свою очередь, позволяет установить многие молекулярно-биологические закономерности в области эпидемиологии, контагеозности и патогенности вируса. К тому же разработанные нами праймеры и зонды были использованы в ПЦР смесях, состоящих из компонентов отечественного производства, что делает разработку легко- и широкодоступной для применения в лабораториях Российской Федерации, это обеспечивает быстрое и надежное внедрение разработки в практику. Используемая в качестве положительного контрольного образца, плазмидная конструкция, несущая фрагмент генома респираторно-синцитиального вируса человека, может быть использована в количественной ПЦР. Это дает возможность оценить вирусную нагрузку в исследуемом образце.
Апробация олигонуклеотидов была осуществлена с использованием назо-фарингеальных смывов от пациентов с симптомами ОРВИ (порядок проведения исследования одобрен этическим комитетом ФБУН ГНЦ ВБ «Вектор» (IRB 00001360)). Экспериментально было показано, что выбранные праймеры и ДНК-зонд обеспечивают надежный синтез целевых ДНК-фрагментов. Специфичность амплификации дополнительно подтверждали секвенированием.
Характеристика набора праймеров и участка амплифицируемой геномной РНК. Предлагаемые к патентованию праймеры фланкируют участок гена кодирующего гликопротеин слияния - fusion protein (F-ген). В первом раунде ПЦР амплифицируется фрагмент генома с 6509 по 7091 нуклеотид (582 п.н.), во втором - с 6767 по 6970 нуклеотид (203 п.н.). Использование в комплекте с диагностическими праймерами флуоресцентно-меченых ДНК-зондов позволяет производить детекцию накопления продуктов амплификации в режиме реального времени.
Важно отметить, что оптимизация условий проведения ПЦР осуществлялась с использованием наборов коммерчески доступных реагентов, приборов и ферментов, предназначенных для массового использования в лабораторной практике, что позволяет быстрое и надежное применение данного изобретения в медицинских и научно-исследовательских лабораториях.
Перечень графических материалов
На фиг.1. показаны результаты анализа клинических образцов методом ПЦР в реальном времени с использованием патентуемых олигонуклеотидов.
Методика конструирования набора диагностических праймеров и флуоресцентно-меченых зондов
На основе теоретического изучения структуры генома респираторно-синцитиального вируса человека на консервативную область гена вирусного гликопротеина слияния - fusion protein (F-ген) были рассчитаны и синтезированы праймеры и флуоресцентно-меченые ДНК-зонды для проведения полимеразной цепной реакции (таблица 1). В ходе работы было проанализировано 1562 имеющихся в базе данных нуклеотидных последовательностей генома респираторно-синцитиального вируса человека.
Методика получения положительных контрольных образцов
Положительные контрольные образцы были получены методом TOPO-T/A клонирования. После чего компетентные клетки Е. coli линии ТОР 10 (Invitrogen, США) были трансформированы полученными плазмидами pCR2.1 (Invitrogen, США), несущими вирусспецифическую вставку синтезированных фрагментов ДНК. В ходе проделанной работы была сконструирована рекомбинантная плазмида: pRSV. Наличие специфической к вирусному геному ДНК-вставки подтверждали секвенированием.
Анализ эффективности проведенной трансформации осуществляли проведением ПЦР в режиме реального времени в соответствии с протоколом, описанным ниже, где в реакционную смесь в качестве положительного образца добавляли 1×TE-буфер, содержащий рекомбинантную плазмиду pRSV, со встройкой вирусспецифического синтезированного ДНК-дуплекса. В качестве отрицательного контрольного образца в реакционную смесь добавляли 1×ТЕ-буфер.
Экстракция вирусной РНК. Вирусную РНК выделяли из 100 мкл назофарингеального смыва с использованием набора «РИБО-преп» (ЦНИИЭ, г.Москва) согласно инструкции производителя.
Реакция обратной транскрипции. Синтез комплементарной ДНК (кДНК) проводили на матрице суммарной РНК с использованием набора реагентов «Реверта-L» (ЦНИИЭ, г.Москва) согласно инструкции производителя.
Проведение полимеразной цепной реакции. Условия проведения амплификации оптимизировали по концентрации ионов магния, концентрации праймеров и зондов в реакционной смеси, температуре отжига праймеров.
Реакцию амплификации проводили в 30 мкл смеси для ПЦР (таблицы 2 и 3), содержащей 1×Taq буфер для амплификации, 2.5 мМ MgCl2, 0.17 мМ каждого из нуклеозидтрифосфатов, 1.5 активных единиц Smart Taq ДНК-полимеразы (все компоненты ООО «Лаборатория МЕДИГЕН»), 20 пМ прямого и обратного праймеров, 8 пМ флуоресцентного ДНК-зонда.
Первый раунд ПЦР проводили согласно программе амплификации (таблица 4) на приборе Mastercycler gradient (BioRad, США). Контроль эффективности прохождения первого раунда ПЦР проводили разделяя продукты амплификации в 2% агарозном геле.
ПЦР в режиме реального времени проводили согласно программе амплификации, представленной в таблице 5. Детекцию интенсивности флуоресценции проводили по каналу - Green 470/510 нм (краситель FAM). Измерение флуоресценции проводили на приборах "Rotor Gene 6000" (Corbet Research, Австралия) и iQ5 (BioRad, США). Результаты оценивали по наличию флюоресценции до 30 цикла (фиг. 1). На фиг. 1 представлены результаты анализа клинических образцов методом ПЦР в реальном времени с использованием патентуемых олигонуклеотидов, из графиках которой видно, что: в образцах №8, 14 обнаружена РНК респираторно-синцитиального вируса человека; К+ - положительный контрольный образец (pRSV).
Апробация патентуемых олигонуклеотидов
Предлагаемые к патентованию олигонуклеотиды были авторами апробированы в эпидемиологическом исследовании по изучению видового разнообразия агентов, вызывавших ОРВИ у жителей г. Новосибирска и Новосибирской области в октябре-апреле 2011-2012 гг. Авторами было исследовано 164 образца назофарингеальных смывов от пациентов с симптомами острой респираторной вирусной инфекции. Этиологический агент заболевания был авторами установлен в 43% случаев (69 образцов). Респираторно-синцитиальный вирус в исследуемых образцах был выявлен в 4% случаев (7 образцов) (фиг. 1). В структуре сочетанных инфекций респираторно-синцитиальный вирус был выявлен авторами в 17,4% случаев (4 образца из 11). Специфичность ПЦР-исследования дополнительно подтверждали секвенированием.
Таким образом, заявляемый набор олигонуклеотидных праймеров и флуоресцентно-меченых зондов обеспечивает наравне с известными аналогами надежную и достоверную детекцию респираторно-синцитиального вируса человека в клинических образцах и других биологических материалах.

Изобретение относится к области биохимии, в частности к набору олигодезоксирибонуклеотидных праймеров и флуоресцентно-меченых зондов для идентификации РНК респираторно-синцитиального вируса человека. Указанный набор содержит две пары олигонуклеотидных праймеров и два флуоресцентно-меченых ДНК-зонда, а именно внешний прямой праймер 5'-AGRCARCARAGTTAYTCYATYATGTC-3', внешний обратный праймер 5'-AATTTATTATWGGTTYMCCYTTTACATA-3', прямой праймер 5'-GACACHATGAAYAGYTTRACATTACC-3', обратный праймер 5'-AAATGTYTTTATDATYCCRCGATTT-3', зонды 5'-FAM-TCTCTAGGAGCCATTGTGTCATGCTATGG-BHQ1-3' и 5'-FAM-TCTCTWGGAGCYATAGTGTCATGYTATGG-BHQ1-3'. Изобретение обеспечивает надежную и достоверную детекцию респираторно-синцитиального вируса человека в клинических образцах и других биологических материалах методом ПЦР. 1 ил., 5 табл.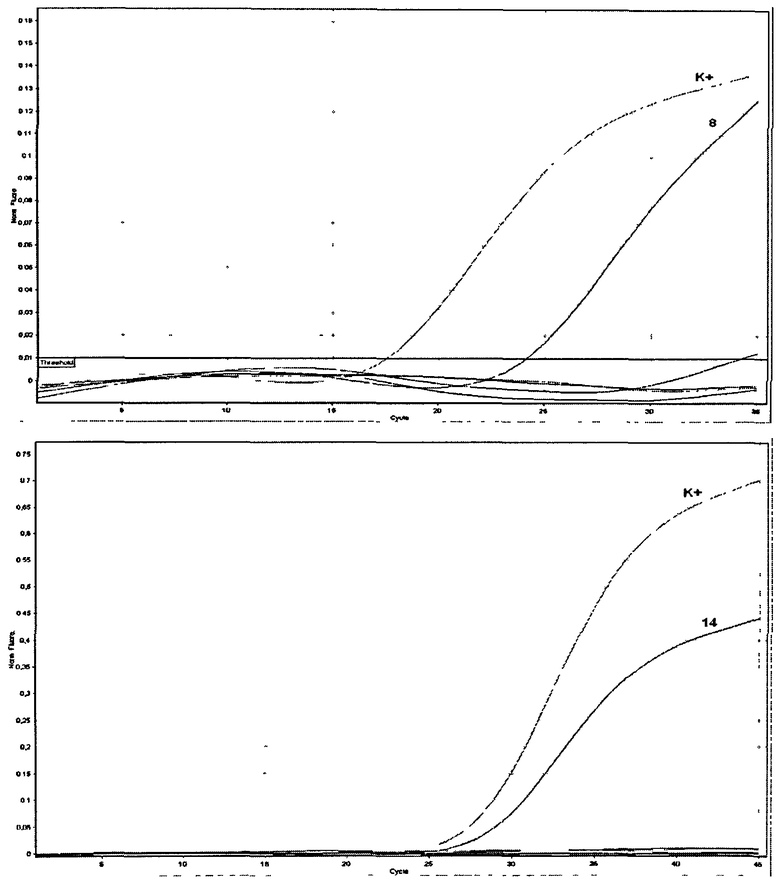
Набор олигодезоксирибонуклеотидных праймеров и флуоресцентно-меченых зондов для идентификации РНК респираторно-синцитиального вируса человека, содержащий две пары олигонуклеотидных полимера, обладающих активностью прямого и обратного праймеров в полимеразной цепной реакции, а также два флуоресцентно-меченых ДНК-зонда, имеющих следующую структуру:
- внешний прямой праймер (nested forward primer) 5'→3'
- внешний обратный праймер (nested reverse primer) 5'→3'
- прямой праймер (forward primer) 5'→3'
- обратный праймер (reverse primer) 5'→3'
- флуоресцентно-меченые ДНК-зонды (probe) 5'→3'
| PATON A.W | |||
| et al., Rapid Detection of Respiratory Syncytial Virus in Nasopharyngeal Aspirates by Reverse Transcription and Polymerase Chain Reaction Amplification, Journal of Clinical Microbiology, 1992, Vol | |||
| Способ обработки медных солей нафтеновых кислот | 1923 |
|
SU30A1 |
| Многолопастный разборный деревянный пропеллер | 1923 |
|
SU901A1 |
| НАБОР ОЛИГОНУКЛЕОТИДНЫХ ПРАЙМЕРОВ И ФЛУОРЕСЦЕНТНОМЕЧЕНЫХ ЗОНДОВ ДЛЯ ВИДОСПЕЦИФИЧНОЙ ЭКСПРЕСС-ИДЕНТИФИКАЦИИ ОРТОПОКСВИРУСОВ НА ОСНОВЕ МУЛЬТИПЛЕКСНОЙ ПЦР В РЕАЛЬНОМ ВРЕМЕНИ | 2010 |
|
RU2427648C1 |
| Устройство для растаривания мешков с сыпучим материалом | 1988 |
|
SU1544656A1 |
| US 20040253582 A1, 16.12.2004 | |||
| FREYMUTH F | |||
| et al., Detection of | |||
Авторы
Даты
2015-02-20—Публикация
2013-02-25—Подача