Текст описания приведен в факсимильном виде.

































































































































| название | год | авторы | номер документа |
|---|---|---|---|
| ИММУНОГЕННЫЕ КОМПОЗИЦИИ ДЛЯ ИММУНИЗАЦИИ СВИНЕЙ ПРОТИВ ЦИРКОВИРУСА ТИПА 3 И СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2016 |
|
RU2744193C2 |
| СЛИТЫЕ ПОЛИПЕПТИДЫ И ВАКЦИНЫ | 2014 |
|
RU2699006C2 |
| ПОЛИВАЛЕНТНЫЕ ИММУНОГЕННЫЕ КОМПОЗИЦИИ PCV2 И СПОСОБЫ ПОЛУЧЕНИЯ ТАКИХ КОМПОЗИЦИЙ | 2006 |
|
RU2577129C2 |
| ПОЛИВАЛЕНТНЫЕ ИММУННОГЕННЫЕ КОМПОЗИЦИИ PCV2 И СПОСОБЫ ПОЛУЧЕНИЯ ТАКИХ КОМПОЗИЦИЙ | 2006 |
|
RU2577127C9 |
| ВАКЦИНА MYCOPLASMA HYOPNEUMONIAE | 2013 |
|
RU2644254C2 |
| КОМБИНИРОВАННАЯ ВАКЦИНА PCV/MYCOPLASMA HYOPNEUMONIAE | 2013 |
|
RU2615443C2 |
| КОМБИНИРОВАННАЯ ВАКЦИНА PCV/MYCOPLASMA HYOPNEUMONIAE/PRRS (PCV/MYCOPLASMA HYOPNEUMONIAE/PRRS COMBINATION VACCINE) | 2013 |
|
RU2644256C2 |
| СНИЖЕНИЕ СОПУТСТВУЮЩИХ ИНФЕКЦИЙ У СВИНЕЙ С ПОМОЩЬЮ АНТИГЕНА PCV2 | 2008 |
|
RU2491092C2 |
| ИММУНОГЕННЫЕ КОМПОЗИЦИИ ДЛЯ ИММУНИЗАЦИИ СВИНЕЙ ПРОТИВ ЦИРКОВИРУСА ТИПА 3 И СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2016 |
|
RU2771533C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ИММУНИЗАЦИИ СВИНЕЙ ПРОТИВ СВИНОГО ЦИРКОВИРУСА | 2008 |
|
RU2493254C9 |
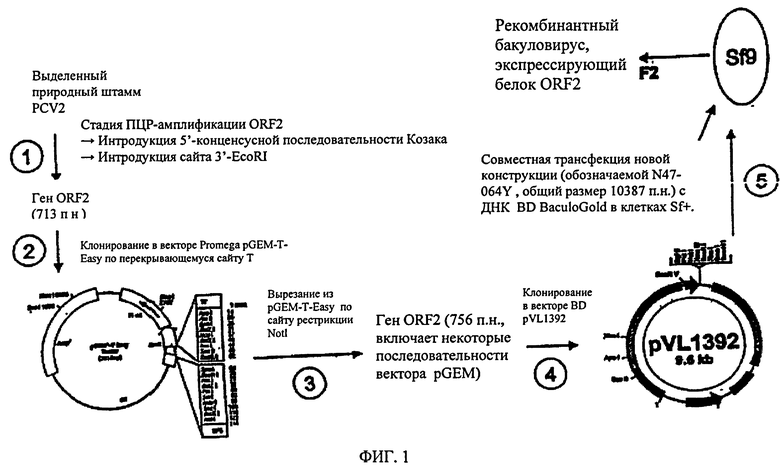
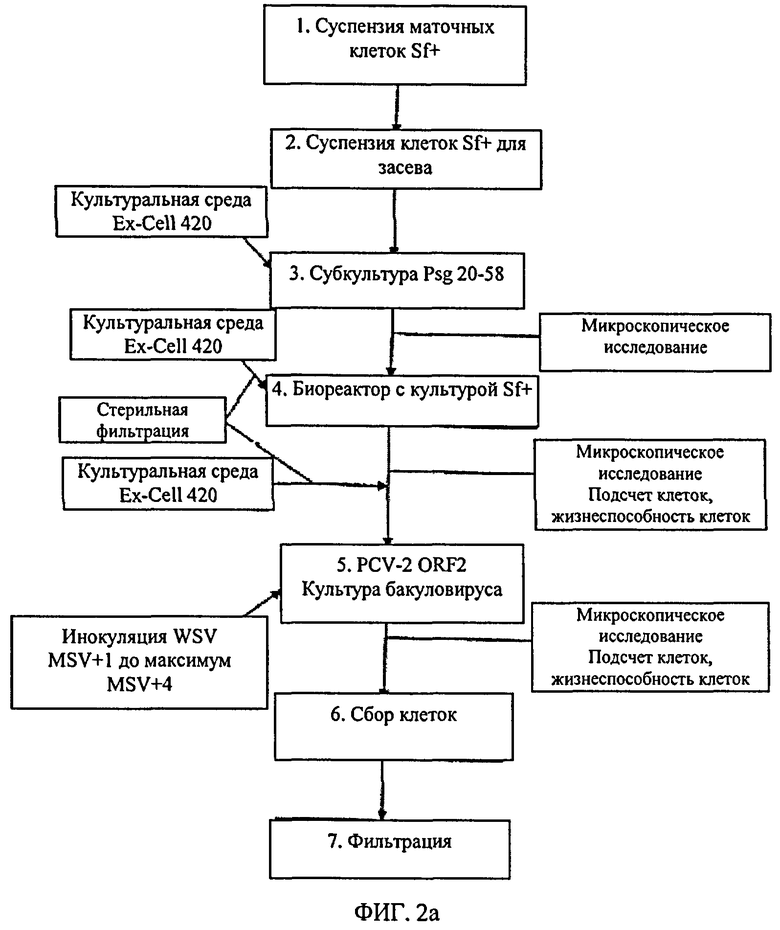
Группа изобретений относится к области медицины, а именно к биофармацевтике, и может быть использована для приготовления комбинированных вакцин. Для этого поливалентная комбинированная вакцина включает антиген цирковируса свиней типа 2 и один дополнительный компонент, эффективный в отношении другого организма, вызывающего заболевание у свиней, в которой антиген цирковируса свиней типа 2 является рекомбинантно экспрессируемым ORF2 белком цирковируса свиней типа 2, выбирается из: i) полипептида, включающего последовательность SEQ ID NO:5, SEQ ID NO:6, SEQ ID NO:9, SEQ ID NO:10 или SEQ ID NO:11, ii) любого полипептида, который по меньшей мере на 80% гомологичен полипептиду i), iii) полипептида, который кодируется ДНК, которая включает последовательность SEQ ID NO:3 или SEQ ID NO:4, iv) любого полипептида, который кодируется полинуклеотидом, который по меньшей мере на 80% гомологичен полинуклеотиду iii), v) любого полипептида, который кодируется нуклеотидными последовательностями SEQ ID NO:3 или SEQ ID NO:4, или любого полипептида, который кодируется последовательностями, отличными от SEQ ID NO:3 или SEQ ID NO:4 вследствие вплоть до 6-20% гомологии последовательности, vi) любого полипептида, отличного от SEQ ID NO:5, или любого полипептида, отличного от SEQ ID NO:6, вследствие вплоть до 6-10% гомологии последовательности. Также предложен способ снижения частоты встречаемости или понижения тяжести проявления инфекций цирковируса свиней типа 2. Группа изобретений позволяет получить высокостабильную комбинированную вакцину PCV2. 3 н. и 22 з.п. ф-лы, 3 ил.
1. Поливалентная комбинированная вакцина, включающая антиген цирковируса свиней типа 2, эффективный для снижения частоты встречаемости или понижения тяжести проявления инфекций цирковируса свиней типа 2, и по меньшей мере один дополнительный компонент иммуногенного действия, эффективный в отношении другого организма, вызывающего заболевание у свиней, в которой антиген цирковируса свиней типа 2 является рекомбинантно экспрессируемым ORF2 белком цирковируса свиней типа 2, выбирается из
i) полипептида, включающего последовательность SEQ ID NO:5, SEQ ID NO:6, SEQ ID NO:9, SEQ ID NO:10 или SEQ ID NO:11,
ii) любого полипептида, который по меньшей мере на 80% гомологичен полипептиду i),
iii) полипептида, который кодируется ДНК, которая включает последовательность SEQ ID NO:3 или SEQ ID NO:4,
iv) любого полипептида, который кодируется полинуклеотидом, который по меньшей мере на 80% гомологичен полинуклеотиду iii),
v) любого полипептида, который кодируется нуклеотидными последовательностями SEQ ID NO:3 или SEQ ID NO:4 или любого полипептида, который кодируется последовательностями, отличными от SEQ ID NO:3 или SEQ ID NO:4 вследствие вплоть до 6-20% гомологии последовательности,
vi) любого полипептида, отличного от SEQ ID NO:5, или любой полипептид, отличный от SEQ ID NO:6, вследствие вплоть до 6-10% гомологии последовательности.
2. Поливалентная комбинированная вакцина по п.1, в которой рекомбинантно экспрессируемым ORF2 белком цирковируса свиней типа 2 является экспрессируемый бакуловирусом ORF2 белок цирковируса свиней типа 2.
3. Поливалентная комбинированная вакцина по п.2, в которой экспрессируемый бакуловирусом ORF2 белок цирковируса свиней типа 2 является ORF2 белок цирковируса свиней типа 2, который выделяют из супернатанта клеточной культуры, инфицированной рекомбинантными бакуловирусными векторами, содержащими ДНК ORF2 белок и экспрессирующий ORF2 белок цирковируса свиней типа 2.
4. Поливалентная комбинированная вакцина по п.1, включающая по меньшей мере 4 мкг рекомбинантно экспрессируемого ORF2 белка цирковируса свиней типа 2 на дозу.
5. Поливалентная комбинированная вакцина по п.1, в которой рекомбинантно экспрессируемый ORF2 белок цирковируса свиней типа 2 является стабильным в течение периода, составляющего 24 месяца.
6. Поливалентная комбинированная вакцина по п.1 в виде одной дозы.
7. Поливалентная комбинированная вакцина по п.1, где указанная одна доза поливалентной комбинированной вакцины дополнительно включает инактивированный вирусный вектор и супернатант клеточной культуры.
8. Поливалентная комбинированная вакцина по п.7, где указанный инактивированный вирусный вектор является рекомбинантным бакуловирусным вектором, кодирующим ORF2 белок вакцины цирковируса свиней типа 2.
9. Поливалентная комбинированная вакцина по п.1, где указанная поливалентная комбинированная вакцина включает BEI.
10. Поливалентная комбинированная вакцина по п.1, где указанная поливалентная комбинированная вакцина включает тиосульфат натрия.
11. Поливалентная комбинированная вакцина по п.2, где указанная поливалентная комбинированная вакцина включает адъювант.
12. Поливалентная комбинированная вакцина по п.11, где указанный адъювант выбирают из группы, включающей акриловую кислоту, метакриловую кислоту и любые их полимеры.
13. Поливалентная комбинированная вакцина по п.11, где указанный адъювант является карбополом в количестве от 500 мкг до 5 мг на дозу.
14. Поливалентная комбинированная вакцина по п.1, в которой указанный дополнительный компонент иммуногенного действия, эффективный в отношении другого организма, вызывающего заболевание у свиней, выбран из группы, состоящей из антигенов: Actinobacillus pleuropneumonia, аденовируса, альфавируса, например, вирусов восточного энцефаломиелита лошадей, Bordetella bronchiseptica, Brachyspira spp., предпочтительно В. hyodyentheriae, В. piosicoli, Brucella suis, предпочтительно биоваров 1, 2 и 3, вируса классической лихорадки свиней, Clostridium spp., предпочтительно Cl. difficile, Cl. perfringens, типов А, В и С, Cl. novyi, Cl. septicum, Cl. tetani, коронавируса, предпочтительно респираторного коронавируса свиней, Eperythrozoonosis suis, Erysipelothrix rhsiopathiae, Escherichia coli, Haemophilus parasuis, предпочтительно подтипов 1, 7 и 14, вируса гемагглютинирующего энцефаломиелита, вируса японского энцефалита, Lawsonia intracellularis, Leptospira spp., предпочтительно Leptospira australis, Leptospira canicola, Leptospira grippotyphosa, Leptospira icterohaemorrhagicae и Leptospira interrogans, Leptospira pomona, Leptospira tarassovi, Mycobacterium spp., предпочтительно M. avium, M. intracellulare, M.bovis, Mycoplasma hyopneumoniae (M. hyo), Pasteurella multocida, цитомегаловируса свиней, парвовируса свиней, вируса репродуктивно-респираторного синдрома свиней (PRRS), вируса псевдобешенства, ротавируса. Salmonella spp., предпочтительно S. thyhimurium и S. choleraesuis, Staph. hyicus, Staphylococcus spp., предпочтительно Streptococcus spp., предпочтительно Strep.suis, вируса герпеса свиней, вируса гриппа свиней, поксвируса свиней, вируса везикулярного стоматита и вируса везикулярной экзантемы свиней.
15. Поливалентная комбинированная вакцина по п. 14, где указанный дополнительный иммуногенно активный компонент является иммуногенно активным компонентом Mycoplasma hyopneumoniae и Procine Reproductive and Respiratory Syndrome Virus.
16. Поливалентная комбинированная вакцина по п. 15 для профилактики инфекций, которые вызываются PCV2 и PRRS.
17. Поливалентная комбинированная вакцина по п. 14, где указанный дополнительный иммуногенно активный компонент является иммуногенно активным компонентом Procine Reproductive and Respiratory Syndrome Virus.
18. Поливалентная комбинированная вакцина по п. 17, где указанная одноразовая доза комбинированной вакцины включает антиген, включенный в Ingelvac PRRS MLV.
19. Поливалентная комбинированная вакцина по п. 18, для профилактики инфекций, которые вызываются PCV2 и PRRS.
20. Поливалентная комбинированная вакцина по п. 14, где указанный дополнительный иммуногенно активный компонент является иммуногенно активным компонентом Mycoplasma hyopneumoniae.
21. Поливалентная комбинированная вакцина по п.20, для профилактики инфекций, которые вызываются PCV2 и Mycoplasma hyopneumoniae.
22. Способ снижения частоты встречаемости или понижения тяжести клинических симптомов, связанных с инфекцией цирковируса свиней типа 2, посредством введения свинье одной дозы поливалентной комбинированной вакцины по любому из пп.1-21.
23. Способ по п.22, где поливалентная комбинированная вакцина вводится в возрасте 2-8 недель.
24. Способ по п.22, где указанная поливалентная комбинированная вакцина вводится свинье в объеме 2 мл.
25. Применение одной дозы поливалентной комбинированной вакцины по любому из пп.1-21 для снижения частоты встречаемости или понижения тяжести клинических симптомов, связанных с инфекцией цирковируса свиней типа 2.
| ИММУНОГЕННАЯ КОМПОЗИЦИЯ, ВЫЗЫВАЮЩАЯ ИММУННЫЙ ОТВЕТ ПРОТИВ ПАРВОВИРУСА И ЦИРКОВИРУСА СВИНЬИ, ВАКЦИНА ПРОТИВ МНОГОСИСТЕМНОГО СИНДРОМА ИСТОЩЕНИЯ СВИНЕЙ (PMWS) (ВАРИАНТЫ), НАБОР ДЛЯ ВАКЦИНАЦИИ И СПОСОБ ЕЕ ОСУЩЕСТВЛЕНИЯ | 1999 |
|
RU2237492C2 |
| US 6391314 B1, 21.05.2002 | |||
| US 5498413 A, 12.03.1996. | |||
Авторы
Даты
2013-07-27—Публикация
2006-12-28—Подача