Данное изобретение относится к области биологии и химии. В частности, изобретение направлено на флуоресцентные белки.
Флуоресцентные белки, включая зеленый флуоресцентный белок (Green Fluorescent Protein, GFP), его мутанты и гомологи, в настоящее время широко известны благодаря их интенсивному использованию в качестве флуоресцентных маркеров in vivo в биомедицинских исследованиях, что детально рассмотрено Lippincott-Schwartz и Patterson в Science, 2003 300 (5616):87-91.
Флуоресцентные белки - это белки, которые способны к флуоресценции при облучением светом подходящей длины волны. Флуоресцентные свойства этих белков обусловлены взаимодействием двух или более аминокислотных остатков, формирующих хромофор, а не флуоресценцией какого-либо одного аминокислотного остатка.
GFP гидромедузы Aequorea aequorea (синоним A. victoria), описан Johnson et al. в J Cell Comp Physiol, 1962, 60:85-104, как часть биолюминесцентной системы медузы, где GFP играет роль вторичного эммитера, преобразовывающего синий свет от фотобелка экворина в зеленый свет.кДНК, кодирующая A. victoria GFP была клонирована Prasher et al. (Gene, 1992, 111(2):229-33). Оказалось, что этот ген может быть гетерологично экспрессирован в практически любом организме благодаря уникальной способности GFP автокаталитически образовывать хромофор (Chalfie et al., Science 263, 1994, 802-805). Эти сведения открыли широкие перспективы для использования GFP в клеточной биологи, в качестве генетически кодируемой флуоресцирующей метки.
GFP был использован в широком спектре приложений, включая исследование экспрессии генов и локализацию белков (Chalfie et al., Science 263, 1994, 802-805, and Heim et al. in Proc. Nat. Acad. Sci., 1994, 91: 12501-12504), как инструмент для визуализации внутриклеточного распределения органелл (Rizzuto et al., Curr. Biology, 1995, 5: 635-642), для визуализации транспорта белков по секреторному пути (Kaether and Gerdes, FEBS Letters, 1995, 369: 267-271).
Проведены многочисленные исследования для улучшения свойств avGFP (Aequorea victoria GFP) и для получения вариантов GFP, пригодных и оптимизированных для различных исследовательских целей. Была проведена оптимизация генетического кода avGFP (codon usage) для повышения уровня экспрессии в клетках млекопитающих ("гуманизированный" GFP, Haas, et al., Current Biology, 1996, 6: 315-324; Yang, et al., Nucleic Acids Research, 1996, 24: 4592-4593). Были получены различные мутанты GFP, в том числе "усиленный зеленый флуоресцентный белок" (EGFP), имеющий две аминокислотные замены: F64L и S65T (Heim et al., Nature 373, 1995, 663-664). Другие мутанты являются синим, голубым и желто-зеленым спектральными вариантами avGFP и содержат замены аминокислотных остатков, формирующих хромофор, и/или остатков, формирующих окружение хромофора.
В 1999 г., гомологи GFP были клонированы из небиолюминесцентных видов Anthozoa (Matz et al., Nature Biotechnol, 1999, 17: 969-973). Это открытие продемонстрировало, что эти белки не являются обязательно компонентом биолюминесцентной системы. GFP-подобные белки из Anthozoa обладали большим спектральным разнообразием и включали циановые, зеленые, желтые, красные флуоресцентные белки и фиолетово-синие нефлуоресцентные хромопротеины (CPs) (Matz et al., Bioessays, 2002, 24(10): 953-959). В дальнейшем кДНК GFP-подобных белков были клонированы из ряда гидроидных медуз и из копепод (Shagin et al., Mol Biol Evol, 2004, 21(5): 841-850). Сегодня семейство GFP-подобных белков включает сотни флуоресцентных и окрашенных гомологов GFP. Сходство этих белков с GFP варьирует от 80-90% до менее, чем 25% идентичности аминокислотной последовательности.
Получены кристаллические структура avGFP дикого типа, GFP S65T мутанта и ряда гомологов GFP (Ormo et al. Science, 1996, 273: 1392-1395; Wall et al. Nat Stmct Biol, 2000, 7: 1133-1138; Yarbrough et al. Proc Nati Acad Sci USA, 2001, 98: 462-467; Prescott et al. Structure (Camb), 2003, 11: 275-284; Petersen et al. J Biol Chem (2003), 278: 44626-44631; Wilmann et al. J Biol Chem, 2005, 280: 2401-2404; Remington et al. Biochemistry, 2005, 44, 202-212; Quillin et al. Biochemistry, 2005, 44: 5774-5787). Было постулировано, что все члены семейства обладают общей 3D структурой, представляющей собой так называемый бочонок из 11 бета-слоев, образующих компактную встречно-параллельную структуру, внутри которой располагается альфа-спираль, содержащая хромофор. Хромофор формируется путем окислительной циклизации трех консервативных аминокислотных остатков в центральном регионе альфа-спирали (Cody et al., Biochemistry, 1993, 32, 1212-1218). Положения аминокислотных остатков, формирующих хромофор, соответствует Ser65-Tyr66-Gly67 региону avGFP. Эти аминокислотные остатки легко могут быть идентифицированы у любого GFP-подобного белка путем выравнивания его последовательности с последовательностью avGFP.
Процесс автокаталитического формирования хромофора белков с различными спектральными свойствами подробно описан в ряде статей и включает несколько химических реакций (Heim et al. Proc Nati Acad Sci USA. 1994; 91:12501-12504; Ormo et al. Science, 1996;273:1392-1395; Yang et al. Nat Biotechnol, 1996, 14: 1246-1251; Brejc et al. J. Proc Natl Acad Sci USA, 199, 94: 2306-2311; Palm et al. Nat Stmct Biol, 1997, 4:361-365; Gurskaya et al., BMC Biochem, 2001, 2:6; Gross et al. Proc Nati Acad Sci USA, 2000, 97:11990-11995; Wall et al. Nat Stmct Biol, 2000, 7:1133-1138; Yarbrough et al., J. Proc Nati Acad Sci USA. 2001, 98:462-467; Pakhomov, A.A. and Martynov, V.I. Chem. Biol, 2008, 15, 755-764; Quillinet al, 2005 Biochemistry, 44, 5774-5787; Yampolsky et al, 2005, Biochemistry, 44, 5788-5793; Shu et al. 2006, Biochemistry 45, 9639-9647; Kikuchi et al, 2008, Biochemistry 47, 11573-11580; Yampolsky et al., Biochemistry, 2009,48 (33), p.8077).
Показано, что флуоресцентный белок KillerRed обладает фототоксическими свойствами, что позволяет использовать его для прицельного уничтожения клеток и биологических молекул (белков, ДНК) непосредственно в живых организмах (Bulina et al., Nat Biotechnol, 2006, Jan, 24(1): 95-9; Bulina et al., Nat Protoc, 2006, 1(2): 947-53).
Пространственная организация мономера KillerRed представляет собой типичный для флуоресцентных белков β-бочонок, образованный 11-ю β-сегментами, с центральной α-спиралью, содержащей хромофор, полученный в результате посттрансляционной модификации хромофор-образующей последовательности Gln65-Ty66-Gly67 (Pletnev et al., J Biol Chem, 2009, 284(46): 32028-32039). В белке KillerRed GFP-подобный домен (β-бочонок) составляют аминокислотные остатки в положениях с 6 по 225, соответствующие положениям с 6 по 229 последовательности avGFP.
Хромофор KillerRed в активной флуоресцентной форме представляет собой планарную бициклическую систему сопряженных двойных связей, состоящую из пятичленного имидазолинонового и фенольного циклов. Фенольный цикл Туr66б принимает цис- ориентацию по отношению к связи Сα-N(66), отвечающую активному флуоресцентному состоянию белка. Эта ориентация стабилизируется двумя водородными связями с Asn145 и через молекулу воды с Thr201. В процессе формирования хромофора Сα атом первого остатка Gln65 принимает sp2 гибридизацию, характеризующуюся плоским тригональным расположением примыкающих связей. При этом, образующаяся частично двойная N-ацилиминная связь N=Cα (Gln65) приводит к расширению сопряженной π-электронной системы, вызывающему сдвиг максимумов длин волн возбуждения и эмиссии в красную область спектра. Ближайшее окружение хромофора сформировано из боковых цепей 17-ти остатков, включая каталитические Arg94 и Glu218. Большинство этих остатков вовлечено в развитую систему водородных связей, как непосредственно, так и через молекулы воды.
Уникальной особенностью пространственной структуры KillerRed является наличие заполненного водой канала, идущего от торца (3-цилиндрической архитектуры белка к центральной области хромофора. Этот канал может облегчать доступ кислорода к хромофору, способствовать выходу активных форм кислорода из белка наружу, а также служить проводником протонов или электронов при фотовозбуждении хромофора. Эта особенность, по-видимому, является одним из ключевых структурных факторов наблюдаемых фототоксических свойств белка.
Белок KillerRed имеет ряд недостатков, затрудняющих его широкое использование. Так, KillerRed является димерным белком. В то же время известно, что димеризация флуоресцентных белков может негативно сказываться на функционировании связанных с ними (закодированных в одной рамке считывания) химерных белков. Таким образом, это свойство ограничивает использование белка KillerRed как инструмента прицельной фотоинактивации химерных белков, а также опосредованной химерными белками фотоинактивации нуклеиновых кислот. Кроме того, фототоксичность KillerRed существенно уступает фототоксичности известных химических фотосенсибилизаторов.
Предлагаемый в настоящей заявке подход направлен на решение этих проблем.
Предлагаемое изобретение обеспечивает выделенные молекулы нуклеиновых кислот, кодирующие химерные белки, включающие два оперативно слитых белка, по существу сходных с белком KillerRed (так называемый KillerRed-tandem). Нуклеиновые кислоты настоящего изобретения получены с помощью рекомбинантных технологий. В предпочтительных воплощениях, нуклеиновые кислоты настоящего изобретения кодируют химерные белки, обладающие фототоксическими свойствами.
Белок, состоящий из двух тандемно соединенных копий белка по существу сходных с белком KillerRed, проявляет свойства мономера и, следовательно, может быть использован для мечения широкого круга целевых белков. Это, в свою очередь, делает возможным осуществление непосредственного контакта KillerRed с клеточными структурами, чувствительными к воздействию окислительного стресса.
Выделенные нуклеиновые кислоты настоящего изобретения кодируют два белка, по существу сходных с белком KillerRed, которые соединены между собой с помощью белкового линкера (KillerRed-tandem).
В некоторых воплощениях, KillerRed-tandem оперативно слит с гистоном. В преимущественных воплощениях, это гистон Н2 В. При экспрессии, белки, слитые с гистоном, локализуются в ядре клетки-хозяина, включаются в состав хроматина и при облучении светом оказывают на него повреждающее действие.
Нуклеотидная последовательность, кодирующая гистон (например, H2B), соединена своим 3'-концом с 5'-концом последовательности, кодирующей два белка, по существу сходных с белком KillerRed. В некоторых воплощениях, между нуклеотидными последовательностями, кодирующими гистон H2B и два белка, по существу сходные с белком KillerRed, присутствует линкерная последовательность, кодирующая несколько аминокислотных остатков.
В некоторых воплощениях, обеспечивается выделенные нуклеиновые кислоты, которые кодируют химерные белки показанные в SEQ ID NO:02, 04, 06 и 08. В некоторых воплощениях, обеспечивается выделенные нуклеиновые кислоты, которые имеют последовательность SEQ ID NO:01, SEQ ID NO:03, SEQ ID NO:05 и SEQ ID NO:07.
Молекулы нуклеиновых кислот, которые отличаются от представленных нуклеотидных последовательностей вследствие вырожденности генетического кода так же входят в рамки настоящего изобретения.
В других воплощениях также обеспечиваются векторы, включающие нуклеиновую кислоту настоящего изобретения. Кроме того, настоящее изобретение обеспечивает кассеты экспрессии, включающие нуклеиновую кислоту настоящего изобретения и регуляторные элементы, необходимые для экспрессии нуклеиновой кислоты в выбранной клетке-хозяине. Кроме того, также обеспечиваются клетки, стабильные клеточные линии, трансгенные животные и трансгенные растения, включающие нуклеиновые кислоты, векторы или экспрессионные кассеты настоящего изобретения.
В других воплощениях обеспечиваются функциональные флуоресцентные белки настоящего изобретения, которые кодируются нуклеиновыми кислотами указанными выше.
Кроме того, обеспечиваются набор, содержащий нуклеиновые кислоты или векторы или экспрессионные кассеты, включающие указанные нуклеиновые кислоты настоящего изобретения.
Краткое описание чертежей
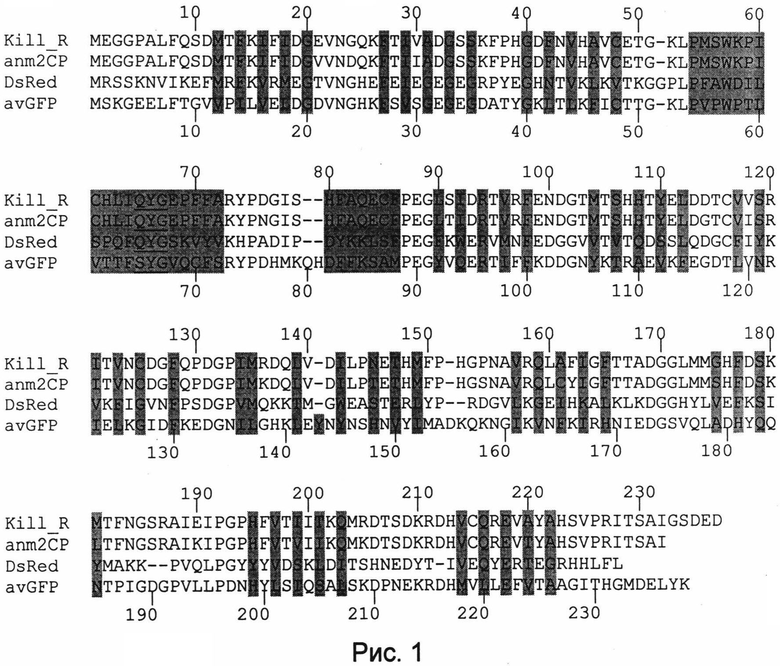
На рис.1 показано выравнивание белка KillerRed (Kill_R, SEQ ID NO:09) и других флуоресцентных белков - хромобелка anm2CP (SEQ ID NO:10) из антомедузы, на основе которого был получен KillerRed, красного флуоресцентного белка DsRed (SEQ ID NO:11) из кораллового полипа Discosoma, и зеленого флуоресцентного белка avGFP (SEQ ID NO:12) из медузы Aequorea victoria. Аминокислотные остатки, формирующие хромофор, подчеркнуты. Аминокислотные остатки, чьи боковые цепи погружены внутрь белковой глобулы, показаны на сером фоне.
На рис.2 показана схема строения химерных белков. Вверху - тандемный KillerRed (tKR), внизу - гистон H2B, слитый с тандемным KillerRed (H2B-tKR). N- и С-концы белков обозначены буквами N и С. Линией обозначены линкерные последовательности.
Подробное описание изобретения
Как указано выше, настоящее изобретение направлено на молекулы нуклеиновых кислот, которые кодируют химерные белки, включающие два оперативно слитых белка, по существу сходных с белком KillerRed. Нуклеиновые кислоты настоящего изобретения получены с помощью рекомбинантных технологий. В предпочтительных воплощениях, нуклеиновые кислоты настоящего изобретения кодируют химерные белки, обладающие фототоксическими свойствами, которые превышают фототоксические свойства белка KillerRed. Также обеспечиваются векторы и кассеты экспрессии, включающие нуклеиновую кислоту настоящего изобретения. Кроме того, обеспечиваются клетки, стабильные клеточные линии, трансгенные животные и трансгенные растения, включающие нуклеиновые кислоты, векторы или экспрессионные кассеты настоящего изобретения.
В других воплощениях обеспечиваются функциональные флуоресцентные белки настоящего изобретения, которые кодируются нуклеиновыми кислотами, указанными выше.
Указанные белковые и нуклеотидные композиции применяются во многих различных приложениях и методах, в частности, в приложениях прицельного уничтожения клеток или блокирования пролиферации клеток с помощью облучения светом определенной длины волны. Наконец, обеспечиваются наборы для их использования в таких методах и приложениях.
Определения
Различные термины, относящиеся к биологическим молекулам настоящего изобретения, используются выше и также в описании и в формуле изобретения.
Используемый здесь, термин "флуоресцентный белок" означает белок, относящийся к семейству GFP-подобных белков, который обладает способностью к флуоресценции; например, он может проявлять низкую, среднюю или интенсивную флуоресценцию при облучении светом с подходящей для возбуждения длиной волны. Флуоресцентное свойство этих белков представляет собой такое свойство, которое является результатом работы хромофора, образующегося путем автокаталитической циклизации трех или более аминокислотных остатков в полипептидной цепи. Как таковые флуоресцентные белки настоящего изобретения не включают белки, которые обладают флуоресценцией за счет отдельных флуоресцирующих остатков, таких как триптофан, тирозин и фенилаланин. Используетмый здесь, термин "avGFP" относится к зеленому флуоресцентному белку из медузы Aequorea victoria, включая варианты avGFP, известные из уровня техники, сконструированные для обеспечения большей флуоресценции или флуоресценции в других цветовых областях. Последовательность дикого типа avGFP была раскрыта в Prasher et al. (1992, Gene 111: 229-33).
Термин "гуманизированный" относится к изменению нуклеотидной последовательности флуоресцентного белка, сделанной для оптимизации генетического кода кодонов для экспрессии в клетках млекопитающих (Yang et al., Nucleic Acids Research, 1996, 24: 4592-4593).
Как здесь используется, термин "выделенный" означает молекулу или клетку, которые находятся в среде, отличной от среды, в которой молекула или клетка находятся в естественных условиях.
Как здесь используется, термин "мутант" или "производное" относятся к белку, раскрытому в настоящем изобретении, в котором одна или более аминокислот добавлены и/или замещены и/или удалены (делегированы) и/или вставлены (инсертированы) в N-конец и/или С-конец, и/или в пределах нативных аминокислотных последовательностей белков настоящего изобретения. Как здесь используется, термин "мутант" относится к молекуле нуклеиновой кислоты, которая кодирует мутантный белок. Кроме того, термин "мутант" здесь относится к любому варианту, который короче или длиннее белка или нуклеиновой кислоты.
Как здесь используется, "гомология" это термин, использующийся для описания взаимосвязи последовательностей нуклеотидов или аминокислот с другими последовательностями нуклеотидов или аминокислот, которая определена степенью идентичности и/или сходства между указанными сравниваемыми последовательностями.
Как здесь используется, аминокислотная или нуклеотидная последовательности "по существу сходны" или "по существу такие же как референсная последовательность, если аминокислотная или нуклеотидная последовательности имеют по крайней мере 85% идентичности с указанной последовательностью внутри выбранного для сравнения региона. Таким образом, по существу сходные последовательности включают те, которые имеют, например, по крайней мере, 85% идентичности, по крайней мере, 90% идентичности, по крайней мере, 95% идентичности или по крайней мере, 96%б 97%б 98% или 99% идентичности. Две последовательности, которые идентичны одна другой, также по существу сходны.
Для целей настоящего изобретения длина сравниваемых последовательностей флуоресцентных белков соответствует длине GFP-домена. GFP-домен может быть идентифицирован с помощью анализа кристаллической структуры флуоресцентного белка или с помощью выравнивания аминокислотной последовательности белка с avGFP. GFP-домен может быть идентифицирован так же с помощью программ для анализа доменной организации белков, таких как Conserved Domain Database (CDD) (http://www.ncbi.nlm.nih.gov/Stmcture/cdd/) и SMART (a Simple Modular Architecture Research Tool, http://smart.embl-heidelberg.de/). Было показано, что в состав домена, формирующего "бочонок" входят аминокислотные остатки, соответствующие положениям с 6 по 229 последовательности avGFP, где позиции соответствующих аминокислотных остатков определяются с помощью выравнивания аминокислотной последовательности белка с avGFP (рис.1). Для белка KillerRed в состав домена входят аминокислотные остатки, соответствующие положениям с 6 по 225. Было показано, что аминоксилотные фрагменты, не входящие в состав GFP-домена, могут содержать делеции, инсерции и замены аминокислотных остатков; при этом не происходит существенного изменения спектральных свойств флуоресцентного белка (Shimozono et al., Biochemistry, 2006,45, 6267-6271; Crameri et al., Nat Biotechnol, 1996, 14: 315-319). Процент идентичности последовательностей определяется на основании референсной последовательности. Алгоритмы для анализа последовательности известны в данной области, такие как BLAST, описанный в Altschul et al., J. Mol. Biol., 1990, 215, pp.403-10). Для целей настоящего изобретения сравнение нуклеотидных и аминокислотных последовательностей производимое с помощью пакета программ Blast, предоставляемого National Center for Biotechnology Information (http://www.ncbi.nlm.nih.gov/blast) с использованием содержащего разрывы выравнивания со стандартными параметрами, может быть использовано для определения уровня идентичности и сходства между нуклеотидными последовательностями и аминокислотными последовательностями.
Как здесь используется, термин "подобные флуоресцентные белки" или "по существу сходные флуоресцентные белки" относится к флуоресцентным белкам, которые имеют GFP-домены, идентичные, по крайней мере, на 85%, как правило, идентичные на 90% или более, чаще всего идентичные, по крайней мере, на 95% или более (например на 96% и более, 97% и более, 98% и более, 99% и более, 100%).
В некоторых воплощениях, термин "подобные флуоресцентные белки" или "по существу сходные флуоресцентные белки" относится к флуоресцентным белкам, которые имеют аминокислотные последовательности целого белка идентичные, по крайней мере, на 85%, как правило идентичные на 90% или более, чаще всего идентичные по крайней мере на 95% или более (например на 96% и более, 97% и более, 98% и более, 99% и более, 100%).
Как здесь используется, термин "функциональный" означает, что нуклеотидная или аминокислотная последовательность может функционировать для указанного испытания или задачи. Термин "функциональный", используемый для описания KillerRed и химерного белка настоящего изобретения, означает, что белок имеет фототоксические свойства.
Как здесь используется, "биохимические свойства" относятся к белковому фолдингу (сворачиванию) и скорости созревания, времени полужизни, способности к агрегации, способности к олигомеризации, рН и температурной стабильности, и другим подобным свойствам.
Как здесь используется, "флуоресцентные свойства" или "спектральные свойства " относятся к коэффициенту молярной экстинкции, при подходящей длине волны, к квантовому выходу флуоресцентции, форме спектра возбуждения флуоресценции или спектра испускания, длине волны, соответствующей максимуму возбуждения флуоресценции, и длине волны, соответствующей максимуму испускания, отношению амплитуды возбуждения флуоресценции при двух разных длинах волн, отношению амплитуды испускания при двух разных длинах волн, времени жизни возбужденного состояния, и анизотропии оптических свойств. Измеряемая разница может быть определена как количество любого количественного флуоресцентного свойства, например, интенсивность флуоресцентции при определенной длине волны, или интегральная флуоресценция на всем спектре испускания.
Как здесь используется, термины "фототоксические свойства" или "фототоксичность" относятся к способности белка вызывать повреждение близлежащих молекул, например близлежащих белков, нуклеиновых кислот, и/или липидов, что в свою очередь может вызывать гибель клеток, остановку клеточных делений или нарушение клеточной дифференцировки и/или пролиферации. Для сравнения фототоксических свойств может быть использована бактериальная система. Например, белки могут быть экспрессированы в клетках бактерий (например, Е.coli) путем транефекции подходящими экспрессирующими векторами, кодирующими указанные белки под контролем промотора, обеспечивающего экспрессию белка в данных бактериальных клетках. Колонии выращивают в течение ночи при 37°C и далее чашки инкубируют при 4°C до полного созревания белков. Для каждого белка отбирают единичную колонию, которую суспендируют в 0.1 мл буфера PBS, после чего половину объема 30 мин облучают активирующим светом определенной интенсивности, а половину оставляют в темноте в качестве контроля. Полученные суспензии клеток высеивают на чашки Петри в различных разведениях и после ночного роста при 37°С подсчитывают число выросших колоний.
Как здесь используется, "агрегация" относится к склонности или способности экспрессированного белка формировать нерастворимый осадок (агрегаты). "Агрегация" должна быть отличаема от "олигомеризации". В частности, мутанты с уменьшенной способностью к агрегации, например, с увеличенной растворимостью, не обязательно имеют уменьшенную способность к олигомеризации.
Как здесь используется, "олигомеризация" относится к сколонности или способности экпрессированного белка формировать комплексы (олигомеры) в результате специфического взаимодействия двух или более полипептидов. Указанное специфическое взаимодействие наблюдается в специальных условиях, например, в физиологических условиях, и относительно стабильно в этих условиях. Ссылка на "способность" белков олигомеризоваться означает, что белки могут формировать димеры, триммеры, тетрамеры или подобные комплексы в специальных условиях. Как правило, флуоресцентные белки обладают способностью к олигомеризации в физиологических условиях, хотя, как здесь описано, флуоресцентные белки могут также олигомеризоваться при других, например, pН, нежели pН при физиологических условиях. Условия, при которых флуоресцентные белки формируют олигомеры или проявляют склонность к олигомеризации могут быть определены с помощью хорошо известных методов, таких как гель-фильтрация или иным способом известным в данной области.
Ссылка на нуклеотидную последовательность "кодирующую" полипептид означает, что с нуклеотидной последовательности в ходе трансляции и транскрипции мРНК продуцируется этот полипептид. При этом может быть указана как кодирующая цепь, идентичная мРНК и обычно используемая в списке последовательностей, так и комплементарная цепь, которая используется как матрица при транскрипции. Как очевидно для любого специалиста в данной области техники, термин также включает любые вырожденные нуклеотидные последовательности кодирующие одинаковую аминокислотную последовательность. Нуклеотидная последовательности кодирующие полипептид включают последовательности, содержащие интроны.
Термин "оперативно связанный" или ему подобный при описании химерных белков относится к полипептидным последовательностям, которые находятся в физической и функциональной связи одна с другой. В наиболее предпочтительных воплощениях, функции полипептидных компонентов химерной молекулы не изменены по сравнению с функциональными свойствами выделенных полипептидных компонентов. Например, белок KillerRed или KillerRed-тандем настоящего изобретения может быть сшит с представляющим интерес партнером слияния. В этом случае химерный белок сохраняет фототоксические свойства белка KillerRed, а представляющий интерес полипептид (например гистон H2 B) сохраняет его оригинальную биологическую активность. Как очевидно для любого специалиста в данной области техники, нуклеотидные последовательности, кодирующие химерный белок, включающий "оперативно связанные" компоненты (белки, полипептиды, линкерные последовательности, белковые домены и т.д.), состоят из фрагментов, кодирующих указанные компоненты, где эти фрагменты ковалентно связаны таким образом, что в ходе трансляции и транскрипции нуклеотидной последовательности продуцируется полноразмерный химерный белок. Иными словами, фрагменты соединены таким образом, что в местах их соединения отсутствуют 'сбойки' рамки считывания и стоп-кодоны.
Молекулы нуклеиновых кислот
Настоящее изобретение обеспечивает молекулы нуклеиновых кислот кодирующие химерный белок, имеющий аминокислотную последовательность, выбранную из SEQ ID NO:02, 04, 06 и 08 и его варианты.
Как здесь используется, молекула нуклеиновой кислоты это молекула ДНК, такая как геномная ДНК или кДНК молекула, или молекула РНК, такая как молекула мРНК. Как здесь используется, термин "кДНК" относится к нуклеиновым кислотам, которые обладают размещением элементов последовательности найденным в нативных зрелых видах мРНК, где элементы последовательности - это экзоны и 5' и 3' некодирующие области.
Молекула нуклеиновой кислоты, кодирующая химерный белок согласно данному изобретению может быть синтезирована из подходящих нуклеозидтрифосфатов. Метод хорошо описан в известных в данной области протоколах. Например, доступность информации о последовательности аминокислот (например, SEQ ID NO:02, 04, 06 или 08.) или информации о нуклеотидной последовательности (например, SEQ ID NO:01, 03, 05 или 07) дает возможность изготовить выделенные молекулы нуклеиновых кислот настоящего изобретении с помощью олигонуклеотидного синтеза. В случае информации о последовательности аминокислот, несколько нуклеиновых кислот отличающихся друг от друга вследствие вырожденности генетического кода может быть синтезировано. Методы выбора вариантов кодонов для требуемого хозяина хорошо известны в данной области.
Синтетические олигонуклеотиды могут быть приготовлены с помощью фосфорамидитного метода, и полученные конструкты могут быть очищены с помощью методов хорошо известных в данной области, таких как высокоэффективная жидкостная хроматография (ВЭЖХ) или других методов как описано, например, в Sambrook et al., Molecular Cloning: A Laboratory Manual, 2nd Ed., 1989, Cold Spring Harbor Press, Cold Spring Harbor, NY, и по инструкции, описанной в, например, United States Dept. of HHS, National Institute of Health (NIH) Guidelines for Recombinant DNA Research. Длинные двухцепочечные молекулы ДНК настоящего изобретения могут быть синтезированы за следующие стадии: несколько меньших фрагментов с необходимой комплементарностью, которые содержат подходящие концы способные к когезии с соседним фрагментом, могут быть. Соседние фргменты могут быть сшиты с помощью ДНК-лигазы или метода, основанного на ПЦР.
В некоторых воплощениях, молекула нуклеиновой кислоты настоящего изобретения - это ДНК (или кДНК) молекула, содержащая открытую рамку считывания, которая кодирует химерный белок настоящего изобретения и способна в подходящих условиях (например, физиологические внутриклеточные условия) быть использована для экспрессии белка в клетке-хозяине. Настоящее изобретение так же охватывает нуклеиновые кислоты, которые гомологичны, по существу сходны, идентичны, или получены из нуклеиновых кислот, кодирующих белки настоящего изобретения. Указанные нуклеиновые кислоты находятся в среде, отличной от среды, в которой они находятся в естественных условиях, например, они выделены, представлены в увеличенном количестве, находятся или экспрессированы в системах in vitro или в клетках или организмах, отличных от тех, в которых они находятся в естественных условиях.
Изменения или различия в нуклеотидной последовательности между высокосходными нуклеотидными последовательностями могут представлять нуклеотидные замены в последовательности, которые возникают в процессе нормальной репликации или дупликации. Другие замены могут быть специально рассчитаны и вставлены в последовательность для определенных целей таких, как изменение кодонов определенных аминокислот или нуклеотидной последовательности регуляторного региона. Такие специальные замены могут быть произведены in vitro с помощью различных технологий мутагенеза или получены в организмах-хозяевах, находящихся в специфических селекционных условиях, которые индуцируют или отбирают эти изменения. Такие специально полученные варианты последовательности могут быть названы "мутантами" или "производными" исходной последовательности.
Нуклеиновая кислота, кодирующая химерный белок, в состав которой входит последовательность, кодирующая интромолекулярный димер мутантного белка KillerRed также обеспечивается настоящим изобретением. Для нужд данного изобретения мутантный вариант белка KillerRed должен обладать фототоксичностью, не меньшей, чем белок KillerRed, и обладать сходными способностями к олигомеризации. В большинстве случаев, мутантный вариант белка KillerRed имеет GFP-домен, который по крайней мере на 85% идентичен (чаще по крайней мере на 90% идентичен, как правило по крайней мере на 95% идентичен) GFP-домену белка KillerRed. Например указанный GFP-домен может быть по крайней мере на 96%, 97%, 98%, 99%, или 100% идентичен GFP-домену белка KillerRed.
Мутантные или производные нуклеиновые кислоты могут быть получены на матричной нуклеиновой кислоте, выбранной из вышеописанных нуклеиновых кислот, путем модификации, делеции или добавления одного или более нуклеотидов в матричной последовательности или их комбинации, для получения варианта матричной нуклеиновой кислоты. Модификации, добавления или делеции могут быть выполнены любым способом, известным в данной области (см. например Gustin et al., Biotechniques, 1993, 14: 22; Barany, Gene, 1985, 37: 111-123; и Colicelli et al., Mol. Gen. Genet, 1985, 199: 537-539, Sambrook et al., Molecular Cloning: A Laboratory Manual, 1989, CSH Press, pp.15.3-15.108), включая подверженный ошибкам ПЦР (error-prone PCR), shuffling, олигонуклеотид-направленный мутагенез, ПЦР со сборкой, парный ПЦР мутагенез, мутагенез in vivo, кассетный мутагенез, рекурсивный множественный мутагенез, экспоненциальный множественный мутагенез, сайт-специфический мутагенез, случайный мутагенез, генная реассемблирование (gene reassembly), генный сайт-насыщающий мутагенез (GSSM), искусственное перестройку с лигированием (SLR) или их комбинации. Модификации, добавления или делеции могут быть также выполнены методом, включающим рекомбинацию, рекурсивную рекомбинацию последовательностей, фосфотиоат-модифицированный мутагенез ДНК, мутагенез на урацил-содержащей матрице, мутагенез с двойным пропуском, точечный восстановительный по рассогласованию мутагенез, мутагенез штамма, дефицитного по восстановлениям, химический мутагенез, радоактивный мутагенез, делетационный мутагенез, рестрикционно-избирательный мутагенез, рестрикционный мутагенез с очисткой, синтез искусственных генов, множественный мутагенез, создание химерных множественных нуклеиновых кислот и их комбинации. В некоторых воплощениях флуоресцентные белки, кодируемые мутантными или производными нуклеиновыми кислотами имеют те же самые флуоресцентные или биохимические свойства как флуоресцентный белок дикого типа. В других воплощениях, мутантные или производные нуклеиновые кислоты кодируют флуоресцентные белки с измененными свойствами.
Кроме того, также обеспечиваются вырожденные варианты нуклеиновых кислот, которые кодируют белки настоящего изобретения. Вырожденные варианты нуклеиновых кислот включают замены кодонов нуклеиновой кислоты на другие кодоны, кодирующие те же самые аминокислоты. В частности, вырожденные варианты нуклеиновых кислот создаются, чтобы увеличить экспрессию в клетке-хозяине. В этом воплощении, кодоны нуклеиновой кислоты, которые не являются предпочтительными или являются менее предпочтительными в генах клетки-хозяина, заменены кодонами, которые обильно представлены в кодирующих последовательностях генов в клетке-хозяине, где указанные замененные кодоны кодируют ту же самую аминокислоту. Особенный интерес представляют гуманизированные версии нуклеиновых кислот настоящего изобретения. Как здесь используется, термин "гуманизированный" относится к заменам, сделанным в последовательности нуклеиновой кислоты для оптимизации кодонов для экспрессии белка в клетках млекопитающих (челвека) (Yang et al., Nucleic Acids Research, 1996, 24: 4592-4593). См. также Патент США №5795737, который описывает гуманизацию белков, раскрытие которого здесь включено ссылкой. Примеры вырожденных вариантов, представляющих интерес, описаны более подробно в экспериментальной части, ниже.
Нуклеиновые кислоты, кодирующие укороченные и удлиненные варианты белков настоящего изобретения так же входят в рамки настоящего изобретения. Как здесь используется, эти варианты белков содержат аминокислотные последовательности с измененными С-, N-, или обоими концами. В удлиненных вариантах, С- или N-конец белка может содержать дополнительные аминокислотные остатки. В укороченных вариантах одна или более (обычно до 11, чаще до 7 и преимущественно до 5) аминокислотных остатков могут быть удалены из последовательности или заменены на любые другие аминокислотные остатки. Такие модификации не изменяют по существу свойства белков, но могут облегчать белковый фолдинг в клетке-хозяине, снижать способность к агрегации или модулировать другие биохимические свойства белков, например, полупериод распада. В некоторых воплощениях, эти модификации не изменяют биохимические свойства белка. Все виды модификаций и мутаций, указанные выше, осуществляются на уровне нуклеиновой кислоты.
Заявленные нуклеиновые кислоты могут быть выделены и получены по существу в очищенной форме. По существу очищенная форма означает, что нуклеиновые кислоты являются по меньшей мере приблизительно на 50% чистыми, обычно по меньшей мере приблизительно на 90% чистыми и обычно являются "рекомбинантными", то есть, фланкированы одним или более нуклеотидов, - с которыми она обычно не связана в хромосоме, встречающейся в природе в ее естественном организме-хозяине.
Также обеспечиваются вектор и другие конструкции нуклеиновой кислоты, содержащие заявленные нуклеиновые кислоты. Подходящие векторы включают вирусные и невирусные векторы, плазмиды, космиды, фаги и т.д., предпочтительно плазмиды, и используются для клонирования, амплификации, экспрессии, переноса и т.д., последовательности нуклеиновой кислоты настоящего изобретения в подходящего хозяина. Выбор подходящего вектора является понятным для квалифицированного специалиста в данной области, и много таких векторов доступны коммерчески. Для приготовления конструкции, полноразмерная нуклеиновая кислота или ее часть обычно вставляются в вектор посредством прикрепления ДНК-лигазой к расщепленному ферментами рестрикции сайту в векторе. Альтернативно, желательная нуклеотидная последовательность может быть вставлена гомологичной рекомбинацией in vivo, обычно, присоединением гомологичных участков к вектору на флангах желательной нуклеотидной последовательности. Гомологичные участки добавляются лигированием олигонуклеотидов или полимеразной цепной реакцией, с использованием праймеров, включающих, например, как гомологичные участки, так и часть желательной нуклеотидной последовательности.
Также обеспечиваются кассеты экспрессии или системы, использованные inter alia для получения заявленных хромогенных или флуоресцентных белков или химерных белков на их основе или для репликации заявленных молекул нуклеиновой кислоты. Кассета экспрессии может существовать как внехромосомный элемент или может быть включена в геном клетки в результате введения указанной кассеты экспрессии в клетку. Для экспрессии генный продукт, кодируемый нуклеиновой кислотой изобретения, экспрессируется в любой удобной системе экспрессии, включая, например, бактериальные системы, дрожжевые, насекомых, земноводных или клетки млекопитающих. В экспрессионном векторе, указанная нуклеиновая кислота является функционально связанной с регуляторной последовательностью, которая может включить промоторы, энхансеры, терминаторы, операторы, репрессоры и индукторы. Методы изготовления кассет экспрессии или систем для экспрессии желаемого продукта известны специалистом, квалифицированным в данной области. Клеточные линии, которые устойчиво экспрессируют белки настоящего изобретения, могут быть выбраны способами, известными в данной области (например ко-трансфекция с селектируемым маркером, таким как dhfr, gpt, неомицин, гигромицин, что делает возможным выявление и выделение транфецированных клеток, которые содержат ген, включенный в геном).
Вышеописанные системы экспрессии могут использоваться в прокариотических или эукариотических хозяевах. Для получения белка могут использоваться клетки-хозяева, такие как Е.coli, В.subtilis, S.cerevisiae, клетки насекомого в комбинации с бакуловирусными векторами, или клетки высшего организма, такого как позвоночные, например, COS 7 клетки, НЕК 293, CHO, ооциты Xenopus и т.д.
Если используется любая вышеупомянутая клетка-хозяин или другие подходящие клетки-хозяева или организмы для репликации и/или экспрессии нуклеиновых кислот изобретения, то полученная реплицированная нуклеиновая кислота, экспрессированный белок или полипептид находятся в рамках притязания изобретения как продукт клетки-хозяина или организма. Продукт может быть выделен подходящим способом, известным в данной области.
Молекулы нуклеиновых кислот настоящего изобретения также могут применяться для экспрессии гена химерного белка в клетке-хозяине. Способ, в котором исследуются клетки на наличие специфических нуклеотиднвх последовательностей, таких как геномная ДНК или РНК, хорошо отработан в данной области. Кратко, выделяют ДНК или мРНК из образца клетки. мРНК может быть амплифицирована ОТ-ПЦР, с использованием обратной транскриптазы для формирования комплементарной цепочки ДНК, с последующей амплификацией с помощью полимеразной цепной реакцией с использованием праймеров, специфических для заявленных последовательностей ДНК. Альтернативно, образец мРНК отделяют с помощью гель-электрофореза, переносят на подходящий носитель, например, нитроцеллюлозу, нейлон и т.д., и затем тестируют фрагментом заявленной ДНК в качестве пробы. Могут также использоваться другие способы, такие как анализы сшивания олигонуклеотидов, гибридизация in situ и гибридизация ДНК-пробами, иммобилизованными на твердый чип.Обнаружение мРНК, гибридизующейся с заявленной последовательностью указывает на экспрессию гена в образце.
Белки
Нуклеиновые кислоты по настоящему изобретению кодируют химерные белки. Заявленные химерные белки состоят из нескольких оперативно слитых белков, соединенных линкерными последовательностями. Структура химерного белка схематически изображена на рисунке 2. Методы получения химерных белков хорошо известны в данной области. Например, части нуклеиновой кислоты, кодирующие различные элементы, могут быть встроены в полилинкер вектора, таким образом, что между различными частями не будет стоп-кодонов в рамке считывания и не будет сбоек рамки считывания. Альтернативно, желательная нуклеотидная последовательность может быть собрана из фрагментов с помощью ДНК-лигазы или ПЦР с праймерами, содержащими части, комплементарные концевым последовательностям соединяемых фрагментов.
Химерный белок по данному изобретению включает интрамолекулярный димер (тандем) белка, по существу сходного с белком KillerRed. В состав тандема входят два одинаковых белка, каждый из которых имеет по крайней мере 85% идентичности (например, по крайней мере 90% идентичности, по крайней мере 95% идентичности или более, например 96%, 97%, 98% или 100%) с белком KillerRed и проявляет сходные или усиленные фототоксические свойства. При экспрессии указанных белков в клетках, они способны к интрамолекулярной димеризации.
Интрамолекулярный димер формируется за счет димеризации входящих в его состав белков, по существу сходных с белком KillerRed. Как результат, полученный интрамолекулярный димер проявляет свойства мономера. Например, при анализе очищенного белка вытеснительной хроматографией (гель-фильтрацией) интрамолекулярный димер имеет ту же подвижность, что и исходный белок, формирующий межмолекулярный димер, что показывает отсутствие межмолекулярной олигомеризации в случае оперативно слитого тандемного белка. Также, тандем белков, по существу сходных с белком KillerRed, может быть успешно использован для создания белков слияния с целевыми клеточными белками, чувствительными к олигомеризации флуоресцентного белка, такими как бета-актин, гистоны, коннексины и др. Правильная внутриклеточная локализация и функционирование таких химерных белков показывает, что тандемный белок проявляет свойства мономера.
Две входящие в состав интрамолекулярного димера белка связаны друг с другом, как показано на рис.2 с помощью полипептидного линкера. Длина и состав аминокислот линкера может быть различен. Например, длина линкера может быть от 1 аминокислотного основания до 100 аминокислотных оснований, чаще 10-50 аминокислотных оснований, например 20, 25, 30,33, 35, 40, 45 аминокислотных оснований. Последовательность аминокислот линкера может варьировать в широких пределах, так как в большинстве случаев не влияет на функционирование интрамолекулярного димера. Примеры линкерных последовательностей показаны в SEQ ID NO:13 и 14.
В некоторых воплощениях, химерный белок по данному изобретению также включает функциональный гистон. Гистоны - это небольшие (120-140 аминокислотных остатков), сильно основные, высококонсервативные белки, находящиеся в ядре клетки и участвующие в укладке геномной ДНК. Гистоны образуют основной элемент организации хроматина - нуклеосомы, вокруг которых закручивается ДНК. Существует пять различных типов гистонов, названных H1/H5, H2A, H2B, H3, H4. Основу нуклеосомы составляют гистоны H2A, H2B, H3, и H4 (по две копии каждого на нуклеосому). Эти гистоны сходны между собой по структуре, представляющей собой характерный мотив «спираль-поворот-спираль-поворот-спираль». Для нужд данного изобретения гистон обеспечивает локализацию химерного белка в ядрах клеток и его связывание с геномной ДНК. Нуклеиновая кислота, кодирующая гистон, оперативно связана с последовательностью, кодирующей интрамолекулярный димер KillerRed с помощью линкерной последовательности, представляющей собой короткий полипептид. Длина линкера может быть от 1 аминокислотного остатка до 50 аминокислотных остатков, чаще 2-20 аминокислотных остатков, например 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15 аминокислотных остатков. Последовательность аминокислот линкера может варьировать в широких пределах, так как в большинстве случаев она не влияет на функционирование входящих в состав химерного белка компонентов. Химерный белок, включающий гистон, обладает способностью локализоваться в ядрах клеток-хозяев и связываться с ядерной ДНК. До перехода в активированное состояние, химерный белок по данному изобретению обладает низкой токсичностью в клетках-хозяевах. До перехода в активированное состояние, химерный белок по данному изобретению обладают способностью к детектируемой флуоресценции. Во многих воплощениях, химерный белок обладают красной или дальне-красной флуоресценцией, то есть имеет максимум возбуждения флуоресценции в диапазоне от приблизительно 450 нм до 700 нм, обычно от приблизительно 470 нм до 650 нм и чаще всего от приблизительно 500 до 600 нм, например, от 550 до 595 нм; тогда как максимум эмиссии заявленного белка лежит в диапазоне от приблизительно 530 до 700 нм, обычно от приблизительно 550 нм до 670 нм и чаще всего от приблизительно 560 до 650 нм, например, от 574 до 637 нм.
Заявленный белок обычно имеет максимальный коэффициет экстинкции в диапазоне от приблизительно 30,000 до 150,000 и обычно от приблизительно 60,000 до 120,000, например, от 90,000 до 120,000. В некоторых воплощениях, флуоресценция заявленного химерного белка может быть обнаружена обычными способами (например, визуальный скрининг, спектрофотометрия, спектрофлуориметрия, флуоресцентная микроскопия, FACS приборами, и т.д.) Яркость флуоресценции белка определяется его квантовым выходом, умноженным на максимальный коэффициент экстинкции и деленным на 1000. В некоторых воплощениях, заявленный белок обладает яркостью флуоресценции в диапазоне от приблизительно 10 до 90, обычно приблизительно от 40 до 80, и чаще всего приблизительно от 50 до 75.
Химерный белок по данному изобретению переходит в активированное состояние под действием света определенной длины волны (активирующего света). В некоторых воплощениях, длина волны активирующего света находится в диапазоне приблизительно от 500 до 610 нм, обычно приблизительно от 520 до 590 нм, и чаще всего приблизительно от 540 до 580 нм.
В активированном состоянии химерный белок по данному изобретению обладает выраженной токсичностью по отношению к клеткам. В некоторых воплощениях, в активированном состоянии химерный белок по данному изобретению теряет способность к флуоресценции. В некоторых воплощениях, в активированном состоянии химерный белок по данному изобретению способен к продукции активных форм кислорода.
В некоторых воплощениях, химерный белок по данному изобретению быстро созревает после экспрессии в клетке-хозяине. Под быстрым созреванием понимается то, что белок достигает своей третичной структуры, которая обеспечивает его спектральные и фототоксические свойства, за короткий период времени. В этих воплощениях, белок укладывается в течение периода времени, который в общем случае не превышает приблизительно 36 ч, обычно не превышает приблизительно 48 ч и чаще не превышает приблизительно 24 ч (например, полупериод укладки может быть 3-5 часов).
Специфические белки, представляющие интерес, включают химерный белок, выбранный из SEQ ID No:02, 04, 06 и 08; и его функциональные мутанты.
Мутанты могут сохранять свойства исходного белка или могут иметь биологические свойства, отличные от форм исходного белков. Термин "биологические свойства" белков настоящего изобретения относится, но не лимитирован, спектральными свойствами, такими как максимум возбуждения флуоресценции, максимум испускания, максимальный коэффициент экстинкции, яркость (например, по сравнению с референсным белков), фотостабильность и подобные; биохимические свойства, такие как in vivo и/или in vitro стабильность (например, полупериод распада); скорость созревания, склонность к агрегации и склонность к олигомеризации и другие подобные свойства (по сравнению с референсным белком). Мутации включают единичные аминокислотные замены, делеции и инсерции одной или более аминокислот, укорочение или удлинение N-конца, укорочение или удлинение С- конца и тому подобное.
Мутанты могут быть получены с использованием стандартных методов молекулярной биологии, как подробно описано в разделе "молекулы нуклеиновых кислот" выше. Примеры обеспечивают общие приемы, и использование стандартных способов, так что специалисты, квалифицированные в данной области, могут легко получить большой ряд дополнительных мутантов и проверить, было ли изменено биологическое (например биохимическое, спектральное, и т.д.) свойство. Например, интенсивность флуоресценции может быть измерена с использованием спектрофлуориметра при различных длинах волн возбуждения.
Также обеспечиваются белки, которые по существу сходны с указанными выше специфическими белками, где по существу сходны означает, что эти белки имеют аминокислотную последовательность, идентичную последовательности исходного белка, по крайней мере, на 85% идентичности, обычно, по крайней мере, 90% и чаще, по крайней мере, 95%, (например 95% и выше; 96% и выше, 97% и выше; 98% и выше: 99% и выше или 100% идентичности последовательности).
Белки настоящего изобретения присутствуют в среде, отличной от их естественной среды; например, они рекомбинантны. Белки настоящего изобретения могут находиться в выделенном состоянии, что означает, что белки по существу свободны от других белков и других биологических молекул, присутствующих в естественной среде, таких как олигосахариды, нуклеиновые кислоты и их фрагменты и т.п., где термин "по существу свободны" в этом случае означает, что меньше чем 70%, обычно меньше чем 60% и чаще меньше чем 50% композиции, содержащей выделенный белок, представляет собой некоторые другие биологические молекулы, чем встречающиеся в природе. В некоторых воплощениях, белки присутствуют в по существу очищенной форме, где "по существу очищенная форма" означает очищенная по меньшей мере на 95%, обычно по меньшей мере на 97% и чаще по меньшей мере на 99%.
Заявленные белки могут быть получены искусственным путем, например, экспрессией рекомбинантной нуклеиновой кислоты, кодирующей последовательность, белка, представляющего интерес, в соответствующем хозяине, как описано выше. Для очистки белка могут применяться любые обычные методики, где подходящие методы очистки белка описаны в Guide to Protein Purification, (Deuthser ed., Academic Press, 1990). Например, лизат может быть приготовлен из исходного источника и очищен с использованием ВЭЖХ, вытеснительной хроматографии, гель-электрофореза, афинной хроматографии и т.п.
Также обеспечиваются антитела, которые специфически связываются с флуоресцентным белком настоящего изобретения. Подходящие антитела могут быть получены, с использованием способов, известных в данной области. Например, поликлональные антитела могут быть получены как описано в (Harlow and Lane Antibodies: A Laboratory Manual, 1988, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, New York), и моноклональные антитела могут быть получены как описано в (Coding Monoclonal Antibodies: Principles and Practice: Production and Application of Monoclonal Antibodies in Cell Biology, Biochemistry and Immunology; 3 rd edition, 1996, Academic Press). Химерные антитела, включая гуманизированные антитела, так же как одноцепочечные антитела и фрагменты антител, такие как Fv, F(ab')2 и Fab также представляют интерес.
Трансформанты
Нуклеиновые кислоты настоящего изобретения могут использованы для получения трансформатов, включая трансгенных организмов или сайт-специфичных генных изменений в клеточных линиях. Трансгенные клетки заявленные в изобретении, содержат одну или более нуклеиновых кислот, заявленных по настоящему изобретению, в качестве трансгена. Для целей изобретения любая приемлемая клетка-хозяин может быть использована, включая прокариотические (например, Escherichia coli, Streptomyces sp., Bacillus subtilis, Lactobacillus acidophilus, и т.д.) или эукариотические клетки-хозяева. Трансгенный организм, заявленный по изобретению, может быть прокариотическим или эукариотическим организмом, включая бактерии, цианобактирии, грибы, растения и животные, в которых одна или больше клеток организма содержат гетерогенную нуклеиновую кислоту, заявленную по изобретению, введенную посредством вмешательства человека, такими способами как технологии трансгеноза, которые известны в данной области.
Выделенная нуклеиновая кислота настоящего изобретения может быть введена в хозяина способами, известными в данной области, например инфицированием, трансфекцией, трансформацией или трансконъюгацией. Способы переноса молекулы нуклеиновой кислоты (то есть. ДНК) в такие организмы широко известны и обеспечивается в ссылках, таких как Sambrook et al. (Molecular Cloning: A Laboratory Manual, 3 nd Ed., 2001, Cold Spring Harbor Press, Cold Spring Harbor, NY).
В одном воплощении, трансгенный организм может быть прокариотическим организмом. Способы трансформации прокариотических хозяев хорошо описаны в данной области (например, см. Sambrook et al. Molecular Cloning: A Laboratory Manual, 2nd edition, 1989 Cold Spring Harbor Laboratory Press и Ausubel et al., Current Protocols in Molecular Biology, 1995, John Wiley & Sons, Inc).
В другом воплощении, трансгенными организмами могут быть грибы, например дрожжами. Дрожжи широко используются как носители для экспрессии гетерогенного гена (например см. Goodey et al Yeast biotechnology, D R Berry et al, eds, 1987, Alien and Unwin, London, p.401) и King et al Molecular and Cell Biology of Yeasts, E F Walton and G Т Yarronton, eds, Blackie, Glasgow, 1989, p.107). Несколько типов дрожжевых векторов доступны, включая интегративные векторы, которые требуют рекомбинации с геномом хозяина для их поддержки, и автономно реплицирующиеся плазмидные векторых.
Другой организм хозяина является животным. Трансгенные животные могут быть получены способами трансгеноза, известными в данной области и обеспечиваются в ссылках, таких как Pinkert, Transgenic Animal Technology: a Laboratory Handbook, 2nd edition, 2203; San Diego: Academic Press; Gersenstein and Vintersten, Manipulating the Mouse Embryo: A Laboratory Manual, 3 rd ed, 2002; Nagy A. (Ed), Cold Spring Harbor Laboratory; Blau et al., Laboratory Animal Medicine, 2nd Ed.,, 2002; Fox J.G., Anderson L.C., Loew F.M., Quimby F.W. (Eds), American Medical Association, American Psychological Association; Gene Targeting: A Practical Approach by Alexandra L. Joyner (Ed.) Oxford University Press; 2nd edition, 2000). Например, трансгенные животные могут быть получены гомологичной рекомбинацией, где изменяется эндогенный локус. Альтернативно, конструкция нуклеиновой кислоты включается случайным образом в геном. Векторы для устойчивого включения включают плазмиды, ретровирусы и другие животные вирусы, YAC, и т.п.
Нуклеиновые кислоты могут быть введены в клетку непосредственно или опосредованно, введением в прекурсор клетки, путем намеренной генетической манипуляции, такой как микроинъекция или инфицирование рекомбинантным вирусом или рекомбинантным вирусным вектором и т.п. Термин «генетическая манипуляция» не включает классическое скрещивание или оплодотворение in vitro, а предпочтительно является направленным на введение рекомбинантных молекул нуклеиновых кислот. Эти молекулы нуклеиновой кислоты могут быть включены в хромосому или они являться внехромосомными реплицирующими ДНК.
Конструкции ДНК для гомологичной рекомбинации будут содержать по меньшей мере часть нуклеиновой кислоты настоящего изобретения, где ген имеет желательную генетическую модификацую(ции) и включает области гомологии с целевым локусом. Конструкциям ДНК для произвольного включения не обязательно содержать область гомологии с медиатором рекомбинации. Легко могут быть включены маркеры для положительной и отрицательной селекции. Способы получения клеток, имеющих целевые генные модификации, через гомологическую комбинацию известны в данной области. Для различных способов трансфекции клеток млекопитающих, см. Keown et al., Meth. Enzymol, 1990, 185: 527-537.
Для эмбриональных стволовых (ЭС) клеток могут быть использованы ЭС клеточные линии или эмбриональные клетки могут быть получены непосредственно от хозяина, такого как мышь, крыса, морская свинка и т.д. Такие клетки выращиваются на подходящем фибропласт-питающем слое или в присутствии фактора ингибирования лейкемии (LIF). Трансформированные ЭС или эмбриональные клетки могут быть использованы для получения трансгенных животных, с помощью подходящего способа, описанного в данной области.
Трансгенные животные могут быть любыми животными, не относящимися к человеку, включая млекопитающее, не относящееся к человеку, (например мышь, крыса), птица или амфибия и т.д., и использованы в функциональном исследовании, скрининге лекарственного средства и т.п. Характерные примеры использования трансгенных животных включают те, которые описанные ниже.
Также могут быть получены трансгенные растения. Способы получения трансгенных растительных клеток и растений описаны в патентах СИТА №№5767367; 5750870; 5739409; 5689049; 5689045; 5674731; 5656466; 5633155; 5629470; 5595896; 5576198; 5538879; 5484956, раскрытия которых включены сюда ссылкой. Способы получения трансгенных растений также рассмотрены в Plant Biochemistry and Molecular Biology (eds. Lea and Leegood, John Wiley & Sons) 1993, p.275 и в Plant Biotechnology and Transgenic Plants (eds. Oksman-Caldentey and Barz), 2002, p.719.
Например, эмбриогенные эксплантаты, содержащие соматические клетки, могут использоваться для получения трансгенного хозяина. После сбора клеток или тканей, экзогенная ДНК, представляющая интерес, вводится в растительные клетки, при этом известен для такого введения ряд различных способов. При наличии выделенных протопластов, возникает возможность для введения через ДНК-опосредованные протоколы передачи гена, включая инкубацию протопластов с очищенной ДНК, такой как плазмида, содержащая целевую экзогенную последовательность, представляющую интерес, в присутствии поливалентных катионов (например, PEG или PLO); или электропорацию протопластов в присутствии выделенной ДНК, включающей целевую экзогенную последовательность. Протопласты, которые успешно включили экзогенную ДНК, затем отбираются, выращиваются в каллус, и в конечном счете в трансгенное растение при контакте с подходящими количествами и отношениями стимулирующих факторов, таких как ауксины и цитокины. Другие подходящие способы получения растения могут использоваться, такие, как применение "генной пушки", или Agrobacterium-опосредованная трансформация, которые доступны для квалифицированных специалистов в данной области.
Способы применения
Белки настоящего изобретения являются генетически кодируемыми флуоресцентными белками - фотосенсибилизаторами, проявляющими рекордные фототоксические свойства при облучении светом, более чем в 1000 раз превышающую токсичность других известных зеленых и красных флуоресцентных белков, включая AvGFP. Они могут быть использованы для селективной инактивации интересующих белков и селективного подавления клеточных делений и пролиферации клеток с адресной доставкой с помощью вирусных векторов и других методов.
Для осуществления селективной инактивации интересующих белков, должна быть получена нуклеиновая кислота, кодирующая белок KillerRed-tandem, оперативно связанный с интересующим белком (партнером слияния). Получение таких конструкций очевидно для любого специалиста в данной области. Полученная конструкция должна быть встроена в вектор, обеспечивающий временную или постоянную экспрессию этой нуклеиновой кислоты в клетках-хозяевах. Вектор может содержать элементы, обеспечивающие адресную доставку конструкции в интересующие клетки, или находится в составе частиц, обеспечивающих адресную доставку. После трансфекции клеток вектором и по истечении времени, необходимого для наработки в клетках продукта экспрессии (химерного белка), может быть осуществлена инактивация интересующего белка путем облучения клеток или клеточных компартментов активирующим светом.
Для осуществления селективного подавления клеточных делений и пролиферации клеток, должна быть получена нуклеиновая кислота, кодирующая белок KillerRed-tandem, оперативно связанный с гистоном (например, гистоном H2B), или другими белками или пептидами, обеспечивающими доставку химерного белка в ядра клеток. Полученная конструкция должна быть введена в клетку (например, в составе экспрессионного вектора). По истечении времени, необходимого для наработки в клетках продукта экспрессии (химерного белка), клетки облучают активирующим светом достаточной интенсивности, чтобы вызвать блокирование клеточных делений и пролиферации. Примеры подобного использования описаны в экспериментальной части ниже.
Следующие примеры предлагаются в качестве иллюстративных, но не ограничивающих.
Пример 1
Создание интрамолекулярного димера KillerRed
Для преодоления негативных последствий межмолекулярной димеризации белка KillerRed был сконструирован вектор, кодирующий две копии белка KillerRed, соединенные аминокислотным линкером (рис.2). В этом случае две копии KillerRed формируют интрамолекулярный димер (тандем), который по сути является мономерной меткой.
Для создания тандема были использованы два типа линкерных последовательностей GHGTGSTGSGSSGTASSEDNNMA (SEQ ID NO:13), и короткий линкер, имеющий аминокислотную последовательность RSPG (SEQ ID NO:14). Было показано, что оба варианта созревают в клетках Е.coli и обладают фототоксическим действием.
Пример 2
Исследование фототоксических свойств тандема KillerRed (tKR) в бактериальных клетках
Тандемные варианты KillerRed были полученны как описано в примере 1. Для сравнения фототоксичности KillerRed и tKR компетентные клетки Е.coli были трансформированы плазмидами на основе вектора pQE30 (Qiagen), обеспечивающими синтез данных белков. Колонии выращивали в течение ночи при 37°C и далее чашки инкубировали 3 дня при 4°C для полного созревания белка. По одной колонии KillerRed и tKR разбалтывали в 0.1 мл буфера PBS, после чего половину объема 30 мин облучали белым светом интенсивностью 1 Вт/см2, а половину оставляли в темноте в качестве контроля. Полученные суспензии клеток высевали на чашки Петри в различных разведениях и после ночного роста при 37°С подсчитывали число выросших колоний. Сравнение количества колоний в облученном и необлученном образцах позволяло оценить количество клеток, погибших от облучения светом. Эти эксперименты показали, что KillerRed и tKR обладают приблизительно одинаковой фототоксичностью для бактериальных клеток (в указанных условиях свет вызывал гибель около 99.9% клеток).
Пример 3
Использование tKR для мечения β-актина
Многие клеточные белки чувствительны к олигомеризации флуоресцентных белков, используемых для их мечения. В частности, к таким белкам принадлежит β-актин. Например, при экспрессии в клетках млекопитающих β-актина, слитого с димерным белком KillerRed, наблюдается образование агрегатов. Тандемные варианты KillerRed были полученны, как описано в Примере 1. Для подтверждения мономерного состояния tKR внутри клетки был сконструированы векторы для экспрессии химерного белка tKR-β-актин. Для этого нуклеиновые кислоты, кодирующие варианты tKR и нукленовая кислота KillerRed (вырезанная из коммерчески доступного вектора pKillerRed-C, Евроген) были клонированы в коммерчески доступный вектор pmKate2-actin (Евроген, Россия) вместо фрагмента нуклеиновой кислоты mKate2. Векторы были использованы для трансфекции клеток HeLa. Флуоресцентная микроскопия клеток HeLa, экспрессирующих данный вектор, показала ожидаемое внутриклеточное распределение красного флуоресцентного сигнала, соответствующее паттерну актина и полностью совпадающее с зеленым сигналом при ко-трансфекции с контрольным вектором, кодирующим химерный белок EGFP-β-актин.
Пример 4
Использование tKR для мечения гистона H2B
Для мечения гистона Н2 В были сконструированы векторы, кодирующие химерные белки, в которых С-конец Н2 В слит с последовательностью KillerRed или tKR через аминокислотный линкер DPPVATLEAT (SEQ ID NO:15), названные соответственно H2B-KillerRed и H2B-tKR (рис.2). Флуоресцентная микроскопия клеток млекопитающих (линии НЕК293, HeLa, HeLa Kyoto), временно трансфицированных вектором H2B-KillerRed, показала, что красный сигнал обладает ожидаемым внутриклеточным распределением, характерным для гистона Н2 В: были окрашены ядра клеток с паттерном интерфазного хроматина. Вместе с тем, флуоресцентных клеток, находящихся на различных стадиях митоза, обнаружено не было. Длительные наблюдения за клетками показали, что клетки, несущие H2B-KillerRed, не способны к делению. Это, очевидно, является следствием нарушения структуры хроматина из-за димеризации KillerRed в составе химерного белка H2B-KillerRed.
Напротив, при экспрессии вектора H2B-tKR нарушений митоза выявлено не было. Так, при временной трансфекции этим вектором клеток млекопитающих (линии НЕК293, HeLa, HeLa Kyoto) наблюдался ожидаемый паттерн внутриклеточной локализации красного флуоресцентного сигнала, соответствующий не только интерфазному хроматину, но и различным стадиям митотического деления. Подсчет количества митозов за определенный промежуток времени (с помощью флуоресцентной микроскопии) показал, что трансфицированные клетки с H2B-tKR делятся приблизительно с той же частотой, что и нетрансфицированные. Таким образом, H2B-tKR не обладает существенной цитотоксичностью (в темновых условиях).
Пример 5
Приготовление стабильно-трансфицированных линий клеток млекопитающих
Линия клеток HeLa Kyoto, стабильно экспрессирующая химерный белок H2B-tKR, была получена с помощью лентивирусной трансдукции. Для этого открытая рамка считывания H2B-tKR было клонирована в лентивирусный вектор pRRLSIN.EFl.WPRE. Трансдукция была проведена согласно стандартным протоколам. Популяция клеток с наибольшей интенсивностью красной флуоресценции была отобрана с помощью проточного флуоресцентного клеточного сортера MoFlo (Dako). Полученная линия стабильно экспрессировала H2B-tKR. Флуоресцентная микроскопия показала ожидаемый паттерн внутриклеточной локализации красного флуоресцентного сигнала, соответствующий интерфазному хроматину и различным стадиям митотического деления. Анализ распределения клеток по стадиям клеточного цикла (G1, S и G2/M) с помощью окраски ДНК йодидом пропидия и проточной цитофлуориметрии показал нормальное количество делящихся клеток в линии HeLa Kyoto H2B-tKR, сходное с таковым в исходной линии HeLa Kyoto.
Пример 6
Анализ фототоксичности H2B-tKR
Фототоксический эффект H2B-tKR первоначально изучали при помощи флуоресцентной микроскопии. В первой серии экспериментов клетки линии HeLa Kyoto, временно или стабильно экспрессирующие H2B-tKR, облучали зеленым светом с помощью флуоресцентного микроскопа (540-580 нм, 0,5 Вт/см2, 2 мин),. Затем продолжали наблюдение за облученными клетками с помощью флуоресцентного микроскопа в течение 48 часов. В течение первых 24 часов наблюдалось полное блокирование клеточного деления в клетках, экспрессирующих H2B-tKR. В течение этого времени ядра клеток сохраняли интерфазную морфологию, ни одна из клеток не поделилась. В то же время, клетки, не экспрессирующие H2B-tKR, сохраняли способность к делению и количество их удвоилось в течение эксперимента. Все облученные клетки, как экспрессирующие H2B-tKR, так и контрольные, не проявляли признаков клеточной гибели (открепления от субстрата, сжатия цитоплазмы, блеббинга (пузырения) мембраны).
Для того чтобы выяснить, повреждается ли ДНК при облучении клеток, экспрессирующих H2B-tKR, был использован белок XRCC1 (X-ray cross complementing factor 1), слитый с желтым флуоресцентным белком (EYFP). Белок XRCC1 является центральной платформой для сборки комплексов, осуществляющих репарацию ДНК. Ранее было показано, что XRCC1 немедленно перераспределяется к местам повреждения ДНК. Клетки HeLa Kyoto были котрансфицированы плазмидами для экспрессии EYFP-XRCC1 и H2B-tKR и анализировались с помощью флуоресцентной микроскопии до и после облучения. Как и ожидалось, до облучения флуоресцентный сигнал EYFP-XRCC1 был равномерно распределен в ядрах интерфазных клеток. Кроме того, часто наблюдались единичные яркие точки, предположительно, соответствующие активным репаративным комплексам. Вскоре после облучения зеленым светом EYFP-XRCC1 быстро (1-3 мин) перераспределялся и формировал множество ярких фокусов флуоресценции в ядрах клеток, экспрессирующих H2B-tKR. В контрольных клетках, экспрессирующих только EYFP-XRCC1, такого перераспределения не наблюдалось. Приведенные данные свидетельствуют об активации системы репарации ДНК, а следовательно, о возникновении повреждений геномной ДНК. Повреждения ДНК, в свою очередь, вероятно, вызывают активацию сверенных точек (чекпойнтов, от англ. checkpoint) клеточного цикла, вызывающих остановку клеточного цикла. После успешной репарации ДНК интерфазные клетки могут восстанавливать способность к пролиферации.
Для изучения воздействия H2B-tKR на митоз, клетки, находящиеся на момент начала эксперимента в метафазе митоза, облучали с помощью флуоресцентного микроскопа (540-580 нм, 0,5 Вт/см2, 2 мин). Во всех случаях после этого наблюдалось нерасхождение хромосом. Интересно, что в большинстве случаях, цитокинез начинался практически без задержки (по сравнению с контрольными облученными клетками, не экспрессирующими H2B-tKR, а также по сравнению с необлученными клетками, экспрессирующими H2B-tKR). Однако клетки были неспособны нормально завершить деление. Хромосомы оставались соединенными, не наблюдалось инициации анафазы, а в дальнейшем, после начала цитокинеза, образовавшаяся перетяжка либо пропадала, либо цитокинез проходил до конца, но отделялась лишь небольшая часть деконденсированного хроматина. В конечном итоге, образовавшиеся тетраплоидные клетки возвращались к интерфазной морфологии.
Изобретение относится к области к области молекулярной биологии и генной инженерии. Предложена выделенная нуклеиновая кислота, кодирующая интрамолекулярный димер KillerRed, оперативно слитый с гистоном, а также кассета экспрессии с данной нуклеиновой кислотой, содержащая ее клетка и белок, кодируемый ею. Изобретение может быть использовано в качестве инструмента прицельной фотоинактивации белков, нуклеиновых кислот и клеток в медицинских целях. 4 н.п. ф-лы, 2 ил.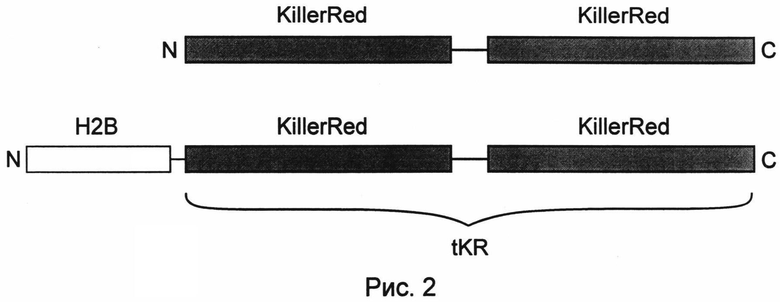
1. Нуклеиновая кислота, кодирующая оперативно слитый интрамолекулярный димер белка KillerRed, оперативно слитый с гистоном, обеспечивающим локализацию химерного белка в ядрах клеток-хозяев, где химерный белок вызывает блокирование клеточных делений и пролиферации при облучении активирующим светом и имеет аминокислотную последовательность, показанную в SEQ ID NO:6.
2. Кассета экспрессии, содержащая (а) регион инициации транскрипции, функциональный в клетке-хозяине; (б) нуклеиновую кислоту по п.1; и (в) регион терминации транскрипции, функциональный в клетке-хозяине, которая будучи интегрированной в геном клетки или при введении в клетку в виде внехромосомного элемента способна обеспечить экспрессию белка, кодируемого нуклеиновой кислотой по п.1.
3. Клетка, продуцирующая химерный белок, кодируемый нуклеиновой кислотой по п.1, и содержащая кассету экспрессии по п.2 как часть экстрахромосомного элемента или интегрированную в геном клетки как результат внедрения указанной кассеты в указанную клетку.
4. Химерный белок, который кодируется нуклеиновой кислотой по п.1, где указанный белок имеет аминокислотную последовательность, показанную в SEQ ID NO:6 и вызывает в клетках по п.3 блокирование клеточных делений и пролиферации при облучении.
| BULINA M.E., LUKYANOV K.A., BRITANOVA O.V., ONICHTCHOUK D., LUKYANOV S., CHUDAKOV D.M | |||
| Chromophore-assisted light inactivation (CALI) using the phototoxic fluorescent protein KillerRed | |||
| Nat Protoc | |||
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| SEREBROVSKAYA E.O., GORODNICHEVA T.V., ERMAKOVA G.V., SOLOVIEVA E.A., SHARONOV G.V., ZAGAYNOVA E.V., CHUDAKOV D.M., LUKYANOV S., | |||
Авторы
Даты
2013-08-27—Публикация
2011-12-07—Подача