Изобретение относится к фармацевтике и касается мазевой композиции, содержащей две активные фармацевтические субстанции, стимулирующие процессы регенерации, предназначенной для лечения повреждений кожи (обморожения, ожоги, эрозии, ссадины, язвы, трещины, раны, в том числе хирургические, др.).
Травматические повреждения кожи различного генеза представляют собой широко распространенный вид патологии человека. Восстановление целостности кожного покрова происходит за счет процессов репаративной регенерации, в основе которой лежат механизмы регенерации физиологической [1]. Поиск возможностей стимулировать эти процессы с целью более быстрого заживления дефекта и уменьшения вероятности возникновения осложнений остается актуальным и в настоящее время.
Ретинола пальмитат (РП) является одним из синтетических аналогов витамина А, обладает широким спектром фармакологической активности, в том числе дерматотропной. Он активизирует пролиферативные процессы в эпидермисе, тормозит терминальную дифференцировку кератиноцитов, усиливает синтез гликозаминогликанов в соединительнотканном слое кожи, стимулирует иммунные процессы в организме. Метилурацил (МУ) является производным пиримидина, представляет собой полученный путем синтеза структурный аналог тимина. Он стимулирует процессы регенерации в органах и тканях, в частности, в коже, печени, миокарде, эпителиях слизистых оболочек и др. [2]. Известен препарат Редецил®, в состав которого входят МУ (диоксометилтетрагидропиримидин) 3 г, ретинола пальмитат 0,5 г, вспомогательные вещества (бутилгидроксианизол 0,05 г, бутилгидрокситолуол 0,05 г, вода очищенная до 100 г, воск эмульсионный 8 г, глицерол 10 г, этанол 95% 10 г) - 100 г [3]. В экспериментах, проведенных на животных, было показано, что эта мазевая композиция, объединяющая в своем составе два стимулятора регенерации - РП и МУ, - способствует более ранней (в сравнении с мазями, содержащими только РП или только МУ) инициации репара-тивных процессов в экспериментальной ожоговой ране, сокращению сроков ее заживления и формированию более полноценного регенерата [4]. Применение этой мази в хирургической практике позволяет оптимизировать сроки лечения (особенно ожогов и гнойных и инфицированных ран), добиться более раннего наступления регенеративных процессов в течении трофических язв и более быстрого их заживления.
Известны составы лекарственных средств для наружного применения, содержащие в качестве стимулятора регенерации только РП [5] или только МУ [6]. Наиболее близким по медицинским показаниям и технической сущности к заявляемому составу является препарат для заживления ран, который содержит три биологически активные фармацевтические субстанции - РП, МУ и диметилсульфоксид (ДМСО), а в качестве стабилизаторов - бутилок-ситолуол (син. - бутилгидрокситолуол, БОТ) и бутилоксианизол (син. - бу-тилгидроксианизол, БОА) [7].
ДМСО, как известно, в значительной степени повышает проникновение веществ через кожу, увеличивая таким образом биодоступность наносимых на нее соединений, может усиливать не только активность, но и токсичность некоторых лекарств, способствует депонированию содержащихся в лекарственных средствах веществ, обладает рядом системных побочных эффектов [8]. Так как мазевые композиции, предназначенные для заживления повреждений кожи, должны быть поверхностно действующими, наличие в их составе соединения, усиливающего системное действие и кумуляцию фармацевтических субстанций, представляется неоправданным.
БОТ и БОА как антиоксиданты широко применяются в фармации и пищевой промышленности, однако известно, что им присущи и некоторые нежелательные эффекты, например, потенциальные канцерогенные свойства, способность повышать уровень холестерина, оказывать раздражающее действие на кожу, глаза и слизистые оболочки, в связи с чем их содержание в лекарственных средствах и пищевых продуктах должно быть регламентировано [9]. Задачей настоящего изобретения является разработка мазевой композиции с репарирующим эффектом, лишенной указанных недостатков.
В соответствии с изобретением описывается комбинированная мазевая композиция для наружного применения, стимулирующая регенераторные процессы в коже, содержащая в качестве активных веществ ретинола пальмитат и метилурацил, а в качестве вспомогательных веществ эмульсионный воск, вазелиновое масло, глицерин, α-токоферол, спирт этиловый и воду при следующем соотношении компонентов, мас.%:
Использование α-токоферола позволяет избежать использования таких компонентов, как ДМСО, бутилгидрокситолуол и бутилгидроксианизол при сохранении высоких ранозаживляющих и эксплуатационных свойств лекарственного препарата.
Лабораторные исследования
Эксперимент 1
Цель: изучить ранозаживляющую способность мази с РП и МУ, содержащей и не содержащей ДМСО.
Материал и методы. Опыты проводили на крысах-самках популяции Вистар со средней массой 200-210 г. Термический ожог вызывали путем наложения под гексеналовым наркозом на 20 сек на лишенную волосяного покрова кожу межлопаточной области спины нагретого в течение 1 мин в кипящей воде (100°С) медного куба массой 50 г с площадью соприкосновения 4 см2. Через сутки на месте ожогов возникали раны в виде изъязвлений, заполненных полненных некротическими массами. На раневую поверхность, начиная с третьего дня эксперимента, наносили мази в количестве 0,5 г, приготовленные на эмульсионной основе, содержащие в качестве активных субстанций 0,5% РП, 3% МУ и 10% ДМСО (1-й вариант) или 0,5% РП и 3% МУ (2-й вариант). Аппликации проводили 6 раз в неделю до полного заживления ран в одной из групп животных. Контролем служили крысы с ожоговыми ранами, не получавшие мазевых аппликаций. На 11-е сутки опыта у всех крыс с поверхности ран удаляли первичный струп. В ходе эксперимента у каждого животного измеряли площадь раневой поверхности. Для этого с помощью аппаратно-программного комплекса «ДиаМорф» (Россия) получали видеоизображения ран, которые затем обрабатывали методом компьютерной морфометрии. Рассчитывали абсолютные значения параметра. Статистическую обработку результатов исследований проводили с использованием t-критерия Стьюдента. Различия средних считали значимыми с уровнем вероятности не менее 95% (в таблицах отмечены звездочкой).
Результаты. Уменьшение площади ран у животных экспериментальных групп в сравнении с контрольными животными отмечалось уже через 4 дня после начала аппликаций мазей. Обе мази на всех исследованных сроках продемонстрировали выраженный репаративный дерматотропный эффект при некоторой вариабельности динамики процесса (табл.1).
Нанесение на раневую поверхность обоих вариантов мази позволило почти в два раза сократить сроки заживления ран по сравнению с показателями контрольной группы.
Таким образом, выведение ДМСО из состава мазевой композиции, содержащей РП и МУ, не внесло существенных изменений в специфическую фармакологическую активность лекарственного препарата.
Эксперимент 2
В заявляемый состав мазевой композиции α-токоферол введен с целью стабилизации ретиноида, и поэтому на первом этапе лабораторных исследований стабильность РП была изучена на примере модельных смесей.
Цель: изучить устойчивость субстанции РП, стабилизированной α-токоферолом.
Объект исследования составили модельные смеси - субстанция РП в вазелиновом масле без антиоксиданта (1) - контроль - и аналогичная комбинация, отличающаяся наличием в ней α-токоферола (2). Начальная концентрация РП в модельных смесях равнялась 1%, концентрация α-токоферола - 0,05%. Образцы были заложены на «ускоренное старение» в стеклянных банках с широким горлом при свободном доступе воздуха в условиях повышенной температуры.
Метод: спектрофотометрия по отношению к раствору стандартного образца.
Результаты анализа количественного содержания РП в модельных смесях, хранившихся при 40°С, представлены в таблице 2.
Из представленных данных следует, что содержание РП в образцах обеих модельных смесей до 22-го дня наблюдения оставалось практически на одном уровне. В дальнейшем концентрация субстанции в контрольном образце, т.е. в модельной смеси без антиоксиданта (1) стала снижаться. Анализ, проведенный в последующие дни, зафиксировал лавинообразное падение концентрации ретиноида в контрольных образцах (рис.1). В модельной смеси с антиоксидантом (2) концентрация ретиноида сохранялась на первоначальном уровне до 36-го дня наблюдения, и только впоследствии было отмечено ее снижение (см. табл.2, рис.1).
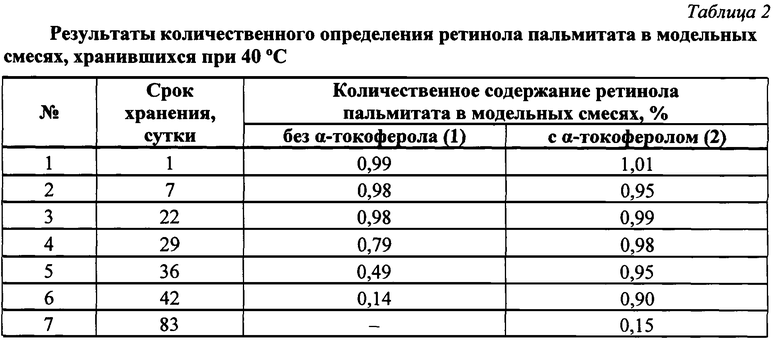
Полученный результат показывает, что присутствие в модельной смеси даже незначительного количества α-токоферола (0,05%) почти в два раза продлевает исходную устойчивость РП, что свидетельствует о наличии у α-токоферола в исследованных условиях выраженного антиокислительного эффекта и, в связи с этим, о перспективности его введения в состав лекарственных средств с целью стабилизации ретиноидов.
Эксперимент 3
Цель: установить эффективную концентрацию α-токоферола, способную затормозить окисление РП на длительный срок.
Объект исследования составили модельные смеси - субстанция РП в вазелиновом масле без антиоксиданта (1) и аналогичные комбинации (2-7), отличающиеся тем, что в них был добавлен α-токоферол в различных концентрациях (табл.3). Начальная концентрация ретиноида в модельных смесях равнялась 1%, α-токоферола - 0,02-0,25%. Образцы были заложены на хранение в стеклянных банках с широким горлом при свободном доступе воздуха при более жестких, чем в 1-м эксперименте, условиях «ускоренного старения» (50°С).
Метод: спектрофотометрия по отношению к стандартному образцу.
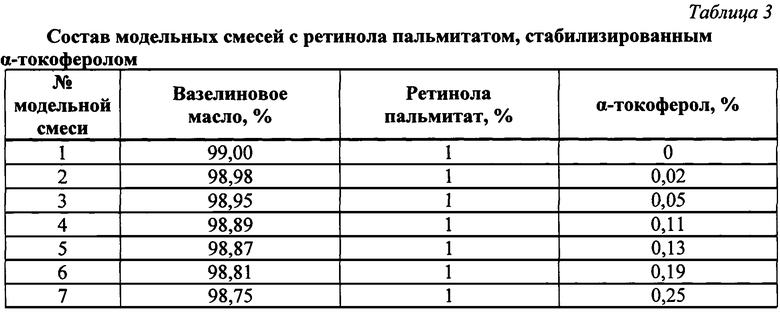
Результаты количественного определения РП в модельных смесях через 53 дня хранения при температуре 50°С представлены на рис.2.
На диаграмме видно, что разные количества α-токоферола в модельных смесях оказывают неравнозначное влияние на устойчивость ретиноида. Добавление антиоксиданта в диапазоне концентраций от 0,02 до 0,05% при хранении при 50°С в течение 53 суток в условиях доступа воздуха оказалось неэффективным. В количестве 0,11% α-токоферол стабилизировал ретиноид, но не в желаемой степени. Наиболее высокие показатели устойчивости РП в исследованных условиях наблюдались при концентрациях α-токоферола в модельных смесях от 0,13 до 0,25% включительно. Т. е. чем больше в смеси антиоксиданта, тем сильнее проявляется его свойство препятствовать окислению/разрушению фармацевтической субстанции (РП); иными словами, стабилизирующий эффект напрямую зависит от концентрации α-токоферола.
Таким образом, экспериментальные исследования стабильности РП при его хранении в условиях ускоренного старения в составе модельных смесей, содержащих в качестве антиоксиданта α-токоферол, продемонстрировали эффективность выбранного подхода к стабилизации ретиноида, т.е. замены в составе лекарственного препарата комбинации антиоксидантов фенольного типа (БОТ и БОА) на синтетический аналог природного витамина Е, и позволили перейти к изучению стабильности РП в составе мазевой композиции заявляемого состава.
Эксперимент 3
Цель: установить продолжительность стабильности фармацевтических субстанций (РП и МУ) в составе мазевых композиций, содержащих разные концентрации α-токоферола.
Объект исследования составили образцы комбинированных мазевых композиций, различающихся по содержанию α-токоферола (0,15; 0,2%).
Метод: высокоэффективная жидкостная хроматография.
Технология приготовления мази
1. Необходимое количество воды помещают в реактор и нагревают до 80°С. Затем в воду высыпают навеску метилурацила и перемешивают до растворения.
2. Параллельно в другой реактор помещают необходимые количества вазелинового масла (часть от общего содержания в препарате) и эмульсионного воска. Нагревают до температуры 75°С, расплавляя их.
3. В небольшое количество вазелинового масла помещают расчетные количества ретинола пальмитата и α-токоферола и смесь тщательно перемешивают.
4. После расплавления жировых компонентов основы (п.2) в реактор добавляют смесь ретинола пальмитата и α-токоферола и перемешивают.
5. В раствор метилурацила в воде (п.1) опускают головку гомогенизатора, включают его (8-10 тыс об./мин) и при активном перемешивании смеси медленно, тонкой струйкой добавляют расплав жировых компонентов мази (п.4). Через 2-5 минут [в зависимости от объема использованного реактора (0,5-3,0 л)] после смешивания всех компонентов препарата мазь окончательно гомогенизируют. Спустя 2-5 минут в реактор добавляют смесь этанола и глицерина, после чего мазь дополнительно гомогенизируют в течение 2 минут.
6. В связи с тем, что мазь содержит термолабильные компоненты (ретинола пальмитат, α-токоферол), разрушение которых усиливается при высоких температурах, ее следует принудительно охладить. После охлаждения мази до 35-40°С ее передают на участок фасовки в тубы.
Мазь должна храниться в сухом месте при температуре от 2 до 8°С. Замораживание не допускается.
Примеры приготовления конкретных композиций
Пример 1.
В реактор 1 с эффективной загрузкой в 100 кг мази отмеривают 62,35 л очищенной воды и нагревают ее до температуры 75-80°С. Включают двигатель рамной мешалки, добавляют 3,0 кг метилурацила и перемешивают до растворения при вращении рамной мешалки.
В реактор 2 отвешивают 8 кг эмульсионного воска, 5 кг вазелинового масла, включают двигатель рамной мешалки и, нагревая смесь до температуры 75-80°С, расплавляют ее.
В специальную емкость отвешивают 1 кг вазелинового масла, 0,5 кг ретинола пальмитата и 0,15 кг α-токоферола. Нагревают смесь до температуры 45-50°С, тщательно перемешивают и переносят в реактор 2.
С помощью роторно-пульсационного аппарата проточного типа смешивают компоненты двух реакторов до получения однородной эмульсии, в которую постепенно добавляют смесь 10 кг этилового спирта и 10 кг глицерина.
Полученную смесь окончательно гомогенизируют, охлаждают до температуры 30-35°С и фасуют в алюминиевые тубы.
Аналогично (по такой же схеме) получена мазь (пример 2), состав которой представлен в таблице 4.
Мазевые композиции по примерам 1 и 2, расфасованные в алюминиевые тубы, были заложены на длительное хранение при температуре 2-8°С.
Результаты количественного определения концентраций фармацевтических субстанций (РП и МУ) в этих мазях на разных сроках хранения представлены в таблице 5.
Как видно из результатов анализа, в процессе хранения образцов мазей, приготовленных по примерам 1 и 2, концентрация МУ на протяжении 2,5 лет хранения сохраняется на первоначальном уровне. Содержание РП в обеих мазях выдерживает необходимый срок хранения: через 2 года концентрация РП в них не снижается ниже допустимого предела. Мази, приготовленные по примерам 1 и 2, достаточно устойчивы и обеспечивают сохранность обеих фармацевтических субстанций в лекарственном препарате на протяжении необходимого срока годности.
Литература
1. Бабаева А.Г. Регенерация: факты и перспективы. - М.: Изд-во РАМН, 2009-336 с.
2. Белоусова Т.А. Фармакологические свойства метилурацила (обзор литературы) // Альманах "Ретиноиды". - М.: ЗАО "Ретиноиды", 2009. - Вып. 28. - С.11-43.
3. Альманах "Ретиноиды". - М.: ЗАО "Ретиноиды", 2010. - Вып.30. - С.4-11.
4. Ноздрин В.И., Яцковский А.Н., Белоусова Т.А. и др. Исследование специфической фармакологической активности препарата Редецил® // Альманах "Ретиноиды". - М.: ЗАО "Ретиноиды", 2010. - Вып. 30. - С.13-23.
5. Патент RU 2036640. - 12.05.1993. - Опубл. Бюлл. №16. - 10.06.95.
6. Патент RU 2135180. - 15.02.1999. - Опубл. Бюлл. №24 - 27.08.99.
7. Патент RU 2004239. - 24.12.1992. - Опубл. Бюлл. №45-46. - 15.12.93.
8. Santos N.C., Figueira-Coelho J., Martins-Silva J., Saldanha C. Multidiscipli-nary utilization of dimethyl sulfoxide: pharmacological, cellular, and molecular aspects // Biochem. Pharmacol. - 2003. - Vol.65, No. 7. - P. - 1035-1041.
9. СанПиН 2.3.2.1293-03. - П.3.4.4.
| название | год | авторы | номер документа |
|---|---|---|---|
| МАЗЬ С ВИТАМИНОМ А, ВОССТАНАВЛИВАЮЩАЯ КОЖУ И ПРЕПЯТСТВУЮЩАЯ ЕЕ ИЗБЫТОЧНОМУ ОРОГОВЕНИЮ | 2013 |
|
RU2527333C1 |
| МАЗЕВАЯ КОМПОЗИЦИЯ ДЛЯ МЕСТНОГО ПРИМЕНЕНИЯ С ПРОТИВОУГРЕВОЙ ФАРМАКОЛОГИЧЕСКОЙ АКТИВНОСТЬЮ | 2012 |
|
RU2500395C1 |
| ПОЛИВИТАМИННАЯ МАЗЬ ДЛЯ СМЯГЧЕНИЯ, ПИТАНИЯ И ЗАЖИВЛЕНИЯ КОЖИ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2008 |
|
RU2397770C1 |
| КОМБИНИРОВАННАЯ МАЗЕВАЯ КОМПОЗИЦИЯ ДЛЯ УМЕНЬШЕНИЯ ИНТЕНСИВНОСТИ ЛОКАЛЬНОЙ ГИПЕРПИГМЕНТАЦИИ КОЖИ | 2011 |
|
RU2450836C1 |
| МАЗЬ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ С НАРУШЕНИЕМ КЕРОТИНИЗАЦИИ И ЦЕЛОСТНОСТИ КОЖИ | 1993 |
|
RU2036640C1 |
| МАЗЬ ДЛЯ ЗАЖИВЛЕНИЯ РАН | 1999 |
|
RU2135180C1 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ГИПЕРКЕРАТОЗОВ, ВРОСШЕГО НОГТЯ, А ТАКЖЕ ДЛЯ ГИГИЕНИЧЕСКОЙ ОБРАБОТКИ НОГТЕЙ, ДЕФОРМИРОВАННЫХ В РЕЗУЛЬТАТЕ ТРАВМЫ И/ИЛИ ВОЗРАСТНЫХ ИЗМЕНЕНИЙ | 2005 |
|
RU2292879C2 |
| Косметическая композиция для кожи и волос человека | 2024 |
|
RU2839865C1 |
| СТАБИЛЬНЫЙ РАСТВОР РЕТИНОЛА ПАЛЬМИТАТА И СПОСОБ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ КОЖИ | 2000 |
|
RU2168996C1 |
| СТАБИЛЬНАЯ ЭМУЛЬСИОННАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ЧЕСОТКИ | 2014 |
|
RU2575571C2 |
Изобретение относится к химико-фармацевтической промышленности и представляет собой комбинированную мазевую композицию для стимуляции регенерации кожи, содержащую ретинола пальмитат, метилурацил, α-токоферол, воск эмульсионный, масло вазелиновое, глицерин, этанол и воду, отличающуюся тем, что содержит компоненты при следующем соотношении, мас.%: ретинола пальмитат 0,5-1,0; метилурацил 2,0-3,5; α-токоферол 0,15-0,2; воск эмульсионный 5,0-15,0; масло вазелиновое 5,0-15,0; глицерин 5,0-15,0; этанол 95% 5,0-15,0; вода дистиллированная до 100,0. Изобретение обеспечивает повышение устойчивости ретинола пальмитата. 2 ил., 2 пр., 5 табл.
Комбинированная мазевая композиция для местного применения, стимулирующая регенераторные процессы в коже, на основе ретиноида и метилурацила, содержащая ретинола пальмитат, метилурацил, α-токоферол, воск эмульсионный, масло вазелиновое, глицерин, этанол и воду при следующем соотношении компонентов, мас.%:
| ПОЛИВИТАМИННАЯ МАЗЬ ДЛЯ СМЯГЧЕНИЯ, ПИТАНИЯ И ЗАЖИВЛЕНИЯ КОЖИ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2008 |
|
RU2397770C1 |
| RU 2004239 C1, 15.12.1993 | |||
| МАЗЬ ДЛЯ ЗАЖИВЛЕНИЯ РАН | 1999 |
|
RU2135180C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ МЕСТНОГО ПРИМЕНЕНИЯ, ОБЛАДАЮЩАЯ АНТИБАКТЕРИАЛЬНЫМ И НЕКРОЛИТИЧЕСКИМ ДЕЙСТВИЕМ, НА ОСНОВЕ ЛИЗОАМИДАЗЫ | 2007 |
|
RU2367469C2 |
| СТАБИЛЬНЫЙ РАСТВОР РЕТИНОЛА ПАЛЬМИТАТА И СПОСОБ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ КОЖИ | 2000 |
|
RU2168996C1 |
Авторы
Даты
2013-10-20—Публикация
2012-06-20—Подача