Изобретение относится к медицине и ветеринарии, а именно к фармакологическим препаратам, применяемым при лечении гнойных ран и ожогов, гнойно-воспалительных заболеваний кожи и др. для ускорения и улучшении условий заживления.
Известны комплексы бактериолитических ферментов, лизирующие грамположительные микроорганизмы, устойчивые к антибиотикам (патенты RU 1549227, C12N 9/00, 1984.10.04; RU 2193063, C12N 9/00, 2000.11.29).
Комплекс бактериолитических ферментов (патент RU 1549227), используемый в медицине под названием лизоамидаза, а в ветеринарии - лизомаст (патент RU 2064299, A61K 35/74, 1993.12.13), состоит из трех бактериолитических ферментов, иммобилизованных на полисахариде, что повышает их стабильность. Полисахарид обеспечивает длительное (в течение нескольких лет) сохранение высокой активности входящих в него ферментов, а также иммуностимулирующие свойства препарата лизоамидаза.
На основе данного комплекса разработан фармакологический препарат, обладающий антибактериальным и некролитическим действием, выпускаемый в виде лиофилизированного порошка, упакованного в 10 мл флаконы по 50 ПЕ, 100 ПЕ с герметично укупоренными резиновыми пробками. При этом в комплект поставки входит растворитель в ампулах по 5 мл из расчета 1 ампула на 50 ПЕ (фармакопейные статьи ФС 42-3329-96 и ФС 42-3332-96).
Препарат применяется в жидком виде в фосфатном буферном растворе с концентрацией 5 ПЕ (50 ЛЕ) в 1 мл; 10 ПЕ (100 ЛЕ) в 1 мл; 25 ПЕ (250 ЛЕ) в 1 мл.
Бактериолитические ферменты, входящие в активный комплекс указанного препарата, разрушают клетки широкого спектра грамположительных патогенных микроорганизмов, таких как стафилококки и стрептококки, в том числе имеющих множественную резистентность к антибиотикам, радиоустойчивые микрококки, менингококки, гонококки, грамположительные бациллы. Благодаря наличию в комплексе протеазы и ферментов, обладающих одновременно и протеолитической активностью, препарат хорошо очищает раны от некротических масс. Фрагменты разрушенных клеток обладают иммуностимулирующим действием.
Клинические исследования препарата показали, что лизоамидаза при лечении гнойных ран мягких тканей ускоряет по сравнению с другими традиционными и нетрадиционными средствами течение раневого процесса. Быстрее снижается содержание микрофлоры, быстрее нормализуется цитограмма, быстрее идет отторжение некротических масс, быстрее происходит грануляция и даже эпителизация тканей. Сроки лечения больных с гнойными ранами мягких тканей сокращались во многих случаях в 2 раза. Лизоамидаза стимулирует репаративные процессы, оказывая, помимо некролитического и бактериолитического действия, влияние на течение 2-ой фазы воспаления, причем не только за счет сокращения 1-ой фазы, что характерно для всех ферментных препаратов, используемых для лечения в подобных случаях, но и за счет непосредственно стимулирующего влияния на клетки грануляционной ткани, воздействуя непосредственно на клетки пролиферата.
Применение известного препарата в виде жидких растворов обладает рядом недостатков, а именно: препарат плохо фиксируется и удерживается на раневой поверхности, что приводит к повышенному расходу активного вещества при лечении; требует предварительного разведения в буферном растворе и специальных мер по предотвращению быстрого высыхания, что не удобно в лечебном процессе. Все это снижает приверженность пациента к лечению. Недостатками данного препарата является также то, что он не обладает местным анестезирующим действием.
Задачей предлагаемого изобретения является создание фармакологического препарата для местного применения в виде мягкой лекарственной формы на основе комплекса бактериолитических и протеолитических ферментов.
Технические результаты, которые могут быть получены при использовании предлагаемого изобретения: расширение области применения, повышение терапевтической активности; улучшение удобства использования; снижения расхода активного вещества; получение анестезирующего эффекта; улучшение микроцикуляции в раневых тканях, ослабление воспалительных процессов, дополнительное стимулирование репаративных процессов.
Для решения поставленной задачи предлагается фармакологический препарат для местного применения в виде мягкой лекарственной формы, состоящий из активного комплекса бактериолитических и протеолитических ферментов, например лизоамидазы, (далее «активный комплекс») и основы, обеспечивающей мягкую лекарственную форму препарата, при следующем соотношении компонентов (мас.%):
Предложенный препарат для местного применения в виде мягкой лекарственной формы дополнительно содержит целевые добавки, совместимые с активным комплексом, при следующем соотношении компонентов (мас.%):
В качестве целевых добавок может быть местноанестезирующее вещество и/или стимулятор репаративных процессов.
Для обеспечения анестезирующего эффекта в предлагаемом фармакологическом препарате может содержаться местноанестезирующее вещество при следующих соотношениях компонентов (мас.%):
При этом местноанестезирующим веществом может быть, например, хиноксикаин, тримекаин, пиромекаин, лидокаин, анестезин (бензокаин) и дибукаин или их смеси.
Кроме того, в предлагаемом фармакологическом препарате может содержаться стимулятор репаративных процессов в количестве (мас.%):
При этом веществом, являющимся стимулятором репаративных процессов, может быть, например, метилурацил, ацемин, этаден, кальция пантотенат, солкосерил, трекрезан или их смесь.
Предлагаемый фармакологический препарат, содержащий местноанестезирующее вещество, может содержать также стимулятор репаративных процессов при следующем соотношении компонентов (мас.%):
В соответствии с предлагаемым изобретением мягкими лекарственными формами на основе комплекса бактериолитических и протеолитических ферментов, типа лизоамидаза, являются мазеобразные мягкие лекарственные формы - мази, гели, кремы, а также формируемые мягкие лекарственные формы - желатиновые капсулы для ректального применения.
В предложенном фармакологическом препарате основа содержит термически стойкую эмульсию перфторорганических соединений с газотранспортными свойствами и смесь гиперосмолярных веществ при следующем соотношении компонентов (мас.%):
Гиперосмолярные вещества содержатся в составе смеси, например, при следующих соотношениях компонентов (мас.%):
Смесь №1:
Смесь №2:
Смесь №3:
Смесь №4:
Смесь №5:
Смесь №6:
Смесь №7:
Смесь №8:
Смесь №9:
Смесь №10:
Смесь №11:
Смесь №12:
Одной из главных задач местного лечения ран и ожогов является проблема подавления болевого синдрома. Для решения этой задачи в предложенном препарате применено местноанестезирующее вещество, в качестве которого могут быть использованы хиноксикаин (производное хинолина), обладающий бактериальной и антиоксидантной активностью; лидокаин; тримекаин, сохраняющий свою активность в кислой среде, которой характеризуется гнойная рана; пиромекаин; анестезин; дибукаин. Лидокаин, тримекаин и пиромекаин наиболее перспективны в составе предлагаемого препарата на гидрофильной основе. Для предлагаемого препарата на жировой основе должны использоваться, например, анестезин (бензокаин) и дибукаин.
Для обеспечения дополнительного стимулирования процессов репарации в ране предложенный препарат на основе комплекса бактерио- и протеолитических ферментов содержит вещество ранозаживляющего действия: метилурацил, ацемин, этаден, кальция пантотенат, солкосерил, трекрезан или их смесь.
Метилурацил, являясь производной пиримидина, обладает анаболической и антикатаболической активностью. Вещество не оказывает местного раздражающего действия, ускоряет процессы клеточной регенерации, сокращая сроки заживления ран, стимулирует клеточные и гуморальные факторы защиты, оказывает противовоспалительное действие, стимулирует эритро- и лейкопоэз.
Ацемин ускоряет регенерацию тканей и процессы эпителизации. Применяется для лечения длительно незаживающих ран и ожогов.
Этаден стимулирует репаративные процессы в эпителиальной и кроветворной тканях, активируя метаболизм нуклеиновых кислот. Показан для лечения термических и лучевых поражений кожи, слизистой оболочки прямой кишки, длительно незаживающих гранулирующих ран и т.д.
Кальция пантотенат является перспективным ранозаживляющим средством. Применяется для лечения ожогов и вяло заживающих ран.
Солкосерил - экстракт крови крупного рогатого скота, освобожденный от протеинов и не обладающий антигенной активностью. Вещество ускоряет рост грануляций и эпителизацию ран, улучшает обменные процессы в тканях.
Трекрезан - триэтаноламмониевая соль 2-метилфеноксиуксусной кислоты. Стимулирует пролиферативно-репаративные процессы, что делает перспективным его применение в хирургической практике для ускорения заживления гнойно-некротических повреждений и послеоперационных ран («Химико-фармацевтический журнал», том 41, №1, 2007 г., стр.3-7).
Аэросил - коллоидная двуокись кремния. Высокодисперсный, микронизированный порошок с размером частиц от 4 до 40 мкм (в основном 10-30 мкм), плотностью 2,2 г/см3, имеет большую удельную поверхность от 50 до 400 м2/г. В воде и спирте в концентрации 1-3% образует мутные взвеси, с жидкостями, имеющими показатель преломления около 1,45, образует прозрачные студнеобразныне системы (глицерин, вазелиновое масло и т.д.). При наружном применении не вызывает раздражения кожи, не нарушает кожный обмен.
С микробиологической точки зрения в связи с наличием внешних полисахаридных оболочек и гидрофильных капсул у грамотрицательных и грамположительных бактерий, которые препятствуют проникновению в микробные клетки гидрофобных антибактериальных веществ, гидрофильные основы предпочтительнее, так как служат проводниками лекарственных средств в микробную клетку.
Гидрофильные основы, которые могут быть применены с комплексом бактериолитических и протеолитических ферментов, например лизоамидазой, в предлагаемом препарате разделены на две группы:
- водорастворимые основы, которые, как правило, содержат воду очищенную, гидрофильные неводные растворители: полиэтиленоксид, например ПЭО-400, 1,2-пропиленгликоль, глицерин, этилцеллозольв, димексид, - и водорастворимые полимеры: полиэтиленоксид, например ПЭО-1500, проксанол, например проксанол-268;
- водосмываемые основы, которые кроме водорастворимых полимеров и гидрофильных неводных растворителей содержат липофильные вещества: высшие жирные спирты, вазелин, вазелиновое масло, ланолин, воски (эти основы, как правило, представляют эмульсии типа масло/вода и требуют присутствия эмульгатора типа масло/вода).
Основы с гиперосмолярными свойствами играют важную роль при местной терапии гнойных ран. Они обеспечивают отток гнойного экссудата из раны, оказывают противовоспалительное действие за счет абсорбции жидкости и снижения отека тканей раны, а также предохраняют ткани от гипергидратации. Часто они способствуют усилению действия антибактериальных веществ.
К веществам, обладающим высокими гиперосмолярными свойствами, относятся полиэтиленоксиды - водорастворимые продукты полимеризации окиси этилена, которые являются физиологически индифферентными соединениями. В этот класс веществ входят гидрофильные неводные растворители (полиэтиленоксид, например ПЭО-400; 1,2-пропиленгликоль; глицерин; этилцеллозольв; димексид) и полимеры (полиэтиленоксид, например ПЭО-1500, проксанол-268). Они легко наносятся на раневую поверхность и равномерно по ней распределяются, улучшая контакт мази с тканями и содержимым раны, хорошо смешиваются с раневым экссудатом и сохраняют при этом свою однородность, малотоксичны и не оказывают раздражающего действия на ткани, не нарушают их физиологических функций.
В гнойной ране ПЭО разной молекулярной массы ведут себя по-разному. Так, молекулы ПЭО-1500 стабильно сохраняют первичную локализацию: они остаются в полости раны и активно связывают воспалительный экссудат, отдавая его в повязку, с которой жидкость испаряется. Освободившиеся молекулы ПЭО-1500 вновь присоединяют к себе воду, и процесс повторяется. Более мелкие молекулы ПЭО-400 обладают способностью проникать вглубь тканей и уже через 2 часа определяются в дне и стенках раны. Образуя комплексы с антибактериальными веществами, ПЭО-400 проводит их в ткани раны, где локализуются микробы. Способность полиэтиленоксидов обеспечивать антимикробному препарату внутритканевое действие принципиально отличает эту мазевую основу от жировых основ или растворов антибиотиков (антисептиков), противомикробное действие которых ограничивается только поверхностью раны, хотя именно глубинная микрофлора определяет выраженность и направленность течения гнойного процесса.
Основное свойство ПЭО состоит в том, что они обладают выраженным дегидратирующим (влагопоглощающим) действием на ткани. Благодаря высокой способности гидратироваться, эти полимеры активно абсорбируют раневой экссудат, а вместе с ним и микробные токсины, продукты распада тканей, а также различные биологически активные вещества лизосомальные ферменты и другие медиаторы воспалительного процесса, прерывая тем самым его прогрессирующее течение. Принципиальное значение имеет тот факт, что в гнойной ране дегидратирующее действие ПЭО распространяется не только на ткани, образующие дно и стенки раневой полости, но и на содержащиеся в ране микробные клетки. Обезвоживание микробных клеток ведет к существенному снижению ее биологической активности и, в том числе, устойчивости к действию тех или иных лекарственных средств. Поэтому в присутствии ПЭО в десятки раз повышается антимикробное действие антибиотиков.
Имеет также значение то, что растворение антибиотиков, сульфаниламидов и других веществ в ПЭО приводит к повышению их дисперсности с увеличением терапевтической активности, чему также способствует более быстрое высвобождение из основы антимикробных веществ. ПЭО является активным проводником лекарственных средств через кожный барьер. Важно то, что эта пенетрирующая без повреждения клеток способность ПЭО усиливается в условиях воспаления.
Гидрофильные основы на полиэтиленоксидах способны растворяться в секретах слизистых оболочек, полностью высвобождать лекарственные вещества, не раздражать слизистую, имеют большой срок годности, высокую физиологическую индифферентность, что способствует их применению в мазеобразных и формируемых мягких лекарственных формах.
Важным медико-биологическим требованием, предъявляемым к мазевым мягким лекарственным формам, является способность смачивать раневую поверхность и растекаться по ней, что обусловлено поверхностно-активными свойствами растворителей, полимеров, поверхностно-активных веществ (ПАВ) и основы в целом. Наиболее выраженную поверхностную активность имеют спирты и этилцеллозольв, которые непригодны для включения в состав основы в больших концентрациях. Из гликолей предпочтительно применение 1,2-пропиленгликоля и ПЭО-400 по сравнению с глицерином, обладающим слабыми поверхностно-активными свойствами.
В Государственном реестре лекарственных средств зарегистрировано 5 полиэтиленоксидов (ПЭО) с различной молекулярной массой: ПЭО-400; ПЭО-1000; ПЭО-1500; ПЭО-2000 и ПЭО-4000.
При смешивании растворителя ПЭО-400 с полимером ПЭО-1500 последний выступает в роли загустителя, который в зависимости от количества в общей массе обеспечивает требуемую консистенцию создаваемой лекарственной формы. Кроме того, ПЭО-1500 является осмотически активным веществом, поглощающим гнойный экссудат за счет связывания молекул воды с гидроксильными и простыми эфирными группами. Данная основа рекомендована для мазевых лекарственных форм, применяемых при местном лечении ран в 1-й фазе раневого процесса.
Проксанол-268 - блоксополимер окисей пропилена и этилена. Проксанол-268 как осмотически активное вещество обеспечивает более равномерный характер абсорбции и обладает более длительным периодом осмотического действия. Общая масса абсорбируемой воды растворами проксанола-268 за 24 часа существенно превосходит таковую в случае применения ПЭО-1500. Это связано с более высокой массой проксанола-268 (в 8,7 раза больше, чем у ПЭО-1500).
Кинетика абсорбции воды растворителями и полимерами зависит от их молекулярной массы, концентрации и строения молекул. Так ПЭО-400 абсорбирует больше воды, чем 1,2-полиэтиленгликоль, и обладает более длительным периодом осмотического действия. Сорбционная активность 1,2-пропиленгликоля сохраняется в течение 4-6 часов. Это обусловлено как более низкой его молекулярной массой по сравнению с ПЭО-400, так и более низким гидрофильно-липофильным балансом (ГЛБ), который для пропиленгликоля составляет 9,38.
Величина гидрофильно-липофильного баланса (ГЛБ) тем больше, чем большей гидрофильностью обладает вещество. Поэтому, чем выше ГЛБ и молекулярная масса, тем сильнее и длительное будет проявляться осмотическое действие вещества при данной концентрации. Значения ГЛБ для некоторых веществ: 1,2-пропиленгликоль - 9,375; глицерин - 11,275; этилцеллозольв - 8,3; ПЭО-400 - 12,49; ПЭО-1500 - 20,74.
1,2-пропиленгликоль, ПЭО-400, ПЭО-1500, проксанол-268 могут быть консервантами в разрабатываемых мягких лекарственных формах.
Нарушение микроциркуляций является одним из основных факторов патогенеза воспалительного процесса. Она включает в себя не только ток крови по артериолам, капиллярам и венулам, но и транскапиллярный обмен, обеспечивающий необходимый для жизни тканевый гомеостаз. Расстройства микроцикуляции делятся на внутрисосудистые изменения, нарушения самих сосудов и внесосудистые изменения. Лечебный спектр препаратов, применяемых с целью улучшения процессов микроциркуляции в тканях раны, в значительной мере может быть реализован за счет их антигистаминного, противовоспалительного и дегидратирующего действия.
Применение гиперосмолярной основы, совместимой с комплексом бактерио- и протеолитических ферментов, улучшает микроциркуляцию в тканях раны за счет ее дегидратирующего действия. При этом применяемая основа, состоящая из гипреосмолярных веществ, обладает косвенным противовоспалительным действием за счет абсорбции жидкости и снижения отека тканей раны.
Димексид - 30%-ный раствор диметилсульфоксида (ДМСО) - применяется как противовоспалительный препарат для наружного применения, инактивирующий гидроксильные радикалы и улучшающий течение метаболических процессов в очаге воспаления. Оказывает также местноанестезирующее, анальгезирующее и противомикробное действие; обладает умеренной фибринолитической активностью. Проникает через кожу, слизистые, оболочку микробных клеток (повышает их чувствительность к антибиотикам) и другие биологические мембраны, не повреждая их, и может проводить разнообразные лекарственные средства в глубину раны. К отрицательным характеристикам димексида следует отнести то, что он быстро сохнет.
Гиалуроновая кислота - полисахарид из семейства глюкозаминогликанов - обладает способностью связывать в 1000 раз больше воды, чем весит сама. Гиалуроновая кислота имеет самую высокую гигроскопичность по сравнению с другими увлажняющими агентами, такими как глицерин и сорбитол. При этом поглощенная вода удерживается внутри геля и не испаряется даже при понижении относительной влажности окружающего воздуха. В силу своей высокой гидрофильности гиалуроновая кислота образует с водой высоковязкие гели, которые увлажняют кожу и слизистые оболочки. Гиалуроновая кислота нетоксична. В составе гелей гиалуроновая кислота оказывает антимикробное, ранозаживляющее и противовоспалительное действие, способствует регенерации эпителия, предотвращает образование грануляционных тканей, спаек, рубцов, нормализирует кровообращение, не вызывает клинических осложнений.
Гиалуроновая кислота положительно влияет на течение местных воспалительных процессов, связывает микрофлору, а также продукты ее распада и жизнедеятельности, обладает выраженным противовоспалительным действием и местноанестезирующим эффектом. В то же время гиалуроновая кислота осуществляет и механическую защиту ран, так как образует тонкую пленку, которая препятствует проникновению в рану факторов внешней среды - болезнетворных агентов. Гели на основе гиалуроновой кислоты используют для лечения местных и общих гнойно-воспалительных процессов, термических и химических ожогов, трофических язв при хронической венозной недостаточности, лучевых поражений кожи, трещин, ссадин, а также для лечения длительно незаживающих ран различной этиологии (патент RU №2195262).
Гиалуронат натрия - натриевая соль гиалуроновой кислоты - хорошо растворима в воде с образованием вязкого бесцветного геля с pH 6,0 -7,5 (0,1%-ный раствор). По своей активности гиалуронат натрия - полный аналог гиалуроновой кислоты, способствует регенерации тканей без образования шрамов, обладает способностью стимулировать клеточную миграцию и пролиферацию. Используется в концентрациях, начиная от 0,01 до 0,5%.
Известно, что перфторорганические эмульсии с газотранспортными свойствами, типа перфторан, использовались при комплексном лечении ран и раневой инфекции (Крылов Н.Л. и др. Гемосорбция и инфузия перфторана в комплексном лечении ран и раневой инфекции. Проблемы интенсивной терапии в клинике. Тезисы научной конференции. 12-13 декабря 1985 г. - М.: Б.и., 1985 г. - стр.12-13). Кроме того, известно, что перфторуглеродные соединения являются перспективными противовоспалительными средствами для лечения кожных болезней и могут применяться в дерматологии и лечебной косметологии (Умеров Ж.Г., Филипов Е.А. Перфторуглеродные соединения - перспективные противовоспалительные средства для лечения кожных болезней. IX Всесоюзный съезд дерматовенерологов. Алма-Ата, 23-27 сентября 1991 г. Тезисы докладов. - М., 1991. - стр.354).
Перфторорганические эмульсии с газотранспортными свойствами обладают ранозаживляющим эффектом, что связано с их влиянием на газообмен прилежащих тканей, поскольку раневое поражение сопровождается нарастающей гипоксией клеток тканей и усиливающимся ацидозом (патент RU №2033163, A61K 33/16, 1995.04.20).
Известны перфторорганические эмульсии с газотранспортными свойствами (например, патент RU №2088217, A61K 9/10, 1993.05.07), которые могут храниться при комнатной температуре не менее 1 года.
Вышеприведенный анализ известных свойств гиперосмолярных веществ позволил подобрать вышеуказанные основы с гиперосмолярными свойствами для предлагаемого фармакологического препарата, содержащего комплекс бактериолитических и протеолитических ферментов.
С использованием этих основ для мягких лекарственных форм, а также комплекса бактериолитических и протеолитических ферментов, местноанастезирующего вещества и стимулятора репаративных процессов предложены композиции гидрофильных мазей, гидрофильных кремов, гидрофильных гелей, которые также могут быть использованы для изготовления желатиновых или других капсул для ректального применения.
Вид лекарственной формы предлагаемого фармакологического препарата зависит от молекулярной массы используемых гиперосмолярных веществ, их соотношения в составе смеси, а также количественного соотношения гиперосмолярной основы с другими компонентами фармакологического препарата. Исходя из этих количественных соотношений, лекарственная форма предлагаемого фармакологического препарата может быть мазью, гелем или кремом.
Наиболее предпочтительной для внешнего применения является мазевая форма, так как она хорошо фиксируется и удерживается на раневой поверхности, дольше обладает терапевтической активностью, дешевле в изготовлении, удобна в использовании, что усиливает мотивацию больного к лечению.
Гидрофильные мази являются гиперосмолярными, вследствие чего при применении могут абсорбировать значительное количество экссудата.
Гидрофильные кремы приготовлены на основе эмульсии вода/масло или вода/масло/вода, стабилизированной подходящими эмульгаторами. К ним также относятся коллоидные дисперсные системы, состоящие из диспергированных в воде или смешенных вводно-гликолевых растворителей высших жирных спиртов или кислот, стабилизированные гидрофильными ПАВ. Кремы представляют собой двух- или многофазные дисперсные системы, дисперсионная среда которых при установленной температуре хранения, как правило, имеет ньютоновский тип течения и низкие значения реологических параметров.
Гидрофильные гели (гидрогели) приготовлены на основах, состоящих из воды, гидрофильного смешенного или неводного растворителя (глицерин, 1,2-пропиленгликоль, полиэтиленоксид ПЭО-400) и гидрофильного гелеобразователя (карбомеры, производные целлюлозы, трагакант, гиалуронат натрия, гиалуроновая кислота и др.). Гели представляют собой одно-, двух- или многофазные дисперсные системы с жидкой дисперсной средой, реологические свойства которых обусловлены присутствием гелеобразователей в сравнительно небольших концентрациях. В этой лекарственной форме гелеобразователи дополнительно могут выполнять роль стабилизаторов дисперсных систем: суспензий или эмульсий.
Желатиновые капсулы для ректального применения с технологической, биофармацевтической и экономической точки зрения. Желатиновая оболочка предохраняет лекарственные вещества от воздействия факторов внешней среды и имеет преимущества перед суппозиториями, так как в ней могут капсулироваться вещества в виде мази, линимента, крема, геля, эмульсии, суспензии и др. Высвобождение лекарственного вещества происходит быстрее и легче, чем у суппозиториев, так как под влиянием слабощелочной среды (pH 7,3-7,6) содержимого прямой кишки желатиновые оболочки набухают, и в таком состоянии даже слабая перистальтика стенки прямой кишки достаточна для ее разрыва и высвобождения содержимого. Количество лекарственного вещества в капсуле, оказывающее необходимый терапевтический эффект, составляет двойную дозу суппозиториев.
Таким образом, производство ректальных средств в желатиновой оболочке позволяет экономить дорогостоящие биологически активные ингредиенты и уменьшить себестоимость препаратов. Ректальные желатиновые капсулы с предлагаемым фармакологическим препаратом отвечают всем требованиям к идеальным суппозиториям и могут применяться в медицине для лечения проктологических заболеваний.
Комплекс бактериолитических и протеолитических ферментов, типа лизоамидаза, в предлагаемом фармакологическом препарате лизирует грамположительные микроорганизмы, в том числе устойчивые к антибиотикам, а также за счет свой протеолитической активности очищает раны от некротических масс, оказывая при этом иммуностимулирующее действие. Кроме этого лизоамидаза стимулирует репаративные процессы за счет стимулирующего влияния на клетки грануляционной ткани.
Применение в предлагаемом препарате местноанестезирующего вещества, как монокомпонента, так и в виде смеси компонентов, значительно подавляет болевой синдром при лечении ран и ожогов. При этом применение местноанестезирующего вещества, обладающего антибактериальной и антиоксидантной активностью, например хиноксикаина, усиливает лечебное действие предложенного фармакологического средства.
Для обеспечения дополнительного стимулирования процессов репарации в ране в предложенном фармакологическом средстве применено, как в виде монокомпонента, так и смеси компонентов с разным механизмом и спектром действия, вещество, стимулирующее репаративные процессы в ране.
Использование гидрофильной основы, состоящей из смеси полиэтиленосидов и проксанола, в предлагаемом фармакологическом препарате обеспечивает быструю доставку активных веществ как к микробным клеткам, так и к клеткам ткани, что повышает терапевтическую активность предложенного препарата. Кроме того, дегидратирование гидрофильной основой клеток грамположительных микроорганизмов снижает их сопротивляемость разрушающему воздействию комплекса бактерио- и протеолитических ферментов. Это также повышает терапевтическую активность предлагаемого препарата. Применение гиперосмолярной основы дополнительно улучшает микроциркуляцию в тканях раны за счет ее дегидратирующего действия, а также оказывает дополнительное противовоспалительное действие за счет абсорбции жидкости и снижения отека тканей раны.
Гипреосмолярная основа обеспечивает отток гнойного экссудата из раны и предохраняет ткани от гипергидратации. Она легко наносится на раневую поверхность, хорошо на ней удерживается, равномерно по ней распределяется, улучшая контакт мази с тканями и содержимым раны, хорошо проникает под струп, хорошо смешивается с раневым экссудатом, сохраняя при этом свою однородность, малотоксична и не оказывает раздражающего действия на ткани, не нарушает их физиологических функций. Растворение активных веществ в полиэтиленоксидной основе повышает их дисперсность и способность к более быстрому высвобождению из основы, что также увеличивает терапевтическую активность предлагаемого препарата. Данная основа является проводником активных веществ через кожный барьер, при этом такая пенетрирующая без повреждения клеток способность усиливается в условиях воспаления.
Гидрофильная основа на полиэтиленоксидах способна растворяться в секретах слизистых оболочек, полностью высвобождая лекарственные вещества, не раздражая при этом слизистую, имеет большой срок годности и высокую физиологическую индифферентность.
Реализация предлагаемого изобретения иллюстрируется следующими примерами, но не ограничивается ими.
Пример 1.
В 100 г мази содержится, г:
эмульсия перфторорганических соединений:
гидрофильные компоненты:
Пример 2. Мазь.
В 100 г мази содержится, г:
смесь №2:
Пример 3. Мазь.
В 100 г мази содержится, г:
смесь №3:
Пример 4.
В 100 г мази содержится, г:
эмульсия перфторорганических соединений:
гидрофильные компоненты:
Пример 5. Мазь.
В 100 г мази содержится, г:
смесь №5
Пример 6. Мазь.
В 100 г мази содержится, г:
смесь №6:
Пример 7. Гель.
В 100 г геля содержится, г:
смесь №7:
Пример 8. Гель.
В 100 г геля содержится, г:
смесь №8:
Пример 9. Гель.
В 100 г геля содержится, г:
смесь №9:
Пример 10. Гель.
В 100 г геля содержится, г:
смесь №10:
Пример 11. Гель.
В 100 г геля содержится, г:
эмульсии перфторорганических соединений
смесь №11:
Пример 12.
В 100 г геля содержится, г:
эмульсия перфторорганических соединений:
гидрофильные компоненты:
Пример 13. Капсулы.
Мазью из примера 2 заполнено 500 шт. желатиновых капсул №00, объемом 0,95 мл. Распадаемость полученных капсул менее 20 мин, что отвечает требованиям ГФ XI (ст.Капсулы, стр.143).
Пример 14.
В 100 г геля содержится, г:
эмульсия перфторорганических соединений:
гидрофильные компоненты
Пример 15.
В 100 г мази содержится, г:
перфторорганическая эмульсия:
гидрофильная основа:
Пример 16.
В 100 г мази содержится, г;
перфторорганическая эмульсия:
гидрофильная основа:
Пример 17.
Возможность использования предлагаемой композиции для лечения гнойно-воспалительного поражения показана на следующей модели. У первой, второй и третьей экспериментальной группы животных, в каждую из которых входило по 10 особей беспородных крыс весом 260-340 г, вызывали образование флегмоны путем введения порядка 108 микробных тел культуры золотистого стафилококка, а также 0,25 мл 25%-ного раствора сульфата магния. Флегмоны у животных развивались в течение 5-7 суток, после чего под масочным наркозом в асептических условиях гнойник вскрывали и лечение гнойно-воспалительного поражения проводили по следующей схеме.
Каждому животному из первой группы на поверхность раны после вскрытия флегмоны в течение 5 суток 1 раз в сутки наносилось около 0,3 мл 1%-ной мази с лизоамидазой (0,003 г) и анестетиком лидокаином (1%) на гидрофильной основе (полиэтиленоксиды) с перфторорганической эмульсией: перфтор[1-(4 метилциклогексил) пипередин] - 25%; стабилизатор лицетин-стандарт - 2,5%; воды очищенной - 22,5%. (по Примеру 15.)
Каждому животному из второй группы на поверхность раны после вскрытия флегмоны в течение 5 суток 1 раз в сутки наносили около 0,3 мл 1%-ной мази с лизоамидазой (0,003 г) - мазь по Примеру 15, но без целевых добавок (без лидокаина).
При этом мазь в первой и второй группе наносили на стерильную салфетку, которая фиксировалась на ране.
У каждого животного из третьей группы поверхность раны после вскрытия флегмоны в течение 5 суток 3 раза в сутки тампонировалась 0,5 мл 1%-ного раствора лизоамидазы (0,005 г) в 0,01 М натрий-фосфатном буферном растворе, которым пропитывалась стерильная салфетка. При этом рану поверх закрывали сухой стерильной салфеткой и полиэтиленовой пленкой с целью уменьшения высыхания повязки и перехода препарата за ее пределы.
Под действием композиции с лизоамидазой в первой второй и третьей группе характер отделяемого в первые 1-3 суток серозно-гнойный и серозно-геморрагический, к третьим суткам, в основном, - серозный. На третьи сутки наблюдался регресс воспалительного процесса, исчезла гипермия, отечность тканей. Грануляции появились во всех группах в основном через 3-4 дня. Эпителизация начиналась в первой группе на 4-5 день, достигая максимума на 7-8 день, во второй и третьей группе - начиналась на 6-8 день, достигая максимума на 8-12 день.
Таким образом, наличие эмульсии перфторорганических соединений в мази с лизоамидазой ускоряло эпителизацию ткани.
Кроме того, фармацевтическая композиция, использованная в первой группе, обладала выраженным анестезирующим действием, так как беспокойство, вялость, снижение аппетита в первой группе животных были значительно менее выражены, особенно в течение 3-5 дней после вскрытия флегмоны, чем во второй и третьей группе.
Пример 18.
У первой, второй и третьей экспериментальной группы животных, в каждую из которых входило по 10 особей беспородных крыс весом 260-340 г, вызывалось образование флегмоны путем введения порядка 10 микробных тел суточной культуры золотистого стафилококка, а также 0,25 мл 25%-ного раствора сульфата магния. Флегмоны у животных развивались в течение 5-7 суток, после чего под масочным наркозом в асептических условиях гнойник вскрывался, и проводилось лечение гнойно-воспалительного поражения по следующей схеме.
Каждому животному из первой группы на поверхность раны после вскрытия флегмоны в течение 8 суток 2 раз в сутки наносили около 0,3 мл 0,2%-ной мази с лизоамидазой (0,0006 г) по Примеру 16.
У каждого животного из второй группы поверхность раны после вскрытия флегмоны в течение 8 суток 4 раза в сутки тампонировали 0,2%-ным раствором лизоамидазы (0,0006 г) в 0,01 М натрий-фосфатном буферном растворе. При этом рану сверху закрывали стерильными салфетками и полиэтиленовой пленкой с целью уменьшения высыхания повязки и перехода препарата за ее пределы.
У каждого животного из третьей группы поверхность раны после вскрытия флегмоны в течение 8 суток 2 раза в сутки обрабатывалась 1%-ным раствором диоксидина. После обработки на рану наносилась около 0,3 мл мази Вишневского.
При этом мазь в первой и третьей группе наносилась на стерильную салфетку, которая фиксировалась на ране.
Под действием фармацевтических композиций с лизоамидазой в первой и второй группе через 4-5 суток у животных происходило очищение ран от гнойно-некротических масс, наблюдался регресс воспалительного процесса, исчезла гипермия, отечность тканей. Грануляции появились в первой и второй группах в основном через 6 суток. Эпителизация начиналась в первой группе на 6-7 сутки, достигая максимума на 9-10 сутки, во второй - начиналась на 8-10 сутки, достигая максимума на 12-14 сутки.
В третьей группе грануляция появлялась к 8-10 суткам от начала лечения. Воспалительные явления стихали медленно. Эпителизация достигала максимума в среднем через 20 - 26 суток.
Пример 19.
Фармацевтическая композиция в виде мазей из вышеприведенных примеров 1 и 2 была заложена на хранение при температуре +8°С в герметично закупоренных банках из темного стекла объемом 50 мл. Проба для определения бактериолитической удельной активности мази с лизоамидазой отбиралась 1 раз в месяц в течение 1 года.
Результаты изменения бактериолитической активности мазей в зависимости от времени хранения даны в таблицах 1 и 2.
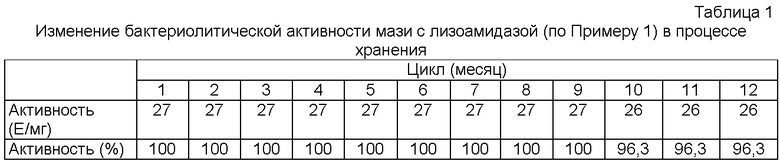
Изменение бактериолитической активности мази (по Примеру 2) в процессе хранения
Бактериолитическая активность лизоамидазы в предлагаемых композициях в условиях хранения при температуре +4÷+8°С (в герметичной посуде) снижается менее, чем на 10% в течение 1 года.
Таким образом, показано, что использование мазевой формы лизоамидазы на гидрофильной основе подтвердило ее преимущество по сравнению с жидкой формой в виде раствора, так как использовалось меньшее количество активного вещества при одном и том же терапевтическом эффекте, рана реже подвергалась обработке, обеспечивалось более удобное и более быстрое нанесение препарата на рану.
Кроме того, использование мазевой формы лизоамидазы подтвердило ее преимущество по сравнению с традиционной формой лечения гнойно-воспалительного заболевания (поскольку время лечения значительно сокращалось), а также по сравнению с жидкой формой в виде раствора лизоамидазы, так как при этом использовалось меньшее количество активного вещества при одном и том же терапевтическом эффекте, обеспечивалось более удобное и более быстрое нанесение препарата на рану.
На базе предложенного решения может быть создан ряд новых лекарственных препаратов в виде мягких лекарственных форм, таких как мазевые и формируемые, содержащих комплекс бактериолитических и протеолитических ферментов типа лизоамидаза.
Предлагаемый препарат лизирует грамположительные микроорганизмы, в том числе резистентные к антибиотикам, имеет высокую терапевтическую активность, улучшает удобство использования, снижает расход активного вещества, дает анестезирующий эффект, дополнительно стимулирует репаративные процессы в ране, улучшает микроциркуляцию.
В предлагаемом препарате в качестве компонента основы использована термоустойчивая перфторорганическая эмульсия, которая усиливает ранозаживляющий эффект предлагаемого препарата.
Проведенный поиск патентных документов не выявил идентичных и сходных технических решений.
Вышеуказанная совокупность признаков предлагаемого фармакологического препарата (состав препарата, его лекарственная форма и количественные соотношения компонентов) ранее не была известна, что говорит о новизне предложенного решения. Совокупность существенных признаков заявляемого фармакологического препарата для наружного применения на основе комплекса бактериолитических и протеолитических ферментов не следует явным образом из изученного уровня техники, имеет существенные отличия от рассмотренных аналогов. До сих пор аналогичного решения не было предложено, хотя препарат лизоамидаза известен с 1989 г. (ВФС 42-1916-89 на лизоамидазу, введенная в действие в сентябре 1989 г.). Поэтому заявитель считает, что заявляемый фармакологический препарат для местного применения на основе комплекса бактериолитических и протеолитических ферментов имеет изобретательский уровень.
Заявляемая фармакологическая композиция может быть рекомендована при лечении гнойных ран и ожогов, гнойно-воспалительных заболеваний кожи, маститов и эндометритов, проктологических заболеваний и др.
Предлагаемая фармакологическая композиция для местного применения на основе комплекса бактериолитических и протеолитических ферментов может быть использована для промышленного серийного выпуска мазеобразных мягких форм, таких как мази, кремы, гели линименты, а также для промышленного выпуска формируемых мягких лекарственных форм: капсул для ректального применения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ НАРУЖНОГО И МЕСТНОГО ПРИМЕНЕНИЯ, ОБЛАДАЮЩАЯ АНТИБАКТЕРИАЛЬНЫМ И НЕКРОЛИТИЧЕСКИМ ДЕЙСТВИЕМ, НА ОСНОВЕ ЛИЗОАМИДАЗЫ | 2007 |
|
RU2367457C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ МЕСТНОГО ПРИМЕНЕНИЯ, ОБЛАДАЮЩАЯ АНТИБАКТЕРИАЛЬНЫМ И НЕКРОЛИТИЧЕСКИМ ДЕЙСТВИЕМ | 2007 |
|
RU2367456C2 |
| ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ ДЛЯ МЕСТНОГО И НАРУЖНОГО ПРИМЕНЕНИЯ НА ОСНОВЕ НИЗКОМОЛЕКУЛЯРНОГО ИНДУКТОРА ИНТЕРФЕРОНА | 2007 |
|
RU2353354C1 |
| ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ ДЛЯ МЕСТНОГО И НАРУЖНОГО ПРИМЕНЕНИЯ НА ОСНОВЕ НИЗКОМОЛЕКУЛЯРНОГО ИНДУКТОРА ИНТЕРФЕРОНА | 2007 |
|
RU2348400C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ МЕСТНОГО И НАРУЖНОГО ПРИМЕНЕНИЯ ДЛЯ ЛЕЧЕНИЯ ТРАВМАТИЧЕСКИХ И ПОСЛЕОПЕРАЦИОННЫХ ПОВРЕЖДЕНИЙ ПЕРИФЕРИЧЕСКОЙ НЕРВНОЙ СИСТЕМЫ | 2007 |
|
RU2369387C2 |
| Фармацевтическая комбинированная композиция для местного и наружного применения на основе бактериолитического и протеолитического комплекса ферментов | 2016 |
|
RU2655808C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ МЕСТНОГО И НАРУЖНОГО ПРИМЕНЕНИЯ ДЛЯ ЛЕЧЕНИЯ ТРАВМАТИЧЕСКИХ И ПОСЛЕОПЕРАЦИОННЫХ ПОВРЕЖДЕНИЙ ПЕРИФЕРИЧЕСКОЙ НЕРВНОЙ СИСТЕМЫ НА ОСНОВЕ СТЕФАГЛАБРИНА | 2007 |
|
RU2371172C2 |
| Фармацевтическая комбинированная композиция для местного и наружного применения на основе диоксидина | 2016 |
|
RU2667974C2 |
| ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ ДЛЯ МЕСТНОГО И НАРУЖНОГО ПРИМЕНЕНИЯ НА ОСНОВЕ НИЗКОМОЛЕКУЛЯРНОГО ИНДУКТОРА ИНТЕРФЕРОНА | 2007 |
|
RU2352330C1 |
| Фармацевтическая комбинированная композиция для лечения гнойных ран на основе фторхинолонов (варианты) | 2016 |
|
RU2682171C2 |
Изобретение относится к медицине, а именно к фармацевтической композиции, применяемой при лечении гнойных ран и ожогов, гнойно-воспалительных заболеваний кожи, для ускорения заживления и улучшения условий заживления. Композиция, обладающая антибактериальным и некролитическим действием, включает активный комплекс бактериолитических и протеолитических ферментов - лизоамидазу и основу, обеспечивающую мягкую лекарственную форму композиции. Основа включает термически устойчивую эмульсию перфторорганических соединений с газотранспортными свойствами и смесь гидрофильных веществ. В качестве смеси гидрофильных веществ основа содержит вещества, выбранные из ряда: проксанол-268, полиэтиленоксиды, пропиленгликоль, димексид, гиалуроновая кислота или гиалуронат натрия, сорбит, глицерин, аэросил. Кроме того, композиция может содержать, по меньшей мере, одну целевую добавку из ряда: анестетик (хиноксикаин, тримекаин, пиромекаин, лидокаин или их смесь), стимулятор репаративных процессов (метилурацил, ацемин, этаден, кальция пантотенат, солкосерил или их смесь) или их смесь. Композиция выполнена в виде мази или геля, суппозиториев или капсул для ректального применения. Технические результаты, которые могут быть получены при использовании предлагаемого изобретения: расширение области применения, повышение терапевтической активности; улучшение удобства использования; снижение расхода активного вещества; получение анестезирующего эффекта; улучшение микроцикуляции в раневых тканях, ослабление воспалительных процессов, дополнительное стимулирование репаративных процессов. 5 з.п. ф-лы, 2 табл.
1. Фармацевтическая композиция для местного применения, обладающая антибактериальным и некролитическим действием, содержащая активный комплекс бактериолитических и протеолитических ферментов - лизоамидазу, отличающаяся тем, что она дополнительно содержит основу, обеспечивающую мягкую лекарственную форму композиции, включающую термически устойчивую эмульсию перфторорганических соединений с газотранспортными свойствами и смесь гидрофильных веществ при следующем соотношении компонентов, мас.%:
2. Фармацевтическая композиция по п.1, отличающаяся тем, что она дополнительно содержит, по крайней мере, одну из следующих целевых добавок из ряда: анестетик, стимулятор репаративных процессов или их смесь при следующем соотношении компонентов, мас.%:
3. Фармацевтическая композиция по п.2, отличающаяся тем, что в качестве анестетика она содержит вещества, выбранные из группы: хиноксикаин, тримекаин, пиромекаин, лидокаин, или их смесь.
4. Фармацевтическая композиция по п.2, отличающаяся тем, что в качестве стимулятора репаративных процессов она содержит вещества, выбранные из группы: метилурацил, ацемин, этаден, пантотенат кальция, солкосерил, или их смесь.
5. Фармацевтическая композиция по п.1, отличающаяся тем, что она выполнена в виде мягкой лекарственной формы - мази или геля или формируемой мягкой лекарственной формы - суппозиториев или капсул для ректального применения.
6. Фармацевтическая композиция по п.2, отличающаяся тем, что в качестве смеси гидрофильных веществ она содержит вещества, выбранные из ряда: проксанол-268, полиэтиленоксиды, пропиленгликоль, димексид, гиалуроновая кислота или гиалуронат натрия, сорбит, глицерин, аэросил.
| БАКТЕРИОЛИТИЧЕСКИЙ КОМПЛЕКС, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ШТАММ ДЛЯ ОСУЩЕСТВЛЕНИЯ СПОСОБА | 2000 |
|
RU2193063C2 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| КУЛАЕВ И.С., Бактериолитические ферменты микробного происхождения в биологии и медицине | |||
| Соросовский Образовательный Журнал, 1997, №3, с.23-31 | |||
| РАНОЗАЖИВЛЯЮЩЕЕ СРЕДСТВО "КОЛЛАГЕНАЗА КК" ШИРОКОГО СПЕКТРА ДЕЙСТВИЯ | 1995 |
|
RU2093166C1 |
Авторы
Даты
2009-09-20—Публикация
2007-05-23—Подача