Настоящее изобретение относится к способу переработки отходов растворов хлорида железа, в частности к способу регенерации оксида железа и хлористоводородной
кислоты.
В черной металлургии, в цинковании и т.д. широко используется промывка хлористоводородной кислотой для удаления ржавчины и увеличения адгезии (снятия окалины), с поверхности продуктов или готовых товаров. Кроме того, выщелачивание из железной руды часто выполняется при помощи хлористоводородной кислоты. Также выводные рамки полупроводников часто подвергаются травлению хлористоводородной кислотой. При этих обработках концентрацию хлористоводородной кислоты обычно поддерживают в диапазоне 12-18% масс. В ходе обработки, свободная хлористоводородная кислота превращается в соли железа и других металлов, постепенно снижая таким образом способность к отмывке и травлению. Поэтому, обычно добавляют свободную хлористоводородную кислоту, создавая таким образом большое количество низкоконцентрированных жидких отходов, содержащих хлорид железа и необязательно свободную хлористоводородную кислоту.
Эти отходы растворов хлорида железа включают хлорид железа(II), хлорид железа(III) или их комбинацию и необязательно продукты реакции с хлористоводородной кислотой других обрабатываемых металлов, подобные хлоридам цинка, никеля, меди, и т.д., и такие жидкости утилизируют как промышленные отходы. В последние годы, затраты на утилизацию или переработку таких промышленных отходов резко повысились, а сама хлористоводородная кислота является относительно дорогой. В связи с этим неэкономично таким образом утилизировать отходы растворов хлорида железа. Учитывая, что такая утилизация также создает большие экологические проблемы и проблемы, связанные с загрязнением, предложены способы регенерации хлористоводородной кислоты, оксида железа, хлорида железа(II) или их комбинаций из отходов растворов хлорид железа.
Одним таким способом является обжиг. В способе обжига отходы растворов хлорида железа, содержащие хлорид железа(II), обжигают и окисляют в обжиговой печи и разделяют на оксид железа и газ, содержащий хлористый водород, из которого газообразную хлористоводородную кислоту поглощают в абсорбере и выделяют в виде хлористоводородной кислоты, с относительно низкой концентрацией около 18% масс.
Другим способом является способ окисления хлором в жидкой фазе, в котором хлор реагирует с отходами растворов хлорида железа, содержащих хлорид железа(II), в результате чего хлорид железа(II) превращается хлорид железа(III), который или снова используют в качестве жидкости травления или выделяют в виде хлорида железа(III) для водоподготовки. Так как в этом способе хлор также реагирует с растворенным железом для получения хлорида железа(III) необходимы переработка и утилизация лишнего хлорида железа(III).
Недавно был предложен способ, в котором отходы растворов хлорида железа, содержащее хлорид железа(II), концентрируют выпариванием, жидкие отходы с более высокой концентрацией хлорида железа(II) окисляют для превращения хлорида железа(II) в хлорид железа(III), и жидкость с высокой концентрацией хлорида железа(III) гидролизуют для получения оксида железа и извлечения высококонцентрированной, по меньшей мере, 20% масс. хлористоводородной кислоты (см. JP 2006-137118 А). Этот способ подобен так называемому процессу PORI как, например, описано в US 3682592 В.
Однако, так как в вышеуказанном способе обжига нагрев требует очень большого количества топлива, затраты на регенерацию хлористоводородной кислоты неизбежно очень высоки. Кроме того, т.к. в процессе сжигания образуются газообразные отходы, следует предпринимать меры по устранению NOx, и возникают проблемы выброса в атмосферу HCl, Cl2, пыли и т.д. Кроме того, эмиссия CO2 от использования топлива также стала проблемой в последние годы.
С другой стороны, в указанном способе окисления хлором в жидкой фазе, хлорид железа(II) может быть превращен в хлорид железа(III) в реакторе. Оборудование является подходящим для небольших объемов и может быть изготовлено по низкой цене. Однако, поскольку используется опасный газообразный хлор под высоким давлением, такое оборудование нуждается в мерах по обеспечению безопасности при использовании газа высокого давления и оборудования для удаления газообразного хлора. Большая проблема заключается в том, что регенерация ограничена хлоридом железа(III) и хлористоводородная кислота извлекается не всегда.
Кроме того, способ, описанный в JP, 2006-137118 А, является эффективным способом, в котором железо извлекают из отходов хлорида железа, содержащего хлорид железа(II), в виде пригодного оксида железа и хлористоводородную кислоту извлекают с высокой концентрацией, по меньшей мере, 20% масс. Однако у получаемого оксида железа очень небольшой диаметр частиц, так что его трудно отделить от маточного раствора и он содержит хлор. Кроме того, трудно эффективно использовать производимую энергию, и поэтому этот способ не эффективен в плане баланса энергии.
Хотя стадия гидролиза процесса РОМ, описанного в US, 3682592 В, может проводиться при более высоких температурах чем процесс, описанный в JP 2006-137118 А, энергия регенерированной хлористоводородной кислоты не полностью используется повторно в процессе, и таким образом затраты энергии в процессе являются высокими.
Целью настоящего изобретения является создание способа, в котором оксид железа легко может быть выделен из раствора хлорида железа, как описано выше, с более высокой чистотой и более широким диапазоном применений, чем в обычных способах, указанный способ, является легко осуществимым с использованием очень небольшого количества энергии, и кроме того целью изобретения является создание способа, в котором регенерируют хлористоводородную кислоту с соответствующей концентрацией, которая используется для промывки, выщелачивания и травления.
Изобретатели исследовали и создали новый способ, который может достичь вышеуказанных целей. Установлено, что при концентрировании указанных отходов растворов хлорида железа до концентрированной жидкости, с содержанием хлорида железа, по меньшей мере, 30% масс. предпочтительно, по меньшей мере, 40% масс. затем превращении хлорида железа(II) (если присутствует) в хлорид железа(III) на стадии окисления и гидролизе полученной жидкости, содержащей хлорид железа(III) при температуре 155-350°C, при поддержании концентрации хлорида железа(III), по меньшей мере, 65% масс, гидролиз будет намного быстрее и более эффективен, и отделенный оксид железа содержит только незначительное количество примесей, таких как хлор и т.д., без образования оксихлорида железа (FeOCl) в качестве побочного продукта. Кроме того, было установлено, что его легче отделить от маточного раствора, из-за большего среднего диаметра частиц.
Кроме того, было установлено, что на стадии конденсации потока, содержащего хлористый водород, выделяющийся на стадии гидролиза, для регенерации хлористоводородной кислоты, также возможно вернуть энергию конденсации созданием температуры, по меньшей мере, 75°С на указанной стадии концентрирования, которую выполняют при пониженном давлении. Установлено, что это чрезвычайно выгодно, потому что тепловая энергия, используемая в общем процессе, может таким образом быть снижена на приблизительно 30-40%. Кроме того, было установлено, что, когда гидролиз проходит в указанном выше диапазоне температур, концентрация регенерированной хлористоводородной кислоты может должным образом регулироваться и составляет, по меньшей мере, около 10% масс., предпочтительно, по меньшей мере, 15% масс. и следовательно может быть выбрана любая концентрация, подходящая для повторного использования.
Эти преимущества не могут быть достигнуты в обычном способе, описанном в JP 2006-137118 А, в котором жидкость, содержащая хлорид железа(III), гидролизуют при пониженном давлении 0,01-0,02 МПа (абсолютное давление), при более низкой температуре 125-150°C.
Настоящее изобретение основано на вышеуказанных результатах и включает следующие основные пункты.
В соответствии с первым аспектом настоящего изобретения предложен способ переработки отходов растворов хлорида железа, содержащего хлорид железа(II), хлорид железа(III) или возможные их смеси и необязательно свободную хлористоводородную кислоту, причем указанный способ включает следующие стадии:
- стадию концентрирования, на которой указанные отходы растворов хлорида железа концентрируют до получения концентрированной жидкости, с общей концентрацией хлорида железа, по меньшей мере, 30% масс., предпочтительно, по меньшей мере, 40% масс.;
- при необходимости стадию окисления, на которой хлорид железа(II), содержащийся в концентрированной жидкости, полученной на указанной стадии концентрирования, окисляют до хлорида железа(III) для получения жидкости, содержащей хлорид железа(III);
- стадию гидролиза, на которой жидкость, содержащую хлорид железа(III), необязательно полученный на указанной стадии окисления, гидролизуют при температуре 155-350°C, поддерживая концентрацию хлорида железа(III) на уровне, по меньшей мере, 65% масс., для получения потока, содержащего хлористый водород, и жидкости, содержащей оксид железа(III),
- стадию разделения, на которой оксид железа(III) отделяют от указанной жидкости, содержащей оксид железа(III), полученной на указанной стадии гидролиза и
- стадию извлечения, на которой поток, содержащий хлористый водород, полученный на указанной стадии гидролиза, конденсируют для извлечения хлористоводородной кислоты с концентрацией, по меньшей мере, 10% масс., предпочтительно, по меньшей мере, 15% масс.,
характеризующийся тем, что энергию конденсации потока, содержащего хлористый водород, полученного на стадии гидролиза, прямо или косвенно используют в качестве источника нагрева на указанной стадии концентрирования, которую выполняют при пониженном давлении.
Указанный способ переработки отходов растворов железа включает две стадии, на которых происходит упаривание. На стадии гидролиза получается поток, содержащий хлористый водород. Другой стадией упаривания является указанная стадия концентрирования. Энергия, необходимая для проведения указанной стадии концентрирования обеспечивается за счет энергии конденсации потока, содержащего хлористый водород, получаемого на указанной стадии гидролиза. Таким образом, общее потребление энергии указанным способом переработки отходов растворов железа снижено на 30-40% по сравнению с общей энергией упаривания отходов растворов железа. Это очень выгодно, потому что потребление энергии в способе прокаливания при переработке хлорида железа определяется полным упариванием указанного раствора хлорида железа.
Кроме того, преимущество способа заключается в том, что воду добавляют к потоку, содержащему хлористый водород, полученному на указанной стадии гидролиза или до или на указанной стадии извлечения, в результате чего проходит конденсация, и таким образом извлечение из указанного потока хлористоводородной кислоты с любой подходящей концентрацией, по меньшей мере, 10% масс. предпочтительно, по меньшей мере, 15% масс, указанный поток, содержащий хлористый водород, является источником нагрева для обеспечения температуры, по меньшей мере, 75°C на указанной стадии концентрирования. Добавлением воды к потоку, содержащему хлористый водород, концентрацию, либо до либо во время конденсации, регулируют так, чтобы она была ниже азеотропной точки для обеспечения температуры конденсации смеси указанного потока, содержащего хлористый водород, и воды, по меньшей мере, равной 75°С. Эта минимальная температура необходима для обеспечения эффективной теплопередачи к концентрированной жидкости на указанной стадии концентрирования.
Также эффективно, если конденсированный водный раствор, полученный на указанной стадии концентрирования, используется в дополнение или вместо указанной воды, добавляемой к потоку, содержащему хлористый водород. Отходы растворов хлорида железа также могут содержать свободный хлористый водород. На указанной стадии концентрирования, на которой отходы растворов хлорида железа концентрируют упариванием, свободный хлористый водород, содержавшийся в указанном растворе хлорида железа, частично испаряется. Если конденсированный пар, полученный на стадии концентрирования, добавлен к потоку, содержащему хлористый водород, который получен на указанной стадии гидролиза, хлористый водород конденсированного пара, полученного на стадии концентрирования, также может быть извлечен. Иначе, хлористый водород в конденсированном потоке, полученном на указанной стадии концентрирования, не может быть регенерирован из-за низкой концентрации хлористого водорода.
В соответствии с настоящим изобретением также предпочтительно, если концентрированную жидкость указанной стадии концентрирования нагревают указанным потоком, содержащим хлористый водород, внешней циркуляцией на стадии концентрирования. Концентрированную жидкость на указанной стадии концентрирования частично удаляют на указанной стадии концентрирования и подают в конденсатор/теплообменник, где энергия конденсации потока, содержащего хлористый водород, получаемого на стадии гидролиза, используется для нагрева указанной концентрированной жидкости. Впоследствии концентрированную жидкость возвращают на указанную стадию концентрирования. Этот способ так называемой рекуперации тепла выгоден, потому что используется только один конденсатор/теплообменник так, что инвестиционные затраты завода минимизируются.
Предпочтительно поток, содержащий хлористый водород, конденсируют для получения хлористоводородной кислоты с концентрацией 20-35% масс. Хлористоводородная кислота с концентрацией в таком диапазоне, может использоваться в широкой области применений для промывки, травления и выщелачивания. В этом случае воду или конденсированный пар, полученный на стадии концентрирования не добавляют к потоку, содержащему хлористый водород, получаемого на указанной стадии гидролиза.
В соответствии с дополнительным осуществлением настоящего изобретения, по меньшей мере, часть жидкости, содержащей оксид железа(III), полученной на указанной стадии гидролиза, возвращают на любую предыдущую стадию. Если стадию окисления проводят в реакторе при постоянном перемешивании, небольшое количество хлоридов железа остается в растворе. Чтобы избежать накопления негидролизованного хлорида железа(II) на стадии гидролиза, часть жидкости, полученной на указанной стадии гидролиза, удаляют и подают на любую предыдущую стадию процесса так, чтобы остающийся в жидкости хлорид железа(II), полученной на стадии гидролиза, повторно был окислен на указанной стадии окисления.
Кроме того, предпочтительно, если используют отходы растворов хлорида железа, полученные при травлении стали, предварительной обработки для цинкования, выщелачивании железной руды хлористоводородной кислотой или от обработки травлением выводных рамок полупроводников.
В соответствии с настоящим изобретением отходы растворов хлорида железа могут быть эффективно переработаны с намного меньшими затратами тепла из внешних источников в форме пара и т.д., чем в обычных способах, может быть произведен оксид железа(III) существенной более высокой чистоты, содержащий только немного примесей, таких как хлор, и т.д., чем в обычных способах, и оксид железа(III) также легко отделяется от маточника за счет большего среднего диаметра частиц. Кроме того, в процессе конденсации потока, содержащего хлористый водород, выделяемого на стадии гидролиза для регенерации хлористоводородной кислоты, указанный поток, содержащий хлористый водород, может быть эффективно использован как источник тепла для создания температуры, по меньшей мере, 75°C на указанной стадии концентрирования, таким образом тепловая энергия, используемая в общем процессе, может быть снижена на приблизительно 30-40%. Кроме того, так как в настоящем изобретении концентрацию регенерированной хлористоводородной кислоты можно соответственно регулировать в диапазоне, по меньшей мере, 10% масс. предпочтительно, по меньшей мере, 15% масс. может быть выбрана любая концентрация кислоты, подходящая для повторного использования.
Отходы растворов хлорида железа настоящего изобретения могут быть получены из отходов хлористоводородной кислоты, полученных, например, при травлении стали, с использованием хлористоводородной кислоты с концентрацией 18-20% масс, в предварительной обработке цинкования, выщелачивании железной руды хлористоводородной кислотой или травлении выводных рамок полупроводников и т.д. Эти отходы растворов хлорида железа содержат хлорид железа(II) (FeCl2), который образуется по реакции хлористоводородной кислоты с железом в процессе промывки, и свободную хлористоводородную кислоту. Кроме того, в процессах промывки и травления хлористоводородная кислота реагирует не только с железом, но также и с другими металлами такими как, например, цинк, никель, медь, алюминий, марганец, хром, титан, кобальт, кальций, натрий и магний и поэтому они содержат один или более этих хлоридов металлов в качестве примеси.
Указанные отходы растворов хлорида железа перерабатывают в соответствии с настоящим изобретением. Настоящее изобретение будет объяснено на примере жидких отходов хлористоводородной кислоты, образующихся при промывке стали хлористоводородной кислотой.
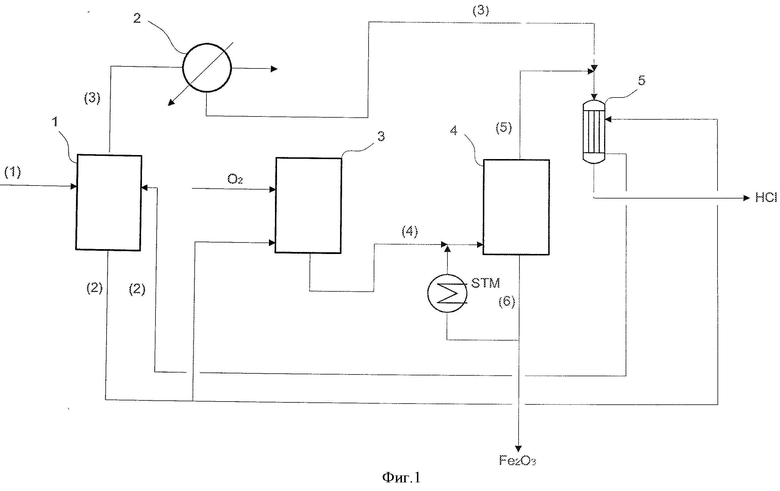
Фиг.1 представляет технологическую схему предпочтительного осуществления настоящего изобретения. Настоящее изобретение включает (А) стадию концентрирования, (В) стадию окисления, (С) стадию гидролиза и (D) стадию разделения и извлечения. Каждая стадия будет объяснена подробно далее.
(А) Стадия концентрирования
Жидкие отходы хлористоводородной кислоты (1) содержат хлорид железа(II) и небольшое количество хлористоводородной кислоты с концентрацией 0-5% масс. На стадии концентрирования воду и свободную хлористоводородную кислоту, содержащиеся в указанных жидких отходах хлористоводородной кислоты, (1) частично испаряют в концентраторе 1. Жидкие отходы хлористоводородной кислоты (1) подают в концентратор 1 и концентрируют при пониженном давлении, предпочтительно 10-50 кПа (абсолютное давление), особенно предпочтительно 20-30 кПа (абсолютное давление), предпочтительно при 65-100°C, особенно предпочтительно при 80-90°C.
Как показано на фиг.1, концентратор 1 нагревают подачей части концентрированной жидкости (2) из аппарата концентрирования 1 в конденсатор 5 и возвратом жидкости, полученной в конденсаторе 5, которая нагрета, по меньшей мере, до 75°C, в аппарат концентрирования 1. В этом случае настоящее изобретение может быть выполнено с намного более низким затратами, чем обычный способ в соответствии с JP 2006-137118 А и US 3682592.
Жидкость после испарения в концентраторе 1 конденсируют в конденсаторе 2 для получения конденсированного водного раствора, содержащего хлористоводородную кислоту, если она присутствует в жидких отходах хлористоводородной кислоты.
На указанной стадии концентрирования жидкие отходы хлористоводородной кислоты (1) концентрируют до содержания хлорида железа(II) предпочтительно, по меньшей мере, 30% масс. более предпочтительно 40-45% масс., испарением водного компонента. Если концентрация хлорида железа(II) будет ниже 30% масс., то реакция окисления будет протекать медленно, что не является предпочтительным. С другой стороны, если концентрация хлорида железа(II) более 50% масс., хлорид железа может кристаллизоваться и осаждаться.
(В) Стадия окисления
Концентрированную жидкость (2), сконцентрированную на стадии концентрирования, до концентрации хлорида железа(II), по меньшей мере, 30% масс. предпочтительно, по меньшей мере, 40% масс. подают в реактор 3 окисления, и хлорид железа(II), содержащийся в концентрированной жидкости (2), окисляют до хлорида железа(III). В связи с тем, что в настоящем изобретении концентрация хлорида железа(II) высокая, как описано выше, скорость реакции окисления также очень высока. В качестве окислителя могут быть использованы как сжатый воздух, так и кислород.
В реакции окисления хлорида железа(II) до хлорида железа(III) хлорид железа(II) реагирует с кислородом и превращается в хлорид железа(III) и оксид железа(III) в соответствии со следующей реакцией
6FeCl2+1,5O2=4FeCl3+Fe2O3
Кроме того, на этой стадии окисления, свободная хлористоводородная кислота, содержащаяся в концентрированной жидкости (2), реагирует с частью хлорида железа(II) и превращается в хлорид железа(III) в соответствии со следующей реакцией
2FeCl2+1/2О2+2HCl=2FeCl3+H2O
Поскольку реакция окисления в соответствии с вышеуказанной реакцией является экзотермической реакцией, температуру окисляемой жидкости контролируют и поддерживают равной 140-160°C при давлении выше атмосферного.
В связи с тем, что на указанной стадии окисления не протекает реакция гидролиза с хлоридом железа(II), полнота окисления хлорида железа(II) до хлорида железа(III) должна быть высокой настолько, на сколько это возможно, предпочтительно, по меньшей мере, 95%, более предпочтительно, по меньшей мере, 99%. Если полнота окисления будет низкой, то FeCl2 будет накапливаться в гидролизируемой жидкости, что не является предпочтительным. Кроме того, примеси хлора, содержащиеся в оксиде железа, получаемом на стадии гидролиза, как описано далее, возрастают, что также не является предпочтительным. Однако преимущество настоящего способа заключается в том, что хлорид железа(II) не будет накапливаться, и по меньшей мере, часть жидкости, содержащей оксид железа(III), получаемой на указанной стадии гидролиза, может быть возвращена на любую предыдущую стадию, как будет показано на фиг.2 описанной далее, и поэтому полнота окисления не должна быть абсолютно полной.
(С) Стадия гидролиза
Впоследствии, указанную жидкость после окисления (4), содержащую хлорид железа(III), подают в реактор гидролиза 4, и хлорид железа(III) гидролизует согласно следующей реакции.
FeCl3+3/2H2O=3HCl+1/2Fe2O3
На стадии гидролиза хлорид железа(III) гидролизует и образуются оксид железа(III) и большое количество хлористого водорода. В настоящем изобретении на этой стадии гидролиза концентрация хлорида железа(III) в жидкости в реакторе 4 гидролиза должна поддерживаться, по меньшей мере, равной 65% масс. предпочтительно 70-80% масс. Если концентрация хлорида железа(III) будет менее 65% масс., то концентрация извлекаемого хлористого водорода будет низкой, что не является предпочтительным. Если, с другой стороны, концентрация хлорида железа(III) будет слишком высокой, то будет образовываться оксихлорид железа (FeOCl) в качестве побочного продукта, что также не является предпочтительным.
Температура проведения гидролиза меняется в соответствии с давлением в реакторе 4 гидролиза, но предпочтительно хлорид железа(III) гидролизуют в кипящем растворе. В любом случае температура составляет предпочтительно 155-350°С, более предпочтительно 160-200°C. Если температура кипения стадии гидролиза будет менее 155°C при концентрации хлорида железа(III), по меньшей мере. 65% масс., то будет образовываться оксихлорид железа (FeOCl) в качестве побочного продукта и оксид железа(III) будет содержать хлор и т.д. в виде примесей. Если давление в реакторе 4 гидролиза является нормальным давлением (атмосферное давление), и если температура гидролиза составляет предпочтительно 160-180°С, особенно предпочтительно 165-175°C, триоксид железа(III) (Fe2O3) может быть получен с существенной более высокой чистотой со средним диаметром частиц предпочтительно 10-70 мкм, более предпочтительно 20-50 мкм, что является идеальным.
Давление в реакторе 4 гидролиза не должно всегда быть нормальным давлением (атмосферное давление). При необходимости давление может быть увеличено до около 0,3 МПа (абсолютное давление) или, чтобы защитить материал, давление может быть снижено предпочтительно до 0,05-0,1 МПа, более предпочтительно до 0,08-0,1 МПа (абсолютное давление).
Как описано выше, стадию гидролиза выполняют при нормальном давлении, при высоком давлении или при низком давлении, поддержанием температуры в указанном выше диапазоне и поддержанием концентрации хлорида железа(III) в жидкости, содержащей хлорид железа(III) в реакторе 4 гидролиза равной, по меньшей мере, 65%, и предпочтительно при поддержании раствора хлорида железа(III), который будет гидролизован в состоянии кипения, предпочтительно при удалении воды и хлористого водорода из реактора 4 гидролиза для получения потока, содержащего хлористый водород.
(4) Стадия разделения и извлечения
Гидролизом, осуществляемым при условиях, описанных выше, в реакторе 4 гидролиза получают оксид железа и поток, содержащий хлористый водород, в соответствии с настоящим изобретением. Оксид железа и хлористоводородную кислоту отделяют и извлекают в соответствии с настоящим изобретением, как описано далее. Средний диаметр частиц оксида железа, содержащего незначительное количество хлора, таков, что легко оксид железа может быть выделен. Регенерированная хлористоводородная кислота может быть доведена до соответствующей концентрации, по меньшей мере, 10% масс. предпочтительно 15% масс,, причем эффективно рекуперируется полезная тепловая энергия, что затруднительно в обычных способах.
В соответствии с настоящим изобретением, частицы оксида железа(III) отделяют от жидкости (6), например, в центрифуге, на пресс фильтре или еще более предпочтительно посредством ленточного фильтра, промывают водой, затем сушат снова в сушильной печи и получают их в форме порошка. По данным рентгенофазового анализа, регенерированный оксид железа является почти исключительно триоксидом железа (Fe2O3), с низким содержанием хлора и большим диаметром частиц. Напротив, у оксида железа, полученного обычными способами небольшой диаметр частиц, он содержит хлор, и он не очень чистый.
Кроме того, как указано выше, средний диаметр частиц (D50) оксида железа(III), регенерированного в соответствии с настоящим изобретением предпочтительно составляет 10-70 мкм, более предпочтительно 20-50 мкм и они легко могут быть отделены и извлечены из маточного раствора. Если температура гидролиза превышает 180°C, указанный выше средний диаметр получаемых частиц может быть меньше, что приводит к намного более трудному отделению от гидролизуемой жидкости (6).
В соответствии с настоящим изобретением поток (5), содержащий хлористый водород, получаемый гидролизом, конденсируют в конденсаторе 5, и выделяют хлористоводородную кислоту, которая в соответствии с настоящим изобретением может быть выделена с любой концентрацией, по меньшей мере, 10% масс. предпочтительно, по меньшей мере, 15% масс. Если концентрация выделенной хлористоводородной кислоты должна быть доведена до более низкой концентрации 15-20% масс., к потоку, содержащему хлористый водород, до его подачи в конденсатор 5 и конденсации могут быть добавлены вода или смесь вода/HCl, выходящая из конденсатора 2, снижая таким образом концентрацию хлористого водорода и обеспечивая высокую температуру конденсации хлористого водорода. В этом случае, в качестве конденсатора 5 используют газожидкостой конденсатор прямого контакта или конденсатор пленочного типа, воду используют как абсорбирующую жидкость и конденсация потока (5), содержащего хлористый водород, проходит в ходе добавления воды или до или во время указанной стадии теплообмена/извлечения. Вода, добавленная к потоку, содержащему хлористый водород, может быть чистой водой из внешнего источника или также может быть использован конденсированный водный раствор (3), полученный на указанной стадии концентрирования. Последний случай еще более эффективен, потому что конденсированный водный раствор содержит хлористый водород, и этот хлористый водород также может быть извлечен. Тепло, полученное из указанного конденсатора 5, предпочтительно имеющего температуру, по меньшей мере, 75°C, используют как тепловую среду для нагрева концентрируемой жидкости (2) на указанной стадии концентрирования. Конечно, также можно использовать поток (5), содержащий хлористый водород, для прямого нагрева концентратора 1, например, введением потока по спиралям, расположенным вокруг концентратора 1.
Альтернативно теплоноситель может быть использован для передачи тепла, получаемого конденсацией потока (5), содержащего хлористый водород, концентратору 1, или снова для нагрева циркулирующей внешней жидкости (2) или нагрева непосредственно концентратора 1.
В любом случае, настоящее изобретение может быть выполнено со значительно более низким затратами, чем обычные способы в соответствии с US 3682592 В или JP 2006-137118 А.
Поскольку в настоящем изобретении хлористоводородную кислоту извлекают с концентрацией до 20% масс., и поэтому температура конденсации потока, содержащего хлористый водород, в конденсаторе 5, высокая, можно легко получить теплоноситель с высокой температурой для процесса конденсации предпочтительно, по меньшей мере, 75°C, более предпочтительно 75°С-110°C, еще более предпочтительно 90°C-108°C. В настоящем изобретении это возможно, потому что гидролиз проводят в указанном диапазоне высокой температуры кипения 155-200°C, и поэтому соответствующее давление обеспечивает высокую температуру конденсации потока, содержащего хлористый водород, получаемого в реакторе 4 гидролиза. Поскольку в обычном способе в соответствии JP 2006-137118 А, гидролиз выполняют при более низкой температуре около 125-150°C из-за пониженного давления, температура любого получаемого теплоносителя будет только 60°C или менее, даже если способ будут выполнять таким же образом. Соответственно трудно эффективно использовать теплоноситель с такой низкой температурой.
С другой стороны, в настоящем изобретении, если концентрация регенерированной хлористоводородной кислоты составляет 20-35% масс., предпочтительно 25-35% масс., извлеченная хлористоводородная кислота подходит для применения в неизменном виде, конденсацию в конденсаторе 5 проводят без какого-либо добавления воды или водного раствора стадии концентрирования, тогда как получающаяся температура тепловой среды зависит от концентрации хлористого водорода в потоке, содержащем хлористый водород. Указанная высококонцентрированная хлористоводородная кислота с концентрацией 20-35% масс. может эффективно использоваться в различных областях.
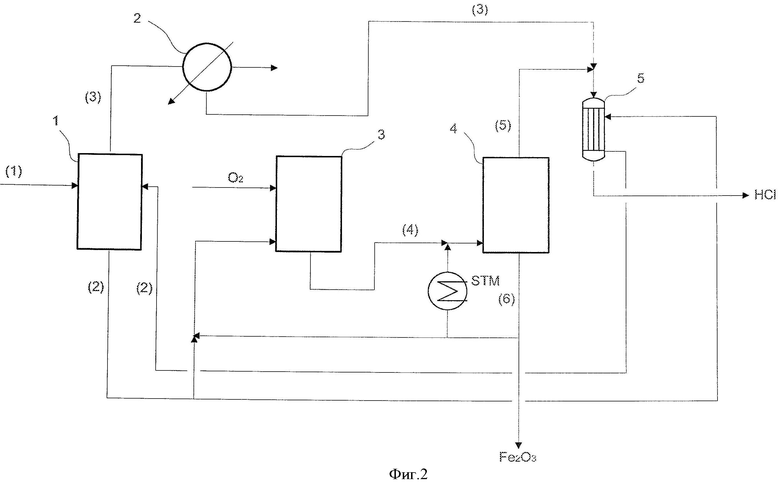
Фиг.2 представляет технологическую схему другого предпочтительного осуществления настоящего изобретения. Номера позиций на фиг.2 означают то же, что на фиг.1. В осуществлении, представленном на фиг.2 часть гидролизованной жидкости, содержащей оксид железа(III) (6), из реактора 4 гидролиза, добавляют к жидкости после окисления (4), подаваемой в реактор 4 гидролиза и возвращаемой в реактор 4 гидролиза. Остаток добавляют к концентрированной жидкости (2) получаемой на стадии концентрирования в примере, показанном на фиг.2. По меньшей мере, часть жидкости, содержащей оксид железа(III), получаемой на указанной стадии гидролиза, возвращают на любую предыдущую стадию. Альтернативно, по меньшей мере, часть жидкости, содержащей оксид железа(III), получаемой на указанной стадии гидролиза, возвращают в раствор отходов хлорида железа или на любую другую предыдущую стадию процесса.
Преимущество этого осуществления заключается в том, что, даже если полнота окисления в реакторе окисления недостаточна, это не даст никаких отрицательных эффектов, таких как снижение степени извлечения хлористоводородной кислоты из-за накопления хлорида железа(III). Далее настоящее изобретение будет описано более конкретно с использованием примеров, но, конечно, следует понимать, что изобретение не ограничено ими. Если не оговорено иное, "процент" означает "процент масс".
Пример 1
Жидкость (1), получаемую в процессе промывки стали хлористоводородной кислотой, обрабатывают согласно технологической схеме фиг.1. Состав отработанной жидкости (1) следующий:
FeCl2: 22,0%, FeCl3: 0,0%, HCl: 1,7%, H2O: 76,5%, Fe2O3: 0,0%. Температура жидкости составляет 70°C.
Отработанную жидкость (1) подают в FRP концентратор 1 со скоростью 15000 кг/час. Давление в концентраторе 1 понижают до 32 кПа использованием вакуумного насоса через конденсатор 2. Жидкость в концентраторе нагревают в конденсаторе 5 потоком, содержащим хлористый водород, выходящим из реактора 4 гидролиза во внешнюю циркуляцию.
7932 кг/час концентрированной жидкости (2) обогащенной по хлориду железа(II), содержащей FeCl2: 41,6%, FeCl3: 0,0%, HCl: 0,6%, H2O: 57,8%, Fe2O3: 0,0%, и 7067 кг/час конденсированной жидкости (3), содержащей FeCl2: 0,0%, FeCl3: 0,0%, HCl: 3,0%, H2O: 97,0%, Fe2O3: 0,0% получают из концентратора 1.
Затем указанную концентрированную жидкость (2) подают в реактор 3 окисления со скоростью 7932 кг/час и окисляют кислородом. В реакторе 3 окисления поддерживают давление 0,7 МПа и температуру 150°С и кислород подают с расходом 206 кг/час. Время нахождения в реакторе окисления составляет 4 часа. Из реактора 3 окисления получают 8139 кг/час жидкости, содержащей оксид железа(III) следующего состава:
FeCl2: 0,0%, FeCl3: 35,1%, HCl: 0,0%, H2O: 56,9%, Fe2O3: 8,1%.
Эту жидкость после окисления (4), содержащую хлорид железа(III), подают в реактор 4 гидролиза. Гидролиз выполняют нагревом жидкости, содержащей оксид железа(III) (6), удаленной из реактора 4 гидролиза через теплообменник 6 и возвращением ее в реактор 4 гидролиза, при поддержании давления 0,1 МПа, температуры 175°С и концентрации хлорида железа(III) 77% масс.
Из-за гидролиза, поток, содержащий хлористый водород (5), полученный в реакторе гидролиза 4 имеет следующий состав:
FeCl2: 0,0%, FeCl3: 0,0%, HCl: 29,0%, Н2О: 82,0%, Fe2O3: 0,0%.
Указанный пар, содержащий хлористый водород (5), подают в газожидкостной конденсатор 5 прямого контакта. В газожидкостном конденсаторе 5, конденсированную жидкость (3), полученную в указанном концентраторе 1 используют как абсорбционную жидкость, и жидкость циркуляции концентратора 1 используют нагретой. Таким образом, хлористоводородную кислоту с концентрацией 18% масс. извлекают из газожидкостного конденсатора 5 прямого контакта. С другой стороны, жидкость, содержащую оксид железа (6), разделяют на твердую и жидкую фазы с использованием центрифуги для получения порошка оксида железа(III) (Fe2O3) со средним диаметром частиц 30 мкм и содержанием 0,1% масс, хлора. Фильтрат возвращают через теплообменник 6 в реактор 4 гидролиза.
Рециркулируемую жидкость концентратора 1, полученную в указанном холодильнике 5 с температурой 95°C, охлаждают до 70°C испарением воды и хлористоводородной кислоты в концентраторе 1. Затем жидкость (2) снова возвращают в газожидкостной конденсатор 5 для нагрева потоком (5), содержащим хлористый водород, получаемым в реакторе 4 гидролиза. В общем процессе, описанном выше, то есть на стадии концентрирования, на стадии окисления и на стадии гидролиза, затраченная энергия идет только на нагрев теплообменника 6, количество тепла, подаваемого с паром, составляет 9200 кг/ч.
Пример 2. Сравнительный пример
Используют отработанную жидкость (1) того же состава, что в примере 1. Способ осуществляют аналогично примеру 1, за исключением того, что стадию гидролиза выполняют при условиях, описанных в JP 2006-137118 А, то есть при пониженном давлением 100 мм Hg при 145°C. В результате поток, содержащий хлористый водород, получаемый в реакторе 4 гидролиза, подают в конденсатор 5 и хлористоводородную кислоту с концентрацией 29% масс. извлекают конденсацией с водной средой. Поскольку температура водной среды выходящей из конденсатора 5 составляет всего 40°C, ее трудно использовать эффективно.
С другой стороны, жидкость (6), содержащую оксид железа(III), полученную в реакторе 4 гидролиза, подвергают разделению на твердую и жидкую фазы со средним диаметром полученных частиц равным 10 мкм или менее, то есть порошок оксида железа чрезвычайно трудно фильтровать. В этом случае, в общем процессе, то есть на стадии концентрирования, на стадии окисления и на стадии гидролиза, количество тепла подаваемого с паром, составляет 17960 кг/ч, на 95% больше чем в примере 1.
Пример 3
В этом примере часть жидкости, содержащей оксид железа(III), полученной на стадии гидролиза в примере 1, добавляют к концентрированной жидкости, содержащей хлорид железа(II), полученной на стадии концентрирования, и подают в вышеуказанный реактор окисления в соответствии с технологической схемой фиг.2. После концентрирования отработанной жидкости (1), полученной на стадии промывки в примере 1, при ее добавлении в качестве жидкости (2) в реактор 3 окисления, жидкость, содержащую оксид железа(III) (6) добавляют с расходом 16000 кг/ч для получения загрузки 23900 кг/ч реактора 3 окисления, получая раствор следующего состава:
FeCl2: 12,7%, FeCl3: 50,4%, HCl: 0,2%, Fe2O3: 0,5%.
В реакторе окисления поддерживают давление 0,7 МПа, температуру 150°C и добавляют 206 кг/ч кислорода, как в примере 1. На этот раз, время нахождения в реакторе окисления составляет 2 часа. 24100 кг/ч жидкости после окисления, содержащей хлорид железа(III), получают из реактора 3 окисления, следующего состава:
FeCl2: 0,7%, FeCl3: 61,3%, HCl: 0,0%, H2O: 34,9%, Fe2O3: 3,1%.
Эту жидкость после окисления, содержащую хлорид железа(III) (4), подают в реактор 4 гидролиза и получают те же результаты, что в примере 1.
На этот раз, время нахождения в реакторе окисления составляет только около половины времени примера 1, и полнота окисления составляет около 90%, но даже при том, что некоторое количество неокисленного FeCl2 остается в гидролизованной жидкости, он не накапливается в системе, и получаются стабильный результаты.
Изобретение может быть использовано в химической промышленности. Для переработки отходов растворов хлорида железа, содержащего хлорид железа(II), хлорид железа(III) или возможные смеси этих веществ и необязательно свободную хлористоводородную кислоту указанные отходы концентрируют при пониженном давлении до получения концентрированной жидкости, с общей концентрацией хлорида железа, по меньшей мере, 30 мас.%, предпочтительно, по меньшей мере, 40 мас.%. При необходимости хлорид железа(II), содержащийся в полученной концентрированной жидкости, окисляют до хлорида железа(III) для получения жидкости, содержащей хлорид железа(III). Далее эту жидкость гидролизуют при температуре 155-350°C, поддерживая концентрацию хлорида железа(III) на уровне, по меньшей мере, 65 мас.% для получения потока, содержащего хлористый водород, и жидкости, содержащей оксид железа(III). Затем проводят стадию разделения, на которой оксид железа(III) отделяют от жидкости, содержащей оксид железа(III). После чего проводят стадию извлечения, на которой поток, содержащий хлористый водород, полученный на указанной стадии гидролиза, конденсируют для извлечения хлористоводородной кислоты с концентрацией, по меньшей мере, 10 мас.% предпочтительно, по меньшей мере, 15 мас.%. При этом энергию конденсации потока, содержащего хлористый водород, полученного на стадии извлечения, прямо или косвенно используют в качестве источника нагрева на стадии концентрирования. Изобретение позволяет получить высокочистый и легко фильтрующийся оксид железа(III), регенерировать хлористоводородную кислоту и снизить потребление энергии на 30-40%. 12 з.п. ф-лы, 2 ил., 3 пр.
1. Способ переработки отходов растворов хлорида железа, содержащего хлорид железа(II), хлорид железа(III) или возможные смеси этих веществ и необязательно свободную хлористоводородную кислоту, который включает следующие стадии:
- стадию концентрирования, на которой указанные отходы растворов хлорида железа концентрируют до получения концентрированной жидкости, с общей концентрацией хлорида железа, по меньшей мере, 30 мас.%, предпочтительно, по меньшей мере, 40 мас.%;
- при необходимости стадию окисления, на которой хлорид железа(II), содержащийся в концентрированной жидкости, полученной на указанной стадии концентрирования, окисляют до хлорида железа(III) для получения жидкости, содержащей хлорид железа(III);
- стадию гидролиза, на которой жидкость, содержащую хлорид железа(III), при необходимости полученный на указанной стадии окисления, гидролизуют при температуре 155-350°C, поддерживая концентрацию хлорида железа(III) на уровне, по меньшей мере, 65 мас.% для получения потока, содержащего хлористый водород, и жидкости, содержащей оксид железа(III), и
- стадию извлечения, на которой оксид железа(III) отделяют от указанной жидкости, содержащей оксид железа(III), полученной на указанной стадии гидролиза и
- стадию извлечения, на которой поток, содержащий хлористый водород, полученный на указанной стадии гидролиза, конденсируют для извлечения хлористоводородной кислоты с концентрацией, по меньшей мере, 10 мас.% предпочтительно, по меньшей мере, 15 мас.%, характеризующийся тем, что энергию конденсации потока, содержащего хлористый водород, полученного на стадии извлечения, прямо или косвенно используют в качестве источника нагрева на указанной стадии концентрирования, которую выполняют при пониженном давлении.
2. Способ по п.1, отличающийся тем, что воду добавляют в поток, содержащий хлористый водород, полученный на указанной стадии гидролиза или до или во время указанной стадии извлечения для осуществления конденсации и извлечения таким образом из указанного потока хлористоводородной кислоты с любой регулируемой концентрацией, составляющей, по меньшей мере, 10 мас.%, предпочтительно, по меньшей мере, 15 мас.%, и указанный поток, содержащий хлористый водород, используют в качестве источника нагрева для обеспечения температуры, по меньшей мере, 75°C на указанной стадии концентрирования.
3. Способ по п.2, отличающийся тем, что конденсированный водный раствор, полученный на указанной стадии концентрирования, используют в дополнение или вместо указанной воды, добавляемой к потоку, содержащему хлористый водород.
4. Способ по любому из пп.1-3, отличающийся тем, что концентрированную жидкость указанной стадии концентрирования нагревают указанным потоком, содержащим хлористый водород, внешней циркуляцией на стадии концентрирования.
5. Способ по любому из пп.1-3, отличающийся тем, что поток, содержащий хлористый водород, конденсируют для получения хлористоводородной кислоты с концентрацией 20-35 мас.%.
6. Способ по п.4, отличающийся тем, что поток, содержащий хлористый водород, конденсируют для получения хлористоводородной кислоты с концентрацией 20-35 мас.%.
7. Способ по любому из пп.1-3 или 6, отличающийся тем, что, по меньшей мере, часть жидкости, содержащей оксид железа(III), полученной указанной стадией гидролиза, возвращают в цикл на любую предыдущую стадию.
8. Способ по п.4, отличающийся тем, что, по меньшей мере, часть жидкости, содержащей оксид железа(III), полученной указанной стадией гидролиза, возвращают в цикл на любую предыдущую стадию.
9. Способ по п.5, отличающийся тем, что, по меньшей мере, часть жидкости, содержащей оксид железа(III), полученной указанной стадией гидролиза, возвращают в цикл на любую предыдущую стадию.
10. Способ по любому из пп.1-3, 6, 8 или 9, отличающийся тем, что отходы растворов хлорида железа получаются при травлении стали, предварительной обработке для цинкования, выщелачивании железной руды хлористоводородной кислотой или травлении выводных рамок полупроводников.
11. Способ по п.4, отличающийся тем, что отходы растворов хлорида железа получаются при травлении стали, предварительной обработке для цинкования, выщелачивании железной руды хлористоводородной кислотой или травлении выводных рамок полупроводников.
12. Способ по п.5, отличающийся тем, что отходы растворов хлорида железа получаются при травлении стали, предварительной обработке для цинкования, выщелачивании железной руды хлористоводородной кислотой или травлении выводных рамок полупроводников.
13. Способ по п.7, отличающийся тем, что отходы растворов хлорида железа получаются при травлении стали, предварительной обработке для цинкования, выщелачивании железной руды хлористоводородной кислотой или травлении выводных рамок полупроводников.
| WO 8603521 A1, 19.06.1986 | |||
| Способ переработки отработанных травильных растворов | 1987 |
|
SU1490086A1 |
| US 3852430 A, 03.12.1974 | |||
| GB 1406945 A, 17.09.1975. | |||
Авторы
Даты
2013-10-20—Публикация
2009-06-18—Подача