Настоящее изобретение относится к области композиционных материалов, конкретно - к светопреобразующим материалам, применяемым медицине, в частности, в офтальмологии и предназначено для коррекции зрения путем имплантации интраокулярных линз (ИОЛ) или искусственного хрусталика глаза после удаления катаракты.
Сущность изобретения: ИОЛ, содержащая коллоидные квантовые точки (КТ), эффективно поглощает вредное для глаз ближнее ультрафилолетовое (УФ) и фиолетовое и синее излучение (250-500 нм) и преобразуют его в видимое оранжево-красное излучение, обладающее фотобиостимулирующими свойствами для структур глаза.
Изобретение посвящено реализации стратегии «полезного солнца» в область офтальмологии. Эта стратегия была сформулирована в 1995 г. в общем виде как принцип для живых систем от клеточного до организменного уровня. Она основана на применении светопреобразующих материалов, содержащих фотолюминофоры (ФЛ), в качестве защитных покрытий или экранов, которые не просто поглощают УФ излучение солнца (стратегия безопасного солнца»), а переизлучают его в биостимулирующий красно-оранжевый свет (стратегия полезного солнца «useful sun»), (Khramov R.N. et al., From "safe sun" strategy toward "useful sun" one, In: Biological Effects of light 1995: proceedings of a symposium, Atlanta, USA, October 9-11, 1995, editors, M.F. Holick and A.M. Kligman, W. de Gruyter, Berlin-New York 1996, p.l92-194.).
Расширению данной стратегии опирается, прежде всего, на результаты прямых (светопребразование) и косвенных (узкополосное лазерное и светодиодное излучение) экспериментов. Важной предпосылкой являются эксперименты, в которых показано, что красный свет светоизлучающих диодов (СИД) для сетчатки глаза является мощным универсальным биостимулятором в процессах ее восстановления как после физических (термических лазерных) повреждений (Whelan и др., 2006), так и при защите сетчатки при ее химических поражениях с метанольной интоксикации организма (Eells и др., 2003). Благотворное действие низкоинтенсивного светодиодного излучения 670 нм в дозе 4 Дж/см2 в этих случаях объясняется фотоактивацией митохондриальной цитохром-с-оксидазы. Следует отметить то, что цитохром-с-оксидаза является первичным акцептором видимого света при фотобиотимуляции было впервые обосновано Кару и Афанасьевой (ДАН, 1995, 342, №5, с.693-695) на культуре клеток. Индуцированные светом первичные реакции в митохондриях сопровождаются каскадом биохимических реакций в других органеллах клетки. Эти реакции связаны с изменением параметров клеточного гомеостаза и, в конечном счете, ответственны за трансдукцию фотосигнала от цитохром с оксидазы митохондрий до клеточного ядра, что и проявляется в виде фотобиостимуляции клеток, облученных низкоинтенсивным светом.
В ряде исследований было установлено, что искусственное излучение оранжево-красного света (600-680 нм) и ближнего инфракрасного (ИК) оказывает лечебно-профилактическое действие не только на сетчатку глаза (при этом эффективность лечения глаукомы и катаракты составляет в среднем около 80%), но и на весь организм (Панков О.П., Офтальмология. В кн. «Низкоинтесивная лазерная терапия», М., 2000 г.
В области офтальмологии стратегия «полезного солнца» в первую очередь направлена на профилактику дистрофических и стабилизацию возрастных изменений макулярной области сетчатки, отвечающей за остроту зрения и цветовосприятие. С возрастом в сетчатке накапливается пигмент липофусцин. Молскула-светоулавливатсль (акцептор), обнаруженная в липофусцине, крайне чувствительна к излучению ультрафиолетового и синего света (350-500 нм), обладающего большой энергией и оказывающего фотоповреждающее действие на ткани глаза. Источниками повреждающего света являются солнечное излучение, лампы дневного освещения, ксеноновые лампы, компьютеры и т.д. При длительном воздействии его на сетчатку молекула-светоулавливатель выделяет свободные радикалы, нарушающие процессы жизнедеятельности в клетках сетчатки, что приводит к их гибели и потере зрения. Фотоповреждение сетчатки приводит к возникновению такого заболевания как возрастная дегенерация макулы (ВДМ). Данное заболевание плохо поддается лечению и может привести к значительной потере зрения или даже к слепоте. Чаще всего возрастная дегенерация макулы возникает у людей старше 50 лет (в России их число таких больных составляет около 2,3 миллионов), в последние годы в связи с развитием ИТ возрастает нагрузка на зрение с ранних лет жизни и данное заболевание начинает проявляться и в молодом возрасте. Поэтому необходимость разработки способов лечения и профилактики ВДМ чрезвычайно актуальна.
Особенно насущной становится проблема защиты сетчатки глаза от фотоповреждения при развитии такого заболевания как катаракта. В нормальном состоянии хрусталик человека имеет усиливающийся с возрастом желтый цвет, блокирующий проникновение УФ и синего света и предохраняющий сетчатку от фотоповреждения. Современные технологии лечения катаракты (микроинвазивная факоэмульсификация) предполагают удаление хрусталика через разрез от 2,0 до 2,75 мм с имплантацией мягких или гибких ИОЛ. Однако при удалении хрусталика удаляется и естественная защита глаза от УФ и синего света, что значительно увеличивает риск развития возрастной дегенерации макулы. Современные модели ИОЛ изготавливаются из высококачественных биосовместимых материалов, что позволяет использовать линзу в течение всей жизни.
Наиболее распространены в последнее время силиконовые, гидрогелевые и акриловые мягкие линзы.
Известна композиция (Mainster, et al., Ophthalmic devices having a highly selective violet light transmissive filter and related methods, United States Patent №7,278,737,2007), включающая в себя желтый краситель, блокирующей более коротковолновое оптическое излучение от границы лежащей в диапазоне 400 до 450 нм., защищающий сетчатку глаз не только от ультрафиолетовых, но и от фиолетовых и синих лучей. Недостатком указанной композиции является, то, что поглощенный материалом ИОЛ свет переходит в тепловую энергию и не позволяет увеличить относительную спектральную плотность выходящего из ИОЛ видимого света.
Известна композиция "ИСКУССТВЕННЫЙ ХРУСТАЛИК" (RU №2045246, 6 A61F 2/16, 1991, 1991, содержащий УФ-абсорбирующую линзу, дозированно изменяющую свой спектр пропускания в видимой его части, выполненную из материала, содержащего полиметилметакрилат, УФ-абсорбирующую добавку 2-/2'-гидрокси-3-трет. бутил-5'-метилфенил/-5-хлорбензотриазол, пластификатор и краситель, отличающийся тем, что, с целью обеспечения защиты сетчатки глаза от фотоповреждающего света, возрастной нормы цветовосприятия, повышения контрастной чувствительности путем снижения светопропускания, линза имеет следующий спектр пропускания на длинах волн:
а материал линзы в качестве красителя содержит N-бутил-4-окси-3-азо/3'-нитрофенил/хинолон при следующем соотношении компонентов, мас.%:
Полиметилметакрилат - Остальное. Недостатком указанной композиции является, то, что абсорбируемый материалом свет переходит в тепловую энергию и не позволяет увеличить относительную спектральную плотность выходящего из материала линзы видимого света.
Известна композиция "ИНТРАОКУЛЯРНАЯ ЛИНЗА И СПОСОБ ЕЕ ИЗГОТОВЛЕНИЯ" (RU. №2114000, 6 B29D 11/02, 1994) из силиконового материала, отличающаяся тем, что в силиконовый материал введена добавка из порфиринов кремния в количестве не более 0,01% от общей массы материала, включающая дигидроксид пиропорфирина кремния и дигидроксид тетрабензопорфирина кремния. Недостатком указанной композиции является, то, что абсорбируемый материалом свет вдиапазоне 350-450 нм переходит в тепловую энергию и не позволяет увеличить относительную спектральную плотность выходящего из материала линзы видимого света.
Наиболее близкой к предлагаемому изобретению является
«КОМПОЗИЦИЯ ДЛЯ ИЗГОТОВЛЕНИЯ ИСКУССТВЕННОГО ХРУСТАЛИКА ГЛАЗА» (RU 2229976, B29D 11/02, 2002). Эта композиция для изготовления искусственного хрусталика глаза на основе полиорганосилоксана включает кроме того платиновый катализатор, ингибитор преждевременной вулканизации и УФ-фильтр в виде наночастиц фуллерена С60. Недостатком этого материала, содержащего фильтры в УФ- и фиолетовом дипазоне, также является то, что поглощенный материалом ИОЛ свет переходит в тепловую энергию и не позволяет увеличить относительную спектральную плотность выходящего из ИОЛ видимого света.
Задача данного изобретения - создание композиции для получения ИОЛ.
Техническим результатом предлагаемого изобретения является не только усиление защиты глаза человека от УФ- и фиолетового цвета, а создание нового качества материала ИОЛ, обуславливающего дополнительное люминесцентное излучение, которое обладает биостимулирующим воздействием.
Поставленная цель достигается тем, что композиция для изготовления интраокулярной линзы на основе полимерного компонента и оптически активной добавки содержит в качестве оптически активной добавки, по крайней мере, одно соединение коллоидных квантовых точек при следующем соотношении компонентов, мас.%:
При этом полиорганосилоксановый полимер содержит полифенилметилсилоксан с концевыми виниловыми группами с платиновым катализатором, полифенилметилсилоксан с концевыми термальными виниловыми группами.
Т.е. в предлагаемую полиорганосилоксановую композицию для изготовления ИОЛ, состоящую из полифенилметилсилоксана с концевыми термальными виниловыми группами (п=1,46) с платиновым катализатором (компонента Б), полифенилметилсилоксана с концевыми терминальными виниловыми группами, (компоненты А), добавляют наночастицы фотолюминофора, где в качестве последних используются коллоидные квантовые точки CdSe/CdS, причем компоненты композиции применяются в следующих количествах, мас.%:
полиорганосилоксан (полифенилметилсилоксан с концевыми терминальными виниловыми группами (п=1,46) с платиновым катализатором, полифенилметилсилоксана с концевыми термальными виниловыми группами (п=1,46)) - 99,95-99,999, коллоидные квантовые точки CdSe/CdS - 0,001-0.500.
Эффективное и оптимальное количество выбранных компонентов заявляемой композиции даны в нижеследующих примерах:
Пример 1.
1.1. Приготовление растворов квантовых точек для введения в полимер.
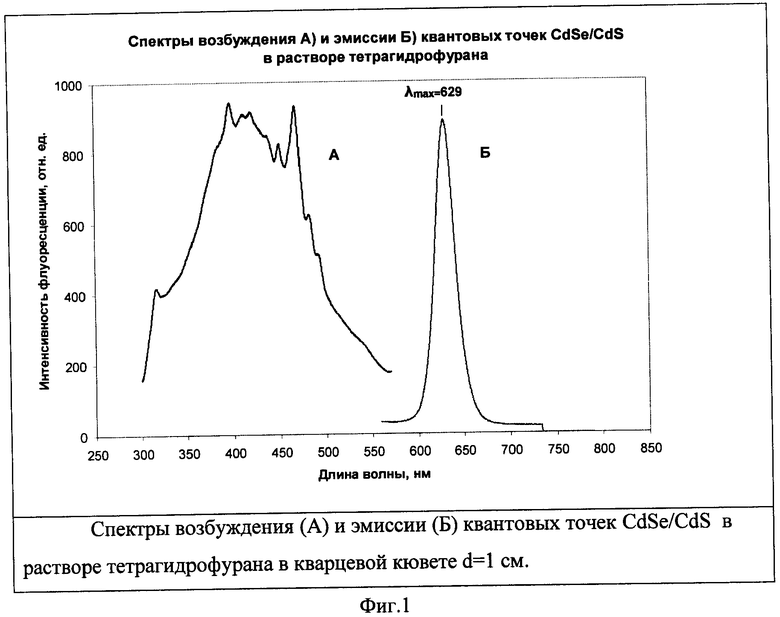
В пробирку с притертой пробкой объемом 10 мл помещается навеска 100 мг (весы точность взвешивания ±1 мг) квантовых точек CdSe/CdS (Спектр возбуждения и поглощения раствора этих КТ показан а Рис.1) и с помощью дозатора пипеточного с постоянным объемом добавляется 1 мл растворителя тетрагидрофурана (ТГФ). Полученная смесь встряхивается с помощью Вортекса (фирма ALMI) до полного растворения КТ (концентрация полученного раствора 10%). Полученная смесь имеет темно-коричневый цвет.
1.2. Приготовление композиционной смеси (А-КТ) из жидкой компоненты А146 компаунда с раствором квантовых точек.
В реакционную колбу объемом 0,5 л, снабженную мешалкой, вводят жидкую компоненту А146 полифенилметилсилоксана, 10 г. и 1 мл 10% раствора квантовых точек в тетрагидрофуране. Полученную смесь перемешивают при комнатной температуре с помощью магнитной мешалки в течение 20 минут до получения однородно окрашенной массы, концентрация квантовых точек в полученной смеси - 1%, откачивают с помощью вакуумного насоса при давлении 0,5-1 мм рт.ст. до полного прекращения газовыделения.
1.3. Очистка композиционной смеси от остатков растворителя.
Композиционную смесь переносят в круглую колбу емкостью 0,5 л из расчета 10 г полифенилметилсилоксана и 1 мл 10% раствора в тетрагидрофуране квантовых точек, колбу присоединяют к роторному испарителю и выпаривают тетрагидрофуран в течение 4 часов при температуре 70°С. Количество тетрагидрофурана в смеси не должно превышать 0,01%. Контроль содержания растворителя осуществляется методом хромато-масс спектрометрии на газовом хроматографе TRACE GC фирмы Тетю Finnigan, США.
1.4. Приготовление композиционного материала полифенилметилсилоксана с квантовыми точками CdSe/CdS для изготовления оптических элементов.
Пример 1. 100 мас.ч. компоненты Б полифенилметилсилоксана с концевыми терминальными виниловыми группами (п=1,46) с платиновым катализатором 0,2 мас.ч., 93 мас.ч. компоненты А полифенилметилсилоксана с концевыми терминальными виниловыми группами (п=1,46), 7 мас.ч. композиции А-КТ (п.1.1-1.3) тщательно перемешивают во фторопластовой чашечке (рис.21). Концентрация полученной смеси 0,0355% КТ.
Пример 2. 100 мас.ч. компоненты Б полифенилметилсилоксана с концевыми терминальными виниловыми группами (п=1,46) с платиновым катализатором 0,2 мас.ч., 80 мас.ч. компоненты А полифенилметилсилоксана с концевыми терминальными виниловыми группами (п=1,46), 20 мас.ч. композиции А-КТ (п.1.1-1.3) тщательно перемешивают во фторопластовой чашечке (рис.2). Концентрация полученной смеси 0,1% КТ.
Пример 3. 100 мас.ч. компоненты Б полифенилметилсилоксана с концевыми терминальными виниловыми группами (п=1,46) с платиновым катализатором 0,2 мас.ч., 70 мас.ч. компоненты А полифенилметилсилоксана с концевыми терминальными виниловыми группами (п=1,46), 30 мас.ч. композиции А-КТ (п.1.1-1.3) тщательно перемешивают во фторопластовой чашечке (рис.2). Концентрация полученной смеси 0,15% КТ.
Пример 4. 100 мас.ч. компоненты Б полифенилметилсилоксана с концевыми терминальными виниловыми группами (п=1,46) с платиновым катализатором 0,2 мас.ч., 60 мас.ч. компоненты А полифенилметилсилоксана с концевыми терминальными виниловыми группами (п=1,46), 40 мас.ч. композиции А-КТ (п.1.1-1.3) тщательно перемешивают во фторопластовой чашечке (рис.2). Концентрация полученной смеси 0,2% КТ.
Пример 5. 100 мас.ч. компоненты Б полифенилметилсилоксана с концевыми терминальными виниловыми группами (п=1,46) с платиновым катализатором 0,2 мас.ч., 40 мас.ч. компоненты А полифенилметилсилоксана с концевыми терминальными виниловыми группами (п=1,46), 60 мас.ч. композиции А-КТ (п.1.1-1.3) тщательно перемешивают во фторопластовой чашечке (рис.2). Концентрация полученной смеси 0,3% КТ.
Композицию, полученную в примерах 1-4, с помощью микродозатора объемом 400 мкл вводят в литьевые формы и помещают в термостат и проводят полимеризацию при Т=120-250°С в течение 5-15 минут. Литьевая форма, состоит из двух половинок. Половинки литьевой формы выполнены в виде цилиндров с полированными торцевыми поверхностями из оптически прозрачного материала - кварца. На внутренней поверхности одной половинки литьевой формы в центральной части имеются углубления, которые при соединении двух половинок формы, образуют оптическую часть хрусталика и опорные элементы, на внутренней поверхности другой половинки формы выполнен подобный рисунок, негативное изображение которого соответствует изображению только оптической части хрусталика. Диоптрийность ИОЛ меняется за счет применения форм с различным радиусом кривизны в области оптической части с шагом в одну диоптрию. Гаптическая часть (форма опорных элементов) обеспечивает максимальную прочность ИОЛ для данного типа материалов и надежную фиксацию ИОЛ в капсульном мешке хрусталика. После завершения термостатирования разъединяют две половинки формы и получают интраокулярные линзы. Материал линз имеет светло желтый цвет. Интенсивность цвета зависит от мас.ч. введенного в композицию количества КТ. Полученные оптические элементы охлаждают до комнатной температуры, затем нагревают до 120±5°С в течение 15 мин.
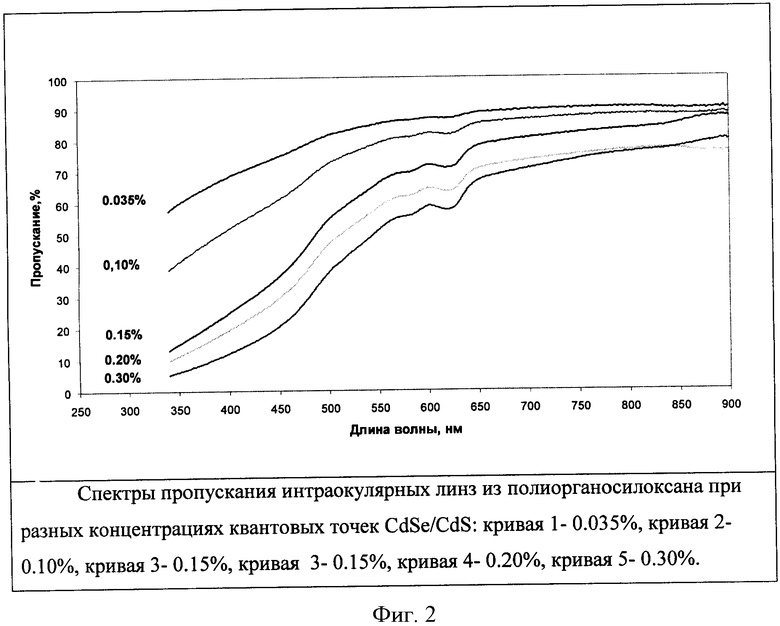
Полученные ИОЛы окрашены в желтоватый цвет и их в центральной части спектр пропускания их показан на рис 2. Спектры поглощения ИОЛ примеров 1, 2, 3, 4, 5 не изменяются после экстракции ИОЛ в аппарате Сокслета бензолом.
Дополнительным преимуществом использования для изготовления ИОЛ силиконовой композиции с добавкой КТ является возможность цитостатического действия КТ.
Из сравнения результатов по примерам 1-5 по зависимости коэффициента пропускания материала ИОЛ от длины волны света (рис.2) видно, что введение в композицию для изготовления ИОЛ КТ CdSe/CdS в количестве 0,035-0,300 мас.%. композиции увеличивает поглощение вредного для глаза УФ и фиолетового света с длиной волны менее 430 нм, с вполне приемлемым светопропусканием в диапазоне 500-750 нм.
По-видимому, наиболее оптимальной для ИОЛ будет концентрация КТ равная 0,15%. При этой концентрации поглощение света с длиной волны 430 нм составляет 35%, что сопоставимо с современными ИОЛ, содержащими желтый фильтр (United States Patent №7,278,737), при этом (рис.2) светопропускание плавно растет и превышает 70%, начиная с 580 нм и выше.
Увеличение концентрации КТ выше 0,200% приводит в к негативному ухудшению прозрачности в видимой области, хотя и с большим увеличением поглощения в УФ и фиолетово-синем диапазоне света.
Однако в случае необходимости увеличить прозрачность ИОЛ в видимой области за счет уменьшения содержания КТ целесообразно вводить какие-либо желтые фильтры, которые эффективно блокируют свет в фиолетово-синем диапазоне волн (400-450 нм). При этом благодаря тому, что спектр возбуждения КТ простирается до 600 нм, в области прозрачности желтого фильтра от 450 нм до границы диапазона возбуждения КТ 600 нм ИОЛ будет получать достаточно много свет для эмиссии. Оценки показывают, что общая интенсивность люминесценции КТ в ИОЛ с желтым фильтром снизится в 1,5-2,0 раза, по сравнению с исходной ИОЛ, содержащей КТ без желтых фильтров.
Добавление КТ не влияет на технологический процесс получения ИОЛ, не снижает физико-механических показателей получаемых ИОЛ. Можно рассчитывать и на ослабление послеоперационных осложнений за счет цитостатических свойств ИОЛ с КТ. Таким образом, предложена композиция, которая позволяет увеличить относительную спектральную плотность выходящего из ИОЛ видимого света в диапазоне (600-650 нм) за счет дополнительной люминесцентной компоненты, обладающей биостимулирующими свойствами, с уменьшенным пропусканием вредного для глаз коротковолнового света в области 250-500 нм и с увеличенной цитостатической активностью ИОЛ.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНТРАОКУЛЯРНАЯ ЛИНЗА И СПОСОБ ЕЕ ИЗГОТОВЛЕНИЯ | 1994 |
|
RU2114000C1 |
| КОМПОЗИЦИЯ ДЛЯ ИЗГОТОВЛЕНИЯ ИСКУССТВЕННОГО ХРУСТАЛИКА ГЛАЗА | 2002 |
|
RU2229976C2 |
| ИСКУССТВЕННЫЙ ХРУСТАЛИК ГЛАЗА | 2005 |
|
RU2306903C2 |
| КОМПОЗИЦИЯ ДЛЯ ИЗГОТОВЛЕНИЯ ИНТРАОКУЛЯРНОЙ ЛИНЗЫ (ИОЛ) И СПОСОБ ИЗГОТОВЛЕНИЯ ТАКОЙ ЛИНЗЫ | 2015 |
|
RU2717083C2 |
| ИНТРАОКУЛЯРНЫЕ ЛИНЗЫ С УНИКАЛЬНОЙ ОТСЕЧКОЙ СИНЕ-ФИОЛЕТОВОГО СВЕТА И УНИКАЛЬНЫМИ ХАРАКТЕРИСТИКАМИ ПРОПУСКАНИЯ СИНЕГО СВЕТА | 2007 |
|
RU2434648C2 |
| МАТЕРИАЛ ДЛЯ ИЗГОТОВЛЕНИЯ ВНЕ- И ВНУТРИГЛАЗНОГО ТРАНСПЛАНТАТА | 1997 |
|
RU2132701C1 |
| ЭЛАСТИЧНЫЙ ИСКУССТВЕННЫЙ ХРУСТАЛИК ГЛАЗА | 2004 |
|
RU2262911C1 |
| ГИДРОГЕЛЕВАЯ ИНТРАОКУЛЯРНАЯ ЛИНЗА И СПОСОБ ЕЕ ФОРМИРОВАНИЯ | 2009 |
|
RU2491034C2 |
| ЭЛАСТИЧНЫЙ ИСКУССТВЕННЫЙ ХРУСТАЛИК И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 1995 |
|
RU2074673C1 |
| ЛИГАНДЫ НА ОСНОВЕ ПОЛИДИМЕТИЛСИЛОКСАНА ДЛЯ КВАНТОВЫХ ТОЧЕК В КРЕМНИЙОРГАНИЧЕСКИХ МАТЕРИАЛАХ | 2013 |
|
RU2648084C2 |
Изобретение относится к медицине, в частности к офтальмологии, и предназначено для коррекции зрения путем имплантации интраокулярных линз (ИОЛ). Композиция для изготовления интраокулярной линзы состоит из полимерного компонента и оптически активной добавки. В качестве оптически активной добавки используется, по крайней мере, одно соединение коллоидных квантовых точек. В качестве полимерного компонента используется полиорганосилоксановый полимер. Изобретение позволяет увеличить относительную спектральную плотность выходящего из ИОЛ видимого света в диапазоне (600-650 нм) за счет дополнительной люминесцентной компоненты, обладающей биостимулирующими свойствами, с уменьшением пропускания вредного для глаз коротковолнового света в области 250-500 нм с увеличением цитостатической активности ИОЛ. 1 з.п. ф-лы, 2 ил., 5 пр.
1. Композиция для изготовления интраокулярной линзы на основе полимерного компонента и оптически активной добавки, отличающаяся тем, что она содержит в качестве оптически активной добавки, по крайней мере, одно соединение коллоидных квантовых точек при следующем соотношении компонентов, мас.%:
2. Композиция по п.1, отличающаяся тем, что полиорганосилоксановый полимер содержит полифенилметилсилоксан с концевыми виниловыми группами с платиновым катализатором, полифенилметилсилоксан с концевыми терминальными виниловыми группами.
| КОМПОЗИЦИЯ ДЛЯ ИЗГОТОВЛЕНИЯ ИСКУССТВЕННОГО ХРУСТАЛИКА ГЛАЗА | 2002 |
|
RU2229976C2 |
| ИСКУССТВЕННЫЙ ХРУСТАЛИК | 1991 |
|
RU2045246C1 |
| ИНТРАОКУЛЯРНАЯ ЛИНЗА И СПОСОБ ЕЕ ИЗГОТОВЛЕНИЯ | 1994 |
|
RU2114000C1 |
| RU 2059671 С1, 10.05.1996 | |||
| US 4206518 А, 10.06.1980. | |||
Авторы
Даты
2013-11-10—Публикация
2009-10-14—Подача