Область техники, к которой относится изобретение
Настоящая заявка испрашивает приоритет предварительной заявки на патент США 61/074,062, поданной 19 июня 2008 года, и 61/197,599, поданной 28 октября 2008 года, все содержание которых включено в настоящую заявку путем отсылки.
Настоящее изобретение относится к области биологии, более конкретно, к области терапии рака. В частности, настоящее изобретение относится к новым пептидам, которые чрезвычайно эффективны в качестве противораковых вакцин, а также к лекарственным средствам для лечения и профилактики опухолей.
Уровень техники
Было продемонстрировано, что CD8-положительные цитотоксические T-лимфоциты (ЦТЛ) узнают эпитоп-пептиды, происходящие из опухолеспецифических антигенов (ОСА), обнаруженных на молекуле главного комплекса гистосовместимости (MHC) класса I, а затем убивают опухолевые клетки. После открытия семейства антигенов меланомы (MAGE), в качестве первого примера ОСА, были обнаружены многие другие ОСА, прежде всего с помощью иммунологических методов (Boon T, Int J Cancer 1993 May 8, 54(2): 177-80; Boon T&van der Bruggen P, J Exp Med 1996 Mar 1, 183(3): 725-9). Некоторые из указанных ОСА в настоящее время подвергаются клиническому испытанию как иммунотерапевтические мишени.
Идентификация новых ОСА, способных стимулировать мощные и специфичные противоопухолевые иммунные ответы, обеспечивает последующую разработку и клиническое применение стратегий пептидного вакцинирования для различных типов рака (Harris CC, J Natl Cancer Inst 1996 Oct 16, 88(20): 1442-55; Butterfield LH et al., Cancer Res 1999 Jul 1, 59(13): 3134-42; Vissers JL et al., Cancer Res 1999 Nov 1, 59(21): 5554-9; van der Burg SH et al., J Immunol 1996 May 1, 156(9): 3308-14; Tanaka F et al., Cancer Res 1997 Oct 15, 57(20): 4465-8; Fujie T et al., Int J Cancer 1999 Jan 18, 80(2): 169-72; Kikuchi M et al., Int J Cancer 1999 May 5, 81(3): 459-66; Oiso M et al., Int J Cancer 1999 May 5, 81(3): 387-94). На сегодняшний день имеется несколько сообщений о клинических испытаниях с использованием указанных пептидов, полученных из опухолеспецифических антигенов. К сожалению, в испытаниях указанных противораковых вакцин пока наблюдалась лишь низкая частота объективных ответов (Belli F et al., J Clin Oncol 2002 Oct 15, 20(20): 4169-80; Coulie PG et al., Immunol Rev 2002 Oct, 188: 33-42; Rosenberg SA et al., Nat Med 2004 Sep, 10(9): 909-15).
ОСА, необходимые для пролиферации и выживания раковых клеток, важны как мишени для иммунотерапии, поскольку использование таких ОСА может минимизировать хорошо описанный риск ускользания раковых клеток от иммунного ответа, который относится к делеции, мутации или отрицательной модуляции ОСА как следствию терапевтически управляемого иммунного отбора.
CDCA1 - ген, ассоциируемый с циклом деления клетки 1, был идентифицирован как представитель класса генов, которые коэкспрессируются с генами клеточного цикла, такими как CDC2, циклин, топоизомераза II и другие (Walker et al., Curr Cancer Drug Targets 2001 May;1(1):73-83). CDCA1, в частности, как обнаружили, был связан с центромерами митотических клеток HeLa и поэтому считался функциональным гомологом дрожжевого Nuf2 (J Cell Biol 2001 Jan 22; 152(2):349-60).
Кроме того, посредством анализа профиля экспрессии генов с использованием полногеномного набора кДНК микрочипов, содержащего 23040 генов (Cancer Res 2006 Nov 1; 66(21):10339-48), CDCA1 также был идентифицирован как новая молекула, позитивно регулируемая при раке молочной железы (WO2005/028676), раке мочевого пузыря (WO 2006/085684), раке пищевода (WO2007/013671), мелкоклеточном раке легкого (МРЛ) (WO2007/013665) и немелкоклеточном раке легкого (НМРЛ) (WO2005/089735), содержание указанных описаний включено путем отсылки в настоящую заявку. Экспрессия CDCA1 в особенности позитивно регулируется в линиях клеток опухолей МРЛ и НМРЛ, хотя в 23 нормальных тканях, за исключением яичка, экспрессия не была обнаружена. Кроме того, отрицательная регуляция экспрессии CDCA1 посредством миРНК вызвала подавление роста клеток в линиях клеток рака легкого, экспрессирующих CDCA1 (WO 2005/089735).
Взятые в совокупности, приведенные данные указывают на то, что CDCA1 является новым, потенциально универсальным онкоантигеном. Таким образом, эпитоп-пептиды, полученные из CDCA1, могут применяться в качестве противораковых иммунотерапевтических средств для лечения широкого ряда раковых опухолей.
Сущность изобретения
Настоящее изобретение частично базируется на открытии подходящих эпитоп-пептидов, которые могут служить мишенями для иммунотерапии. С учетом того, что CDCA1 позитивно регулируются во многих типах рака, включая рак молочной железы, рак мочевого пузыря, немелкоклеточный рак легкого, мелкоклеточный рак легкого и рак пищевода, настоящее изобретение направлено на указанный продукт гена, ассоциируемого с циклом деления клетки 1 (CDCA1) (SEQ ID NO: 35, кодируемый геном GenBank NM_145697 (SEQ ID NO: 34)) для дальнейшего анализа. В частности были отобраны продукты гена CDCA1, содержащие эпитоп-пептиды, которые индуцируют ЦТЛ, специфичные к соответствующим молекулам. Мононуклеарные клетки периферической крови (МКПК), полученные от здорового донора, стимулировали с использованием HLA-A*2402 связывающих кандидатных пептидов, полученных из CDCA1. Были получены линии ЦТЛ, которые специфично узнают HLA-A24 положительные клетки-мишени, сенсибилизированные соответствующими кандидатными пептидами, и были идентифицированы HLA-A24 рестриктированные эпитоп-пептиды, которые могут вызвать мощные и специфичные иммунные ответы против CDCA1. Представленные результаты демонстрируют, что CDCA1 является сильно иммуногенным, а его эпитопы представляют собой эффективные мишени для противоопухолевой иммунотерапии.
Таким образом, цель настоящего изобретения состоит в предоставлении пептидов, обладающих способностью индуцировать ЦТЛ, а также имеющих аминокислотную последовательность, выбранную из SEQ ID NO: 3, 4, 11, 14, 22 и 23. Настоящее изобретение рассматривает модифицированные пептиды, имеющие аминокислотную последовательность SEQ ID NO: 3, 4, 11, 14, 22 или 23, в которой одна, две или более аминокислот заменены, введены, удалены или добавлены, при условии, что модифицированные пептиды сохраняют исходную способность индуцировать ЦТЛ.
При введении субъекту, настоящие пептиды презентируются на поверхности антигенпрезентирующих клеток или экзосомы и индуцируют ЦТЛ, направленные против соответствующих пептидов. Поэтому цель настоящего изобретения состоит в обеспечении антигенпрезентирующих клеток и экзосом, презентирующих любой из настоящих пептидов, а также способов индукции антигенпрезентирующих клеток.
Противоопухолевый иммунный ответ индуцируется путем введения настоящих CDCA1 полипептидов или полинуклеотида, кодирующего полипептиды, а также экзосом и антигенпрезентирующих клеток, которые презентируют CDCA1 полипептиды. Таким образом, цель настоящего изобретения состоит в предоставлении фармацевтических средств, содержащих полипептиды настоящего изобретения или кодирующих их полинуклеотиды, а также экзосомы и антигенпрезентирующие клетки, содержащие их в качестве активных компонентов. Фармацевтические средства настоящего изобретения находят конкретное применение в качестве вакцин.
Другая цель настоящего изобретения состоит в предоставлении способов лечения и/или профилактики (то есть, предотвращения возникновения) раковых новообразований (опухолей), и/или предотвращения их постоперативного рецидива, а также способов индукции ЦТЛ, способов индукции противоопухолевого иммунитета, где указанные способы включают стадию введения CDCA1 полипептидов, полинуклеотидов, кодирующих CDCA1 полипептиды, экзосом или антигенпрезентирующих клеток, презентирующих CDCA1 полипептиды, или фармацевтических средств согласно изобретению. Кроме того, ЦТЛ согласно изобретению также находят применение в качестве вакцин против рака. Примеры раковых опухолей, рассматриваемые в соответствии с настоящим изобретением, включают, помимо прочих, рак молочной железы, рак мочевого пузыря, рак пищевода, мелкоклеточный рак легкого (МРЛ) и немелкоклеточный рак легкого (НМРЛ).
В дополнение к вышесказанному, другие цели и признаки изобретения станут понятными в большей мере при прочтении последующего подробного описания в совокупности с сопровождающими фигурами и примерами. Впрочем, следует понимать, что и предыдущая сущность и последующее подробное описание изобретения относятся к примерам осуществления и не должны ограничивать изобретение или другие дополнительные варианты осуществления изобретения. В частности, хотя изобретение описано в настоящей заявке в отношении ряда конкретных вариантов осуществления, будет очевидно, что описание служит для пояснения изобретения и не должно рассматриваться как ограничение изобретения. У специалистов, квалифицированных в данной области техники, могут возникнуть идеи относительно различных модификаций и применений, не отступающих от сущности и объема изобретения, как описано в соответствии с прилагаемой формулой. Аналогичным образом, другие объекты, признаки, эффекты и преимущества настоящего изобретения будут очевидны из приведенной сущности и конкретных вариантов осуществления, описанных ниже, и будут с легкостью ясны специалистам, квалифицированным в данной области техники. Такие объекты, признаки, эффекты и преимущества будут очевидны из вышеизложенного в сочетании с сопровождающими примерами, данными, фигурами и всеми вытекающими из этого рациональными выводами, отдельно или с рассмотрением ссылок, включенных в настоящую заявку.
Краткое описание фигур
Различные аспекты и применения настоящего изобретения станут ясны квалифицированному специалисту после рассмотрения краткого описания фигур и подробного описания настоящего изобретения, а также его предпочтительных вариантов осуществления, следующих ниже.
[Фиг. 1] Фигура 1 составлена из серии фотографий (a)-(g), на которых изображены результаты IFN-гамма ELISPOT анализа ЦТЛ, индуцированных пептидами, полученными из CDCA1. ЦТЛ в лунках #8, стимулированные CDCA1-A24-10-119 (SEQ ID NO: 3) (a), #1, стимулированные CDCA1-A24-10-335 (SEQ ID NO: 4) (b), #1, стимулированные CDCA1-A24-10-48 (SEQ ID NO: 11) (c), #4, стимулированные CDCA1-A24-10-5 (SEQ ID NO: 14) (d), #2, стимулированные CDCA1-A24-9-8 (SEQ ID NO: 22) (e), и #2, стимулированные CDCA1-A24-9-56 (SEQ ID NO: 23) (f), показали мощную выработку IFN-гамма по сравнению с контролем, соответственно. Напротив, какой-либо определенной секреции IFN-гамма против сенсибилизированных пептидом клеток-мишеней в ЦТЛ, стимулированных CDCA1-A24-10-74 (SEQ ID NO: 2) (g), не обнаруживали. Клетки в лунках, обозначенных прямоугольной рамкой, использовали для получения линий ЦТЛ. На фигурах "+" указывает выработку IFN-гамма против клеток-мишеней, сенсибилизированных соответствующим пептидом, а "-" указывает выработку IFN-гамма против клеток-мишеней, не сенсибилизированных никакими пептидами.
[Фиг. 2] Фигура 2 составлена из серии линейных графиков (a)-(g), на которых представлены результаты анализа IFN-гамма ELISA на линиях ЦТЛ, полученных с CDCA1-A24-10-119 (SEQ ID NO: 3) (a), CDCA1-A24-10-335 (SEQ ID NO: 4) (b), CDCA1-A24-10-48 (SEQ ID NO: 11) (c), CDCA1-A24-10-5 (SEQ ID NO: 14) (d), CDCA1-A24-9-8 (SEQ ID NO: 22) (e) и CDCA1-A24-9-56 (SEQ ID NO: 23) (f) в вышеуказанном анализе IFN-гамма ELISA. Результаты демонстрируют, что линии ЦТЛ, полученные при стимуляции каждым пептидом, показали мощную выработку IFN-гамма по сравнению с контролем. Напротив, в линии ЦТЛ, полученной с CDCA1-A24-10-74 (SEQ ID NO: 2) (g), какой-либо определенной секреции IFN-гамма против сенсибилизированных пептидом клеток-мишеней не наблюдали. На фигурах "+" указывает выработку IFN-гамма против клеток-мишеней, сенсибилизированных соответствующим пептидом, а "-" указывает выработку IFN-гамма против клеток-мишеней, не сенсибилизированных никакими пептидами.
[Фиг. 3] Фигура 3 представляет собой линейный график, изображающий продукцию IFN-гамма ЦТЛ клона, полученного путем серийного разведения из линии ЦТЛ, стимулированной с использованием SEQ ID NO: 23. Результаты демонстрируют, что клон ЦТЛ, полученный путем стимуляции с использованием SEQ ID NO: 23, показал мощную выработку IFN-гамма по сравнению с контролем. На фигуре "+" указывает выработку IFN-гамма против клеток-мишеней, сенсибилизированных SEQ ID NO: 23, а "-" указывает выработку IFN-гамма против клеток-мишеней, не сенсибилизированных никакими пептидами.
[Фиг. 4] Фигура 4 представляет собой линейный график, на котором показана специфическая активность ЦТЛ против клеток-мишеней, которые экзогенно экспрессируют CDCA1 и HLA-A*2402. Клон ЦТЛ, полученный с использованием CDCA1-A24-9-56 (SEQ ID NO: 23), показал высокую специфическую активность ЦТЛ против клеток COS7, трансфицированных и с CDCA1, и с HLA-A*2402 (ромб). Напротив, против клеток-мишеней, экспрессирующих HLA-A*2402 (треугольник) или CDCA1 (круг), какой-либо существенной специфической активности ЦТЛ не обнаружили.
Описание вариантов осуществления
Хотя любые методы и материалы, подобные или эквивалентные описанным в настоящей заявке, могут применяться при практическом осуществлении или испытании вариантов осуществления настоящего изобретения, ниже описаны предпочтительные способы, устройства и материалы. Впрочем, прежде чем будут описаны настоящие материалы и методы, следует понимать, что настоящее изобретение не ограничивается конкретными размерами, формами, измерениями, материалами, методологиями, методиками и т.д., описанными в настоящей заявке, поскольку они могут изменяться в соответствии со стандартным экспериментированием и оптимизацией. Необходимо также понимать, что терминология, используемая в описании, служит исключительно в целях описания конкретных версий или вариантов осуществления и не предназначена для ограничения объема настоящего изобретения, ограничиваемого только в соответствии с прилагаемой формулой.
Содержание каждой публикации, описание патента или заявки на патент, упомянутых в настоящем описании, прямо включено в настоящую заявку путем отсылки в полном объеме. Впрочем, в настоящей заявке ничто не следует рассматривать как допущение того, что изобретение не имеет правомочия предшествовать подобному описанию в силу предшествующего изобретения.
I. Определения
Если не указано иное, все технические и научные термины, используемые в настоящей заявке, имеют такое же значение, под которым они обычно понимаются средним специалистом в области техники, к которой относится настоящее изобретение. Впрочем, в случае коллизии, настоящее описание, включая определения, будет иметь преимущественную силу.
Артикли единственного числа, используемые в оригинальном тексте настоящей заявки, означают "по меньшей мере, один", если прямо не указано иное.
Термины "полипептид", "пептид" и "белок" в настоящей заявке используются попеременно, и относятся к полимеру из аминокислотных остатков. Термины относятся к полимерам аминокислот, в которых один или более аминокислотных остатков являются модифицированными остатками, или неприродными остатками, такими как искусственный химический миметик соответствующей природной аминокислоты, а также к природным полимерам аминокислот.
Термин "аминокислота", используемый в настоящей заявке, относится к природным и синтетическим аминокислотам, а также аналогам аминокислот и миметикам аминокислот, которые функционируют аналогично природным аминокислотам. Природные аминокислоты представляют собой аминокислоты, кодируемые генетическим кодом, а также аминокислоты, модифицированные после трансляции в клетках (например, гидроксипролин, гамма-карбоксиглутамат и O-фосфосерин). Фраза "аналог аминокислоты" относится к соединениям, которые имеют такую же основную химическую структуру (альфа-атом углерода связан с водородом, карбокси-группой, аминогруппой и R группой), как и природная аминокислота, но содержат модифицированную группу R или модифицированные скелеты (например, гомосерин, норлейцин, метионинсульфоксид, метионинметилсульфоний). Фраза "миметик аминокислоты" относится к химическим соединениям, которые имеют различные структуры, но имеют функции, подобные функциям обычных аминокислот.
Аминокислоты могут быть обозначены в настоящей заявке своими общеизвестными трехбуквенными символами или однобуквенными символами, рекомендованными Комиссией по биохимической номенклатуре IUPAC-IUB.
Термины "ген", "полинуклеотид", "нуклеотид" и "нуклеиновая кислота" в настоящей заявке используются попеременно и, если прямо не указано иное, обозначаются своими общепринятыми однобуквенными кодами.
Если не указано иное, термин "рак" относится к раковым опухолям, сверхэкспрессирующим ген CDCA1, включая, например, рак молочной железы, рак мочевого пузыря, рак пищевода, мелкоклеточный рак легкого (МРЛ) и немелкоклеточный рак легкого (НМРЛ).
Если не указано иное, термины "цитотоксический T-лимфоцит", "цитотоксическая T-клетка" и "ЦТЛ" в настоящей заявке используются попеременно и, если прямо не указано иное, относятся к подгруппе T-лимфоцитов, которые способны узнавать "чужие" клетки (например, опухолевые клетки, клетки, инфицированные вирусом) и вызывать гибель таких клеток.
II. Пептиды
Чтобы продемонстрировать, что пептиды, полученные из CDCA1, функционируют как антиген, узнаваемый цитотоксическими T-лимфоцитами (ЦТЛ), пептиды, полученные из CDCA1 (SEQ ID NO: 35), анализировали, чтобы определить, являлись ли они эпитопами антигена, рестриктированными HLA-A24, которые являются часто встречаемыми HLA аллелями (Date Y et al., Tissue Antigens 47: 93-101, 1996; Kondo A et al., J Immunol 155: 4307-12, 1995; Kubo RT et al., J Immunol 152: 3913-24, 1994). Кандидатные HLA-A24-связывающие пептиды, полученные из CDCA1, идентифицировали на основании их аффинностей связывания с HLA-A24. После in vitro стимуляции T-клеток дендритными клетками (ДК), нагруженными указанными пептидами, успешно получали линии ЦТЛ, используя каждый из следующих пептидов:
CDCA1-A24-10-119 (SEQ ID NO: 3),
CDCA1-A24-10-335 (SEQ ID NO: 4),
CDCA1-A24-10-48 (SEQ ID NO: 11),
CDCA1-A24-10-5 (SEQ ID NO: 14),
CDCA1-A24-9-8 (SEQ ID NO: 22) и
CDCA1-A24-9-56 (SEQ ID NO: 23).
Полученные линии ЦТЛ демонстрировали мощную специфичную активность ЦТЛ против клеток-мишеней, сенсибилизированных соответствующими пептидами. Данные результаты показывают, что CDCA1 является антигеном, узнаваемым ЦТЛ, и что пептиды являются эпитоп-пептидами CDCA1, рестриктированными HLA-A24.
Поскольку ген CDCA1 сверхэкспрессируется в большинстве раковых тканей, включая, например, рак молочной железы, рак мочевого пузыря, рак пищевода, мелкоклеточный рак легкого (МРЛ) и немелкоклеточный рак легкого (НМРЛ), он представляет собой хорошую мишень для иммунотерапии. Таким образом, в настоящем изобретении предложены нонапептиды (пептиды, состоящие из девяти аминокислотных остатков) и декапептиды (пептиды, состоящие из десяти аминокислотных остатков), соответствующие ЦТЛ-узнаваемым эпитопам CDCA1. Наиболее предпочтительные примеры нонапептидов и декапептидов настоящего изобретения включают пептиды, состоящие из аминокислотной последовательности, выбранной из SEQ ID NO: 3, 4, 11, 14, 22 и 23.
В большинстве случаев, программы, доступные на данный момент в Интернете, такие как программы, описанные в Parker KC et al., J Immunol 1994 Jan 1, 152(1): 163-75, могут использоваться для вычисления аффинностей связывания между различными пептидами и антигенами HLA in silico. Аффинность связывания с антигенами HLA может быть измерена, как описано, например, в Parker KC et al., J Immunol 1994 Jan 1, 152(1): 163-75; и Kuzushima K et al., Blood 2001, 98(6): 1872-81. Способы определения аффинности связывания описаны, например, в Journal of Immunological Methods, 1995, 185: 181-190 и Protein Science, 2000, 9: 1838-1846. Таким образом, настоящее изобретение охватывает определенные пептиды CDCA1, которые связываются с антигенами HLA, идентифицированными с применением таких известных программ.
Нонапептиды и декапептиды настоящего изобретения необязательно могут быть фланкированы дополнительными аминокислотными остатками, с условием, что пептид сохраняет свою способность индуцировать ЦТЛ. Такие пептиды, обладающие способностью индуцировать ЦТЛ, в большинстве случаев имеют длину менее чем приблизительно 40 аминокислот, часто менее чем приблизительно 20 аминокислот, обычно меньше чем приблизительно 15 аминокислот. Конкретная аминокислотная последовательность (последовательности), фланкирующая пептиды, состоящие из аминокислотной последовательности, выбранной из SEQ ID NO: 3, 4, 11, 14, 22 и 23, не ограничена и может состоять из аминокислот любого типа, при условии, что это не нарушает способность исходного пептида индуцировать ЦТЛ. Таким образом, настоящее изобретение также обеспечивает пептиды, обладающие способностью индуцировать ЦТЛ и имеющие аминокислотную последовательность, выбранную из SEQ ID NO: 3, 4, 11, 14, 22 и 23.
В большинстве случаев модификация одной, двух или более аминокислот в белке не будет влиять на функцию белка, а в некоторых случаях даже будет усиливать требуемую функцию исходного белка. Фактически, модифицированные пептиды (то есть, пептиды, состоящие из аминокислотной последовательности, в которой были модифицированы два или несколько аминокислотных остатков (то есть, заменены, добавлены, удалены или вставлены) по сравнению с исходной референсной последовательностью), как известно, сохраняли биологическую активность исходного пептида (Mark et al., Proc Natl Acad Sci USA 1984, 81: 5662-6; Zoller and Smith, Nucleic Acids Res 1982, 10: 6487-500; Dalbadie-McFarland et al., Proc Natl Acad Sci USA 1982, 79: 6409-13). Таким образом, в одном варианте осуществления пептиды настоящего изобретения могут обладать способностью индуцировать ЦТЛ и иметь аминокислотную последовательность, выбранную из SEQ ID NO: 3, 4, 11, 14, 22 и 23, в которой одна, две или даже больше аминокислот добавлено, вставлено, удалено и/или заменено.
Специалистам, квалифицированным в данной области, известно, что обычно при индивидуальных дополнениях или заменах в аминокислотной последовательности, при которых изменяется одна аминокислота или малый процент аминокислот, свойства исходной боковой цепи аминокислоты сохраняются. При этом они часто упоминаются как "консервативные замены" или "консервативные модификации", при которых изменение белка приводит к получению модифицированного белка, имеющего аналогичную исходному белку функцию. Таблицы консервативных замен, в которых приводятся функционально подобные аминокислоты, известны в уровне техники. Примерами свойств боковых цепей аминокислот являются гидрофобные аминокислоты (A, I, L, M, F, P, W, Y, V), гидрофильньные аминокислоты (R, D, N, C, E, Q, G, H, K, S, T), а также боковые цепи, имеющие следующие функциональные группы или характеристики одновременно: алифатическую боковую цепь (G, A, V, L, I, P); боковую цепь, содержащую гидроксильную группу (S, T, Y); боковую цепь, содержащую атом серы (C, M); боковую цепь, содержащую карбоксильную и амидную группу (D, N, E, Q); боковую цепь, содержащую основание (R, K, H); и боковую цепь, содержащую ароматическую группу (H, F, Y, W). Кроме того, каждая из следующих восьми групп содержит аминокислоты, которые являются консервативными заменами друг для друга:
1) Аланин (A), глицин (G);
2) Аспарагиновая кислота (D), глутаминовая кислота (E);
3) Аспарагин (N), глутамин (Q);
4) Аргинин (R), лизин (K);
5) Изолейцин (I), лейцин (L), метионин (M), валин (V);
6) Фенилаланин (F), тирозин (Y), триптофан (W);
7) Серин (S), треонин (T); и
8) Цистеин (C), метионин (M) (см., например, Creighton, Proteins 1984).
Такие консервативно модифицированные пептиды также рассматриваются как пептиды настоящего изобретения. Впрочем, пептиды настоящего изобретения не ограничиваются этим и могут включать неконсервативные модификации, при условии, что модифицированный пептид сохраняет способность исходного пептида индуцировать ЦТЛ. Кроме того, модифицированные пептиды не должны исключать ЦТЛ-индуцирующие пептиды полиморфных вариантов, межвидовых гомологов и аллелей CDCA1.
В целях сохранения необходимой способности индуцировать ЦТЛ, можно модифицировать (вставить, добавить, удалить и/или заменить) небольшое количество (например, 1, 2 или несколько) или небольшой процент аминокислот. В данном случае термин "несколько" означает 5 или меньше аминокислот, например, 3 или меньше. Процент модифицируемых аминокислот составляет предпочтительно 20% или меньше, более предпочтительно 15% или меньше, еще более предпочтительно 10% или меньше или 1-5%.
Анализ гомологии предпочтительных пептидов настоящего изобретения CDCA1-A24-10-119 (SEQ ID NO: 3), CDCA1-A24-10-335 (SEQ ID NO: 4), CDCA1-A24-10-48 (SEQ ID NO: 11), CDCA1-A24-10-5 (SEQ ID NO: 14), CDCA1-A24-9-8 (SEQ ID NO: 22) и CDCA1-A24-9-56 (SEQ ID NO: 23) подтвердил, что указанные пептиды не имеют существенной гомологии с пептидами, полученным из каких-либо других известных продуктов генов человека. Таким образом, возможность указанных пептидов вызывать неизвестные или нежелательные иммунные ответы при применении для иммунотерапии значительно снижена. Соответственно, указанные пептиды, как ожидают, будут крайне полезны для стимулирования иммунитета против CDCA1 у больных раком.
В случае применения в контексте иммунотерапии, пептиды настоящего изобретения должны быть презентированы на поверхности клетки или экзосомы, предпочтительно в виде комплекса с HLA антигеном. Таким образом, предпочтительно выбрать пептиды, которые не только индуцируют ЦТЛ, но также обладают высокой аффинностью связывания к HLA антигену. С этой целью, пептиды могут быть модифицированы заменой, вставкой, делецией и/или дополнением аминокислотных остатков, с получением модифицированного пептида, обладающего повышенной аффинностью связывания. В дополнение к пептидам, которые естественно презентируются, поскольку регулярность последовательностей пептидов, презентируемых при связывании с HLA антигенами, уже известна (J Immunol 1994, 152: 3913; Immunogenetics 1995, 41: 178; J Immunol 1994, 155: 4307), модификации, основанные на такой регулярности, могут быть введены в иммуногенные пептиды изобретения. Например, может потребоваться заменить вторую аминокислоту с N-конца фенилаланином, тирозином, метионином или триптофаном, и/или аминокислоту на C-конце фенилаланином, лейцином, изолейцином, триптофаном или метионином, чтобы повысить афинность связывания HLA-A24. Таким образом, пептиды, которые имеют аминокислотную последовательность, выбранную из SEQ ID NO: 3, 4, 11, 14, 22 и 23, в которой вторая аминокислота с N-конца аминокислотной последовательности SEQ ID NO заменена фенилаланином, тирозином, метионином или триптофаном, и/или в которой аминокислота на C-конце последовательности SEQ ID NO заменена фенилаланином, лейцином, изолейцином, триптофаном или метионином, включены в настоящее изобретение. Замены могут быть введены не только в концевые аминокислоты, но и в положение потенциального ТКР-узнавания пептидов. В нескольких исследованиях было продемонстрировано, что аминокислотные замены в пептиде могут соответствовать или превосходить исходные, например, CAP1, p53(264-272), Her-2/neu(369-377) или gp100(209-217) (Zaremba et al. Cancer Res. 57, 4570-4577, 1997, T. K. Hoffmann et al. J Immunol. (2002) Feb 1;168(3):1338-47., S. O. Dionne et al. Cancer Immunol immunother. (2003) 52: 199-206, а также S. O. Dionne et al. Cancer Immunology, Immunotherapy (2004) 53, 307-314).
Настоящее изобретение также рассматривает присоединение одной-двух аминокислот к N- и/или C-концу описанных пептидов. Подобные модифицированные пептиды, обладающие высокой аффинностью связывания к HLA-антигену и сохраняющие способность индуцировать ЦТЛ, также включены в настоящее изобретение.
Впрочем, когда последовательность пептида идентична части аминокислотной последовательности эндогенного или экзогенного белка, имеющего другую функцию, могут развиваться побочные эффекты, такие как аутоиммунные нарушения и/или аллергические симптомы против определенных веществ. Таким образом, сначала предпочтительно выполнить поиск гомологии, используя доступные базы данных, чтобы избежать ситуаций, в которых последовательность пептида соответствует аминокислотной последовательности другого белка. Когда из поиска гомологии становится ясно, что не существует пептид даже с 1 или 2 аминокислотными различиями по сравнению с целевым пептидом, целевой пептид может быть модифицирован с целью повышения его аффинности связывания с HLA антигенами, и/или повышения его способности индуцировать ЦТЛ без какой-либо опасности таких побочных эффектов.
Хотя пептиды, обладающие вышеописанной высокой аффинностью связывания к HLA антигенам, как ожидают, будут очень эффективны, кандидатные пептиды, которые выбраны согласно наличию высокой аффинности связывания в качестве индикатора, далее исследуют на предмет присутствия способности индуцировать ЦТЛ. В данном случае, фраза "способность индуцировать ЦТЛ" указывает на способность пептида индуцировать цитотоксические T-лимфоциты (ЦТЛ) при презентировании на антигенпрезентирующих клетках. Кроме того, "способность индуцировать ЦТЛ " включает способность пептида индуцировать активацию ЦТЛ, пролиферацию ЦТЛ, активировать ЦТЛ лизис клеток-мишеней и увеличивать выработку IFN-гамма в ЦТЛ.
Подтверждение способности индуцировать ЦТЛ осуществляют путем индуцирования антигенпрезентирующих клеток, несущих MHC-антигены человека (например, B-лимфоциты, макрофаги и дендритные клетки (ДК)), или более конкретно, ДК, полученные из мононуклеарных лейкоцитов периферической крови человека, и, после стимуляции пептидами, смешивания с CD8-положительными клетками, с последующим измерением уровня продукции IFN-гамма, который секретируют ЦТЛ против клеток-мишеней. В качестве реакционной системы могут использоваться трансгенные животные, экспрессирующие человеческий HLA-антиген (например, описанные в BenMohamed L, Krishnan R, Longmate J, Auge C, Low L, Primus J, Diamond DJ, Hum Immunol 2000 Aug, 61(8): 764-79, связанные статьи, книги, Linkout Induction of CTL response by a minimal epitope vaccine in HLA A*0201/DR1 transgenic mice: dependence on HLA class II restricted T(H) response). Например, целевые клетки могут быть помечены радиоактивным изотопом 51Cr и т.п., при этом цитотоксическая активность может быть вычислена из радиоактивности, испускаемой клетками-мишенями. В альтернативе, способность индуцировать ЦТЛ может быть оценена путем измерения уровня IFN-гамма, вырабатываемого и секретируемого ЦТЛ в присутствии антигенпрезентирующих клеток (АПК), которые несут иммобилизованные пептиды, и визуализации зоны ингибирования на среде с использованием моноклональных антител против IFN-гамма.
В результате исследования способности пептидов индуцировать ЦТЛ, как описано выше, было обнаружено, что пептиды, которые имеют высокую аффинность связывания к HLA-антигену, не обязательно обладают высокой способностью индуцировать ЦТЛ. Однако из всех идентифицированных и проанализированных пептидов, нонапептиды или декапептиды, которые имеют аминокислотную последовательность, выбранную из SEQ ID NO: 3, 4, 11, 14, 22 и 23, как обнаружили, демонстрировали наиболее высокую способность индуцировать ЦТЛ, а также высокую аффинность связывания к HLA-антигену. Таким образом, указанные пептиды представляются как предпочтительные варианты осуществления настоящего изобретения.
В дополнение к вышеописанным модификациям, пептиды настоящего изобретения также могут быть связаны с другими веществами, при условии, что получаемый в результате связанный пептид сохраняет способность исходного пептида индуцировать ЦТЛ. Примеры подходящих веществ включают, например, пептиды, липиды, сахара и сахаридные цепи, ацетильные группы, природные и синтетические полимеры и т.д. Пептиды могут содержать модификации, такие как гликозилирование, окисление боковой цепи или фосфорилирование, и т.д., если модификации не приводят к исчезновению биологической активности исходного пептида. Данные виды модификаций могут быть выполнены с целью придания дополнительных функций (например, функции направленного действия и функции доставки) или стабилизирования полипептида.
Например, для повышения in vivo стабильности полипептида, как известно из уровня техники, вводят D-аминокислоты, миметики аминокислот или неприродные аминокислоты; данная концепция может быть также приспособлена к настоящим полипептидам. Стабильность полипептида может быть оценена множеством способов. Например, пептидазы и различные биологические среды, такие как человеческая плазма и сыворотка, могут использоваться для анализа стабильности (см., например, Verhoef et al., Eur J Drug Metab Pharmacokin 1986, 11: 291-302).
Пептиды настоящего изобретения презентируются на поверхности клетки (например, антигенпрезентирующей клетки) или экзосомы в виде комплексов в комбинации с HLA-антигенами, а затем индуцируют ЦТЛ. Поэтому пептиды, формирующие комплексы с HLA-антигенами на поверхности клетки, или экзосомы также включены в настоящее изобретение. Такие экзосомы могут быть получены, например, с использованием способов, подробно описанных в опубликованных заявках на патент Японии Kohyo. Hei 11-510507 и WO99/03499, и могут быть получены с использованием АПК, полученных от пациентов, подвергнутых лечению и/или профилактике. Экзосомы или клетки, презентирующие пептиды настоящего изобретения, могут быть введены в виде вакцин.
Тип HLA-антигенов, содержащихся в вышеуказанных комплексах, должен соответствовать типу HLA-антигенов субъекта, нуждающегося в лечении и/или профилактике. Например, у населения Японии, HLA-A24, в особенности HLA-A2402, является наиболее распространенным, и поэтому подходит для лечения пациента в Японии. Использование типа A24, который экспрессируется на высоком уровне у японцев и европейцев, благоприятно для получения эффективных результатов, при этом такие подтипы, как A2402, также находят применение. Как правило, в клинике тип HLA-антигена пациента, нуждающегося в лечении, исследуют заранее, что позволяет провести надлежащий выбор пептидов, имеющих высокие уровни аффинности связывания к специфическому антигену, или обладающих способностью индуцировать ЦТЛ посредством презентирования антигена.
При использовании типа A24 HLA-антигена для экзосомы или клетки, предпочтительно применяются пептиды, которые имеют аминокислотную последовательность, выбиранную из SEQ ID NO: 3, 4, 11, 14, 22 и 23.
В данном случае, пептиды настоящего изобретения могут быть также описаны как "CDCA1 пептид(ы)" или "CDCA1 полипептид(ы)".
III. Получение CDCA1 пептидов
Пептиды изобретения могут быть получены с использованием известных методов. Например, пептиды могут быть получены искусственно, с применением методов генной инженерии или химического синтеза. Пептид изобретения может быть синтезирован индивидуально или в виде более длинных полипептидов, состоящих из двух или более пептидов. Затем пептиды могут быть выделены, то есть, очищены так, чтобы они практически не содержали других природных белков клетки-хозяина и их фрагментов, или любых других химических веществ.
Пептид настоящего изобретения может быть получен с помощью химического синтеза, основанного на выбранной аминокислотной последовательности. Примеры стандартных методов синтеза пептидов, которые могут быть применены в синтезе, включают:
(i) Peptide Synthesis, Interscience, New York, 1966;
(ii) The Proteins, Vol. 2, Academic Press, New York, 1976;
(iii) Peptide Synthesis (на японском языке), Maruzen Co., 1975;
(iv) Basics and Experiment of Peptide Synthesis (на японском языке), Maruzen Co., 1985;
(v) Development of Pharmaceuticals (второй том) (на японском языке), Vol. 14 (peptide synthesis), Hirokawa, 1991;
(vi) WO99/67288; и
(vii) Barany G. & Merrifield R.B., Peptides Vol. 2, "Solid Phase Peptide Synthesis", Academic Press, New York, 1980, 100-118.
В альтернативе, настоящие пептиды могут быть получены с применением любого известного метода генной инженерии для получения пептидов (например, Morrison J, J Bacteriology 1977, 132: 349-51; Clark-Curtiss & Curtiss, Methods in Enzymology (eds. Wu et al.) 1983, 101: 347-62). Например, сначала получают подходящий вектор, несущий полинуклеотид, кодирующий целевой пептид в экспрессируемой форме (например, расположенный после регулиряторной последовательности, соответствующей последовательности промотора), которым затем трансформируют подходящую клетку-хозяина. Затем клетку-хозяина культивируют, получая требуемый пептид. Пептид может также быть получен in vitro с применением системы трансляции in vitro.
IV. Полинуклеотиды
Настоящее изобретение также обеспечивает полинуклеотид, который кодирует любой из вышеупомянутых пептидов настоящего изобретения. Они включают полинуклеотиды, полученные из природного гена CDCA1 (GenBank NM_145697 (SEQ ID NO: 34)), а также полинуклеотиды, которые имеют консервативно модифицированную нуклеотидную последовательность. В данном случае, фраза "консервативно модифицированная нуклеотидная последовательность" относится к последовательностям, которые кодируют идентичные или по существу идентичные аминокислотные последовательности. Вследствие вырожденности генетического кода, большое количество функционально идентичных нуклеиновых кислот кодирует тот или иной белок. Например, кодоны GCA, GCC, GCG и GCU кодируют аминокислоту аланин. Таким образом, в каждом положении, в котором аланин определен кодоном, кодон может быть изменен на любой из соответствующих описанных кодонов, без изменения кодируемого полипептида. Подобные изменения нуклеиновой кислоты являются "молчащими вариациями" и являются одним из вариантов консервативно модифицированных вариаций. Каждая последовательность нуклеиновой кислоты в настоящей заявке, которая кодирует пептид, также описывает каждую возможную молчащую вариацию нуклеиновой кислоты. Среднему специалисту в данной области известно, что каждый кодон в нуклеиновой кислоте (кроме AUG, который обычно является единственным кодоном для метионина, и TGG, который обычно является единственным кодоном для триптофана) может быть модифицирован с получением функционально идентичной молекулы. Таким образом, каждая молчая вариация нуклеиновой кислоты, которая кодирует пептид, в неявном виде описана в каждой раскрытой последовательности.
Полинуклеотид настоящего изобретения может состоять из ДНК, РНК и их производных. ДНК предпочтительно состоит из таких оснований, как A, T, C и G, при этом в РНК T заменено U.
Полинуклеотид настоящего изобретения может кодировать несколько пептидов настоящего изобретения, с или без промежуточной аминокислотной последовательности между ними. Например, промежуточная аминокислотная последовательность может обеспечивать сайт расщепления (например, последовательность узнавания фермента) полинуклеотида или транслированных пептидов. Кроме того, полинуклеотид может включать любые дополнительные последовательности в кодирующей последовательности, которая кодирует пептид настоящего изобретения. Например, полинуклеотид может являться рекомбинантным полинуклеотидом, который включает регуляторные последовательности, требуемые для экспрессии пептида, или может являться вектором экспрессии (плазмидой) с маркерными генами и т.п. В большинстве случаев, подобные рекомбинантные полинуклеотиды могут быть получены посредством манипуляции полинуклеотидами с помощью стандартных генноинженерных методов, например, с использованием полимераз и эндонуклеаз.
Для получения полинуклеотидов настоящего изобретения могут использоваться и рекомбинантные, и химические методы синтеза. Например, полинуклеотид может быть получен путем встраивания в соответствующий вектор, который может экспрессироваться при трансфекции в компетентную клетку. В альтернативе, полинуклеотид может быть амплифицирован с использованием методов ПЦР или экспрессии в подходящих организмах-хозяевах (см., например, Sambrook et al., Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory, New York, 1989). В альтернативе, полинуклеотид может быть синтезирован с использованием методов твердофазного синтеза, как описано в Beaucage SL&Iyer RP, Tetrahedron 1992, 48: 2223-311; Matthes et al., EMBO J 1984, 3: 801-5.
V. Антигенпрезентирующие клетки (АПК)
Настоящее изобретение также обеспечивает антигенпрезентирующие клетки (АПК), которые презентируют комплексы, сформированные между HLA-антигенами и пептидами настоящего изобретения, на своей поверхности. АПК, которые получены путем контакта с пептидами настоящего изобретения или путем введения нуклеотидов, кодирующих пептиды настоящего изобретения в экспрессируемой форме, могут быть получены от пациентов, которые подвергнуты лечению и/или профилактике, и могут быть введены в виде вакцин или в комбинации с другими лекарственными средствами, включая пептиды настоящего изобретения, экзосомы или цитотоксические T-клетки.
АПК не ограничиваются конкретным видом клеток и включают дендритные клетки (ДК), клетки Лангерганса, макрофаги, B-клетки и активированные T-клетки, которые, как известно, презентируют на своей поверхности белковые антигены, узнаваемые лимфоцитами. Поскольку ДК являются типичными АПК, обладающими наиболее сильной индуцирующей активностью в отношении ЦТЛ из всех АПК, ДК находят применение в качестве АПК настоящего изобретения.
Например, АПК может быть получена посредством индукции ДК из моноцитов периферической крови с их последующим контактом (стимуляцией) с пептидами настоящего изобретения in vitro, ex vivo или in vivo. При введении пептидов настоящего изобретения субъектам, АПК, которые презентируют пептиды настоящего изобретения, индуцируются в организме субъекта. Фраза "индукция АПК" включает контакт (стимуляцию) клеток с пептидами настоящего изобретения, или нуклеотидами, кодирующими пептиды настоящего изобретения, с презентированием комплексов, формируемых между HLA-антигенами и пептидами настоящего изобретения, на поверхности клетки. В альтернативе, после введения пептидов настоящего изобретения в АПК для того, чтобы АПК презентировали пептиды, АПК могут быть введены субъекту в виде вакцины. Например, введение ex vivo может включать стадии:
a) получения АПК от первого субъекта,
b) контакт АПК из стадии a) с пептидом, и
c) введение нагруженных пептидом АПК второму субъекту.
Первый субъект и второй субъект могут являться одним и тем же лицом или могут являться различными лицами. В альтернативе, согласно настоящему изобретению, предложено применение пептидов настоящего изобретения для приготовления фармацевтической композиции, индуцирующей антигенпрезентирующие клетки. Кроме того, настоящее изобретение предоставляет способ приготовления фармацевтической композиции, индуцирующей антигенпрезентирующие клетки, включающий стадию смешивания или включения пептида настоящего изобретения в лекарственную форму с фармацевтически приемлемым носителем. Кроме того, настоящее изобретение также предоставляет пептиды настоящего изобретения для индукции антигенпрезентирующих клеток. АПК, полученные в стадии (b), могут быть введены субъекту в виде вакцины.
Согласно аспекту настоящего изобретения, АПК имеют высокий уровень способности индуцировать ЦТЛ. В термине "высокий уровень способности индуцировать ЦТЛ", высокий уровень относится к соответствующему уровню в отсутствие контакта АПК с пептидом или при контакте с пептидами, которые не могут индуцировать ЦТЛ. Такие АПК, обладающие высоким уровнем способности индуцировать ЦТЛ, могут быть получены методом, который включает стадию переноса генов, содержащих полинуклеотиды, которые кодируют пептиды настоящего изобретения, в АПК in vitro. Введенные гены могут находиться в форме ДНК или РНК. Примеры методов введения включают, без особых ограничений, различные методы, традиционно применяемые в данной области, такие как липофекция, электропорация, при этом также может применяться метод с использованием фосфата кальция. Более конкретно, это может быть выполнено, как описано в Cancer Res 1996, 56: 5672-7; J Immunol 1998, 161: 5607-13; J Exp Med 1996, 184: 465-72; опубликованный японский перевод Международной публикации 2000-509281. При переносе гена в АПК, ген подвергается транскрипции, трансляции и т.п. в клетке, после чего полученный белок процессируется MHC класса I или класса II и проходит через путь презентирования с последующим презентированием пептидов.
VI. Цитотоксические T-клетки
Цитотоксическая T-клетка, индуцированная против любого из пептидов настоящего изобретения, усиливает иммунный ответ, направленный против раковых клеток in vivo, и, таким образом, может применяться в качестве вакцины, по существу аналогично пептидам. Таким образом, настоящее изобретение также обеспечивает выделенные цитотоксические T-клетки, которые специфично индуцированы или активированы любым из настоящих пептидов.
Такие цитотоксические T-клетки могут быть получены путем: (1) введения пептидов настоящего изобретения субъекту, сбора цитотоксических T-клеток у субъекта, или (2) контакта (стимулирования) полученных от субъекта АПК и CD8-положительных клеток или мононуклеарных лейкоцитов периферической крови in vitro с пептидами настоящего изобретения с последующим выделением цитотоксических T-клеток.
Цитотоксические T-клетки, которые были индуцированы посредством стимуляции с использованием АПК, которые презентируют пептиды настоящего изобретения, могут быть получены от пациентов, которые подвергаются лечению и/или профилактике, и могут быть введены самостоятельно или в комбинации с другими лекарственными средствами, включая пептиды настоящего изобретения или экзосомы, в целях регулирующих эффектов. Полученные цитотоксические T-клетки специфично действуют против клеток-мишеней, презентирующих пептиды настоящего изобретения, например, те же пептиды, которые применяются для индукции. Клетки-мишени могут являться клетками, которые эндогенно экспрессируют CDCA1, или клетками, которые трансфицированы геном CDCA1, причем клетки, которые презентируют пептид настоящего изобретения на поверхности вследствие стимуляции пептидом, могут также служить мишенями для атаки активированных ЦТЛ.
VII. T-клеточный рецептор (ТКР)
Настоящее изобретение также обеспечивает композицию, содержащую нуклеиновые кислоты, кодирующие полипептиды, которые способны формировать субъединицу T-клеточного рецептора (ТКР), а также способы ее применения. Субъединицы ТКР обладают способностью формировать ТКР, которые придают T-клеткам специфичность против опухолевых клеток, презентирующих CDCA1. С помощью методов, известных из уровня техники (WO2007/032255 и Morgan et al., J Immunol, 171, 3288 (2003)), могут быть идентифицированы нуклеиновые кислоты альфа- и бета-цепей как субъединицы ТКР на ЦТЛ, индуцированных одним или более пептидами настоящего изобретения. Производные ТКР могут связывать клетки-мишени, презентирующие пептид CDCA1 с высокой авидностью, и необязательно опосредовать эффективный цитолиз клеток-мишеней, презентирующих пептид CDCA1 in vivo и in vitro.
Нуклеиновые кислоты, кодирующие субъединицы ТКР, могут быть включены в подходящие векторы, например ретровирусные векторы. Указанные векторы известны в уровне техники. Нуклеиновые кислоты или векторы, содержащие их, предпочтительно могут быть перенесены в T-клетку, например, T-клетку, полученную от пациента. Предпочтительно, изобретение обеспечивает готовую к применению композицию, позволяющую произвести быструю модификацию собственных T-клеток пациента (или T-клеток другого млекопитающего) с быстрым и легким получением модифицированных T-клеток, обладающих превосходными киллерными свойствами в отношении раковых клеток.
Кроме того, настоящее изобретение обеспечивает ЦТЛ, которые получены путем трансдукции с использованием нуклеиновых кислот, кодирующих полипептиды субъединиц ТКР, которые связываются с пептидом CDCA1, например, SEQ ID NO: 3, 4, 11, 14, 22 и 23 в отношении HLA-A24. Трансфектированные ЦТЛ способны мигрировать к раковым клеткам in vivo, причем из них могут быть получены культуры с использованием известных методов культивирования in vitro (например, Kawakami et al., J Immunol., 142, 3452-3461 (1989)). T-клетки изобретения могут применяться для получения композиции, которая может применяться при лечении или профилактике рака у пациента, испытывающего потребность в лечении или защите (WO2006/031221).
Предотвращение и профилактика включают любую деятельность, которая уменьшает процент смертности или тяжесть заболевания. Предотвращение и профилактика могут происходить "на первичных, вторичных и третичных уровнях профилактики". Тогда как первичное предотвращение и профилактика позволяют избежать развития болезни, вторичный и третичный уровни предотвращения и профилактики охватывают действия, нацеленные на предотвращение и профилактику прогрессии заболевания и появления симптомов, а также уменьшение отрицательного воздействия уже развившейся болезни, восстанавливая функцию и уменьшая связанные с болезнью осложнения. В альтернативе, предотвращение и профилактика включают широкий диапазон профилактических терапий, нацеленных на облегчение тяжести конкретного нарушения, например, уменьшение пролиферации и метастазирования опухолей, уменьшение ангиогенеза.
Лечение и/или профилактика рака, и/или профилактика постоперативного рецидива рака включают любую из следующих стадий, таких как хирургическое удаление раковых клеток, ингибирование роста злокачественных клеток, инволюцию или регрессию опухоли, индукцию ремиссии и подавление возникновения рака, регрессию опухоли и уменьшение или ингибирование метастазирования. Фактически лечение и/или профилактика рака уменьшают смертность и улучшают прогноз у лиц, имеющих рак, уменьшают уровни опухолевых маркеров в крови и облегчают детектируемые симптомы, сопровождающие рак. Например, уменьшение или улучшение симптомов фактически составляют лечение и/или профилактику, включающие 10%, 20%, 30% или больший процент уменьшения, или стабилизацию болезни.
VIII. Фармацевтические средства или композиции
Поскольку экспрессия CDCA1 специфически повышена при нескольких типах рака, включая рак молочной железы, рак мочевого пузыря, рак пищевода, мелкоклеточный рак легкого (МРЛ) и немелкоклеточный рак легкого (НМРЛ), по сравнению с нормальной тканью (Cancer Res 2006 Nov 1; 66(21):10339-48, WO2005/028676, WO2005/089735, WO2006/085684, WO2007/013665, WO2007/013671), пептиды настоящего изобретения или полинуклеотиды, кодирующие пептиды, могут применяться для лечения и/или профилактики рака или опухоли, и/или для предотвращения их постоперативного рецидива. Таким образом, настоящее изобретение предоставляет фармацевтическое средство или композицию для лечения и/или для профилактики рака или опухоли, и/или предотвращения их постоперативного рецидива, которые включают один или более пептидов настоящего изобретения, или полинуклеотидов, кодирующих пептиды, в качестве активного компонента. В альтернативе, настоящие пептиды могут экспрессироваться на поверхности любой из вышеуказанных экзосом или клеток, таких как АПК, для применения их в качестве фармацевтических средств или композиций. Кроме того, вышеуказанные цитотоксические T-клетки, которые направлены на любой из пептидов изобретения, также могут применяться в качестве активного компонента настоящих фармацевтических средств или композиций.
В другом варианте осуществления настоящее изобретение также обеспечивает применение активного компонента, выбранного из следующего:
(a) пептид настоящего изобретения,
(b) нуклеиновая кислота, кодирующая такой пептид, раскрытый в настоящей заявке, в экспрессируемой форме,
(c) АПК или экзосома, презентирующие пептид настоящего изобретения на своей поверхности, и
(d) цитотоксическая T-клетка настоящего изобретения,
в производстве фармацевтической композиции или средства для лечения рака или опухоли.
В альтернативе настоящее изобретение дополнительно обеспечивает активный компонент, выбранный из следующего:
(a) пептид настоящего изобретения,
(b) нуклеиновая кислота, кодирующая такой пептид, раскрытый в настоящей заявке, в экспрессируемой форме,
(c) АПК или экзосома, презентирующие пептид настоящего изобретения на своей поверхности, и
(d) цитотоксические T-клетки настоящего изобретения,
для применения в лечении рака или опухоли.
В альтернативе настоящее изобретение дополнительно обеспечивает способ приготовления фармацевтической композиции или средства для лечения рака или опухоли, включающий стадию включения в лекарственную форму фармацевтически или физиологически приемлемого носителя с активным компонентом, выбранным из следующего:
(a) пептид настоящего изобретения,
(b) нуклеиновая кислота, кодирующая такой пептид, раскрытый в настоящей заявке, в экспрессируемой форме,
(c) АПК или экзосома, презентирующие пептид настоящего изобретения на своей поверхности, и
(d) цитотоксические T-клетки настоящего изобретения,
в качестве активных компонентов.
В другом варианте осуществления настоящее изобретение также обеспечивает способ приготовления фармацевтической композиции или средства для лечения рака или опухоли, включающий стадию введения активного компонента в лекарственную форму с фармацевтически или физиологически приемлемым носителем, где активный компонент выбран из следующего:
(a) пептид настоящего изобретения,
(b) нуклеиновая кислота, кодирующая такой пептид, раскрытый в настоящей заявке, в экспрессируемой форме,
(c) АПК или экзосома, презентирующие пептид настоящего изобретения на своей поверхности, и
(d) цитотоксические T-клетки настоящего изобретения.
В альтернативе, фармацевтическая композиция или средство настоящего изобретения могут применяться для профилактики рака или опухоли и/или предотвращения их постоперативного рецидива.
Настоящие фармацевтические средства или композиции находят применение в качестве вакцины. В рамках настоящего изобретения фраза "вакцина" (также называемая иммуногенной композицией) относится к веществу, которое обладает функцией вызывать противоопухолевый иммунитет при введении животным.
Фармацевтические средства или композиции настоящего изобретения могут применяться для лечения и/или профилактики раковых новообразований или опухолей, и/или предотвращения их постоперативного рецидива у субъектов или пациентов, включая человека и любое другое млекопитающее, включающее, помимо прочих, мышь, крысу, морскую свинку, кролика, кошку, собаку, овцу, козу, свинью, рогатый скот, лошадь, обезьяну, бабуина и шимпанзе, в особенности коммерчески важное животное или одомашненное животное.
Согласно настоящему изобретению, полипептиды, которые имеют аминокислотную последовательность, выбранную из SEQ ID NO: 3, 4, 11, 14, 22 и 23, как обнаружили, являлись HLA-A24-рестриктированными эпитоп-пептидами или кандидатами, которые могут вызывать мощный и специфичный иммунный ответ. Таким образом, настоящие фармацевтические средства, которые включают любой из указанных полипептидов, имеющих аминокислотные последовательности SEQ ID NO: 3, 4, 11, 14, 22 и 23, в особенности подходят для введения субъектам, имеющим HLA-антиген HLA-A24. То же относится к фармацевтическим средствам или композициям, которые содержат полинуклеотиды, кодирующие любой из указанных полипептидов.
Раковые новообразования или опухоли, подвергаемые лечению с применением фармацевтических средств или композиций настоящего изобретения, не ограничены, и включают все виды раковых новообразований или опухолей, ассоциированных с CDCA1, включая например, рак молочной железы, рак мочевого пузыря, рак пищевода, мелкоклеточный рак легкого (МРЛ) и немелкоклеточный рак легкого (НМРЛ).
Настоящие фармацевтические средства или композиции, в дополнение к вышеуказанным активным компонентам, могут содержать другие пептиды, которые обладают способностью индуцировать ЦТЛ против злокачественных клеток, другие полинуклеотиды, кодирующие другие пептиды, другие клетки, которые презентируют другие пептиды, и т.п. В настоящей заявке неограничивающими примерами других пептидов, которые обладают способностью индуцировать ЦТЛ против злокачественных клеток, являются опухолеспецифические антигены (например, идентифицированные ОСА).
При необходимости фармацевтические средства или композиции настоящего изобретения в качестве активного компонента необязательно могут включать другие терапевтические вещества, при условии, что вещество не ингибирует противоопухолевый эффект активного компонента, например, любого из настоящих пептидов. Например, лекарственные формы могут включать противовоспалительные средства, аналгезирующие средства, химиотерапевтические средства и т.п. В дополнение к содержанию других терапевтических веществ в лекарственном препарате непосредственно, лекарственные препараты настоящего изобретения также могут быть введены последовательно или одновременно с одним или несколькими другими фармакологическими средствами. Количества лекарственного препарата и фармакологического средства зависят, например, от того, какое фармакологическое средство (средства) применяется, от заболевания, которое лечат, а также от схемы и путей введения.
Необходимо понимать, что в дополнение к компонентам, конкретно указанным в настоящей заявке, фармацевтические средства или композиции настоящего изобретения могут включать другие средства, стандартные в данной области техники, которые относятся к типу рассматриваемой лекарственной формы.
В одном варианте осуществления настоящего изобретения настоящие фармацевтические средства или композиции могут быть включены в изделия и наборы, содержащие материалы, применяемые для лечения патологических состояний заболевания, которое подвергают лечению, например, рака. Изделие может включать контейнер любого из настоящих фармацевтических средств или композиций с этикеткой. Подходящие контейнеры включают флаконы, ампулы и пробирки. Контейнеры могут быть изготовлены из различных материалов, таких как стекло или пластмасса. Этикетка на контейнере должна указывать, что агент применяется для лечения или профилактики одного или более состояний заболевания. Этикетка может также указывать способы введения и т.д.
В дополнение к контейнеру, описанному выше, набор, включающий фармацевтическое средство или композицию настоящего изобретения, необязательно может дополнительно включать второй контейнер, содержащий фармацевтически приемлемый разбавитель. Он может дополнительно включать другие материалы, необходимые с коммерческой и пользовательской позиции, включая другие буфера, разбавители, фильтры, иглы, шприцы и вкладыши с инструкциями по применению.
Фармацевтические средства или композиции при необходимости могут быть предоставлены в упаковке или дозирующем устройстве, которое может содержать одну или более единичных лекарственных форм, содержащих активный компонент. Упаковка может, например, включать металлическую фольгу или пластиковую пленку, такую как блистерная упаковка. Упаковка или дозирующее устройство могут сопровождаться инструкциями по введению.
(1) Фармацевтические средства или композиции, содержащие пептиды в качестве активного компонента
Пептид настоящего изобретения может быть введен непосредственно в форме фармацевтического средства или композиции, или, при необходимости, включен в лекарственную форму с помощью стандартных фармацевтических методов. В последнем случае, в дополнение к пептидам настоящего изобретения, носители, наполнители и т.п., которые обычно применяются при изготовлении лекарственных средств, при необходимости могут быть включены без определенных ограничений. Примерами таких носителей является стерилизованная вода, физиологический раствор, фосфатный буфер, культуральная жидкость и т.п. Кроме того, фармацевтические средства или композиции могут содержать, при необходимости, стабилизаторы, суспензии, консерванты, поверхностно-активные вещества и т.п. Фармацевтические средства или композиции настоящего изобретения могут применяться против рака.
Пептиды настоящего изобретения могут быть приготовлены в комбинации, состоящей из двух или более пептидов настоящего изобретения, для индукции ЦТЛ in vivo. Комбинация пептидов может иметь форму смеси или конъюгата, полученного с применением стандартных методов. Например, пептиды могут быть химически связаны или экспрессированы в виде единой слитой полипептидной последовательности. Пептиды в комбинации могут быть одинаковыми или различными.
При введении пептидов настоящего изобретения, пептиды презентируются в высокой плотности HLA-антигенами на АПК, при этом индуцируются ЦТЛ, которые специфично реагируют с комплексом, сформированным между презентированным пептидом и HLA-антигеном. В альтернативе, АПК, которые презентируют любой из пептидов настоящего изобретения на своей поверхности и могут быть получены путем стимуляции АПК (например, ДК), полученных от субъекта, пептидами настоящего изобретения, могут быть введены субъекту, в результате чего ЦТЛ индуцируются у субъекта, и может быть повышена агрессивность в отношении раковых клеток.
Фармацевтические средства или композиции для лечения и/или профилактики рака или опухоли, включающие пептид настоящего изобретения в качестве активного компонента, могут также включить адъювант, который, как известно, эффективно активирует клеточный иммунитет. В альтернативе, фармацевтические средства или композиции могут быть введены с другими активными компонентами или могут быть введены в виде лекарственной формы в гранулах. Адъювант относится к соединению, который усиливает иммунный ответ против белка при одновременном (или последовательном) введении с белком, обладающим иммунологической активностью. Адъюванты, рассматриваемые в настоящей заявке, описаны в литературе (Cl Clin Microbiol Rev 1994, 7: 277-89). Примеры подходящих адъювантов включают, помимо прочего, фосфат алюминия, гидроксид алюминия, алюмокалиевые квасцы, холерный токсин, токсин сальмонеллы и т.п.
Кроме того, могут применяться липосомные лекарственные формы, гранулированные лекарственные формы, в которых пептид пришит к гранулам диаметром несколько микронов, а также лекарственные формы, в которых пептид связан с липидом.
В некоторых вариантах осуществления фармацевтические средства или композиции настоящего изобретения могут дополнительно включать компонент, который примирует ЦТЛ. Липиды были идентифицированы как агенты, способные примировать ЦТЛ in vivo против вирусных антигенов. Например, остатки пальмитиновой кислоты могут быть присоединены к эпсилон- и альфа-аминогруппам остатка лизина, а затем связаны с пептидом настоящего изобретения. Затем липидированный пептид можно вводить либо непосредственно в мицелле, либо в виде частицы, включенной в липосому, или эмульгированной в адъюванте. В качестве другого примера липида, примирующего ответы ЦТЛ, липопротеины E. coli, такие как трипальмитоил-S-глицерилцистеинлизерилсерин (P3CSS), могут применяться для примирования ЦТЛ, когда они ковалентно связаны с соответствующим пептидом (см., например, Deres et al., Nature 1989, 342: 561-4).
Способ введения может быть пероральным, внутрикожным, подкожным, внутривенной инъекцией и т.п., а также системным введением или местным введением вблизи целевых участков. Введение может быть выполнено с помощью разового введения или усилено многократным введением. Доза пептидов настоящего изобретения может регулироваться в зависимости от болезни, подвергаемой лечению, возраста пациента, веса, способа введения и т.д., и обычно составляет 0,001-1000 мг, например, 0,001-1000 мг, например, 0,1-10 мг, и может вводиться один раз в течение нескольких дней или нескольких месяцев. Специалист, квалифицированный в данной области, может правильно подобрать подходящую дозу.
(2) Фармацевтические средства или композиции, содержащие полинуклеотиды в качестве активного компонента
Фармацевтические средства или композиции настоящего изобретения могут также содержать нуклеиновые кислоты, кодирующие пептиды, раскрытые в настоящей заявке, в экспрессируемой форме. В настоящей заявке фраза "в экспрессируемой форме" означает, что полинуклеотид при введении в клетку экспрессируется in vivo в вид полипептида, который вызывает противоопухолевый иммунитет. В приведенном примере осуществления последовательность нуклеиновой кислоты целевого полинуклеотида включает регуляторные элементы, необходимые для экспрессии полинуклеотида. Полинуклеотид(ы) может быть сконструирован таким образом, чтобы обеспечивалось стабильное интегрирование в геном целевой клетки (см., например, Thomas KR & Capecchi MR, Cell 1987, 51: 503-12, относительно описания кассетных векторов для гомологичной рекомбинации). См., например, Wolff et al., Science 1990, 247: 1465-8; патенты США 5580859; 5589466; 5804566; 5739118; 5736524; 5679647; и WO 98/04720. Примеры технологий доставки на основе ДНК включают "голую ДНК", облегченную (бупивакаин, полимеры, пептид-опосредованную) доставку, комплексы катионных липидов, а также доставку на частицах ("генная пушка") или доставку, опосредованную давлением (см., например, патент США 5922687).
Пептиды настоящего изобретения могут также экспрессироваться с помощью вирусных или бактериальных векторов. Примеры векторов экспрессии включают аттенуированные вирусы, такие как вирусы осповакцины или оспы-дифтерита птиц. Данный подход включает применение вируса осповакцины, например, в качестве вектора, для экспрессии нуклеотидных последовательностей, которые кодируют пептид. При введении в хозяйский организм, рекомбинантный вирус осповакцины экспрессирует иммуногенный пептид, и, таким образом, вызывает иммунный ответ. Векторы на основе вируса осповакцины и способы, применяемые в методиках иммунизации, описаны, например, в патенте США 4722848. Другим вектором является БЦЖ (бацилла Кальметта-Герена). Векторы на основе БЦЖ описаны в Stover et al., Nature 1991, 351: 456-60. Большое разнообразие других векторов, применяемых для терапевтического введения или иммунизации, например, адено и аденоассоциируемые вирусные векторы, ретровирусные векторы, векторы Salmonella typhi, векторы на основе детоксифицированного сибиреязвенного токсина и т.п., также известны. См., например, Shata et al., Mol Med Today 2000, 6: 66-71; Shedlock et al., J Leukoc Biol 2000, 68: 793-806; Hipp et al., In Vivo 2000, 14: 571-85.
Доставка полинуклеотида в организм субъекта может быть прямой, когда субъект непосредственно подвергается контакту с вектором, несущим полинуклеотид, либо опосредованной, когда сначала целевым полинуклеотидом in vitro трансформируют клетки, а затем клетки переносят в организм субъекта. Два вышеописанных подхода известны как генная терапия in vivo и ex vivo, соответственно.
По поводу общих обзоров относительно методов генной терапии см. Goldspiel et al., Clinical Pharmacy 1993, 12: 488-505; Wu and Wu, Biotherapy 1991, 3: 87-95; Tolstoshev, Ann Rev Pharmacol Toxicol 1993, 33: 573-96; Mulligan, Science 1993, 260: 926-32; Morgan & Anderson, Ann Rev Biochem 1993, 62: 191-217; Trends in Biotechnology 1993, 11(5): 155-215. Стандартные методы, известные в области генной инженерии, которые могут также применяться в настоящем изобретении, описаны в руководствах Ausubel et al., Current Protocols in Molecular Biology, John Wiley & Sons, NY, 1993; а также Krieger, Gene Transfer and Expression, A Laboratory Manual, Stockton Press, NY, 1990.
Способ введения может быть пероральным, внутрикожным, подкожным, внутривенной инъекцией и т.п., также находит применение системное введение или местное введение вблизи целевых участков. Введение может быть выполнено с помощью разового введения или усилено многократным введением. Доза полинуклеотида в подходящем носителе или клетках, трансформированных полинуклеотидом, кодирующим пептиды настоящего изобретения, может регулироваться в зависимости от болезни, подвергаемой лечению, возраста пациента, веса, способа введения и т.д., и обычно составляет 0,001-1000 мг, например, 0,001-1000 мг, например, 0,1-10 мг, и может вводиться один раз в течение нескольких дней или нескольких месяцев. Специалист, квалифицированный в данной области, может правильно подобрать подходящую дозу.
IX. Способы с применением пептидов, экзосом, АПК и ЦТЛ
Пептиды настоящего изобретения и полинуклеотиды, кодирующие такие пептиды, могут применяться для индукции АПК и ЦТЛ. Экзосомы и АПК настоящего изобретения также могут применяться для индукции ЦТЛ. Пептиды, полинуклеотиды, экзосомы и АПК могут применяться в комбинации с любыми другими соединениями при условии, что данные соединения не ингибируют их способность индуцировать ЦТЛ. Таким образом, любые из вышеуказанных фармацевтических средств или композиций настоящего изобретения могут применяться для индукции ЦТЛ, и, кроме того, фармацевтические средства или композиции настоящего изобретения, которые включают пептиды и полинуклеотиды, также могут применяться для индукции АПК, как описано ниже.
(1) Способ индукции антигенпрезентирующих клеток (АПК)
Настоящее изобретение обеспечивает способы индукции АПК с применением пептидов настоящего изобретения или полинуклеотидов, кодирующих пептиды. Индукция АПК может быть выполнена, как описано выше в разделе "VI. Антигенпрезентирующие клетки". Настоящее изобретение также обеспечивает способ индукции АПК, которые обладают высоким уровнем способности индуцировать ЦТЛ, индукция которых также была упомянута в разделе "VI. Антигенпрезентирующие клетки", выше.
(2) Способ индукции ЦТЛ
Кроме того, настоящее изобретение обеспечивает способы индукции ЦТЛ с применением пептидов настоящего изобретения, полинуклеотидов, кодирующих пептиды, экзосом или АПК, презентирующих пептиды. Настоящее изобретение также обеспечивает способы индукции ЦТЛ с применением полинуклеотида, кодирующего полипептид, который способен формировать субъединицу T-клеточного рецептора (ТКР), узнающую комплекс пептидов настоящего изобретения и HLA-антигенов. Предпочтительно, способы индукции ЦТЛ включают, по меньшей мере, одну стадию, выбранную из группы, состоящей из:
a: контактирования CD8-положительной T-клетки с антигенпрезентирующей клеткой и/или экзосомой, которая презентирует на своей поверхности комплекс HLA-антигена и пептида настоящего изобретения, и
b: введение полинуклеотида, кодирующего полипептид, который способен формировать субъединицу ТКР, узнающую комплекс пептида настоящего изобретения и HLA-антигена, в CD8-положительную T-клетку.
При введении пептидов настоящего изобретения субъекту, в организме субъекта индуцируются ЦТЛ, и повышается сила иммунного ответа, направленного против раковых клеток. В альтернативе пептиды и полинуклеотиды, кодирующие пептиды, могут применяться в ex vivo терапевтическом способе, в котором полученные от субъекта АПК и CD8-положительные клетки или мононуклеарные лейкоциты периферической крови подвергают контактированию (стимулируют) с пептидами настоящего изобретения in vitro, а после индукции ЦТЛ, активированные клетки ЦТЛ переносят обратно в организм субъекта. Например, способ может включать следующие стадии:
a) забор АПК у субъекта,
b) контактирование АПК стадии a) с пептидом,
c) смешивание АПК стадии b) с CD8+ T-клетками и совместное культивирование с целью индукции ЦТЛ, и
d) сбор CD8+ T-клеток из смешанной культуры стадии c).
В альтернативе, согласно настоящему изобретению, предложено применение пептидов настоящего изобретения для приготовления фармацевтического средства или композиции, индуцирующих ЦТЛ. Кроме того, настоящее изобретение обеспечивает способ приготовления фармацевтического средства или композиции, индуцирующих ЦТЛ, включающий стадию смешивания или включения в лекарственную форму пептида настоящего изобретения с фармацевтически приемлемым носителем. Кроме того, настоящее изобретение также обеспечивает пептид настоящего изобретения для индукции ЦТЛ.
CD8+ T-клетки, обладающие цитотоксической активностью, полученные в стадии d), могут быть введены субъекту в качестве вакцины. АПК, смешиваемые с CD8+ T-клетками в вышеуказанной стадии c), также могут быть получены путем переноса гена, кодирующего настоящие пептиды, в АПК, как подробно описано выше в разделе "VI. Антигенпрезентирующие клетки", впрочем, это не следует рассматривать как ограничение. Таким образом, любые АПК или экзосомы, которые эффективно презентируют настоящие пептиды T-клеткам, могут применяться в настоящем способе.
Следующие примеры представлены для пояснения настоящего изобретения и содействия среднему специалисту в данной области при его осуществлении и применении. Примеры не следует рассматривать как какое-либо ограничение объема изобретения.
ПРИМЕРЫ
Материалы и методы
Линии клеток
Лимфобластная клеточная линия A24 (A24LCL) была получена с помощью трансформации вирусом Эпштейна-Барра HLA-A24-положительного B-лимфоцита человека.
Выбор кандидатных пептидов, полученных из CDCA1
9-мерные и 10-мерные пептиды, полученные из CDCA1, которые связываются с HLA-A*2402, предсказывали с использованием программы "BIMAS" для предсказания потенциальных пептидных фрагментов, связываемых MHC-I человека, (http://www-bimas.cit.nih.gov/molbio/hla_bind), алгоритмы описаны Parker KC et al. (J Immunol 1994, 152(1): 163-75) и Kuzushima K et al. (Blood 2001, 98(6): 1872-81). Указанные пептиды синтезировали в American Peptide Company Inc. (Sunnyvale, CA) согласно стандартной методике твердофазного синтеза и очищали с помощью обращенно-фазовой высокоэффективной жидкостной хроматографии (ВЭЖХ). Чистоту (>90%) и идентичность пептидов определяли с помощью аналитической ВЭЖХ и масс-спектрометрического анализа, соответственно. Пептиды растворяли в диметилсульфоксиде (ДМСО) в концентрации 20 мг/мл и хранили при -80°C.
Индукция ЦТЛ in vitro
Моноцитарные дендритные клетки (ДК) использовали в качестве антигенпрезентирующих клеток (АПК) для индукции ответов цитотоксических T-лимфоцитов (ЦТЛ) против пептидов, презентированных на человеческом лейкоцитарном антигене (HLA). ДК были получены in vitro, как описано в литературе (Nakahara S et al., Cancer Res 2003 Jul 15, 63(14): 4112-8). В частности, мононуклеарные клетки периферической крови (МКПК), выделенные у нормальных добровольцев (HLA-A*2402-положительных) с использованием раствора Ficoll-Plaque (Pharmacia), разделяли по адгезии к пластмассовой чашке для тканевой культуры (Becton Dickinson), обогащая их фракцией моноцитов. Обогащенную моноцитами популяцию клеток культивировали в присутствии 1000 Е/мл гранулоцитарно-макрофагального колониестимулирующего фактора (ГМ-КСФ) (R&D System) и 1000 Е/мл интерлейкина (IL)-4 (R&D System) в среде AIM-V (Invitrogen), содержащей 2% термоинактивированной аутологичной сыворотки (AS). Через 7 дней культивирования, цитокин-индуцировнные ДК сенсибилизировали 20 мкг/мл каждого из синтезированных пептидов в присутствии 3 мкг/мл бета-2-микроглобулина в течение 3 часов при 37°C в среде AIM-V. Полученные клетки, как оказалось, экспрессировали ДК-ассоциированные молекулы, такие как CD80, CD83, CD86 и HLA класса II, на своей поверхности (данные не показаны). Затем указанные ДК, сенсибилизированные пептидами, инактивировали Митомицином C (MMC) (30 мкг/мл в течение 30 минут) и смешивали в соотношении 1:20 с аутологичными CD8+ T-клетками, полученными посредством положительной селекции с использованием набора CD8 Positive Isolation Kit (Dynal). Данные культуры переносили в 48-луночные планшеты (Corning); каждая лунка содержала 1,5×104 ДК, сенсибилизированных пептидами, 3×105 CD8+ T-клеток и 10 нг/мл IL-7 (R&D System) в 0,5 мл среда AIM-V/2% AS. Через три дня в культуры добавляли IL-2 (CHIRON) до конечной концентрации 20 МЕ/мл. В день 7 и 14 T-клетки дополнительно стимулировали аутологичными ДК, сенсибилизированными пептидами. В каждом случае ДК получали таким же способом, как описано выше. ЦТЛ тестировали против сенсибилизированных пептидами клеток A24LCL после 3-го раунда стимуляции пептидами в день 21 (Tanaka H et al., Br J Cancer 2001 Jan 5, 84(1): 94-9; Umano Y et al., Br J Cancer 2001 Apr 20, 84(8): 1052-7; Uchida N et al., Clin Cancer Res 2004 Dec 15, 10(24): 8577-86; Suda T et al., Cancer Sci 2006 May, 97(5): 411-9; Watanabe T et al., Cancer Sci 2005 Aug, 96(8): 498-506).
Методика размножения ЦТЛ
ЦТЛ размножали в культуре, используя метод, подобный описанному Riddell et al. (Walter EA et al., N Engl J Med 1995 Oct 19, 333(16): 1038-44; Riddell SR et al., Nat Med 1996 Feb, 2(2): 216-23). В общей сложности 5×104 ЦТЛ суспендировали в 25 мл среды AIM-V/5% AS с 2 видами линий B-лимфобластных клеток человека, инактивированных MMC, в присутствии 40 нг/мл моноклонального антитела к CD3 (Pharmingen). Через один день после получения, к культурам добавляли 120 МЕ/мл IL-2. В культуры добавляли свежую среду AIM-V/5% AS, содержащую 30 МЕ/мл IL-2 в дни 5, 8 и 11 (Tanaka H et al., Br J Cancer 2001 Jan 5, 84(1): 94-9; Umano Y et al., Br J Cancer 2001 Apr 20, 84(8): 1052-7; Uchida N et al., Clin Cancer Res 2004 Dec 15, 10(24): 8577-86; Suda T et al., Cancer Sci 2006 May, 97(5): 411-9; Watanabe T et al., Cancer Sci 2005 Aug, 96(8): 498-506).
Получение культур клонов ЦТЛ
Приготавливали разведения ЦТЛ 0,3, 1 и 3 на лунку в 96-луночных круглодонных микропланшетах (Nalge Nunc International). ЦТЛ культивировали с 2 видами линий B-лимфобластных клеток человека при плотности 1×104 клеток/лунка, 30 нг/мл антитела к CD3 и 125 Е/мл IL-2 в среде AIM-V, содержащей 5% AS, в общем объеме 150 мкл/лунка. В среду через 10 дней добавляли 50 мкл/лунка IL-2, достигнув конечной концентрации IL-2 125 Е/мл. Активность ЦТЛ проверяли на 14-ый день, а клоны ЦТЛ размножали, используя такую же методику, как описано выше (Uchida N et al., Clin Cancer Res 2004 Dec 15, 10(24): 8577-86; Suda T et al., Cancer Sci 2006 May, 97(5): 411-9; Watanabe T et al., Cancer Sci 2005 Aug, 96(8): 498-506).
Специфичная активность ЦТЛ
Для определения специфичной активности ЦТЛ проводили интерферон (IFN)-гамма ферментный спот-иммуноанализ (ELISPOT) и IFN-гамма твердофазный иммуноферментный анализ (ELISA). В частности, сенсибилизированные пептидами A24LCL (1×104/лунка) получали в качестве клеток-стимуляторов. Культуры клеток в 48 лунках использовали в качестве клеток-респондеров. IFN-гамма анализ ELISPOT и IFN-гамма анализ ELISA проводили согласно методике производителя.
Получение линий клеток, принудительно экспрессирующих целевой ген и/или HLA-A24
кДНК, кодирующие открытую рамку считывания целевых генов или HLA-A24, амплифицировали с помощью ПЦР. ПЦР-амплифицированный продукт клонировали в вектор pCAGGS. Плазмиды трансфицировали в линию COS7, которая представляет собой "нулевую" клеточную линию по целевым генам и HLA-A24, используя липофектамин 2000 (Invitrogen) согласно методике, рекомендованной производителем. Через 2 для после трансфекции, трансфицированные клетки собирали с использованием Versene® (Invitrogen) и использовали в качестве клеток-мишеней (5×104 клеток/лунка) для анализа активности ЦТЛ.
Результаты
Предсказание HLA-A24-связывающих пептидов, полученных из CDCA1
В Таблице 1 показаны HLA-A*2402-связывающие пептиды CDCA1 в порядке убывания аффинности связывания. В общей сложности отобрали и исследовали 40 пептидов, обладающих потенциальной аффинностью связывания к HLA-A24, чтобы определить эпитоп-пептиды.
Стартовое положение указывает число аминокислотных остатков от N-конца CDCA1.
Балл связывания получен из "BIMAS".
Индукция ЦТЛ предсказанными пептидами из CDCA1, рестриктированными HLA-A*2402, и получение линий ЦТЛ, стимулированных пептидами, полученными из CDCA1
ЦТЛ для указанных пептидов, полученных из CDCA1, получали согласно методикам, описанным в разделе "Материалы и методы". Специфичная активность ЦТЛ в отношении пептидов определяли с помощью IFN-гамма анализа ELISPOT (Фигуры 1a-f). Было показано, что CDCA1-A24-10-119 (SEQ ID NO: 3), CDCA1-A24-10-335 (SEQ ID NO: 4), CDCA1-A24-10-48 (SEQ ID NO: 11), CDCA1-A24-10-5 (SEQ ID NO: 14), CDCA1-A24-9-8 (SEQ ID NO: 22) и CDCA1-A24-9-56 (SEQ ID NO: 23) демонстрировали мощную выработку IFN-гамма по сравнению с контрольными лунками. Кроме того, клетки в положительной лунке #8, стимулированные CDCA1-A24-10-119 (SEQ ID NO: 3), #1, стимулированные CDCA1-A24-10-335 (SEQ ID NO: 4), #1, стимулированные CDCA1-A24-10-48 (SEQ ID NO: 11), #4, стимулированные CDCA1-A24-10-5 (SEQ ID NO: 14), #2, стимулированные CDCA1-A24-9-8 (SEQ ID NO: 22), и #2, стимулированные CDCA1-A24-9-56 (SEQ ID NO: 23), размножили и получили соответствующие линии ЦТЛ. Активность ЦТЛ в полученных линиях ЦТЛ определяли с помощью IFN-гамма анализа ELISA (Фигуры 2a-f). Было показано, что все линии ЦТЛ демонстрировали мощную продукцию IFN-гамма против клеток-мишеней, сенсибилизированных соответствующим пептидом, по сравнению с клетками-мишенями без сенсибилизации пептидами. С другой стороны, при стимуляции другими пептидами не удалось получить линий ЦТЛ, несмотря на то, что данные пептиды обладали возможной связывающей активностью в отношении HLA-A*2402. Например, типичные отрицательные данные ответа ЦТЛ, стимулированных CDCA1-A24-10-74 (SEQ ID NO: 2), показаны на Фигуре 1g и Фигуре 2g. Представленные результаты указывают, что шесть пептидов, полученных из CDCA1, обладают способностью индуцировать мощные линии ЦТЛ.
Получение линий ЦТЛ клонов против CDCA1 специфичных пептидов
Линии клонов ЦТЛ получали путем серийного разведения из линий ЦТЛ, как описано в разделе "Материалы и методы", а затем с помощью IFN-гамма анализа ELISA определяли выработку IFN-гамма из клонов ЦТЛ против клеток-мишеней, сенсибилизированных пептидом. Мощную продукцию IFN-гамма обнаружили в клонах ЦТЛ, стимулированных с использованием SEQ ID NO: 23, как показано на Фигуре 3.
Специфичная активность ЦТЛ против клеток-мишеней, экзогенно экспрессирующих CDCA1 и HLA-A*2402
Стабильные линии ЦТЛ, индуцированные против указанных пептидов, исследовали на способность узнавать клетки-мишени, которые экзогенно экспрессируют молекулы CDCA1 и HLA-A*2402. Специфичную активность ЦТЛ против клеток COS7, трансфицированных полноразмерными генами молекул CDCA1 и HLA-A*2402 (специфичная модель клеток-мишеней, экзогенно экспрессирующих ген CDCA1 и HLA-A*2402), анализировали, используя линии ЦТЛ, индуцированные соответствующим пептидом, в качестве клеток-эффекторов. Клетки COS7, трансфицированные либо полноразмерным геном CDCA1, либо полноразмерным геном HLA-A*2402, получали в качестве контроля. Как показано на Фигуре 4, ЦТЛ, стимулированные с использованием SEQ ID NO: 23, демонстрировали мощную активность ЦТЛ против клеток COS7, экспрессирующих CDCA1 и HLA-A*2402. С другой стороны, какой-либо существенной специфичной активности ЦТЛ против контроля не обнаружили. Таким образом, представленные данные четко демонстрируют, что пептид, имеющий аминокислотную последовательность SEQ ID NO: 23, естественно презентируется на целевых клетках с молекулой HLA-A*2402 и узнается ЦТЛ. Результаты указывают, что данный пептид, полученный из CDCA1, может применяться для иммунотерапии рака, в особенности, как вакцина против рака у пациентов с опухолями, экспрессирующими CDCA1.
Анализ гомологии антигенных пептидов
ЦТЛ, стимулированные CDCA1-A24-10-119 (SEQ ID NO: 3), CDCA1-A24-10-335 (SEQ ID NO: 4), CDCA1-A24-10-48 (SEQ ID NO: 11), CDCA1-A24-10-5 (SEQ ID NO: 14), CDCA1-A24-9-8 (SEQ ID NO: 22) и CDCA1-A24-9-56 (SEQ ID NO: 23), показали существенную и специфичную активность ЦТЛ. Полученный результат может быть обусловлен тем, что последовательности CDCA1-A24-10-119 (SEQ ID NO: 3), CDCA1-A24-10-335 (SEQ ID NO: 4), CDCA1-A24-10-48 (SEQ ID NO: 11), CDCA1-A24-10-5 (SEQ ID NO: 14), CDCA1-A24-9-8 (SEQ ID NO: 22) и CDCA1-A24-9-56 (SEQ ID NO: 23) гомологичны пептидам, полученным из других молекул, которые, как известно, сенсибилизируют иммунную систему человека. Чтобы исключить подобную возможность, проводили анализ гомологии указанных пептидных последовательностей, используя алгоритм BLAST (http://www.ncbi.nlm.nih.gov/blast/blast.cgi), который не выявил последовательностей с существенной гомологией. Результаты, полученные в анализах гомологии, указывают, что последовательности CDCA1-A24-10-119 (SEQ ID NO: 3), CDCA1-A24-10-335 (SEQ ID NO: 4), CDCA1-A24-10-48 (SEQ ID NO: 11), CDCA1-A24-10-5 (SEQ ID NO: 14), CDCA1-A24-9-8 (SEQ ID NO: 22) и CDCA1-A24-9-56 (SEQ ID NO: 23) уникальны, и, таким образом, существует низкая вероятность того, что указанные молекулы индуцируют случайные иммунные ответы на некие посторонние молекулы.
В заключение необходимо отметить, что были идентифицированы новые эпитоп-пептиды HLA-A24, полученные из CDCA1, и было продемонстрировано, что они могут применяться в иммунотерапии рака.
Промышленная применимость
В настоящем изобретении описаны новые ОСА, в особенности, полученные из CDCA1, которые вызывают мощные и специфичные противоопухолевые иммунные ответы и могут применяться при большом разнообразии типов рака. Такие ОСА гарантируют дальнейшее развитие в качестве пептидных вакцин против заболеваний, связанных с CDCA1, например, раковых опухолей, более конкретно, опухоли яичка, рака поджелудочной железы, рака мочевого пузыря, немелкоклеточного рака легкого, мелкоклеточного рака легкого и рака пищевода.
Хотя в настоящей заявке изобретение описано подробно и в отношении конкретных вариантов осуществления, следует понимать, что предыдущее описание является примерным и пояснительным по своему характеру и служит для иллюстрации изобретения и его предпочтительных вариантов осуществления. Посредством стандартного экспериментирования, специалист, квалифицированный в данной области техники, с легкостью сумеет оценить, что в настоящее изобретение могут быть внесены различные изменения и модификации, без отступления от сущности и объема изобретения, границы которого определяются в соответствии с прилагаемой формулой.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПЕПТИД, ПОЛУЧЕННЫЙ ИЗ CDCA1, И СОДЕРЖАЩАЯ ЕГО ВАКЦИНА | 2015 |
|
RU2699543C2 |
| МОДИФИЦИРОВАННЫЕ ПЕПТИДЫ MELK И СОДЕРЖАЩИЕ ИХ ВАКЦИНЫ | 2011 |
|
RU2580035C2 |
| ПЕПТИДЫ FOXM1 И ВАКЦИНЫ, СОДЕРЖАЩИЕ ИХ | 2010 |
|
RU2560431C2 |
| ПЕПТИД, ПОЛУЧЕННЫЙ ИЗ URLC10, И СОДЕРЖАЩАЯ ЕГО ВАКЦИНА | 2015 |
|
RU2700881C2 |
| ПЕПТИД, ПОЛУЧЕННЫЙ ИЗ KOC1, И СОДЕРЖАЩАЯ ЕГО ВАКЦИНА | 2015 |
|
RU2699542C2 |
| ПЕПТИДЫ ТЕМ8 И СОДЕРЖАЩИЕ ИХ ВАКЦИНЫ | 2008 |
|
RU2498993C2 |
| ПЕПТИД, ПОЛУЧЕННЫЙ ИЗ DEPDC1, И СОДЕРЖАЩАЯ ЕГО ВАКЦИНА | 2016 |
|
RU2765574C2 |
| ПЕПТИДЫ HJURP И СОДЕРЖАЩИЕ ИХ ВАКЦИНЫ | 2011 |
|
RU2570560C2 |
| ПЕПТИДЫ UBE2T И СОДЕРЖАЩИЕ ИХ ВАКЦИНЫ | 2013 |
|
RU2663350C2 |
| ПЕПТИДЫ ТОРК И СОДЕРЖАЩИЕ ИХ ВАКЦИНЫ | 2012 |
|
RU2633503C2 |








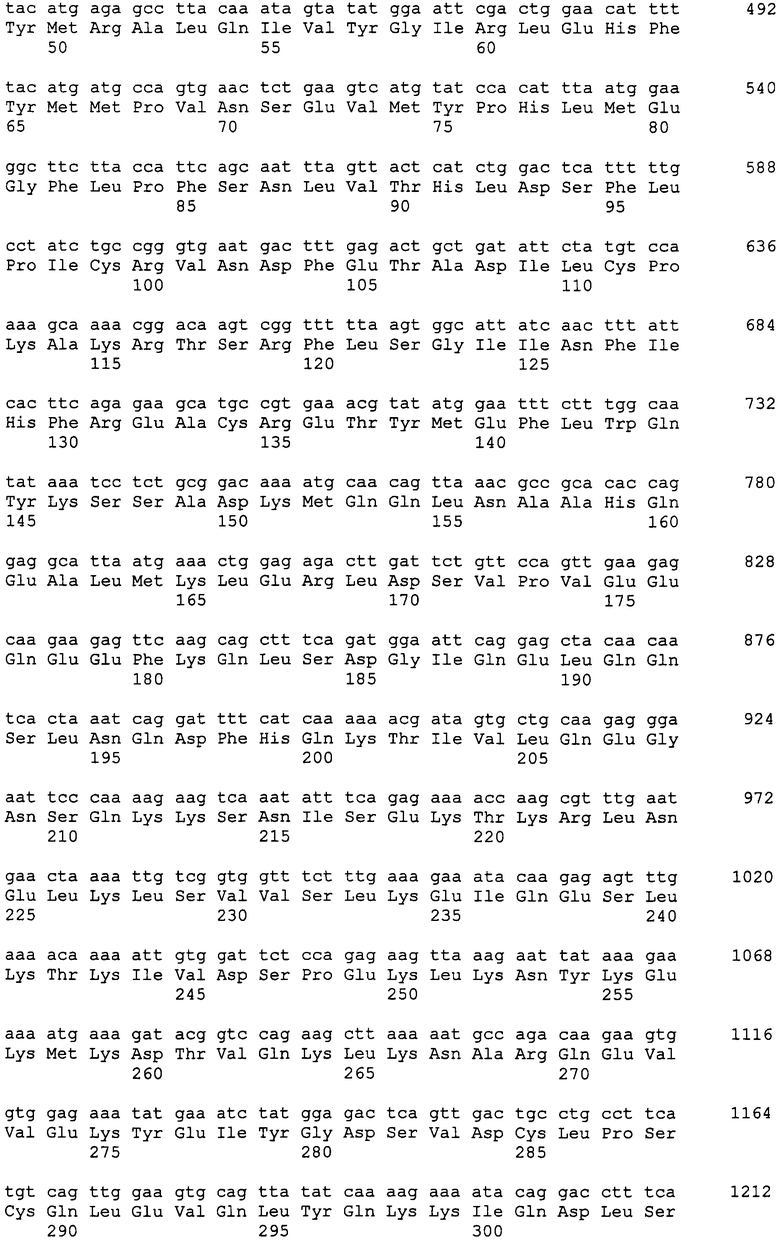



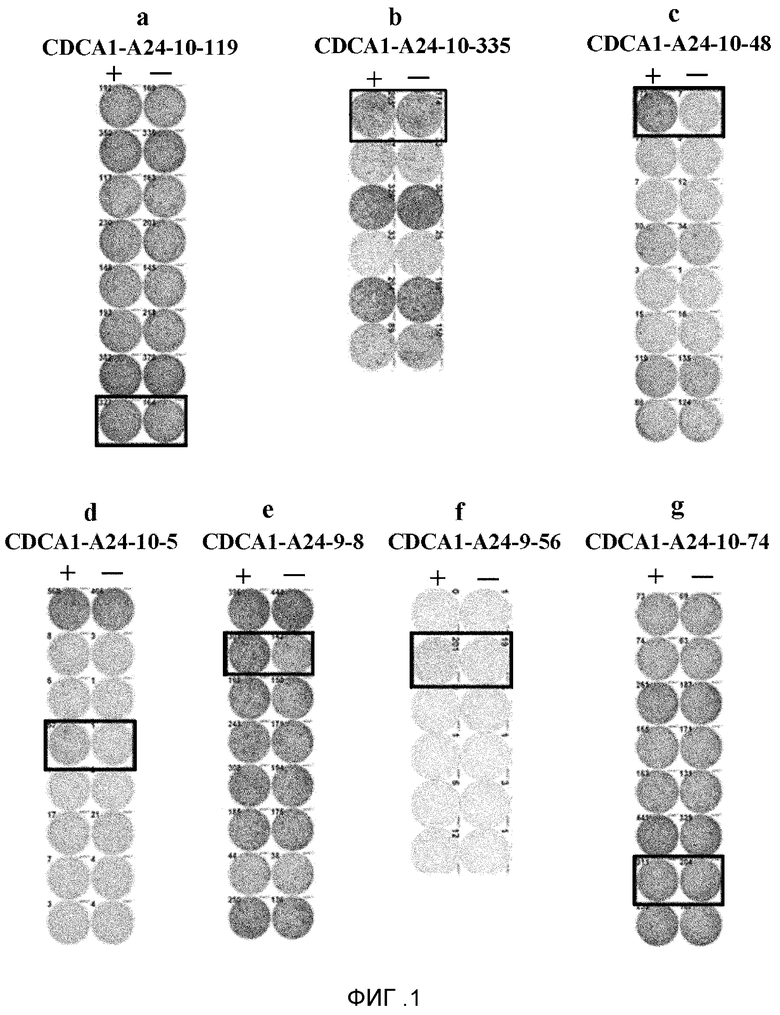
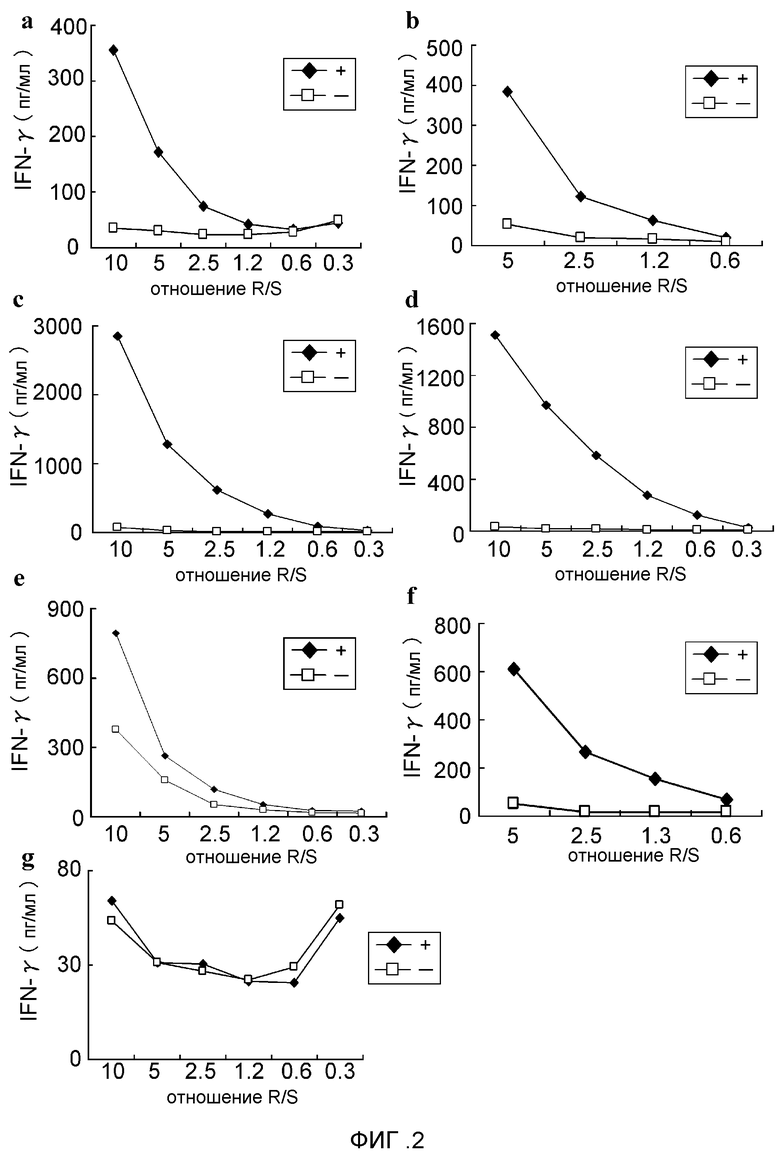
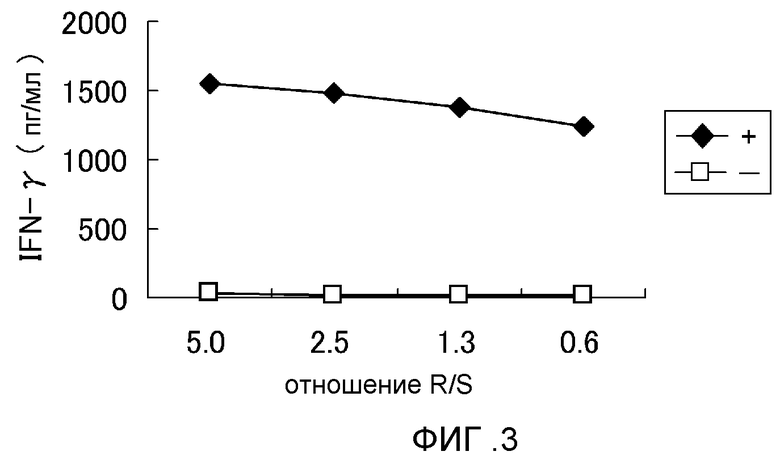
Изобретение относится к области биотехнологии, конкретно к получению вакцин против рака, и может быть использовано в медицине. Выделенный пептид, обладающий способностью индуцировать цитотоксический Т-лимфоцит (ЦТЛ) в присутствии антигенпрезентирующей клетки, несущей HLA-A*2402, используют для получения антигенпрезентирующих клеток и соответственно ЦТЛ. Полученные ЦТЛ используют для специфичного действия против раковых клеток, экспрессирующих CDCA1. Изобретение позволяет разработать эффективную вакцину для индукции противоопухолевого иммунитета у субъекта, у которого антиген HLA представляет собой HLA-A*2402. 13 н. и 3 з.п. ф-лы, 4 ил., 1 табл., 1 пр.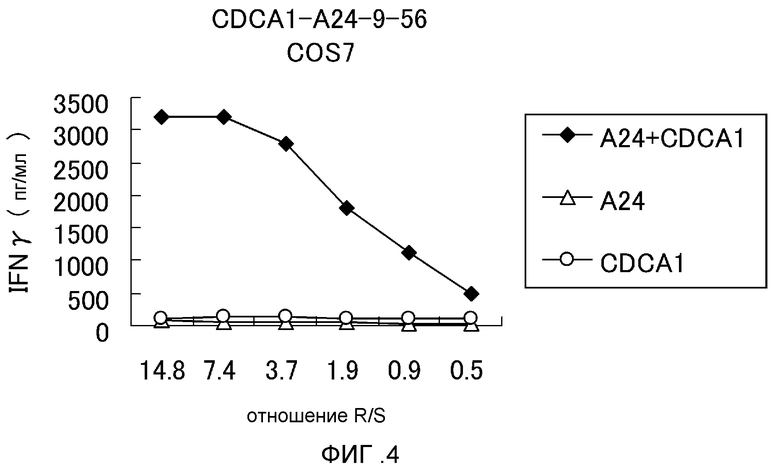
1. Выделенный пептид, обладающий способностью индуцировать цитотоксический Т-лимфоцит (ЦТЛ) в присутствии антигенпрезентирующей клетки, несущей HLA-A*2402, где пептид представляет собой (а) или (b) ниже:
(a) пептид, характеризующийся аминокислотной последовательностью, выбранной из группы, состоящей из: SEQ ID NO: 3, 4, 11, 14, 22 и 23; и
(b) пептид, характеризующийся аминокислотной последовательностью, в которой вторая аминокислота с N-конца аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 3, 4, 11, 14, 22 и 23, модифицирована, чтобы представлять собой аминокислоту, выбранную из группы, состоящей из фенилаланина, тирозина, метионина и триптофана, и/или С-концевая аминокислота аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 3, 4, 11, 14, 22 и 23, модифицирована, чтобы представлять собой аминокислоту, выбранную из группы, состоящей из фенилаланина, лейцина, изолейцина, триптофана и метионина.
2. Выделенный полинуклеотид, кодирующий пептид по п.1.
3. Способ индукции антигенпрезентирующей клетки, несущей HLA- А*2402, со способностью индуцировать ЦТЛ с применением пептида по п.1.
4. Способ по п.3, где указанный способ включает стадию контактирования антигенпрезентирующей клетки, несущей HLA-A*2402, с пептидом по п.1.
5. Выделенная антигенпрезентирующая клетка, обладающая способностью индуцировать ЦТЛ, которая презентирует комплекс, образованный между HLA-A*2402 и пептидом по п.1 на своей поверхности.
6. Антигенпрезентирующая клетка по п.5, где указанная клетка индуцирована способом по п.3 или 4.
7. Способ индукции ЦТЛ с применением:
(a) пептида по п.1 и антигенпрезентирующей клетки, несущей HLA-А*2402; или
(b) антигенпрезентирующей клетки, которая презентирует комплекс, образованный между HLA-A*2402 и пептидом по п.1 на своей поверхности.
8. Способ по п.7, где указанный способ включает стадию контактирования CDS-положительной Т-клетки с антигенпрезентирующей клеткой, которая презентирует комплекс, образованный между HLA-A*2402 и пептидом по п.1 на своей поверхности.
9. Средство для индукции ЦТЛ, где указанное средство включает антигенпрезентирующую клетку, которая презентирует комплекс, образованный между HLA-A*2402 и пептидом по п.1 на своей поверхности, в качестве активного компонента.
10. Средство для индукции ЦТЛ в присутствии антигенпрезентирующей клетки, несущей HLA-A*2402, где средство включает пептид по п.1 в качестве активного компонента.
11. Выделенный ЦТЛ для специфичного действия против раковых клеток, экспрессирующих CDCA1, который индуцирован с применением способа, включающего стадию контактирования CDS-положительной Т-клетки с антигенпрезентирующей клеткой, которая презентирует комплекс, образованный между HLA-A*2402 и пептидом по п.1 на своей поверхности in vitro.
12. Фармацевтическое средство, включающее в качестве активного компонента от 0,001 мг до 1000 мг по меньшей мере одного пептида по п.1 в комбинации с фармакологически приемлемым носителем, составленное для цели, выбранной из группы, состоящей из:
(i) лечения рака;
(ii) профилактики рака;
(iii) предотвращения постоперативного рецидива рака; и
(iv) комбинации перечисленного,
где указанная фармацевтическая композиция составлена для введения субъекту, у которого антиген HLA представляет собой HLA-A*2402.
13. Способ индукции иммунного ответа против рака у субъекта, у которого антиген HLA представляет собой HLA-А*2402, включающий стадию введения указанному субъекту пептида по п.1 в дозе от 0,001 мг до 1000 мг.
14. Способ индукции иммунного ответа против рака у субъекта, у которого антиген HLA представляет собой HLA-A*2402, включающий стадии:
(a) получение антигенпрезентирующей клетки у субъекта;
(b) контактирование антигенпрезентирующей клетки со стадии (а) с пептидом по п.1; и
(c) введение антигенпрезентирующей клетки со стадии (b) субъекту.
15. Способ индукции иммунного ответа против рака у субъекта, у которого антиген HLA представляет собой HLA-A*2402, включающий стадии:
(a) получение антигенпрезентирующей клетки и CDS-положительной Т-клетки у субъекта;
(b) контактирование антигенпрезентирующей клетки со стадии (а) с пептидом по п.1;
(c) смешивание антигенпрезентирующей клетки со стадии с CD8- положительной Т-клеткой со стадии (а) и совместное культивирование для индукции ЦТЛ; и
(d) введение ЦТЛ, индуцированного на стадии (с), субъекту.
16. Вакцина для индукции противоопухолевого иммунитета у субъекта, у которого антиген HLA представляет собой HLA-A*2402, включающая от 0,001 мг до 1000 мг пептида по п.1 в качестве активного компонента.
| HARAO, MICHIKO, Cell division cycle associated 1, an ideal lung cancer antigen for immunotherapy, identified using cDNA microarray analysis, DOCTOR′S THESIS, GRADUATE SCHOOL OF MEDICAL SCIENCES, March 2008 | |||
| KUMAMOTO UNIVERSITY, KUMAMOTO, JAPAN | |||
| WO 2004080148 A2, 23.09.2004 | |||
| HARAO, MICHIKO ET AL., CDCA1, a novel cancer-testis antigen useful |
Авторы
Даты
2013-12-27—Публикация
2009-06-18—Подача