Область техники
Данное изобретение относится к имплантируемым медицинским устройствам и, в частности, к имплантируемым ограничивающим желудок устройствам.
Уровень техники
Ожирение становится растущей проблемой, в частности, в США, поскольку число тучных людей продолжает увеличиваться и становится больше известно об отрицательном воздействии ожирения на здоровье. Болезненное ожирение, при котором человек имеет вес, на 100 фунтов или больше превышающий идеальный вес тела, представляет значительную опасность возникновения серьезных проблем со здоровьем. В соответствии с этим, большое внимание уделяется лечению страдающих ожирением пациентов. Один способ лечения болезненного ожирения состоит в расположении ограничивающего устройства, такого как удлиненный бандаж, вокруг верхней части желудка. Желудочный бандаж обычно содержит заполненный текучей средой баллон с фиксированными концевыми точками, который окружает желудок как раз ниже соединения пищевода с желудком с образованием небольшого желудочного мешка над бандажом и уменьшенным отверстием стомы в желудок. Когда текучая среда вводится в баллон, то бандаж расширяется к желудку, создавая ограничение входу пищи или стомы в желудок. Для уменьшения этого ограничения текучую среду удаляют из бандажа. Действие бандажа состоит в уменьшении доступного объема желудка и тем самым количества пищи, которое можно потреблять до ощущения полноты.
Устройства ограничения пищи содержат также механически регулируемые бандажи, которые аналогичным образом окружают верхнюю часть желудка. Эти бандажи включают любое количество упругих материалов или передаточных устройств, а также приводных элементов для регулирования бандажей. Дополнительно к этому, были разработаны желудочные бандажи, которые включают как гидравлические, так и механические приводные элементы. Пример такого регулируемого желудочного бандажа раскрыт в патенте США № 6067991 с названием «Механическое устройство для ограничения приема пищи», выданный 30 мая 2000 г., полное содержание которого включается в данное описание. Известно также ограничение доступного объема для пищи в полости желудка посредством имплантации надуваемого эластомерного баллона внутри самой полости желудка. Баллон заполняется текучей средой для расширения к стенкам желудка и тем самым для уменьшения доступного для пищи объема внутри желудка.
При каждом из указанных устройств для ограничения пищи безопасное, эффективное лечение требует обеспечения возможности регулярного мониторинга и регулирования устройства для изменения степени ограничения, применяемого в желудке. При применении бандажных устройств желудочный мешок над бандажом значительно увеличивается в размере после первоначальной имплантации. В соответствии с этим сначала отверстие стомы в желудке необходимо выполнять достаточно большим для обеспечения приема пациентом адекватного питания во время адаптации желудка к бандажному устройству. При увеличении желудочного мешка в размере бандаж можно регулировать для изменения размера стомы. Дополнительно к этому, желательно изменять размер стомы для согласования с изменениями тела пациента или режимом лечения, или в более срочном случае для устранения препятствия или сильного расширения кишечника. Обычно регулирование гидравлического желудочного бандажа требует планового посещения пациентом клиники, во время которого используется игла Хубера и шприц для прохождения через кожу пациента для добавления или удаления текучей среды из баллона через ввод. В последнее время разработаны имплантируемые насосы, которые обеспечивают возможность неинвазивного регулирования бандажа. Внешнее программирующее устройство соединяется с имплантированным насосом с использованием телеметрии для управления насосом. Во время планового посещения врач размещает удерживаемую в руке часть программирующего устройства вблизи желудочного имплантанта и передает энергию и сигналы управления в имплантант. Имплантант в свою очередь регулирует уровни текучей среды в бандаже и передает ответные сигналы в программирующее устройство.
Во время этого регулирования желудочного бандажа трудно определять, как проходит регулирование и будет ли регулирование иметь желаемый эффект. В качестве попытки определения эффективности регулирования некоторые врачи используют флюороскопию с проглатыванием бария при выполнении регулирования. Однако флюороскопия является дорогостоящей и не желательной за счет доз радиации, получаемых как врачом, так и пациентом. Другие врачи просят пациента выпить стакан воды во время или после регулирования для определения, может ли проходить вода через регулируемую стому. Однако этот способ лишь подтверждает, что пациенту не затруднена проходимость, но не обеспечивает информацию об эффективности регулирования. Часто врач просто использует метод попыток, основанный на предыдущем опыте, и результаты регулирования выясняются лишь через несколько часов или дней, когда пациент ощущает полное затруднение прохождения в полость желудка, или же бандаж вызывает эрозию ткани желудка за счет чрезмерного давления со стороны бандажа.
Кроме того, имплантируемые насосы, известные из уровня техники, такие как центробежные или поршневые насосы, требуют много энергии во время работы. Потребление энергии таких насосов ограничивает их использование для частого регулирования уровня текучей среды в бандаже. Имеющиеся насосы также требуют большие корпуса для размещения механического насосного механизма, передач и двигателей, что дополнительно ограничивает возможность использования имплантируемых насосов. Необходимы также дополнительные компоненты, такие как клапаны, для поддерживания давления текучей среды в бандаже, когда в обычные насосы не подается энергия. Пример имплантируемой насосной системы описан в публикации США № 2005/0277974 с названием «Термодинамический реверсивный инфузивный насос для использования в качестве дистанционно управляемого желудочного бандажа» от 28 мая 2004 г.
В соответствии с этим предлагаются способы и устройства для использования с ограничивающим желудок устройством и, в частности, предлагаются способы и устройства, которые обеспечивают возможность регулирования ограничивающих желудок устройств.
Сущность изобретения
Данное изобретение предлагает в целом системы и способы для формирования ограничения в пациенте. В одном примере выполнения система ограничения включает имплантируемое ограничивающее устройство и имплантируемый микро-электромеханический (MEMS) насос, соединенный по потоку текучей среды с ограничивающим устройством. Не обязательно имплантируемый ввод может быть соединен по потоку текучей среды с имплантируемым ограничивающим устройством и насосом. Имплантируемое ограничивающие устройство выполнено с возможностью регулирования и предназначено для создания ограничения в пациенте, и имплантируемый ввод, если он имеется, предназначен для приема текучей среды из источника текучей среды вне пациента. Имплантируемый насос MEMS имеет камеру для текучей среды, расположенную внутри корпуса насоса. Камера насоса имеет впускной клапан, расположенный между камерой для текучей среды и входной камерой, и выпускной клапан, расположенный между камерой для текучей среды и выходной камерой. Насос включает также насосную мембрану, соединенную по текучей среде с камерой для текучей среды, и электрод вблизи насосной мембраны. Насосная мембрана предназначена для отклонения в ответ на прикладываемое к электроду напряжение. Отклонение насосной мембраны создает разницу давления между камерой для текучей среды и входной и выходной камерами для управления потоком текучей среды через насос. Впускной и выпускной клапаны предназначены для открывания и закрывания в ответ на изменения давления в камере для текучей среды. Текучая среда может проходить в ограничивающей системе в направлении от насоса MEMS к ограничивающему устройству или же в направлении от ограничивающего устройства к насосу MEMS. В одном варианте выполнения насос может быть соединен с возможностью прохождения текучей среды с имплантируемым вводом. Система может также включать имплантируемый датчик, соединенный с ограничивающим устройством и предназначенный для измерения, по меньшей мере, давления внутри ограничивающего устройства. Система ограничения может, не обязательно, включать резервуар текучей среды, соединенный с насосом. Резервуар текучей среды предназначен для удерживания текучей среды и может быть предназначен для удерживания приблизительно 0,1-20 мл текучей среды.
Насос можно приводить в действие вручную для движения текучей среды к ограничивающему устройству или от него. В качестве альтернативного решения, насос может приводиться в действие автоматически, с помощью таких технологий как управление с помощью таймера или программируемого приведения в действие в ответ на определенные измеряемые параметры. В одном варианте выполнения имплантируемый насос вызывает изменение давления внутри ограничивающего устройства в соответствии с программируемым расписанием.
Кроме того, предлагаются способы регулирования давления в имплантируемом ограничивающем устройстве. В одном варианте выполнения способ может включать измерение клинически релевантного параметра, регулирование давления внутри ограничивающего устройства в ответ на измеренный клинически релевантный параметр посредством приведения в действие насоса, соединенного с возможностью прохождения текучей среды с ограничивающим устройством. В одном варианте выполнения насос может быть микро-электромеханическим (MEMS) устройством для создания нагнетательного действия для перемещения текучей среды через насос. Измерение клинически релевантного параметра можно осуществлять с использованием имплантируемого датчика. Клинически релевантный параметр может быть давлением, в этом случае имплантируемый датчик является датчиком давления. В таком варианте выполнения измеренное давление сравнивается с диапазоном желаемого давления, и давление внутри ограничивающего устройства регулируется для нахождения приблизительно внутри диапазона желаемого давления, если измеренное давление не лежит в диапазоне желаемого давления. В одном варианте выполнения насос может приводиться в действие автоматически, хотя возможны также другие технологии приведения в действие, включая приведение в действие вручную.
В еще одном варианте выполнения предусмотрен имплантируемый микро-электромеханический (MEMS) насос с соединением по текучей среде с источником текучей среды и с мишенью текучей среды, при этом насос MEMS предназначен для избирательной транспортировки текучей среды между источником текучей среды и мишенью текучей среды. Источник текучей среды и мишень текучей среды могут быть имплантированы внутри тела и/или могут быть компонентами, естественно присутствующими внутри тела. Текучая среда может быть любой текучей средой, включая текучую среду, которая является или содержит один или несколько терапевтических и/или биологически активных веществ.
Краткое описание чертежей
Для лучшего понимания изобретения ниже приводится его подробное описание со ссылками на прилагаемые чертежи, на которых схематично изображено:
фиг.1А - вариант выполнения системы ограничения приема пищи;
фиг.1В - вариант выполнения имплантируемой части системы ограничения приема пищи, согласно фиг.1А, в изометрической проекции;
фиг.2А - устройство ограничения приема пищи, согласно фиг.1А, в изометрической проекции;
фиг.2В - устройство ограничения приема пищи, согласно фиг.1А, наложенное поверх соединения кишечника с желудком пациента;
фиг.3 - вариант выполнения корпуса инъекционного ввода, согласно фиг.1А, в изометрической проекции;
фиг.4 - вариант выполнения корпуса датчика, согласно фиг.1А, в изометрической проекции;
фиг.5 - имплантируемая часть системы ограничения приема пищи, согласно варианту выполнения изобретения, в изометрической проекции;
фиг.6 - разрез примера выполнения имплантируемого насоса MEMS;
фиг.7А - разрез насоса, согласно фиг.6, в исходном состоянии;
фиг.7В - разрез насоса, согласно фиг.6, с изображением отклонения мембраны при подаче тока в электрод;
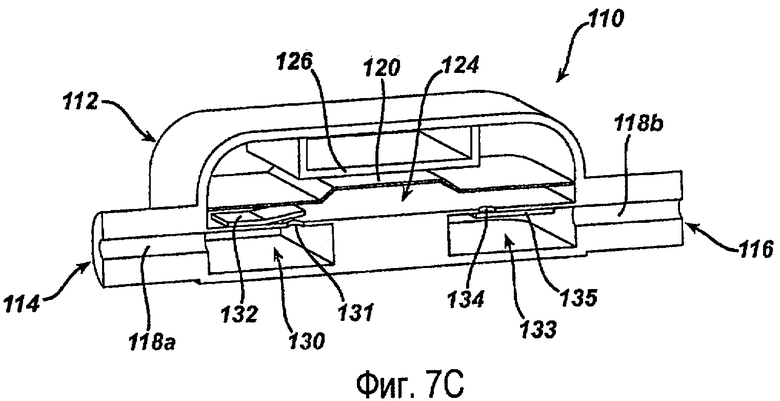
фиг.7С - разрез насоса, согласно фиг.6, с открытым впускным клапаном в ответ на изменение давления в камере для текучей среды;
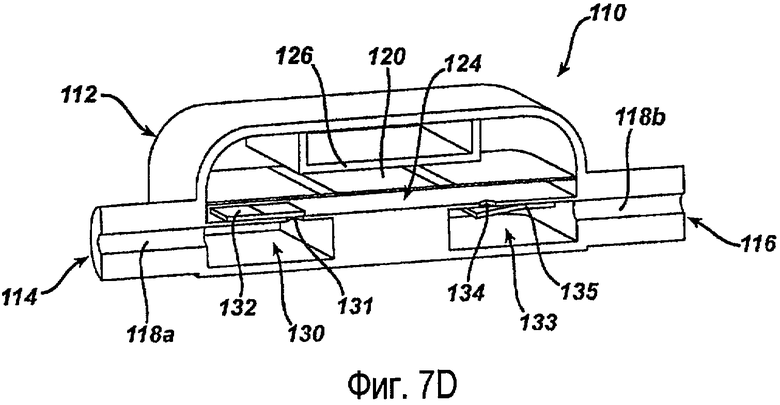
фиг.7D - разрез насоса, согласно фиг.6, с открытым выпускным клапаном в ответ на изменение давления в камере для текучей среды;
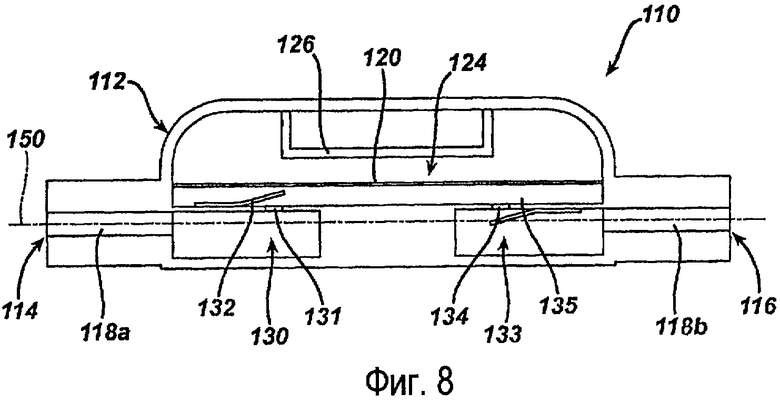
фиг.8 - насос, согласно фиг.6, с изображением пути прохождения текучей среды через насос.
Подробное описание изобретения
Ниже приводится описание некоторых примеров выполнения для обеспечения общего понимания принципов структуры, функции, изготовления и использования предлагаемых устройств и способов. Один или более примеров этих вариантов выполнения иллюстрированы на прилагаемых чертежах. Для специалистов в данной области техники понятно, что устройства и способы, описание которых приводится здесь и которые показаны на прилагаемых чертежах, не ограничиваются этими примерами выполнения, и объем данного изобретения задается лишь формулой изобретения. Признаки, показанные или описанные в связи с одним примером выполнения, можно комбинировать с признаками других вариантов выполнения. Эти модификации и вариации включаются в объем данного изобретения.
Данное изобретение предлагает в целом системы и способы для формирования ограничения в пациенте. В целом, системы и способы позволяют регулировать давление или объем текучей среды в ограничивающем устройстве. Регулирование давления или объема осуществляется посредством использования имплантируемого насоса. Имплантируемый насос обеспечивает возможность регулирования давления или объема текучей среды в ограничивающем устройстве без необходимости добавления текучей среды из наружного источника.
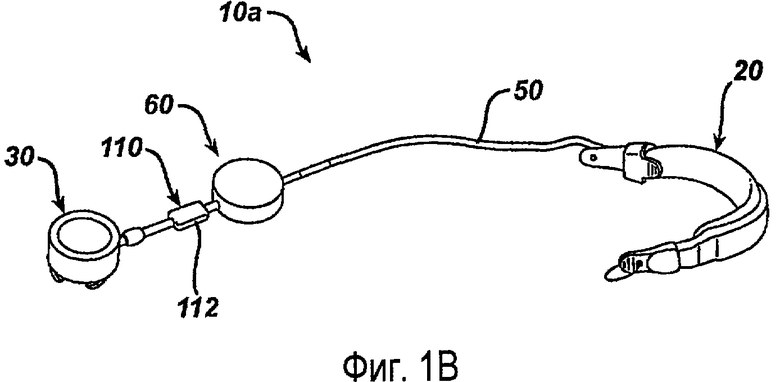
Хотя данное изобретение можно использовать с различными системами ограничения, известными из уровня техники, на фиг.1А показан пример выполнения системы 10 ограничения приема пищи при использовании в пациенте. Как показано на фиг.1А, система 10 включает в основном имплантируемую часть 10а и наружную часть 10b. На фиг.1В показана имплантируемая часть 10а вне пациента. Имплантируемая часть 10а включает регулируемый желудочный бандаж 20, который предназначен для расположения вокруг верхней части желудка 40 пациента, и корпус 30 инъекционного ввода, который соединен по текучей среде с регулируемым желудочным бандажом 20, например, через катетер 50.
Корпус 30 инъекционного ввода предназначен для обеспечения возможности ввода и удаления текучей среды из желудочного бандажа 20 для регулирования за счет этого размера бандажа и тем самым давления, прикладываемого к желудку. Таким образом, корпус 30 инъекционного ввода может быть имплантирован в месте внутри тела, которое доступно через ткань. Обычно инъекционные вводы расположены в боковой подреберной зоне живота пациента под кожей и слоями жировой ткани. Хирурги также обычно имплантируют инъекционные вводы на грудине пациента.
Внутренняя часть 10а может также включать чувствительное или измерительное устройство, соединенное с возможностью прохождения текучей среды с замкнутым контуром текучей среды в имплантируемой части 10а, так что измерительное устройство может выполнять измерения любого параметра, относящегося к имплантируемым ограничивающим устройствам. Такие клинически релевантные параметры включают, но не ограничиваясь этим, температуру, давление, изменения давления, акустический сигнал, полное сопротивление ткани, изменения полного сопротивления ткани, химический состав, изменения химического состава, отсчет импульсов, ширину и амплитуду импульсов. Хотя обсуждаемые здесь способы и устройства могут относиться к любому параметру, в примере выполнения измерения относятся к давлению, и описание способов и устройств приводится ниже применительно к измерению давления текучей среды в замкнутом контуре текучей среды. Хотя измерительное устройство может иметь различные конфигурации и может быть расположено в любом месте вдоль внутренней части 10а, включая внутри корпуса 30 инъекционного ввода, в показанном варианте выполнения измерительное устройство выполнено в виде датчика давления, который расположен внутри корпуса 60 датчика, расположенного вблизи корпуса 30 инъекционного ввода. Катетер 50 может включать первую часть, которая соединена между желудочным бандажом 20 и корпусом 60 датчика, и вторую часть, которая соединена между корпусом 60 датчика и корпусом 30 инъекционного ввода.
Дополнительно к измерению давления текучей среды внутри внутренней части 10а, можно также измерять давление текучей среды внутри кишечника и/или желудка 40 с использованием любого подходящего устройства, такого как эндоскопный манометр. В качестве не имеющего ограничительного характера примера, такие измерения давления текучей среды можно сравнивать с давлением текучей среды внутри внутренней части 10а, измеренным перед, во время или после регулирования давления внутри внутренней части 10а. Другие подходящие использования измеренного внутри кишечника и/или желудка 40 давления понятны для специалистов в данной области техники.
Как показано дополнительно на фиг.1А, наружная часть 10b включает в основном считывающее давление устройство 70, которое предназначено для расположения на поверхности кожи над корпусом 60 датчика (который может быть имплантирован под толстой тканью, например, толщиной свыше 10 см) для неинвазивной связи с корпусом 60 датчика и получения тем самым результатов измерения давления. Считывающее давление устройство 70 может быть, не обязательно, электрически соединено (в этом варианте выполнения через узел 80 электрического кабеля) с управляющим блоком 90, который может отображать измеренные давления или другие данные, полученные из считывающего давление устройства 70.
На фиг.1В показана более подробно имплантируемая часть 10а. В показанном варианте выполнения имплантируемая часть 10а включает регулируемый желудочный бандаж 20, корпус 30 инъекционного ввода, который соединен по текучей среде с регулируемым желудочным бандажом 20, корпус 60 датчика и насос 110. В показанном на фиг.1В варианте выполнения насос 110 содержится в основном внутри корпуса 112 насоса.
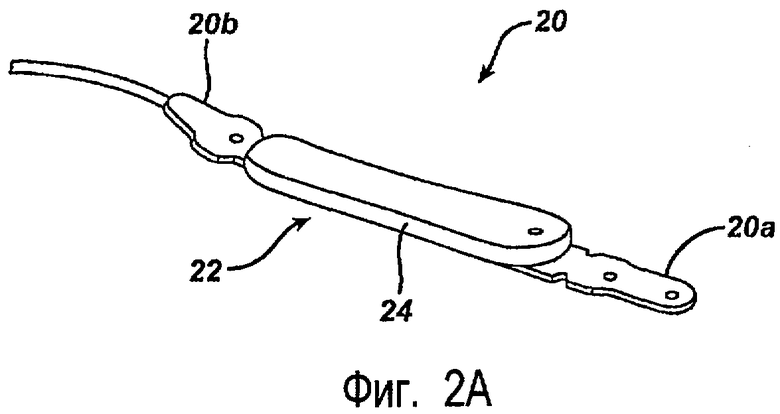
На фиг.2А детально показан желудочный бандаж 20. Хотя желудочный бандаж 20 может иметь различные конфигурации, и в данном изобретении можно использовать различные желудочные бандажи, известные в настоящее время в уровне техники, в показанном варианте выполнения желудочный бандаж 20 имеет в основном удлиненную форму с опорной структурой 22, имеющей первый и второй противоположные концы 20а, 20b, которые можно скреплять друг с другом. Можно использовать различные технологии сопряжения для скрепления концов 20а, 20b друг с другом. В показанном варианте выполнения концы 20А, 20b выполнены в виде лент, которые соединяются при наложении друг на друга. Желудочный бандаж 20 может также включать элемент с изменяемым объемом, такой как надуваемый баллон 24, который расположен или образован на одной стороне опорной структуры 22 и предназначен для расположения вблизи ткани. Баллон 24 может расширяться и сокращаться к наружной стенке желудка с образованием регулируемого отверстия для контролируемого ограничения прохода пищи в желудок.
Для специалистов в данной области техники понятно, что желудочный бандаж может иметь различные конфигурации, более того, что различные способы и устройства, согласно изобретению, одинаково применимы к другим типам имплантируемых бандажей. Например, бандажи используются для лечения недержания фекалий, как описано в патенте США № 6461292, полное содержание которого включается в данное описание. Бандажи можно также использовать для лечения недержания мочи, как описано в заявке на патент США № 2003/0105385, полное содержание которой включается в данное описание. Бандажи можно также использовать для лечения изжоги и/или кислотного рефлюкса, как раскрыто в патенте США № 6470 892, полное содержание которого включается в данное описание. Бандажи можно также использовать для лечения импотенции, как описано в заявке на патент США № 2003/0114729, полное содержание которой включается в данное описание.
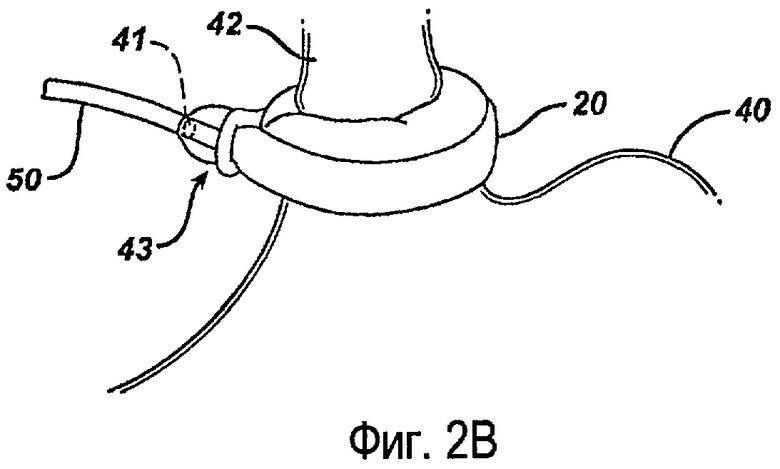
На фиг.2В показан регулируемый желудочный бандаж 20, нанесенный поверх желудочно-кишечного соединения пациента. Как показано на фигуре, бандаж 20 охватывает, по меньшей мере, верхнюю часть желудка вблизи с соединением с кишечником 42. После имплантации бандажа 20 предпочтительно в плоской конфигурации, в которой бандаж содержит мало текучей среды или не содержит ее, бандаж 20 можно надувать, например, с использованием соляного раствора, для уменьшения размера отверстия стомы. Для специалистов в данной области техники понятно, что можно использовать различные технологии, включая механические и электрические технологии, для регулирования бандажа. На фиг.2В показано альтернативное расположение датчика 41 давления, который расположен в стяжке 43 бандажа 20.
Корпус 30 инъекционного ввода текучей среды может также иметь различные конфигурации. В показанном на фиг.3 варианте выполнения корпус 30 инъекционного ввода текучей среды имеет в основном цилиндрическую форму, при этом дальняя или нижняя поверхность и периферийная стенка проходят от нижней поверхности и задают ближнее отверстие 32. Ближнее отверстие 32 может включать проницаемую для иглы перегородку, проходящую поперек и обеспечивающую доступ к резервуару текучей среды (не виден на фиг.3), образованному внутри корпуса. Перегородка 34 предпочтительно расположена в достаточно близком положении, так что глубина резервуара достаточна для размещения открытой вершины иглы, такой как игла Хубера, так что можно осуществлять передачу текучей среды. Перегородка 34 предпочтительно выполнена так, что она самостоятельно герметизируется после прокалывания иглой и удаления иглы. Как показано на фиг.3, ввод 30 может дополнительно включать соединительный элемент 36 в виде катетерной трубки, который соединен по текучей среде с резервуаром и предназначен для соединения с катетером (например, катетером 50). Для специалистов в данной области техники понятно, что корпус может быть выполнен из различных материалов, включая нержавеющую сталь, титан или полимерные материалы, и перегородка 34 аналогичным образом может быть выполнена из различных материалов, включая силикон.
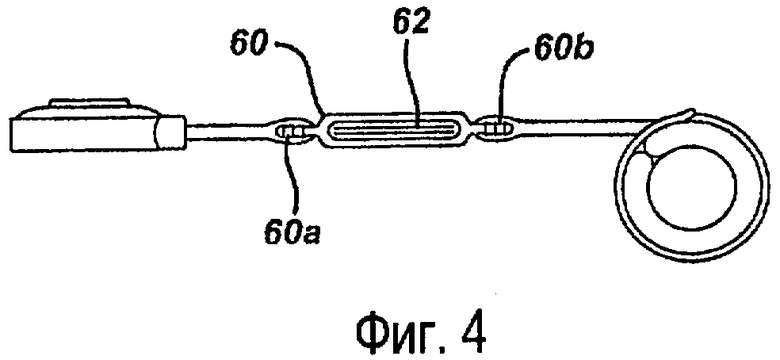
Как указывалось выше, система 10 может также включать устройство измерения давления, соединенное с замкнутым контуром текучей среды и предназначенное для измерения давления (например, давления текучей среды), которое соответствует количеству ограничения, приложенного с помощью регулируемого желудочного бандажа 20 к желудку 40 пациента. Измерение давления позволяет человеку (например, врачу, сестре, пациенту) оценивать эффективность и функции ограничения, созданного посредством регулирования бандажа. В показанном на фиг.4 варианте выполнения устройство измерения давления выполнено в виде датчика 62 давления, расположенного внутри корпуса 60 датчика. Однако устройство измерения давления может быть расположено в любом месте внутри закрытого гидравлического контура, и различные примеры расположения и конфигурации подробно раскрыты в публикации США № 2006/0211913 с названием «Неинвазивное измерение давления в регулируемом ограничивающем устройстве с текучей средой» от 7 марта 2006 г., полное содержание которой включается в данное описание.
В целом, показанный корпус 60 датчика включает вход 60а и выход 60b, которые соединены с возможностью прохождения текучей среды с имплантируемой частью 10а. Уже имплантированный катетер 50 можно снабжать корпусом 60 датчика посредством разрезания катетера 50 и введения шиповидных соединителей (или любых других соединителей, таких как зажимы, клипсы, клей, сварка и т.д.) в разрезанные концы катетера 50. Датчик 62 может быть расположен внутри корпуса 60 и предназначен для реагирования на изменения давления текучей среды внутри гидравлического контура и преобразования изменений давления в пригодную для использования форму данных. Датчик 62 давления, расположенный внутри корпуса 60, может осуществлять измерение и мониторинг регулированного состояния бандажа статично или во время нагнетания текучей среды.
Хотя это и не показано, система измерения давления может также включать микроконтроллер, ТЕТ/катушку телеметрии и конденсатор. Не обязательно, система измерения давления может дополнительно включать датчик температуры (не изображен). Микроконтроллер, ТЕТ/катушка телеметрии и конденсатор могут быть соединены друг с другом через печатную плату (не изображена) или любые другие подходящие компоненты. Понятно, что ТЕТ/катушка телеметрии и конденсатор могут совместно образовывать настроенный контур для приема энергии из наружной части и передачи измеренного давления в устройство считывания давления.
Можно использовать различные датчики давления, известные из уровня техники, такие как беспроводные датчики давления, предлагаемые фирмой CardioMEMS, Inc. of Atlanta, Georgia, хотя подходящие датчики MEMS можно получать из любого другого источника, включая, но не ограничиваясь этим, фирмы Integrating Sensing Systems (ISSYS) и Remon Medical. Пример выполнения датчика давления MEMS описан в патенте США № 6855115, полное содержание которого включается в данное описание лишь в качестве иллюстрации. Понятно также, что подходящие датчики давления могут включать, но не ограничиваясь этим, емкостные, пьезоэлектрические, силиконовые или ультразвуковые (акустические) датчики давления, а также различные другие устройства, способные измерять давление.
Считывающее давление устройство 70 может также иметь различные конфигурации, и пример выполнения считывающего давление устройства подробно раскрыт в публикациях заявок на патент США № 2006/0189888 и 2006/0199997, полное содержание каждой из которых включается в данное описание. В целом, считывающее давление устройство 70 обеспечивает возможность неивазивного измерения давления текучей среды внутри имплантированной части, даже когда корпус 30 инъекционного ввода или корпус 60 датчика имплантирован под толстым слоем (по меньшей мере, свыше 10 см) подкожной жировой ткани. Врач может прикладывать считывающее давление устройство 70 к коже пациента вблизи места расположения датчика и наблюдать считываемое давление на дисплее управляющего блока 90. Считывающее давление устройство 70 можно также съемно закреплять на пациенте, например, во время длительного наблюдения, с использованием поясов, клея и других хорошо известных способов. Считывающее давление устройство 70 может работать через обычную ткань или хирургические бумажные повязки и может также включать снимаемое покрытие (не изображено), которое можно заменять для каждого пациента.
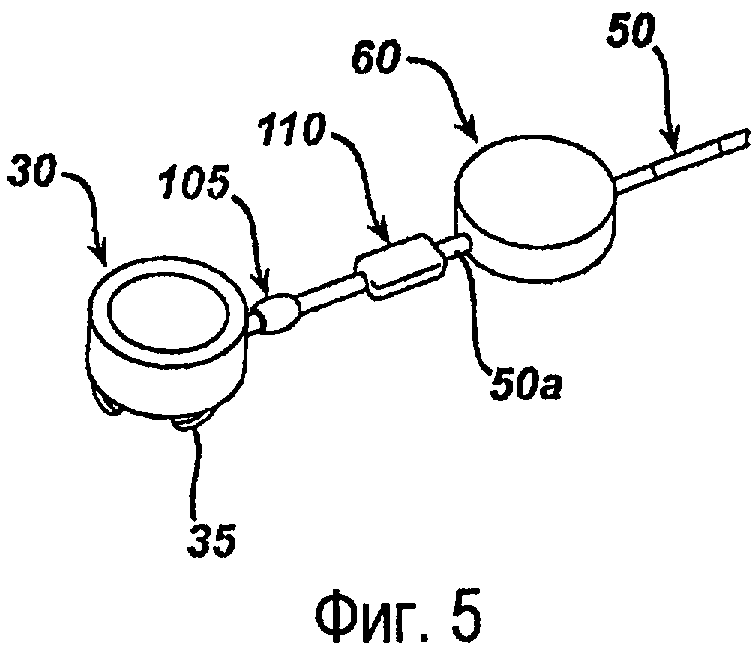
На фиг.5 показан вариант выполнения ближнего конца имплантируемой части 10а (смотри фиг.1А и 1В) имплантируемой ограничивающей системы 10. Как показано на фигуре, ближний конец имплантируемой части 10а включает корпус 30 инъекционного ввода, который соединен по текучей среде с резервуаром 105 и насосом 110. Ближний конец может также включать корпус 60 датчика, а также один или несколько проводников 101 для датчика/электропитания. Канал 50а обеспечивает соединение по текучей среде между отдельными компонентами ближнего конца имплантируемой части 10а. Катетер 50 обеспечивает соединение по текучей среде между ближним концом имплантируемой части 10а, показанной на фиг.5, и нижним по потоку ограничивающим устройством 20 (смотри фиг.1В). Хотя компоненты показаны на фиг.5 в линейной конфигурации, для специалистов в данной области техники понятно, что компоненты могут быть соединены в любой другой последовательности и конфигурации, например, в Т-образной или Y-образной конфигурации.
Как показано на фиг.5, корпус 30 инъекционного ввода, если он имеется, может, не обязательно, включать крепежное устройство, такое как крючки 35, которые можно использовать для крепления корпуса 30 инъекционного ввода внутри тела пациента. Хотя на фиг.5 показано, что корпус 30 расположен на линии с резервуаром 105, насосом 110 и корпусом 60 датчика, корпус 30 может быть соединен с другими компонентами и каналом 50а по-другому, например, в Т-образной или Y-образной конфигурации. Сам корпус 30 инъекционного ввода является не обязательным, поскольку имплантируемую ограничивающую систему 10 (смотри фиг.1В) можно заполнять текучей средой перед имплантацией или во время имплантации. Давление в нижнем по потоку ограничивающем устройстве 20 (смотри фиг.1В) затем можно регулировать с использованием насоса 110 для перемещения текучей среды в ограничивающее устройство 20 или из него.
Резервуар 105 обеспечивает не обязательное средство для удерживания дополнительного запаса текучей среды. Например, резервуар 105 может содержать 0,1-20 мл текучей среды. Как показано на фигуре, резервуар 105 может быть частью канала 50а с большим диаметром, чем номинальный диаметр канала 50а. Можно использовать различные другие конфигурации для создания резервуара 105, такие как отдельные компоненты резервуара, соединенные с возможностью прохождения текучей среды с каналом 50а или любыми другими компонентами, т.е. корпусом 30 инъекционного ввода, насосом 110 или корпусом 60 датчика. Хотя на фиг.5 показано, что резервуар 105 расположен между насосом 110 и корпусом 60 инъекционного ввода, для специалистов в данной области техники понятно, что резервуар 105 может быть соединен с другими компонентами и каналом 50а по-другому, например, в Т-образной или Y-образной конфигурации. Понятно также, что резервуар 105 не обязательно должен содержать достаточно текучей среды для заполнения или опустошения всего бандажа 20 (смотри фиг.1А и 1В). Например, во время первого заполнения бандажа 20 текучая среда может подаваться с помощью инъекции через корпус 30 инъекционного ввода. В это время насос 110 можно удерживать в открытом положении. В качестве альтернативного решения, можно заполнять резервуар 105, а затем текучая среда может подаваться в бандаж 20 с помощью насоса 110. При достаточном заполнении бандажа 20, т.е. при достаточном закрывании желудка для ограничения прохождения, резервуар 105 можно заполнять достаточным количеством текучей среды для выполнения будущих потребностей заполнения и регулирования без необходимости добавления текучей среды через корпус 30 инъекционного ввода. Для специалистов в данной области техники понятно, что резервуар 105 не является обязательным, и в варианте выполнения без резервуара 105 (не изображен), канал 50а может, не обязательно, содержать достаточно текучей среды для обеспечения возможности регулирования количества текучей среды в бандаже 20.
Показанный на фиг.5 вариант выполнения содержит, не обязательно, корпус 60 датчика, который находится в соединении по текучей среде с компонентами ближнего конца имплантируемой части 10а (смотри фиг.1В). Хотя на фиг.5 показано, что корпус 60 датчика расположен в линию с катетером 50 и каналом 50а, для специалистов в данной области техники понятно, что датчик 60 может быть соединен с другими компонентами по-другому, например, в Т-образной или Y-образной конфигурации. В качестве альтернативного решения, датчик может быть расположен в других местах в системе, например, на самом бандаже. Проводники 101 датчика/электропитания могут обеспечивать соединение между корпусом 60 датчика и насосом 110 для подачи электропитания в насос, как будет подробно описано ниже.
Имплантируемый насос 110 имеет функцию перемещения текучей среды в бандаж 20 и из него для увеличения или уменьшения давления по потребности внутри бандажа. Хотя насос может иметь различные конструкции, в одном примере выполнения насос основан на технологии микро-электромеханических систем (MEMS), как будет подробно пояснено ниже. В целом, технология MEMS характеризуется использованием элементов субмиллиметрового размера. Использование технологии MEMS для образования имплантируемого насоса 110 обеспечивает несколько преимуществ, таких как небольшой размер, требуемое низкое напряжение и простота относительно количества движущихся частей. Дополнительные преимущества включают небольшую стоимость изготовления, улучшенные рабочие характеристики, высокую точность, быстрое время реагирования и конфигурации, которые не достижимы в большем масштабе.
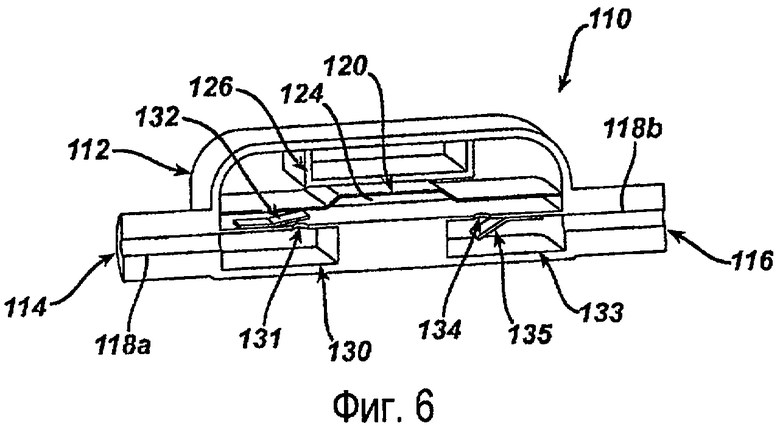
На фиг.6 показан пример выполнения насоса MEMS. Как показано на фигуре, насос 110 содержится в целом внутри корпуса 112 насоса, имеющего ближний конец 114 и дальний конец 116, каждый из которых включает внутренний просвет 118а, 118b. Внутренние просветы 118а, 118b соединены с возможностью прохождения текучей среды с компонентами ближнего конца имплантируемой части 10а (смотри фиг.1В). Корпус 112 насоса может быть, не обязательно, выполнен в виде единого целого с каналом 50а (смотри фиг.5), так что насос 110 соединен по текучей среде с катетером 50 и нижним по потоку ограничивающим бандажом 20. Как показано на фигуре, насос 110 может включать электрод 126 вблизи насосной мембраны 122, расположенной в соединении по текучей среде с камерой 124 для текучей среды. Насос 110 может также включать входную камеру 130 и выходную камеру 133. Входная камера 130 может быть соединена по текучей среде с камерой 124 для текучей среды через входное отверстие 131. Аналогичным образом, выходная камера 133 может быть соединена по текучей среде с камерой 124 для текучей среды через выходное отверстие 134. Насос может также включать впускной клапан 132 и выпускной клапан 135. При использовании, как будет подробно пояснено ниже, мембрана 122 предназначена для отклонения в ответ на приложение напряжения к электроду 126, за счет чего создается разница давления между камерой 124 текучей среды и входной камерой 130 и/или выходной камерой. Корпус 112 насоса может иметь различные конфигурации, однако в показанном примере выполнения он выполнен в линию с каналом 50а. Форма и размер корпуса 112 насоса, а также материалы, используемые для выполнения корпуса 112 и его внутренних компонентов, могут изменяться в зависимости от планируемого использования. Устройства MEMS обычно выполняются из силикона, однако могут также выполняться из полимеров, металлов или сплавов с памятью формы. В определенных примерах выполнения корпус 112 насоса может быть выполнен из биосовместимого полимера, такого как силикон или латекс. Другие подходящие биосовместимые эластомеры и полимеры включают, но не ограничиваясь этим, синтетический полиизопрен, хлоропрен, фторэластомер, нитрил, фторсиликон, поливинилидендифторид (PVDF) и жидкокристаллический полимер (LCP).
Для специалистов в данной области техники понятно, что материалы можно выбирать для получения желаемых механических свойств. Хотя это и не изображено, корпус 112 может также включать другие признаки для облегчения его крепления к медицинскому устройству, источнику текучей среды и т.д.
Для специалистов в данной области техники понятно, что микро-насосное устройство для текучей среды может быть образовано из двух слоев эластомерного материала. Один слой содержит каналы для протекающей текучей среды (т.е. поточный слой), в то время как другой слой (например, управляющий слой) содержит каналы, которые отклоняют мембранный клапан в поточный канал и останавливают поток жидкости при сдавливании с помощью воздуха/текучей среды. Для специалистов в данной области техники понятно, что клапаны могут быть включены в матрицу MEMS.
Насос 110 может быть выполнен в различных конфигурациях. В показанном варианте выполнения корпус 112 насоса включает ряд камер для текучей среды. Основная камера 124 для текучей среды образована внутри корпуса 112 насоса и соединена по текучей среде с насосной мембраной 120. Кроме того, основная камера 124 для текучей среды соединена по текучей среде с входной камерой 130 и выходной камерой 133 через входное отверстие 131 и выходное отверстие 134. Входная камера 130 и выходная камера 133 отделены от основной камеры 124 для текучей среды с помощью впускного клапана 132 и выпускного клапана 135. Клапаны могут иметь различные конфигурации. В показанном варианте выполнения впускной клапан 132 и выпускной клапан 135 выполнены в виде плоских пружин, которые напряжены в закрытом положении, т.е. напряжены в положении, предотвращающем поток текучей среды через отверстия 131 и 134. Впускной клапан 132 может быть расположен внутри основной камеры 124 текучей среды и обеспечивает прохождение текучей среды из входной камеры 130 в основную камеру 124 для текучей среды. Выпускной клапан 135 может быть расположен внутри выходной камеры 133 и обеспечивает прохождение текучей среды из основной камеры 124 в выходную камеру 133. Для специалистов в данной области техники понятно, что места расположения впускного клапана 132 и выпускного клапана 135 взаимозаменяемы. Для специалистов в данной области техники также понятно, что входная камера 130 и выходная камера 133 могут быть не обязательными, одна или обе. Например, один или оба внутренних просветов 118а, 118b могут быть соединены непосредственно с основной камерой 124 для текучей среды. В такой конфигурации впускной клапан 132 и/или выпускной клапан 135 может быть выполнен, например, внутри внутренних просветов 118а и 118b. Как указывалось выше, элементы насоса 110, включая клапаны 135, 135, могут быть выполнены в субмиллиметровом масштабе.
Насосная мембрана 120 может быть также выполнена в различных конфигурациях. В показанном варианте выполнения насосная мембрана 120 расположена внутри корпуса 112 и соединена по текучей среде с основной камерой 124 для текучей среды. Насосная мембрана 120 может быть выполнена из подходящего биосовместимого полимера или металла, который реагирует на электрическое поле, создаваемое при приложении напряжения к электроду 126. Электрод 126 может также иметь различные конфигурации. В показанном варианте выполнения электрод 126 образован внутри корпуса 112 насоса и расположен вблизи насосной мембраны 120. Для специалистов в данной области техники понятно, что электрод 126 может быть расположен в любом месте. Например, электрод 126 может быть расположен в нижней поверхности насосной камеры 124. Для специалистов в данной области техники также понятно, что электрод 126 должен быть выполнен из стойкого к коррозии материала, такого как платина или другие благородные металлы, для обеспечения стойкости к агрессивным текучим средам, таким как соляной раствор.
Одним из преимуществ использования технологии MEMS для выполнения насоса является небольшой габаритный размер и обеспечиваемые небольшие регулирования объема. Например, наибольший размер всего насоса может быть меньше примерно 5 мм, включая управляющую электронику. Хотя насос можно выполнять для получения любого желаемого расхода, расход может быть очень небольшим и составлять 0,1-0,5 мл/мин. Полное изменение объема, требуемое для необходимого регулирования давления, может обеспечиваться при работе насоса с таким расходом. Например, полный объем, подаваемый в бандаж 20, может быть меньше 1 мл для заданного желаемого регулирования.
Как показано на фигуре, электрод 126 расположен вблизи насосной мембраны 120. Положением насосной мембраны 120 можно управлять с помощью напряжения, прикладываемого к электроду 126. Для специалистов в данной области техники понятно, что напряжение может изменяться в зависимости от различных факторов, как будет пояснено ниже, и обычно находится в диапазоне от примерно 2 до примерно 200 В. Напряжение, прикладываемое к электроду, может зависеть от нескольких факторов, таких как, например, скорость переключения, необходимые для переключения или отклонения силы, и надежность устройства MEMS. Например, для более высокой скорости переключения приблизительно 25 мкс может быть необходимо напряжение приблизительно 10-15 В, в то время как для более низких скоростей переключения обычно требуется напряжение меньше приблизительно 5 В. В альтернативном примере выполнения можно использовать высоковольтные электростатические исполнительные механизмы, для которых требуется напряжение в диапазоне приблизительно 10-300 В. Электрод 126 может быть соединен с батареей или другим источником энергии. Когда насос 110 предназначен для имплантации внутри пациента, электрод 126 может быть соединен с трансформатором, который предназначен для имплантации под кожу и выполнен с возможностью хранения энергии и/или приема энергии из внешнего источника, расположенного вне тела пациента. Например, трансформатор или источник энергии может быть расположен в корпусе 60 датчика, и проводники датчика/электропитания (не изображены) могут подавать энергию к электроду 126. В качестве альтернативного решения, энергия может подаваться с помощью внешнего устройства (например, считывающего устройства 70, показанного на фиг.1А), которое может подавать энергию через кожу в корпус 60 датчика (смотри фиг.5), например, когда внешнее устройство перемещается близко к корпусу 60 датчика. Внешнее устройство может быть мобильным (например, настенным или удерживаемым в руке устройством, которое можно качать или другим образом размещать вблизи корпуса 60 датчика), или стационарным (например, установленным у постели, на столе или на тележке, которую пациент может придвигать ближе).
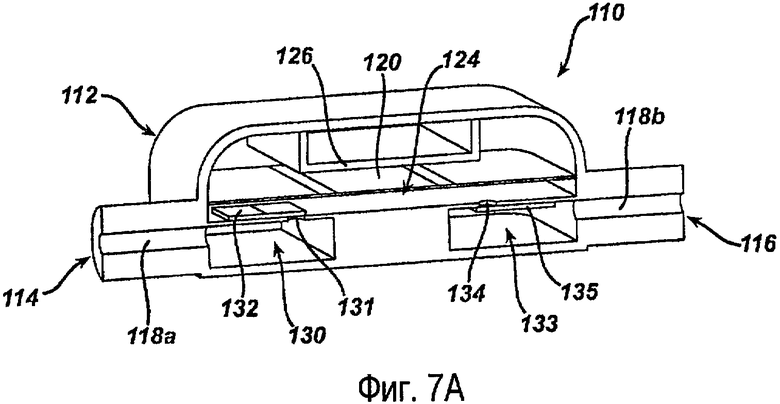
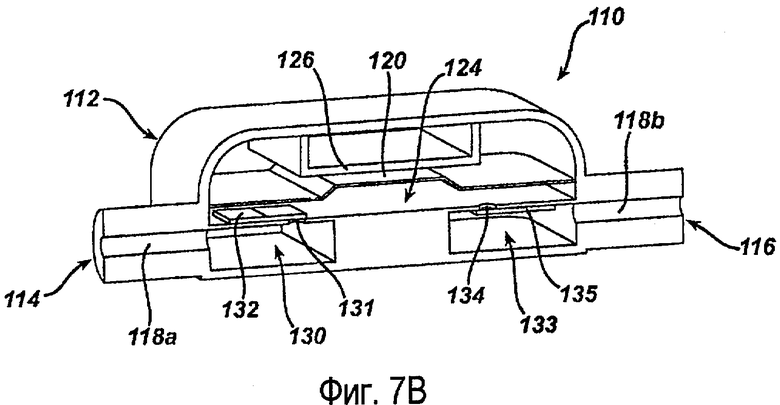
На фиг.7А-7D иллюстрирован в качестве примера способ создания разницы давления внутри насоса 110 для перемещения текучей среды через насос 120. В одном примере выполнения насос перемещает текучую среду в дальнем направлении к бандажу (смотри фиг.1В), который расположен вдали от насоса 110. На фиг.7А насос 110 показан в исходном положении, в котором насосная мембрана 120 по существу не отклонена, и впускной клапан 132 и выпускной клапан 135 закрыты. При приложении напряжения к электроду 126 насосная мембрана 120 отклоняется и притягивается к электроду 126, насколько позволяют свойства материала, как показано на фиг.7В. В качестве альтернативного решения, жесткий упор (не изображен) ограничивает перемещение мембраны 120 для точного управления ее движением. Для специалистов в данной области техники понятно, что когда электрод 126 расположен в других местах, как указывалось выше, насосная мембрана может, наоборот, отталкиваться от электрода.
Увеличение объема в основной камере 124 для текучей среды вызывает падение давления относительно давления во входной и выходной камерах 130, 133. Как показано на фиг.7С, перепад давления между входной камерой 130 и основной камерой 124 для текучей среды приводит к открыванию впускного клапана 132, что позволяет текучей среде проходить в основную камеру 124 для текучей среды, пока не будет выровнено давление. В течение этого времени разница давления между основной камерой 124 и выходной камерой 133 вынуждает выпускной клапан 135 оставаться закрытым. После заполнения текучей средой из входной камеры 130 основной камеры 124 напряжение, приложенное к электроду 126, уменьшается, что позволяет насосной мембране 120 вернуться в исходное положение. Уменьшение объема в основной камере 124 для текучей среды в результате перемещения насосной мембраны 120 обратно в свое исходное положение вызывает подъем давления в основной камере 124 относительно давления во входной и выходной камерах 130, 133. Как показано на фиг.7D, разница давления между основной камерой 124 и выходной камерой 135 вызывает открывание выпускного клапана 135, что позволяет текучей среде перемещаться в выходную камеру 133, пока не будет выровнено давление. В течение этого времени разница давления между основной камерой 124 и входной камерой 130 вынуждает впускной клапан 132 оставаться закрытым. Процесс, показанный на фиг.7А-7D, можно при необходимости повторять для продолжения нагнетательного действия.
На фиг.8 показан путь 150 прохождения текучей среды через насос 110. В показанном варианте выполнения насос перемещает текучую среду в дальнем направлении к бандажу (смотри фиг.1В), который расположен вдали от насоса 110. Текучая среда движется из внутреннего просвета 118а на ближнем конце 114 насоса 110 во входную камеру 130 и через впускной клапан 132 в основную камеру 124 для текучей среды. Затем текучая среда проходит через выпускной клапан 135 в выходную камеру 133 и через внутренний просвет 118b дальнего конца 116 насоса 110. Для специалистов в данной области техники понятно, что расположение камер для текучей среды и клапанов может быть при необходимости модифицировано для обеспечения возможности прохождения текучей среды в ближнем направлении от бандажа (смотри фиг.1В). Например, поскольку бандаж является стороной высокого давления системы, можно просто открывать возвратный клапан для выхода текучей среды из бандажа. В качестве альтернативного решения, второй насос MEMS может быть ориентирован в противоположном первому насосу направлении для нагнетания текучей среды от бандажа.
Данное изобретение предлагает также способ регулирования давления в системе 10 с имплантируемым ограничивающим устройством. В одном варианте выполнения способ может включать измерение клинически релевантного параметра и регулирование давления внутри ограничивающего устройства в ответ на измерение клинически релевантного параметра посредством приведения в действие насоса, соединенного по текучей среде с ограничивающим устройством 20. Насос на основе MEMS может быть насосом типа, описанного применительно к фиг.6-8. То есть насос может быть микро-электромеханическим устройством, способным создавать нагнетательное действие для движения текучей среды через насос. Клинически релевантный параметр можно измерять с использованием имплантируемого датчика.
В одном варианте выполнения клинически релевантным параметром является давление, хотя понятно, что он может включать любой из указанных выше других параметров, а также другие клинически релевантные параметры. В этом варианте выполнения можно измерять давление с использованием имплантируемого датчика 62 давления, как указывалось выше. Способ может включать измерение давления в имплантированном ограничивающем устройстве 10а, сравнение измеренного давления с желаемым давлением (включая диапазон желаемого давления) и регулирование давления внутри ограничивающего устройства 10а для его примерного равенства с желаемым давлением (или диапазоном желаемого давления), если измеренное давление не равно желаемому давлению (или диапазону желаемого давления), посредством приведения в действие насоса, соединенного по текучей среде с ограничивающим устройством 20, с целью достижения желаемого давления (или диапазона желаемого давления) в ограничивающем устройстве.
В одном варианте выполнения приведение в действие насоса 110 осуществляется автоматически, если измеренный клинически релевантный параметр (например, давление и т.д.) в бандаже 20 выше желаемой величины или диапазона, в этом случае текучая среда выкачивается из бандажа 20 для уменьшения давления. И наоборот, если измеренный параметр в бандаже 20 меньше желаемой величины или диапазона, то текучая среда нагнетается в бандаж (например, из резервуара или имплантированного катетера), пока не будет достигнут желаемый параметр. В еще одном варианте выполнения, если измеренный клинически релевантный параметр (например, абсолютное давление в течение заданного времени, градиент давления и т.д.) в бандаже 20 соответствует не желательным привычкам принятия пищи, то текучая среда нагнетается в бандаж (например, из резервуара или из имплантированного катетера), пока не будет создано достаточное ограничение. Ограничение обеспечивает обратную связь с пациентом (которая может быть мгновенной или замедленной) на прекращение приема пищи посредством вызывания физиологического ответа (например, рвоты и т.д.). Ограничение удерживается до появления запускающего события (например, проходящего времени) для возврата системы в нормальное рабочее состояние. С целью безопасности может быть предусмотрена отмена, которая может быть активирована пациентом или другим обслуживающим лицом. Эту отмену можно приводить в действие с помощью функции в наружной части 10b системы 10 ограничения приема пищи. Можно использовать другие технологии для автоматического приведения в действие, такие как управление с помощью таймера, или же система может быть запрограммирована на включение насоса в ответ на некоторые измеренные параметры или события или в соответствии с программируемым расписанием. Например, имплантируемый насос может вызывать увеличение давления внутри ограничивающего устройства (т.е. перемещать текучую среду к ограничивающему устройству), когда пациент должен принимать пищу, или же когда пациент не спит (или во время избранного времени в течение дня), и вызывать уменьшение давления внутри ограничивающего устройства (т.е. перемещать текучую среду от ограничивающего устройства), когда пациент спит (или во время других выбранных часов в течение дня). Для специалистов в данной области техники понятно, что можно использовать программируемое расписание в зависимости от множества факторов, включая тип дня (праздники, рабочие дни, суббота и воскресенье), ожидаемую деятельность пациента и т.п. Для специалистов в данной области техники понятно, что давлением в бандаже 20 можно управлять с использованием методов замкнутого контура, таких как схемы управления PID (линейно-интегральные-дифференциальные) или других подходящих методов, включая цифровые схемы управления.
Для специалистов в данной области техники понятно, что в конструкцию насоса могут быть встроены определенные элементы безопасности для обеспечения дополнительных возможностей в случае неправильной работы или потери энергии. Например, если обнаруживается отсутствие энергии (или неправильная работа), или же остающаяся энергия падает ниже заданного предельного значения, то система может быть выполнена с возможностью возврата в свободное состояние, в котором ограничение снято и/или открыто, пока не будет восстановлен уровень энергии или устранены неполадки.
Раскрытые здесь устройства могут быть предназначены для выбрасывания после единственного применения или для многократного применения. Однако в любом случае устройство может быть восстановлено для повторного использования после, по меньшей мере, одного применения. Восстановление может включать любую комбинацию стадий разборки устройства с последующей очисткой или заменой отдельных частей и последующей сборки. В частности, устройство можно разбирать, и любое количество отдельных деталей или частей можно избирательно заменять или удалять в любой комбинации. После очистки и/или замены конкретных частей устройство можно снова собирать для последующего использования в месте восстановления, или же командой хирургов непосредственно перед хирургической операцией. Для специалистов в данной области техники понятно, что при восстановлении устройства можно использовать различные технологии для разборки, чистки/замены и повторной сборки. Использование таких технологий и получаемое восстановленное устройство входят все в объем данной заявки.
Указанное устройство предпочтительно обрабатывают перед хирургической операцией. Сначала получают новую или использованную систему и при необходимости очищают. Затем систему можно стерилизовать с помощью любой известной и подходящей технологии, включая стерилизацию оксидом этилена. Согласно одной технологии стерилизации, систему помещают в закрытый и герметизированный контейнер, такой как пластмассовый или TYVEK пакет. Затем контейнер и систему помещают в поле радиации, которая может пронизывать контейнер, такой как гамма-излучение, рентгеновское излучение или электроны высокой энергии. Излучение убивает бактерии на системе и в контейнере. Затем стерилизованную систему хранят в стерильном контейнере. Герметизированный контейнер сохраняет систему стерильной до его открывания в медицинском учреждении.
Предпочтительно, устройство стерилизуют. Это осуществляется с помощью известных для специалистов в данной области техники способов, включая бета- или гамма-излучение, оксид этилена, пар.
Для специалистов в данной области техники понятны другие признаки и преимущества изобретения на основе указанных выше вариантов выполнения. В соответствии с этим, изобретение не ограничивается вышеприведенным описанием и чертежами, если это не указано в прилагаемой формуле изобретения. Полное содержание указанных публикаций и ссылок включается в данное описание.
| название | год | авторы | номер документа |
|---|---|---|---|
| АВТОМАТИЧЕСКИ РЕГУЛИРУЮЩАЯСЯ БАНДАЖНАЯ СИСТЕМА | 2009 |
|
RU2493784C2 |
| СПОСОБЫ И УСТРОЙСТВА ДЛЯ ФИКСИРОВАНИЯ ОРИЕНТАЦИИ АНТЕННЫ В ОГРАНИЧИТЕЛЬНОЙ СИСТЕМЕ | 2009 |
|
RU2506050C2 |
| СИСТЕМА И СПОСОБ СТЕРИЛИЗАЦИИ ИМПЛАНТИРУЕМОГО МЕДИЦИНСКОГО УСТРОЙСТВА | 2009 |
|
RU2497483C2 |
| АНАЛИЗ ДАННЫХ ДЛЯ ИМПЛАНТИРУЕМОГО ОГРАНИЧИВАЮЩЕГО УСТРОЙСТВА И УСТРОЙСТВА РЕГИСТРАЦИИ ДАННЫХ | 2009 |
|
RU2502460C2 |
| УСТРОЙСТВО ДЛЯ НЕИНВАЗИВНОГО ИЗМЕРЕНИЯ ДАВЛЕНИЯ ТЕКУЧЕЙ СРЕДЫ В РЕГУЛИРУЕМОМ СУЖАЮЩЕМ УСТРОЙСТВЕ | 2006 |
|
RU2430687C2 |
| ЭНЕРГОСНАБЖЕНИЕ ИМПЛАНТИРУЕМЫХ СИСТЕМ ОГРАНИЧЕНИЯ С ПРИМЕНЕНИЕМ ТЕМПЕРАТУРЫ | 2009 |
|
RU2495646C2 |
| АНАЛИЗ ФИЗИОЛОГИЧЕСКИХ ПАРАМЕТРОВ ДЛЯ ИМПЛАНТИРУЕМОГО УСТРОЙСТВА ОГРАНИЧЕНИЯ И РЕГИСТРИРУЮЩЕГО УСТРОЙСТВА | 2009 |
|
RU2501519C2 |
| ДИСТАНЦИОННЫЙ МОНИТОРИНГ И РЕГУЛИРОВКА УСТРОЙСТВА ОГРАНИЧЕНИЯ ПОТРЕБЛЕНИЯ ПИЩИ | 2006 |
|
RU2456918C2 |
| УПРАВЛЕНИЕ ДАВЛЕНИЕМ В РЕГУЛИРУЕМЫХ ОГРАНИЧИТЕЛЬНЫХ УСТРОЙСТВАХ | 2009 |
|
RU2499564C2 |
| ПОРТ ДЛЯ ПОДКОЖНЫХ ИНЪЕКЦИЙ СО СТАБИЛИЗИРУЮЩИМИ ЭЛЕМЕНТАМИ | 2006 |
|
RU2428221C2 |


Группа изобретений относится к медицине. Медицинская ограничивающая система содержит: имплантируемое ограничивающее устройство, которое является регулируемым и предназначено для образования ограничения в пациенте; и имплантируемый микроэлектромеханический насос, соединенный с возможностью прохождения текучей среды с ограничивающим устройством. Система выполнена с возможностью возврата при отсутствии энергии или падения энергии ниже заданного предельного значения в состояние, в котором ограничение является по меньшей мере одним из свободного или открытого состояния. Раскрыто имплантируемое медицинское устройство, выполненное с использованием имплантируемого микроэлектромеханического насоса. Изобретения обеспечивают снижение размеров имплантируемого оборудования. 2. н. и ф-лы, 11 з.п. ф-лы, 8 ил.
1. Медицинская ограничивающая система для образования ограничения в пациенте, содержащая:
имплантируемое ограничивающее устройство, которое является регулируемым и предназначено для образования ограничения в пациенте; и
имплантируемый микроэлектромеханический (MEMS) насос, соединенный с возможностью прохождения текучей среды с ограничивающим устройством;
при этом система выполнена с возможностью возврата при отсутствии энергии или падения энергии ниже заданного предельного значения в состояние, в котором ограничение является по меньшей мере одним из свободного или открытого состояния.
2. Система по п.1, дополнительно содержащая имплантируемый ввод, выполненный с возможностью приема текучей среды из источника текучей среды снаружи пациента, при этом имплантируемый ввод соединен по текучей среде с имплантируемыми ограничивающим устройством и насосом.
3. Система по п.1, дополнительно содержащая имплантируемый датчик, соединенный с ограничивающим устройством.
4. Система по п.3, в которой имплантируемый датчик предназначен для измерения, по меньшей мере, давления внутри ограничивающего устройства.
5. Система по п.1, в которой насос MEMS дополнительно содержит:
корпус насоса;
камеру для текучей среды, расположенную внутри корпуса и имеющую впускной клапан, расположенный между камерой для текучей среды и входной камерой, и выпускной клапан, расположенный между камерой для текучей среды и выходной камерой;
насосную мембрану, соединенную по текучей среде с камерой для текучей среды; и
электрод вблизи насосной мембраны,
при этом насосная мембрана предназначена для отклонения в ответ на приложение напряжения к электроду с образованием разницы давления между камерой для текучей среды и входной и выходной камерами для управления потоком текучей среды через насос.
6. Система по п.5, в которой впускной и выпускной клапаны предназначены для открывания и закрывания в ответ на изменения давления в камере для текучей среды.
7. Система по п.5, в которой текучая среда движется в направлении от насоса MEMS к ограничивающему устройству.
8. Система по п.5, в которой текучая среда движется в направлении от ограничивающего устройства к насосу MEMS.
9. Система по п.1, в которой имплантируемый насос вызывает изменение давления внутри ограничивающего устройства в соответствии, по меньшей мере, с одним из обнаруживаемого события или программируемого расписания.
10. Система по п.1, дополнительно содержащая резервуар для текучей среды, соединенный по текучей среде с насосом MEMS.
11. Система по п.10, в которой резервуар для текучей среды предназначен для удерживания текучей среды в диапазоне приблизительно 0,1-20 мл.
12. Система по п.1, в которой насос служит в качестве клапана, который способен избирательно управлять прохождением текучей среды посредством разрешения, предотвращения или ограничения прохождения текучей среды.
13. Имплантируемое медицинское устройство, содержащее:
имплантируемый микроэлектромеханический (MEMS) насос, соединенный по текучей среде с источником текучей среды и объектом для текучей среды, при этом насос MEMS предназначен для избирательной транспортировки текучей среды между источником текучей среды и объектом для текучей среды,
при этом насос снабжен элементами безопасности для обеспечения возврата медицинской ограничивающей системы при отсутствии энергии или падении энергии ниже заданного предельного значения в состояние, в котором ограничение является по меньшей мере одним из свободного или открытого состояния.
| US 2007265645, 15.11.2007 | |||
| WO 2007030750 А1, 15.03.2007 | |||
| US 2007025868 A1, 01.02.2007 | |||
| US 2006189878 A1, 24.08.2006 | |||
| БАНДАЖНОЕ УСТРОЙСТВО ДЛЯ ЖЕЛУДКА | 2000 |
|
RU2255712C2 |
Авторы
Даты
2014-02-10—Публикация
2009-02-11—Подача