Изобретение относится к новым биологически активным химическим соединениям, относящимся к классу бисфосфонатов (полифосфонатам), обладающим высокой противоопухолевой активностью, которые могут применяться в медицине и ветеринарии для лечения раковых заболеваний и профилактики метастазирования опухолей, в том числе и для опухолей с поражением костной ткани.
Онкологические заболевания являются одними из наиболее тяжелых и опасных заболеваний человека, они являются одной из основных причин смерти человека в современном мире. Для достижения максимального эффекта лечения раковых заболеваний используется совокупность различных подходов. Как правило, применяют хирургический метод удаления опухоли с последующим лечением химиопрепаратами и лучевой терапией. Однако сложность лечения обусловлена большим количеством разнообразных опухолей человека, метастазированием и устойчивостью многих опухолей к химиопрепаратам и лучевой терапии. В последние годы для лечения онкологических заболеваний стали апробировать такие новые подходы, как фотодинамическая терапия, онколитические вирусы, иммунотерапия с помощью антител и иммунных клеток, генная терапия и вакцинация раковыми антигенами. В экспериментах на животных получены весьма обнадеживающие результаты эксперименты, но они также позволили сделать главный вывод - лечение опухоли должно быть строго индивидуальным, что обусловливает необходимость подбора конкретного вида(ов) и метода(ов) лечения.
Сегодня известно много различных химиопрепаратов для лечения онкологических заболеваний. Однако их количество и главное качество полностью не покрывают потребности борьбы с раковыми заболеваниями и требуют создания новых противоопухолевых препаратов.
Предшествующий уровень техники
Одним из перспективных противораковых препаратов является золедроновая кислота, относящаяся к полифосфонатам (В.Г.Иванов, В.Ф.Семиглазов, В.В.Семиглазов, P.M.Палтуев, П.В.Криворотько, А.А.Малодушева, С.С.Гурбанов, Р.В.Донских. Бисфосфонаты в клинической онкологии: использование у больных солидными опухолями // Медицинский журнал: Фарматека. - М.: Бионика, 2007. - №18. - С.23-28), широко используемая для лечения онкологических заболеваний костей. Препарат выпускается под наименованиями «Резорба», «Zometa», «Zomera», «Aclasta», «Reclast». Его противораковая активность достаточно хорошо изучена. Известно медицинское средство на основе бисфосфонатов или аминоглюконатов в виде солей для предотвращения и лечения остеопороза, остеоартрита, рака, гиперкальцинемии, многократной миеломы (патент Китая № CN 1475218, МПК A61K 31/7008, опубл. 18.02.2004). Известно применение бисфосфоната при приготовлении лекарственного средства для лечения остеобластических метастазов, связанных с раком предстательной железы. Вводимый в составе лекарственного средства бисфосфонат используют в дополнение к противоопухолевой терапии.
Известны также некоторые другие бисфосфонаты, нашедшие применение в медицинской практике. Например, такие соединения, как памидроновая, алендроновая, ризедроновая, тилудроновая, клодроновая кислоты и некоторые их фармацевтически приемлемые соли. Некоторые бисфосфонаты включают также имидазольную, оксазольную, изооксазольную, оксадиазольную, тиазольную, тиадиазольную, пиридиновую, 1,2,3-триазольную, 1,2,4-триазольную или бензимидазольную группу и т.д.
Бисфосфонаты также широко используются для подавления активности остеокласта при различных доброкачественных и злокачественных заболеваниях, которые вызывают чрезмерную или несоответствующую резорбцию кости. Сравнительно недавно их стали использовать для лечения метастазов в костной ткани и при множественной миеломе (см. Fleisch H, 1997, Bisphosphonates clinical. In Bisphosphonates in Bone Disease. From the Laboratory to the Patient. Eds: The Parthenon Publishing Group, New York/London, pp.68-163).
Наиболее близким аналогом изобретения является фармацевтический продукт на основе бисфосфонатов, например, в форме готового к использованию раствора золедроновой кислоты (формула I) или ее фармацевтически приемлемой соли (патент РФ №2358739, МПК A61K 31/663, опубл. 20.06.2009 г.).
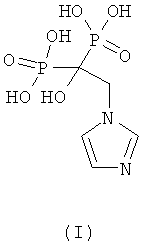
Однако вышеуказанные аналоги имеют следующие недостатки: часто они имеют сложную многостадийную технологию получения, что в конечном итоге повышает стоимость препаратов. Кроме того, в инструкциях по применению препаратов на основе золедровой кислоты содержится предупреждение относительно их почечной токсичности. Управление по контролю качества пищевых продуктов и лекарственных препаратов (Министерство здравоохранения, США) обязало производителей золедроновой кислоты писать в аннотации, что этот препарат повышает риск почечной недостаточности. В соответствии с предупреждением золедроновая кислота также может привести к тяжелому обезвоживанию пациентов. Рекомендуется проведение мониторинга уровня креатинина в крови для оценки состояния почек пациента.
Другим важным обстоятельством является то, что опыт использования различных противоопухолевых препаратов показывает: (а) необходимость использования комбинации нескольких препаратов для повышения эффективности лечения опухоли; (б) существование опухолей, устойчивых к действию одного препарата, что требует использования нескольких различных химиопрепаратов в зависимости от тактики лечения; (в) индивидуальная переносимость пациентом химиопрепарата также может варьировать в очень широких пределах. Это является одним из существенных недостатков существующих химиопрепаратов. Преодолеть этот недостаток возможно только через создание новых высокоэффективных противоопухолевых препаратов для комплексной химиотерапии раковых заболеваний.
Техническим результатом предлагаемого изобретения является получение нового химического соединения, имеющего технологию получения с использованием доступных реагентов, обладающего высоким индексом селективности (способность уничтожать раковые клетки, не затрагивая при этом клетки с нормальным фенотипом) и выраженным противораковым действием в отношении различных видов опухолей человека и животных.
Технический результат достигается созданием нового биологически активного органического соединения - тетраэтил-2-(2,2,6,6-тетраметилпиперидин-4-иламино)-этилен-1,1-бисфосфоната, формула II:
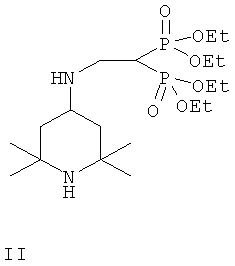
проявляющего противоопухолевую активность в отношении различных видов опухолей человека и животных, которое может найти применение в медицинской практике в качестве препарата для лечения онкологических заболеваний.
Соединение II получают взаимодействием 4-амино-2,2,6,6-тетраметилпиперидина с тетраэтил-этен-1,1-диилбис(фосфонатом), взятыми в соотношении 1:1, без растворителя в течение 10 часов по следующей схеме:
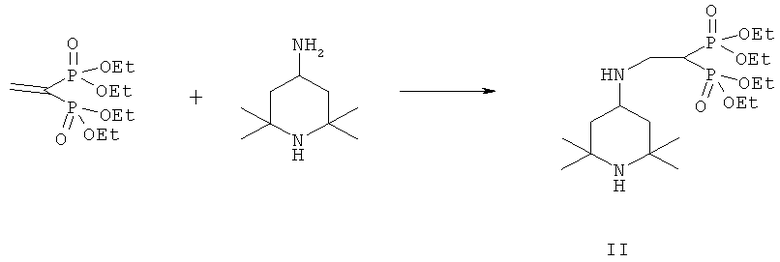
Сопоставительный анализ с аналогами показывает, что заявляемое соединение принципиально отличается от аналога [патент РФ №2358739] тем, что содержит в молекуле тетраметилпиперидиновую структуру, находящуюся в непосредственной близости от бис(фосфонатной) части.
Пример 1. Получение тетраэтил-2-(2,2,6,6-тетраметилпиперидин-4-иламино)-этилен-1,1-бисфосфоната (II). К 180 мг (0,6 ммоль) тетраэтил-этен-1,1-диилбис(фосфоната) прибавляется 94 мг (0,6 ммоль) 4-амино-2,2,6,6-тетраметилпиперидина. Через 12 часов наблюдается полное отсутствие исходных реагентов (контроль по 1Н ЯМР). Очистка с использованием колоночной хроматографии (SiO2, CHCl3:МеОН 18:1, Rf=0.8). Жидкость. Выход: 85%. Найдено, %: C 49.75, H 9.36, N 6.10, P 13,38. C19H42N2O6P2. Вычислено, %: C 49.99, H 9.27, N 6.14, P 13.57.
ИК (KBr, см-1): 975.8, 1024.0, 1099.2, 1164.8, 1249.7, 1392.4, 1444.4, 1479.2, 1643.1, 2875.4, 2908.2, 2935.2, 2985.3
1Н ЯМР (400 МГц, CDCl3, δ м.д.): 0.84 (АВд, 2H, J=11.6 Гц, 12.7 Гц, 2*CH2 акс); 1.10 (с, 6H, 2*СН3); 1.18 (с, 6Н, 2*CH3); 1.34 (т, 12Н, J=7 Гц, 4*СН3); 1.82 (АВд, 2Н, J=3.6 Гц, 12.7 Гц, 2*CH2, экв); 2.58 (тт, 1H, J=6 Гц, 23.5 Гц, P-CH-P); 2.90 (тт, 1Н, J=3.6 Гц, 11.6 Гц, CH-NH); 3.19 (дт, 2Н, J=6 Гц, 17 Гц, CH2-NH); 4.12-4.22 (м, 8H, 4*СН2). 13С ЯМР (100 МГц, CDCl3, δ м.д.): 16.25 (дд, J=2.4 Гц, 6.3 Гц, 4*CH3, Et); 28.47 (2*CH3); 34.87 (2*CH3); 37.71 (т, J=132 Гц, P-CH-P); 42.33 (т, J=4 Гц, NH-CH2); 45.63 (2*CH2); 49.02 (CH-NH); 50.78 (2*CMe2); 62.52 (дд, J=6,7 Гц, 33.5 Гц, 4*CH2, Et).
Способ получения заявляемого вещества прост в исполнении (реализуется в одну стадию), исходные вещества доступны, выход составляет 85% от теоретически рассчитанного. Предлагаемое соединение устойчиво на воздухе, легко растворимо в хлороформе, диметилформамиде и диметилсульфоксиде, мало растворимо в воде. Хорошо растворяется в воде при небольшом подкислении.
Пример 2. Исследование противоопухолевой активности заявляемого соединения.
Использовали культуры опухолевых клеток А431 (клетки эпидермоидной карциномы человека), SW480 (клетки аденокарциномы толстой кишки человека), RD (рабдомиосаркома человека), Mel-8 (меланома человека) и нормальную диплоидную культуру MRC-5 (клетки легочного эпителия эмбриона человека). Клетки культивировали в среде Игла ДМЕМ (Gibco BRL), содержащей 5-10% эмбриональной сыворотки теленка (Gibco BRL), 2 мМ L-глютамина, 80 мкг/мл гентамицина сульфата при 37°C в культуральных пластиковых флаконах (Costar, США). Для снятия клеток с субстрата применяли 0.25%-ный раствор трипсина и 0.02-ный раствор версена (ФГУН ГНЦ ВБ «Вектор») в соотношении 1:1.
Определение противоопухолевой (цитотоксической) активности соединений in vitro (МТТ-тест). МТТ-тест выполняли по методике, описанной в [Niks M and Otto M. (1990) Towards an optimized MTT assay. J. Immunol. Meth. 130 (1), 149-151]. Клетки А431, SW480, MRC-5 в концентрации 5×104 в 100 мкл среды Игла ДМЕМ, содержащей 10% эмбриональной сыворотки теленка, помещали в лунки 96-луночных культуральных микропланшет и инкубировали 24 ч при 37°C в атмосфере, содержащей 5% CO2. Затем в лунки добавляли по 50 мкл растворенных в DMSO исследуемых соединений и их трехкратных разведений. В контрольные лунки вносили трехкратные разведения DMSO на культуральной среде. Каждая экспериментальная точка выполнялась в трех повторах (три лунки на каждое разведение соответствующего соединения и контроля). После чего культуральные микропланшеты инкубировали 48 ч, 96 ч и 168 ч при вышеуказанных условиях. Затем в соответствующих культуральных микропланшетах содержащую исследуемые соединения среду удаляли, в лунки добавляли 200 мкл среды без сыворотки и вносили 10 мкл раствора MTT (исходная концентрация 5 мг/мл в фосфатном буфере) и дополнительно инкубировали микропланшеты в течение 6 часов. По окончании инкубации среду удаляли и добавляли по 150 мкл DMSO для растворения образовавшихся в результате реакции синих кристаллов формазана. Оптическую плотность растворенного в DMSO формазана измеряли на микропланшетном спектрофотометре Multiscan при длине волны 492 нМ. 50% цитотоксическую концентрацию (CC50) рассчитывали согласно [Niks M and Otto M. (1990) Towards an optimized MTT assay. J. Immunol. Meth. 130 (1), 149-151].
Противоопухолевая (цитотоксическая) активность в отношении опухолевых и нормальных диплоидных клеток человека представлены в таблице 1. Значения CC50 (мкг/мл) приведены с учетом ориентировочной растворимости исследуемых соединений в DMSO. Культуру клеток MRC-5 использовали в качестве контрольных нормальных клеток с целью определения возможной избирательности цитотоксического воздействия исследуемых соединений в отношении опухолевых клеток. Степень избирательности цитотоксичности выражали через индекс селективности (ИС), представляющий собой отношение CC50 исследуемого соединения для клеток нормального фенотипа к TC50 (токсическая концентрация) для опухолевых клеток. Достаточно высокая противоопухолевая активность показана для заявляемого соединения (II) и его аналога (I). Цитоксичность этих соединений для опухолевых культур клеток варьирует в диапазоне значений CC50 от 0.4 до 31 мкг/мл и сравнима с цитоксической активностью коммерчески выпускаемого противоопухолевого препарата эмбихин (CC50 для клеток А431-3 мкг/мл.
Для заявляемого соединения (II) обнаружена избирательность цитотоксичности сразу для двух используемых опухолевых клеточных культур А431 и SW-480 с индексом селективности 5,9 и 9,1 соответственно. Индексы селективности используемых в настоящее время противоопухолевых хемотерапевтических средств обычно не превышают 4-8 [Ring C.J. (2002) Cytolytic viruses as potential anti-cancer agents. J. of Gen. Virol., 83, 491-502]. Обращает на себя внимание тот факт, что соединение (I) (аналог) проявляло свою цитотоксическую активность на более поздние сроки инкубации (96 и 168 ч) только в отношении одного типа клеток А431 при наличии высокого индекса селективности только при инкубации 168 часов, тогда как заявляемое соединение (II) было эффективно в течение всего периода наблюдения, то есть проявляло выраженную противопухолевую активность уже через 48 часов инкубирования.
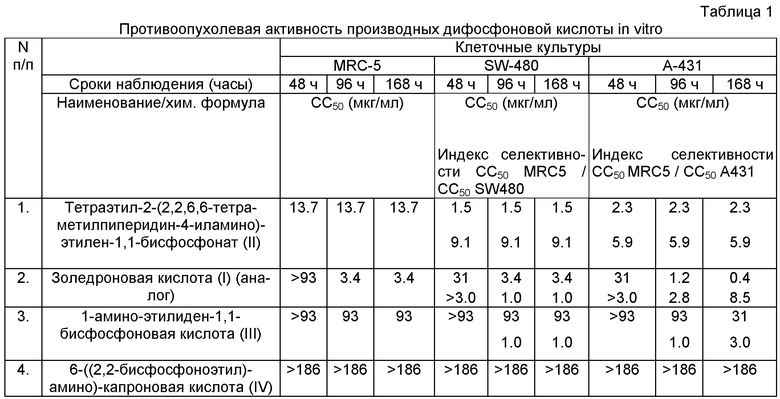
Примечание: Исследуемые соединения (III) и (IV) были синтезированы заявителями и использовались как соединения сравнения, не проявляющие значимой цитотоксичности в отношении исследованных культур клеток (отрицательный контроль).
Цитотоксичность соединения (II) дополнительно исследовали с использованием опухолевых культур человека: MCF-7 (рак молочной железы), RD, Mel-8 и одной культуры клеток человека нормального фенотипа - MCF-10A. Соединение (II) также обладает избирательной цитотоксичностью к опухолевым клеткам RD и Mel-8 по отношению к обеим нормальным клеточным культурам (ИС от 2.2 для MRC5/RD и Mel-8 до 11.1 для MCF-10A/SW480).
Таким образом, технический результат изобретения подтверждается тем, что заявляемое соединение, формула II, проявляет высокую противоопухолевую активность по отношению к раковым клеткам человека А431, SW-480, RD, Mel-8 при индексе селективности от 2,2 до 11,1.
Пример 3. Оценка противоопухолевого действия заявляемого препарата (II) для мышей линии C57BL/6 с привитой опухолью мышиной легочной карциномы Льюиса CRL-1642 LLC.
Исследование проводили согласно методологии, изложенной в работе [Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ. / Под ред Р.У.Хабриева, М.: 2005]. Культуру клеток мышиной легочной карциномы Льюиса CRL-1642 LLC культивировали как монослойную в среде Игла ДМЕМ - F12 (Gibco BRL), содержащей 5-10% эмбриональной сыворотки теленка (Gibco BRL), 2 мМ L-глютамина, 80 мкг/мл гентамицина сульфата при 37°C в культуральных пластиковых флаконах (Costar, США). Привитие опухолевых клеток осуществляли посредством подкожного введения 107 клеток CRL-1642 LLC в 0.2 мл среды ДМЕМ - F12 самкам мышей линии C57BL/6 весом 16-18 г. Обработку мышей C57BL/6 исследуемым соединением (II) проводили двукратно посредством внутрибрюшинного введения 0.2 мл раствора соединения (II) в физиологическом растворе: первая инъекция через сутки после введения опухолевых клеток, вторая через 13 суток. Тетраэтил-2-(2,2,6,6-тетраметилпиперидин-4-иламино)-этилен-1,1-бисфосфонат (II) вводился в дозе 1.0 мг на мышь на инъекцию. Выбор дозы соединения (II) обусловлен его токсичностью для мышей C57BL/6 и был определен в предварительных экспериментах. В качестве препарата сравнения использовали циклофосфамид. Циклофосфамид (аналог) является широко используемым фармакопейным высокоэффективным противоопухолевым препаратом, выпускаемым также под торговыми марками Endoxan, Cytoxan, Neosar, Procytox, Revimmune, Циклофосфан (Takimoto C.H., Calvo E. "Principles of Oncologic Pharmacotherapy" in Pazdur R., Wagman L.D., Camphausen K.A., Hoskins WJ. (Eds) Cancer Management: A Multidisciplinary Approach. 11 ed. 2008). Препарат в течение длительного времени широко используется для лечения людей. Циклофосфамид обладает широким спектром противоопухолевой активности против мелкоклеточного рака легкого, рака яичников, рака молочной железы, рака шейки и тела матки, рака мочевого пузыря, рака предстательной железы, нейробластомы, ретинобластомы, лимфогранулематоза, лимфосаркомы, неходжкинских лимфом, ретикулосаркомы, остеогенной саркомы, множественной миеломы, хронических лимфо- и миелолейкозов, острых лимфо-, миело- и монобластных лейкозов, а также ряда микозов и аутоиммунных заболеваний.
Циклофосфамид вводили по вышеуказанной схеме в дозе 1.0 мг/мышь. Группе контрольных мышей с привитыми опухолями вводили 0.2 мл PBS на инъекцию. Каждая группа состояла из 10 животных. Прогрессию опухолей оценивали визуально и посредством измерения на 21 и 32 сутки после привития. Объем опухолей определяли следующим образом: максимальная длина опухоли, умноженная на ее ширину в квадрате, деленная на два. Для каждой группы животных рассчитывали среднюю продолжительность жизни (СПЖ).
Уровень токсичности заявляемого соединения (II) и ффективного химиотерапевтического противоракового препарата сравнения (циклофосфамид) для мышей определяли при однократном внутрибрюшинном введении. Токсичность выражали через ЛД50 (50% летальная доза). ЛД50 для исследуемых соединений составили:
>5.0 мг/мышь для тетраэтил-2-(2,2,6,6-тетраметилпиперидин-4-иламино)-этилен-1,1-бисфосфоната (заявляемое соединение);
>5.0 мг/мышь для циклофосфамида.
Результаты оценки противоопухолевой активности соединения (II) представлены в таблице 2. Отмечена 100%-ная эффективность привития саркомы Льюиса, сопровождающаяся различной степенью прогрессии привитых опухолей у опытных и контрольной групп животных. На момент первого измерения объемов опухолей (21 сутки после привития опухолей, 20 сутки после первого введения и 7 сутки после второго введения исследуемых соединений) наблюдался выраженный ингибирующий эффект в группах животных, обработанных циклофосфамидом и тетраэтил-2-(2,2,6,6-тетраметил-пиперидин-4-иламино)-этилен-1,1-бисфосфонатом (II). Причем максимальный эффект на этот срок отмечался в группе животных после лечения циклофосфамидом. Так, средний объем опухолей в группе циклофосфамидом составил 0.26 мл, а в группе тетраэтил-2-(2,2,6,6-тетраметилпиперидин-4-иламино)-этилен-1,1-бисфосфоната (II) - 0.92 мл и 2.47 мл в контрольной группе. На момент второго измерения объемов опухолей (32 сутки после привития опухолей, 31 сутки после первого введения и 18 сутки после второго введения исследуемых соединений) существенное ингибирование прогрессии опухолей отмечено в группах животных получивших бисфосфонат (II) и циклофосфамид. У животных после введения заявляемого соединения (II) на этот срок эффект несколько более выражен, чем у получавших циклофосфамид: средний объем опухолей 2.70 мл и 3.22 мл соответственно против 6.05 мл в контрольной группе мышей. С этими данными хорошо согласуются результаты определения средней продолжительности жизни в группах животных: увеличение СПЖ по отношению к контрольной группе животных приблизительно на 25 процентов (8 суток) в группе заявляемого соединения (II) и на 15% (5 суток) в группе животных, получавших циклофосфамид.
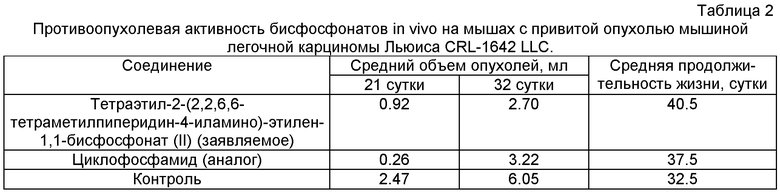
Возможно, что изменение схемы терапии с учетом особенностей фармакодинамики и фармакокинетики заявляемого соединения позволит добиться более выраженного ингибирования роста опухолей, что будет сопровождаться существенным увеличением средней продолжительности жизни.
На мышиной модели показано, что тетраэтил-2-(2,2,6,6-тетраметилпиперидин-4-иламино)-этилен-1,1-бисфосфонат (II) (заявляемое соединение) обладает выраженной противоопухолевой активностью, которая характеризуется снижением размера опухоли, существенным увеличением средней продолжительности жизни животных. По своей противоопухолевой активности заявляемое соединение превосходит активность высокоактивного фармакопейного противоракового препарата циклофосфамид.
Таким образом, технический результат изобретения подтверждается тем, что заявляемый препарат обладает выраженной противоопухолевой активностью по отношению к различным опухолевым клеточным культурам человека, таким как - А431, SW-480, RD, Mel-8, при индексе селективности от 2,2 до 11,1. Заявляемый препарат способен оказывать значительное противоопухолевое действие при лечении мышей с привитой опухолью мышиной легочной карциномы Льюиса CRL-1642 LLC. В экспериментах на животных он обеспечивает снижение размеров опухоли и существенное увеличение продолжительности жизни животных.
| название | год | авторы | номер документа |
|---|---|---|---|
| N-[3-ОКСОЛУП-20(29)-ЕН-28-ОИЛ]-2,2,6,6-ТЕТРАМЕТИЛПИПЕРИДИН-4-ИЛАМИН, ОБЛАДАЮЩИЙ ЦИТОТОКСИЧЕСКОЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ ОПУХОЛЕВЫХ КЛЕТОК ЧЕЛОВЕКА | 2017 |
|
RU2641900C1 |
| Пептид, обладающий противоопухолевой и антиметастатической активностью, и готовая лекарственная форма на его основе | 2018 |
|
RU2682039C1 |
| УНИВЕРСАЛЬНЫЙ ПРОМОТОР ДЛЯ ЭКСПРЕССИИ ТЕРАПЕВТИЧЕСКИХ ГЕНОВ В КЛЕТКАХ МЛЕКОПИТАЮЩИХ | 2013 |
|
RU2551784C1 |
| Противоопухолевое средство | 2015 |
|
RU2609871C1 |
| СПОСОБ ПОЛУЧЕНИЯ СИСТЕМЫ НАПРАВЛЕННОЙ ДОСТАВКИ БЕЛКОВЫХ МОЛЕКУЛ (ОНКОЛИТИЧЕСКИХ БЕЛКОВ) В ОПУХОЛЕВЫЕ ТКАНИ НА ОСНОВЕ АКТИВИРОВАННЫХ ЛИМФОЦИТОВ | 2013 |
|
RU2552609C1 |
| Натрий-кобальт-полигалактуронат, обладающий противоопухолевой активностью | 2023 |
|
RU2794885C1 |
| Титановый имплантат с функцией локальной иммунотерапии для остеореконструктивной хирургии и профилактики местного рецидива онкологического заболевания и способ его изготовления | 2021 |
|
RU2779367C1 |
| Фторсодержащие бензилированные изатины, обладающие противоопухолевой активностью | 2022 |
|
RU2802016C1 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК pAd5-f, НЕСУЩАЯ ФРАГМЕНТ ГЕНОМА АДЕНОВИРУСА 5 ТИПА С ДЕЛЕЦИЕЙ В ГЕНЕ E1B-55K, И ШТАММ МУТАНТНОГО АДЕНОВИРУСА Ade12, ОБЛАДАЮЩИЙ СЕЛЕКТИВНОЙ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2001 |
|
RU2194755C2 |
| Противоопухолевое средство на основе рекомбинантного штамма вируса осповакцины и способ его получения | 2019 |
|
RU2730657C1 |
Изобретение относится к противоопухолевому соединению формулы
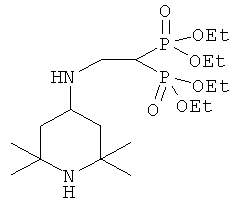
Предложено новое противоопухолевое соединение, обладающее высоким индексом селективности по отношению к раковым клеткам в сравнении с клетками нормального фенотипа и выраженным противоопухолевым действием в отношении опухолей человека и животных, которое может применяться в медицине и ветеринарии для лечения раковых заболеваний и профилактики метастазирования опухолей, в том числе с поражением костной ткани. 2 пр., 2 табл.
Тетраэтил-2-(2,2,6,6-тетраметилпиперидин-4-иламино)-этилен-1,1-бисфосфонат следующей формулы:
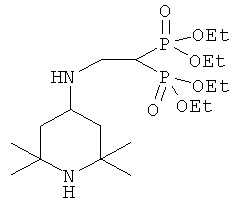
обладающий противоопухолевой активностью по отношению к опухолям человека и животных in vitro и in vivo.
| ФАРМАЦЕВТИЧЕСКИЕ ПРОДУКТЫ, СОДЕРЖАЩИЕ БИФОСФОНАТЫ | 2004 |
|
RU2358739C2 |
| CN 1475218 A, 18.02.2004 | |||
| ТИОЗАМЕЩЕННЫЕ ПИРИДИНИЛБИСФОСФОНОВЫЕ КИСЛОТЫ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ ИЛИ ЭФИРЫ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБ ЛЕЧЕНИЯ | 1993 |
|
RU2124019C1 |
Авторы
Даты
2014-02-10—Публикация
2013-01-30—Подача