Предлагаемое изобретение относится к органической химии, конкретно к способу селективного получения 3,3′-[метиленбис(1,4-фенилен)]-, 3,3′-[оксибис(1,4-фенилен)]- и 3,3′-(3,3′-диметоксибифенил-4,4′-диил)-бис-1,5,3-дитиазепинанов общей формулы (1):
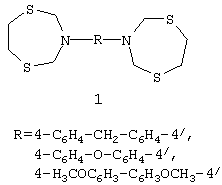
Азот и серусодержащие гетероциклы известны как антибактериальные, антигрибковые и антивирусные агенты (Stillings М.R., Welbourn А.P., Walter D.J. Substituted 1,3,4-thiadiazoles with anticonvulsant activity // Med. Chem. 1986, 29, 2280; Kidwai M., Negi N., Chaudhary S.R. Cyclothiomethylation of arge hydrazines with formaldehyde // Acta Pharma, 1995, 45, 511; Тюкавкина H.А., Зурабян С.Э., Белобородов В.Л. и др. Органическая химия. М.: Дрофа, 2008, 66). Они перспективны в качестве катализаторов, биологически активных комплексообразователей, селективных сорбентов и экстрагентов драгоценных металлов [Deutsche Gold- und Silber-Scheideanstalt vormals Roessler. F.P. 1,341,792/1963 (Chem. Abs., 1964, 60, 5528d)], специальных реагентов для подавления жизнедеятельности бактерий в различных технических средах (от легкой промышленности до нефти) (Джемилев У.М., Алеев Р.С, Дальнова Ю.С., Кунакова Р.В., Хафизова С.Р., Ковтуненко С.В., Калимуллин А.А., Андрианов В.М., Исмагилов Ф.Р., Гафиатуллин Р.Р. Средство для подавления роста сульфатвосстанавливающих бактерий. Патент РФ №2160233, 2000; Джемилев У.М., Алеев Р.С., Дальнова Ю.С., Кунакова Р.В., Хафизова С.Р. Средство для подавления роста сульфатвосстанавливающих бактерий. Патент РФ №2206726, 2003).
Известен способ (Патент РФ №2333910; Б.И., 2008, №26) получения 5-(2-[5-{2-[1,3,5-дитиазинан-5-ил]этил}-4-метил-1,3,5-тиадиазинан-3-ил]-этил}1,3,5-дитиазинана (2) взаимодействием метилтриэтилтетрамина с насыщенным сероводородом водным раствором формальдегида, взятых в мольном соотношении метилтриэтилтетрамин: формальдегид: сероводород, равном 1:6:4, при температуре 20°C с выходом 63.5%.
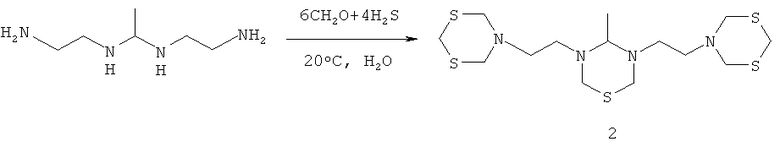
Известным способом не могут быть получены 3,3′-[метиленбис(1,4-фенилен)]-, 3,3′-[оксибис(1,4-фенилен)]- и 3,3′-(3,3′-диметоксибифенил-4,4′-диил)-бис-1,5,3-дитиазепинаны общей формулы (1).
Известен способ [Fr. Pat. 1,341, 792/1963 (Chem. Abs., 1964, 60, 5528d)] получения производных бис-1,3,5-дитиазинана, в частности 5-[2-[1,3,5-дитиазинан-5-ил]этил]1,3,5-дитиазинана (3), взаимодействием гидросульфида натрия (NaHS) с этилендиамином и формальдегидом по схеме:
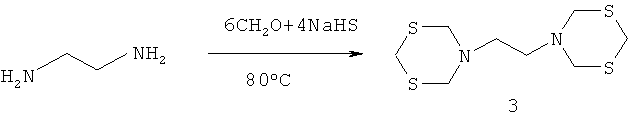
Известный способ не позволяет получать 3,3'-[метиленбис(1,4-фенилен)]-, 3,3′-[оксибис(1,4-фенилен)]- и 3,3′-(3,3′-диметоксибифенил-4,4′-диил)-бис-1,5,3-дитиазепинаны общей формулы (1).
Известен способ (С.Р.Хафизова, В.Р.Ахметова, Л.Ф.Коржова, Т.В.Хакимова, Г.Р.Надыргулова, Р.В.Кунакова, Э.А.Круглов, У.М.Джемилев. Многокомпонентная конденсация алифатических аминов с формальдегидом и сероводородом // Изв. АН. Сер. хим., 2005, 2, 423) получения 5-[2-[1,3,5-дитиазинан-5-ил]этил]1,3,5-дитиазинана (3) трехкомпонентной конденсацией сероводорода с формальдегидом и этилендиамином, взятых в мольном соотношении 1:6:4, соответственно, при температуре 80°C с выходом 44%.
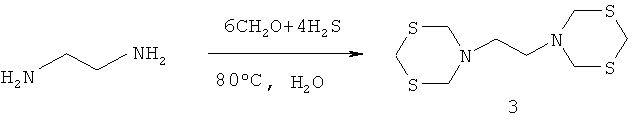
Известный способ не технологичен, так как предполагает применение газообразного и чрезвычайно токсичного сероводорода, который при высокой концентрации не имеет запаха, но даже однократное его вдыхание может вызвать мгновенную смерть. Кроме того, известным способом не могут быть получены 3,3′-[метиленбис(1,4-фенилен)]-, 3,3′-[оксибис(1,4-фенилен)]- и 3,3′-(3,3′-диметоксибифенил-4,4′-диил)-бис-1,5,3-дитиазепинаны общей формулы (1).
Таким образом, в литературе отсутствуют сведения о селективном получении 3,3′-[метиленбис(1,4-фенилен)]-, 3,3′-[оксибис(1,4-фенилен)]- и 3,3′-(3,3′-диметоксибифенил-4,4′-диил)-бис-1,5,3-дитиазепинанов общей формулы (1).
Предлагается новый способ получения 3,3′-[метиленбис(1,4-фенилен)]-, 3,3′-[оксибис(1,4-фенилен)]- и 3,3′-(3,3′-диметоксибифенил-4,4′-диил)-бис-1,5,3-дитиазепинанов общей формулы (1).
Сущность способа заключается во взаимодействии ариламина общей формулы H2N-R-NH2, где R=4-С6Н4-СН2-C6H4-4′, 4-С6Н4-O-С6Н4-4′, 4-H3COC6H3-C6H3OCH3-4′ (диаминодифенилметан, диаминодифенилоксид или диметоксибензидин) с N-трет-бутил-дитиазепинаном в среде аргона в присутствии катализатора Sm(NO3)3·6H2O при мольном соотношении ариламин:N-трет-бутил-1,5,3-дитиазепинан:Sm(NO3)3·6H2O=10:20:(0.3-0.7), предпочтительно 10:20:0.5, при комнатной температуре (~20°C) и атмосферном давлении в системе растворителей этанол-хлороформ в течение 2.5-3.5 ч. Выход 3,3′-[метиленбис(1,4-фенилен)]-, 3,3′-[оксибис(1,4-фенилен)]- и 3,3′-(3,3′-диметоксибифенил-4,4′-диил)-бис-1,5,3-дитиазепинанов (1) составляет 52-65%. Реакция протекает по схеме:

4-С6Н4-СН2-C6H4-4′, 4-С6Н4-O-С6Н4-4′, 4-H3COC6H3-C6H3OCH3-4′
3,3′-[Метиленбис(1,4-фенилен)]-, 3,3′-[оксибис(1,4-фенилен)]- и 3,3′-(3,3′-диметоксибифенил-4,4′-диил)-бис-1,5,3-дитиазепинаны общей формулы (1) образуются только лишь с участием диаминодифенилметана, диаминодифенилоксида или диметоксибензидина и N-трет-бутил-1,5,3-дитиазепинана под действием катализатора Sm(NO3)3·6H2O. В присутствии других диаминов (например, алкандиаминов) целевые продукты (1) не образуются.
Проведение реакции в присутствии катализатора Sm(NO3)3·6H2O больше 7 мол.% по отношению к ариламину не приводит к существенному увеличению выхода целевого продукта (1). Использование в реакции катализатора Sm(NO3)3·6H2O менее 3 мол.% снижает выход (1), что связано с уменьшением каталитически активных центров в реакционной массе. Реакции проводили при комнатной температуре ~20°C. При более высокой температуре (например, 60°C) снижается селективность реакции и увеличиваются энергозатраты, при меньшей температуре (например, 0°C) снижается скорость реакции. Опыты проводили в системе растворителей этанол-хлороформ, т.к. в них хорошо растворяются исходные реагенты.
Существенные отличия предлагаемого способа:
В известном способе реакция идет с участием в качестве исходного реагента газообразного сероводорода при температуре 80°C с образованием шестичленных N,S-содержащих гетероциклов, а именно, 5-[2-[1,3,5-дитиазинан-5-ил]этил]1,3,5-дитиазинана (3). Известный способ не позволяет получать индивидуальные 3,3′-[метиленбис(1,4-фенилен)]-, 3,3′-[оксибис(1,4-фенилен)]- и 3,3′-(3,3′-диметоксибифенил-4,4′-диил)-бис-1,5,3-дитиазепинаны общей формулы (1).
В предлагаемом способе реакция идет с участием в качестве исходных реагентов N-трет-бутил-1,5,3-дитиазепинана и диаминодифенилметана, диаминодифенилоксида или диметоксибензидина под действием катализатора Sm(NO3)3·6H2O при температуре 20°C. В отличие от известных предлагаемый способ позволяет получать индивидуальные 3,3′-[метиленбис(1,4-фенилен)]-, 3,3′-[оксибис(1,4-фенилен)]- и 3,3′-(3,3′-диметоксибифенил-4,4′-диил)-бис-1,5,3-дитиазепинаны общей формулы (1), синтез которых в литературе не описан.
Способ поясняется следующими примерами:
ПРИМЕР 1. В сосуд Шленка, установленный на магнитной мешалке, в атмосфере аргона помещают 198 мг (10 ммолей) диаминодифенилметана в 5 мл этанола, 22 мг (0.5 ммолей) Sm(NO3)3·6H2O, затем прикапывают 382 мг (20 ммолей) N-трет-бутил-1,5,3-дитиазепинана в 5 мл хлороформа. Реакционную смесь перемешивают при комнатной температуре (~20°C) в течение 3 ч, добавляют 2 мл дистиллированной воды и экстрагируют хлороформом. Хлороформную фракцию хроматографируют на колонке с SiO2 и выделяют 3,3′-[метилен-бис-(1,4-фенилен)]бис-1,5,3-дитиазепинан с выходом 60%.
Другие примеры, подтверждающие способ, приведены в табл.1.
Все опыты проводили в системе растворителей этанол-хлороформ при комнатной температуре (~20°C).
Спектральные характеристики 3,3′-[метилен-бис-(1,4-фенилен)]бис-1,5,3-дитиазепинана1:
(1 Контроль реакции осуществляли методом ТСХ на пластинах Silufol W-254, проявляли парами I2. Для колоночной хроматографии использовали силикагель КСК (100-200 мкм). Температура плавления определена на приборе РНМК 80/2617. Спектры ЯМР 1D (1H 13C) и 2D (COSY, HSQC, НМВС) сняты на спектрометре Broker Avance 400 (100.62 МГц для 13C и 400.13 МГц для 1H) по стандартным методикам фирмы Bruker, внутренний стандарт Me4Si, растворитель - CDCl3. Масс спектры получены на приборе MALDI TOF/TOF AUTOFLEX III фирмы Bruker).
Белое кристаллическое вещество, т.пл. 145-147°C, Rf 0.80 (Sorbfil, бензол-этанол, 9:1). Спектр ЯМР 1H (400 МГц, CDCl3), δ, м. д. (J, Гц): 3.07 (8Н, уш. с, Н-6, Н-6′, Н-7, Н-7′); 3.87 (2Н, уш. с, Н-14); 4.77 (8Н, уш. с, Н-2, Н-2′, Н-4, Н-4′); 6.87 (4Н, д, J=8.8 Гц, Н-9, Н-13, Н-9′, Н-13′); 7.14 (4Н, д, J=8.8 Гц, Н-10, Н-12, Н-10′, Н-12′). Спектр ЯМР 13С, δ, м. д.: 35.8 (С-6, С-6′, С-7, С-7′); 40.1 (С-14); 55.2 (С-2, С-2′, С-4, С-4′); 116.1 (С-9, С-9′, С-13, С-13′); 129.6 (С-10, С-10′, С-12, С-12′); 133.1 (С-11, С-11′); 144.0 (С-8, С-8′). MALDI TOF, m/z 457.172 [M+Na]+ (C21H26N2S4Na).
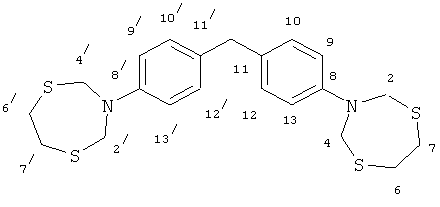
Спектральные характеристики 3,3′-[оксибис-1,4-фенилен)]бис-1,5,3-дитиазепинана2:
(2 Контроль реакции осуществляли методом ТСХ на пластинах Silufol W-254, проявляли парами I2. Для колоночной хроматографии использовали силикагель КСК (100-200 мкм). Спектры ЯМР 1D (1H 13C) и 2D (COSY, HSQC, НМВС) сняты на спектрометре Broker Avance 400 (100.62 МГц для 13C и 400.13 МГц для 1H) по стандартным методикам фирмы Bruker, внутренний стандарт Me4Si, растворитель - CDCl3. Масс спектры получены на приборе MALDI TOF/TOF AUTOFLEX III фирмы Bruker).
Светло-желтое масло, Rf 0.85 (Sorbfil, бензол-этанол, 9:1). Спектр ЯМР 1H (400 МГц, CDC13), δ, м. д. (J, Гц): 3.06 (8Н, уш. с, Н-6, Н-6′, Н-7, Н-7′); 4.73 (8Н, уш. с, Н-2, Н-2′, Н-4, Н-4′); 6.89 (4Н, д, J=9.2 Гц, Н-9, Н-13, Н-9′, Н-13′); 6.96 (4Н, д, J=8.8 Гц, Н-10, Н-12, Н-10′, Н-12′). Спектр ЯМР 13C, δ, м. д.: 35.9 (С-6, С-6′, С-7, С-7′); 55.7 (С-2, С-2′, С-4, С-4′); 117.7 (С-9, С-9′, С-13, С-13′); 119.5 (С-10, С-10′, С-12, С-12′); 141.8 (С-8, С-8′); 151.3 (С-11, С-11′). MALDI TOF, m/z 436.228 [М] (C20H24N2OS4).
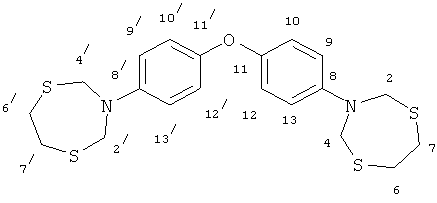
Спектральные характеристики 3.3′-(3.3′-диметоксибиФенил-4,4'-диил)-бис-1,5,3-дитиазепинана3:
(3 Контроль реакции осуществляли методом ТСХ на пластинах Silufol W-254, проявляли парами I2. Для колоночной хроматографии использовали силикагель КСК (100-200 мкм). Температура плавления определена на приборе РНМК 80/2617. Спектры ЯМР 1D (1H 13C) и 2D (COSY, HSQC, НМВС) сняты на спектрометре Broker Avance 400 (100.62 МГц для 13C и 400.13 МГц для 1H) по стандартным методикам фирмы Bruker, внутренний стандарт Me4Si, растворитель - CDCl3. Масс-спектры получены на приборе MALDI TOF/TOF AUTOFLEX III фирмы Bruker).
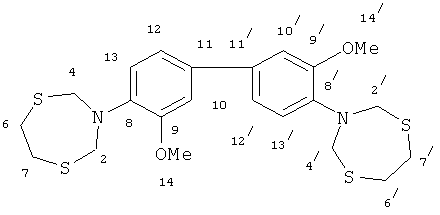
Белое кристаллическое вещество, т.пл. 237-239°C, Rf 0.95 (Sorbfil, бензол-этанол, 9:1). Спектр ЯМР 1H (400 МГц, CDCl3), δ, м. д.: 3.12 (8Н, уш. с, Н-6, Н-6′, Н-7, Н-7′); 3.94 (6Н, уш. с, Н-14, Н-14′); 4.80 (8Н, уш. с, Н-2, Н-2′, Н-4, Н-4′); 7.06 (4Н, м, Н-10, Н-12, Н-10′, Н-12′); 7.28 (2Н, м, Н-13, Н-13′). Спектр ЯМР 13C, δ, м.д.: 36.9 (С-6, С-6′, С-7, С-7′); 55.6 (С-14, С-14′); 57.6 (С-2, С-2′, С-4, С-4′); 110.4 (С-13, С-13′); 111.5 (С-10, С-10′); 119.3 (С-11, С-11′); 121.5 (С-12, С-12′); 147.4 (С-8, С-8′); 152.3 (С-9, С-9′). MALDI TOF, m/z 480.232 [М] (C22H28N2O2S4).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ СЕЛЕКТИВНОГО ПОЛУЧЕНИЯ 3,3'-[БИС-(1,4-ФЕНИЛЕН)]БИС-1,5,3-ДИТИАЗЕПИНАНОВ | 2012 |
|
RU2529506C2 |
| СПОСОБ ПОЛУЧЕНИЯ 3,3'-(1,2-ФЕНИЛЕН)-БИС-1,5,3-ДИТИАЗЕПИНАНА И 3,3'-[МЕТИЛЕН-БИС-(1,4-ФЕНИЛЕН)]-БИС-1,5,3-ДИТИАЗЕПИНАНА | 2011 |
|
RU2467006C1 |
| СПОСОБ СЕЛЕКТИВНОГО ПОЛУЧЕНИЯ 3,3'-[БИС(1,4-ФЕНИЛЕН)]БИС-1,3,5-ДИТИАЗИНАНОВ | 2012 |
|
RU2529509C2 |
| СПОСОБ ПОЛУЧЕНИЯ 3, 3'-[ОКСА(ТИА)АЛКАН-альфа, омега-ДИИЛ]-БИC-1, 5, 3-ДИТИАЗЕПИНАНОВ | 2012 |
|
RU2518482C2 |
| СПОСОБ ПОЛУЧЕНИЯ α,ω-БИС-(1,5,3-ДИТИАЗЕПИНАН-3-ИЛ)АЛКАНОВ | 2011 |
|
RU2478634C2 |
| СПОСОБ ПОЛУЧЕНИЯ 3,3'-(3,6-ДИОКСАОКТАН-1,8-ДИИЛ)БИС-1,5,3-ДИТИАЗЕПИНАНА И ЕГО ПРИМЕНЕНИЕ В КАЧЕСТВЕ СРЕДСТВА С ФУНГИЦИДНОЙ АКТИВНОСТЬЮ | 2013 |
|
RU2547267C2 |
| СПОСОБ ПОЛУЧЕНИЯ 3-(1-АДАМАНТИЛ)- И 3-[1-(1-АДАМАНТИЛ)ЭТИЛ]-1,5,3-ДИТИАЗЕПИНАНОВ | 2013 |
|
RU2551668C1 |
| СПОСОБ ПОЛУЧЕНИЯ (1,5,3-ДИТИАЗЕПИНАН-3-ИЛ)(ТИО)ФЕНОЛОВ | 2011 |
|
RU2478623C2 |
| СПОСОБ ПОЛУЧЕНИЯ 4-(1,5,3-ДИТИАЗЕПИНАН-3-ИЛ)-БЕНЗОЙНОЙ И 5-(1,5,3-ДИТИАЗЕПИНАН-3-ИЛ)-2-ГИДРОКСИБЕНЗОЙНОЙ КИСЛОТ | 2012 |
|
RU2529516C2 |
| СПОСОБ ПОЛУЧЕНИЯ α,ω-БИС-(1,5,3-ДИТИАЗЕПИНАН-3-ИЛ)АЛКАНОВ | 2011 |
|
RU2466999C1 |
Изобретение относится к органической химии, конкретно к способу получения 3,3′-[метиленбис(1,4-фенилен)]-, 3,3′-[оксибис(1,4-фенилен)]- и 3,3′-(3,3′-диметоксибифенил-4,4′-диил)-бис-1,5,3-дитиазепинанов общей формулы (1):
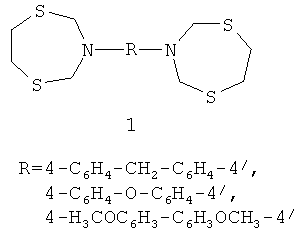
который заключается в том, что ариламины [диаминодифенилметан, диаминодифенилоксид, диметоксибензидин] подвергают взаимодействию с N-трет-бутил-1,5,3-дитиазепинаном в присутствии катализатора Sm(NO3)3·6H2O в атмосфере аргона при мольном соотношении ариламин : N-трет-бутил-1,5,3-дитиазепинан : Sm(NO3)3·6H2O = 10 : 20 : (0.3-0.7) при температуре ~20°C в системе растворителей этанол-хлороформ в течение 2.5-3.5 ч. Технический результат: разработан новый способ получения 3,3′-[метиленбис(1,4-фенилен)]-, 3,3′-[оксибис(1,4-фенилен)]- и 3,3′-(3,3′-диметоксибифенил-4,4′-диил)-бис-1,5,3-дитиазепинанов, которые могут найти применение в качестве антибактериальных, антигрибковых и антивирусных агентов, биологически активных комплексообразователей, селективных сорбентов и экстрагентов драгоценных металлов, специальных реагентов для подавления жизнедеятельности бактерий в различных технических средах (от легкой промышленности до нефти). 1 табл., 1 пр.
Способ получения 3,3′-[метиленбис(1,4-фенилен)]-, 3,3′-[оксибис(1,4-фенилен)]- и 3,3′-(3,3′-диметоксибифенил-4,4′-диил)-бис-1,5,3-дитиазепинанов общей формулы (1):

отличающийся тем, что ариламины [диаминодифенилметан, диаминодифенилоксид, диметоксибензидин] подвергают взаимодействию с N-трет-бутил-1,5,3-дитиазепинаном в присутствии катализатора Sm(NO3)3·6H2O в атмосфере аргона при мольном соотношении ариламин : N-трет-бутил-1,5,3-дитиазепинан : Sm(NO3)3·6H2O = 10 : 20 : (0.3-0.7) при температуре ~20°C в системе растворителей этанол-хлороформ в течение 2.5-3.5 ч.
| СПОСОБ СЕЛЕКТИВНОГО ПОЛУЧЕНИЯ α,ω-БИС-(1,3,5-ДИТИАЗИНАН-5-ИЛ)-3-ОКСОПЕНТАНА И α,ω-БИС-(1,3,5-ДИТИАЗИНАН-5-ИЛ)-3,6-ДИОКСООКТАНА | 2010 |
|
RU2459823C2 |
| СПОСОБ ПОЛУЧЕНИЯ МОНО-(ДИ-, ТЕТРА-)МЕТИЛ-1,2-БИС-(1,3,5-ДИТИАЗИНАН-5-ИЛ)ЭТАНОВ | 2010 |
|
RU2443702C2 |
| US 3281417 A1, 25.10.1966 | |||
Авторы
Даты
2014-06-10—Публикация
2012-09-27—Подача