Изобретение относится к области медицины и может быть использовано для повышения эффективности лечения хронической сердечной недостаточности, преимущественно 1 и 2 стадии, в том числе и при комплексной терапии в сочетании с известными стандартными лекарственными средствами, применяемыми для лечения заболеваний сердечно - сосудистой системы.
Из уровня техники известен препарат для лечения хронической сердечной недостаточности (ХСН), на основе активированных -потенцированных форм сверхмалых доз антител к С - концевому фрагменту AT1 рецептора ангиотензина II (Сравнительное изучение кардиопротективного действия кардоса и лозартана при экспериментальной хронической сердечной недостаточности. Тюренков И.Н. и др., Материалы 9-го Всероссийского научно- образовательного форума «Кардиология 2007». Москва, 2007, с.284-285). Однако данный препарат не во всех случаях может обеспечить достаточную терапевтическую эффективность.
Изобретение направлено на повышения эффективности комплексной терапии хронической сердечной недостаточности, преимущественно 1 и 2 стадии.
Решение поставленной задачи обеспечивается тем, что в способе лечения хронической сердечной недостаточности, путем введения в организм лекарственного средства на основе активированной -потенцированной формы сверхмалых доз аффинно очищенных антител к рецептору ангиотензина II, приготовленную путем многократного последовательного разведения и внешнего воздействия, согласно изобретению, дополнительно одновременно и сочетано вводят активированную - потенцированную форму сверхмалых доз аффинно очищенных антител к эндотелиальной NO - синтазе.
При этом используют активированную - потенцированную форму антител к С - концевому фрагменту AT1 - рецептора ангиотензина II и активированную - потенцированную форму антител к эндотелиальной NO - синтазе.
Кроме того, активированную - потенцированную форму антител к С - концевому фрагменту AT1 - рецептора ангиотензина II и активированную - потенцированную форму антител к эндотелиальной NO - синтазе используют в виде активированного - потенцированного водного или водно - спиртового раствора каждого компонента, полученного в процессе последовательного многократного разведения в водном или водно - спиртовом растворителе и промежуточного внешнего механического воздействия - вертикального встряхивания.
Причем используют фармацевтическую композицию, приготовленную в виде единого лекарственного препарата - одной лекарственной формы, которая включает смесь различных гомеопатических разведении антител к С - концевому фрагменту AT1 - рецептора ангиотензина II в сочетании со смесью различных гомеопатических разведении антител к эндотелиальной NO - синтазе.
При этом, предпочтительно использование фармацевтической композиции на основе активированной - потенцированной формы сверхмалых доз аффинно очищенных антител к С - концевому фрагменту AT1 - рецептора ангиотензина II и к эндотелиальной NO - синтазе в сочетании с известными стандартными лекарственными средствами, применяемыми для лечении заболеваний сердечно - сосудистой системы следующих групп: ингибиторы АПФ в т.ч. комбинированные, диуретики, β-адреноблокаторы, нитраты, сердечные гликозиды, антагонисты кальция, гиполипидемические средства, антиагреганты, антигипоксанты, антикоагулянты.
Решение поставленной задачи обеспечивается также тем, что лекарственное средство для лечения хронической сердечной недостаточности на основе активированной - потенцированной формы сверхмалых доз аффинно очищенных антител к рецептору ангиотензина II, согласно изобретению, выполнено в виде фармацевтической композиции и дополнительно содержит в качестве усиливающего компонента активированную - потенцированную форму антител к эндотелиальной NO - синтазе.
При этом активированную - потенцированную форму антител к рецептору ангиотензина II и к эндотелиальной NO - синтазе используют в виде активированного - потенцированного водного или водно - спиртового раствора, полученного в процессе последовательного многократного разведения матричного раствора соответствующих антител в водном или водно - спиртовом растворителе и промежуточного внешнего механического воздействия - вертикального встряхивания.
Кроме того, фармацевтическая композиция может быть выполнена в твердой лекарственной форме и содержать эффективное количество нейтрального носителя, насыщенного смесью активированной - потенцированной формы антител к рецептору ангиотензина II и активированной - потенцированной формы антител к эндотелиальной NO - синтазе, и фармацевтически приемлемые добавки, которые могут включать лактозу, целлюлозу микрокристаллическую и магния стеарат.
При этом водные или водно - спиртовые растворы активированных - потенцированных форм антител к рецептору ангиотензина Пик эндотелиальной NO - синтазе получены путем многократного последовательного разведения и промежуточного внешнего воздействия из матричных растворов аффинно очищенных антител к рецептору ангиотензина II и к эндотелиальной NO - синтазе с концентрацией 0,5-5,0 мг/мл.
Кроме того, каждый из компонентов сверхмалых доз аффинно очищенных антител используют в виде смеси различных, преимущественно сотенных, гомеопатических разведении.
Фармацевтическая композиция может содержать действующие компоненты: активированную - потенцированную форму антител к С -концевому фрагменту AT1 - рецептора ангиотензина Пик эндотелиальной NO - синтазе в соотношении 1:1, при этом каждый компонент используют в сверхмалой дозе в виде смеси трех соответствующих матричных растворов, разведенных в 10012, 10030, и 100 раз, что эквивалентно сотенным гомеопатическим разведениям С 12, С 30, С 200.
Заявленную фармацевтическую композицию на основе активированной - потенцированной формы сверхмалых доз аффинно очищенных антител к С - концевому фрагменту AT1 - рецептора ангиотензина II и к эндотелиальной NO - синтазе возможно использовать в сочетании с известными стандартными лекарственными средствами, применяемыми для лечении заболеваний сердечно -сосудистой системы следующих групп:
- ингибиторы АПФ в т.ч. комбинированные (энап,эналаприл, капотен, ренитек, престариум (берлиприл,диротон, капотен, квадроприл, моноприл, ренитек, престариум, нолипрел-форте, энап-Н));
- диуретики (фуросемид, верошпирон, гипотиазид, арифон ретард, индапамид, гипотиазид, диувер, индап, индапамид);
- β-адреноблокаторы (эгилок, атенолол, конкор, беталок ЗОК);
- нитраты (диласидом, кардикет, кардикет-реторд, митролинат, МоноМак, моночинкве, нитроглицерин, нитросорбид, оликард, пектрол, сиднофарм);
- сердечные гликозиды (дигоксин);
- антагонисты кальция (нормодипин, кордафлекс, амловас, амлодипин, амловас, амлотоп, кардилопин, кордафлекс, кордипин ХЛ);
- гиполипидемические средства (вазилип, липримар, липтонорм, симвагексал, симвастол, симвокард, симгал, тулип);
- антиагреганты (аспирин, кардиАСК, кардиомагнил, тромбоАСС);
- антигипоксанты (предуктал MB, предуктал, тримектал);
- антикоагулянты (варфарин).
Заявленную фармацевтическую композицию рекомендуется принимать, предпочтительно, по 1-2 таблетке 2-4 раза в день.
При лечении лечения ХСН возможно раздельное применение в виде двух отдельно приготовленных препаратов как в виде растворов, так и в твердых лекарственных формах (таблеток), каждая из которых содержит активированную - потенцированную форму сверхмалых доз аффинно очищенных антител к С - концевому фрагменту AT1 - рецептора ангиотензина II и, соответственно, активированную - потенцированную форму сверхмалых доз аффинно очищенных антител к эндотелиальной NO - синтазе.
Предложенное сочетание активированных - потенцированных форм антител к С - концевому фрагменту АТ1 - рецептора ангиотензина Пик эндотелиальной синтазе оксида азота (NO - синтазе) в фармацевтической композиции (т.е. формы антител к С - концевому фрагменту AT1 - рецептора ангиотензина Пик эндотелиальной NO - синтазе, приготовленных путем многократного последовательного разведения и промежуточного внешнего воздействия - вертикального встряхивания, которая обладает активностью в фармакологических моделях и/или клинических методах лечения ХСН) обеспечивает получение неожиданного синергетического терапевтического эффекта, который заключается в более выраженном действии на сосудистое ремоделирование и дисфункцию эндотелия, играющую значимую роль в развитии и прогрессировании ХСН, а также на улучшение качества жизни пациентов, морфофункциональные параметры сердца и толерантность к физической нагрузке, что подтверждено клиническими испытаниями.
При этом применение заявленной фармацевтической композиции при лечении больных с заболеваниями кардиоваскулярной системы приводит к улучшению качества жизни, в частности у больных улучшаются показатели качества жизни, оцениваемые по критериям депрессии, тревоги, длительности ходьбы, повышение толерантности к физической нагрузке, и т.д.
Кроме того, полученное в соответствии с изобретением техническое решение расширяет арсенал лекарственных средств, предназначенных для комплексной терапии хронической сердечной недостаточности.
Фармацевтическую композицию приготовляют, преимущественно, следующим образом.
Для приготовления гомеопатически активированной потенцированной формы действующих компонентов используют моноклональные или, преимущественно, поликлональные антитела, которые могут быть получены по известным технологиям - методикам, описанным, например, в книге: Иммунологические методы, под ред. Г.Фримеля, М., «Медицина», 1987, с.9-33; или, например, в статье Laffly Е., Sodoyer R. Hum. Antibodies. Monoclonal and recombinant antibodies, 30 years after. - 2005 - Vol.14. - N 1-2. P.33-55.
Моноклональные антитела получают, например, с помощью гибридомной технологии. Причем начальная стадия процесса включает иммунизацию, основанную на принципах, уже разработанных при приготовлении поликлональных антисывороток. Дальнейшие этапы работы предусматривают получение гибридных клеток, продуцирующих клоны одинаковых по специфичности антител. Их выделение в индивидуальном виде проводится теми же методами, что и в случае поликлональных антисывороток.
Поликлональные антитела могут быть получены активной иммунизацией животных. Для этого по специально разработанной схеме животным делают серию инъекций требуемым в соответствии с изобретением веществом - антигеном: эндотелиальной NO - синтазой и С - концевым фрагментом АТ1 - рецептора ангиотензина II. В результате проведения такой процедуры получают моноспецифическую антисыворотку с высоким содержанием антител, которую и используют для получения активированной - потенцированной формы. При необходимости проводят очистку антител, присутствующих в антисыворотке, например, методом аффинной хроматографии, путем применения фракционирования солевым осаждением или ионообменной хроматографии.
Предпочтительным для приготовления заявленной фармацевтической композиции является использование поликлональных антител к эндотелиальной NO - синтазе и к С - концевому фрагменту AT1 - рецептора ангиотензина II, которые в качестве матричного (первичного) раствора с концентрацией 0,5 - 5,0 мг/мл, используют для последующего приготовления активированной - потенцированной формы.
Предпочтительной для приготовления каждого компонента является использование смеси трех водно-спиртовых разведении первичного матричного раствора антител, разведенных соответственно в 10012, 10030, и 100200 раз, что соответствует сотенным гомеопатическим разведениям С 12, С30 и С 200. При выполнении заявленного лекарственного средства в твердой лекарственной форме на лактозу наносится смесь указанных компонентов.
Предпочтительным для приготовления заявленного лекарственного препарата является использование поликлональных антител к С - концевому фрагменту AT1 - рецептора ангиотензина II и эндотелиальной NO - синтазе, которые могут быть получены иммунизацией кроликов следующим образом.
Для получения поликлональных антител к С - концевому фрагменту AT1 - рецептора ангиотензина II в качестве иммуногена (антигена) для иммунизации кроликов используют адъювант и С - концевой фрагмент AT1 - рецептора ангиотензина II выбираемый, например, из следующей группы:


Возможно для получения поликлональных антител к С - концевому фрагменту AT1 - рецептора ангиотензина II использование в качестве иммуногена (антигена) С - концевой фрагмент рецептора AT1 ангиотензина II человека с добавленным к N концу Цистеином (С):

Перед отбором крови за 7 - 9 дней проводят 1-3 внутривенных инъекций для повышения уровня антител. В процессе иммунизации у кроликов отбирают небольшие пробы крови для оценки количества антител. Максимальный уровень иммунного ответа на введение большинства растворимых антигенов достигается через 40-60 дней после первой инъекции. После окончания первого цикла иммунизации кроликов в течение 30 дней дают восстановить здоровье и проводят реиммунизацию, включающую 1-3 внутривенные инъекции. Для получения антисыворотки из иммунизированных кроликов собирают кровь в центрифужную пробирку объемом 50 мл. С помощью деревянного шпателя удаляют со стенок пробирки образовавшиеся сгустки и помещают палочку в сгусток, образовавшийся в центре пробирки. Кровь помещают в холодильник (температура 4°С) на ночь. На следующий день удаляют сгусток, прикрепившийся к шпателю, и центрифугируют оставшуюся жидкость при 13000g в течение 10 мин. Супернатант (надосадочная жидкость) является антисывороткой. Полученная антисыворотка должна быть желтого цвета. Добавляют к антисыворотке 20% (весовая концентрация) NaN3 до конечной концентрации 0,02% и хранят до использования в замороженном состоянии при температуре -20°С. Для выделения из антисыворотки антител к С - концевому фрагменту AT1 рецептора ангиотензина П производят абсорбцию на твердой фазе в следующей последовательности:
1. 10 мл антисыворотки кролика разбавляют в 2 раза 0,15 М NaCl добавляют 6,26 г Na2SO4, перемешивают и инкубируют 12-16 ч при 4°С;
2. выпавший осадок удаляют центрифугированием, растворяют в 10 мл фосфатного буфера и затем диализуют против того же буфера в течение ночи при комнатной температуре;
3. после удаления осадка центрифугированием раствор наносят на колонку с ДЭАЭ-целлюлозой, уравновешенную фосфатным буфером;
4. фракцию антител определяют, измеряя оптическую плотность элюата при 280 нм.
Затем производят очистку антител методом аффинной хроматографии путем прикрепления полученных антител к С - концевому фрагменту AT1 - рецептора ангиотензина II, который находится на нерастворимом матриксе с последующим элюированием концентрированными растворами соли.
Полученный, таким образом, буферный раствор поликлональных кроличьих антитела к С - концевому фрагменту AT1 - рецептора ангиотензина II, очищенных на антигене, с концентрацией 0,5 - 5,0 мг/мл, предпочтительно 2,5 - 3,0 мг/мл, используют в качестве матричного (первичного) раствора для последующего приготовления активированной - потенцированной формы.
Поликлональные антитела к эндотелиальной NO - синтазе получают аналогичным вышеуказанным способом, используя в качестве иммуногена (антигена) для иммунизации кроликов адъювант и цельную молекулу эндотелиальной NO - синтазы следующей последовательности:


Возможно для получения поликлональных антител к эндотелиальной NO - синтазе использование в качестве иммуногена (антигена) цельной молекулы эндотелиальной NO - синтазы следующей последовательности:
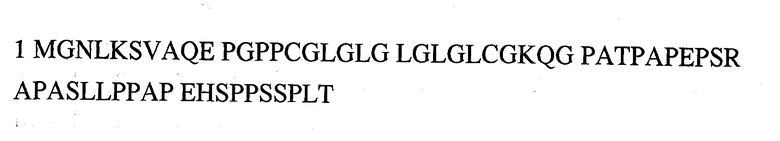


Возможно для получения поликлональных антител к эндотелиальной NO - синтазе использование в качестве иммуногена (антигена) синтетического пептида эндотелиальной NO - синтазы, выбранного, например, из следующих аминокислотных последовательностей:

Активированную - потенцированную форму каждого компонента готовят путем равномерного уменьшения концентрации в результате последовательного разведения 1 части упомянутого матричного раствора в 9 частях (для десятичного разведения) или в 99 частях (для сотенного разведения) или в 999 частях (для тысячного разведения) нейтрального растворителя с многократным вертикальным встряхиванием ("динамизацией") каждого полученного разведения и использованием отдельных емкостей для каждого последующего разведения до получения требуемой потенции - кратности разведения по гомеопатическому методу (см., например, В.Швабе "Гомеопатические лекарственные средства", М., 1967 г., с.14-29).
Например, для приготовления 12-го сотенного разведения С 12 одну часть упомянутого матричного раствора антител к С - концевому фрагменту AT1 - рецептора ангиотензина II с концентрацией 3,0 мг/мл разводят в 99 частях нейтрального водного или водно - спиртового растворителя (преимущественно 70% этилового спирта) и многократно (10 и более раз) вертикально встряхивают - потенцируют полученное 1-е сотенное С1 разведение. Из 1-го сотенного С1 разведения приготовляют 2-ое сотенное разведение С2. Данную операцию повторяют 11 раз, получая 12-е сотенное разведение С 12. Таким образом, 12-е сотенное разведение С 12 представляет собой раствор, полученный разбавлением последовательно в разных емкостях 12 раз 1-ой части исходного матричного раствора антител к С - концевому фрагменту AT1 - рецептора ангиотензина II с концентрацией 3,0 мг/мл в 99- ти частях нейтрального растворителя, т.е. раствор приготовленный из матричного раствора, разведенного в 10012 раз, что эквивалентно сотенному гомеопатическому разведению С 12. Аналогичные операции с соответствующей кратностью разведения проводят для получения разведении С 30 и С 200.
При использовании в качестве биологически активного жидкого компонента смеси различных гомеопатических, преимущественно сотенных, разведении, действующего вещества каждый компонент состава (например, С 12, С 30, С 200) приготовляют раздельно по описанной выше технологии до их предпоследнего разведения (соответственно, до получения С 11, С29, С 199) и затем вносят в соответствии с составом смеси в одну емкость по одной части каждого компонента и смешивают с требуемым количеством растворителя (соответственно, с 97 частями для сотенного разведения). При этом получают активированную - потенцированную форму антител к С - концевому фрагменту AT1 - рецептора ангиотензина П в сверхмалой дозе каждого компонента, приготовленную из матричного раствора, разведенного в 10012, в 10030 в 100200, что эквивалентно смеси сотенных гомеопатических разведении С12, С30 и С200.
Возможно использование действующего вещества в виде смеси других различных гомеопатических, разведении, например, десятичных и или сотенных, (D 20, С 30, С 100 или С12, С30, С50 и т.д.), эффективность которых определяют экспериментально.
При потенцировании вместо встряхивания в процессе уменьшения концентрации также можно осуществлять внешнее воздействие ультразвуком, электромагнитным или иным физическим воздействием.
Для получения заявленной фармацевтической композиции водные или водно - спиртовые растворы действующих компонентов смешивают, преимущественно, в соотношении 1:1 и используют в жидкой лекарственной форме. Предпочтительно, фармацевтическая композиция содержит активированную - потенцированную форму антител к С -концевому фрагменту AT1 - рецептора ангиотензина Пик эндотелиальной NO - синтазе в сверхмалой дозе каждого компонента в сверхмалой дозе каждого компонента, приготовленной из матричного раствора, разведенного в 10012, в 10030 в 10020, что эквивалентно смеси сотенных гомеопатических разведении С12, С30 и С200.
Заявленная фармацевтическая композиция может быть использована и в твердой лекарственной форме, которая содержит эффективное количество гранул нейтрального носителя - лактозы, насыщенного путем пропитывания до насыщения смесью водных или водно - спиртовых растворов активированной - потенцированной формой антител к С - концевому фрагменту AT1 - рецептора ангиотензина II и активированную - потенцированную форму антител к эндотелиальной NO - синтазе, и фармацевтически приемлемые добавки, включающие, преимущественно, лактозу, целлюлозу микрокристаллическую и магния стеарат.
Для получения твердой оральной формы заявленного лекарственного средства производят в установке кипящего слоя (например, типа «Hüttlin Pilotlab» производства компании Hüttlin GmbH) орошение до насыщения вводимых в псевдоожиженный - кипящий слой гранул нейтрального вещества - лактозы (молочного сахара) с размером частиц 150 - 300 мкм, предварительно полученным водным или водно - спиртовым раствором активированных - потенцированных форм антител к С - концевому фрагменту AT1 - рецептора ангиотензина II и к эндотелиальной синтазе оксида азота (NO - синтазе), преимущественно, в соотношении 1 кг раствора антител на 5 или 10 кг лактозы (1:5-1:10) с одновременной сушкой в потоке подаваемого под решетку нагретого воздуха при температуре не выше 40°С. Расчетное количество 0,17-0,34 от массы твердой оральной формы) высушенных гранул, насыщенных активированной - потенцированной формой антител, загружают в смеситель и смешивают с микрокристаллической целлюлозой, вводимой в количестве 3-8 масс. частей от общей массы загрузки - от массы твердой оральной формы. Затем в эту смесь добавляют 25 - 45 масс. частей от общей массы загрузки «ненасыщенной» чистой лактозы (для снижения стоимости и некоторого упрощения и ускорения технологического процесса без снижения эффективности лечебного воздействия) и стеарат магния в количестве 0,1 - 0,3 масс. частей от общей массы загрузки. Полученную таблеточную массу равномерно перемешивают и таблетируют прямым сухим прессованием (например, в таблет - прессе Korsch - XL 400) с формированием круглых таблеток массой 150 - 500 мг. После таблетирования получают таблетки массой 300 мг, пропитанные водно -спиртовым раствором (3,0 - 6,0 мг/табл.) активированной -потенцированной формой антител к С - концевому фрагменту ATi -рецептора ангиотензина II и NO - синтазы в сверхмалой дозе, каждого компонента, приготовленной из матричного раствора, разведенного в 10012, в 10030 в 100200, что эквивалентно смеси сотенных гомеопатических разведении С12, С30 и С200.
Предпочтительно заявленную фармацевтическую композицию рекомендуется принимать по 1-2 таблетке 2-4 раза в день.
Для проведения экспериментальных исследований были использованы антитела, приготовленные по заказу специализированной фармацевтической фирмой.
Пример 1.
Для экспериментального исследования эффективности заявленного технического решения была использована фармацевтическая композиция, содержащая водные растворы активированных - потенцированных форм (сверхмалые дозы - СМД) антител к С - концевому фрагменту AT1 - рецептора ангиотензина II и к эндотелиальной NO - синтазе, приготовленные из матричного (исходного) раствора с концентрацией 3,0 мг/мл, при этом каждый компонент взят в смеси гомеопатических разведениях С12, С30, С200.
Исследования проводились на 80 пациентов в двойном слепом плацебо-контролируемом, рандомизированном исследовании. Пациенты (ХСН II-IV функционального класса (ФК), фракцией выброса левого желудочка (ФВ ЛЖ) менее 40%) были разделены на 4 равные группы: в течение 6 месяцев в дополнении к основной терапии (β-блокатор бисопролол, ингибитор АПФ эналаприл, при отсутствии противопоказаний аспирин, допускался прием диуретиков, нитратов, дигоксина) группы 1 получали СМД антител к С - концевому фрагменту AT1 - рецептора ангиотензина II (смесь гомеопатических разведении С 12, С30, С200) (3 таб/сут, n=20); группы 2 - СМД антител к эндотелиальной NO - синтазе (смесь гомеопатических разведении С 12, С30, С200) (3 таб/сут, n=20); группы 3 - фармацевтическую композицию на основе СМД антител к С-концевому фрагменту AT1 - рецептора ангиотензина II и к эндотелиальной NO - синтазе (смесь гомеопатических разведении С 12, С30, С200) (3 таб/сут, n=20)%; группы 4 - плацебо (3 таб/сут, n=20). Группы были сопоставимы по исходным характеристикам: по полу и возрасту и тяжести (ФК ХСН и ФВ ЛЖ) и длительности заболевания.
До и после лечения у пациентов оценивали влияние вводимых препаратов, на сосудистое ремоделирование и дисфункцию эндотелия, играющую значимую роль в развитии и прогрессировании ХСН.
Влияние препаратов на процессы сосудистого ремоделирования оценивали по скорости распространения пульсовой волны (СПВ) (система «Colson») на каротидно-феморальном (CF) (эластический тип) и каротидно-радиальном (CR) (мышечный тип) сегментах артерий.
В таблице 1 приведена динамика показателей скорости распространения пульсовой волны на каротидно-феморальном (CF) (эластический тип) и каротидно-радиальном (CR) (мышечный тип) сегментах артерий.
Через 6 месяцев лечения только в группе 3 было отмечено достоверное влияние заявленной фармацевтической композиции на жесткость артерий мышечного типа. В группе 1, принимающей СМД антител к С - концевому фрагменту AT1 - рецептора ангиотензина II, и в группе 3, принимающей заявленную фармацевтическую композицию, достоверно повышалась жесткость артерий эластического типа.
Пример 2.
Для экспериментального исследования эффективности заявленного технического решения была использована фармацевтическая композиция, содержащая водные растворы активированных -потенцированных форм (сверхмалые дозы - СМД) антител к С -концевому фрагменту AT1 - рецептора ангиотензина II и к эндотелиальной NO - синтазе, приготовленные из матричного (исходного) раствора с концентрацией 3,0 мг/мл, при этом каждый компонент взят в смеси гомеопатических разведениях С 12, С30, С200. Исследования проводились на 80 пациентов в двойном слепом плацебо-контролируемом, рандомизированном исследовании. Пациенты (ХСН II-IV функционального класса (ФК), фракцией выброса левого желудочка (ФВ ЛЖ) менее 40%) были разделены на 4 равные группы: в течение 6 месяцев в дополнении к основной терапии (β-блокатор бисопролол, ингибитор АПФ эналаприл, при отсутствии противопоказаний аспирин, допускался прием диуретиков, нитратов, дигоксина) группы 1 получали СМД антител к С - концевому фрагменту AT1 - рецептора ангиотензина II (смесь гомеопатических разведении С 12, С30, С200) (3 таб/сут, n=20); группы 2 - СМД антител к эндотелиальной NO - синтазе (смесь гомеопатических разведении С12, С30, С200) (3 таб/сут, n=20); группы 3 - заявленную фармацевтическую композицию на основе СМД антител к С - концевому фрагменту AT1 - рецептора ангиотензина Пик эндотелиальной NO - синтазе (смесь гомеопатических разведении С 12, С30, С200) (3 таб/сут, n=20); группы 4 - плацебо (3 таб/сут, n=20). Группы были сопоставимы по исходным характеристикам: по полу и возрасту и тяжести (ФК ХСН и ФВ ЛЖ) и длительности заболевания.
До и после лечения у пациентов оценивали качество жизни (Миннесотский и Канзасский опросники), морфофункциональные параметры сердца и толерантность к физической нагрузке.
Результаты исследования в виде динамики основных показателей эффективности лечения приведены в таблице 2.
Через 6 месяцев лечения в группе 1 у пациентов, получавших СМД антител к С - концевому фрагменту AT1 - рецептора ангиотензина II, было отмечено достоверное улучшение качества жизни, улучшение систолической функции левого желудочка, повышение толерантности к физической нагрузке. В группе 2 - достоверно снижался уровень тревоги и депрессии и качество жизни, оцененное с помощью Канзасского опросника. Проведенное исследование показало, что наибольшим терапевтическим эффектом при добавлении к стандартной терапии ХСН обладает заявленная фармацевтическая композиция, которую получала группа 3, в которой была зафиксирована достоверная положительная динамика по всем изучаемым параметрам.
Предложенное сочетание активированных - потенцированных форм антител к С - концевому фрагменту AT1 - рецептора ангиотензина II и к эндотелиальной синтазе оксида азота (NO - синтазе) в фармацевтической композиции обеспечивает получение неожиданного синергетического терапевтического эффекта, который заключается в более выраженном действии на сосудистое ремоделирование и дисфункцию эндотелия, играющую значимую роль в развитии и прогрессировании ХСН, а также на улучшение качества жизни пациентов, морфофункциональные параметры сердца и толерантность к физической нагрузке, что подтверждено клиническими испытаниями.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ КОМПЛЕКСНОЙ ТЕРАПИИ ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ | 2010 |
|
RU2525155C2 |
| СПОСОБ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ АРТЕРИАЛЬНОЙ ГИПЕРТЕНЗИИ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ АРТЕРИАЛЬНОЙ ГИПЕРТЕНЗИИ | 2010 |
|
RU2525156C2 |
| СПОСОБ ЛЕЧЕНИЯ ВЕГЕТОСОСУДИСТОЙ ДИСТОНИИ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ВЕГЕТОСОСУДИСТОЙ ДИСТОНИИ | 2010 |
|
RU2523557C2 |
| СПОСОБ ПОВЫШЕНИЯ ФАРМАКОЛОГИЧЕСКОЙ АКТИВНОСТИ ДЕЙСТВУЮЩЕГО ВЕЩЕСТВА ЛЕКАРСТВЕННОГО СРЕДСТВА И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2014 |
|
RU2572706C1 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ КОРРЕКЦИИ ЭНДОТЕЛИАЛЬНОЙ ДИСФУНКЦИИ | 2011 |
|
RU2543331C2 |
| СПОСОБ ПОВЫШЕНИЯ ФАРМАКОЛОГИЧЕСКОЙ АКТИВНОСТИ ДЕЙСТВУЮЩЕГО ВЕЩЕСТВА ЛЕКАРСТВЕННОГО СРЕДСТВА И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2010 |
|
RU2526153C2 |
| СПОСОБ ЛЕЧЕНИЯ ОЖИРЕНИЯ И СОПУТСТВУЮЩИХ МЕТАБОЛИЧЕСКИХ РАССТРОЙСТВ И ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ОЖИРЕНИЯ И СОПУТСТВУЮЩИХ МЕТАБОЛИЧЕСКИХ РАССТРОЙСТВ | 2010 |
|
RU2552221C2 |
| СПОСОБ ЛЕЧЕНИЯ ОЖИРЕНИЯ И СОПУТСТВУЮЩИХ МЕТАБОЛИЧЕСКИХ РАССТРОЙСТВ | 2013 |
|
RU2582393C2 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ КОРРЕКЦИИ ЭНДОТЕЛИАЛЬНОЙ ДИСФУНКЦИИ | 2011 |
|
RU2543332C2 |
| СПОСОБ КОРРЕКЦИИ ЭНДОТЕЛИАЛЬНОЙ ДИСФУНКЦИИ | 2011 |
|
RU2527689C2 |
Настоящая группа изобретения относится к медицине, а именно к кардиологии, и касается лечения хронической сердечной недостаточности. Для этого вводят фармацевтическую композицию, содержащую активированную - потенцированную форму сверхмалых доз антител к рецептору ангиотензина II и активированную - потенцированную форму сверхмалых доз антител к эндотелиальной NO - синтазе. Это обеспечивает улучшение качества жизни и повышение толерантности к физическим нагрузкам у данной группы больных. 2 н. и 9 з.п.ф-лы, 2пр., 2 таб.
1. Способ лечения хронической сердечной недостаточности, путем введения в организм лекарственного средства на основе активированной-потенцированной формы сверхмалых доз аффинно очищенных антител к рецептору ангиотензина II, приготовленную путем многократного последовательного разведения и внешнего воздействия, характеризующийся тем, что дополнительно одновременно и сочетано вводят активированную-потенцированную форму сверхмалых доз аффинно очищенных антител к эндотелиальной NO-синтазе.
2. Способ по п.1, характеризующийся тем, что используют активированную-потенцированную форму антител к С-концевому фрагменту AT1-рецептора ангиотензина II и активированную-потенцированную форму антител к эндотелиальной NO-синтазе.
3. Способ по п.1 или п.2, характеризующийся тем, что активированную-потенцированную форму антител к С-концевому фрагменту AT1-рецептора ангиотензина II и активированную-потенцированную форму антител к эндотелиальной NO-синтазе используют в виде активированного-потенцированного водного или водно-спиртового раствора каждого компонента, полученного в процессе последовательного многократного разведения в водном или водно-спиртовом растворителе и промежуточного внешнего механического воздействия - вертикального встряхивания.
4. Способ лечения по п.1 или п.2, характеризующийся тем, что используют фармацевтическую композицию, приготовленную в виде единого лекарственного препарата - одной лекарственной формы, которая включает смесь различных гомеопатических разведении антител к С-концевому фрагменту AT1-рецептора ангиотензина II в сочетании со смесью различных гомеопатических разведении антител к эндотелиальной NO-синтазе.
5. Способ лечения по п.1 или п.2, характеризующийся тем, что используют фармацевтическую композицию на основе активированной-потенцированной формы сверхмалых доз аффинно очищенных антител к С-концевому фрагменту AT1-рецептора ангиотензина II и к эндотелиальной NO-синтазе в сочетании с известными стандартными лекарственными средствами, применяемыми для лечении заболеваний сердечно-сосудистой системы следующих групп: ингибиторы АПФ в т.ч. комбинированные, диуретики, β-адреноблокаторы, нитраты, сердечные гликозиды, антагонисты кальция, гиполипидемические средства, антиагреганты, антигипоксанты, антикоагулянты.
6. Лекарственное средство для лечения хронической сердечной недостаточности по п.1 на основе активированной-потенцированной формы сверхмалых доз аффинно очищенных антител к рецептору ангиотензина II, характеризующееся тем, что выполнено в виде фармацевтической композиции и дополнительно содержит в качестве усиливающего компонента активированную-потенцированную форму антител к эндотелиальной NO-синтазе.
7. Лекарственное средство по п.6, характеризующееся тем, что активированную-потенцированную форму антител к рецептору ангиотензина II и к эндотелиальной NO-синтазе используют в виде активированного-потенцированного водного или водно-спиртового раствора, полученного в процессе последовательного многократного разведения матричного раствора соответствующих антител в водном или водно-спиртовом растворителе и промежуточного внешнего механического воздействия - вертикального встряхивания.
8. Лекарственное средство по п.6 или п.7, характеризующееся тем, что фармацевтическая композиция выполнена в твердой лекарственной форме и содержит эффективное количество нейтрального носителя, насыщенного смесью активированной-потенцированной формы антител к рецептору ангиотензина II и активированной-потенцированной формы антител к эндотелиальной NO-синтазе, и фармацевтически приемлемые добавки.
9. Лекарственное средство по п.6 или п.7, характеризующееся тем, что водные или водно-спиртовые растворы активированных-потенцированных форм антител к рецептору ангиотензина II и к эндотелиальной NO-синтазе получены путем многократного последовательного разведения и промежуточного внешнего воздействия из матричных растворов аффинно очищенных антител к рецептору ангиотензина Пик эндотелиальной NO-синтазе с концентрацией 0,5÷5,0 мг/мл.
10. Лекарственное средство по п.6 или п.7, характеризующееся тем, что каждый из компонентов сверхмалых доз аффинно очищенных антител используют в виде смеси различных, преимущественно сотенных, гомеопатических разведении.
11. Лекарственное средство по п.8, характеризующееся тем, что фармацевтически приемлемые добавки включают лактозу, целлюлозу микрокристаллическую и магния стеарат.
| СПОСОБ КОРРЕКЦИИ ПАТОЛОГИЧЕСКИХ ИММУННЫХ РЕАКЦИЙ И ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2001 |
|
RU2195317C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМБИНАЦИЯ ЭТИЛМЕТИЛГИДРОКСИПИРИДИНА СУКЦИНАТА И ПИРИДОКСИНА, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И СПОСОБ ЛЕЧЕНИЯ | 2008 |
|
RU2405552C2 |
| US 20090088435 A1 02.04.2009 | |||
| АГЕЕВ Ф.Т | |||
| и др | |||
| "Эндотелиальная дисфункция и сердечная недостаточность: патогенетическая связь и возможности терапии ингибиторами ангиотензинпревращающего фермента" | |||
| Перекатываемый затвор для водоемов | 1922 |
|
SU2001A1 |
Авторы
Даты
2014-07-20—Публикация
2011-03-17—Подача