Изобретение относится к области медицины и может быть использовано для повышения эффективности лечения ожирения, преимущественно экзогенно-конституционального, и в том числе в сочетании с нарушениями липидного обмена, включая метаболический синдром.
Согласно данным Международной рабочей группы по проблеме ожирения (International Obesity Task Force), более 300 млн. человек на нашей планете страдают ожирением, а еще 800 млн. человек имеют избыточную массу тела. При сохранении таких высоких темпов роста заболеваемости к 2025 г. ожидается двукратное увеличение числа страдающих ожирением.
Избыточный вес и ожирение являются одной из наиболее распространенных проблем в развитых странах и повышают риск развития заболеваний сердечно-сосудистой системы, дислипидемии, сахарного диабета 2 типа, онкологических заболеваний.
Среди современных препаратов, используемых для снижения массы тела, можно выделить три основные группы - препараты периферического и центрального действия усиливающие «сжигание» калорий, препараты, снижающие поступления жиров в организм, и препараты центрального действия (регуляторы аппетита) (Padwal R.S., Majumdar S.R., Drug treatments for obesity: orlistat, sibutramine, and rimonabant. Lancet 2007; 366 (9555):71-7). Препараты всех групп имеют множественные побочные эффекты, в связи с чем их применение в повседневной практике крайне ограничено. Таким образом, разработка и внедрение новых безопасных и эффективных препаратов для снижения массы тела являются весьма актуальными.
Из уровня техники известна композиция для лечения ожирения и резистентности к инсулину при регуляции уровня глюкозы в крови, содержащая соединение, выделенное из натурального источника и очищенное, выбираемое из группы, включающей антоцианин, антоцианидин и их смеси (RU 2359689 С2, A61K 36/45, 10.09.2008). Однако при использовании данной композиции возникает сложностью подбора дозы.
Также известно использование лекарственного препарата на основе антител к липазе для лечения ожирения у млекопитающих (WO/1999/002187, A61K 38/00, 21.01.1999). Однако данный препарат может вызывать выраженные побочные эффекты и вследствие этого применяется в незначительном числе случаев.
Из уровня техники известно лекарственное средство для перорального лечения ожирения, сахарного диабета и других заболеваний, сопровождающихся нарушением толерантности к глюкозе, содержащее антитела к бета-субъединице рецептора инсулина в активированной форме (WO 2007/149010 A1, A61K 39/395, 27.12.2007). Однако данное лекарственное средство эффективно только у части больных, имеющих инсулинорезистентность.
Изобретение направлено на создание эффективного способа лечения ожирения и связанных с ним метаболических расстройств без побочных эффектов и соответствующего лекарственного средства центрального и периферического действия на основе антител к известному каннабиноидному рецептору человека (Ken Mackie. Cannabinoid receptors as therapeutic targets. The Annual Review of Pharmacology and Toxicology, 2006. 46:101-122).
Решение поставленной задачи обеспечивается тем, что в способе лечения ожирения и/или излишнего веса и сопутствующих метаболических расстройств путем введения в организм лекарственного средства, согласно изобретению, лекарственное средство содержит активированную - потенцированную форму антител к каннабиноидному рецептору человека в виде активированного - потенцированного водного или водно-спиртового раствора, полученного в процессе последовательного многократного разведения в водном или водно-спиртовом растворителе и промежуточного внешнего механического воздействия - вертикального встряхивания.
Возможно использование активированной - потенцированной формы антител к цельной молекуле каннабиноидного рецептора I типа человека или полипептидному фрагменту с последовательностью, выбираемой, например, из следующей группы:
QRGTQKSIII;
EKLQSVCSDIFPHIDETYL;
IQRGTQKSIIIHTSEDGKVQVTRPDQARM;
KAHSHAVRMIQRGTQKSIIIHTSEDGKVQVTRPDQARMDIRLAKT;
MSVSTDTSAEAL;
TEFYNKSLSSFKENEENIQCGENFMDIECFMVLNPS;
AQPLDNSMGDSDCLHKHAN;
GTQKSIIIHTSEDG;
MTAGDNPQLVPADQVNITEFYNKSLSSFKENEENIQCGENFMDIECFMVLN;
VVAFCLMWTIAIVI;
EFYNKSLSSFKENEENIQCGENFMDIECFMVLNPSQQLAIAVLSLTL;
NEENIQCGE;
GSPFQEKMTAGDNPQLVPADQVNITEFYNKSL;
AYKRIVTRPKAVVAFCLMWTIAIVIAVLPLLGWN.
При этом активированную - потенцированную форму антител к каннабиноидному рецептору I типа человека используют в сверхмалой дозе, полученной сверхразведением исходного матричного раствора в 10012, 10030 и 100200 раз.
Решение поставленной задачи обеспечивается также тем, что лекарственное средство для лечения ожирения, согласно изобретению, содержит активированную - потенцированную форму антител к цельной молекуле или полипептидному фрагменту каннабиноидного рецептора человека в виде активированного - потенцированного водного или водно-спиртового раствора, полученного в процессе последовательного многократного разведения в водном или водно-спиртовом растворителе и промежуточного внешнего механического воздействия - вертикального встряхивания.
При этом водный или водно-спиртовой раствор активированной - потенцированной формы антител к каннабиноидному рецептору I типа человека получен путем многократного последовательного разведения и промежуточного внешнего воздействия из матричного раствора аффинно очищенных антител к каннабиноидному рецептору I типа человека с концентрацией 0,5÷5,0 мг/мл.
Предпочтительно лекарственное средство содержит активированную - потенцированную форму антител к каннабиноидному рецептору I типа человека в сверхмалой дозе, приготовленной из матричного раствора, сверхразведенного в 10012, в 10030 в 100200, что эквивалентно смеси сотенных гомеопатических разведений С12, С30 и С200.
Кроме того, лекарственное средство может быть выполнено в твердой лекарственной форме и содержать эффективное количество нейтрального носителя, насыщенного водным или водно-спиртовым раствором активированной - потенцированной формы антител к каннабиноидному рецептору I типа человека, и фармацевтически приемлемые добавки.
При этом фармацевтически приемлемые добавки могут включать лактозу, целлюлозу микрокристаллическую и магния стеарат.
Заявленный технический результат обусловлен тем, что известные каннабиноидные рецепторы 1 типа и эндоканнабиноиды представляют собой единую систему в гипоталамусе, которая, воздействуя на специфические участки мезолимбической области головного мозга, влияет на чувство насыщения и регулирует аппетит и, как результат, потребление пищи. При этом предложенное лекарственное средство на основе активированной - потенцированной формы антител к каннабиноидному рецептору человека (т.е. формы антител к каннабиноидному рецептору человека, приготовленной по гомеопатической технологии потенцирования путем многократного последовательного разведения и промежуточного внешнего воздействия - вертикального встряхивания, которая обладает активностью в фармакологических моделях и/или клинических методах лечения ожирения), обеспечивает получение неожиданного терапевтического эффекта, который заключается в нормализации углеводного и липидного обмена, приводящей к снижению массы тела без побочных явлений, что подтверждено экспериментально на адекватных (валидных) моделях.
Кроме того, полученное в соответствии с изобретением техническое решение расширяет арсенал лекарственных средств центрального действия, предназначенных для эффективного лечения ожирения и/или излишнего веса без побочных эффектов. В том числе и в составе комплексной терапии.
Лекарственное средство приготовляют, преимущественно, следующим образом.
Для приготовления гомеопатически активированной - потенцированной формы действующего вещества - антител к каннабиноидному рецептору человека используют моноклональные или, преимущественно, поликлональные антитела, которые могут быть получены по известным технологиям - методикам, описанным, например, в книге: Иммунологические методы, под ред. Г. Фримеля, М., «Медицина», 1987, с. 9-33; или, например, в статье Laffly Е., Sodoyer R. Hum. Antibodies. Monoclonal and recombinant antibodies, 30 years after. - 2005 - Vol. 14. - N 1-2. P. 33-55.
Моноклональные антитела получают, например, с помощью гибридомной технологии. Причем начальная стадия процесса включает иммунизацию, основанную на принципах, уже разработанных при приготовлении поликлональных антисывороток. Дальнейшие этапы работы предусматривают получение гибридных клеток, продуцирующих клоны одинаковых по специфичности антител. Их выделение в индивидуальном виде проводится теми же методами, что и в случае поликлональных антисывороток.
Поликлональные антитела могут быть получены активной иммунизацией животных. Для этого по специально разработанной схеме животным делают серию инъекций требуемым в соответствии с изобретением веществом - антигеном: каннабиноидным рецептором I типа человека. В результате проведения такой процедуры получают моноспецифическую антисыворотку с высоким содержанием антител, которую и используют для получения активированной - потенцированной формы. При необходимости проводят очистку антител, присутствующих в антисыворотке, например, методом аффинной хроматографии, путем применения фракционирования солевым осаждением или ионообменной хроматографии.
Для иммунизации кроликов можно использовать в качестве иммуногена (антигена) адъювант и цельную молекулу каннабиноидного рецептора I типа человека следующей последовательности:
MKSILDGLAD TTFRTITTDL LYVGSNDIQY EDIKGDMASK
LGYFPQKFPL TSFRGSPFQE KMTAGDNPQL VPADQVNITE
FYNKSLSSFK ENEENIQCGE NFMDIECFMV LNPSQQLAIA
VLSLTLGTFT VLENLLVLCV ILHSRSLRCR PSYHFIGSLA
VADLLGSVIF VYSFIDFHVF HRKDSRNVFL FKLGGVTASF
TASVGSLFLT AIDRYISIHR PLAYKRIVTR PKAVVAFCLM
WTIAIVIAVL PLLGWNCEKL QSVCSDIFPH IDETYLMFWI
GVTSVLLLFI VYAYMYILWK AHSHAVRMIQ RGTQKSIIIH
TSEDGKVQVT RPDQARMDIR LAKTLVLILV VLIICWGPLL
AIMVYDVFGK MNKLIKTVFA FCSMLCLLNS TVNPIIYALR
SKDLRHAFRS MFPSCEGTAQ PLDNSMGDSD CLHKHANNAA
SVHRAAESCI KSTVKIAKVT MSVSTDTSAE AL
или, преимущественно, полипептидный фрагмент каннабиноидного рецептора I типа человека с последовательностью, выбираемой, например, из следующей группы:
QRGTQKSIII;
EKLQSVCSDIFPHIDETYL;
IQRGTQKSIIIHTSEDGKVQVTRPDQARM;
KAHSHAVRMIQRGTQKSIIIHTSEDGKVQVTRPDQARMDIRLAKT;
MSVSTDTSAEAL;
TEFYNKSLSSFKENEENIQCGENFMDIECFMVLNPS;
AQPLDNSMGDSDCLHKHAN;
GTQKSIIIHTSEDG;
MTAGDNPQLVPADQVNITEFYNKSLSSFKENEENIQCGENFMDIECFMVLN;
VVAFCLMWTIAIVI;
EFYNKSLSSFKENEENIQCGENFMDIECFMVLNPSQQLAIAVLSLTL;
NEENIQCGE;
GSPFQEKMTAGDNPQLVPADQVNITEFYNKSL;
AYKRIVTRPKAVVAFCLMWTIAIVIAVLPLLGWN
Перед отбором крови за 7-9 дней проводят 1-3 внутривенных инъекций для повышения уровня антител. В процессе иммунизации у кроликов отбирают небольшие пробы крови для оценки количества антител. Максимальный уровень иммунного ответа на введение большинства растворимых антигенов достигается через 40-60 дней после первой инъекции. После окончания первого цикла иммунизации кроликов в течение 30 дней дают восстановить здоровье и проводят реиммунизацию, включающую 1-3 внутривенные инъекции. Для получения антисыворотки из иммунизированных кроликов собирают кровь в центрифужную пробирку объемом 50 мл. С помощью деревянного шпателя удаляют со стенок пробирки образовавшиеся сгустки и помещают палочку в сгусток, образовавшийся в центре пробирки. Кровь помещают в холодильник (температура 4°C) на ночь. На следующий день удаляют сгусток, прикрепившийся к шпателю, и центрифугируют оставшуюся жидкость при 13000 g в течение 10 мин. Супернатант (надосадочная жидкость) является антисывороткой. Полученную антисыворотку, которая должна быть желтого цвета, хранят до использования в замороженном состоянии при температуре -70°C. Для выделения из антисыворотки антител к каннабиноидному рецептору I типа человека производят абсорбцию на твердой фазе в следующей последовательности:
1. 10 мл антисыворотки кролика разбавляют в 2 раза 0,15 М NaCl добавляют 6,26 г Na2SO4, перемешивают и инкубируют 12-16 ч при 4°C;
2. выпавший осадок удаляют центрифугированием, растворяют в 10 мл фосфатного буфера и затем диализуют против того же буфера в течение ночи при комнатной температуре;
3. после удаления осадка центрифугированием раствор наносят на колонку с ДЭАЭ-целлюлозой, уравновешенную фосфатным буфером;
4. фракцию антител определяют, измеряя оптическую плотность элюата при 280 нм.
Затем производят очистку антител методом аффинной хроматографии путем прикрепления полученных антител к каннабиноидному рецептору I типа человека, который находится на нерастворимом матриксе с последующим элюированием концентрированными растворами соли.
Полученный, таким образом, буферный раствор поликлональных кроличьих антител к каннабиноидному рецептору I типа человека, очищенных на антигене, с концентрацией 0,5÷5,0 мг/мл, предпочтительно 2,0÷2,5 мг/мл, используют в качестве матричного (первичного) раствора для последующего приготовления активированной - потенцированной формы.
Активированную - потенцированную форму действующего вещества - антител к каннабиноидному рецептору I типа человека в сверхмалой дозе готовят путем равномерного уменьшения концентрации в результате последовательного разведения 1 части упомянутого матричного раствора в 9 частях (для десятичного разведения) или в 99 частях (для сотенного разведения С) или в 999 частях (для тысячного разведения М) нейтрального водного или водно-спиртового растворителя с многократным вертикальным встряхиванием - потенцированием (или "динамизацией") каждого полученного разведения и использованием отдельных емкостей для каждого последующего разведения до получения требуемой потенции - кратности разведения по гомеопатическому методу (см., например, В. Швабе "Гомеопатические лекарственные средства", М., 1967 г., с. 14-29).
Например, для приготовления 12-го сотенного разведения С12 одну часть упомянутого матричного раствора антител к каннабиноидному рецептору I типа человека с концентрацией 2,5 мг/мл разводят в 99 частях нейтрального водного или водно-спиртового растворителя и многократно (10 и более раз) вертикально встряхивают - потенцируют полученное 1-е сотенное С1 разведение. Из 1-го сотенного С1 разведения приготовляют 2-е сотенное разведение С2. Данную операцию повторяют 11 раз, получая 12-е сотенное разведение С12. Таким образом, 12-е сотенное разведение С12 представляет собой раствор, полученный разбавлением последовательно в разных емкостях 12 раз 1-й части исходного матричного раствора антител к каннабиноидному рецептору I типа человека с концентрацией 2,5 мг/мл в 99-ти частях нейтрального растворителя, т.е. раствор, полученный сверхразведением исходного матричного раствора в 10012 раз. Аналогичные операции с соответствующей кратностью разведения проводят для получения разведении С30 и С200.
При использовании в качестве биологически активного жидкого компонента смеси различных гомеопатических, преимущественно сотенных, разведений, действующего вещества каждый компонент состава (например, С12, С30, С200) приготовляют раздельно по описанной выше технологии до их предпоследнего разведения (соответственно, до получения С11, С29, С199) и затем вносят в соответствии с составом смеси в одну емкость по одной части каждого компонента и смешивают с требуемым количеством растворителя (соответственно, с 97 частями для сотенного разведения). При этом получают активированную - потенцированную форму антител к каннабиноидному рецептору I типа человека в сверхмалой дозе, полученной сверхразведением исходного матричного раствора в 10012, 10030, 100200 раз, эквивалентной смеси сотенных гомеопатических разведении С12, С30, С200.
Возможно использование действующего вещества в виде смеси других различных гомеопатических разведений, например, десятичных и/или сотенных (D20, С30, С100 или С12, С30, С50 и т.д.), эффективность которых определяют экспериментально.
При потенцировании вместо встряхивания в процессе уменьшения концентрации также можно осуществлять внешнее воздействие ультразвуком, электромагнитным или иным физическим воздействием.
Заявленное лекарственное средство может быть использовано в твердой лекарственной форме, которая содержит эффективное количество гранул нейтрального носителя - лактозы, насыщенного путем пропитывания до насыщения водным или водно-спиртовым раствором активированной - потенцированной формы антител к каннабиноидному рецептору I типа человека, и фармацевтически приемлемые добавки, включающие, преимущественно, лактозу, целлюлозу микрокристаллическую и магния стеарат. Твердую лекарственную форму приготовляют таблетированием из таблеточной массы, которая содержит 8÷10 масс. частей гранул лактозы, орошенных в псевдоожиженном-кипящем слое водным или водно-спиртовым раствором активированной - потенцированной формы антител к каннабиноидному рецептору I типа человека, 2÷7 масс. частей увлажненной 70% спиртом лактозы, пропитанных до насыщения водным или водно-спиртовым раствором активированной - потенцированной формы антител к каннабиноидному рецептору I типа человека, и фармацевтически приемлемые добавки, включающие 75÷95 масс. частей чистой лактозы, 8÷15 масс. частей микрокристаллической целлюлозы и 0,8÷1,2 масс. частей стеарата магния. Масса таблетки может составлять 150÷500 мг. Предпочтительно использовать таблетки массой 250÷300 мг, которые включают 3,0÷6,0 мг/табл активированной - потенцированной формы водно-спиртовых разведений субстанции - действующего вещества поликлональных кроличьих антител к каннабиноидному рецептору I типа человека, очищенных на антигене, в сверхмалой дозе, полученной сверхразведением исходного матричного раствора в 10012, 10030, 100200 раз, эквивалентной смеси сотенных гомеопатических разведений С12, С30, С200 (сверхмалые дозы - СМД анти-КР).
Предпочтительно для эффективного лечения ожирения или излишнего веса рекомендуется применять заявленное лекарственное средство по 1-2 таблетке (держать во рту до полного растворения) 2-4 раза в день.
Для проведения экспериментальных исследований были использованы поликлональные антитела, приготовленные по заказу специализированной фармацевтической фирмой.
Пример 1.
Для лечения ожирения неоднократно проводились попытки использовать психоактивные вещества (антидепрессанты, ноотропы, различные эндорфины, энкефалины, эндоканнабиноиды), воздействующие на систему позитивного эмоционального подкрепления и, прежде всего, функциональную активность «центров удовольствия» в латеральном гипоталамусе. Однако из-за выраженных побочных действий, развития привыкания (пристрастия) эффективное и одновременно безопасное лекарственное средство центрального действия до сих пор не создано.
Заявленное лекарственное средство по направленности действия - рецептор каннабиноидный 1 типа - является центральным, но в связи использованием особой технологии потенцирования оказывает воздействие на рецептор, приводящее к его сенситизации и вследствие этого - повышению чувствительности к эндогенным каннабиноидам.
Данный эффект подтверждается следующим экспериментом: проведено изучение влияния препарата на основе активированной - потенцированной формы поликлональных кроличьих антител к каннабиноидному рецептору I типа человека, очищенных на антигене, в сверхмалой дозе, полученной сверхразведением исходного матричного раствора в 10012, 10030, 100200 раз, эквивалентной смеси сотенных гомеопатических разведений С12, С30, С200 (сверхмалые дозы - СМД анти-КР) на функциональное состояние каннабиноидного рецептора 1 типа (in vitro) в 2 режимах: в режиме агониста и в режиме антагониста.
Режим агониста:
Перед внесением в лунки микропланшета (96-луночный планшет, объем лунки 250 μl) клетки суспендировали в буфере HBSS (Invitrogen), содержащем 20 мМ HEPES (рН=7.4). Клетки преинкубировали в течение 10 минут при комнатной температуре вместе с добавлением 20 мкл препарата СМД анти-КР. После преинкубации в лунки добавляли активатор аденилатциклазы NKH477. Клетки инкубировали в течение 10 минут 37°С и лизировали. В лунки вносили флуоресцентный акцептор (цАМФ, меченный D2) и флуоресцентный донор (антитела к цАМФ, меченные криптатом европия).
В качестве базального контроля вместо препарата СМД анти-КР суспензию клеток преинкубировали в присутствии HBSS буфера (20 мкл). В качестве стимулированного контроля вместо СМД анти-КР суспензию клеток преинкубировали в присутствии референсного агониста СР 55940 (20 мкл).
Функциональную активность (по концентрации цАМФ) оценивали методом гомогенной флуоресценции с временным разрешением (HTRF). Интенсивность флуоресценции в базальном контроле принимается за фоновую и ее значение вычитается из интенсивностей флуоресценции в опыте (СМД анти-КР) и контроле (СР 55940):
Измеренный специфический ответ клетки на введение СМД анти-КР вычисляется по формуле: интенсивность флуоресценции в опыте (СМД анти-КР) - интенсивность флуоресценции в базальном контроле.
Измеренный специфический ответ клетки на введение референсного агониста (СР 55940) вычисляется по формуле: интенсивность флуоресценции в контроле (СР 55940) - интенсивность флуоресценции в базальном контроле.
Результаты выражаются в процентах от специфического ответа клетки на введение референсного агониста в стимулированном контроле:
% ответа референсного агониста = ((измеренный специфический ответ/специфический ответ в контроле на введение референсного агониста)×100%).
Режим антагониста:
Перед внесением в лунки микропланшета (96-луночный планшет, объем лунки 250 µl) клетки суспендировали в буфере HBSS (Invitrogen), содержащем 20 мМ HEPES (рН=7.4). Клетки преинкубировали в течение 5 минут при комнатной температуре вместе с добавлением 20 мкл препарата СМД анти-КР. После добавления в лунки референсного агониста СР 55940 клетки инкубировали 10 минут при комнатной температуре. Далее в лунки добавляли активатор аденилатциклазы NKH477. Клетки инкубировали в течение 10 минут 37°С и лизировали. В лунки вносили флуоресцентный акцептор (цАМФ, меченный D2) и флуоресцентный донор (антитела к цАМФ, меченные криптатом европия).
В качестве базального контроля вместо СМД анти-КР суспензию клеток преинкубировали в присутствии референсного антагониста AM 281 (20 мкл). В лунки с базальным контролем не добавляли референсный агонист СР 55940. В качестве стимулированного контроля суспензию клеток преинкубировали в присутствии HBSS буфера, содержащего 20 мМ HEPES (рН=7.4), и референсного агониста СР 55940 (20 мкл).
Функциональную активность (по концентрации цАМФ) оценивали методом гомогенной флуоресценции с временным разрешением (HTRF). Интенсивность флуоресценции в базальном контроле принимается за фоновую и ее значение вычитается из интенсивностей флуоресценции в опыте (СМД анти-КР) и контроле (СР 55940):
Измеренный специфический ответ клетки на введение СМД анти-КР вычисляется по формуле: интенсивность флуоресценции в опыте (СМД анти-КР) - интенсивность флуоресценции в базальном контроле.
Измеренный специфический ответ клетки на введение референсного агониста (СР 55940) вычисляется по формуле: интенсивность флуоресценции в контроле (СР 55940) - интенсивность флуоресценции в базальном контроле.
Результаты выражаются в процентах ингибирования специфического ответа клетки на введение референсного агониста (СР 55940) в контроле:
% ингибирования ответа референсного агониста = 100% - ((измеренный специфический ответ/специфический ответ в контроле на введение референсного агониста)×100%)
В результате исследований показано (см. таблицу 1), что СМД анти-КР изменяет функциональную активность каннабиноидного рецептора 1 типа, оцененную по концентрации внутриклеточной цАМФ.
Образец (сверхмалые дозы антител к каннабиноидному рецептору I типа (смесь гомеопатических разведений С12+С30+С200)) проявляет свойства агониста каннабиноидному рецептору I типа, выраженность модифицирующего эффекта которого составляет 21% от эффекта стандартного агониста СР55940 (эффект стандартного агониста принимается за 100%).
Пример 2.
Для исследования свойств заявленного лекарственного средства был использован водный раствор активированной - потенцированной формы поликлональных кроличьих антител к каннабиноидному рецептору I типа человека, очищенных на антигене, в сверхмалой дозе, полученной сверхразведением исходного матричного раствора в 10012, 10030, 100200 раз эквивалентной смеси сотенных гомеопатических разведений С12, С30, С200 (сверхмалые дозы - СМД анти-КР).
В исследовании использованы 40 мышей-самцов линии С57В1 (вес на начало исследования 13,5-15,5 г). 10 мышей получали обычный стандартный корм (стандартная диета), 30 мышей - стандартный корм с высококалорийными добавками (высококалорийная диета) и одновременно либо дистиллированную воду (контроль, 0,4 мл/кг), либо сибутрамин1 (1Меридиа 10 мг капсулы, Abbott GMBH, Германия) (10 мг/кг), либо СМД анти-КР (0,4 мл/кг). Все препараты вводили внутрижелудочно 1 раз в день в течение 5 месяцев. До начала введения препаратов (исходно), а также каждую неделю после начала их введения измеряли потребление мышами корма. Потребление корма оценивали как среднее количество пищи (г), потребленного мышью за 1 и 2 месяца исследования, и как среднее количестве корма на 10 г массы тела мыши.
Мыши в группе низкокалорийной диеты потребляли в среднем за весь период наблюдения на 15% меньше корма, чем мыши на высококалорийной диете (табл.2). И сибутрамин и СМД анти-КР снижали потребление корма, причем эффект сибутрамина был выражен несколько выше: препарат снижал потребление корма в неделю на 19,3% (р<0,05), в то время как СМД анти-КР - только на 9,3% относительно контроля (р>0,05). На Таблице 2 представлены результаты влияния СМД анти-КР и сибутрамина на потребление пищи мышами С57В1 (средние значения за 5 месяцев наблюдения), М±m.
Однако при анализе динамики потребления корма были выявлены следующие особенности. На двадцатой неделе эксперимента мыши на высокожировой диете, получавшие СМД анти-КР, потребляли больше корма по сравнению с первой неделей эксперимента, что показано на Таблице 3.
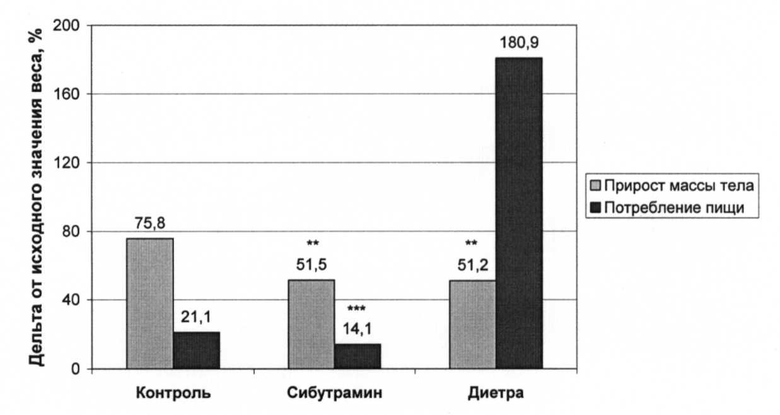
При этом у мышей, получавших СМД анти-КР, по-прежнему наблюдалось снижение прироста массы тела на 51,2% относительно контроля. Сибутрамин на последней двадцатой неделе эксперимента также снижал прирост массы тела на 51,5% по сравнению с контрольной группой.
Пример 3.
Для исследования свойств заявленного лекарственного средства был использован водный раствор активированной - потенцированной формы поликлональных кроличьих антител к каннабиноидному рецептору I типа человека, очищенных на антигене, в сверхмалой дозе, сверхмалой дозе, полученной сверхразведением исходного матричного раствора в 10012, 10030, 100200 раз, эквивалентной смеси сотенных гомеопатических разведений С12, С30, С200 (сверхмалые дозы - СМД анти-КР).
В исследовании использованы 33 мышей-самцов линии С57В1 (вес на начало исследования 13,09±0,738 г). Мыши получали модифицированную диету с высоким (45%) содержанием жира и одновременно либо дистиллированную воду (контроль, 0,2 мл/кг), либо сибутрамин (10 мг/кг), либо антител к каннабиноидному рецептору I типа человека, очищенных на антигене, смесь сотенных гомеопатических разведений С12+С30+С200 (сверхмалые дозы - СМД анти-КР) (0,2 мл/кг). Все препараты СМД анти-КР вводили внутрижелудочно 1 раз в день в течение 2 месяцев. До начала введения препаратов (исходно), а также каждую неделю после начала их введения измеряли вес мышей на электронных весах Philips Cucina HR 239016 (Венгрия). Прирост массы тела мышей оценивали в % от исходного.
Начиная с 6 недели введения, СМД анти-КР снижала прирост массы тела мышей, содержащихся на высокожировой диете. В таблице 3 представлена средняя еженедельная масса (г) мышей С57В16, получавших высокожировую диету и СМД анти-КР (0,2 мл/мышь) или сибутрамин 10 мг/кг) (М±m). На Таблице 4 показан прирост массы тела мышей.
Таким образом, препарат СМД анти-КР снижает пророст массы тела мышей на высокожировой диете, снижая потребление ими пищи и не уступает по эффективности известному широко используемому для снижения массы тела препарату сибутрамину.
Пример 4.
Для исследования свойств заявленного лекарственного средства были использованы таблетки массой 300 мг, пропитанные водно-спиртовым раствором (6 мг/табл.) активированной - потенцированной формы поликлональных кроличьих антител к каннабиноидному рецептору I типа человека, очищенных на антигене, в сверхмалой дозе, полученной сверхразведением исходного матричного раствора в 10012, 10030, 100200 раз, эквивалентной смеси сотенных гомеопатических разведений С12, С30, С200 (сверхмалые дозы - СМД анти-КР).
В исследование принимали участие 80 добровольцев (20 мужчин и 60 женщин) в возрасте от 20 до 69 лет (средний возраст составил 40,2±1,26 года), 68,7% из которых страдали избыточной массой тела или ожирением (I-III степени), которые принимали по 1-й таблетке 2 раза в день. В Таблице 5 представлены демографические и антропометрические показатели пациентов, включенных в исследование. В анализ безопасности были включены данные всех пациентов, участвовавших в исследовании (n=80). В течение всего периода наблюдения за пациентами отмечалась хорошая переносимость препарата. Нежелательные явления отсутствовали. Все пациенты исследуемых групп завершили лечение в сроки, установленные протоколом исследования, досрочно выбывших пациентов не было. При оценке влияния СМД анти-КР на изменение массы тела испытуемых выявлено, что использование препарата привело к снижению массы тела 56 (70%) пациентов. У 24 (30%) пациентов вес оставался неизменным, или незначительно увеличивался, однако следует отметить, что среди указанных пациентов 14 (17,5%) исходно имели нормальную массу тела (ИМТ<25 кг/м2).
В динамике наблюдения у пациентов, ответивших на терапию, отмечалось статистически достоверное снижение массы тела (р<0,001), которое уже через 15 дней приема СМД анти-КР составило 1,1 кг (1,3%), а через 1 месяц достигло 1,9 кг (2,2%) от исходного значения, что показано в Таблице 6.
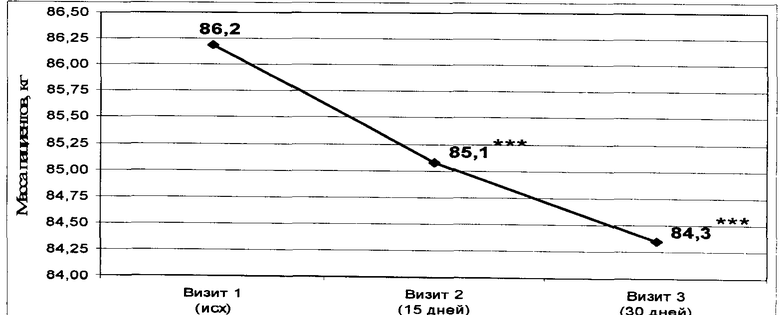
Также в указанной группе пациентов уже через 1 неделю после начала приема СМД анти-КР отмечалось статистически значимое (р<0,001) уменьшение окружности талии и окружности бедер, которое к окончанию терапии достигло 2,3% и 2,7% соответственно. В Таблице 7 представлена динамика изменения окружности талии и окружности бедер.
При оценке выраженности чувства голода пациентов по Визуальной аналоговой шкале (ВАШ) исходно показано, что наибольшая интенсивность чувства голода отмечалось у пациентов в вечернее время. По окончании 1 месяца приема СМД анти-КР уровень голода в вечерние часы снизился достоверно (р<0,001) с 49,4±3,75 до 42,0±4,32 баллов. В утреннее и дневное время также отмечалась тенденция к снижению выраженности чувства голода (с 20,5±3,23 до 13,6±1,78 баллов в утренние часы, с 44,7±3,45 до 27,3±3,72 баллов в дневные часы), которая, однако, не достигла статистически значимых значений к окончанию терапии, что возможно связано с недостаточным числом пациентов и умеренными исходными значениями показателей.
Таким образом, в проведенном клиническом исследовании СМД анти-КР подтверждена высокая переносимость препарата, нежелательные явления при приеме препарата отсутствовали.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ ОЖИРЕНИЯ И СОПУТСТВУЮЩИХ МЕТАБОЛИЧЕСКИХ РАССТРОЙСТВ | 2013 |
|
RU2582393C2 |
| СПОСОБ ВОЗДЕЙСТВИЯ НА ФУНКЦИОНАЛЬНУЮ АКТИВНОСТЬ КАННАБИНОИДНОГО РЕЦЕПТОРА | 2013 |
|
RU2557971C2 |
| Способ лечения патологического синдрома и лекарственное средство центрального и периферического действия для лечения патологического синдрома | 2011 |
|
RU2610438C2 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ОСНОВЕ ВЕЩЕСТВА, ВЛИЯЮЩЕГО НА ЭНДОКАННАБИНОИДНУЮ СИСТЕМУ | 2013 |
|
RU2568896C2 |
| СПОСОБ ЛЕЧЕНИЯ ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ | 2011 |
|
RU2523451C2 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ, СОПРОВОЖДАЮЩИХСЯ НЕЙРОТОКСИЧЕСКИМИ НАРУШЕНИЯМИ, И СПОСОБ ЛЕЧЕНИЯ ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ, СОПРОВОЖДАЮЩИХСЯ НЕЙРОТОКСИЧЕСКИМИ НАРУШЕНИЯМИ | 2010 |
|
RU2446821C2 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ, СОПРОВОЖДАЮЩИХСЯ НЕЙРОТОКСИЧЕСКИМИ НАРУШЕНИЯМИ, И СПОСОБ ЛЕЧЕНИЯ ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ, СОПРОВОЖДАЮЩИХСЯ НЕЙРОТОКСИЧЕСКИМИ НАРУШЕНИЯМИ | 2010 |
|
RU2522499C2 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ | 2014 |
|
RU2595807C2 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ГРИППА У ПТИЦ | 2007 |
|
RU2332236C1 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ НЕВРОЛОГИЧЕСКО-ПОВЕДЕНЧЕСКИХ РАССТОРОЙСТВ РАЗВИТИЯ И СПОСОБ ЛЕЧЕНИЯ НЕВРОЛОГИЧЕСКО-ПОВЕДЕНЧЕСКИХ РАССТРОЙСТВ РАЗВИТИЯ | 2011 |
|
RU2536230C2 |
Группа изобретений относится к медицине, а именно к эндокринологии, и касается лечения ожирения и сопутствующих метаболических расстройств. Для этого вводят лекарственное средство, содержащее активированную-потенцированную форму антител к каннабиноидному рецептору человека I типа. Это обеспечивает эффективное снижение веса и коррекцию метаболических нарушений при отсутствии побочных эффектов. 2 н. и 4 з.п. ф-лы, 7 табл., 4 пр.
1. Способ лечения ожирения и сопутствующих метаболических расстройств путем введения в организм лекарственного средства, характеризующийся тем, что лекарственное средство содержит активированную-потенцированную форму антител к каннабиноидному рецептору человека в виде активированного-потенцированного водного или водно-спиртового раствора, полученного в процессе последовательного многократного разведения матричного раствора в водном или водно-спиртовом растворителе и промежуточного внешнего механического воздействия - вертикального встряхивания.
2. Способ по п.1, характеризующийся тем, что используют активированную-потенцированную форму антител к цельной молекуле или полипептидному фрагменту каннабиноидного рецептора I типа человека.
3. Лекарственное средство для лечения ожирения и сопутствующих метаболических расстройств по п.1, характеризующееся тем, что содержит активированную-потенцированную форму антител к каннабиноидному рецептору человека I типа в виде активированного-потенцированного водного или водно-спиртового раствора, полученного в процессе последовательного многократного разведения в водном или водно-спиртовом растворителе и промежуточного внешнего механического воздействия - вертикального встряхивания.
4. Лекарственное средство по п.3, характеризующееся тем, что водный или водно-спиртовой раствор активированной-потенцированной формы антител к каннабиноидному рецептору I типа человека получен путем многократного последовательного разведения и промежуточного внешнего воздействия из матричного раствора аффинно очищенных антител к каннабиноидному рецептору I типа человека с концентрацией 0,5-5,0 мг/мл.
5. Лекарственное средство по п.3, характеризующееся тем, что выполнено в твердой лекарственной форме и содержит эффективное количество гранул нейтрального носителя, насыщенного водным или водно-спиртовым раствором активированной-потенцированной формы антител к каннабиноидному рецептору I типа человека, и фармацевтически приемлемые добавки.
6. Лекарственное средство по п.5, характеризующееся тем, что фармацевтически приемлемые добавки включают лактозу, целлюлозу микрокристаллическую и магния стеарат.
| СПОСОБ ЛЕЧЕНИЯ ИЛИ ПРЕДУПРЕЖДЕНИЯ ОЖИРЕНИЯ | 2002 |
|
RU2314121C9 |
| ПОЛИПЕПТИД ОЖИРЕНИЯ (ОВ)(ВАРИАНТЫ), ЕГО АНАЛОГ (ВАРИАНТЫ) И СЛИТЫЙ БЕЛОК (ВАРИАНТЫ), ИЗОЛИРОВАННАЯ МОЛЕКУЛА НУКЛЕИНОВОЙ КИСЛОТЫ, МОЛЕКУЛА ДНК, РЕКОМБИНАНТНЫЙ ВЕКТОР КЛОНИРОВАНИЯ, РЕКОМБИНАНТНЫЙ ВЕКТОР ЭКСПРЕССИИ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, МОНОКЛОНАЛЬНОЕ И ПОЛИКЛОНАЛЬНОЕ АНТИТЕЛО | 1995 |
|
RU2273645C9 |
| MX 2008002028 A (AMYLIN PHARMACEUTICALS INC) 27.03.2008 | |||
| БУТРОВА С.Л | |||
| и др | |||
| "Лечение ожирения" Российский медицинский журнал, 2001, т | |||
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| УСТАНОВКА ДЛЯ КАРБЮРИРОВАНИЯ ВОЗДУХА С АВТОМАТИЧЕСКИМ ВКЛЮЧЕНИЕМ ВОЗДУШНОГО НАСОСА | 1924 |
|
SU1140A1 |
| ЛАРИОНОВА В.И | |||
| и др | |||
| ЩИТОВОЙ ДЛЯ ВОДОЕМОВ ЗАТВОР | 1922 |
|
SU2000A1 |
| Найдено | |||
Авторы
Даты
2015-06-10—Публикация
2010-07-15—Подача