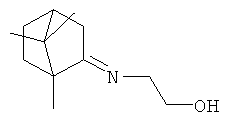
Изобретение относится к химии и медицине, а именно к лекарственным средствам, конкретно к известному соединению 1,7,7-триметилбицикло[2.2.1]гептан-2-илиден-аминоэтанолу формулы I (включая его пространственные изомеры, в том числе оптически активные формы):
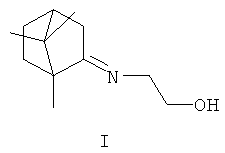
у которого выявлена новая биологическая активность, заключающаяся в ингибировании репродукции вируса гриппа.
Вирусы гриппа представляют серьезную угрозу для здоровья человека в связи с легкостью передачи через верхние дыхательные пути. Разработка новых лекарственных средств лечения и профилактики вирусных инфекций - одна из актуальных задач современной фармакологии и медицинской химии, поскольку глобализация, мобильность населения и характер передачи вирусных инфекций способствуют их активному распространению по всему миру. Эпидемия «птичьего» гриппа H5N1 (1997-2006) и затем пандемия гриппа 2009 г., вызванная вирусом свиного происхождения A(H1N1)pdm09, сделали настоятельно необходимой ревизию состояния проблемы с разработкой противовирусных препаратов [Киселев О.И. Химиопрепараты и химиотерапия гриппа. Санкт-Петербург, Росток, 2012].
Противовирусные средства для лечения гриппа представляют собой крайне ограниченную группу лекарственных препаратов, причем для большинства из них известна лекарственная резистентность. Создание противовирусных препаратов - это ближайшая перспектива развития медицинской науки в области создания средств лечения и профилактики вирусных инфекций [Еропкин М.Ю., Зарубаев В.В. Современное состояние разработок новых антивирусных препаратов против гриппа и ОРВИ // Фармацевтический бюллетень, 2012, №1, с. 68]. Благодаря особенностям организации генома (отсутствие механизма коррекции ошибок репликации) и короткому жизненному циклу вирус гриппа обладает высокой скоростью мутаций. Как результат антигенная структура вируса в высокой степени подвержена изменениям в результате селективного давления иммунной системы организма-хозяина. Кроме того, применение химиопрепаратов воспринимается вирусом как фактор селекции, в результате чего также происходит формирование устойчивых штаммов. Эти два процесса приводят к появлению вариантов вирусов, способных избегать как активности нейтрализующих антител, и тем самым ускользать от иммунного ответа организма, так и преодолевать действие химиопрепаратов, исходно направленных на определенный этап репродукции вируса. При этом каждый тип вируса имеет свой механизм приспособления к химическому препарату [Ison M.G. Antivirals and resistance: influenza virus // Current Opinion in Virology. 2011, V. 1, P.563-573].
Ингибировать репродукцию вируса гриппа можно на разных стадиях его жизненного цикла, на этом основана классификация противовирусных средств по механизму действия.
Известны ингибиторы нейраминидазы, зарегистрированные в России: Озельтамивир (Тамифлю) и Занамивир (Реленза), а также используемые в США: Перамивир (Рапиакта) и Ланинамивир (Инавир), которые действуют на этапе почкования вновь синтезированных вирионов гриппа из оболочки клетки, блокируя отщепление частиц вирусного потомства от поверхности клеток [Ison MG. Clinical use of approved influenza antivirals: therapy and prophylaxis. // Influenza Other Respi Viruses. 2013; 7 Suppi 1:7-13]. Практика применения ингибиторов нейраминидазы в лечении гриппа показала, что высокая эффективность этой группы препаратов ограничена ранней стадией инфекции.
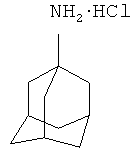
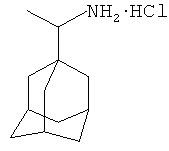
Известны противовирусные препараты прямого действия на репликацию вирусов гриппа, например, препарат Ремантадин (α-метил-1-адамантилметиламина гидрохлорид) и Амантадин (1-аминоадамантан) [Davies, W.L.; Grunert, R.R.; Haff, R.F.; McGahen, J.W.; Neumayer, E.M.; Paulshock, M.; Watts, J.C.; Wood, T.R.; Hermann, E.C.; Hoffmann, C.E. Antiviral Activity of 1-Adamantanamine (Amantadine) // Science, 1964, V.144, P.862]. Данные соединения блокируют белок М2 вируса гриппа, препятствуя тем самым процессу расщепления гемагглютинина и слияния мембран вируса и лизосомальной вакуоли [Scholtissek С., Quack G., Klenk H.D., Webster R.G. // Antiviral Res. 1998, V.37, P.83-95]. Механизм действия этих препаратов изучен достаточно полно [Cady S.D., Schmidt-Rohr К., Wang J., Soto C.S., DeGrado W.F., Hong M.H. Structure of the amantadine binding site of influenza М2 proton channels in lipid bilayers // Nature. 2010. Vol.463. P.689-692]. Белок M2 в виде тетрамера является ионным каналом, функционирующим в качестве протонного насоса. Известно, что данные препараты необратимо ингибируют M2-белок и тем самым останавливают поток протонов через мембраны вирионов, что необходимо для снижения pH, расщепления гемагглютинина и реализации его функции как фактора слияния вирусной и клеточной мембран. Ремантадин блокирует активность ионных каналов и нарушает тем самым процесс «раздевания» вируса.
Вместе с тем, конкретная локализация сайта связывания ремантадина с M2-белком однозначно не выяснена. Анализ этого комплекса при помощи ядерного магнитного резонанса обнаружил четыре равноценных сайта связывания, доступных со стороны липидного бислоя между трансмембранными участками тетрамера M2. При этом ремантадин ингибирует ионный канал аллостерически, т.е. не связываясь непосредственно с активным центром, а стабилизируя закрытое состояние M2 [Cross ТА, Dong H, Sharma M, Busath DD, Zhou HX. М2 protein from influenza A: from multiple structures to biophysical and functional insights. Curr Opin Virol. 2012; 2: 128-33].
Альтернативная модель предполагает прямое блокирование ионной поры молекулой ремантадина, которая гидрофобным адамантильным участком координируется с аминокислотой серии в 31 положении белка. Замена данной аминокислоты традиционно обуславливает развитие лекарственной устойчивости вирусов гриппа [Cady SD, Schmidt-Rohr К, Wang J, Soto CS, Degrade WF, Hong M. Structure of the amantadine binding site of influenza М2 proton channels in lipid bilayers. Nature. 2010; 463: 689-92]. Первая модель, таким образом, дает большую, по сравнению со второй, свободу для разработки ингибиторов вирусного M2-белка в силу менее жестких стерических ограничений.
Адамантановые препараты значительно дешевле и проще в производстве, чем коммерчески доступные ингибиторы нейраминидазы, что делает их более доступными для лечения и профилактики гриппа среди населения. Однако в настоящее время в результате широкого использования адамантановых препаратов (ремантадин и амантадип) значительно утрачены их противовирусные свойства в отношении вирусов гриппа A. Потерю активности в основном связывают с мутацией в трансмембранном домене белка М2 вируса гриппа.
Интерес к соединениям, действующим на белок M2, особенно усилился в связи с открытием аминоспиро[5,5]ундеканов и спиропиперидинов [Duque M.D., Torres E., Valverde E., et. al. Inhibitors of the M2 channel of influenza A virus // Recent Advances in Pharmaceutical Sciences, 2011, P.35-64]. Адамантаны как класс каркасных соединений явились стартовой основой в конструировании большого класса противовирусных препаратов [Zoidis G., Kolocouris N., Naesens L., Clercq E.D. Design and synthesis of 1,2-annulated adamantane piperidines with anti-influenza virus activity // Bioorganic&Medicinal Chemistry, 2009, N.17, P.1534]. Кроме хорошо известного ремантадина, сравнимой с ним противовирусной активностью обладает достаточно обширный класс соединений.
Известны средства на основе каркасных соединений - бананинов -ингибиторы репликации коронавируса SARS, являющиеся наиболее близкими к классическим адамантанам [Tanner J.A., Zheng B.J., Zhou. J., et. al. The Adamantane-Derived Bananins Are Potent Inhibitors of the Helicase Activities and Replication of SARS Coronavirus // Chemistry & Biology, 2005, V.12, P.303].
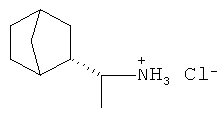
Каркасные соединения остаются привлекательными в качестве основы для дизайна противовирусных препаратов. Так, известно средство на основе дейтифорина (2-(1'-аминоэтил)бицикло[2.2.1]гептана, являющееся одним из наиболее интересных препаратов на основе природных бициклических каркасных соединений - борнанов [Патент RU 2448692 С2, опубл. 27.04.2012].
Известны средства, синтезированные на основе природного пинанового остова, являющиеся ингибиторами вируса гриппа [Zhao X, Li С, Zeng S, Hu W. Discovery of highly potent agents against influenza A virus // Eur J Med Chem. 2011; 46:52-7], превосходящими вирусингибирующее действие препарата сравнения - амантадина в 240 раз при тестировании на амантадин-чувствительном штамме вируса. Однако авторы работы не приводят данные по токсичности исследуемых соединений, в связи с чем нельзя говорить о высоком химиотерапевтическом индексе синтезированных веществ.
Наиболее близким к заявляемому соединению - прототипом является дейтифорин, представляющий собой фармацевтическую соль 2-(1'-аминоэтил)бицикло[2.2.1]гептана общей формулы II:
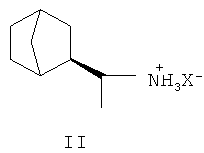
Недостатком известного соединения является невысокая противовирусная активность.
Задачей изобретения является выявление нового эффективного ингибитора репродукции вируса гриппа, которое может быть синтезировано из доступных реагентов.
Технический результат: повышение эффективности подавления репродукции вируса гриппа и расширение ассортимента ингибиторов репродукции вируса гриппа для преодоления лекарственной устойчивости современных вирусных штаммов.
Поставленная задача решается применением известного соединения, представляющего собой 1,7,7-триметилбицикло[2.2.1]гептан-2-илидеи-аминоэтанол формулы I (включая его пространственные изомеры, в том числе оптически активные формы):
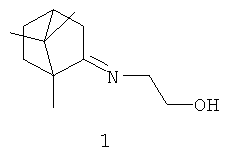
у которого выявлена новая биологическая активность, заключающаяся в ингибирующем действии на репродукцию вируса гриппа.
Соединение I известно и описано в работе [Gavrilov К., Tsarev V., Zheglov S., et. al., N-Bidentate Phosphites with a Chiral Ketimine Fragment, Their Application in Enantioselective Allylic Substitution and Comparison with Phosphine Analogues // Synthesis -2007, V.11, P.1717-1723].
Предлагаемое соединение может быть получено следующим образом.
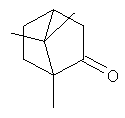
В качестве исходного для синтеза целевого соединения I используют камфору и аминоэтанол. В результате взаимодействия камфоры с аминоспиртом получают 1,7,7-триметилбицикло[2.2.1]гептан-2-илиден-аминоэтанол формулы I. Реакцию проводят в условиях азеотропной отгонки воды с использованием в качестве катализатора безводного ZnCl2.
Исследования биологической активности соединения I, проведенные в отношении вируса гриппа, показали крайне высокую эффективность данного вещества как ингибитора репродукции этого вируса.
Полученные количественные показатели ингибирования подтверждают высокую степень подавления репликации вируса гриппа в культуре клеток MDCK соединением I, превышающую тот же показатель у эталонов сравнения - амантадина и ремантадина в 120 и более раз. Использование в качестве препаратов сравнения адамантановых производных обусловлено сходством структур: наличием каркасных структурных фрагментов как в соединении I, так и в эталонах сравнения.
Изобретение иллюстрируется следующими примерами:
Пример 1.
Получение 1,7,7-триметилбицикло[2.2.1]гептан-2-илиден-аминоэтанола.
К раствору 10 г камфоры (0.065 моль) в толуоле (30 мл) добавляют 8 мл аминоэтанола (0.13 моль) в 20 мл толуола и 0.1 г безводного ZnCl2. Реакцию ведут при постоянном кипении реакционной массы в течение 28 ч в аппарате Сокслета, заполненном прокаленными молекулярными ситами 4A. Контроль над реакцией осуществлялся по ГЖХ и ХМС. Реакционную смесь промывают насыщенным раствором Nad, экстрагируют СН2Сl2, сушат Na2SO4, удаляют растворитель. Соединение I очищают вакуумной перегонкой, т.кип. 112-114°C при 2 мм рт.ст., выделяют с выходом 82%. Спектр ЯМР совпадает с опубликованным ранее [Gavrilov К., Tsarev V., Zheglov S., Korlyukov A., Antipin M., Davankov V. P,N-Bidentate Phosphites with a Chiral Ketimine Fragment, Their Application in Enantioselective Allylic Substitution and Comparison with Phosphine Analogues // Synthesis - 2007, - V.11, P.1717-1723]. Т.пл. 66-67°C.
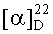
Пример 2.
Изучение токсичности заявленного соединения I.
Токсичность продуктов была изучена в отношении клеток MDCK. Клетки MDCK сеяли в 96-луночные планшеты и культивировали при 37°C в среде MEM с добавлением 10% сыворотки крупного рогатого скота в атмосфере 5% CO2 (в газопроточном инкубаторе Sanyo-175) до состояния монослоя. Из исследуемого соединения I готовили маточный раствор концентрации 10 мг/мл в диметилсульфоксиде, после чего готовили серию двукратных разведении препаратов в среде MEM от 1000 до 3,75 мкг/мл. Растворенный препарат вносили в лунки планшетов и инкубировали 2 суток при 37°C. По истечении этого срока клетки промывали 2 раза по 5 минут фосфатно-солевым буфером и количество живых клеток оценивали при помощи микротетразолиевого теста (МТТ). С этой целью в лунки планшетов добавляли по 100 мкл раствора (5 мг/мл) 3-(4,5-диметилтиазолил-2) 2,5-дифенилтетразолия бромида (ICN Biochemicals Inc., Aurora, Ohio) на физиологическом растворе. Клетки инкубировали при 37°C в атмосфере 5% CO2 в течение 2 часов и промывали 5 минут фосфатно-солевым буфером. Осадок растворяли в 100 мкл на лунку ДМСО, после чего оптическую плотность в лунках планшетов измеряли па многофункциональном ридере Victor 1420 (Perkin Elmer, Finland) при длине волны 535 нм. По результатам теста для каждого продукта определяли 50% цитотоксическую дозу (CTD50), т.е. концентрацию соединения, вызывающую гибель 50% клеток в культуре. Результаты приведены в таблице.
Пример 3.
Изучение противовирусной активности соединения I. Определение противовирусной активности препарата проводили на клетках MDCK в 96-луночных планшетах для клеточных культур. Соединение растворяли в поддерживающей среде для клеток, вносили в лунки панелей с клеточным монослоем и инкубировали в течение 1 часа при 36°C в атмосфере 5% CO2.
Из вируссодержащей жидкости (штамм A/California/07/09 (H1N1)pdm09) готовили серию десятикратных разведении от 10-1 до 10-7, добавляли в лунки с препаратами и инкубировали при 36°C в течение 48 часов в атмосфере 5% CO2. По окончании срока инкубации 100 мкл культуральной жидкости смешивали с равным объемом 1% куриных эритроцитов в отдельных планшетах с круглым дном. Учет результатов проводили через 60 минут инкубации при 20°C. За титр вируса принимали величину, обратную десятичному логарифму наибольшего разведения исходного вируса, способного вызвать положительную реакцию гемагглютинации в лунке и выражали в количестве 50% инфекционных доз (ID50). Вирусингибирующее действие исследуемых соединений оценивали по снижению титра вируса в опыте по сравнению с контролем. На основании полученных данных рассчитывали 50% ингибирующую дозу ED50, то есть концентрацию препарата, снижающую уровень вирусной репликации вдвое (на 0,3 lg ID50), и химиотерапевтический индекс, или индекс селективности (SI), представляющий собой отношение CTD50 к ED50.
В процессе исследования ингибирования репродукции вируса гриппа соединением I и эталонами сравнения (амантадином, ремантадином и дейтифорином) были получены результаты, приведенные в таблице.
Из таблицы видно, что соединение I проявляет выраженную противовирусную активность наряду с низкой токсичностью. Химиотерапевтический индекс соединения I превышает таковой у препаратов сравнения в 100 и более раз.
Преимуществом данного соединения является его активность в отношении ремантадин-устойчивого штамма вируса гриппа A/California/07/09 (H1N1)pdm09, что свидетельствует о перспективности применения его для терапии современных эпидемически актуальных вирусов, подавляющее большинство которых устойчивы к ремантадину.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИМИНОПРОИЗВОДНЫЕ КАМФОРЫ - ЭФФЕКТИВНЫЕ ИНГИБИТОРЫ РЕПРОДУКЦИИ ВИРУСА ГРИППА (штамм A/California/07/09 (H1N1)pdm09) | 2014 |
|
RU2554934C1 |
| ИМИНОПРОИЗВОДНЫЕ КАМФОРЫ, СОДЕРЖАЩИЕ АРОМАТИЧЕСКИЙ ИЛИ ГЕТЕРОАРОМАТИЧЕСКИЙ ФРАГМЕНТ, - ИНГИБИТОРЫ РЕПРОДУКЦИИ ВИРУСА ГРИППА (штамм A/California/07/09 (H1N1)pdm09) | 2015 |
|
RU2607451C1 |
| СИММЕТРИЧНЫЕ ДИИМИНЫ НА ОСНОВЕ КАМФОРЫ - ИНГИБИТОРЫ РЕПРОДУКЦИИ ВИРУСА ГРИППА (ШТАММ A/California/07/09 (H1N1)pdm09) | 2013 |
|
RU2520967C1 |
| ПРИМЕНЕНИЕ (1S,3aR,4R,7aS)-N-(2,2,4,7a-ТЕТРАМЕТИЛОКТАГИДРО-1,4-ЭТАНОИНДЕН-3а-ИЛ)-АЦЕТАМИДА В КАЧЕСТВЕ ИНГИБИТОРА РЕПРОДУКЦИИ ВИРУСА ГРИППА | 2016 |
|
RU2616255C1 |
| ПРИМЕНЕНИЕ АЛИФАТИЧЕСКИХ ИМИНОПРОИЗВОДНЫХ КАМФОРЫ В КАЧЕСТВЕ ЭФФЕКТИВНЫХ ИНГИБИТОРОВ РЕПРОДУКЦИИ ВИРУСА ГРИППА штамм A/California/07/09 (H1N1) pdm09 и A/Puerto Rico/8/34 (H1N1) | 2016 |
|
RU2651754C1 |
| 6,13,13-ТРИМЕТИЛ-6,8,9,12-ТЕТРАГИДРО-6,9-МЕТАНОАЗЕПИНО[2,1-b]ХИНАЗОЛИН-10(7Н)-ОН В КАЧЕСТВЕ ИНГИБИТОРА ВИРУСОВ ГРИППА А | 2017 |
|
RU2664331C1 |
| ФАРМАЦЕВТИЧЕСКИЕ СОЛИ АМИНОБИЦИКЛО[2.2.1]ГЕПТАНОВ КАК ИНГИБИТОРЫ ТРАНСКРИПЦИОННОГО ФАКТОРА NF-KB С ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ (ВАРИАНТЫ) И ИХ ПРИМЕНЕНИЕ | 2009 |
|
RU2448692C2 |
| ПРОИЗВОДНЫЕ 1-(1-АДАМАНТИЛ)ЭТИЛАМИНА И ИХ ПРОТИВОВИРУСНАЯ АКТИВНОСТЬ | 2011 |
|
RU2461544C1 |
| Аминокислотные производные 2-норборнануксусной кислоты и их противогриппозная активность | 2017 |
|
RU2676699C1 |
| 1-[ω-АРИЛОКСИАЛКИЛ(БЕНЗИЛ)]ЗАМЕЩЕННЫЕ 2-АМИНОБЕНЗИМИДАЗОЛЫ, ОБЛАДАЮЩИЕ АКТИВНОСТЬЮ В ОТНОШЕНИИ ВИРУСА ГРИППА | 2012 |
|
RU2570906C2 |
Изобретение относится к области фармацевтики и медицины и касается применения 1,7,7-триметилбицикло[2.2.1]гептан-2-илиден-аминоэтанола формулы I в качестве ингибитора репродукции вируса гриппа. Изобретение обеспечивает повышение эффективности подавления репликации вируса гриппа и снижение токсичности. 1 табл., 3 пр.
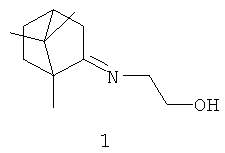
Применение 1,7,7-триметилбицикло[2.2.1]гептан-2-илиден-аминоэтанола формулы I:

в качестве ингибитора репродукции вируса гриппа.
| ФАРМАЦЕВТИЧЕСКИЕ СОЛИ АМИНОБИЦИКЛО[2.2.1]ГЕПТАНОВ КАК ИНГИБИТОРЫ ТРАНСКРИПЦИОННОГО ФАКТОРА NF-KB С ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ (ВАРИАНТЫ) И ИХ ПРИМЕНЕНИЕ | 2009 |
|
RU2448692C2 |
| СТЕРЕОИЗОМЕРЫ ТРИЦИКЛОДЕКАН-9-ИЛКСАНТОГЕНАТА | 2008 |
|
RU2470915C2 |
| ПРОТИВОВИРУСНЫЙ ПРЕПАРАТ "ПОЛИРЕМ" | 1994 |
|
RU2071323C1 |
| ПОЛИАНИОННЫЕ ПРОИЗВОДНЫЕ НОРБОРНАНА, СПОСОБ ПОЛУЧЕНИЯ И ИНГИБИТОРЫ РЕПРОДУКЦИИ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА НА ИХ ОСНОВЕ | 2004 |
|
RU2281297C2 |
Авторы
Даты
2014-10-10—Публикация
2013-04-22—Подача