Настоящее изобретение относится к химии поликарбонатов, прежде всего к способу получения поликарбоната на границе раздела фаз и переработке по меньшей мере части образующегося при этом содержащего хлорид щелочного металла раствора на дополнительной стадии электролиза хлорида щелочного металла.
Получение поликарбонатов на границе раздела фаз является общеизвестным способом. Поликарбонаты обычно получают непрерывном способом, включающим синтез фосгена и его последующее взаимодействие с бисфенолами в присутствии щелочи и катализатора, предпочтительно азотсодержащего катализатора, агентов обрыва цепей и при необходимости используемых агентов разветвления цепей, которое осуществляют в смеси водной щелочной фазы и фазы органического растворителя на границе раздела фаз.
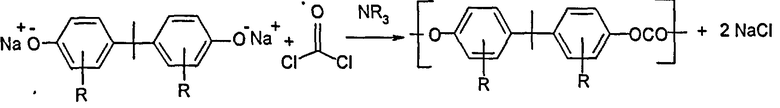
Принцип получения поликарбонатов на границе раздела фаз известен из литературы и описан, например, в Schnell, „Chemistry and Physics of Polycarbonates", Polymer Reviews, Volume 9, Interscience Publishers, New York, London, Sydney, 1964, стр.33-70; D.C.Prevorsek, B.T.Debona, Y.Kesten, Corporate Research Center, Allied Chemical Corporation, Morristown, New Jersey 07960: „Synthesis of Poly(ester Carbonate) Copolymers", Journal of Polymer Science, Polymer Chemistry Edition, Vol.18 (1980), стр.75-90; D.Freitag, U.Grigo, P.R.Muller, N.Nouvertne, BAYER AG, "Polycarbonats", Encyclopedia of Polymer Science and Engineering, Volume 11, Second Edition, 1988, стр.651-692, а также Dres. U. Grigo, K.Kircher, P.R-Muller "Polycarbonate" в Becker/Braun, Kunststoff-Handbuch, Band 3/1, Polycarbonate, Polyacetale, Polyester, Celluloseester, Carl Hanser, Munchen, Wiene, 1992, с.118-145.
Способ синтеза поликарбонатов на границе раздела фаз, называемый также межфазным способом, давно и успешно используют на практике. Он позволяет получать термопластичные поликарбонаты, находящие применение, например, в производстве носителей информации (дисков CD и DVD), а также оптической и медицинской продукции.
В качестве важных качественных характеристик поликарбонатов часто упоминают их высокую термостойкость и низкую склонность к пожелтению. Однако качеству образующейся в процессе их производства отработанной воды до последнего времени уделяется мало внимания. При этом особое значение для возможной дальнейшей переработки отработанной воды, например, на очистной установке или окислением остаточной органики методом озонолиза прежде всего имеет содержание в ней остаточных органических соединений, в частности фенолов. Методы, преимущественно используемые для последующей обработки отработанной воды с целью снижения количества присутствующих в ней фенольных компонентов, приводятся, например, в японской заявке на патент JP 08245780 А (фирма Idemitsu), немецкой заявке на патент DE 19510063 А1 (фирма Bayer), а также в японских заявках на патент JP 03292340 A, JP 03292341 А и JP 02147628 А (фирма Teijin).
Содержание в отработанной воде остаточной органики, например, такой как бисфенолы или используемые, например, в качестве агентов обрыва цепей фенолы, можно ограничить, получая поликарбонаты при избытке фосгена. Однако использование подобной технологии нежелательно по экономическим причинам.
В случае синтеза поликарбонатов при уменьшенном избытке фосгена возникает опасность неполного превращения бисфенола или монофенола и попадания последних в отработанную воду. Кроме того, существует опасность осложнения процессов разделения фаз и промывки, обусловленная присутствием в полимере остаточных поверхностно-активных фенольных ОН-групп. Вследствие этого в некоторых случаях из органической фазы удается экстрагировать не все водорастворимые примеси. Подобное обстоятельство, в свою очередь, может негативно отразиться на качестве целевого продукта.
Таким образом, можно констатировать, что синтез обладающих высоким качеством поликарбонатов непрерывным межфазным способом при одновременном низком содержании остаточной органики в отработанной воде возможен лишь в случае использования значительного избытка фосгена или благодаря последующей обработке отработанной воды, которая, однако, связана с проблемами разделения фаз, а, следовательно, с ущербом качеству поликарбоната, что снижает экономичность способа.
Ближайшим аналогом настоящего изобретения следует считать немецкую заявку на патент DE-A 4227372 тех же заявителей, в описании которой уже приводятся данные относительно аппаратурного оформления предлагаемого в настоящем изобретении способа. Однако в отличие от предлагаемого в настоящем изобретении решения в заявке DE-A 4227372 отсутствуют сведения относительно количеств и прежде всего соотношений между циркулирующими эдуктами, не говоря уже о возможности обеспечения особенно низкого содержания остаточной органики, такой как фенолы и бисфенолы, в отработанной воде посредством особым образом регулируемых количеств и соотношений эдуктов.
Однако указанный выше известный способ требует выполнения дорогостоящих операций очистки отработанной воды, содержащей значительные количества остаточных бисфенолов или фенолов (в дальнейшем называемых также остаточными фенолами), которые могут оказывать опасное воздействие на окружающую среду и удаление которых на очистных сооружениях представляет собой серьезную проблему.
Обычно содержащий хлорид натрия раствор освобождают от растворителей и органических остатков, а затем утилизируют.
Однако из европейской заявки на патент ЕР 1200359 В1 (международной заявки на патент WO 2000/078682 А1) или заявки США на патент US-A 6340736 известно также о возможности очистки содержащих хлорид натрия сточных вод озонолизом и их пригодности для последующего использования на стадии электролиза хлорида натрия. Однако недостатком метода озонолиза являются чрезвычайно высокие затраты.
Согласно европейской заявке на патент ЕР 541114 А2 из потока содержащей хлорид натрия отработанной воды полностью выпаривают воду и остающуюся соль с органическими примесями подвергают тепловой обработке, приводящей к деструкции органических компонентов. При этом особенно предпочтительным является использование инфракрасного излучения. Недостатком предлагаемой в заявке технологии является ее нерентабельность, обусловленная необходимостью полного испарения воды.
Согласно международной заявке на патент WO 03/070639 А1 отработанную воду процесса производства поликарбонатов очищают экстракцией метиленхлоридом, после чего направляют на электролиз хлорида натрия. Однако предлагаемым в указанном изобретении способом можно рекуперировать не более 14% хлорида натрия, присутствующего в отработанной воде производства поликарбонатов, поскольку подача на электролиз больших количеств отработанной воды может привести к нарушению водного баланса процесса электролиза. Условием соблюдения баланса является использование для электролиза хлорида натрия отработанной воды, содержащей 10% NaCl, и транспорт через ионообменную мембрану четырех молей воды на моль натрия.
Типичное содержание хлорида натрия в образующихся при производстве поликарбонатов растворах, содержащих хлорид натрия, составляет от 6 до 10% масс. Таким образом, полностью рекуперировать содержащийся в подобных растворах хлорид натрия не представляется возможным. Из раствора с концентрацией хлорида натрия 10% масс. путем стандартного электролиза хлорида натрия с использованием стандартной ионообменной мембраны, которая обеспечивает транспорт 3,5 молей воды на моль натрия, удается регенерировать лишь около 13% хлорида натрия. Даже при концентрировании содержащего хлорид натрия раствора до насыщения (то есть до концентрации NaCl, составляющей 25%) удавалось бы рекуперировать не более 38% присутствующего в соответствующем насыщенном растворе хлорида натрия. В уровне техники отсутствуют сведения о возможности полной регенерации содержащего хлорид натрия раствора. В соответствии с международной заявкой на патент WO-A 01/38419 содержащий хлорид натрия раствор может быть подвергнут термическому упариванию, что позволяет направлять в электролитическую ячейку высококонцентрированный раствор хлорида натрия. Однако подобное упаривание является чрезвычайно энергоемким и дорогостоящим.
Исходя из рассмотренного выше уровня техники, в основу настоящего изобретения была положена задача предложить способ, позволяющий с высоким выходом получать продукты высокой степени чистоты и одновременно уменьшить негативное воздействие отработанной воды на окружающую среду, соответственно снизить остроту проблем, связанных с переработкой отработанной воды на очистных сооружениях, благодаря максимально возможному повторному использованию хлорида натрия, содержащегося в отработанных водных растворах, которые образуются в процессе производства поликарбонатов.
При регенерации хлорида натрия прежде всего следует уделять внимание необходимости превращения хлорида натрия в хлор, едкий натр и при необходимости водород при минимальном расходе энергии, а следовательно, экономичном использовании ресурсов.
Обнаружено, что при непрерывном получении поликарбонатов взаимодействием бисфенолов с фосгеном в инертном растворителе или смеси инертных растворителей в присутствии основания (оснований) и катализатора (катализаторов) оптимальное повторное использование хлорида натрия, растворенного в образующейся на границе раздела фаз отработанной воде, может быть реализовано без дорогостоящей очистки благодаря тому, что после установления показателя рН в области 8 или менее и простой обработки активированным углем отработанную воду направляют непосредственно на электрохимическое окисление содержащегося в ней хлорида натрия до хлора, едкого натра и при необходимости водорода, причем хлор можно возвращать на стадию синтеза фосгена.
Таким образом, объектом настоящего изобретения является способ получения поликарбоната на границе раздела фаз и переработки, по меньшей мере, части образующегося при этом раствора, содержащего хлорид щелочного металла, на дополнительной стадии электролиза хлорида щелочного металла, который включает следующие стадии:
(a) получение фосгена взаимодействием хлора с монооксидом углерода,
(b) взаимодействие полученного на стадии а) фосгена по меньшей мере с одним бисфенолом в присутствии, по меньшей мере, одного основания, предпочтительно, по меньшей мере, одного содержащего щелочной металл основания, прежде всего основания, содержащего натрий, по меньшей мере, одного катализатора с основным характером и, по меньшей мере, одного органического растворителя, с образованием поликарбоната и раствора, содержащего хлорид щелочного металла, прежде всего хлорид натрия,
(c) выделение и переработку полученного на стадии b) поликарбоната,
(d) отделение остающегося на стадии с) раствора, содержащего хлорид щелочного металла, от остатков растворителя и остатков катализатора прежде всего путем отгонки этого раствора с водяным паром и обработки адсорбентами, прежде всего активированным углем,
(e) электрохимическое окисление, по меньшей мере, части содержащего хлорид щелочного металла раствора стадии d) с образованием хлора, щелочи и при необходимости водорода,
который заключается в том, что при отделении раствора, реализуемом на стадии d) перед его обработкой адсорбентами, показатель рН раствора устанавливают на уровне 8 или ниже, и,
(f) по меньшей мере, часть полученного на стадии е) хлора возвращают на стадию а) синтеза фосгена и/или
(д) по меньшей мере часть полученной на стадии е) щелочи возвращают на стадию b) синтеза поликарбоната.
Реакционную отработанную воду стадии b), содержащую растворенный хлорид щелочного металла, или по меньшей мере часть промывочной воды стадии с) переработки поликарбоната предпочтительно используют совместно.
Пригодными бисфенолами являются дигидроксидиарилалканы общей формулы (I):
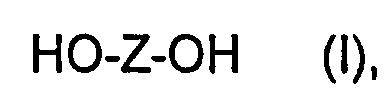
в которой Z означает двухвалентный органический остаток с 6-30 атомами углерода, содержащий одну или несколько ароматических групп. Примерами соединений, которые можно использовать на стадии b) предлагаемого в изобретении способа, являются дигидроксидиарилалканы, такие как гидрохинон, резорцин, дигидроксидифенил, бис-(гидроксифенил)алканы, бис(гидроксифенил)циклоалканы, бис(гидрокси-фенил)сульфиды, бис(гидроксифениловые) эфиры, бис(гидроксифенил)-кетоны, бис(гидроксифенил)сульфоны, бис(гидроксифенил)сульфоксиды, α,α'-бис(гидроксифенил)диизопропилбензолы, а также их алкилированные, алкилированные и галогенированные в ядро производные.
Предпочтительными дигидроксидиарилалканами являются 4,4'-дигидро-ксидифенил, 2,2-бис(4-гидроксифенил)-1-фенилпропан, 1,1-бис(4-гидро-ксифенил)фенилэтан, 2,2-бис(4-гидроксифенил)пропан (бисфенол А, (ВРА)), 2,4-бис(4-гидроксифенил)-2-метилбутан, 1,3-бис[2-(4-гидроксифенил)-2-пропил]бензол (бисфенол М), 2,2-бис(3-метил-4-гидроксифенил)пропан, бис-(3,5-диметил-4-гидроксифенил)метан, 2,2-бис(3,5-диметил-4-гидрокси-фенил)пропан, бис(3,5-диметил-4-гидроксифенил)сульфон, 2,4-бис(3,5-диметил-4-гидроксифенил)-2-метилбутан, 1,3-бис[2-(3,5-диметил-4-гидроксифенил)-2-пропил]бензол, 1,1-бис-(4-гидроксифенил)циклогексан и 1,1-бис-(4-гидроксифенил)-3,3,5-триметилциклогексан (бисфенол ТМС).
Особенно предпочтительными дигидроксидиарилалканами являются 4,4'-дигидроксидифенил, 1,1-бис(4-гидроксифенил)фенилэтан, 2,2-бис(4-гидроксифенил)пропан (бисфенол А (ВРА)), 2,2-бис(3,5-диметил-4-гидрокси-фенил)пропан, 1,1-бис(4-гидроксифенил)циклогексан и 1,1-бис(4-гидрокси-фенил)-3,3,5-триметилциклогексан (бисфенол ТМС).
Указанные выше и другие пригодные дигидроксидиарилалканы описаны, например, в заявках США на патент US-A 2999835, US-A 3148172, US-A 2991273, US-A 3271367, US-A 4982014 и US-A 2999846, немецких заявках на патент DE-А 1570703, DE-A 2063050, DE-A 2036052, DE-A 2211956 и DE-A 3832396, французской заявке на патент FR-А 1561518, a также в монографии Н.Schnell, Chemistry and Physics of Polycarbonates, Interscience Publishers, New-York, 1964, стр.28 и следующие, стр.102 и следующие, и в D.G.Legrand, J.T.Bendler, Handbook of Polycarbonate Science and Technology, Marcel Dekker, New-York, 2000, стр.72 и следующие.
В случае предлагаемого в изобретении получения гомополикарбонатов используют только один бисфенол, в то время как в случае предлагаемого в изобретении получения сополикарбонатов используют несколько бисфенолов, причем используемые бисфенолы, равно как и любые другие используемые для синтеза указанных карбонатов химикаты и вспомогательные вещества, очевидно, могут содержать примеси, образующиеся в процессе их синтеза, а также попадающие в них при межоперационной транспортировке и хранении, хотя и следует стремиться к использованию максимально чистых исходных продуктов.
Следует подчеркнуть, что для осуществления предлагаемого в изобретении способа можно использовать практически любые известные бисфенолы.
В соответствии с предлагаемым в изобретении способом бисфенолы используют в виде водного щелочного раствора, содержание бисфенолов в котором составляет от 10 до 20% масс., предпочтительно от 12,5 до 17,5% масс. в пересчете на общую массу этого раствора. Количество щелочи в подобном водном щелочном растворе составляет от 1,0 до 3,0 молей на моль бисфенола и зависит от растворимости используемого бисфенола.
Фосген предпочтительно используют в виде раствора по меньшей мере в одном органическом растворителе. Содержание фосгена в этом растворе предпочтительно составляет от 7 до 10% масс., особенно предпочтительно от 8 до 9,5% масс.
Пригодные агенты обрыва и агенты разветвления цепей известны из литературы. Некоторые из подобных агентов приведены, например, в немецкой заявке на патент DE-A 3833953. Предпочтительно используемыми агентами обрыва цепей являются фенол или алкилфенолы, прежде всего фенол, п-трет-бутилфенол, изооктилфенол, кумилфенол, их сложные эфиры с хлоругольной кислотой, хлорангидриды монокарбоновых кислот или смеси агентов обрыва цепи. Предпочтительными агентами обрыва цепей являются фенол, кумилфенол, изооктилфенол и пара-трет-бутилфенол.
Примерами соединений, пригодных для использования в качестве агентов разветвления цепей, являются ароматические или алифатические соединения, содержащие более трех гидроксильных групп, предпочтительно три или четыре гидроксильные группы. Примерами особенно пригодных соединений с тремя или более фенольными гидроксильными группами являются флороглюцин, 4,6-диметил-2,4,6-три(4-гидроксифенил)-гептен-2,4,6-диметил-2,4,6-три(4-гидроксифенил)гептан, 1,3,5-три-(4-гидроксифенил)бензол, 1,1,1-три(4-гидроксифенил)этан, три(4-гидроксифенил)фенилметан, 2,2-бис-4,4-бис(4-гидроксифенил)циклогексил]пропан, 2,4-бис(4-гидроксифенилизопропил)фенол и тетра(4-гидроксифенил)-метан.
Примерами других трифункциональных соединений, пригодных для использования в качестве агентов разветвления цепей, являются 2,4-дигидроксибензойная кислота, тримезиновая кислота, цианурхлорид и 3,3-бис(3-метил-4-гидроксифенил)-2-оксо-2,3-дигидроиндол.
Особенно предпочтительными агентами разветвления цепей являются 3,3-бис(3-метил-4-гидроксифенил)-2-оксо-2,3-дигидроиндол и 1,1,1-три(4-гидроксифенил)этан.
Основаниями, используемыми на стадии b) для образования бисфенолята, могут являться гидроксиды щелочных металлов, выбранных из группы, включающей натрий, калий и литий гидроксиды, однако при необходимости можно использовать также гидроксиды щелочноземельных металлов. Предпочтительными основаниями являются гидроксиды щелочных металлов, например, таких как натрий и калий гидроксиды, или смеси этих гидроксидов. Еще более предпочтительным основанием является водный раствор едкого натра. В соответствии с предлагаемым в изобретении способом предпочтительно используют коммерчески доступные растворы едкого натра, особенно предпочтительно содержащие от 20 до 60% масс., еще более предпочтительно от 30 до 50% масс. гидроксида натрия. В предпочтительных вариантах предлагаемого в изобретении способа используют едкий натр, получаемый непосредственно реализуемым методом амальгамирования или мембранным методом электролиза, используемым для получения хлора и щелочного металла.
В качестве используемых на стадии b) катализаторов с основным характером в принципе пригодны любые известные катализаторы для синтеза поликарбонатов на границе раздела фаз. Пригодными катализаторами взаимодействия, реализуемого на стадии b) предлагаемого в изобретении способа, предпочтительно являются третичные амины, например, такие как триэтил амин, трибутиламин или триоктиламин, N-алкилпиперидины, например, такие как N-этилпиперидин, N-метилпиперидин, N-изопропил-пиперидин или N-н-пропилпиперидин, пиридин, четвертичные соли аммония, например, такие как гидроксид, хлорид, бромид, гидросульфат или тетрафтороборат тетрабутиламмония, трибутилбензиламмония или тетраэтиламмония, а также соединения фосфония, которые соответствуют указанным выше аммониевым соединениям. Подобные соединения описаны в литературе и являются типичными, коммерчески доступными и известными специалистам катализаторами межфазных реакций. Общее количество используемых катализаторов составляет от 0,001 до 10% мол., предпочтительно от 0,01 до 8% мол. и особенно предпочтительно от 0,05 до 5% мол. в пересчете на моли используемого бисфенола (используемых бисфенолов).
Пригодный катализатор с основным характером может обладать открытой или циклической структурой, причем особенно предпочтительным катализатором является триэтиламин и этилпиперидин. В соответствии с предлагаемым в изобретении новым способом катализатор предпочтительно используют на стадии b) в виде раствора в органическом растворителе, концентрация которого составляет от 1 до 55% масс.
Фосген можно использовать на стадии b) в жидком или газообразном состоянии или в виде раствора в инертном растворителе.
Инертными органическими растворителями, предпочтительно используемыми на стадии b) предлагаемого в изобретении способа, являются любые известные растворители, которые при температуре 20°С способны растворять по меньшей мере 5% масс. поликарбоната, а также смеси подобных растворителей. Пригодными растворителями являются ароматические и/или алифатические хлорированные углеводороды, предпочтительно дихлорметан, трихлорэтилен, 1,1,1-трихлорэтан, 1,1,2-трихлорэтан, хлорбензол и их смеси. Однако можно использовать также ароматические углеводороды, такие как бензол, толуол, м-ксилол, п-ксилол или о-ксилол, ароматические эфиры, такие как анизол, или смеси указанных растворителей друг с другом или указанными выше хлорированными растворителями. Предпочтительными растворителями являются, например, дихлорметан, толуол, изомеры дихлорэтана и хлорпропана, хлорбензол, хлортолуол или их смеси. В качестве растворителя предпочтительно используют дихлорметан или смесь дихлорметана с хлорбензолом. Особенно предпочтительными растворителями являются дихлорметан и смеси дихлорметана с монохлорбензолом, в еще более предпочтительных вариантах смеси дихлорметана с монохлорбензолом с соотношением компонентов от 20:80 до 75:25 масс.ч.
В течение всего синтеза поликарбоната показатель рН предпочтительно поддерживают в диапазоне от 8,5 до 14, особенно предпочтительно от 9,5 до 13. Регулирование показателя рН осуществляют путем первоначального введения щелочи, используемой в необходимом для растворения бисфенолов количестве, и ее дополнительного дозирования по ходу синтеза. Показатель рН водной фазы предпочтительно посредством однократного или многократного последующего дозирования щелочи, при необходимости осуществляемого во время и после дозирования фосгена, следует поддерживать в щелочном диапазоне, то есть предпочтительно в интервале от 8,5 до 12, особенно предпочтительно от 9,5 до 12, тогда как после добавления катализатора он должен находиться в интервале от 10 до 14, особенно предпочтительно от 10 до 13. Последующее дозирование щелочи при необходимости можно осуществлять также в виде соответствующего последующего дозирования раствора бисфенола в щелочи.
Получаемые предлагаемым в изобретении способом поликарбонаты в виде любых формованных изделий, листов или пленок можно использовать для осуществляемого известными методами применения, например, в автомобильной отрасли или в сфере оптики, а также для производства оптических и магнитооптических носителей данных.
Синтез поликарбоната на стадии b) можно осуществлять в непрерывном или периодическом режиме, причем предпочтительным является использование непрерывного режима, особенно предпочтительно режима поршневого течения в отсутствие существенного обратного перемешивания. Подобный режим может быть реализован, например, в трубчатых реакторах. Смешивание водной и органической фаз можно осуществлять посредством известных смесительных устройств, например, таких как встроенные трубчатые смесители, статические смесители и/или, например, насосы.
Синтез поликарбоната на стадии b) особенно предпочтительно осуществляют в две ступени.
В предпочтительном варианте предлагаемого в изобретении способа молярное отношение используемых на стадии b) фосгена и бисфенола находится в интервале от 1:1,12 до 1:2,22, предпочтительно от 1:1,14 до 1:1,20. Растворитель используют в таком количестве, чтобы по завершении синтеза поликарбонат находился в виде раствора концентрацией от 5 до 60% масс., предпочтительно от 20 до 45% масс.
Реализуемый на стадии b) прежде всего в непрерывном режиме общий синтез поликарбоната (взаимодействие фосгена с бисфенолом (бисфенолами) и дополнительную поликонденсацию) можно осуществлять в котлах с мешалками, трубчатых реакторах, циркуляционных реакторах, каскадах котлов с мешалками или соответствующих комбинированных системах, причем особенно предпочтительным является смешивание водной и органической фаз посредством смесительных устройств, осуществляемое таким образом, чтобы расслоение водной и органической фаз происходило по возможности лишь после полного взаимодействия исходных реагентов, то есть в отсутствие в реакционной системе омыляемого хлора фосгена или сложных эфиров хлоругольной кислоты.
В особенно предпочтительном варианте выполнения стадии b) предлагаемого в изобретении способа непрерывное совмещение органической фазы с водной фазой реализуют в системе аппаратов, включающей снабженный контуром циркуляции теплообменник, а также один или несколько последовательно соединенных котлов, предназначенных для выдержки реагентов, и одну или несколько предназначенных для выдержки реагентов труб (трубчатых реакторов), при необходимости с использованием одного или нескольких смесительных устройств. При этом с целью оптимизации условий осуществления стадии b) в указанной системе аппаратов можно устанавливать особые реакционные условия при одновременном регулировании особого соотношения между дозируемыми в реактор с циркуляционным контуром исходными компонентами и расходом циркулирующей реакционной эмульсии. Подобная технология известна специалистам и описана, например, в европейской заявке на патент ЕР-А 1 249 463.
Непрерывно синтезируемый указанным образом поликарбонат прежде всего характеризуется отличными качественными характеристиками, например низким показателем пожелтения (YI) и низким содержанием концевых фенольных ОН-групп, причем предоставляется возможность одновременного соблюдения низкого содержания остаточной органики (остаточного содержания фенолов) в отработанной воде, что является благоприятным фактором для ее переработки на стадии электролиза.
На стадии с), реализуемой после стадии синтеза b), содержащую поликарбонат органическую фазу обычно промывают предпочтительно водной жидкостью и после каждой операции промывки органическую фазу с максимально возможной полнотой отделяют от водной фазы. Промывку предпочтительно осуществляют деминерализованной водой. В результате промывки и отделения промывочной жидкости обычно получают мутный раствор поликарбоната. Для отделения катализатора в качестве промывочной жидкости используют водные жидкости, например разбавленную минеральную кислоту, такую как соляная или фосфорная кислота, а для дальнейшей очистки деминерализованную воду. Концентрация HCl или Н3РО4 в промывочной жидкости может составлять, например, от 0,5 до 1,0% масс. Органическую фазу предпочтительно промывают, например, по меньшей мере дважды.
В качестве устройств для отделения промывочной жидкости от органической фазы можно использовать в принципе известные разделительные емкости, сепараторы, центрифуги или коагуляторы, а также соответствующие комбинированные системы.
После отделения промывочной жидкости получают поликарбонат чрезвычайно высокой степени чистоты, составляющей более 99,85% (без учета подлежащего отделению растворителя).
В предпочтительном варианте осуществления предлагаемого в изобретении способа отделенные на стадии с) промывочные жидкости после при необходимости реализуемого выделения из них остатков катализатора и/или остатков органического растворителя можно повторно использовать для осуществления предлагаемого в изобретении способа.
При этом выполняемые на стадии с) выделение и переработку образовавшегося на стадии b) поликарбоната предпочтительно можно осуществлять по меньшей мере в две следующие ступени:
аа) разделение содержащей поликарбонат органической фазы и реакционной отработанной воды, содержащей растворенный хлорид щелочного металла,
bb) по меньшей мере однократная, предпочтительно по меньшей мере двукратная, особенно предпочтительно пятикратная промывка полученной на стадии аа) содержащей поликарбонат органической фазы и отделение соответствующей промывочной жидкости.
В некоторых случаях может потребоваться отделение по меньшей мере одной из промывочных жидкостей ступени bb) от остатков катализатора и при необходимости от остатков органического растворителя, которое осуществляют путем установления показателя рН промывочной жидкости в области по меньшей мере 9, предпочтительно по меньшей мере 10, особенно предпочтительно в интервале от 10 до 11 добавлением по меньшей мере одного соединения с основным характером и путем последующей экстракции по меньшей мере одним инертным органическим растворителем или предпочтительно последующей отгонки раствора с водяным паром. В качестве используемых для регулирования показателя рН соединений с основным характером пригодны, например, гидроксиды или карбонаты щелочных или щелочноземельных металлов. Соединения с основным характером можно использовать в твердом состоянии или в виде водных растворов. Предпочтительно используют щелочи, особенно предпочтительно раствор едкого натра.
По меньшей мере часть образующейся на ступени bb) промывочной жидкости предпочтительно можно использовать для частичной замены воды, используемой на стадии b) для приготовления раствора едкого натра, прежде всего для регулирования концентрации этого раствора. В предпочтительном варианте предлагаемого в изобретении способа по меньшей мере часть промывочной жидкости после реализации ступени bb) перед возвращением на стадию b) (стадию синтеза поликарбоната) можно использовать для разбавления приготавливаемой на стадии е) щелочи.
Дополнительным преимуществом предпочтительного варианта предлагаемого в изобретении способа, предусматривающего возвращение отделенных на стадии с) промывочных жидкостей в реализуемый предлагаемым в изобретении способом технологический процесс, является сокращение объема сбрасываемых сточных вод.
После стадии синтеза осуществляют выделение поликарбоната из его раствора в используемом для синтеза органическом растворителе или смеси растворителей, например, в метиленхлориде или смеси метиленхлорида с хлорбензолом.
Поликарбонат можно выделять из указанного раствора испарением растворителя, реализуемым посредством нагревания, вакуумирования или распыления с нагретым газом-носителя. Другими возможными методами выделения поликарбоната являются, например, кристаллизация и осаждение.
В случае, если концентрирование раствора поликарбоната, сопровождаемое его возможным выделением, осуществляют отгонкой растворителя при необходимости путем перегрева и снижения давления, речь идет о методе равновесного мгновенного испарения. Подобный метод известен специалистам и приведен, например, в "Thermische Trennverfahren", издательство VCH, 1988, стр.114. В случае если подлежащий упариванию раствор поликарбоната распыляют совместно с газом-носителем, речь идет о распылительном испарении/распылительной сушке, описанных, например, в Vauck, "Gmndoperationen chemischer Verfahrenstechnik", DeutscherVerlag für Grundstoffindustrie, 2000, 11-е издание, стр.690. Указанные методы описаны в патентной литературе и учебниках и известны специалистам.
В результате термического удаления растворителей (отгонки), соответственно их удаления методом равновесного мгновенного испарения, получают высококонцентрированные расплавы поликарбоната. В случае использования метода равновесного мгновенного испарения полимерные растворы под небольшим избыточным давлением неоднократно нагревают до температуры, превышающей температуру кипения при нормальном давлении, после чего снижают давление соответствующих перегретых растворов в резервуаре с пониженным, например, нормальным давлением. В этом случае к благоприятным результатам скорее приведет концентрирование или иная тепловая обработка полимерного раствора, реализуемая в несколько ступеней (от двух до четырех), нежели слишком длительный перегрев раствора.
Остатки растворителя из полученных указанным выше образом высококонцентрированных расплавов поликарбонатов могут быть удалены либо непосредственной переработкой расплава в испарительных экструдерах (смотри, например, бельгийскую заявку на патент ВЕ-А 866991, европейскую заявку на патент ЕР-А 0411510, заявку США на патент US-A 4980105 и немецкую заявку на патент DE-A 3332065), тонкопленочных выпарных аппаратах (смотри, например, европейскую заявку на патент ЕР-А 00267025), выпарных аппаратах с падающей пленкой или струйных испарителях, либо фрикционным компактированием (смотри, например, европейскую заявку на патент ЕР-А 0460450), при необходимости также с добавлением газа-носителя, такого как азот или диоксид углерода, или с использованием вакуума (смотри, например, европейские заявки на патент ЕР-А 003996, ЕР-А 0256003 и заявку США на патент US-A 4423207), а в другом варианте также последующей кристаллизацией (смотри, например, немецкую заявку на патент DE-A 3429960) и/или «вытапливанием» остатков растворителя в твердой фазе (смотри, например, заявку США на патент US-A 3986269 и немецкую заявку на патент DE-A 2053876). Указанные способы и необходимые для их реализации устройства также описаны в литературе и известны специалистам.
Гранулированный поликарбонат можно получать непосредственным формованием из расплава и последующим гранулированием (если это представляется возможным) или осуществляемым на воздухе или в жидкости (чаще всего в воде) формованием с помощью экструдеров с разгрузочным шнеком. В случае экструзионного формования добавки можно вводить в расплав поликарбоната перед экструдером, при необходимости используя для этого статические смесители, или в сам экструдер посредством дополнительного бокового экструдера.
В другом варианте раствор поликарбоната можно подвергать распылительному испарению. При необходимости нагретый раствор поликарбоната распыляют соплом в сосуд с пониженным давлением или совместно с нагретым газом-носителем, например азотом, аргоном или водяным паром, в сосуд с нормальным давлением. В зависимости от концентрации полимерного раствора в том и другом случае получают порошок (разбавленный раствор) или чешуйки (концентрированный раствор) полимера, последние остатки растворителя из которого при необходимости подлежат удалению указанными выше методами. Затем компаундирующей экструзией с последующим формованием может быть осуществлено гранулирование поликарбоната. В данном случае добавки также можно вводить в расплав вне экструдера или непосредственно в экструдере. Нередко может возникать необходимость в реализации стадии компактирования порошка и чешуек перед экструзией, обусловленная их низкой насыпной плотностью.
Значительные количества поликарбоната могут быть выделены добавлением к промытому и при необходимости дополнительно сконцентрированному раствору поликарбоната осадителя. При этом в качестве осадителя используют вещество, неспособное растворять поликарбонат. Предпочтительным является использование незначительных количеств осадителя, а также при необходимости выдержка между добавлением очередных порций осадителя. Может оказаться благоприятным также использование разных осадителей. Пригодными осадителями являются, например, алифатические или циклоалифатические углеводороды, прежде всего гептан, изооктан или циклогексан, спирты, например, такие как метанол, этанол или изопропанол, кетоны, например, такие как ацетон, или смеси указанных соединений. Осаждение, как правило, осуществляют медленным добавлением полимерного раствора к осадителю. Выделенные осаждением поликарбонаты могут быть подвергнуты переработке в гранулят, как при описанном выше распылительном испарении, и при необходимости снабжены добавками.
В соответствии с другим вариантом продукты осаждения и кристаллизации или находящиеся в тонкодисперсном состоянии аморфные затвердевшие продукты подвергают кристаллизации путем пропускания паров одного или нескольких осадителей поликарбоната при одновременном нагревании до температуры ниже температуры стеклования и дополнительной поликонденсации, осуществляемой с целью повышения молекулярной массы. В случае если при этом образуются олигомеры, при необходимости содержащие разные концевые группы (фенольные группы и группы, производные агентов обрыва цепей), то речь идет о твердофазной поликонденсации.
Очищенные указанными выше методами поликарбонаты обладают отличным качеством, в связи с чем в дальнейшем из них могут быть изготовлены высококачественные формованные детали.
Остающийся после реализации стадии с) отработанный реакционный водный раствор, содержащий хлорид щелочного металла, в предпочтительном варианте освобождают от легколетучих органических примесей, например, таких как остатки используемого для синтеза поликарбоната органического растворителя и при необходимости используемого катализатора, например, путем дистилляции или отгонки с водяным паром. После их удаления остается отработанная вода с высоким содержанием растворенного хлорида натрия (от 5 до 10% масс.) и растворенного карбоната натрия (от 0,3 до 1,5% масс.). При этом карбонаты образуются, например, вследствие гидролиза фосгена, в качестве побочной реакции происходящего при синтезе поликарбоната. Кроме того, отработанная вода содержит органические соединения, например фенолы (в частности, незамещенный фенол, алкилфенолы).
Для последующей обработки предварительно очищенной отработанной воды в качестве адсорбента предпочтительно используют активированный уголь.
Согласно предпочтительному варианту предлагаемого в изобретении способа регулирование (снижение) показателя рН на стадии d) осуществляют посредством соляной кислоты или хлористого водорода. В принципе возможное, однако нежелательное использование недорогой серной кислоты приводило бы к тому, что при снижении показателя рН наблюдалось бы образование сульфата натрия, который при последующем электролизе концентрировался бы в контуре циркуляции анолита. Поскольку, например, ионообменные мембраны в соответствии с рекомендациями их изготовителя можно эксплуатировать только до определенной концентрации сульфата натрия в анолитах, потребовалось бы выводить большее количество анолита, чем в случае использования соляной кислоты или водородхлорида, образующих требуемый хлорид натрия.
Ниже подробно рассматривается технология электролиза хлорида щелочного металла. При этом описание электролиза хлорида натрия следует рассматривать в качестве примера, поскольку, как указано выше, предлагаемый в изобретении способ в принципе применим для переработки хлорида любого щелочного металла (прежде всего хлоридов лития, натрия или калия), однако предпочтительный вариант способа предусматривает использование хлорида натрия, соответственно едкого натра, на предшествующих электролизу стадиях.
Для электролиза содержащих хлорид натрия растворов обычно используют, например, технологию мембранного электролиза (смотри, например, Peter Schmittinger, CHLORINE, издательство Wiley-VCH, 2000). При этом используют двухкамерную электролитическую ячейку, которая состоит из анодного пространства с анодом и катодного пространства с катодом. Анодное и катодное пространства отделены друг от друга ионообменной мембраной. В анодное пространство вводят раствор хлорида натрия, содержание которого обычно составляет более 300 г/л. На аноде протекает окисление ионов хлорида до хлора, который выводят из ячейки с обедненным хлоридом натрия раствором (содержание NaCl составляет около 200 г/л). Под действием электрического поля ионы натрия перемещаются через ионообменную мембрану в катодное пространство. При подобном перемещении в зависимости от типа мембраны каждый моль натрия захватывает от 3,5 до 4 молей воды. Вследствие этого происходит снижение содержания воды в анолите. В отличие от анолитов вода в катодной камере расходуется вследствие протекающего в ней электролиза воды до гидроксидных ионов и водорода. Поступающей в католиты с ионами натрия воды достаточно, чтобы поддерживать концентрацию раствора едкого натра на выходе из катодной камеры в интервале от 31 до 32% масс. при концентрации на входе 30% и плотности тока 4 кА/м2. В катодном пространстве происходит электрохимическое восстановление воды, в результате которого образуются гидроксидные ионы и водород.
В другом варианте в качестве катода можно использовать также газодиффузионный электрод, на котором происходит взаимодействие кислорода с электронами, приводящее к образованию гидроксидных ионов, однако образование водорода отсутствует. Гидроксидные ионы образуют с проникающими в катодное пространство через ионообменную мембрану ионами натрия едкий натр. В катодную камеру обычно вводят раствор едкого натра концентрацией 30% масс., а выводят раствор едкого натра концентрацией от 31 до 32% масс. Целью электролиза является получение раствора едкого натра с максимально высокой концентрацией, поскольку обычно едкий натр хранят и транспортируют в виде раствора концентрацией 50% масс. Однако современные коммерчески доступные мембраны неустойчивы по отношению к щелочному раствору с концентрацией выше 32% масс., в связи с чем едкий натр вынуждены концентрировать термическим упариванием.
В случае электролиза хлорида натрия в анолиты с раствором хлорида натрия вводят дополнительную воду, однако в католиты через мембрану перемещается только вода. В случае если вместе с раствором хлорида натрия в анолиты вводят больше воды, чем может быть транспортировано к католитам, концентрация хлорида натрия в анолите снижается, и электролиз не может больше протекать в непрерывном режиме. При слишком низких концентрациях хлорида натрия возможно протекание побочной реакции образования кислорода.
Для экономичной подачи максимальных количеств содержащих хлорид натрия растворов на электролиз хлорида натрия может быть выгодным повышение интенсивности транспорта воды через мембрану. Согласно заявке США на патент US-A-4025405 повышение интенсивности транспорта воды можно обеспечить благодаря выбору надлежащих мембран. Эффект интенсификации транспорта воды позволяет отказаться от добавления воды, обычно необходимого для обеспечения требуемой концентрации щелочи.
Согласно заявке США на патент US-A-3773634 электролиз при интенсивном транспорте воды через мембрану может протекать при условии, что концентрация щелочи составляет от 31 до 43% масс., а содержание хлорида натрия находится в интервале от 120 до 250 г/л.
Недостатком обоих рассмотренных выше методов является пониженный выход по току.
Согласно предпочтительному варианту предлагаемого в изобретении способа стадию d) (отделение содержащей хлорид натрия реакционной отработанной воды после расслоения фаз и удаления растворителя, а также при необходимости используемого катализатора) осуществляют отгонкой с водяным паром и, после установления необходимого показателя рН обработкой активированным углем.
После этого содержащую хлорид щелочного металла отработанную воду можно направлять непосредственно на электролиз е).
В отличие от уровня техники (международной заявки на патент WO 03/70639 А1), согласно которому для электролиза NaCl можно использовать не более 13% хлорида натрия, содержащегося в отработанной воде производства поликарбонатов, предлагаемый в изобретении способ позволяет рекуперировать из отработанной воды более 13% хлорида натрия.
Согласно другому предпочтительному варианту предлагаемого в изобретении способа предусматривается удаление воды из содержащей хлорид щелочного металла отработанной воды методом концентрирования. Таким образом, предпочтительным является способ, отличающийся тем, что содержащий хлорид щелочного металла раствор стадии а) перед осуществляемым на стадии е) электролизом концентрируют методом мембранной дистилляции, осмотической дистилляции или обратного осмоса.
При этом можно использовать, например, обратный осмос, особенно предпочтительно мембранную дистилляцию или мембранные контакторы (смотри Melin, Rautenbach, Memranverfahren, Springer, Berlin, 2003). Комбинирование предлагаемого в изобретении режима эксплуатации электролитических ячеек с методами концентрирования теоретически позволяет рекуперировать из отработанной воды до 68% хлорида натрия. Это относится к случаю электролиза хлорида натрия, осуществляемого с целью производства лишь такого количества хлора, которое необходимо для синтеза фосгена, и лишь такого количества едкого натра, которое необходимо для получения поликарбоната, причем хлор, предназначенный для иного применения, не производят.
Новый способ предусматривает также возможность осуществления электролиза хлорида щелочного металла, при котором отсутствует образование водорода на катоде, причем катод заменяют газодиффузионным электродом, на котором происходит восстановление кислорода до гидроксидных ионов.
В случае если, например, в месте потребления сопряженного продукта отсутствует потребность в водороде для осуществления химических реакций, можно отказаться от обязательного образования водорода при электролизе. Преимуществом подобного отказа является экономия потребляемой для электролиза энергии, обусловленная пониженным напряжением в случае использования газодиффузионного электрода.
Содержание хлорида натрия в реакционной отработанной воде производства поликарбоната обычно составляет до 10% масс. Концентрация хлорида натрия в случае объединения реакционной отработанной воды с промывочной водой составляет, например, около 6% масс. В случае потребления образующегося при электролизе хлора и едкого натра исключительно для производства поликарбоната переработке электролизом может быть подвергнута лишь незначительная часть содержащей хлорид натрия отработанной воды. Так, например, в случае обычных ионообменных мембран и стандартных рабочих параметров электролиза можно использовать лишь около 7% хлорида натрия, содержащегося в отработанном водном растворе производства поликарбонатов, содержащем 6% масс. хлорида натрия. Стандартными следует считать следующие рабочие параметры электролиза хлорида натрия: концентрация рассола на выходе от 200 до 240 г/л и концентрация едкого натра от 31 до 32% масс. Таким образом, полное рекуперирование образующегося хлорида натрия до последнего времени не представлялось возможным. В то же время концентрирование раствора хлорида натрия термическим испарением воды в настоящее время является нерентабельным, поскольку получаемый хлорид натрия слишком дешев, чтобы его следовало выделять подобным методом.
В соответствии с предлагаемым в изобретении способом из образующейся отработанной воды при содержании в ней 10% масс.NaCl можно рекуперировать значительно больше хлорида натрия, нежели 13%, если выполнять электролиз исключительно с целью получения хлора и едкого натра, потребляемого в производстве поликарбоната. Электролиз хлорида натрия обычно осуществляют в месте нахождения нескольких химических потребителей хлора, в связи с чем отсутствует готовность к рекуперированию содержащего хлорид натрия раствора, поступающего от всех потребителей. В случае если потребителем образующихся при электролизе едкого натра и хлора являются не только изготовители поликарбонатов, доля рекуперируемого из отработанной воды хлорида натрия возрастает.
Другой предпочтительный вариант нового способа предусматривает концентрирование отработанной воды производства поликарбонатов посредством твердого хлорида щелочного металла и подачу концентрированной отработанной воды на электролиз. Благодаря этому можно повторно использовать более 13% хлорида щелочного металла, содержащегося в отработанной воде производства поликарбоната.
Однако подобный вариант предполагает использование хлора и щелочи не только для производства поликарбонатов.
Для электролиза е) особенно предпочтительно используют, соответственно на электролиз направляют содержащую хлорид щелочного металла отработанную воду, показатель рН которой составляет менее 7. Показатель рН устанавливают на указанном уровне предпочтительно с помощью соляной кислоты, хотя для этого можно использовать также газообразный хлористый водород.
В соответствии с другим предпочтительным вариантом способа электролиз хлорида натрия осуществляют таким образом, чтобы концентрация хлорида натрия в выходящем из электролитической ячейки растворе NaCl составляла менее 200 г/л. В соответствии с этим концентрация выходящей из электролитической ячейки щелочи может составлять менее 30% масс.
Транспорт воды через мембрану зависит не только от рабочих параметров электролиза, но и от типа используемой мембраны. В соответствии с предлагаемым в изобретении способом предпочтительно используют ионообменные мембраны, которые в условиях осуществления предлагаемого в изобретении способа (концентрации хлорида натрия и щелочи) обеспечивают транспорт через мембрану более 4,5 молей воды на моль натрия.
При этом плотность тока в расчете на единицу площади мембраны прежде всего составляет от 2 до 6 кА/м2. Особенно предпочтительно используют аноды с увеличенной поверхностью. Под анодами с увеличенной поверхностью подразумевают аноды, физическая поверхность которых значительно выше по сравнению с проектной поверхностью. Анодами с увеличенной поверхностью являются, например, электроды, которые обладают пенообразной или войлокообразной структурой. Аноды с подобной структурой характеризуются чрезвычайно развитой поверхностью и сильно сниженной локальной плотностью тока. Поверхность анода предпочтительно следует выбирать таким образом, чтобы локальная плотность тока в пересчете на физическую поверхность электрода составляла менее 3 кА/м2. Чем больше поверхность анода и ниже локальная плотность тока, тем более низкой может быть концентрация хлорида натрия в рассоле и тем большее количество хлорида натрия может быть рекуперировано из отработанной воды.
Показатель рН содержащей хлорид щелочного металла отработанной воды перед осуществлением электролиза (стадии е)) предпочтительно должен быть ниже 7, особенно предпочтительно он должен составлять от 0,5 до 6.
Электролиз хлорида щелочного металла следует выполнять таким образом, чтобы концентрация хлорида натрия в выходящем из электролитической ячейки растворе хлорида натрия составляла от 100 до 280 г/л и/или концентрация выходящей из электролитической ячейки щелочи составляла от 13 до 33% масс.
Особенно предпочтительными являются концентрации растворов хлорида щелочного металла, позволяющие эксплуатировать электролитическую ячейку при пониженных напряжениях. В этом случае концентрация выходящего из электролитической ячейки раствора хлорида щелочного металла предпочтительно составляет от 110 до 220 г/л и/или концентрация выходящей из электролитической ячейки щелочи составляет от 20 до 30% масс.
Используемые для электролиза ионообменные мембраны предпочтительно должны обеспечивать транспорт более 4,0 молей воды на моль натрия, особенно предпочтительно от 5,5 до 6,5 молей воды на моль натрия.
В соответствии с предпочтительным вариантом способа электролиз е) осуществляют при температуре от 70 до 100°С, предпочтительно от 80 до 95°С.
Электролиз осуществляют при абсолютном давлении, составляющем от 1 до 1,4 бар, предпочтительно от 1,1 до 1,2 бар.
Отношение давлений в анодом и катодном пространство прежде всего выбирают таким образом, чтобы давление в катодном пространстве превышало давление в анодном пространстве.
Разность давлений в катодном и анодном пространствах в особенно предпочтительном варианте способа должна с оставлять от 20 до 150 мбар, предпочтительно от 30 до 100 мбар.
В случае пониженных концентраций хлорида щелочного металла можно использовать также аноды с особым покрытием. Подобное покрытие помимо оксида рутения прежде всего может содержать также другие компоненты на основе благородных металлов 7-й и 8-й побочных групп периодической системы элементов. Так, например, анодное покрытие может быть легировано соединениями палладия. Кроме того, можно использовать покрытия на основе алмазов.
Параметры или характеристики, приведенные в общем случае и предпочтительных вариантах изобретения, можно любым образом комбинировать друг с другом, а также с другими параметрами и предпочтительными вариантами.
Приведенные ниже примеры служат для пояснения настоящего изобретения и не ограничивают его объема.
Примеры
Приведенные ниже примеры предусматривают использование отработанной воды синтеза поликарбонатов, содержащей хлорид натрия.
Пример 1. Добавление содержащей хлорид натрия реакционной отработанной воды в систему электролиза хлорида натрия: добавление реакционной отработанной воды процесса синтеза поликарбоната с концентрацией хлорида натрия 10% масс.
В циркуляционный реактор через смонтированный перед насосом Т-образный штуцер дозировали 24000 кг/ч щелочного раствора бисфенола А, содержащего 15% масс. бисфенола А (ВРА) и 2,1 моля едкого натра на моль бисфенола, а через другой Т-образный штуцер раствор фосгена в растворителе, состоящем из 50% масс. метиленхлорида и 50% масс. монохлорбензола, причем расход фосгена составлял 1848 кг/ч, расход растворителя 20400 кг/ч.
Для обеспечения надлежащей щелочности дозировали 360 кг/ч раствора едкого натра концентрацией 32% и реакционную смесь через теплообменник и предназначенный для выдержки резервуар без мешалки вновь направляли к насосу при одновременном дозировании указанных материальных потоков.
Измеряемый расходомером расход реакционной смеси в циркуляционном контуре составлял 260 м3/ч.
Температура составляла 36°С.
Частичное количество эмульсии из предназначенного для выдержки резервуара, расход которой был аналогичен расходу поступающего исходного сырья, направляли посредством другого насоса в точку перед местом подачи бисфенола и фосгена и перекачивали через трубчатый реактор. В этот поток дозировали 1050 кг/ч раствора едкого натра концентрацией 32% масс., а также 134 кг/ч п-трет-бутилфенола, растворенного в 536 кг смеси растворителей. По истечении времени пребывания, составляющего 10 минут, дозировали 18 кг/ч N-этилпиперидина в виде раствора в смеси растворителей (50 частей метиленхлорида и 50 частей монохлорбензола) концентрацией 4,8%, и эмульсию другим насосом перекачивали через другой трубчатый реактор.
По истечении дополнительного времени пребывания, составляющего 10 минут, эмульсию разделяли в сепараторе, и раствор поликарбоната отмывали от электролита известными методами, например, посредством центрифуги.
Раствор поликарбоната концентрировали в выпарных устройствах и освобождали от остатков растворителя в испарительном экструдере.
Определяли характеристики гранулированного поликарбоната.
Измеренный согласно ASTM Е 313 показатель пожелтения (YI) гранулята составлял 1,35.
Измеренная согласно ISO 1628/4 характеристическая вязкость (ηrel) гранулята составляла 1,195.
Содержание концевых фенольных ОН-групп, измеренное методом УФ-спектроскопии (546 нм) после цветной реакции с TiCl4 на фенольные концевые группы, составляло 85 млн-1.
Реакционную отработанную воду в данном примере не соединяли с водными фазами, а освобождали от остатков растворителя и катализатора отгонкой с водяным паром. После нейтрализации соляной кислотой и обработки активированным углем получали реакционную отработанную воду с содержанием хлорида натрия 10% масс. и содержанием свободного бисфенола А (ВРА) и фенолов, составляющим менее 2 млн-1 (УФ-спектроскопия водной фаза при 294 нм, например, на спектрометре фирмы Perkin-Elmer).
Реакционную отработанную воду можно было направлять в электролитическую ячейку для электролиза хлорида натрия без дополнительной очистки.
Электролиз осуществляли, например, в лабораторной электролитической ячейке с анодом площадью 0,01 м2. Плотность тока составляла 4 кА/м2, температура на выходе из катодного пространства составляла 88°С, на выходе из анодного пространства 89°С. Использовали электролитическую ячейку со стандартным анодным и катодным покрытием фирмы DENORA (Германия). Использовали ионообменную мембрану DuPont Nation® 982 WX. Напряжение электролиза составляло 3,02 В. Через анодную камеру перекачивали содержащий хлорид натрия раствор с расходом 1,0 кг/ч. Концентрация хлорида натрия в поступающем в анодную камеру растворе составляла 25% масс. Из анодной камеры отбирали раствор хлорида натрия концентрацией 20% масс. К отбираемому из анодной камеры раствору хлорида натрия добавляли 0,125 кг/ч реакционной отработанной воды синтеза поликарбоната с концентрацией хлорид натрия 10% масс. и 0,076 кг/ч твердого хлорида натрия. Затем раствор вновь направляли в анодную камеру. Транспорт воды через мембрану составлял 3,5 моля на моль натрия. 1% выводимого из электролитической ячейки раствора хлорида натрия отбрасывали, что соответствовало расходу раствора с концентрацией хлорида натрия 20% масс., составляющему 0,008 кг/ч.
Расход направляемого к катоду раствора едкого натра составлял 1,107 кг/ч. Концентрация поступающего в катодную камеру раствора едкого натра составляла 30% масс., концентрация отбираемого из нее раствора едкого натра составляла 31,9% масс. От объемного потока отбирали 0,188 кг/ч щелочи концентрацией 31,9% масс., к остатку добавляли 0,0664 кг/ч воды и возвращали в катодную камеру.
Источником 14% подвергнутого электролизу хлорида натрия являлась реакционная отработанная вода синтеза поликарбоната.
Пример 2. Добавление содержащей хлорид натрия реакционной отработанной воды в систему электролиза хлорида натрия с газодиффузионным электродом: добавление реакционной отработанной воды процесса синтеза поликарбоната с концентрацией хлорида натрия 10% масс.
Качественные показатели отработанной воды соответствовали указанным в примере 1. В связи с отсутствием необходимости использования водорода для синтеза поликарбоната можно было отказаться от получения водорода при электролизе. Поэтому электролиз осуществляли с использованием газодиффузионных электродов. Плотность тока составляла 4 кА/м2, температура на выходе из катодного пространства составляла 88°С, на выходе из анодного пространства 89°С. Использовали электролитическую ячейку со стандартным анодным покрытием фирмы DENORA (Германия). Использовали ионообменную мембрану фирмы DuPont, Nation® 982 WX. Напряжение электролиза составляло 2,11 В. В анодную камеру подавали 0,65 кг/ч раствора хлорида натрия концентрацией 25% масс., отбираемый из анодной камеры раствор содержал 18% масс. хлорида натрия. К отбираемому из анодной камеры раствору хлорида натрия добавляли 0,163 кг/ч реакционной отработанной воды с содержанием хлорида натрия 10% масс. и 0,0715 кг/ч твердого хлорида натрия. Затем раствор вновь направляли в анодную камеру. Транспорт воды через мембрану составлял 4,9 молей на моль натрия.
Расход подаваемого в катодное пространство раствора едкого натра составлял 1,107 кг/ч. Концентрация поступающего в катодную камеру раствора едкого натра составляла 30% масс., концентрация отбираемого из нее раствора едкого натра составляла 31,0% масс. От объемного потока отбирали 0,192 кг/ч щелочи концентрацией 31,0% масс., к остатку добавляли 0,0345 кг/ч воды и возвращали в катодную камеру.
Доля превращенного хлорида натрия, содержавшегося в реакционной отработанной воде синтеза поликарбоната, составляла 18,6%.
Пример 3. Добавление содержащей хлорид натрия реакционной отработанной воды в систему электролиза хлорида натрия с газодиффузионным электродом: добавление реакционной отработанной воды процесса синтеза поликарбоната с концентрацией хлорида натрия 10% масс.
Качественные показатели отработанной воды соответствовали указанным в примере 1. В связи с отсутствием необходимости использования водорода для синтеза поликарбоната можно было отказаться от получения водорода при электролизе. Поэтому электролиз осуществляли с использованием газодиффузионных электродов. Плотность тока составляла 4 кА/м2, температура на выходе из катодного пространства составляла 88°С, на выходе из анодного пространства 89°С. Использовали электролитическую ячейку со стандартным анодным покрытием фирмы DENORA (Германия). Использовали ионообменную мембрану фирмы DuPont, Nafion® 982 WX. Напряжение электролиза составляло 1,96 В. В анодную камеру подавали 0,65 кг/ч раствора хлорида натрия концентрацией 25% масс., отбираемый из анодной камеры раствор содержал 16,3% масс. хлорида натрия. Отбрасывали 1% отбираемого из анодной камеры раствора хлорида натрия, что соответствовало расходу 0,00309 кг/ч. К отбираемому из анодной камеры раствору хлорида натрия добавляли 0,173 кг/ч реакционной отработанной воды с содержанием хлорида натрия 10% масс. и 0,0703 кг/ч твердого хлорида натрия. Затем раствор вновь направляли в анодную камеру. Транспорт воды через мембрану составлял 5,26 молей на моль натрия.
Расход подаваемого в катодное пространство раствора едкого натра составлял 1,107 кг/ч. Концентрация поступающего в катодную камеру раствора едкого натра составляла 30,0% масс., концентрация отбираемого из нее раствора едкого натра составляла 30,7% масс. От объемного потока отбирали 0,194 кг/ч щелочи концентрацией 30,7% масс., к остатку добавляли 0,0263 кг/ч воды и возвращали в катодную камеру.
Доля превращенного хлорида натрия, содержавшегося в реакционной отработанной воде синтеза поликарбоната, составляла 19,8%.
Пример 4. Рецикл водных фаз переработки поликарбоната (стадии с)) на стадию синтеза поликарбоната: добавление отработанной водной фазы на стадию синтеза поликарбоната
Данный пример выполняли аналогично примеру 1, однако после отделения органической фазы от реакционного отработанного водного раствора хлорида щелочного металла на ступени аа) органическую фазу (содержащий поликарбонат раствор) промывали водой, соляной кислотой с концентрацией 0,6%, а затем вновь несколько раз промывали водой.
Показатель рН отдельных или объединенных водных фаз стадии переработки поликарбоната устанавливали посредством водного раствора гидроксида натрия в области 10, после чего водные фазы освобождали от остатков растворителя и катализатора экстракцией метиленхлоридом или отгонкой с водяным паром. Полученные после фазового расслоения водные фазы можно было использовать для частичной замены воды, используемой для приготовления раствора едкого натра, используемого для синтеза поликарбоната.
Первую промывную фазу можно было также соединять с реакционной отработанной водой и после удаления остатков растворителя и катализатора направлять на электролиз хлорида натрия.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ДИАРИЛКАРБОНАТА И ПЕРЕРАБОТКА, ПО МЕНЬШЕЙ МЕРЕ, ОДНОЙ ЧАСТИ ОБРАЗОВАННОГО ПРИ ЭТОМ РАСТВОРА, СОДЕРЖАЩЕГО ХЛОРИД ЩЕЛОЧНЫХ МЕТАЛЛОВ, В НАХОДЯЩЕМСЯ НИЖЕ ПО ТЕХНОЛОГИЧЕСКОЙ ЦЕПОЧКЕ ЭЛЕКТРОЛИЗЕ ХЛОРИДА ЩЕЛОЧНЫХ МЕТАЛЛОВ | 2007 |
|
RU2484082C2 |
| СПОСОБ ПОЛУЧЕНИЯ ДИАРИЛКАРБОНАТА | 2010 |
|
RU2536998C2 |
| АЛКИЛФЕНОЛ ДЛЯ УСТАНОВЛЕНИЯ МОЛЕКУЛЯРНОГО ВЕСА И СОПОЛИКАРБОНАТ С УЛУЧШЕННЫМИ СВОЙСТВАМИ | 2009 |
|
RU2505556C2 |
| СПОСОБ ПОЛУЧЕНИЯ ДИАРИЛКАРБОНАТА | 2008 |
|
RU2496765C2 |
| МАТЕРИАЛЫ ПОДЛОЖКИ ДЛЯ ПРОЗРАЧНЫХ ЛИТЫХ ИЗДЕЛИЙ | 2005 |
|
RU2410241C2 |
| МАТЕРИАЛЫ ПОДЛОЖКИ ДЛЯ ПРОЗРАЧНЫХ ЛИТЫХ ИЗДЕЛИЙ | 2005 |
|
RU2421763C2 |
| ПОЛИКАРБОНАТЫ И СОПОЛИКАРБОНАТЫ С УЛУЧШЕННОЙ АДГЕЗИЕЙ К МЕТАЛЛУ | 2007 |
|
RU2451035C2 |
| ПОЛИКАРБОНАТЫ С ХОРОШЕЙ СМАЧИВАЕМОСТЬЮ | 2005 |
|
RU2412956C2 |
| ПОЛИКАРБОНАТЫ С ХОРОШЕЙ СМАЧИВАЕМОСТЬЮ | 2005 |
|
RU2410400C2 |
| СВЕРХЧИСТЫЕ ПОЛИКАРБОНАТЫ С ХОРОШЕЙ СОБСТВЕННОЙ ОКРАСКОЙ И ВЫСОКОЙ ТЕРМОСТАБИЛЬНОСТЬЮ, УСТРОЙСТВО И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2010 |
|
RU2566822C2 |
Изобретение относится к способу получения поликарбоната на границе раздела фаз и последующего электролиза содержащей хлорид натрия технологической отработанной воды, который включает следующие стадии:
a) получение фосгена взаимодействием хлора с монооксидом углерода,
b) взаимодействие полученного на стадии а) фосгена, по меньшей мере, с одним бисфенолом в присутствии, по меньшей мере, одного основания, по меньшей мере, одного катализатора с основным характером и, по меньшей мере, одного органического растворителя с образованием поликарбоната и раствора, содержащего хлорид щелочного металла,
c) выделение и переработку полученного на стадии b) поликарбоната,
d) отделение остающегося на стадии с) раствора, содержащего хлорид щелочного металла, от остатков растворителя и остатков катализатора прежде всего путем отгонки с водяным паром и обработки адсорбентами, прежде всего активированным углем,
e) электрохимическое окисление, по меньшей мере, части содержащего хлорид щелочного металла раствора стадии d) с образованием хлора, щелочи и при необходимости водорода,
отличающемуся тем, что при отделении раствора, реализуемом на стадии d) перед его обработкой адсорбентами, показатель рН раствора устанавливают на уровне 8 или ниже и
f) по меньшей мере, часть полученного на стадии е) хлора возвращают на стадию а) и/или,
g) по меньшей мере, часть полученной на стадии е) щелочи возвращают на стадию b) синтеза поликарбоната. Технический результат - упрощение технологии, связанное с возможностью подачи раствора на электролиз без очистки, возможностью использовать выделенные из отходов компоненты в процессе. 13 з.п. ф-лы, 4 пр.
1. Способ получения поликарбоната на границе раздела фаз и переработки, по меньшей мере, части образующегося при этом раствора, содержащего хлорид щелочного металла, на дополнительной стадии электролиза хлорида щелочного металла, который включает следующие стадии:
a) получение фосгена взаимодействием хлора с монооксидом углерода,
b) взаимодействие полученного на стадии а) фосгена, по меньшей мере, с одним бисфенолом в присутствии, по меньшей мере, одного основания, по меньшей мере, одного катализатора с основным характером и, по меньшей мере, одного органического растворителя с образованием поликарбоната и раствора, содержащего хлорид щелочного металла,
c) выделение и переработку полученного на стадии b) поликарбоната,
d) отделение остающегося на стадии с) раствора, содержащего хлорид щелочного металла, от остатков растворителя и остатков катализатора прежде всего путем отгонки с водяным паром и обработки адсорбентами, прежде всего активированным углем,
e) электрохимическое окисление, по меньшей мере, части содержащего хлорид щелочного металла раствора стадии d) с образованием хлора, щелочи и при необходимости водорода,
отличающийся тем, что при отделении раствора, реализуемом на стадии d) перед его обработкой адсорбентами, показатель рН раствора устанавливают на уровне 8 или ниже, и,
f) по меньшей мере, часть полученного на стадии е) хлора возвращают на стадию а) и/или,
g) по меньшей мере, часть полученной на стадии е) щелочи возвращают на стадию b) синтеза поликарбоната.
2. Способ по п.1, отличающийся тем, что электрохимическое окисление, по меньшей мере, части содержащего хлорид щелочного металла раствора стадии d) осуществляют до хлора и едкого натра с использованием в качестве катода газодиффузионных электродов.
3. Способ по п.1, отличающийся тем, что, по меньшей мере, часть содержащего хлорид щелочного металла очищенного раствора стадии d) подают в контур циркуляции рассола мембранного электролиза, с целью получения хлора, раствора едкого натра и при необходимости водорода.
4. Способ по п.1, отличающийся тем, что, с целью повышения концентрации хлорида щелочного металла, к раствору хлорида щелочного металла при электролизе на стадии е) добавляют дополнительный хлорид щелочного металла.
5. Способ по п.1, отличающийся тем, что показатель рН содержащего хлорид щелочного металла раствора на стадии очистки d) устанавливают ниже 7 прежде всего добавлением соляной кислоты или хлористого водорода.
6. Способ по п.1, отличающийся тем, что содержание хлорида щелочного металла в растворе, поступающем на электролиз хлорида щелочного металла, составляет от 100 до 280 г/л, предпочтительно от 110 до 220 г/л, и/или концентрация получаемого при электролизе раствора едкого натра составляет от 13 до 33% масс., предпочтительно от 20 до 32% масс.
7. Способ по п.1, отличающийся тем, что для электролиза на стадии е) используют ионообменные мембраны, транспорт воды через которые составляет более четырех молей на моль натрия.
8. Способ по п.1, отличающийся тем, что электролиз выполняют при плотности тока от 2 до 6 кА/м2, причем плотность тока рассчитывают на основании площади мембраны.
9. Способ по п.1, отличающийся тем, что электролиз на стадии е) выполняют при температуре от 70 до 100°С, предпочтительно от 80 до 95°С.
10. Способ по п.1, отличающийся тем, что раствор стадии d), содержащий хлорид щелочного металла, перед выполняемым на стадии е) электролизом концентрируют мембранным методом.
11. Способ по п.1, отличающийся тем, что для реакции на стадии b) в качестве бисфенола(-ов) используют дигидроксидиарилалкан(-ы) общей формулы (I):
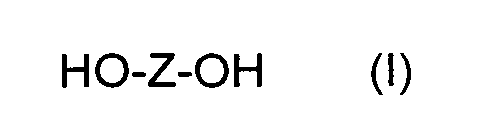
в которой Z означает двухвалентный органический остаток с 6-30 атомами углерода, содержащий одну или несколько ароматических групп.
12. Способ по п.1, отличающийся тем, что в качестве бисфенола(-ов) на стадии b) используют 4,4′-дигидроксидифенил, 2,2-бис(4-гидрокси-фенил)-1-фенилпропан, 1,1-бис(4-гидроксифенил)фенилэтан, 2,2-бис-(4-гидроксифенил)пропан, 2,4-бис(4-гидроксифенил)-2-метилбутан, 1,3-бис[2-(4-гидроксифенил)-2-пропил]-бензол, 2,2-бис(3-метил-4-гидроксифенил)пропан, бис(3,5-диметил-4-гидрокси-фенил)метан, 2,2-бис(3,5-диметил-4-гидроксифенил)пропан, бис(3,5-диметил-4-гидроксифенил)сульфон, 2,4-бис(3,5-диметил-4-гидроксифенил)-2-метилбутан, 1,3-бис[2-(3,5-диметил-4-гидрокси-фенил)-2-пропил]бензол, 1,1-бис(4-гидрокси-фенил)циклогексан и/или 1,1-бис(4-гидроксифенил)-3,3,5-триметилциклогексан.
13. Способ по п.1, отличающийся тем, что используют содержащую растворенный хлорид щелочного металла реакционную отработанную воду стадии b) или, по меньшей мере, ее часть с промывочной водой со стадии переработки с) поликарбоната.
14. Способ по одному из пп.1-13, отличающийся тем, что стадию с) выполняют, по меньшей мере, в две следующие ступени:
аа) разделение содержащей поликарбонат органической фазы и реакционной отработанной воды, содержащей растворенный хлорид щелочного металла,
bb) по меньшей мере, однократная промывка полученной на ступени аа) содержащей поликарбонат органической фазы,
причем, по меньшей мере, часть промывочной(-ых) фазы(-) ступени c)bb) при необходимости после отделения от остатков катализатора и при необходимости от остатков органического растворителя используют в качестве частичной замены воды для приготовления раствора едкого натра, предназначенного для выполнения стадии b).
Авторы
Даты
2014-11-20—Публикация
2009-02-26—Подача