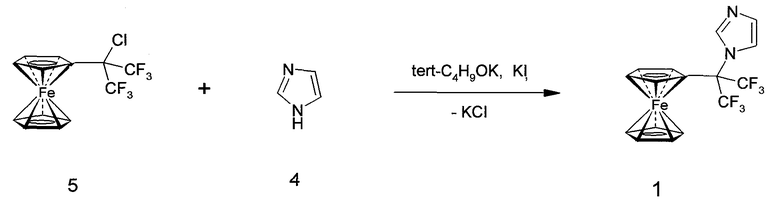
Изобретение относится к новым соединениям, а именно к фторированному ферроценилсодержащему производному имидазола формулы 1, проявляющему противоопухолевую активность, и способам его получения.
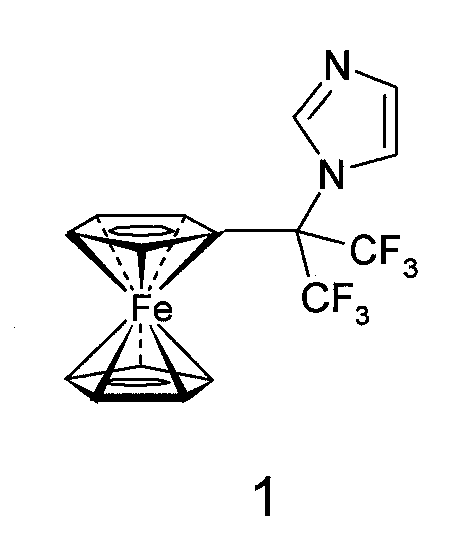
Указанное соединение наиболее эффективно может быть использовано в медицине для химиотерапии онкологических заболеваний.
Соединение 1, его свойства и способы получения в литературе не описаны. До сих пор не были известны ферроценильные производные гетероциклов, содержащие атомы фтора не в гетероцикле, а в алкильной цепи, соединяющей гетероцикл с ферроценильным заместителем.
Известно, что производные ферроцена обладают выраженной противоопухолевой активностью. Впервые противоопухолевая активность была выявлена на солях феррициния [Р. Köpf-Maier, H. Köpf, E.W. Neuse. Ferricenium salts - the first antineoplastic iron compounds. Angew. Chem. Int. Ed. 1984, 23(6), 456-457; P. Köpf-Maier, H. Köpf, E.W. Neuse. Ferricenium complexes: A new type of water-soluble antitumor agent. J. Cancer. Res. din. Oncol. 1984, 108, 336-340; D. Osella, M. Ferrali, P. Zanello, F. Laschi, M. Fontani, C. Nervi, G. Cavigiolio, On the Mechanism of the Antitumor Activity of Ferrocenium Derivatives, Inorg. Chim. Acta, 2000, 306, 42-48].
В настоящее время в медицинской практике применяют производное ферроцена «Ферроцерон» (натриевая соль о-карбоксибензоилферроцена), используемое для лечения заболеваний, связанных с дефицитом железа в организме [А.Н. Несмеянов, Л.Г. Богомолова, Н.С. Кочеткова, В.Д. Вильчевская, Н.П. Палицын, И.Г. Андрианова, О.П. Богомолова. Лекарственный препарат., Авт. свид. СССР №263807, кл. A61K 31/295 (1966), Б.И. №41, 1977; А.N. Nesmeyanov, L.G. Bogomolova, N.S. Kochetkova, V.D. Vil'chevskaya, N.P. Palitsyn, Yu. Yu. Gorelikova, I.G. Andrianova, О.Р. Belozerova, V. Kh. Syundyukova. (2-Carboxybenzoyl)ferrocene sodium salt, патент Великобритании GB 1320046, A61K 1/295, C07F 17/02, C.A. 79: 78966, 1973; A.N. Nesmeyanov, L.G. Bogomolova, I.G. Andrianova, V.D. Vilchevskaya, N.S. Kochetkova, Khim. - Farm. Zh. 1972; 6(4), 61]. Указанная натриевая соль о-карбоксибензоилферроцена также обладает противоопухолевым действием (торможение роста опухоли (ТРО) Ca755 70%, B16 70%, LD50 60 мг/кг) [А.А. Simenel, S.V. Samarina, L.V. Snegur, Z.A. Starikova, L.A. Ostrovskaya, N.V. Bluchterova, M.M. Fomina, o-Carboxybenzoylferrocene. Bioactivity and Chemical Modifications, Appl. Organomet. Chem., 2008, 22, 276-280].
Известно, что высокой противоопухолевой активностью обладают ферроцифены, являющиеся аналогами тамоксифена (антиэстрогена).

Они могут быть использованы для лечения гормон-зависимых видов рака груди [S. Top, J. Tang, A. Vessieres, D. Carrez, С. Provot, G. Jaouen, Ferrocenyl hydroxytamoxifen: a prototype for a new range of oestradiol receptor site-directed cytotoxics, Chem. Commun. 1996, 955-956, S. Top, A. Vessieres, C. Cabestaing, I. Laios, G. Leclercq, C. Provot, G. Jaouen, Studies on organometallic selective estrogen receptor modulators. (SERMs) Dual activity in the hydroxy-ferrocifen series, J. Organomet. Chem. 637, 500-506 (2001), S. Top, A. Vessieres, G. Leclercq, J. Quivy, J. Tang, J. Vaissermann, M. Huche, G. Jaouen, Synthesis, Biochemical Properties and Molecular Modelling Studies of Organometallic Specific Estrogen Receptor Modulators (SERMs), the Ferrocifens and Hydroxyferrocifens: Evidence for an Antiproliferative Effect of Hydroxyferrocifens on both Hormone-Dependent and Hormone-Independent Breast Cancer Cell Lines, Chem. Eur. J. 9, 5223-5236].
Аналогами заявляемого соединения являются ферроценилалкилазолы, проявляющие ярко выраженный противоопухолевый эффект и обладающие низкой токсичностью, которая существенно ниже токсичности широко применяемых в настоящее время противоопухолевых препаратов платины, например, цисплатина [А.А. Simenel, E.A. Morozova, L.V. Snegur, S.I. Zykova, V.V. Kachala, L.A. Ostrovskaya, N.V. Bluchterova, M.M. Fomina, Simple route to ferrocenylalkyl nucleobases. Antitumor activity in vivo, Appl. Organomet. Chem., 2009, 23, 219-224, L.V. Snegur, Yu.S. Nekrasov, N.S. Sergeeva, Zh.V. Zhilina, V.V. Gumenyuk, Z.A. Starikova, А.А. Simenel, N.B. Morozova, I.K. Sviridova, V.N. Babin, Ferrocenylalkyl azoles: bioactivity, synthesis, structure, Appl. Organomet. Chem., 2008, 22, 139-147].
Наиболее близкими по структуре и свойствам к заявляемому соединению являются такие производные ферроцена, как 1-(ферроценилметил)бензимидазол (П-1) и 1-(ферроценилметил)тимин (П-2), ингибирующие рост карциномы Ca755
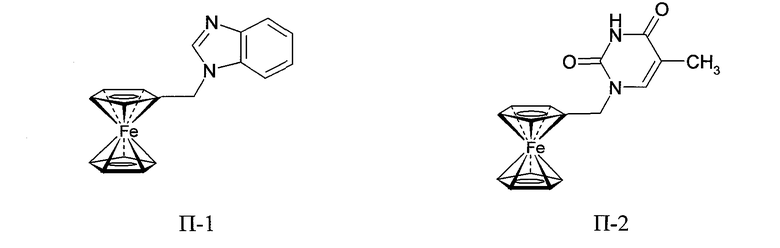
[L.V. Snegur, A.A. Simenel, Yu. S. Nekrasov, N.В. Morozova, et al. Synthesis, structure and redox potentials of biologically active ferrocenylalkyl azoles. J. Organomet. Chem., 2004, 689, 2473-2479); A.A. Simenel, E.A. Morozova, L.V. Snegur, S.I. Zykova, V.V. Kachala, L.A. Ostrovskaya, N.V. Bluchterova, M.M. Fomina, Simple route to ferrocenylalkyl nucleobases. Antitumor activity in vivo, Appl. Organomet. Chem., 2009, 23, 219-224].
Известно, что серьезным недостатком всех противоопухолевых препаратов является их тяжелая переносимость животными и человеком, связанная с их токсичностью. При лечении такими препаратами, как правило, наблюдается интоксикация жизненно важных систем организма, изменение поведенческих функций, потеря веса и т.п., что в результате может привести даже к летальному исходу.
Известен способ получения ферроценилалкилазолов (аналогов заявляемого соединения), который заключается во взаимодействии α-гидроксиалкилферроценов с нуклеофильными агентами в присутствии кислотных катализаторов [В.И. Боев. Дис. д-ра хим. наук. С.-Пб. Технол. ин-т, Санкт-Петербург, 1993; Л.В. Снегур. Дис. канд. хим. наук. ИНЭОС им. А.Н. Несмеянова РАН, Москва, 1993]. Взаимодействие эквимольных количеств α-гидроксиалкилферроцена и нуклеофильного субстрата проводят при интенсивном перемешивании в двухфазной системе: органический растворитель (CH2Cl2, C2H4Cl2, CHCl3, CCl4, бензол) - водный раствор (45-70%) кислоты HX (X=BF4, ClO4, I). Однако указанным способом не удается получить заявляемое соединение 1, исходя из соответствующего фторсодержащего спирта и имидазола.
Известен способ получения ферроценилалкильных производных имидазола, заключающийся во взаимодействии α-гидроксиалкилферроценов 2 с 1,1'-карбонилдиимидазолом (3) при кипячении в метиленхлориде [А.А. Simenel, E.A. Morozova, Yu.V. Kuzmenko, L.V. Snegur. J. Organomet. Chem., 2003, 665, 13-14; А.А. Simenel, Yu.V. Kuzmenko, E.A. Morozova, M.M. Ilyin, I.F. Gun'ko, L.V. Snegur. J. Organomet Chem. 2003, 688, 138-143] (схема 1)
Схема 1
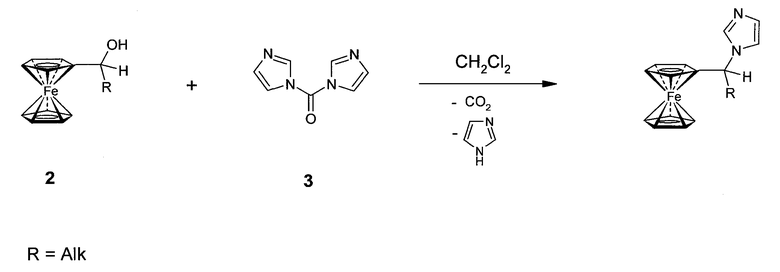
Однако указанным способом в результате взаимодействия соответствующего α-гидроксиалкилферроцена (1-ферроценил-1-трифторметил-2,2,2-трифторэтанола 2a) с 1,1'-карбонилдиимидазолом (3) при кипячении в метиленхлориде также не удалось получить заявляемое соединение. Указанный способ аналогичен заявляемому способу A и был выбран в качестве его прототипа.
Задачей настоящего изобретения является получение ранее неизвестных фторсодержащих ферроценильных производных гетероциклов, обладающих высокой противоопухолевой активностью и низкой токсичностью, а также разработка способов получения таких производных.
Поставленная задача решается заявляемым соединением 1-(1,1,1,3,3,3-гексафтор-2-ферроценилпроп-2-ил)имидазолом формулы 1, обладающим противоопухолевой активностью и низкой токсичностью, и способами его получения: способом А, включающим взаимодействие соответствующего α-гидроксиалкилферроцена, в качестве которого используют 1-ферроценил-1-трифторметил-2,2,2-трифторэтанол, с 1,1'-карбонилдиимидазолом при кипячении в толуоле; или способом Б, который заключается во взаимодействии 1-[1,1,1,33,3-гексафтор-2-хлорпроп-2-ил]-ферроцена с имидазолом и трет.-бутилатом калия (мольное соотношение реагентов 1:1,2:1,2), в толуоле при кипячении при добавлении йодида калия в качестве катализатора или без катализатора.
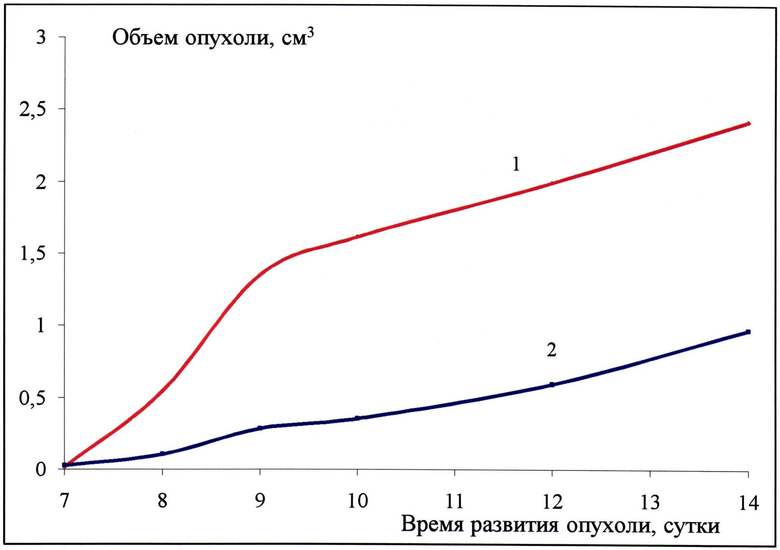
На чертеже представлены данные испытаний заявляемого соединения формулы 1 на противоопухолевую активность в виде кинетических кривых, иллюстрирующих влияние заявляемого соединения (испытываемого под шифром AS-01) на развитие карциномы Ca-755. На оси абсцисс указано время после перевивки опухоли (в сутках); на оси ординат - объем опухоли (см3). Кривую 2 получают при введении мышам соединения формулы 1 100 мг/кг в сутки, перорально, 8-кратно, ежедневно, начиная со следующих суток после перевивки опухоли; кривая 1 - контроль.
Онкобиологическое изучение соединения формулы 1 проведено в Федеральном государственном бюджетном учреждении науки Институте биохимической физики им. Н.М. Эмануэля Российской академии наук (ИБХФ РАН), включенном на основании решения МЗ РФ в Перечень организаций и учреждений, осуществляющих проведение доклинических исследований лекарственных средств (Разрешение МЗ РФ №01-45122/06 от 21.09.2006 г.).
Проведено исследование острой токсичности и противоопухолевой активности заявляемого соединения 1 на модели солидной опухоли мышей (карцинома Ca-755) в условиях in vivo. Карцинома Ca-755 представляет собой опухоль, известную своей устойчивостью к химиотерапевтическим воздействиям.
Показано, что соединение 1 обладает противоопухолевым действием в отношении карциномы Ca-755, вызывая торможение ее роста на 80% по сравнению с контролем (10 сутки развития опухоли). Соединение 1 в дозе 400-800 мг/кг при пероральном однократном введении хорошо переносится интактными животными (мыши BDF1) и не приводит к изменению поведенческих реакций мышей. Обнаруженная чувствительность карциномы Ca-755 к соединению 1 при хорошей переносимости соединения животными указывает на целесообразность дальнейшего углубленного исследования фармакологического механизма действия и противоопухолевых свойств заявляемого соединения.
Для получения заявляемого соединения 1 предлагается два способа его получения. Заявляемый способ А позволяет получать соединение 1 из 1-ферроценил-1-трифторметил-2,2,2-трифторэтанола 2a [М.I. Bruce, F.G. Stone, В.I. Thomson J. Organomet. Chem. 77, (1974), 77.] и 1,1'-карбонилдиимидазола 3. Взаимодействие указанных реагентов проводят в толуоле при кипячении и мольном соотношении реагентов 2a и 3, равном 1:1,2 (схема 2, пример 1). Способ А аналогичен способу-прототипу, применяемому для получения ферроценилалкильных производных имидазола [А.А. Simenel, E.A. Morozova, Yu.V. Kuzmenko, L.V. Snegur. J. Organomet. Chem., 2003, 665, 13-14; А.А. Simenel, Yu.V. Kuzmenko, E.A. Morozova, M.M. Ilyin, I.F. Gun'ko, L.V. Snegur. J. Organomet. Chem. 2003, 688, 138-143], и отличается тем, что реакцию проводят в высококипящем растворителе, таком как толуол, а в качестве исходного α-гидроксиалкилферроцена используют 1-ферроценил-1-трифторметил-2,2,2-трифторэтанол 2a. Исходное соединение 2a получают по методике, описанной в работе [М.I. Bruce, F.G. Stone, В.I. Thomson J. Organomet. Chem. 77, (1974), 77]. Способ А позволяет получать соединение 1 с выходом более 70%. Необходимость проведения реакции при более высокой температуре, чем в способе-прототипе, в данном случае обусловлена более низкой реакционной способностью исходного спирта 2a по сравнению с другими ферроценилкарбинолами, что связано с электроноакцепторным влиянием трифторметильных групп и стерическими затруднениями.
Схема 2
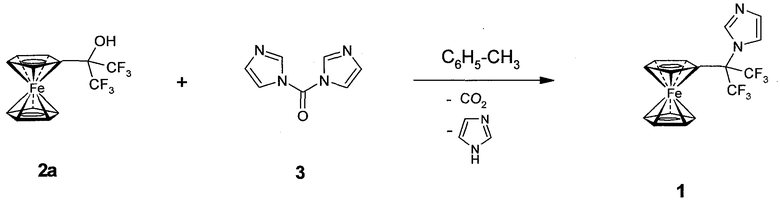
Второй заявляемый способ (Б) основан на взаимодействии имидазола (4) и 1-(1,1,1,3,3,3-гексафтор-2-хлорпроп-2-ил)ферроцена (5) и позволяет получать заявляемое соединение с выходом более 70%. Исходное соединение 5 и имидазол 4 растворяют в толуоле и кипятят в присутствии трет-бутилата калия в качестве акцептора HCl (схема 3, примеры 2-3). Добавка незначительного количества безводного йодида калия существенно повышает выход целевого продукта (пример 2).
Схема 3
Заявляемый способ Б является новым и оригинальным в ряду ферроценов, так как в качестве исходного соединения использует 1-(1,1,1,3,3,3-гексафтор-2-хлорпроп-2-ил)ферроцен (5), вещество, которое является первым представителем стабильных хлорметилферроценов [В.И. Дяченко, А.С. Перегудов, И.В. Ананьев, М.Ю. Антипин, Ю.С. Некрасов, В.И. Соколов, С.М. Игумнов. 1-(1,1,1,3,3,3-Гексафтор-2-хлорпроп-2-ил)ферроцен - первый стабильный представитель хлорметилферроценов, Изв. Акад. наук, Сер. хим., 2011, №4, с.748-749]. Остальные хлорметилферроцены разлагаются даже при комнатной температуре. Соединение 5 стабильно при комнатной температуре и при нагревании. Указанное соединение использовано как реагент, обладающий высокой региоселективностью и умеренной реакционной способностью, для введения перфторалкилферроценильного фрагмента, что позволило избежать образования продуктов диалкилирования.
Заявляемое соединение, в отличие от других производных ферроцена, можно легко получить с использованием простых технологичных способов, не требующих применения жестких условий, специального оборудования, инертной атмосферы и высоких температур.
Заявляемое соединение обладает оптимальным соотношением липофильных и гидрофильных свойств, так как оно обладает в нейтральной форме повышенной растворимостью в липидах (благодаря объемному перфторированному заместителю), что увеличивает скорость транспорта соединения через биологические мембраны опухолевых клеток, а в организме оно может переходить в ионную форму (благодаря окислению ферроценового фрагмента до феррициния, а также протонированию имидазола), что способствует транспорту в полярных биологических жидкостях (кровь, лимфа).
Заявляемое соединение 1 обладает противоопухолевым действием в отношении карциномы Ca-755, вызывая торможение ее роста на 80% по сравнению с контролем (10 сутки развития опухоли) и хорошо переносится животными в дозе 400-800 мг/кг при пероральном однократном введении хорошо переносится интактными животными (мыши BDF1) и вызывает увеличение их веса. Факт увеличения веса является неожиданным и не наблюдается у известных веществ, обладающих противоопухолевым действием.
Техническим результатом изобретения является новое вещество, обладающее противоопухолевой активностью и низкой токсичностью, расширяющее ассортимент противоопухолевых агентов.
Изобретение иллюстрируется конкретными примерами его осуществления и данными биологических испытаний, приведенными ниже.
Пример 1. (Способ А). Смесь 0,352 г 1 ммоль 1-ферроценил-1-трифторметил-2,2,2-трифторэтанола 2a и 0,18 г (1,2 ммоль) 1,1'-карбонилдиимидазола 3 кипятят в безводном толуоле в течение трех часов. Реакционную массу охлаждают, добавляют 50 мл эфира и экстрагируют 20% раствором фосфорной кислоты (2×50 мл). Объединенные водные фракции подщелачивают до pH 5 и экстрагируют хлористым метиленом (2×50 мл). Органическую часть сушат над безводным сернокислым натрием. Растворитель удаляют. Продукт очищают колоночной хроматографией на силикагеле, элюент - хлористый метилен. Получают 0,285 г соединения 1. Выход 71%.
Пример 2 (Способ Б.). Смесь 0,370 г (1 ммоль) 1-[1,1,1,3,3,3-гексафтор-2-хлорпроп-2-ил]-ферроцена 5, 0,102 г (1,2 ммоль) имидазола 4, 0,135 г (1,2 ммоль) трет-бутилата калия и 0,12 ммоль безводного йодида калия кипятят в безводном толуоле в течение суток. Реакционную массу охлаждают, растворитель удаляют, остаток очищают колоночной хроматографией на силикагеле, элюент - хлористый метилен. После удаления растворителя в вакууме получают 0,294 г соединения 1 в виде красно-коричневого масла, которое кристаллизуется при охлаждении, т.пл. 30-31°C. Выход 73%.
Масс-спектр: m/z (%): 402 (100) [M]+, 335 (55) [M-Im]+.
1H ЯМР (CDCl3, δ, мд): 4,03-4,29 (м, 9H, Fc), 4,61 (кв, 1H, CH) 7,11 (с, 1H, CH); 7,19 (с, 1H, CH); 7,47 (с, 1H, CH).
Пример 3 (Способ Б.). Смесь 0,370 г (1 ммоль) 1-[1,1,1,3,3,3-гексафтор-2-хлорпроп-2-ил]-ферроцена 5, 0,102 г (1,2 ммоль) имидазола 4 и 0,135 г (1,2 ммоль) трет-бутилата калия кипятят в безводном толуоле в течение суток. Реакционную массу охлаждают, растворитель удаляют, остаток очищают колоночной хроматографией на силикагеле, элюент - хлористый метилен. После удаления растворителя в вакууме получают 0,230 г соединения 1. Выход 57%.
Ниже представлены результаты испытаний 1-(1,1,1,3,3,3-гексафтор-2-ферроценилпроп-2-ил)имидазола 1 на противоопухолевую активность. Исследована острая токсичность и противоопухолевая активность соединения 1 на модели солидной опухоли мышей (карцинома Ca-755) в условиях in vivo.
Материалы и методы
Препарат. Соединение 1 (препарат AS-01) - 1-(1,1,1,3,3,3-гексафтор-2-ферроценилпроп-2-ил)имидазол (C16H12F6FeN2, M 402,03).
Соединение 1 представляет собой легкоплавкие кристаллы коричневого цвета без запаха, нерастворимые в воде, растворимые в спиртах, ДМСО, органических растворителях. Вещество подлежит хранению в холодильнике в защищенной от света упаковке (со временем разлагается на свету).
Биологические испытания соединения 1 проведены при введении препарата мышам перорально (п/о) в растворе подсолнечного масла в концентрации 10 мг/мл.
Определение острой токсичности препарата проводили при его однократном введении интактным мышам в диапазоне доз от 400 до 800 мг/кг, п/о.
Противоопухолевая активность препарата оценивалась при восьмикратном ежедневном п/о введении в разовой дозе 100 мг/кг. Суммарная доза препарата - 800 мг/кг.
Лабораторные животные. Эксперименты проводили на инбредных мышах - гибридах первого поколения f1(C57B1/6xDBA2) - BDF1 разведения питомника РАМН "Столбовая". В опытах использовано 60 мышей, самцов с массой тела 20-22 г.
Экспериментальная модель. В качестве опухолевой тест-системы использована перевиваемая солидная опухоль мышей - аденокарцинома Ca-755. Опухоль перевивалась под кожу правого бока мышей измельченными фрагментами опухолевой ткани в соответствии со стандартной методикой [Трещалина Е.М., Жукова О.С., Герасимова Г.К., Андронова Н.В., Гарин A.M. «Методические указания по изучению противоопухолевой активности фармакологических веществ» // «Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ» (ред. Р.У. Хабриев). Издание 2. // Москва, «Медицина», 2005, с.637-651].
Оценка противоопухолевого эффекта. Показателями ростингибирующего эффекта соединения служили различия в кинетике роста опухолей (коэффициент торможения роста опухоли ТРО, %) у леченых (Т) и контрольных (С) животных. Коэффициент торможения роста опухоли ТРО, % определяли из соотношения: ТРО=(РС-PT)/PC%, где PC и PT - объем (или масса) опухоли в группах контрольных и леченых животных, соответственно.
Для изучения кинетики роста опухолей проводили измерение двух взаимно-перпендикулярных размеров опухолевого узла на протяжении всего периода развития опухолей. Объем опухоли вычисляли в соответствии с формулой для эллипсоида как V=ab2/2, где a - длина, b - ширина и высота опухолевого узла. Масса опухоли соответствует ее объему, поскольку плотность опухолевой ткани принято считать равной 1 г/см3. Каждая группа животных, получавших определенную дозу препарата, состояла из 6 мышей при 8 животных в контроле [Трещалина Е.М., Жукова О.С., Герасимова Г.К., Андронова Н.В., Гарин A.M. «Методические указания по изучению противоопухолевой активности фармакологических веществ» // «Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ» (ред. Р.У. Хабриев). Издание 2. // Москва, «Медицина», 2005, с.637-651].
Результаты исследования
Первичное онкобиологическое изучение соединения 1 (препарата AS-01) включало определение острой токсичности и переносимости животными препарата при его однократном п/о введении, а также оценку влияния AS-01 на развитие солидной опухоли - карциномы Ca-755.
Токсичность препарата
Определение острой токсичности соединения 1 препарата проводили при однократном п/о введении интактным мышам линии BDF1 в диапазоне доз от 400 до 800 мг/кг. Соединение вводили животным в виде раствора в подсолнечном масле в концентрации 10 мг/мл. Объем вводимого п/о раствора соединения 1 колебался в зависимости от дозы в пределах от 0,8 мл до 1,6 мл.
В исследованном диапазоне доз соединение 1 не вызывало гибели животных при наблюдении за ними в течение одного месяца.
Внешний вид животных, получавших препарат, их аппетит, активность, подвижность, поведенческие реакции, деятельность желудочно-кишечного тракта соответствовали норме и свидетельствовали о физически бодром, здоровом состоянии мышей.
Необходимо подчеркнуть, что соединение 1 при однократном п/о введении в диапазоне доз 400-800 мг/кг не только хорошо переносится животными, но вызывает значительное увеличение массы их тела - на 67-98%, при 10% увеличении массы тела у контрольных животных в течение периода наблюдения (1 месяц).
Влияние соединения 1 в примененных дозах на динамику изменения массы тела мышей на протяжении 28 суток характеризуют данные, представленные в таблице 1.
Такая хорошая переносимость животными соединения 1 не характерна для веществ, проявляющих противоопухолевую активность, этот результат требует дальнейших специальных исследований и косвенным образом указывает на возможность принципиальных отличий в механизме действия соединения 1 от механизма действия других ферроценсодержащих соединений, в том числе вышеупомянутых соединений П-1 и П-2.
Противоопухолевая активность препарата
Изучение противоопухолевой активности соединения 1 (препарата AS-01) проведено на модели перевиваемой опухоли мышей - карциноме Ca-755 (мыши линии BDF1).
Соединение 1 вводили мышам в дозе 100 мг/кг в сутки п/о в растворе подсолнечного масла по 0,2 мл ежедневно, восьмикратно, начиная со следующих суток после перевивки опухоли.
Влияние препарата на развитие карциномы Ca-755 характеризуют данные, представленные на чертеже (в виде кинетических кривых) и в таблице 2.
Как видно из представленных данных, применение соединения 1 вызывает весьма значительное ингибирование опухолевого роста.
Значения коэффициента торможения роста опухоли составляют 78 и 60% на 10 и 14 сутки после перевивки опухоли, соответственно (см. чертеж, табл.2).
Таким образом, исследование противоопухолевой активности соединения 1 позволило установить, что указанное соединение обладает определенным противоопухолевым действием в отношении карциномы Ca-755, вызывая торможение ее роста почти на 80% по сравнению с контролем (10 сутки развития опухоли).
ЗАКЛЮЧЕНИЕ
Проведенное онкобиологическое изучение соединения 1 (AS-01) позволило обнаружить его следующие свойства.
- Соединение 1 в диапазоне доз 400-800 мг/кг при п/о однократном введении хорошо переносится интактными животными (мыши BDF1), вызывает значительное увеличение массы их тела (60-90%) по сравнению с контролем и не приводит к изменению поведенческих реакций мышей в течение периода наблюдения (1 месяц);
- Хорошая переносимость животными соединения 1, выразившаяся в увеличении массы их тела под влиянием соединения 1, является нехарактерным свойством для веществ, проявляющих противоопухолевую активность, это требует дальнейших специальных исследований и косвенным образом указывает на возможность принципиальных отличий в механизме действия соединения 1 и механизме действия других ферроценсодержащих соединений (в том числе вышеупомянутых соединений П-1 и П-2).
- Соединение 1 обладает определенным противоопухолевым действием в отношении карциномы Ca-755, вызывая торможение ее роста на 80% по сравнению с контролем (10 сутки развития опухоли).
- Обнаруженная чувствительность к соединению 1 карциномы Ca-755 - опухоли, известной своей устойчивостью к химиотерапевтическим воздействиям - при хорошей переносимости препарата животными, выразившейся в увеличении массы их тела под влиянием соединения 1, указывает на целесообразность дальнейшего углубленного исследования фармакологического механизма действия и противоопухолевых свойств препарата на расширенном спектре перевиваемых опухолей животных при различных режимах его применения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ФЕРРОЦЕНИЛАЛКИЛЬНЫХ ПРОИЗВОДНЫХ С,C'-ДИПИРАЗОЛИЛСЕЛЕНИДА | 2019 |
|
RU2732409C1 |
| ФЕРРОЦЕНИЛАЛКИЛЬНЫЕ ПРОИЗВОДНЫЕ ДИПИРАЗОЛИЛСЕЛЕНИДОВ В КАЧЕСТВЕ БИОЛОГИЧЕСКИ АКТИВНЫХ СОЕДИНЕНИЙ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ) | 2019 |
|
RU2714891C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВООПУХОЛЕВОЙ И АНАЛЬГЕТИЧЕСКОЙ АКТИВНОСТЬЮ | 1996 |
|
RU2121839C1 |
| СРЕДСТВА, ПОДАВЛЯЮЩИЕ РОСТ РАКОВЫХ КЛЕТОК | 1993 |
|
RU2098096C1 |
| Применение 4-фенил-3,4-дигидро-2H-бензо[e][1,3]оксазин-2-тиона в лечении злокачественных опухолевых заболеваний | 2024 |
|
RU2840496C1 |
| Производное класса N-гликозидов индоло[2,3-а]пирроло[3,4-с]карбазол-5,7-дионов - N-{ 12-(β-D-ксилопиранозил)-5,7-диоксо-индоло[2,3-а]пирроло[3,4-с] карбазол-6-ил} пиридин-2-карбоксамид, обладающее цитотоксической и противоопухолевой активностью | 2017 |
|
RU2667906C1 |
| КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ ЖЕЛЕЗА - ФЕРРОЦЕНИЛАЛКИЛПОЛИФТОРАЗОЛЫ, ОБЛАДАЮЩИЕ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 1996 |
|
RU2089507C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 1991 |
|
RU2025125C1 |
| СРЕДСТВО, ПОВЫШАЮЩЕЕ ПРОТИВООПУХОЛЕВЫЙ ЭФФЕКТ МЕТОТРЕКСАТА | 2009 |
|
RU2411947C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВООПУХОЛЕВЫМ ДЕЙСТВИЕМ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2007 |
|
RU2349317C1 |
Изобретение относится к новому производному ферроцена 1-(1,1,1,3,3,3-гексафтор-2-ферроценилпроп-2-ил)-имидазолу формулы
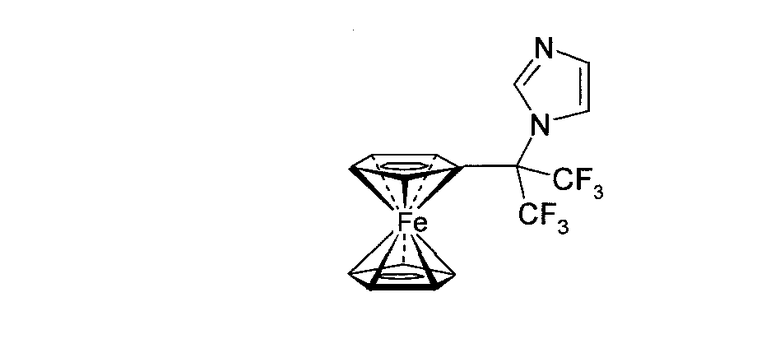 ,
,
проявляющему противоопухолевую активность. Также предложен способ его получения (варианты). Изобретение позволяет получить новое производное ферроцена, которое может быть использовано в медицине для химиотерапии онкологических заболеваний. 3 н. и 1 з.п. ф-лы, 1 ил., 2 табл., 3 пр.
1. 1-(1,1,1,3,3,3-Гексафтор-2-ферроценилпроп-2-ил)-имидазол формулы
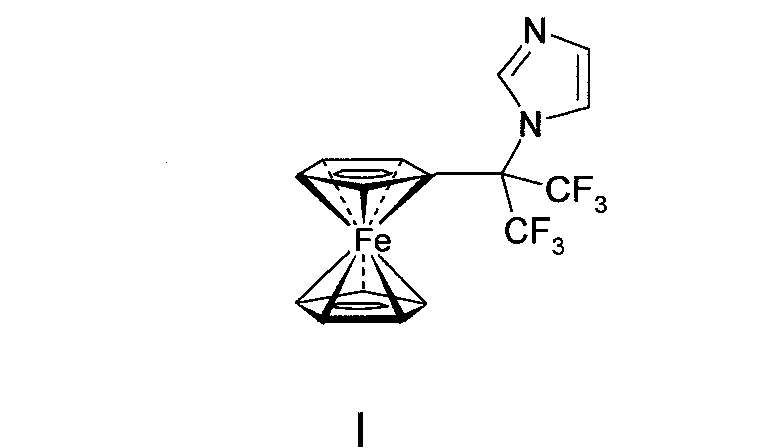
проявляющий противоопухолевую активность.
2. Способ получения соединения по п.1 взаимодействием соответствующего α-гидроксиалкилферроцена с 1,1'-карбонилдиимидазолом при кипячении в растворителе, отличающийся тем, что взаимодействие проводят в толуоле при температуре кипения толуола, а в качестве α-гидроксиалкилферроцена используют 1-ферроценил-1-трифторметил-2,2,2-трифторэтанол.
3. Способ получения соединения по п.1, заключающийся во взаимодействии 1-[1,1,1,3,3,3-гексафтор-2-хлорпроп-2-ил]ферроцена, имидазола и трет.-бутилата калия при мольном соотношении реагентов 1:1,2:1,2, которое проводят в толуоле при кипячении.
4. Способ по п.3, отличающийся тем, что дополнительно вводят йодид калия в качестве катализатора при мольном соотношении трет.-бутилата калия и йодида калия 10:1.
| SIMENEL A.A | |||
| et al, Synthesis and enantiomeric resolution of ferrocenylalkyl azoles, J | |||
| Organomet | |||
| Chem., 2003, v | |||
| Колосниковая решетка с охлажденными водой колосниками | 1925 |
|
SU688A1 |
| Прибор для определения всасывающей силы почвы | 1921 |
|
SU138A1 |
| SIMENEL A.A | |||
| et al, Simple rouye to ferrocenylalkyl nucleobases | |||
| Antitumor activity in vivo, Appl | |||
| Organomet | |||
| Chem., 2009, v | |||
| Прибор для равномерного смешения зерна и одновременного отбирания нескольких одинаковых по объему проб | 1921 |
|
SU23A1 |
| Прибор для записи звуковых волн | 1920 |
|
SU219A1 |
| SNEGUR L.V | |||
| et al, Synthesis, structure and redox potentials of biologically | |||
Авторы
Даты
2014-11-20—Публикация
2013-07-05—Подача