Изобретение относится к медицине, а именно к фармакологии и онкологии, и может найти применение в лечении злокачественных опухолевых заболеваний человека, в том числе детей.
В основе современного лечения злокачественных опухолевых заболеваний человека лежит применение классических химиотерапевтических лекарственных препаратов (Signal Transduct Target Ther. 2021, 6, 201). Недостатками этих лекарственных средств является их высокая токсичность, обусловливающая повреждение здоровых клеток и тканей организма, а также формирование к ним нечувствительности или резистентности опухолевых клеток (Curr Treat Options Oncol. 2020, 21, 27; Int J Mol Sci. 2021, 22, 4673). Появление средств иммунобиологической и молекулярно-направленной - таргетной - терапии позволило отчасти решить проблему токсичности и эффективности борьбы с опухолевым процессом, однако, тем не менее, ни один терапевтический протокол в настоящее время не обходится без использования в своем составе классических химиопрепаратов. Это обусловливает необходимость поиска новых, менее токсичных и более эффективных соединений - кандидатов в лекарственные препараты.
Из уровня науки и техники известен химиотерапевтический лекарственный препарат циклофосфамид, обладающий противоопухолевой активностью в отношении злокачественных клеток эпителиального и неэпителиального происхождения (Pediatr Blood Cancer. 2017, 64, 8; Antineoplastic Agents. 2023 PMID: 31643354), выбранный нами в качестве прототипа. Недостатками препарата являются его высокая токсичность, узкий спектр антибластомного действия, и невысокая антиметастатическая активность.
Известно, что производные бензоксазин-2-тиона используются в синтезе ингибиторов ДНК-зависимой протеинкиназы и фосфоинозитид-3-киназы (Eur. J. Med. Chem. 2012, 57, 85), НАД-зависимой сиртуин-2 деацетилазы (Arch. Pharm. Chem. Life Sci. 2017, 350, e1700097), ацетилхолинэстеразы (J. Enzyme Inhib. Med. Chem. 2018, 33, 1506) проявляют антидепрессантную (Патент GB 1162628; заявл. Societa Farmaceutici Italia. 22.07.1968; опубл. 27.08.1969), противотуберкулёзную (Eur. J. Med. Chem. 2000, 35, 733; Farmaco 2001, 56, 803; Bioorg. Med. Chem. 2010, 18, 8178) виды физиологической активности.
Технический результат заключается в снижении токсичности и повышении фармакологической противоопухолевой и антиметастатической активности.
Технический результат достигается, тем, что 4-фенил-3,4-дигидро-2H-бензо[e][1,3]оксазин-2-тиона формулы (I)
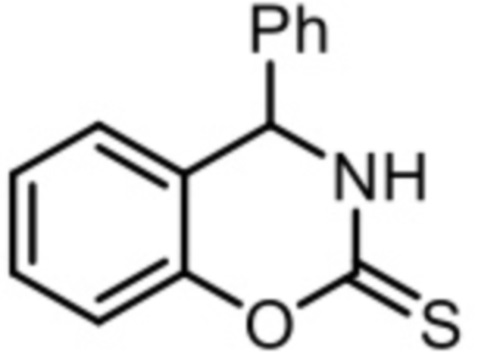 (I)
(I)
обладает противоопухолевой и антиметастатической активностью.
Фармакологическая активность соединения формулы (I) представлена в нижеследующих примерах.
Пример 1. Острая токсичность соединения формулы (I) и прототипа
Острая токсичность I изучена в опытах на белых беспородных мышах (60 особей обоего пола весом 19-22 г, полученных из питомника филиала «Андреевка» ФГБУН НЦБМТ ФМБА России) при внутрибрюшинном введении соединения формулы (I) в виде раствора в 0,9% изотоническом растворе хлорида натрия в объеме 0,8-1,0 мл в возрастающих концентрациях. В случае превышения общего объема вводимого вещества 1,0 мл осуществляли кратное введение через каждые 30 мин.
Показатель ЛД50 рассчитывали методом Личфилда-Уилкоксона (Методические рекомендации по изучению общетоксического действия лекарственных средств / Руководство по проведению доклинических исследований лекарственных средств. Часть первая. - М.: Гриф и К, 2012, 25-35; Токсикология лекарственных средств. - М.: Издательский дом "Русский врач", 2003, 20-24). Результаты исследования соединения формулы (I), а также прототипа циклофосфамида представлены в табл. 1.
Из предлагаемых в таблице данных видно, что заявляемое соединение формулы (I) более, чем в полтора раза менее токсично, нежели прототип циклофосфамид при внутрибрюшинном введении. При этом соединение формулы (I) относится к классу 3 (умеренно токсичные вещества) классификации токсичности химических веществ в соответствии с ГОСТом 12.1.007 - 76 (Хим.-фарм. журнал. 2003. 37, 32-34).
Пример 2. Противоопухолевая активность соединения формулы (I) в культуре опухолевых клеток человека
Противоопухолевая активность соединения формулы (I) изучена в культурах опухолевых клеток человека - нейробластомы SH-SY5Y, гепатоцеллюлярной карциномы HepG2 и уротелиальной карциномы Т24 - при их инкубации в присутствии соединения формулы (I) в диапазоне концентраций от 10-12 до 10-3 М в течение 48 часов.
Противоопухолевую активность изучали в клеточных опухолевых системах, полученных из банка опухолевых штаммов ФГБУ «Национальный медицинский исследовательский центр онкологии им. Н.Н. Блохина» Минздрава России. Клеточные культуры инкубировали в 96-луночных планшетах в среде DMEM с прибавлением 10% эмбриональной телячьей сыворотки, 1% пенициллина и стрептомицина во влажной среде СО2 инкубатора при температуре 37°С. Для оценки противоопухолевой цитотоксичности использовали тридцатую генерацию культуры после ее разморозки (Методические рекомендации по доклиническому изучению противоопухолевой активности лекарственных средств / Руководство по проведению доклинических исследований лекарственных средств. Часть первая. - М.: Гриф и К, 2012, 640-654).
Противоопухолевое действие оценивали в соответствии с международными рекомендациями по изучению специфической активности противоопухолевых препаратов в тесте выживаемости клеток с хлоридом трифенилтетразолия (J. Immunol. Methods. 1983, 65, 55-63).
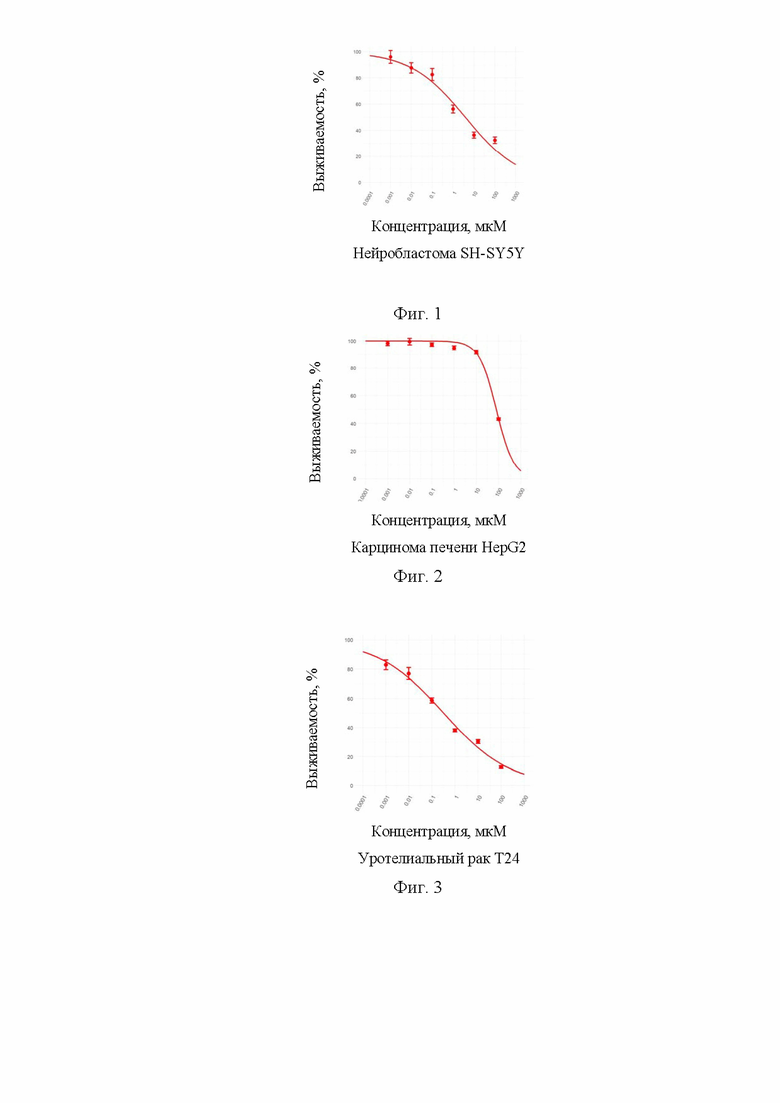
Результаты исследования противоопухолевого действия соединения формулы (I) в культурах опухолевых клеток представлены на Фиг. 1. Из представленных данных видно, что инкубация соединения формулы (I) в возрастающих в культуре опухолевых клеток эпителиального и неврогенного происхождения сопровождается зависимой от концентрации гибелью клеток. Вычисленные для соединения формулы (I) значения средне-цитотоксической концентрации (IC50) составили: для культуры нейробластомы SH-SY5Y - 3,82 мкМ, гепатоцеллюлярной карциномы HepG2 - 78,55 мкМ и для уротелиальной карциномы Т24 - 0,32 мкМ.
Таким образом, соединение формулы (I) обладает цитотоксичностью в отношении опухолевых клеток, имеющих эпителиальное и неврогенное происхождение.
Пример 3. Противоопухолевая и антиметастатическая активность соединения формулы (I) на модели сингенной опухоли - карциномы легкого Льюиса у мышей С57Вl/6
Противоопухолевая и антиметастатическая активность соединения формулы (I) изучена в опытах на 30 мышах-самках линии С57Вl/6, полученных из питомника SPF-лабораторных животных - филиала ФГБУН Институт биоорганической химии им. академиков М.М. Шемякина и Ю.А. Овчинникова Российской академии наук (г. Пущино) при внутрибрюшинном введении заявляемого соединения формулы (I) и циклофосфамида (прототип) в дозе, составляющей 1% от показателя ЛД50 при данном пути введения, объемом 0,8-1,0 мл в 0,9% изотоническом растворе хлорида натрия, через 72 часа после перевивки опухоли в течение 7 суток.
Противоопухолевую и антиметастатическую активность изучали на сингенной опухолевой системе - карциноме легкого Льюиса - из банка опухолевых штаммов ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет). Опухоль воспроизводили трехступенчатой перевивкой клеток опухолевого штамма (Методические рекомендации по доклиническому изучению противоопухолевой активности лекарственных средств / Руководство по проведению доклинических исследований лекарственных средств. Часть первая. - М.: Гриф и К, 2012, 640-654).
Противоопухолевое и антиметастатическое действие оценивали в соответствии с международными рекомендациями по изучению специфической активности противоопухолевых препаратов (Cancer Chemother. Rep. 1972, 3, 1-103).
Результаты исследования противоопухолевого и антиметастатического действия соединения формулы (I) на модели сингенной опухоли - карциномы легкого Льюиса - представлены в табл. 2 и 3. Из представленных в табл. 2 данных видно, что внутрибрюшинное введение соединения формулы (I) в дозе 1,7 мг/кг в сутки в течение 7 суток сопровождается статистически значимыми различиями в объеме опухоли между контрольной группой и группой животных, получавших прототип в эквитоксической дозе, на 14-х и 22-х сутках наблюдения. В эти же временные интервалы статистической значимостью отличался и индекс торможения роста опухоли. У 40% животных в группе мышей, получавших соединение формулы (I), регистрировали ремиссию опухолевого процесса, чего не было в группе животных, получавших прототип. Помимо этого, были зафиксированы статистически значимые различия как в частоте метастазирования, так и в количестве поверхностных метастазов в легкие животных при сравнении с мышами контрольной группы и группы животных, получавших прототип в эквитоксической дозе, на 31-е сутки формирования опухоли.
Таким образом, в отличие от прототипа, соединение формулы (I) отличается большей силой противоопухолевого в отношении первичного опухолевого узла и антиметастатического действия, формирующегося в месте трансплантации опухолевых клеток в организм мышей.
Пример 4. Противоопухолевая и антиметастатическая активность соединения формулы (I) на животной модели с использованием ксенографта человеческой опухоли - уротелиальной карциномы
Противоопухолевую и антиметастатическую активность соединения формулы (I) изучили в опытах на 8-10 недельных 15 мышах-самках линии атимических мышей BALB/c nu/nu, полученных из питомника SPF-лабораторных животных - филиала ФГБУН Институт биоорганической химии им. академиков М.М. Шемякина и Ю.А. Овчинникова Российской академии наук (г. Пущино) при внутрибрюшинном введении соединения общей формулы (I) и циклофосфамида (прототип) в дозе, составляющей 1% от показателя ЛД50 при данном пути введения, объемом 0,8-1,0 мл в 0,9% изотоническом растворе натрия хлорида, через 72 часа после перевивки опухоли в течение 7 суток.
Противоопухолевую и антиметастатическую активность изучали на опухолевой системе - ксенографте уротелиальной карциномы мочевого пузыря - из банка опухолевых штаммов ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет). Опухоль воспроизводили трёхступенчатой перевивкой клеток опухолевого штамма подкожно животным в область левого бедра (Методические рекомендации по доклиническому изучению противоопухолевой активности лекарственных средств / Руководство по проведению доклинических исследований лекарственных средств. Часть первая. - М.: Гриф и К, 2012, 640-654).
Фармакологическое действие оценивали в соответствии с международными рекомендациями по изучению специфической активности противоопухолевых препаратов (Cancer Chemother. Rep. 1972, 3, 1-103).
Результаты исследования противоопухолевого и антиметастатического действия соединения формулы (I) на модели уротелиальной карциномы представлены в табл. 4 и 5. Из представленных в табл. 3 и 4 данных хорошо видно, что внутрибрюшинное введение соединения формулы (I) в дозе 1,7 мг/кг в сутки в течение 7 суток сопровождается статистически значимыми различиями в объеме опухоли между контрольной группой и группой животных, получавших прототип в эквитоксической дозе, на 14-х и 22-х сутках наблюдения. Кроме того, были зафиксированы статистически значимые различия как в количестве, так и объеме метастатического поражения головного мозга и легких животных при сравнении с мышами контрольной группы и группы животных, получавших прототип в эквитоксической дозе, на 31-е сутки формирования опухоли.
Таким образом, в отличие от прототипа, соединение формулы (I) отличается большей противоопухолевой и антиметастатической активностью в отношении ксенографта уротелиальной карциномы, перевитого в организм атимичных линейных мышей.
Исследования проведены в соответствии с этическими требованиями к работе с экспериментальными животными («Правила проведения работ с использованием экспериментальных животных» (приказ МЗ СССР № 755 от 12.08.1987 г.), Федеральным законом «О защите животных от жестокого обращения» от 01.01.1997 г., Приказом Министерства здравоохранения Российской Федерации от 01.04.2016 г. №199н «Об утверждении правил надлежащей лабораторной практики», ГОСТом 33216-2014 «Руководство по содержанию и уходу за лабораторными животными. Правила содержания и ухода за лабораторными грызунами и кроликами» (введен в действие 01.07.2016 г.) и одобрены НЭК ФГБУ «НМИЦ ДГОИ им. Дмитрия Рогачева» Минздрава России.
По сравнению с известным решением применение соединения формулы (I) позволяет снизить острую токсичность, увеличить силу противоопухолевого и атиметастатического эффекта при формировании сингенной модели опухоли у мышей, а также повысить противоопухолевую и антиметастатическую активность при уротелиальной карциноме.
Таблица 1
Примечание: * - различия статистически достоверны (р=0,004, одномерный дисперсионный анализ, критерий t Стьюдента).
Таблица 2
1,0 мг/кг, n=5
1,7 мг/кг, n=5
Примечание: * - различия при сравнении с контролем с карциномой легкого Льюиса статистически достоверны при р<0,05; а - различия при сравнении с контролем и циклофосфамидом (прототипом) статистически достоверны при р<0,05 (одномерный дисперсионный анализ, критерий Ньюмена-Кейлса).
Таблица 3
1,0 мг/кг, n=5
1,7 мг/кг, n=5
Примечание: * - различия при сравнении с контролем с опухолью статистически достоверны при р<0,05 (точный критерий Фишера); а - различия при сравнении с контролем и циклофосфамидом (прототипом) статистически достоверны при р<0,05 (одномерный дисперсионный анализ, критерий Ньюмена-Кейлса).
Таблица 4
1,0 мг/кг, n=5
1,7 мг/кг, n=5
Примечание: * - различия при сравнении с контролем с ксенографтом опухоли мочевого пузыря статистически достоверны при р<0,05; а - различия при сравнении с контролем и циклофосфамидом (прототипом) статистически достоверны при р<0,05 (одномерный дисперсионный анализ, критерий Ньюмена-Кейлса).
Таблица 5
1,0 мг/кг, n=5
1,7 мг/кг, n=5
Примечание: * - различия при сравнении с контролем с опухолью статистически достоверны при р<0,05 (точный критерий Фишера); а - различия при сравнении с контролем и циклофосфамидом (прототипом) статистически достоверны при р<0,05 (одномерный дисперсионный анализ, критерий Ньюмена-Кейлса).
Фиг. 1. Результаты исследования противоопухолевого действия соединения формулы (I) в культурах опухолевых клеток Нейробластомы SH-SY5Y.
Фиг. 2. Результаты исследования противоопухолевого действия соединения формулы (I) в культурах опухолевых клеток Карцинома печени HepG2.
Фиг. 3. Результаты исследования противоопухолевого действия соединения формулы (I) в культурах опухолевых клеток Уротелиальный рак Т24.
| название | год | авторы | номер документа |
|---|---|---|---|
| 2-Аминия-7-(диэтиламино)-4-(4-метоксибензо[d][1,3]диоксол-5-ил)-4Н-хромен-3-карбонитрила N-ацетиламиноэтаноат, проявляющий противоопухолевую активность | 2018 |
|
RU2674987C1 |
| Новое производное 9-аминоакридона, обладающее противоопухолевой и антиметастатической активностью | 2021 |
|
RU2810783C2 |
| Производные 2-аминохроменов проявляющие противоопухолевую активность. Фармацевтические композиции | 2018 |
|
RU2704262C1 |
| СРЕДСТВО ДЛЯ КОРРЕКЦИИ ЦИТОТОКСИЧЕСКИХ ЭФФЕКТОВ ПАРАНЕОПЛАСТИЧЕСКИХ ПРОЦЕССОВ И ХИМИОТЕРАПИИ, ОБЛАДАЮЩЕЕ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2011 |
|
RU2447888C1 |
| Лиофилизат на основе Bacillus subtilis для перепрограммирования иммунитета в противоопухолевом направлении | 2023 |
|
RU2821073C1 |
| Средство, обладающее противоопухолевым действием, для лечения онкологических заболеваний | 2018 |
|
RU2761429C2 |
| Средство, обладающее одновременно протекторным действием в отношении здоровых органов и тканей и адъювантным действием при радио- и химиотерапии опухолей | 2015 |
|
RU2646497C2 |
| СРЕДСТВО С ПРОТИВООПУХОЛЕВОЙ И АНТИМЕТАСТАТИЧЕСКОЙ АКТИВНОСТЬЮ, ПРОТИВОВОСПАЛИТЕЛЬНЫМ И ПРОТИВОАЛЛЕРГЕННЫМ ДЕЙСТВИЕМ | 2018 |
|
RU2686672C1 |
| ТЕТРАЭТИЛ-2-(2,2,6,6-ТЕТРАМЕТИЛПИПЕРИДИН-4-ИЛАМИНО)-ЭТИЛЕН-1,1-БИСФОСФОНАТ, ОБЛАДАЮЩИЙ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2013 |
|
RU2506085C1 |
| ПРОТИВОВОСПАЛИТЕЛЬНОЕ СРЕДСТВО С АНТИКОАГУЛЯНТНОЙ, ПРОТИВООПУХОЛЕВОЙ И АНТИМЕТАСТАТИЧЕСКОЙ АКТИВНОСТЬЮ | 2009 |
|
RU2412712C1 |
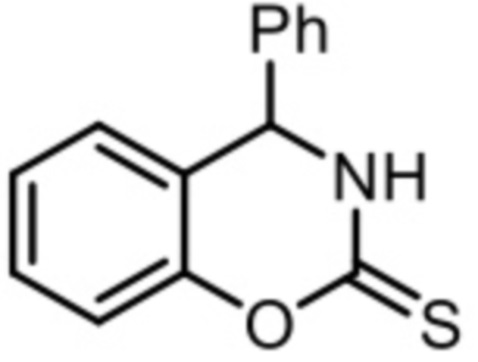
Изобретение относится к медицине, а именно к фармакологии и онкологии. Предложено применение 4-фенил-3,4-дигидро-2H-бензо[e][1,3]оксазин-2-тиона формулы (I), представленной ниже, в лечении злокачественных опухолевых заболеваний. Применение соединения формулы (I) позволяет снизить острую токсичность, увеличить силу противоопухолевого и антиметастатического эффекта при формировании сингенной модели опухоли, а также повысить противоопухолевую и антиметастатическую активность при уротелиальной карциноме. 3 ил., 5 табл., 4 пр.
 (I)
(I)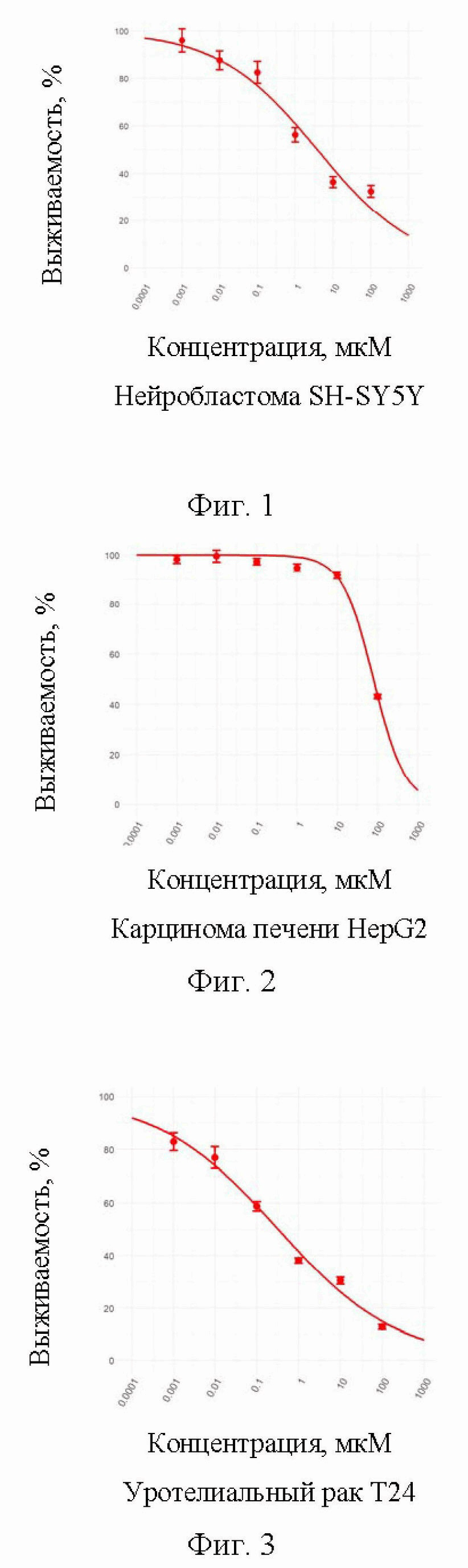
Применение 4-фенил-3,4-дигидро-2H-бензо[e][1,3]оксазин-2-тиона формулы (I)
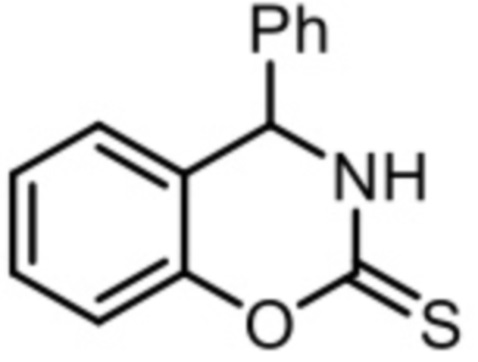 (I)
(I)
в лечении злокачественных опухолевых заболеваний.
| KOBAYASHI K | |||
| et al | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| FRESNEAU B | |||
| et al | |||
| Investigating the heterogeneity of alkylating agents’ efficacy and toxicity between sexes: A systematic review and meta-analysis of randomized trials comparing | |||
Авторы
Даты
2025-05-26—Публикация
2024-05-21—Подача