Изобретение относится к медицине, точнее к хирургии, и может найти применение при лечении новообразований печени.
В последние годы во всем мире наблюдается отчетливая тенденция к увеличению числа больных с очаговыми образованиями печени как злокачественного, так и доброкачественного характера. Так, гепатоцеллюлярный рак в России составляет 1,7-2,2% всех злокачественных новообразований, метастатическое поражение печени выявляется у 20-70% онкологических больных. Гемангиомы печени встречаются на аутопсии в 0,4-7,3% случаев.
Обширные анатомические резекции печени являются основным методом радикального хирургического лечения больных со злокачественными опухолями, а также доброкачественными новообразованиями печени больших размеров.
Благодаря совершенствованию техники операции и внедрению современных технологий, летальность после обширных резекций печени за последнее время заметно снизилась и составляет при типичных резекциях по данным зарубежных статистик 2-6%. По данным отечественных авторов, летальность после удаления гигантских новообразований печени несколько выше и составляет 4,1-9,5%, а при радикальных операциях по поводу альвеококкоза печени достигает 16,2%.
В то же время, в нестандартных ситуациях - при гигантских размерах новообразований, превышающих 15 см в диаметре, локализации их в кавальных или глиссоновых воротах печени, а также у больных с низким функциональным резервом печени - риск развития угрожающих жизни осложнений продолжает оставаться чрезвычайно высоким.
По заключению хирургов, после любой резекции печени остаются различные по объему резидуальные полости в области культи печени или в поддиафрагмальном пространстве, в которых при неполном гемо- и холестазе скапливаются желчь и кровь. При недостаточном или неправильном дренировании остаточных полостей они инфицируются, что приводит к возникновению поддиафрагмального абсцесса или абсцесса в области культи печени. Особенно велика опасность этих осложнений после больших и предельно больших резекций, когда остаточные полости достигают огромных размеров и полная ликвидация их не всегда удается известными способами.
Одним из наиболее частых осложнений после обширных резекций печени (240 операций) было формирование ограниченных жидкостных скоплений (гематом, билом, серозной жидкости) в зоне резекции печени. Данное осложнение было отмечено у 38 (15,8%) больных (Н.А. Назаренко. Обширные резекции печени: дис.… д.м.н. - Москва, 2005. - 248 с.). К факторам риска развития гнойно-септических осложнений (поддиафрагмальный абсцесс), частота которых достигает 13%, относится скопление жидкости в зоне оперативного вмешательства. При этом частота сердечно-легочных осложнений достигает 20% (В.В. Макарова. Послеоперационные осложнения при резекциях печени: Афтореф. канд. Дисс. - М., 2007. - 25 с.).
По данным исследователей, наиболее частыми осложнениями после операций на печени являются гнойно-воспалительные осложнения со стороны брюшной полости (нагноение остаточных полостей после резекций печени, поддиафрагмальные и подпеченочные абсцессы), частота которых варьирует от 15% до 30% случаев. Подобные осложнения значительно ухудшают результаты лечения, являясь причиной летальных исходов у четверти больных, уступая в этом только острой печеночной недостаточности. Таким образом, выбор оптимального способа дренирования брюшной полости после операций на печени занимает важное место в профилактике и лечении гнойно-воспалительных осложнений.
Развитие новообразований правой половины печени, особенно при достижении ими больших размеров, сопряжено с анатомическими изменениями, обусловленными дислокацией соседних с печенью органов, и вторичными функционально-приспособительными реакциями, связанными с повышением внутрибрюшного давления, высоким стоянием правого купола диафрагмы и снижением дыхательного объема правого легкого. Одним из спонтанно возникающих приспособительных физиологических механизмов коррекции дыхательной недостаточности вследствие снижения экскурсии диафрагмы может служить смена брюшного типа дыхания на грудной. Эволюция указанных функционально-приспособительных реакций со стороны организма пациента растянута во времени и зависит от скорости увеличения новообразования, которая при злокачественных опухолях может исчисляться месяцами, а при доброкачественных заболеваниях (гемангиомы, кисты, аденомы, паразитарные поражения) - годами. Хирургическое вмешательство с удалением гигантского новообразования правой доли печени путем выполнения ее обширной резекции изменяет топографоанатомические взаимоотношения органов как брюшной, так и грудной полостей. Как следствие этого, возникает необходимость достижения в короткие сроки раннего послеоперационного периода функционально-приспособительных изменений к новым анатомическим условиям. Организм больного, ослабленный основным заболеванием, перенесенным хирургическим вмешательством с интраоперационной кровопотерей, в большинстве случаев не способен самостоятельно справиться с указанными задачами. При этих обстоятельствах лечебные действия должны быть направлены не только на поддержание витальных функций пациента и сокращение сроков их восстановления, но и на профилактику возможных осложнений.
Задачи хирургического лечения гигантских новообразований правой половины печени включают выполнение резекции печени, а также устранение «остаточной» полости, которая формируется в правом поддиафрагмальном пространстве за счет одномоментного удаления новообразований большого объема. Для устранения скопления раневого отделяемого в «остаточной» полости применяются различные системы дренирования с использованием от трех до пяти профильных дренажей и активного вакуум-аспирирования.
Наиболее близким к предлагаемому является способ дренирования, описанный В.А. Журавлевым (В.А. Журавлев. Большие и предельно большие резекции печени. - Изд-во Сарат. ун-та, 1986. - 216 с.). Способ заключается в том, что после удаления новообразования печени путем выполнения правосторонней гемигепатэктомии в правое поддиафрагмальное пространство и к раневой поверхности оставшейся части печени устанавливаются силиконовые перфорированные дренажи в количестве от 3 до 5 в зависимости от величины остаточной полости, образовавшейся после удаления части печени с опухолью. В послеоперационном периоде все дренажи подсоединяются к внешнему устройству, обеспечивающему активную аспирацию раневого отделяемого (серозная жидкость, желчь, кровь) за счет создания разряжения в замкнутой системе: брюшная полость - дренажные трубки - емкость для сбора раневого отделяемого. Использование указанного количества дренажей с активной вакуум-аспирацией позволяет обеспечить сбор и удаление раневого содержимого из-под правого купола диафрагмы и от раневой поверхности печени в раннем послеоперационном периоде.
Несмотря на наличие положительных свойств рассмотренного метода при выполнении стандартных резекция печени по поводу новообразований, не превышающих в диаметре 15 см, имеются и существенные недостатки, которые с очевидностью проявляются при удалении гигантских новообразований правой половины печени. По заключению самого автора, устранение остаточных полостей огромных размеров и полная ликвидация их не всегда удается предложенными ранее и известными способами дренирования. Устранению «остаточной» полости путем использования различного количества и конструкций дренажей не позволяет достичь полной ее инволюции за средний период послеоперационного пребывания пациента в хирургическом стационаре. Сокращение времени дренирования правого поддиафрагмального пространства приводит к формированию резидуальной полости с угрозой ее вторичного инфицирования по дренажному каналу. Удлинение периода дренирования сопряжено с необходимостью пребывания пациента в стационаре или амбулаторно-поликлинического долечивания с увеличением общего времени потери трудоспособности. Кроме того, указанный способ дренирования не позволяет предупредить легочные осложнения, обусловленные ателектазом нижней доли правого легкого, так как не устраняет пролабирование правого купола диафрагмы в направлении грудной полости, которое в раннем послеоперационном периоде связано с повышением внутрибрюшного давления из-за пареза кишечника. В этих условиях, в связи с дыхательной недостаточностью из-за уменьшения дыхательного объема, сохраняется необходимость в более длительной вспомогательной искусственной вентиляции легких.
Технический результат настоящего изобретения состоит в уменьшении остаточной полости после удаления гигантских новообразований правой половины печени за счет гофрирования мышечной части диафрагмы и ротации левой половины печени вправо.
Этот результат достигается тем, что в известном способе дренирования с активной вакуум-аспирацией полости, оставшейся после больших и предельно больших резекций печени, согласно изобретению, непосредственно после удаления гигантского новообразования на мышечную часть диафрагмы по всей ее полуокружности накладывают гофрирующие швы вдоль линии прикрепления диафрагмы к грудной клетке с отступом от этой линии внутрь на 3-4 см, затем пересекают круглую и серповидную связки и левую половину печени ротируют вправо относительно оси, образованной нижней полой веной, на угол в 45-60° относительно сагиттальной плоскости, после чего печень фиксируют наложением швов между пересеченными круглой и серповидной связками, с одной стороны, и правым куполом диафрагмы - с другой, а дренирование поддиафрагмального пространства осуществляют силиконовыми трубками в количестве не более трех.
Наложение гофрирующих швов на мышечную часть диафрагмы позволяет создать дубликатуру диафрагмы, что обеспечивает, после завязывания швов, уменьшение пролабирования купола диафрагмы в направлении грудной клетки, способствуя тем самым расправлению нижней доли правого легкого и устранению ее ателектаза. При этом одновременное перемещение правого купола диафрагмы в направлении брюшной полости позволяет значительно уменьшить остаточную полость, образующуюся после удаления гигантского новообразования.
Перемещение левой половины печени вправо, после пересечения круглой и серповидной связок, путем ротации ее остатка вокруг оси, образованной нижней полой веной, на угол в 45-60° относительно сагиттальной плоскости и фиксация печени в таком положении в поддиафрагмальном пространстве швами, наложенными между пересеченными круглой и серповидной связками, с одной стороны, и правым куполом диафрагмы - с другой, позволяют значительно уменьшить остаточную полость, образующуюся после удаления гигантского новообразования.
Одномоментное уменьшение остаточной полости на завершающем этапе операции позволяет использовать для ее дренирования меньшее количество силиконовых перфорированных трубок (не более трех), что снижает вероятность осложнений, обусловленных самими дренажами.
Описанные технические приемы позволяют одномоментно уменьшить размеры «остаточной» полости, образующейся после удаления гигантских новообразований правой половины печени, а дренирование поддиафрагмального пространства силиконовыми трубками в количестве не более трех с активной вакуум-аспирацией позволяет в сроки до 7-10 суток избежать формирования резидуальной полости, снижая при этом сроки пребывания пациента в стационаре и общее время его нетрудоспособности. Кроме того, в послеоперационном периоде снижается частота легочных осложнений, обусловленных возможным ателектазом нижней доли правого легкого, уменьшением дыхательного объема и жизненной емкости легких.
Сущность способа поясняется примерами.
ПРИМЕР 1. Пациентка С., 1970 г.р. (№ истории 3883/12), была госпитализирована в хирургическое отделение РНЦРХТ 21.11.2012 с диагнозом: Гигантская опухоль правой половины печени.
Из анамнеза заболевания известно, что летом 2010 года по данным ультразвукового исследования и многослойной спиральной компьютерной томографии была выявлена опухоль правой доли печени. Пациентка госпитализирована в многопрофильную больницу по месту жительства, где была выполнена эксплоративная лапаротомия, биопсия опухоли. Результаты патоморфологического исследования биопсийного материала: эмбриональная саркома печени. В послеоперационном периоде проведено 5 курсов химиоэмболизации печени. Радикальное оперативное вмешательство не выполнялось. За последние 3 месяца отмечалось значительное увеличение размеров опухоли печени.
При осмотре пациентки в день поступления ее в стационар отмечалось значительное увеличение размеров живота за счет гигантской опухоли, исходящей из печени (рис.1а, б - внешний вид живота пациентки в двух проекциях, маркером отмечено расположение реберных дуг и границы нижней полуокружности опухоли печени).
27.11.2012 была выполнена многослойная спиральная компьютерная томография живота, подтвердившая наличие гигантской опухоли, замещавшей всю правую половину печени и оттеснявшей рядом расположенные органы (почку, тонкую, толстую кишку, двенадцатиперстную кишку и поджелудочную железу, нижнюю полую вену) и занимавшей большую часть брюшной полости. (рис.2, стрелкой указана сдавленная и оттесненная опухолью нижняя полая вена).
05.12.2012 - Лапаротомия по Starzl. Ревизия органов брюшной полости. Правосторонняя расширенная гемигепатэктомия. Холецистэктомия. Дренирование брюшной полости.
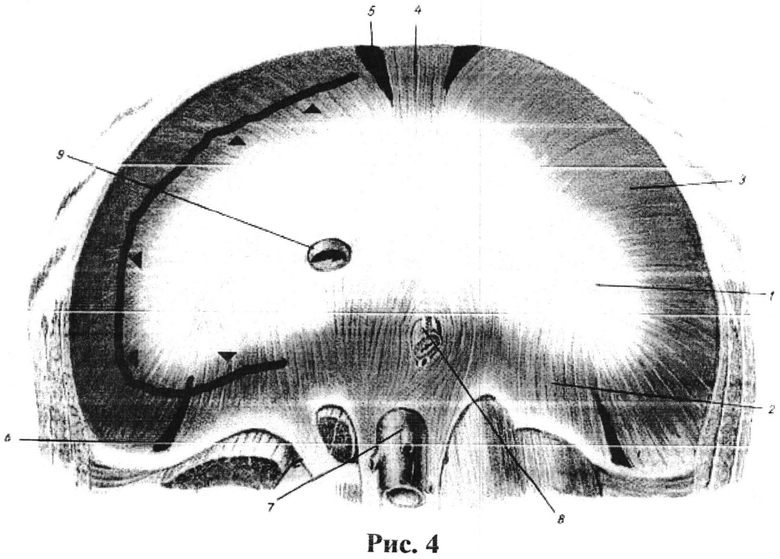
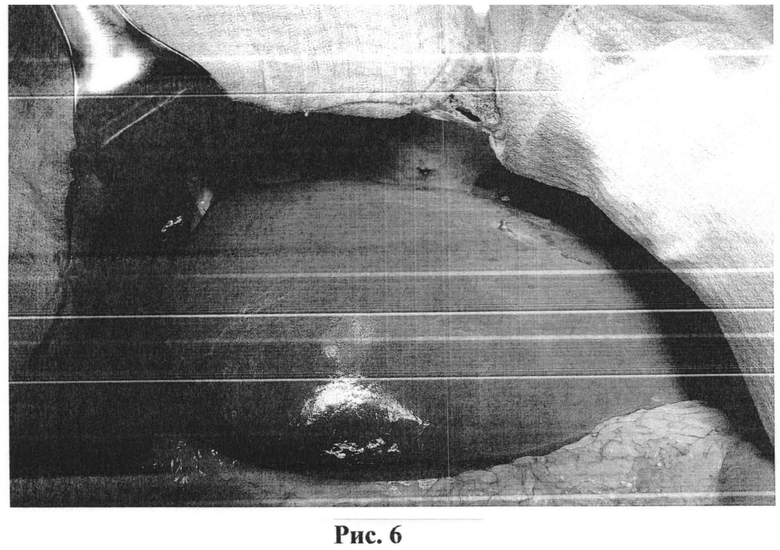
Под эндотрахеальным наркозом произведена лапаротомия по Starzl с лирообразным горизонтальным разрезом ниже пупка с резекцией хрящевой части X ребра. В брюшной полости умеренное количество плоскостных спаек, асцита. Канцероматоза нет. Практически всю брюшную полость занимала гигантская опухоль, исходящая из правой доли печени размерами 50×40×40 см. Органы брюшной полости смещены влево, печень распластана по опухоли, двенадцатиперстная кишка оттеснена в левую половину брюшной полости, интимно спаяна с правой долей печени. Правая почка находилась над лоном, содержала три кисты, которые были вскрыты и полость кист обработана аргоно-плазменным коагулятором. В малом тазу определялись рубцово-деформированные яичники, в правом яичнике - лимфоцеле. Опухоль печени спаяна с органами брюшной полости, однако спайки относительно рыхлые. При мобилизации двенадцатиперстной кишки и отделении ее от печени выявлена язва двенадцатиперстной кишки, пенетрирующая в желчный пузырь. Дефект кишки в области пенетрации ушит двухрядным швом. Выполнена полная мобилизация опухоли. Визуализирована нижняя полая вена (НПВ) ниже и выше печени, взята на держалки; гепатодуоденальная связка взята на держалки. Выполнена проба с полным пережатием связки и НПВ - толерантность к пережатию удовлетворительная. НПВ в над- и подпеченочных сегментах, гепатодуоденальная связка пережаты сосудистыми отщепами, выполнена правосторонняя расширенная гемигепатэктомия с прошиванием плоскости резекции ленточным викрилом. Препарат опухоли удален (рис.3, внешний вид удаленной опухоли). Ушиты щелевидные дефекты в НПВ, зажимы сняты. Беспеченочный период 15 минут. Гемостаз. Через культю пузырного протока установлен Т-образный дренаж в холедох. На мышечную часть перерастянутого правого купола диафрагмы, вдоль линии прикрепления его к грудной клетке, по всей полуокружности с отступом от этой линии на 4 см внутрь наложены гофрирующие швы (рис.4, схематическое изображение линии швов на мышечной части диафрагмы) с формированием дупликатуры диафрагмы (рис.5, этап наложения гофрирующих швов на мышечную часть правого купола диафрагмы). Выполнена нефропексия с фиксацией правой почки в правой поясничной области. Произведено перемещение оставшейся части печени в правое поддиафрагмальное пространство путем ротации ее вправо вокруг оси, образованной нижней полой веной, на угол в 60° относительно сагиттальной плоскости и фиксацией печени в таком положении путем сшивания ранее пересеченных круглой и серповидной связок печени с правым куполом диафрагмы (рис.6). Через отдельные разрезы брюшной стенки установлены три дренажа: в правое поддиафрагмальное пространство, к винслову отверстию, в малый таз. Контроль гемостаза - сухо. Счет салфеток и инструментов верен. Послойный шов раны петлей. Асептическая наклейка. После перевода пациентки в палату интенсивной терапии дренажи соединены с системой активной вакуум-аспирации.
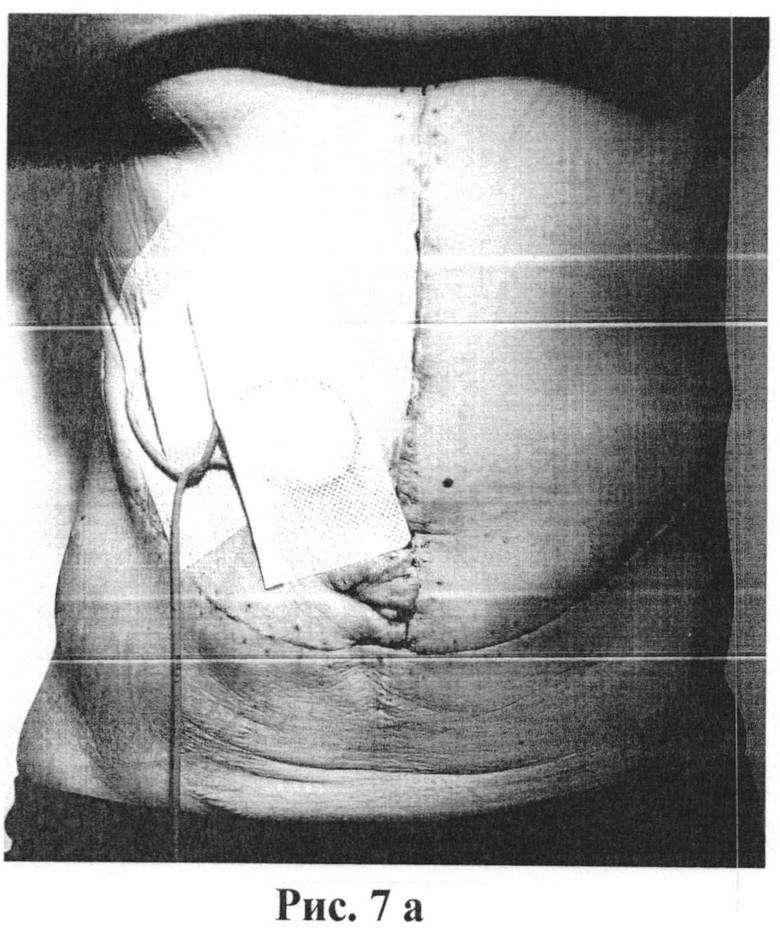
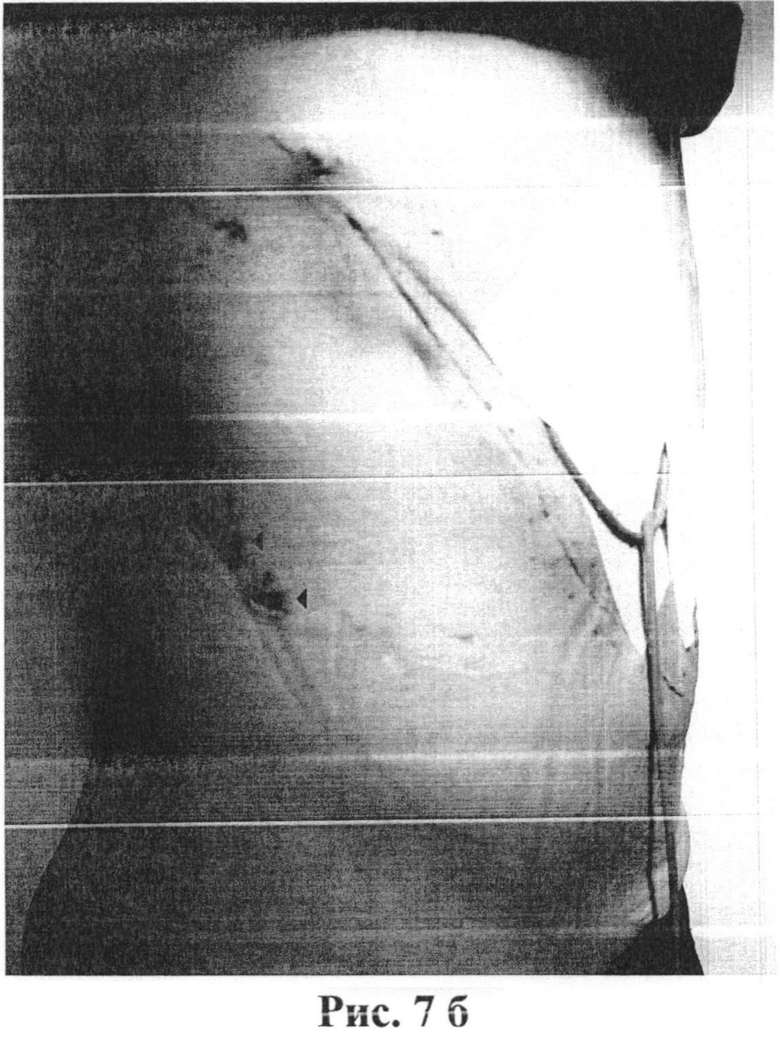
Послеоперационный период протекал без осложнений. Силиконовый дренаж из полости малого таза удален через двое суток, оставшиеся дренажи из-под правого поддиафрагмального пространства удалены на 10-е сутки. Заживление послеоперационной раны - первичным натяжением. Пациентка выписана через три недели после операции. Общий вид живота перед выпиской представлен на рис.7а, б (стрелки указывают места ранее стоявших дренажей).
Через год после операции пациентке проведено контрольное обследование. Признаков рецидива опухоли не выявлено. При многослойной спиральной компьютерной томографии определялась гипертрофия оставшихся отделов печени. При этом остаток левой половины печени сохранил свое расположение под правым куполом диафрагмы с ротацией вправо на угол в 60° относительно сагиттальной плоскости вокруг оси, образованной нижней полой веной (рис.8, вершина угла совпадает с центром поперечного сечения нижней полой вены, стрелками отмечена линия фиксирующих швов между круглой и серповидной связок, с одной стороны, и куполом диафрагмы - с другой).
ПРИМЕР 2. Пациентка Р., 1963 г.р. (№ истории 705), проживающая в Санкт-Петербурге, была госпитализирована в клинику ФГУ ЦНИРРИ Росздрава 23.11.2006 г. с диагнозом: Гигантская кавернозная гемангиома правой половины печени. Желчнокаменная болезнь, хронический калькулезный холецистит.
При поступлении беспокоили ощущения распирания и эпизодические кратковременные тупые боли в правом подреберье, которые провоцировались физическими нагрузками.
Считала себя больной с февраля 2006 года, когда при профилактическом обследовании отмечено отклонение биохимических показателей крови от нормальных значений, свидетельствующих о печеночной дисфункции. При ультразвуковом исследовании была выявлена опухоль печени, занимающая всю правую ее половину.
Для уточнения характера опухоли, распространенности поражения печени и определения тактики лечения выполнена многослойная спиральная компьютерная томография с болюсным конрастированием. Полученные данные свидетельствовали о принадлежности выявленной опухоли к гигантской кавернозной гемангиоме, которая занимала правую половину печени и распространялась на I сегм. печени, сдавливая и смещая нижнюю полую вену влево, а правую почку книзу. Программная 3D-реконструкция полученных изображений позволила установить распространенность гемангиомы на гилусные ворота печени (полюс опухоли прилежал к стенке левой ветви воротной вены) и вариант артериального кровоснабжения органа. Правая половина печени с гемангиомой кровоснабжалась правой печеночной артерией, являвшейся продолжением собственной печеночной артерии, а левая печеночная артерия отходила от чревного ствола. Опухоль распространялась на кавальные ворота печени и по верхнемедиальному контуру соприкасалась со стволом средней печеночной вены.
30.11.2006 г. была выполнена операция. Под эндотрахеальным наркозом произведена лапаротомия по Starzl, правосторонняя расширенная гемигепатэктомия, холецистэктомия, наружное дренирование холедоха по Пиковскому, дренирование брюшной полости (продолжительность операции 5 ч 30 мин, кровопотеря 1500 мл).
При ревизии брюшной полости выявлено, что из правой доли печени, практически, замещая весь ее объем, исходила большая кавернозная гемангиома диаметром до 20 см. Большая часть гемангиомы располагалась в забрюшинном пространстве, оттесняя «остатки» правой доли печени кпереди. Оставшаяся часть паренхимы правой доли атрофична, в виде «плаща» прикрывала узел гемангиомы спереди. Заднемедиальный контур гемангиомы смещал ретропеченочный отдел нижней полой вены и I сегмент влево. При этом ткань опухоли муфтообразно охватывала нижнюю полую вену по ее правой полуокружности и отодвигала книзу правую почку. Медиальный полюс опухоли достигал гилусных ворот печени. На небольшом протяжении капсула опухоли прилежала к стенке левой ветви воротной вены. Левая половина печени значительно гипертрофирована. В желчном пузыре определялся одиночный конкремент.
Произведена перевязка и пересечение пузырной артерии. Пузырный проток перевязан со стороны шейки желчного пузыря и пересечен. Выполнено наружное дренирование холедоха через культю пузырного протока по Пиковскому. В гилусных воротах печени идентифицирована, перевязана и пересечена правая печеночная артерия. Желчные протоки (от секторов печени) сливаются в общий печеночный проток по типу тетрафуркации. Идентифицированы оба желчных протока от правых медиального и латерального секторов, перевязаны и пересечены. Правая ветвь воротной вены диаметром до 10 мм проходима, сдавлена и оттеснена книзу нижним полюсом гемангиомы. Левая ветвь воротной вены расширена до 15-17 мм. Произведена перевязка и пересечение правой ветви воротной вены. После перевязки афферентных сосудов к правой доле печени отмечено уменьшение объема гемангиомы на треть, снижение напряжения капсулы опухоли. Благодаря этому удалось выполнить мобилизацию правой доли печени с пересечением ее связок. Продвигаясь вдоль капсулы гемангиомы, последняя отделена от верхнего полюса и сосудистой ножки правой почки, правого надпочечника, переднебоковых стенок ретропеченочного отдела нижней полой вены. При этом перевязаны, прошиты и пересечены короткие и правая печеночные вены.
По линии демаркации выполнено разделение паренхимы печени с использованием водоструйного диссектора и перевязкой, клипированием и пересечением сосудисто-секреторных трубчатых структур вдоль плоскости резекции. Правая половина печени с гемангиомой и желчным пузырем удалена. Окончательный гемостаз на раневой поверхности печени достигнут с использованием прошивных лигатур и аргоноплазменного коагулятора. Герметичность желчных протоков проверена гидравлической пробой. С целью уменьшения «остаточной» полости, образовавшейся после удаления гигантской гемангиомы правой половины печени, на мышечную часть перерастянутого правого купола диафрагмы, вдоль линии прикрепления его к грудной клетке, по всей полуокружности с отступом от этой линии на 3 см внутрь наложены гофрирующие швы. Произведено перемещение оставшейся части печени в правое поддиафрагмальное пространство путем ротации ее вправо вокруг оси, образованной нижней полой веной, на угол в 45° относительно сагиттальной плоскости и фиксацией печени в таком положении путем сшивания ранее пересеченных круглой и серповидной связок печени с правым куполом диафрагмы. Дренированы правое поддиафрагмальное и подпеченочное пространства двумя силиконовыми трубками, выведенными наружу через дополнительные разрезы передней брюшной стенки. Контроль гемостаза. Счет инструментов и материала. Послойный шов операционной раны. Асептическая повязка. После перевода пациентки в палату интенсивной терапии дренажи соединены с системой активной вакуум-аспирации.
Операция выполнялась с использованием аппарата реинфузии крови. В послеоперационном периоде выполнялась однократная пункция правой плевральной полости с удалением 550 мл реактивного выпота. Оба дренажа из брюшной полости последовательно удалены на 5 и 6 сутки от момента выполнения операции. Заживление послеоперационной раны - первичным натяжением. Пациентка была выписана в удовлетворительном состоянии на амбулаторное лечение через 2 недели после операции.
Через пять лет проведено контрольное обследование пациентки. Каких-либо функциональных отклонений со стороны печени и признаков рецидива заболевания не было выявлено.
К настоящему времени предлагаемым способом за период с 2006 г. были прооперированы 10 пациентов с гигантскими новообразованиями правой половины печени (гемангиомы - 4, кисты - 2, альвеококкоз - 2, первичный рак печени - 1, эмбриональная саркома - 1). Все пациенты были выписаны из клиники в сроки от 14 до 20 суток после операции. При этом продолжительность дренирования брюшной полости варьировало от 7 до 10 суток. Ни у одного из пациетов не было отмечено гнойных и легочных осложнений, обусловленных неполной инволюцией остаточной полости после удаления гигантских новообразований правой половины печени или ателектазами нижней доли правого легкого.
Предлагаемый способ по сравнению с известными имеет ряд существенных преимуществ.
1. Позволяет одномоментно значительно уменьшить остаточную полость после удаления гигантского новообразования, что не обеспечивает ни один из известных нам способов. 2. Обеспечивает уменьшение пролабирования купола диафрагмы, расправление нижней доли правого легкого и устранение ее ателектаза непосредственно во время операции. И в послеоперационном периоде отмечено снижение частоты легочных осложнений, увеличение дыхательного объема и жизненной емкости легких.
3. Не увеличивает срок пребывания больного в клинике сверх того, который необходим для долечивания его после оперативного вмешательства.
4. Позволяет уменьшить количество используемых дренажей (не более трех) для удаления и сбора раневого отделяемого (кровь, желчь, серозная жидкость) при тех же средних сроках их использования.
Способ разработан в отделе интервенционной радиологии и оперативной хирургии РНЦ РХТ и прошел клиническую апробацию у 10 больных с положительным результатом.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОРГАНОСОХРАНЯЮЩЕЙ РОБОТ-АССИСТИРОВАННОЙ ИНТРАКОРПОРАЛЬНОЙ РЕЗЕКЦИИ ПОЧКИ С ПРИМЕНЕНИЕМ ИЗОЛИРОВАННОЙ ФАРМАКО-ХОЛОДОВОЙ ИШЕМИИ КАРДИОПЛЕГИЧЕСКИМ РАСТВОРОМ | 2023 |
|
RU2812295C1 |
| Способ интраоперационной визуализации объемных образований печени | 2024 |
|
RU2833520C1 |
| СПОСОБ УСТАНОВКИ ДРЕНАЖЕЙ ПРИ ПАНКРЕАТОДУОДЕНАЛЬНОЙ РЕЗЕКЦИИ | 2022 |
|
RU2789210C1 |
| РАНОРАСШИРИТЕЛЬ | 1990 |
|
RU2006210C1 |
| СПОСОБ ЛЕЧЕНИЯ ПЕРИТОНИТА | 1996 |
|
RU2147444C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ГИЛЮСНОЙ ХОЛАНГИОКАРЦИНОМЫ ПЕЧЕНИ | 2006 |
|
RU2314044C1 |
| Способ рентгенэндоваскулярной эмболизации висцеральных ветвей через артерии верхних конечностей при помощи катетера Headhunter при различных патологиях желудочно-кишечного тракта | 2016 |
|
RU2652743C1 |
| Способ бескровной резекции селезенки | 2018 |
|
RU2675355C1 |
| Способ органосохраняющего минимально инвазивного лечения кист печени и селезенки | 2020 |
|
RU2738044C1 |
| Способ лапароскопической левосторонней латеральной секторэктомии печени | 2016 |
|
RU2628056C1 |





Изобретение относится к медицине, а именно к хирургии, и может быть использовано при лечении новообразований печени. После удаления гигантского новообразования на мышечную часть диафрагмы по всей ее полуокружности накладывают гофрирующие швы вдоль линии прикрепления диафрагмы к грудной клетке с отступом от этой линии внутрь на 3-4 см. Пересекают круглую и серповидную связки. Левую половину печени ротируют вправо относительно оси, образованной нижней полой веной, на угол в 45-60° относительно сагиттальной плоскости. Печень фиксируют наложением швов между пересеченными круглой и серповидной связками, с одной стороны, и правым куполом диафрагмы - с другой. Дренирование поддиафрагмального пространства осуществляют силиконовыми трубками в количестве не более трех с активной вакуум-аспирацией. Способ позволяет уменьшить остаточную полость после удаления гигантского новообразования за счет гофрирования мышечной части диафрагмы и ротации левой половины печени вправо, снизить частоту легочных осложнений, увеличить дыхательный объем и жизненную емкость легких за счет пролабирования купола диафрагмы, расправления нижней доли правого легкого и устранения ее ателектаза непосредственно во время операции, а также избежать формирования резидуальной полости и сократить сроки пребывания пациента в стационаре за счет дренирования поддиафрагмального пространства силиконовыми трубками в количестве не более трех с активной вакуум-аспирацией. 8 ил., 2 пр.
Способ профилактики осложнений после резекции печени при гигантских новообразованиях ее правой половины, включающий дренирование с активной вакуум-аспирацией полости, оставшейся после больших и предельно больших резекций печени, отличающийся тем, что непосредственно после удаления гигантского новообразования на мышечную часть диафрагмы по всей ее полуокружности накладывают гофрирующие швы вдоль линии прикрепления диафрагмы к грудной клетке с отступом от этой линии внутрь на 3-4 см, затем пересекают круглую и серповидную связки и левую половину печени ротируют вправо относительно оси, образованной нижней полой веной, на угол в 45-60° относительно сагиттальной плоскости, после чего печень фиксируют наложением швов между пересеченными круглой и серповидной связками, с одной стороны, и правым куполом диафрагмы - с другой, а дренирование поддиафрагмального пространства осуществляют силиконовыми трубками в количестве не более трех.
| ЖУРАВЛЕВ В | |||
| А | |||
| Большие и предельно большие резекции печени | |||
| Саратов : Изд-во Саратовского мед | |||
| Пневматический водоподъемный аппарат-двигатель | 1917 |
|
SU1986A1 |
| СПОСОБ КОРРЕКЦИИ ОСТАТОЧНОЙ ПОЛОСТИ ПРИ ЭХИНОКОККЭКТОМИИ ПЕЧЕНИ У ВЗРОСЛЫХ | 1998 |
|
RU2177743C2 |
| Горный компас | 1945 |
|
SU69969A1 |
| ГРИГОРЯН Р.А | |||
| Абдоминальная хирургия | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| М | |||
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| SHAN JIN | |||
| Management of post-hepatectomy complications | |||
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
Авторы
Даты
2014-11-27—Публикация
2014-01-15—Подача