Изобретение относится к способу получения новых азотсодержащих гетероциклических соединений, а именно 1-гидрокси-3-R-индол-5,6-дикарбонитрилов, которые могут быть использованы в качестве прекурсоров для синтеза биологически активных веществ, для синтеза фталоцианинов, гексазоцикланов.
Данные соединения являются новыми, и из уровня техники нам не известны способы получения таких соединений.
Задачей изобретения является разработка способа получения 1-гидрокси-3-R-индол-5,6-дикарбонитрилов структурной формулы:
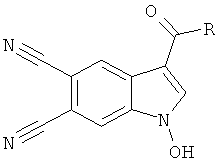
где R=С6Н5 или 4-СН3С6Н4, или 4-ОСН3С6Н4, или 2-тиенил.
Поставленная задача достигается тем, что способ синтеза 1-гидрокси-3-R-индол-5,6-дикарбонитрилов включает две стадии. На первой стадии при взаимодействии замещенных 4-нитро-5-(2-оксоэтил)фталонитрилов, полученных по патенту RU 2443681 С2, опуб. 27.02.2012, и хлорокиси фосфора POCl3 происходит образование соответствующих 4-замещенных 5-нитрофталонитрилов. На второй стадии 4-замещенные 5-нитрофтало-нитрилы восстанавливают двухлористым оловом с получением 1-гидрокси-3-R-индол-5,6-дикарбонитрилов.
Вышеуказанные соединения получают следующей реакцией:
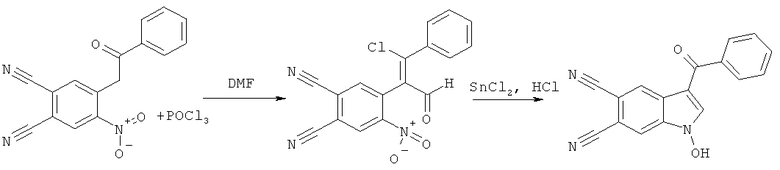 ,
,
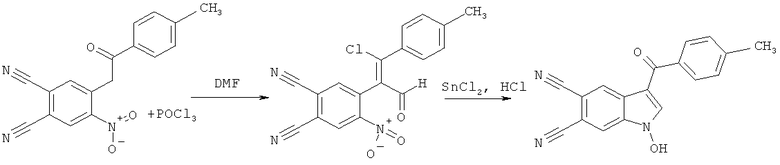 ,
,
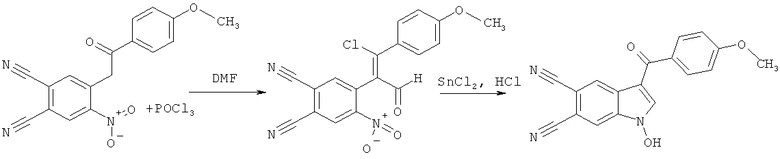 ,
,
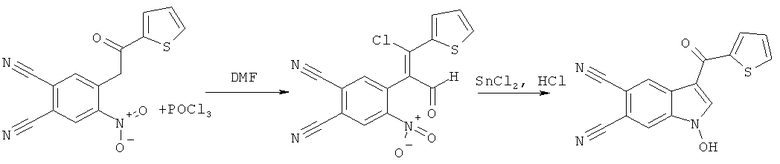
при условиях, описанных ниже.
На первой стадии взаимодействие реагентов протекает при температуре 90…110°C и мольном соотношении 1:2-3, соответственно, в течение 2.5-5 часов в растворе ДМФА. Полученную реакционную массу охлаждают, выливают в холодный 5…20-ый % раствор гидрокарбоната натрия. Выпавший кристаллический осадок 4-замещенного 5-нитрофталонитрила отфильтровывают и перекристаллизовывают из спирта. Сушат на воздухе. На второй стадии к раствору двухлористого олова в концентрированной соляной кислоте при температуре 30…50°C при интенсивном перемешивании прибавляют раствор полученного 4-замещенного 5-нитрофталонитрила в этиловом спирте при мольном соотношении 2.8-4.5:1, соответственно, и времени реакции 1-2 часа. Выпавший осадок 1-гидрокси-3-R-индол-5,6-дикарбонитрилов отфильтровывают и перекристаллизовывают из спирта. Сушат на воздухе.
Все приведенные отличительные признаки являются существенными, и только заявляемая совокупность признаков позволяет достичь технического результата.
Строение всех синтезированных соединений определено на основании совокупности данных ИК-, ЯМР-спектроскопий и масс-спектрометрии.
Изобретение иллюстрируется следующими примерами.
Пример 1. 3-бензоил-1-гидрокси-1H-индол-5,6-дикарбонитрил:
К раствору 0.018 моль POCl3 в 3 мл ДМФА прибавляют 0.006 моль 4-нитро-5-(2-оксо-2-фенилэтил)фталонитрила, перемешивают при температуре 100°C в течение 4 часов, затем реакционную массу охлаждают, выливают в холодный 10%-ый раствор гидрокарбоната натрия. Выпавший кристаллический осадок отфильтровывают, тщательно промывают водой и перекристаллизовывают из спирта. Сушат на воздухе. Далее к раствору 0.01 моль двухлористого олова в 2 мл концентрированной соляной кислоты прибавляют раствор 0.003 моль 4-[(E)-2-хлор-1-формил-2-фенилвинил]-5-нитрофталонитрила в 2 мл спирта и перемешивают при температуре 40°C в течение полутора часов. Полученную реакционную массу охлаждают, а образовавшийся осадок 1-гидрокси-3R-индол-5,6-дикарбонитрила отфильтровывают и перекристаллизовывают из спирта. Получают 0.46 г (53% от теории) 3-бензоил-1-гидрокси-1H-индол-5,6-дикарбонитрила - аморфный осадок бледно-желтого цвета, Тпл.=205-206°C.
Пример 2. 1-гидрокси-3-(4-метилбензоил)-1H-индол-5,6-дикарбо-нитрил:
К раствору 0.018 моль POCl3 в 3 мл ДМФА прибавляют 0.006 моль 4-[2-(4-метилфенил)-2-оксоэтил]-5-нитрофталонитрила, перемешивают при температуре 105°C в течение 3.5 часов, затем реакционную массу охлаждают, выливают в холодный 15%-ый раствор гидрокарбоната натрия. Выпавший кристаллический осадок отфильтровывают, тщательно промывают водой и перекристаллизовывают из спирта. Сушат на воздухе. Далее к раствору 0.01 моль двухлористого олова в 2 мл концентрированной соляной кислоты прибавляют раствор 0.003 моль 4-[(E)-2-хлор-1-формил-2-(4-метилфенил)винил]-5-нитрофталонитрила в 2 мл спирта и перемешивают при температуре 45°C в течение 2 часов. Полученную реакционную массу охлаждают, а образовавшийся осадок 1-гидрокси-3-R-индол-5,6-дикарбонитрила отфильтровывают и перекристаллизовывают из спирта. Получают 0.72 г (80% от теории) 1-гидрокси-3-(4-метилбензоил)-1H-индол-5,6-дикарбонитрила - аморфный осадок бледно-желтого цвета, Тпл.=272-273°C.
Пример 3. 1-гидрокси-3-(4-метоксибензоил)-1H-индол-5,6-дикарбо-нитрил:
К раствору 0.018 моль POCl3 в 3 мл ДМФА прибавляют 0.006 моль 4-[2-(4-метоксифенил)-2-оксоэтил]-5-нитрофталонитрила, перемешивают при температуре 110°C в течение 5 часов, затем реакционную массу охлаждают, выливают в холодный 20%-ый раствор гидрокарбоната натрия. Выпавший кристаллический осадок отфильтровывают, тщательно промывают водой и перекристаллизовывают из спирта. Сушат на воздухе. Далее к раствору 0.01 моль двухлористого олова в 2 мл концентрированной соляной кислоты прибавляют раствор 0.003 моль 4-[(E)-2-хлор-1-формил-2-(4-метоксифенил)винил]-5-нитрофталонитрила в 2 мл спирта и перемешивают при температуре 50°C в течение 2 часов. Полученную реакционную массу охлаждают, а образовавшийся осадок 1-гидрокси-3-R-индол-5,6-дикарбонитрила отфильтровывают и перекристаллизовывают из спирта. Получают 0.68 г (71% от теории) 1-гидрокси-3-(4-метоксибензоил)-1H-индол-5,6-дикарбонитрила - аморфный осадок бледно-желтого цвета, Тпл.=291-293°C.
Пример 4. 1-гидрокси-3-(3-тиенилкарбонил)-1H-индол-5,6-дикарбо-нитрил:
К раствору 0.018 моль POCl3 в 3 мл ДМФА прибавляют 0.006 моль 4-нитро-5-[2-оксо-2-(3-тиенил)этенил]фталонитрила, перемешивают при температуре 90°C в течение 2.5 часов, затем реакционную массу охлаждают, выливают в холодный 5%-ый раствор гидрокарбоната натрия. Выпавший кристаллический осадок отфильтровывают, тщательно промывают водой и перекристаллизовывают из спирта. Сушат на воздухе. Далее к раствору 0.01 моль двухлористого олова в 2 мл концентрированной соляной кислоты прибавляют раствор 0.003 моль 4-[(E)-2-хлор-1-формил-2-тиофен-2-илэтенил]-5-нитро-фталонитрила в 2 мл спирта и перемешивают при температуре 30°C в течение 1 часа. Полученную реакционную массу охлаждают, а образовавшийся осадок 1-гидрокси-3-R-индол-5,6-дикарбонитрила отфильтровывают и перекристаллизовывают из спирта. Получают 0.42 г (48% от теории) 1-гидрокси-3-(4-метоксибензоил)-1H-индол-5,6-дикарбонитрила - аморфный осадок бледно-желтого цвета, Тпл.=234-235°C.
Физико-химические характеристики 1-гидрокси-3-R-индол-5,6-дикарбонитрилов приведены в Таблице 1.
Техническим результатом изобретения является получение новых химических соединений достаточной степени чистоты, которые могут быть использованы в качестве прекурсоров для синтеза биологически активных веществ, для синтеза фталоцианинов, гексазоцикланов.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 2,3-дизамещенных 1-гидрокси-1H-индол-5,6-дикарбонитрилов | 2017 |
|
RU2641006C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ 4-ГИДРОКСИ-3-ОКСО-3,4-ДИГИДРО-2Н-1,4-БЕНЗОКСАЗИН-6,7-ДИКАРБОНИТРИЛОВ НА ОСНОВЕ 4-БРОМ-5-НИТРОФТАЛОНИТРИЛА | 2009 |
|
RU2425047C9 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ БЕНЗОФУРАН-5,6-ДИКАРБОНИТРИЛОВ | 2009 |
|
RU2429235C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ 3-ФОРМИЛИНДОЛ-5,6-ДИКАРБОНИТРИЛОВ | 2014 |
|
RU2570202C1 |
| Способ получения 2-замещенных 1-гидроксипирроло[3,4-f]индол-5,7-(1Н,6Н)-дионов | 2015 |
|
RU2613582C1 |
| Способ получения 2-замещенных 1-гидрокси-1Н-индол-5,6-дикарбоновых кислот | 2015 |
|
RU2613559C1 |
| Способ получения 3-ацилзамещенных 2-арил(гетерил)-1Н-индол-5,6-дикарбонитрилов | 2017 |
|
RU2640351C1 |
| СПОСОБ ПОЛУЧЕНИЯ 3-ЗАМЕЩЕННЫХ 1,2-БЕНЗИЗОКСАЗОЛ-5,6-ДИКАРБОНИТРИЛОВ | 2010 |
|
RU2446164C2 |
| СПОСОБ ПОЛУЧЕНИЯ 4-ГИДРОКСИ-5-(R-1H-ПИРАЗОЛ)-БЕНЗОЛ-1,2-ДИКАРБОНИТРИЛОВ | 2014 |
|
RU2557058C1 |
| СПОСОБ ПОЛУЧЕНИЯ 3-ЗАМЕЩЕННЫХ 2-АМИНО-1-ГИДРОКСИ-5,6-ДИЦИАНОИНДОЛОВ НА ОСНОВЕ 4-БРОМ-5-НИТРОФТАЛОНИТРИЛА | 2009 |
|
RU2425031C1 |
Изобретение относится к способу получения 1-гидрокси-3-R-индол-5,6-дикарбонитрилов структурной формулы:
 , где R=С6Н5 или 4-СН3С6Н4, или 4-ОСН3С6Н4, или 2-тиенил, который включает две стадии, при этом на первой стадии замещенные 4-нитро-5-(2-оксоэтил)фталонитрилы реагируют с хлорокисью фосфора POCl3, взаимодействие указанных реагентов протекает при температуре 90…110°C и мольном соотношении 1:2-3, соответственно, в течение 2.5-5 часов в растворе ДМФА, затем реакционную массу охлаждают, выливают в холодный 5…40-ный % раствор гидрокарбоната натрия, далее выпавший кристаллический осадок отфильтровывают и перекристаллизовывают из спирта, сушат на воздухе, а на второй стадии к раствору двухлористого олова в концентрированной соляной кислоте при температуре 30…50°C при интенсивном перемешивании прибавляют раствор полученного 4-замещенного 5-нитрофталонитрила в этиловом спирте при мольном соотношение 2.8-4.5:1, соответственно, и времени реакции 1-2 часа, полученную реакционную массу охлаждают, образовавшийся осадок 1-гидрокси-3-R-индол-5,6-дикарбонитрилов отфильтровывают и перекристаллизовывают из спирта, сушат на воздухе. Технический результат: разработан способ получения индол-дикарбонитрилов, которые могут быть использованы в качестве прекурсоров для синтеза биологически активных веществ, для синтеза фталоцианинов, гексазоцикланов. 1 табл. 4 пр.
, где R=С6Н5 или 4-СН3С6Н4, или 4-ОСН3С6Н4, или 2-тиенил, который включает две стадии, при этом на первой стадии замещенные 4-нитро-5-(2-оксоэтил)фталонитрилы реагируют с хлорокисью фосфора POCl3, взаимодействие указанных реагентов протекает при температуре 90…110°C и мольном соотношении 1:2-3, соответственно, в течение 2.5-5 часов в растворе ДМФА, затем реакционную массу охлаждают, выливают в холодный 5…40-ный % раствор гидрокарбоната натрия, далее выпавший кристаллический осадок отфильтровывают и перекристаллизовывают из спирта, сушат на воздухе, а на второй стадии к раствору двухлористого олова в концентрированной соляной кислоте при температуре 30…50°C при интенсивном перемешивании прибавляют раствор полученного 4-замещенного 5-нитрофталонитрила в этиловом спирте при мольном соотношение 2.8-4.5:1, соответственно, и времени реакции 1-2 часа, полученную реакционную массу охлаждают, образовавшийся осадок 1-гидрокси-3-R-индол-5,6-дикарбонитрилов отфильтровывают и перекристаллизовывают из спирта, сушат на воздухе. Технический результат: разработан способ получения индол-дикарбонитрилов, которые могут быть использованы в качестве прекурсоров для синтеза биологически активных веществ, для синтеза фталоцианинов, гексазоцикланов. 1 табл. 4 пр.
Способ получения 1-гидрокси-3-R-индол-5,6-дикарбонитрилов общей формулы:

где R=C6H5 или 4-CH3C6H4, или 4-OCH3C6H4, или 2-тиенил,
заключающийся в том, что метод синтеза включает две стадии, при этом на первой стадии замещенные 4-нитро-5-(2-оксоэтил)фталонитрилы реагируют с хлорокисью фосфора POCl3, взаимодействие указанных реагентов протекает при температуре 90…110°C и мольном соотношении 1:2-3, соответственно, в течение 2.5-5 часов в растворе ДМФА, затем реакционную массу охлаждают, выливают в холодный 5…40-ный % раствор гидрокарбоната натрия, далее выпавший кристаллический осадок отфильтровывают и перекристаллизовывают из спирта, сушат на воздухе, а на второй стадии к раствору двухлористого олова в концентрированной соляной кислоте при температуре 30…50°C при интенсивном перемешивании прибавляют раствор полученного 4-замещенного 5-нитрофталонитрила в этиловом спирте при мольном соотношении 2.8-4.5:1, соответственно, и времени реакции 1-2 часа, полученную реакционную массу охлаждают, образовавшийся осадок 1-гидрокси-3-R-индол-5,6-дикарбонитрилов отфильтровывают и перекристаллизовывают из спирта, сушат на воздухе.
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
| СПОСОБ ПОЛУЧЕНИЯ 3-ЗАМЕЩЕННЫХ 2-АМИНО-1-ГИДРОКСИ-5,6-ДИЦИАНОИНДОЛОВ НА ОСНОВЕ 4-БРОМ-5-НИТРОФТАЛОНИТРИЛА | 2009 |
|
RU2425031C1 |
Авторы
Даты
2014-12-10—Публикация
2013-07-19—Подача