В настоящей заявке заявляется приоритет предварительной заявки на патент США № 61/145611, поданной 19 января 2009 года, которая во всей своей полноте включена в данное описание посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к соединениям, которые ингибируют активность антиапоптотических белков Bcl-2, к композициям, содержащим указанные соединения, и к способам лечения заболеваний, при которых экспрессируются антиапоптотические белки Bcl-2.
ПРЕДПОСЫЛКИ К СОЗДАНИЮ ИЗОБРЕТЕНИЯ
Антиапоптотические белки Bcl-2 связаны с рядом заболеваний. Поэтому в области терапии существует потребность в соединениях, которые ингибируют активность антиапоптотических белков Bcl-2.
Сверхэкспрессия белков Bcl-2 коррелирует со стойкостью к химиотерапии, с клиническими результатами, с развитием заболевания, с общим прогнозом дальнейшего течения болезни или с их сочетанием при различных видах рака и заболеваниях иммунной системы.
Вовлечение белков Bcl-2 в развитие рака мочевого пузыря, рака мозга, рака молочной железы, рака костного мозга, рака шейной области, хронического лимфолейкоза, колоректального рака, рака пищевода, гепатоцеллюлярного рака, лимфобластного лейкоза, фолликулярной лимфомы, лимфолейкоза, вызываемого Т-лимфоцитами или В-клетками, меланомы, миелогенного лейкоза, миеломы, рака полости рта, рака яичников, немелкоклеточного рака легкого или рака простаты, мелкоклеточного рака легкого, рака селезенки и т.п. описано в одновременно находящейся на рассмотрении международной заявке PCT US 2004/36770, опубликованной как WO 2005/049593, и международной заявке PCT US 2004/37911, опубликованной как WO 2005/024636.
Вовлечение белков Bcl-2 в иммунные и аутоиммунные заболевания описано в Current Allergy and Asthma Reports 2003, 3, 378-384; British Journal of Haematology 2000, 110(3), 584-90; Blood 2000, 95(4), 1283-92; и New England Journal of Medicine 2004, 351(14), 1409-1418. Вовлечение белков Bcl-2 в развитие артрита раскрыто в находящейся на рассмотрении предварительной заявке на патент США № 60/988479. Вовлечение белков Bcl-2 в отторжение трансплантата костного мозга раскрыто в находящейся на рассмотрении заявке на патент США № 11/941196.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Таким образом, один вариант осуществления настоящего изобретения касается соединений или их терапевтически приемлемых солей, пролекарств, метаболитов или солей пролекарств указанных соединений, которые пригодны в качестве ингибиторов антиапоптотических белков Bcl-2, при этом указанные соединения имеют формулу I

где
A1 представляет собой фурил, имидазолил, изотиазолил, изоксазолил, оксадиазолил, оксазолил, пиразинил, пиразолил, пиридазинил, 2-пиридинил, 4-пиридинил, пиримидинил, пирролил, тетразолил, тиазолил, тиадиазолил, тиенил, триазинил, триазолил, циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил; каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или A1A; A1A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
где A1 не замещен или замещен одним, или двумя, или тремя, или четырьмя, или пятью независимо выбранными заместителями R1, OR1, SR1, S(O)R1, SO2R1, C(O)R1, C(O)OR1, OC(O)R1, NHR1, N(R1)2, C(N)C(O)R1, C(O)NHR1, C(O)N(R1)2, C(O)NHOH, C(O)NHOR1, C(O)NHSO2R1, NHC(O)R1, NR1C(O)R1, NHC(O)OR1, NR1C(O)OR1, NR1C(O)NHR1, NR1C(O)N(R1)2, NHC(O)NH2, NHC(O)NHR1, NHC(O)N(R1)2, SO2NH2, SO2NHR1, SO2N(R1)2, NHS(O)R1, NHSO2R1, NR1SO2R1, NHSO2NHR1, N(CH3)SO2N(CH3)R1, (O), NH2, NO2, N3, OH, F, Cl, Br, I, CN, CF3, OCF3, CF2CF3, OCF2CF3, C(O)H, C(O)OH, C(N)NH2, C(N)NHR1, C(N)N(R1)2, CNOH, CNOCH3, C(O)NH2 или C(O)OR1A;
R1 представляет собой R2, R3, R4 или R5;
R1A представляет собой циклоалкил, циклоалкенил или циклоалкинил;
R2 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R2A; R2A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R3 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R3A; R3A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R4 представляет собой циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R4A; R4A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R5 представляет собой алкил, алкенил или алкинил, каждый из которых не замещен или замещен одним, или двумя, или тремя независимо выбранными заместителями R6, NC(R6A)(R6B), R7, OR7, SR7, S(O)R7, SO2R7, NHR7, N(R7)2, C(O)R7, C(O)NH2, C(O)NHR7, C(O)N(R7)2, NHC(O)R7, NR7C(O)R7, NHSO2R7, NHC(O)OR7, SO2NH2, SO2NHR7, SO2N(R7)2, NHC(O)NH2, NHC(O)NHR7, NHC(O)CH(CH3)NHC(O)CH(CH3)NH2, NHC(O)CH(CH3)NHC(O)CH(CH3)NHR1, OH, (O), C(O)OH, N3, CN, NH2, CF3, CF2CF3, F, Cl, Br или I;
R6 представляет собой C2-C5-спироалкил, каждый из которых не замещен или замещен заместителями OH, (O), N3, CN, CF3, CF2CF3, F, Cl, Br, I, NH2, NH(CH3) или N(CH3)2;
R6A и R6B независимо выбраны из алкила или вместе с атомом N, к которому они присоединены, образуют R6C;
R6C представляет собой азиридин-1-ил, азетидин-1-ил, пирролидин-1-ил или пиперидин-1-ил, каждый из которых имеет один фрагмент CH2, не замененный или замененный O, C(O), CNOH, CNOCH3, S, S(O), SO2 или NH;
R7 представляет собой R8, R9, R10 или R11;
R8 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R8A; R8A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R9 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R9A; R9A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R10 представляет собой циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R10A; R10A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R11 представляет собой алкил, алкенил или алкинил, каждый из которых не замещен или замещен одним, или двумя, или тремя независимо выбранными заместителями R12, OR12, SR12, S(O)R12, SO2R12, C(O)R12, C(O)OR12, OC(O)R12, OC(O)OR12, NH2, NHR12, N(R12)2, NHC(O)R12, NR12C(O)R12, NHS(O)2R12, NR12S(O)2R12, NHC(O)OR12, NR12C(O)OR12, NHC(O)NH2, NHC(O)NHR12, NHC(O)N(R12)2, NR12C(O)NHR12, NR12C(O)N(R12)2, C(O)NH2, C(O)NHR12, C(O)N(R12)2, C(O)NHOH, C(O)NHOR12, C(O)NHSO2R12, C(O)NR12SO2R12, SO2NH2, SO2NHR12, SO2N(R12)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR12, C(N)N(R12)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R12 представляет собой R13, R14, R15 или R16;
R13 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R13A; R13A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R14 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R14A; R14A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R15 представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R15A; R15A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R16 представляет собой алкил, алкенил или алкинил;
Z1 представляет собой R26 или R27;
Z2 представляет собой R28, R29 или R30;
Z1A и Z2A, оба, отсутствуют или вместе образуют CH2, CH2CH2 или Z12A;
Z12A представляет собой C2-C6-алкен, в котором один или два фрагмента CH2 заменены NH, N(CH3), S, S(O) или SO2;
L1 представляет собой R37, OR37, SR37, S(O)R37, SO2R37, C(O)R37, C(O)OR37, OC(O)R37, OC(O)OR37, NHR37, C(O)NH, C(O)NR37, C(O)NHOR37, C(O)NHSO2R37, SO2NH, SO2NHR37, C(N)NH, C(N)NHR37;
R26 представляет собой фенилен, который не конденсирован или конденсирован с бензолом, или гетероареном, или R26A; R26A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R27 представляет собой гетероарилен, который не конденсирован или конденсирован с бензолом, или гетероареном, или R27A; R27A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R28 представляет собой фенилен, который не конденсирован или конденсирован с бензолом, гетероареном или R28A; R28A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R29 представляет собой гетероарилен, который не конденсирован или конденсирован с бензолом, или гетероареном, или R29A; R29A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R30 представляет собой циклоалкилен, циклоалкенилен, гетероциклоалкилен или гетероциклоалкенилен, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R30A; R30A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R37 представляет собой простую связь или R37A;
R37A представляет собой алкилен, алкенилен или алкинилен, каждый из которых не замещен или замещен одним, или двумя, или тремя независимо выбранными заместителями R37B, OR37B, SR37B, S(O)R37B SO2R37B, C(O)R37B, C(O)OR37B, OC(O)R37B, OC(O)OR37B, NH2, NHR37B, N(R37B)2, NHC(O)R37B, NR37BC(O)R37B, NHS(O)2R37B, NR37BS(O)2R37B, NHC(O)OR37B, NR37BC(O)OR37B, NHC(O)NH2, NHC(O)NHR37B, NHC(O)N(R37B)2, NR37BC(O)NHR37B, NR37BC(O)N(R37B)2, C(O)NH2, C(O)NHR37B, C(O)N(R37B)2, C(O)NHOH, C(O)NHOR37B, C(O)NHSO2R37B, C(O)NR37BSO2R37B, SO2NH2, SO2NHR37B, SO2N(R37B)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR37B, C(N)N(R37B)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R37B представляет собой алкил, алкенил, алкинил, фенил, гетероарил, циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил;
Z3 представляет собой R38, R39 или R40;
R38 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R38A; R38A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R39 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R39A; R39A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R40 представляет собой циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R40A; R40A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
где фрагменты, представленные группами R26 и R27, не замещены или замещены (т.е. если Z1A и Z2A отсутствуют) или дополнительно не замещены или дополнительно замещены (т.е. если Z1A и Z2A присутствуют) одним или несколькими заместителями R41, OR41, SR41, S(O)R41, SO2R41, C(O)R41, C(O)OR41, OC(O)R41, OC(O)OR41, NH2, NHR41, N(R41)2, NHC(O)R41, NR41C(O)R41, NHS(O)2R41, NR41S(O)2R41, NHC(O)OR41, NR41C(O)OR41, NHC(O)NH2, NHC(O)NHR41, NHC(O)N(R41)2, NR41C(O)NHR41, NR41C(O)N(R41)2, C(O)NH2, C(O)NHR41, C(O)N(R41)2, C(O)NHOH, C(O)NHOR41, C(O)NHSO2R41, C(O)NR41SO2R41, SO2NH2, SO2NHR41, SO2N(R41)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR41, C(N)N(R41)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R41 представляет собой R42, R43, R44 или R45;
R42 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R42A; R42A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R43 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R43A; R43A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R44 представляет собой циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R44A; R44A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R45 представляет собой алкил, алкенил или алкинил, каждый из которых не замещен или замещен одним или двумя независимо выбранными заместителями R46, OR46, SR46, S(O)R46, SO2R46, C(O)R46, C(O)OR46, OC(O)R46, OC(O)OR46, NH2, NHR46, N(R46)2, NHC(O)R46, NR46C(O)R46, NHS(O)2R46, NR46S(O)2R46, NHC(O)OR46, NR46C(O)OR46, NHC(O)NH2, NHC(O)NHR46, NHC(O)N(R46)2, NR46C(O)NHR46, NR46C(O)N(R46)2, C(O)NH2, C(O)NHR46, C(O)N(R46)2, C(O)NHOH, C(O)NHOR46, C(O)NHSO2R46, C(O)NR46SO2R46, SO2NH2, SO2NHR46, SO2N(R46)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR46, C(N)N(R46)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R46 представляет собой алкил, алкенил или алкинил, R47, R48 или R49;
R47 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R47A; R47A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R48 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R48A; R48A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R49 представляет собой циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R49A; R49A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
где фрагменты, представленные группами R42, R43, R44, R47, R48 и R49, независимо не замещены или замещены одним или несколькими независимо выбранными заместителями R50, OR50, SR50, S(O)R50, SO2R50, C(O)R50, C(O)OR50, OC(O)R50, OC(O)OR50, NH2, NHR50, N(R50)2, NHC(O)R50, NR50C(O)R50, NHS(O)2R50, NR50S(O)2R50, NHC(O)OR50, NR50C(O)OR50, NHC(O)NH2, NHC(O)NHR50, NHC(O)N(R50)2, NR50C(O)NHR50, NR50C(O)N(R50)2, C(O)NH2, C(O)NHR50, C(O)N(R50)2, C(O)NHOH, C(O)NHOR50, C(O)NHSO2R50, C(O)NR50SO2R50, SO2NH2, SO2NHR50, SO2N(R50)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR50, C(N)N(R50)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R50 представляет собой R51, R52, R53 или R54;
R51 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R51A; R51A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R52 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R52A; R52A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R53 представляет собой циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R53A; R53A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R54 представляет собой алкил, алкенил или алкинил, каждый из которых не замещен или замещен одним, или двумя, или тремя независимо выбранными заместителями R55, OR55, SR55, S(O)R55, SO2R55, C(O)R55, C(O)OR55, OC(O)R55, OC(O)OR55, NH2, NHR55, N(R55)2, NHC(O)R55, NR55C(O)R55, NHS(O)2R55, NR55S(O)2R55, NHC(O)OR55, NR55C(O)OR55, NHC(O)NH2, NHC(O)NHR55, NHC(O)N(R55)2, NR55C(O)NHR55, NR55C(O)N(R55)2, C(O)NH2, C(O)NHR55, C(O)N(R55)2, C(O)NHOH, C(O)NHOR55, C(O)NHSO2R55, C(O)NR55SO2R55, SO2NH2, SO2NHR55, SO2N(R55)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR55, C(N)N(R55)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R55 представляет собой алкил, алкенил, алкинил, фенил, гетероарил, циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил;
где каждый вышеуказанный циклический фрагмент независимо не замещен, дополнительно не замещен, замещен или дополнительно замещен одним или несколькими независимо выбранными заместителями R57, OR57, SR57, S(O)R57, SO2R57, C(O)R57, C(O)OR57, OC(O)R57, OC(O)OR57, NH2, NHR57, N(R57)2, NHC(O)R57, NR57C(O)R57, NHS(O)2R57, NR57S(O)2R57, NHC(O)OR57, NR57C(O)OR57, NHC(O)NH2, NHC(O)NHR57, NHC(O)N(R57)2, NR57C(O)NHR57, NR57C(O)N(R57)2, C(O)NH2, C(O)NHR57, C(O)N(R57)2, C(O)NHOH, C(O)NHOR57, C(O)NHSO2R57, C(O)NR57SO2R57, SO2NH2, SO2NHR57, SO2N(R57)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR57, C(N)N(R57)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R57 представляет собой R58, R59, R60 или R61;
R58 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R58A; R58A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R59 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R59A; R59A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R60 представляет собой циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R60A; R60A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R61 представляет собой алкил, алкенил или алкинил, каждый из которых не замещен или замещен одним, или двумя, или тремя независимо выбранными заместителями R62, OR62, SR62, S(O)R62, SO2R62, C(O)R62, C(O)OR62, OC(O)R62, OC(O)OR62, NH2, NHR62, N(R62)2, NHC(O)R62, NR62C(O)R62, NHS(O)2R62, NR62S(O)2R62, NHC(O)OR62, NR62C(O)OR62, NHC(O)NH2, NHC(O)NHR62, NHC(O)N(R62)2, NR62C(O)NHR62, NR62C(O)N(R62)2, C(O)NH2, C(O)NHR62, C(O)N(R62)2, C(O)NHOH, C(O)NHOR62, C(O)NHSO2R62, C(O)NR62SO2R62, SO2NH2, SO2NHR62, SO2N(R62)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR62, C(N)N(R62)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R62 представляет собой R63, R64, R65 или R66;
R63 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R63A; R63A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R64 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R64A; R64A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R65 представляет собой циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R65A; R65A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R66 представляет собой алкил, алкенил или алкинил, каждый из которых не замещен или замещен одним, или двумя, или тремя независимо выбранными заместителями R67, OR67, SR67, S(O)R67, SO2R67, C(O)R67, C(O)OR67, OC(O)R67, OC(O)OR67, NH2, NHR67, N(R67)2, NHC(O)R67, NR67C(O)R67, NHS(O)2R67, NR67S(O)2R67, NHC(O)OR67, NR67C(O)OR67, NHC(O)NH2, NHC(O)NHR67, NHC(O)N(R67)2, NR67C(O)NHR67, NR67C(O)N(R67)2, C(O)NH2, C(O)NHR67, C(O)N(R67)2, C(O)NHOH, C(O)NHOR67, C(O)NHSO2R67, C(O)NR67SO2R67, SO2NH2, SO2NHR67, SO2N(R67)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR67, C(N)N(R67)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R67 представляет собой алкил, алкенил, алкинил, фенил, гетероарил, циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил;
где фрагменты, представленные группами R58, R59, R60, R63, R64, R65 и R67, не замещены или замещены одним или несколькими независимо выбранными заместителями R68, OR68, SR68, S(O)R68, SO2R68, C(O)R68, C(O)OR68, OC(O)R68, OC(O)OR68, NH2, NHR68, N(R68)2, NHC(O)R68, NR68C(O)R68, NHS(O)2R68, NR68S(O)2R68, NHC(O)OR68, NR68C(O)OR68, NHC(O)NH2, NHC(O)NHR68, NHC(O)N(R68)2, NR68C(O)NHR68, NR68C(O)N(R68)2, C(O)NH2, C(O)NHR68, C(O)N(R68)2, C(O)NHOH, C(O)NHOR68, C(O)NHSO2R68, C(O)NR68SO2R68, SO2NH2, SO2NHR68, SO2N(R68)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR68, C(N)N(R68)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R68 представляет собой R69, R70, R71 или R72;
R69 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R69A; R69A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R70 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R70A; R70A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R71 представляет собой циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R71A; R71A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R72 представляет собой алкил, алкенил или алкинил, каждый из которых не замещен или замещен одним, или двумя, или тремя независимо выбранными заместителями R73, OR73, SR73, S(O)R73, SO2R73, C(O)R73, C(O)OR73, OC(O)R73, OC(O)OR73, NH2, NHR73, N(R73)2, NHC(O)R73, NR73C(O)R73, NHS(O)2R73, NR73S(O)2R73, NHC(O)OR73, NR73C(O)OR73, NHC(O)NH2, NHC(O)NHR73, NHC(O)N(R73)2, NR73C(O)NHR73, NR73C(O)N(R73)2, C(O)NH2, C(O)NHR73, C(O)N(R73)2, C(O)NHOH, C(O)NHOR73, C(O)NHSO2R73, C(O)NR73SO2R73, SO2NH2, SO2NHR73, SO2N(R73)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR73, C(N)N(R73)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R73 представляет собой алкил, алкенил, алкинил, фенил, гетероарил, циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил; и
фрагменты, представленные группами R69, R70 и R71, не замещены или замещены одним или несколькими независимо выбранными заместителями NH2, C(O)NH2, C(O)NHOH, SO2NH2, CF3, CF2CF3, C(O)H, C(O)OH, C(N)NH2, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I.
В другом варианте осуществления формулы (I)
A1 представляет собой фурил, имидазолил, изотиазолил, изоксазолил, пиразолил, пирролил, тиазолил, тиадиазолил, тиенил, триазолил, гетероциклоалкил или гетероциклоалкенил; каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или A1A; A1A представляет собой гетероциклоалкен;
где A1 не замещен или замещен одним, или двумя, или тремя, или четырьмя, или пятью независимо выбранными заместителями R1, OR1, C(O)OR1, NHR1, N(R1)2, C(N)C(O)R1, C(O)NHR1, NHC(O)R1, NR1C(O)R1, (O), NO2, F, Cl, Br, I, CF3;
R1 представляет собой R2, R3, R4 или R5;
R2 представляет собой фенил;
R3 представляет собой гетероарил;
R4 представляет собой гетероциклоалкил;
R5 представляет собой алкил или алкенил, каждый из которых не замещен или замещен заместителями R7, SR7, N(R7)2, NHC(O)R7, F, Cl, Br или I;
R7 представляет собой R8, R9, R10 или R11;
R8 представляет собой фенил;
R9 представляет собой гетероарил;
R10 представляет собой гетероциклоалкил;
R11 представляет собой алкил;
Z1 представляет собой R26;
Z2 представляет собой R30;
L1 представляет собой R37;
R26 представляет собой фенилен;
R30 представляет собой гетероциклоалкилен;
R37 представляет собой R37A;
R37A представляет собой алкилен или алкенилен, каждый из которых не замещен или замещен R37B;
R37B представляет собой фенил;
Z3 представляет собой R38 или R40;
R38 представляет собой фенил;
R40 представляет собой циклоалкил или циклоалкенил;
где фрагменты, представленные группами R26 и R27, не замещены или замещены группой OR41;
R41 представляет собой R42 или R43;
R42 представляет собой фенил, который не конденсирован или конденсирован с гетероареном;
R43 представляет собой гетероарил, который не конденсирован или конденсирован с гетероареном;
где каждый вышеуказанный циклический фрагмент независимо не замещен, дополнительно не замещен, замещен или дополнительно замещен одним или несколькими независимо выбранными заместителями R57, OR57, C(O)OR57, F, Cl, Br или I;
R57 представляет собой R58 или R61;
R58 представляет собой фенил;
R61 представляет собой алкил; и
где фрагменты, представленные группой R58, не замещены или замещены одним или несколькими независимо выбранными заместителями F, Cl, Br или I.
Другой вариант осуществления настоящего изобретения касается соединений или их терапевтически приемлемых солей, пролекарств, метаболитов или солей пролекарств указанных соединений, которые пригодны в качестве ингибиторов антиапоптотических белков Bcl-2, при этом указанные соединения имеют формулу II

где
A1 представляет собой фурил, имидазолил, изотиазолил, изоксазолил, оксадиазолил, оксазолил, пиразинил, пиразолил, пиридазинил, 2-пиридинил, 4-пиридинил, пиримидинил, пирролил, тетразолил, тиазолил, тиадиазолил, тиенил, триазинил, триазолил, циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил; каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или A1A; A1A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
где A1 не замещен или замещен одним, или двумя, или тремя, или четырьмя, или пятью независимо выбранными заместителями R1, OR1, SR1, S(O)R1, SO2R1, C(O)R1, C(O)OR1, OC(O)R1, NHR1, N(R1)2, C(N)C(O)R1, C(O)NHR1, C(O)N(R1)2, C(O)NHOH, C(O)NHOR1, C(O)NHSO2R1, NHC(O)R1, NR1C(O)R1, NHC(O)OR1, NR1C(O)OR1, NR1C(O)NHR1, NR1C(O)N(R1)2, NHC(O)NH2, NHC(O)NHR1, NHC(O)N(R1)2, SO2NH2, SO2NHR1, SO2N(R1)2, NHS(O)R1, NHSO2R1, NR1SO2R1, NHSO2NHR1, N(CH3)SO2N(CH3)R1, (O), NH2, NO2, N3, OH, F, Cl, Br, I, CN, CF3, OCF3, CF2CF3, OCF2CF3, C(O)H, C(O)OH, C(N)NH2, C(N)NHR1, C(N)N(R1)2, CNOH, CNOCH3, C(O)NH2 или C(O)OR1A;
R1 представляет собой R2, R3, R4 или R5;
R1A представляет собой циклоалкил, циклоалкенил или циклоалкинил;
R2 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R2A; R2A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R3 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R3A; R3A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R4 представляет собой циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R4A; R4A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R5 представляет собой алкил, алкенил или алкинил, каждый из которых не замещен или замещен одним, или двумя, или тремя независимо выбранными заместителями R6, NC(R6A)(R6B), R7, OR7, SR7, S(O)R7, SO2R7, NHR7, N(R7)2, C(O)R7, C(O)NH2, C(O)NHR7, C(O)N(R7)2, NHC(O)R7, NR7C(O)R7, NHSO2R7, NHC(O)OR7, SO2NH2, SO2NHR7, SO2N(R7)2, NHC(O)NH2, NHC(O)NHR7, NHC(O)CH(CH3)NHC(O)CH(CH3)NH2, NHC(O)CH(CH3)NHC(O)CH(CH3)NHR1, OH, (O), C(O)OH, (O), N3, CN, NH2, CF3, CF2CF3, F, Cl, Br или I;
R6 представляет собой C2-C5-спироалкил, каждый из которых не замещен или замещен группами OH, (O), N3, CN, CF3, CF2CF3, F, Cl, Br, I, NH2, NH(CH3) или N(CH3)2;
R6A и R6B независимо выбраны из алкила или вместе с атомом N, к которому они присоединены, образуют R6C;
R6C представляет собой азиридин-1-ил, азетидин-1-ил, пирролидин-1-ил или пиперидин-1-ил, каждый из которых имеет один фрагмент CH2, не замененный или замененный O, C(O), CNOH, CNOCH3, S, S(O), SO2 или NH;
R7 представляет собой R8, R9, R10 или R11;
R8 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R8A; R8A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R9 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R9A; R9A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R10 представляет собой циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R10A; R10A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R11 представляет собой алкил, алкенил или алкинил, каждый из которых не замещен или замещен одним, или двумя, или тремя независимо выбранными заместителями R12, OR12, SR12, S(O)R12, SO2R12, C(O)R12, C(O)OR12, OC(O)R12, OC(O)OR12, NH2, NHR12, N(R12)2, NHC(O)R12, NR12C(O)R12, NHS(O)2R12, NR12S(O)2R12, NHC(O)OR12, NR12C(O)OR12, NHC(O)NH2, NHC(O)NHR12, NHC(O)N(R12)2, NR12C(O)NHR12, NR12C(O)N(R12)2, C(O)NH2, C(O)NHR12, C(O)N(R12)2, C(O)NHOH, C(O)NHOR12, C(O)NHSO2R12, C(O)NR12SO2R12, SO2NH2, SO2NHR12, SO2N(R12)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR12, C(N)N(R12)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R12 представляет собой R13, R14, R15 или R16;
R13 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R13A; R13A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R14 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R14A; R14A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R15 представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R15A; R15A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R16 представляет собой алкил, алкенил или алкинил;
где фрагмент, представленный группой R101, представляет собой заместители H, R41, OR41, SR41, S(O)R41, SO2R41, C(O)R41, C(O)OR41, OC(O)R41, OC(O)OR41, NH2, NHR41, N(R41)2, NHC(O)R41, NR41C(O)R41, NHS(O)2R41, NR41S(O)2R41, NHC(O)OR41, NR41C(O)OR41, NHC(O)NH2, NHC(O)NHR41, NHC(O)N(R41)2, NR41C(O)NHR41, NR41C(O)N(R41)2, C(O)NH2, C(O)NHR41, C(O)N(R41)2, C(O)NHOH, C(O)NHOR41, C(O)NHSO2R41, C(O)NR41SO2R41, SO2NH2, SO2NHR41, SO2N(R41)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR41, C(N)N(R41)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R41 представляет собой R42, R43, R44 или R45;
R42 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R42A; R42A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R43 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R43A; R43A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R44 представляет собой циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R44A; R44A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R45 представляет собой алкил, алкенил или алкинил, каждый из которых не замещен или замещен одним или двумя независимо выбранными заместителями R46, OR46, SR46, S(O)R46, SO2R46, C(O)R46, C(O)OR46, OC(O)R46, OC(O)OR46, NH2, NHR46, N(R46)2, NHC(O)R46, NR46C(O)R46, NHS(O)2R46, NR46S(O)2R46, NHC(O)OR46, NR46C(O)OR46, NHC(O)NH2, NHC(O)NHR46, NHC(O)N(R46)2, NR46C(O)NHR46, NR46C(O)N(R46)2, C(O)NH2, C(O)NHR46, C(O)N(R46)2, C(O)NHOH, C(O)NHOR46, C(O)NHSO2R46, C(O)NR46SO2R46, SO2NH2, SO2NHR46, SO2N(R46)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR46, C(N)N(R46)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R46 представляет собой алкил, алкенил или алкинил, R47, R48 или R49;
R47 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R47A; R47A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R48 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R48A; R48A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R49 представляет собой циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R49A; R49A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
фрагменты, представленные группами R42, R43, R44, R47, R48 и R49, независимо не замещены или замещены одним или несколькими независимо выбранными заместителями R50, OR50, SR50, S(O)R50, SO2R50, C(O)R50, C(O)OR50, OC(O)R50, OC(O)OR50, NH2, NHR50, N(R50)2, NHC(O)R50, NR50C(O)R50, NHS(O)2R50, NR50S(O)2R50, NHC(O)OR50, NR50C(O)OR50, NHC(O)NH2, NHC(O)NHR50, NHC(O)N(R50)2, NR50C(O)NHR50, NR50C(O)N(R50)2, C(O)NH2, C(O)NHR50, C(O)N(R50)2, C(O)NHOH, C(O)NHOR50, C(O)NHSO2R50, C(O)NR50SO2R50, SO2NH2, SO2NHR50, SO2N(R50)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR50, C(N)N(R50)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R50 представляет собой R51, R52, R53 или R54;
R51 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R51A; R51A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R52 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R52A; R52A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R53 представляет собой циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R53A; R53A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R54 представляет собой алкил, алкенил или алкинил, каждый из которых не замещен или замещен одним, или двумя, или тремя независимо выбранными заместителями R55, OR55, SR55, S(O)R55, SO2R55, C(O)R55, C(O)OR55, OC(O)R55, OC(O)OR55, NH2, NHR55, N(R55)2, NHC(O)R55, NR55C(O)R55, NHS(O)2R55, NR55S(O)2R55, NHC(O)OR55, NR55C(O)OR55, NHC(O)NH2, NHC(O)NHR55, NHC(O)N(R55)2, NR55C(O)NHR55, NR55C(O)N(R55)2, C(O)NH2, C(O)NHR55, C(O)N(R55)2, C(O)NHOH, C(O)NHOR55, C(O)NHSO2R55, C(O)NR55SO2R55, SO2NH2, SO2NHR55, SO2N(R55)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR55, C(N)N(R55)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R55 представляет собой алкил, алкенил, алкинил, фенил, гетероарил, циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил;
где каждый вышеуказанный циклический фрагмент независимо не замещен, дополнительно не замещен, замещен или дополнительно замещен одним или несколькими независимо выбранными заместителями R57, OR57, SR57, S(O)R57, SO2R57, C(O)R57, C(O)OR57, OC(O)R57, OC(O)OR57, NH2, NHR57, N(R57)2, NHC(O)R57, NR57C(O)R57, NHS(O)2R57, NR57S(O)2R57, NHC(O)OR57, NR57C(O)OR57, NHC(O)NH2, NHC(O)NHR57, NHC(O)N(R57)2, NR57C(O)NHR57, NR57C(O)N(R57)2, C(O)NH2, C(O)NHR57, C(O)N(R57)2, C(O)NHOH, C(O)NHOR57, C(O)NHSO2R57, C(O)NR57SO2R57, SO2NH2, SO2NHR57, SO2N(R57)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR57, C(N)N(R57)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R57 представляет собой R58, R59, R60 или R61;
R58 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R58A; R58A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R59 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R59A; R59A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R60 представляет собой циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R60A; R60A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R61 представляет собой алкил, алкенил или алкинил, каждый из которых не замещен или замещен одним, или двумя, или тремя независимо выбранными заместителями R62, OR62, SR62, S(O)R62, SO2R62, C(O)R62, C(O)OR62, OC(O)R62, OC(O)OR62, NH2, NHR62, N(R62)2, NHC(O)R62, NR62C(O)R62, NHS(O)2R62, NR62S(O)2R62, NHC(O)OR62, NR62C(O)OR62, NHC(O)NH2, NHC(O)NHR62, NHC(O)N(R62)2, NR62C(O)NHR62, NR62C(O)N(R62)2, C(O)NH2, C(O)NHR62, C(O)N(R62)2, C(O)NHOH, C(O)NHOR62, C(O)NHSO2R62, C(O)NR62SO2R62, SO2NH2, SO2NHR62, SO2N(R62)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR62, C(N)N(R62)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R62 представляет собой R63, R64, R65 или R66;
R63 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R63A; R63A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R64 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R64A; R64A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R65 представляет собой циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R65A; R65A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R66 представляет собой алкил, алкенил или алкинил, каждый из которых не замещен или замещен одним, или двумя, или тремя независимо выбранными заместителями R67, OR67, SR67, S(O)R67, SO2R67, C(O)R67, C(O)OR67, OC(O)R67, OC(O)OR67, NH2, NHR67, N(R67)2, NHC(O)R67, NR67C(O)R67, NHS(O)2R67, NR67S(O)2R67, NHC(O)OR67, NR67C(O)OR67, NHC(O)NH2, NHC(O)NHR67, NHC(O)N(R67)2, NR67C(O)NHR67, NR67C(O)N(R67)2, C(O)NH2, C(O)NHR67, C(O)N(R67)2, C(O)NHOH, C(O)NHOR67, C(O)NHSO2R67, C(O)NR67SO2R67, SO2NH2, SO2NHR67, SO2N(R67)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR67, C(N)N(R67)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R67 представляет собой алкил, алкенил, алкинил, фенил, гетероарил, циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил;
где фрагменты, представленные группами R58, R59, R60, R63, R64, R65 и R67, не замещены или замещены одним или несколькими независимо выбранными заместителями R68, OR68, SR68, S(O)R68, SO2R68, C(O)R68, C(O)OR68, OC(O)R68, OC(O)OR68, NH2, NHR68, N(R68)2, NHC(O)R68, NR68C(O)R68, NHS(O)2R68, NR68S(O)2R68, NHC(O)OR68, NR68C(O)OR68, NHC(O)NH2, NHC(O)NHR68, NHC(O)N(R68)2, NR68C(O)NHR68, NR68C(O)N(R68)2, C(O)NH2, C(O)NHR68, C(O)N(R68)2, C(O)NHOH, C(O)NHOR68, C(O)NHSO2R68, C(O)NR68SO2R68, SO2NH2, SO2NHR68, SO2N(R68)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR68, C(N)N(R68)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R68 представляет собой R69, R70, R71 или R72;
R69 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R69A; R69A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R70 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R70A; R70A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R71 представляет собой циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R71A; R71A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R72 представляет собой алкил, алкенил или алкинил, каждый из которых не замещен или замещен одним, или двумя, или тремя независимо выбранными заместителями R73, OR73, SR73, S(O)R73, SO2R73, C(O)R73, C(O)OR73, OC(O)R73, OC(O)OR73, NH2, NHR73, N(R73)2, NHC(O)R73, NR73C(O)R73, NHS(O)2R73, NR73S(O)2R73, NHC(O)OR73, NR73C(O)OR73, NHC(O)NH2, NHC(O)NHR73, NHC(O)N(R73)2, NR73C(O)NHR73, NR73C(O)N(R73)2, C(O)NH2, C(O)NHR73, C(O)N(R73)2, C(O)NHOH, C(O)NHOR73, C(O)NHSO2R73, C(O)NR73SO2R73, SO2NH2, SO2NHR73, SO2N(R73)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR73, C(N)N(R73)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R73 представляет собой алкил, алкенил, алкинил, фенил, гетероарил, циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил; и
фрагменты, представленные группами R69, R70 и R71, не замещены или замещены одним или несколькими независимо выбранными заместителями NH2, C(O)NH2, C(O)NHOH, SO2NH2, CF3, CF2CF3, C(O)H, C(O)OH, C(N)NH2, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I.
Другой вариант осуществления настоящего изобретения касается соединений или их терапевтически приемлемых солей, пролекарств, метаболитов или солей пролекарств указанных соединений, которые пригодны в качестве ингибиторов антиапоптотических белков Bcl-2, при этом указанные соединения имеют формулу III

где
A1 представляет собой фурил, имидазолил, изотиазолил, изоксазолил, оксадиазолил, оксазолил, пиразинил, пиразолил, пиридазинил, 2-пиридинил, 4-пиридинил, пиримидинил, пирролил, тетразолил, тиазолил, тиадиазолил, тиенил, триазинил, триазолил, циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил; каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или A1A; A1A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
где A1 не замещен или замещен одним, или двумя, или тремя, или четырьмя, или пятью независимо выбранными заместителями R1, OR1, SR1, S(O)R1, SO2R1, C(O)R1, C(O)OR1, OC(O)R1, NHR1, N(R1)2, C(N)C(O)R1, C(O)NHR1, C(O)N(R1)2, C(O)NHOH, C(O)NHOR1, C(O)NHSO2R1, NHC(O)R1, NR1C(O)R1, NHC(O)OR1, NR1C(O)OR1, NR1C(O)NHR1, NR1C(O)N(R1)2, NHC(O)NH2, NHC(O)NHR1, NHC(O)N(R1)2, SO2NH2, SO2NHR1, SO2N(R1)2, NHS(O)R1, NHSO2R1, NR1SO2R1, NHSO2NHR1, N(CH3)SO2N(CH3)R1, (O), NH2, NO2, N3, OH, F, Cl, Br, I, CN, CF3, OCF3, CF2CF3, OCF2CF3, C(O)H, C(O)OH, C(N)NH2, C(N)NHR1, C(N)N(R1)2, CNOH, CNOCH3, C(O)NH2 или C(O)OR1A;
R1 представляет собой R2, R3, R4 или R5;
R1A представляет собой циклоалкил, циклоалкенил или циклоалкинил;
R2 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R2A; R2A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R3 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R3A; R3A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R4 представляет собой циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R4A; R4A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R5 представляет собой алкил, алкенил или алкинил, каждый из которых не замещен или замещен одним, или двумя, или тремя независимо выбранными заместителями R6, NC(R6A)(R6B), R7, OR7, SR7, S(O)R7, SO2R7, NHR7, N(R7)2, C(O)R7, C(O)NH2, C(O)NHR7, C(O)N(R7)2, NHC(O)R7, NR7C(O)R7, NHSO2R7, NHC(O)OR7, SO2NH2, SO2NHR7, SO2N(R7)2, NHC(O)NH2, NHC(O)NHR7, NHC(O)CH(CH3)NHC(O)CH(CH3)NH2, NHC(O)CH(CH3)NHC(O)CH(CH3)NHR1, OH, (O), C(O)OH, N3, CN, NH2, CF3, CF2CF3, F, Cl, Br или I;
R6 представляет собой C2-C5-спироалкил, каждый из которых не замещен или замещен группами OH, (O), N3, CN, CF3, CF2CF3, F, Cl, Br, I, NH2, NH(CH3) или N(CH3)2;
R6A и R6B независимо выбраны из алкила или вместе с атомом N, к которому они присоединены, образуют R6C;
R6C представляет собой азиридин-1-ил, азетидин-1-ил, пирролидин-1-ил или пиперидин-1-ил, каждый из которых имеет один фрагмент CH2, не замененный или замененный O, C(O), CNOH, CNOCH3, S, S(O), SO2 или NH;
R7 представляет собой R8, R9, R10 или R11;
R8 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R8A; R8A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R9 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R9A; R9A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R10 представляет собой циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R10A; R10A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R11 представляет собой алкил, алкенил или алкинил, каждый из которых не замещен или замещен одним, или двумя, или тремя независимо выбранными заместителями R12, OR12, SR12, S(O)R12, SO2R12, C(O)R12, C(O)OR12, OC(O)R12, OC(O)OR12, NH2, NHR12, N(R12)2, NHC(O)R12, NR12C(O)R12, NHS(O)2R12, NR12S(O)2R12, NHC(O)OR12, NR12C(O)OR12, NHC(O)NH2, NHC(O)NHR12, NHC(O)N(R12)2, NR12C(O)NHR12, NR12C(O)N(R12)2, C(O)NH2, C(O)NHR12, C(O)N(R12)2, C(O)NHOH, C(O)NHOR12, C(O)NHSO2R12, C(O)NR12SO2R12, SO2NH2, SO2NHR12, SO2N(R12)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR12, C(N)N(R12)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R12 представляет собой R13, R14, R15 или R16;
R13 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R13A; R13A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R14 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R14A; R14A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R15 представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R15A; R15A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R16 представляет собой алкил, алкенил или алкинил;
где фрагмент, представленный группой R101, представляет собой заместители H, R41, OR41, SR41, S(O)R41, SO2R41, C(O)R41, C(O)OR41, OC(O)R41, OC(O)OR41, NH2, NHR41, N(R41)2, NHC(O)R41, NR41C(O)R41, NHS(O)2R41, NR41S(O)2R41, NHC(O)OR41, NR41C(O)OR41, NHC(O)NH2, NHC(O)NHR41, NHC(O)N(R41)2, NR41C(O)NHR41, NR41C(O)N(R41)2, C(O)NH2, C(O)NHR41, C(O)N(R41)2, C(O)NHOH, C(O)NHOR41, C(O)NHSO2R41, C(O)NR41SO2R41, SO2NH2, SO2NHR41, SO2N(R41)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR41, C(N)N(R41)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R41 представляет собой R42, R43, R44 или R45;
R42 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R42A; R42A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R43 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R43A; R43A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R44 представляет собой циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R44A; R44A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R45 представляет собой алкил, алкенил или алкинил, каждый из которых не замещен или замещен одним или двумя независимо выбранными заместителями R46, OR46, SR46, S(O)R46, SO2R46, C(O)R46, C(O)OR46, OC(O)R46, OC(O)OR46, NH2, NHR46, N(R46)2, NHC(O)R46, NR46C(O)R46, NHS(O)2R46, NR46S(O)2R46, NHC(O)OR46, NR46C(O)OR46, NHC(O)NH2, NHC(O)NHR46, NHC(O)N(R46)2, NR46C(O)NHR46, NR46C(O)N(R46)2, C(O)NH2, C(O)NHR46, C(O)N(R46)2, C(O)NHOH, C(O)NHOR46, C(O)NHSO2R46, C(O)NR46SO2R46, SO2NH2, SO2NHR46, SO2N(R46)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR46, C(N)N(R46)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R46 представляет собой алкил, алкенил или алкинил, R47, R48 или R49;
R47 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R47A; R47A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R48 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R48A; R48A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R49 представляет собой циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R49A; R49A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
фрагменты, представленные группами R42, R43, R44, R47, R48 и R49, независимо не замещены или замещены одним или несколькими независимо выбранными заместителями R50, OR50, SR50, S(O)R50, SO2R50, C(O)R50, C(O)OR50, OC(O)R50, OC(O)OR50, NH2, NHR50, N(R50)2, NHC(O)R50, NR50C(O)R50, NHS(O)2R50, NR50S(O)2R50, NHC(O)OR50, NR50C(O)OR50, NHC(O)NH2, NHC(O)NHR50, NHC(O)N(R50)2, NR50C(O)NHR50, NR50C(O)N(R50)2, C(O)NH2, C(O)NHR50, C(O)N(R50)2, C(O)NHOH, C(O)NHOR50, C(O)NHSO2R50, C(O)NR50SO2R50, SO2NH2, SO2NHR50, SO2N(R50)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR50, C(N)N(R50)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R50 представляет собой R51, R52, R53 или R54;
R51 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R51A; R51A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R52 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R52A; R52A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R53 представляет собой циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R53A; R53A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R54 представляет собой алкил, алкенил или алкинил, каждый из которых не замещен или замещен одним, или двумя, или тремя независимо выбранными заместителями R55, OR55, SR55, S(O)R55, SO2R55, C(O)R55, C(O)OR55, OC(O)R55, OC(O)OR55, NH2, NHR55, N(R55)2, NHC(O)R55, NR55C(O)R55, NHS(O)2R55, NR55S(O)2R55, NHC(O)OR55, NR55C(O)OR55, NHC(O)NH2, NHC(O)NHR55, NHC(O)N(R55)2, NR55C(O)NHR55, NR55C(O)N(R55)2, C(O)NH2, C(O)NHR55, C(O)N(R55)2, C(O)NHOH, C(O)NHOR55, C(O)NHSO2R55, C(O)NR55SO2R55, SO2NH2, SO2NHR55, SO2N(R55)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR55, C(N)N(R55)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R55 представляет собой алкил, алкенил, алкинил, фенил, гетероарил, циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил;
где каждый вышеуказанный циклический фрагмент независимо не замещен, дополнительно не замещен, замещен или дополнительно замещен одним или несколькими независимо выбранными заместителями R57, OR57, SR57, S(O)R57, SO2R57, C(O)R57, C(O)OR57, OC(O)R57, OC(O)OR57, NH2, NHR57, N(R57)2, NHC(O)R57, NR57C(O)R57, NHS(O)2R57, NR57S(O)2R57, NHC(O)OR57, NR57C(O)OR57, NHC(O)NH2, NHC(O)NHR57, NHC(O)N(R57)2, NR57C(O)NHR57, NR57C(O)N(R57)2, C(O)NH2, C(O)NHR57, C(O)N(R57)2, C(O)NHOH, C(O)NHOR57, C(O)NHSO2R57, C(O)NR57SO2R57, SO2NH2, SO2NHR57, SO2N(R57)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR57, C(N)N(R57)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R57 представляет собой R58, R59, R60 или R61;
R58 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R58A; R58A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R59 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R59A; R59A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R60 представляет собой циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R60A; R60A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R61 представляет собой алкил, алкенил или алкинил, каждый из которых не замещен или замещен одним, или двумя, или тремя независимо выбранными заместителями R62, OR62, SR62, S(O)R62, SO2R62, C(O)R62, C(O)OR62, OC(O)R62, OC(O)OR62, NH2, NHR62, N(R62)2, NHC(O)R62, NR62C(O)R62, NHS(O)2R62, NR62S(O)2R62, NHC(O)OR62, NR62C(O)OR62, NHC(O)NH2, NHC(O)NHR62, NHC(O)N(R62)2, NR62C(O)NHR62, NR62C(O)N(R62)2, C(O)NH2, C(O)NHR62, C(O)N(R62)2, C(O)NHOH, C(O)NHOR62, C(O)NHSO2R62, C(O)NR62SO2R62, SO2NH2, SO2NHR62, SO2N(R62)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR62, C(N)N(R62)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R62 представляет собой R63, R64, R65 или R66;
R63 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R63A; R63A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R64 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R64A; R64A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R65 представляет собой циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R65A; R65A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероцикл оалкен;
R66 представляет собой алкил, алкенил или алкинил, каждый из которых не замещен или замещен одним, или двумя, или тремя независимо выбранными заместителями R67, OR67, SR67, S(O)R67, SO2R67, C(O)R67, C(O)OR67, OC(O)R67, OC(O)OR67, NH2, NHR67, N(R67)2, NHC(O)R67, NR67C(O)R67, NHS(O)2R67, NR67S(O)2R67, NHC(O)OR67, NR67C(O)OR67, NHC(O)NH2, NHC(O)NHR67, NHC(O)N(R67)2, NR67C(O)NHR67, NR67C(O)N(R67)2, C(O)NH2, C(O)NHR67, C(O)N(R67)2, C(O)NHOH, C(O)NHOR67, C(O)NHSO2R67, C(O)NR67SO2R67, SO2NH2, SO2NHR67, SO2N(R67)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR67, C(N)N(R67)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R67 представляет собой алкил, алкенил, алкинил, фенил, гетероарил, циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил;
где фрагменты, представленные группами R58, R59, R60, R63, R64, R65 и R67, не замещены или замещены одним или несколькими независимо выбранными заместителями R68, OR68, SR68, S(O)R68, SO2R68, C(O)R68, C(O)OR68, OC(O)R68, OC(O)OR68, NH2, NHR68, N(R68)2, NHC(O)R68, NR68C(O)R68, NHS(O)2R68, NR68S(O)2R68, NHC(O)OR68, NR68C(O)OR68, NHC(O)NH2, NHC(O)NHR68, NHC(O)N(R68)2, NR68C(O)NHR68, NR68C(O)N(R68)2, C(O)NH2, C(O)NHR68, C(O)N(R68)2, C(O)NHOH, C(O)NHOR68, C(O)NHSO2R68, C(O)NR68SO2R68, SO2NH2, SO2NHR68, SO2N(R68)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR68, C(N)N(R68)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R68 представляет собой R69, R70, R71 или R72;
R69 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R69A; R69A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R70 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R70A; R70A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R71 представляет собой циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R71A; R71A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R72 представляет собой алкил, алкенил или алкинил, каждый из которых не замещен или замещен одним, или двумя, или тремя независимо выбранными заместителями R73, OR73, SR73, S(O)R73, SO2R73, C(O)R73, C(O)OR73, OC(O)R73, OC(O)OR73, NH2, NHR73, N(R73)2, NHC(O)R73, NR73C(O)R73, NHS(O)2R73, NR73S(O)2R73, NHC(O)OR73, NR73C(O)OR73, NHC(O)NH2, NHC(O)NHR73, NHC(O)N(R73)2, NR73C(O)NHR73, NR73C(O)N(R73)2, C(O)NH2, C(O)NHR73, C(O)N(R73)2, C(O)NHOH, C(O)NHOR73, C(O)NHSO2R73, C(O)NR73SO2R73, SO2NH2, SO2NHR73, SO2N(R73)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR73, C(N)N(R73)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R73 представляет собой алкил, алкенил, алкинил, фенил, гетероарил, циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил; и
фрагменты, представленные группами R69, R70 и R71, не замещены или замещены одним или несколькими независимо выбранными заместителями NH2, C(O)NH2, C(O)NHOH, SO2NH2, CF3, CF2CF3, C(O)H, C(O)OH, C(N)NH2, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I.
Наконец, другой вариант осуществления настоящего изобретения касается соединений, имеющих формулу I, которые представляют собой
4-[4-(циклогексилметил)-4-метоксипиперидин-1-ил]-N-{[5-({(1R)-3-(диметиламино)-1-[(фенилтио)метил]пропил}амино)-4-нитротиен-2-ил]сульфонил}бензамид;
N-{[5-({(1R)-3-(диметиламино)-1-[(фенилтио)метил]пропил}амино)-4-нитротиен-2-ил]сульфонил}-4-[4-метокси-4-(3-метилбензил)пиперидин-1-ил]бензамид;
N-{[5-({(1R)-3-(диметиламино)-1-[(фенилтио)метил]пропил}амино)-4-нитротиен-2-ил]сульфонил}-4-[4-(3,3-дифенилпроп-2-енил)пиперазин-1-ил]бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(4-{[2-(фенилтио)этил]амино}пиперидин-1-ил)сульфонил]бензамид;
N-[(4-{ацетил[2-(фенилтио)этил]амино}пиперидин-1-ил)сульфонил]-4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(4-{метил[2-(фенилтио)этил]амино}пиперидин-1-ил)сульфонил]бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-{[5-({(1R)-3-[изопропил(метил)амино]-1-[(фенилтио)метил]пропил}амино)-4-нитротиен-2-ил]сульфонил}бензамид;
4-(4-{[2-(4-хлорфенил)циклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-{[5-({(1R)-3-[изопропил(метил)амино]-1-[(фенилтио)метил]пропил}амино)-4-нитротиен-2-ил]сульфонил}бензамид;
4-(4-{[2-(4-хлорфенил)-5,5-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-{[5-({(1R)-3-[изопропил(метил)амино]-1-[(фенилтио)метил]пропил}амино)-4-нитротиен-2-ил]сульфонил}бензамид;
N-{[(5Z)-5-(ацетилимино)-4-метил-4,5-дигидро-1,3,4-тиадиазол-2-ил]сульфонил}-4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензамид;
N-{[2-(ацетиламино)-4-метил-1,3-тиазол-5-ил]сульфонил}-4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензамид;
N-({5-[(бензоиламино)метил]тиен-2-ил}сульфонил)-4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(6-хлоримидазо[2,1-b][1,3]тиазол-5-ил)сульфонил]бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-(морфолин-4-илсульфонил)бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(2,4-диметил-1,3-тиазол-5-ил)сульфонил]бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-{[4-фенил-5-(трифторметил)тиен-3-ил]сульфонил]бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(5-фтор-3-метил-1-бензотиен-2-ил)сульфонил]бензамид;
N-(1,3-бензотиазол-2-илсульфонил)-4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-(тиен-2-илсульфонил)бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(5,7-диметил[1,2,4]триазоло[1,5-a]пиримидин-2-ил)сульфонил]бензамид;
этил 4-{[(4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензоил)амино]сульфонил}-5-метил-1,2-дифенил-1H-пиррол-3-карбоксилат;
метил 5-{[(4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензоил)амино]сульфонил}-1-метил-1H-пиррол-2-карбоксилат;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-{[5-(1,3-диметил-1H-пиразол-5-ил)изоксазол-4-ил]сульфонил}бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(4-хлор-3-метилизотиазол-5-ил)сульфонил]бензамид;
N-[(5-бром-3-метил-1-бензотиен-2-ил)сульфонил]-4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-({5-[(E)-2-(1,2,4-оксадиазол-3-ил)винил]тиен-2-ил}сульфонил)бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-{[1-(2-хлорэтил)-3,5-диметил-1H-пиразол-4-ил]сульфонил}бензамид;
5-{[(4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензоил)амино]сульфонил}-N-(1-этилпропил)-1,3,4-тиадиазол-2-карбоксамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(5-хлор-1,3-диметил-1H-пиразол-4-ил)сульфонил]бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(4-нитро-5-пиперидин-1-илтиен-2-ил)сульфонил]бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(5-изоксазол-5-ил-2-фурил)сульфонил]бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(3,5-диметилизоксазол-4-ил)сульфонил]бензамид;
4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-2-(1H-индол-5-илокси)-N-({4-нитро-5-[(3-пирролидин-1-илпропил)амино]тиен-2-ил}сульфонил)бензамид;
4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-[(5-{[3-(диметиламино)пропил]амино}-4-нитротиен-2-ил)сульфонил]-2-(1H-индол-5-илокси)бензамид;
4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-2-(1H-индол-5-илокси)-N-({5-[(3-морфолин-4-илпропил)амино]-4-нитротиен-2-ил}сульфонил)бензамид;
N-{[5-({(1R)-3-(диметиламино)-1-[(фенилтио)метил]пропил}амино)-4-нитротиен-2-ил]сульфонил}-4-{4-[2-(трифторметил)бензилиден]пиперидин-1-ил}бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метилен]пиперидин-1-ил}-N-[(1,1-диоксидотетрагидротиен-3-ил)сульфонил]бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метилен]пиперидин-1-ил}-N-[(5-хлор-3-метил-1-бензотиен-2-ил)сульфонил]бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(5-хлор-3-метил-1-бензотиен-2-ил)сульфонил]-2-феноксибензамид;
2-(3-хлорфенокси)-4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-Ν-[(5,7-диметил[1,2,4]триазоло[1,5-a]пиримидин-2-ил)сульфонил]бензамид;
4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-[(5,7-диметил[1,2,4]триазоло[1,5-a]пиримидин-2-ил)сульфонил]-2-[(6-фтор-1H-индол-5-ил)окси]бензамид;
4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-2-[(6,7-дифтор-1H-индол-5-ил)окси]-N-[(5,7-диметил[1,2,4]триазоло[1,5-a]пиримидин-2-ил)сульфонил]бензамид;
трет-бутил (2S)-2-{[(5-{[4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-2-(1H-пирроло[2,3-b]пиридин-5-илокси)бензоил]сульфамоил}-4-метил-1,3-тиазол-2-ил)окси]метил}морфолин-4-карбоксилат;
трет-бутил (2S)-2-{[(5-{[2-(1H-бензимидазол-4-илокси)-4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)бензоил]сульфамоил}-4-метил-1,3-тиазол-2-ил)окси]метил}морфолин-4-карбоксилат;
4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-({2-[(4-фтортетрагидро-2H-пиран-4-ил)метокси]-4-метил-1,3-тиазол-5-ил}сульфонил)-2-(1H-пирроло[2,3-b]пиридин-5-илокси)бензамид;
2-(1H-бензимидазол-4-илокси)-4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-({2-[(4-фтортетрагидро-2H-пиран-4-ил)метокси]-4-метил-1,3-тиазол-5-ил}сульфонил)бензамид;
трет-бутил (2S)-2-{[(5-{[4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-2-(1H-индазол-4-илокси)бензоил]сульфамоил}-4-метил-1,3-тиазол-2-ил)окси]метил}морфолин-4-карбоксилат;
4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-({2-[(4-фтортетрагидро-2H-пиран-4-ил)метокси]-4-метил-1,3-тиазол-5-ил}сульфонил)-2-(1H-индазол-4-илокси)бензамид;
и их терапевтически приемлемые соли, пролекарства, соли пролекарств и метаболиты.
Другой вариант осуществления настоящего изобретения касается композиции для лечения рака мочевого пузыря, рака мозга, рака молочной железы, рака костного мозга, рака шейной области, хронического лимфолейкоза, колоректального рака, рака пищевода, гепатоцеллюлярного рака, лимфобластного лейкоза, фолликулярной лимфомы, лимфолейкоза, вызываемого Т-лимфоцитами или В-клетками, меланомы, миелогенного лейкоза, миеломы, рака полости рта, рака яичников, немелкоклеточного рака легкого, рака простаты, мелкоклеточного рака легкого или рака селезенки, при этом указанная композиция включает инертный наполнитель и терапевтически эффективное количество соединения формулы (I).
Другой вариант осуществления настоящего изобретения касается способа лечения рака мочевого пузыря, рака мозга, рака молочной железы, рака костного мозга, рака шейной области, хронического лимфолейкоза, колоректального рака, рака пищевода, гепатоцеллюлярного рака, лимфобластного лейкоза, фолликулярной лимфомы, лимфолейкоза, вызываемого Т-лимфоцитами или В-клетками, меланомы, миелогенного лейкоза, миеломы, рака полости рта, рака яичников, немелкоклеточного рака легкого, хронического лимфолейкоза, миеломы, рака простаты, мелкоклеточного рака легкого или рака селезенки у пациента, включающий введение пациенту терапевтически эффективного количества соединения формулы (I).
Другой вариант осуществления настоящего изобретения касается способа лечения рака мочевого пузыря, рака мозга, рака молочной железы, рака костного мозга, рака шейной области, хронического лимфолейкоза, колоректального рака, рака пищевода, гепатоцеллюлярного рака, лимфобластного лейкоза, фолликулярной лимфомы, лимфолейкоза, вызываемого Т-лимфоцитами или В-клетками, меланомы, миелогенного лейкоза, миеломы, рака полости рта, рака яичников, немелкоклеточного рака легкого, хронического лимфолейкоза, миеломы, рака простаты, мелкоклеточного рака легкого или рака селезенки у пациента, включающий введение пациенту терапевтически эффективного количества соединения формулы (I) и терапевтически эффективного количества одного дополнительного терапевтического средства или более одного дополнительного терапевтического средства.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В данном описании переменные фрагменты представлены идентификаторами (заглавными буквами с числовыми и/или буквенными верхними индексами) и могут быть специально определены.
Следует понимать, что подходящие валентности выдержаны для всех фрагментов и их сочетаний и что одновалентные фрагменты, содержащие более одного атома, изображены слева направо и присоединены своими левыми концами, а двухвалентные фрагменты также изображены слева направо.
Следует также понимать, что конкретный вариант переменного фрагмента в данном описании может быть тем же самым или различным, как и другой конкретный вариант переменного фрагмента, имеющего тот же самый идентификатор.
Термин "алкенил" в данном описании означает прямую или разветвленную углеводородную цепь, содержащую от 2 до 10 атомов углерода, которая включает по меньшей мере одну двойную углерод-углеродную связь. Термин "Cx-Cyалкенил" означает прямую или разветвленную углеводородную цепь, имеющую по меньшей мере одну углерод-углеродную двойную связь и содержащую от x до y атомов углерода. Термин "C2-C4алкенил" означает алкенильную группу, содержащую 2-4 атома углерода. Отдельные примеры алкенила включают, однако этим не ограниваясь, бута-2,3-диенил, этенил, 2-пропенил, 2-метил-2-пропенил, 3-бутенил, 4-пентенил, 5-гексенил, 2-гептенил, 2-метил-1-гептенил и 3-деценил.
Термин "алкенилен" означает двухвалентную группу, полученную из углеводорода с прямой или разветвленной цепью, которая включает от 2 до 4 атомов углерода и содержит по меньшей мере одну двойную углерод-углеродную связь. Термин "Cx-Cyалкенилен" означает двухвалентную группу, полученную из прямой или разветвленной углеводородной цепи, содержащей по меньшей мере одну углерод-углеродную двойную связь и включающей от x до y атомов углерода. Отдельные примеры алкенилена включают, однако этим не ограниваясь, -CH=CH- и -CH2CH=CH-.
Термин "алкил" в данном описании означает прямую или разветвленную цепь насыщенного углеводорода, содержащую от 1 до 10 атомов углерода. Термин "Cх-Cyалкил" означает прямую или разветвленную цепь насыщенного углеводорода, содержащего от x до y атомов углерода. Например "C2-C10алкил" означает прямую или разветвленную цепь насыщенного углеводорода, содержащую от 2 до 10 атомов углерода. Примеры алкила включают, однако этим не ограниваясь, метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, изобутил, трет-бутил, н-пентил, изопентил, неопентил, н-гексил, 3-метилгексил, 2,2-диметилпентил, 2,3-диметилпентил, н-гептил, н-октил, н-нонил и н-децил.
Термин "алкилен" означает двухвалентную группу, полученную из прямой или разветвленной цепи насыщенного углеводорода, имеющую от 1 до 10 атомов углерода, например, от 1 до 4 атомов углерода. Термин "Cх-Cyалкилен" означает двухвалентную группу, полученную из прямой или разветвленной цепи насыщенного углеводорода, содержащую от x до y атомов углерода. Например "C2-C6алкилен" означает прямую или разветвленную цепь насыщенного углеводорода, содержащую от 2 до 6 атомов углерода. Примеры алкилена включают, однако этим не ограниваясь, -CH2-, -CH2CH2-, -CH2CH2CH2-, -CH2CH2CH2CH2- и -CH2CH(CH3)CH2-.
Термин "алкинил" в данном описании означает углеводородную группу с прямой или разветвленной цепью, содержащую от 2 до 10 атомов углерода и включающую по меньшей мере одну тройную углерод-углеродную связь. Термин "Cx-Cyалкинил" означает углеводородную группу с прямой или разветвленной цепью, содержащую от x до y атомов углерода. Отдельные примеры алкинила включают, однако этим не ограниваясь, ацетиленил, 1-пропинил, 2-пропинил, 3-бутинил, 2-пентинил и 1-бутинил.
Термин "алкинилен" в данном описании означает двухвалентный радикал, полученный из углеводородной группы с прямой или разветвленной цепью, содержащей от 2 до 10 атомов углерода и включающей по меньшей мере одну тройную углерод-углеродную связь.
Термин "арил" в данном описании означает фенил.
Термин "циклический фрагмент" в данном описании означает бензол, фенил, фенилен, циклоалкан, циклоалкил, циклоалкилен, циклоалкен, циклоалкенил, циклоалкенилен, циклоалкин, циклоалкинил, циклоалкинилен, гетероарен, гетероарил, гетероциклоалкан, гетероциклоалкил, гетероциклоалкен, гетероциклоалкенил и спироалкил.
Термин "циклоалкилен", или "циклоалкил", или "циклоалкан" в данном описании означает моноциклическую или мостиковую углеводородную кольцевую систему. Моноциклический циклоалкил представляет собой карбоциклическую кольцевую систему, содержащую от трех до восьми атомов углерода, ноль гетероатомов и ноль двойных связей. Примеры моноциклических кольцевых систем включают циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и циклооктил. Моноциклическое кольцо может содержать один или два алкиленовых мостика, каждый из которых включает один, два или три атома углерода и каждый из которых связывает два несмежных атома углерода кольцевой системы. Не ограничивающие настоящее изобретения примеры подобных мостиковых циклоалкильных кольцевых систем включают бицикло[3.1.1]гептан, бицикло[2.2.1]гептан, бицикло[2.2.2]октан, бицикло[3.2.2]нонан, бицикло[3.3.1]нонан, бицикло[4.2.1]нонан, трицикло[3.3.1.03,7]нонан (октагидро-2,5-метанопентален или норадамантан) и трицикло[3.3.1.13,7]декан (адамантан). Моноциклический и мостиковый циклоалкил может быть присоединен к фрагменту родительской молекулы посредством любого способного к замещению атома, имеющегося в циклической системе.
Термин "циклоалкенилен", или "циклоалкенил", или "циклоалкен" в данном описании означает кольцевую систему моноциклического или мостикового углеводорода. Моноциклический циклоалкенил имеет четыре, пять, шесть, семь или восемь атомов углерода и не содержит гетероатомов. Четырехчленные циклические системы имеют одну двойную связь, пяти- или шестичленные циклические системы имеют одну или две двойные связи, а семи- или восьмичленные циклические системы имеют одну, две или три двойные связи. Отдельные примеры моноциклических циклоалкенильных групп включают, однако этим не ограниваясь, циклобутенил, циклопентенил, циклогексенил, циклогептенил и циклооктенил. Моноциклическое циклоалкенильное кольцо может содержать один или два алкиленовых мостика, каждый из которых включает один, два или три атома углерода и каждый из которых связывает два несмежных атома углерода циклической системы. Отдельные примеры бициклических циклоалкенильных групп включают, однако этим не ограниваясь, 4,5,6,7-тетрагидро-3aH-инден, октагидронафталинил и 1,6-дигидропентален. Моноциклический и бициклический циклоалкенил может быть присоединен к фрагменту родительской молекулы посредством любого способного к замещению атома, имеющегося в циклических системах.
Термин "циклоалкин", или "циклоалкинил", или "циклоалкинилен" в данном описании означает кольцевую систему моноциклического или мостикового углеводорода. Моноциклический циклоалкинил содержит восемь или более атомов углерода, не содержит гетероатомов и включает одну или более тройных связей. Моноциклическое циклоалкинильное кольцо может содержать один или два алкиленовых мостика, каждый из которых включает один, два или три атома углерода и каждый из которых связывает два несмежных атома углерода циклической системы. Моноциклический и мостиковый циклоалкинил может быть присоединен к фрагменту родительской молекулы посредством любого способного к замещению атома, имеющегося в циклических системах.
Термин "гетероарен", или "гетероарил", или "гетероарилен" в данном описании означает пятичленное или шестичленное ароматическое ядро, имеющее по меньшей мере один атом углерода и один или более чем один независимо выбранных атомов азота, кислорода или серы. Гетероарены по настоящему изобретению соединены посредством любого смежного атома в кольце при условии, что выполняются требования валентности. Отдельные примеры гетероарила включают, однако этим не ограниваясь, фуранил (включая, однако этим не ограниваясь, фуран-2-ил), имидазолил (включая, однако этим не ограниваясь, 1H-имидазол-1-ил), изоксазолил, изотиазолил, оксадиазолил, оксазолил, пиридинил (например, пиридин-4-ил, пиридин-2-ил, пиридин-3-ил), пиридазинил, пиримидинил, пиразинил, пиразолил, пирролил, тетразолил, тиадиазолил, тиазолил, тиенил (включая, однако этим не ограниваясь, тиен-2-ил, тиен-3-ил), триазолил и триазинил.
Термин "гетероциклоалкан", или "гетероциклоалкил", или "гетероциклоалкилен" в данном описании означает моноциклический или мостиковый трех-, четырех-, пяти-, шести-, семи- или восьмичленный цикл, содержащий по меньшей мере один гетероатом, независимо выбранный из группы, включающей O, N и S, и не содержащий двойные связи. Моноциклический и мостиковый гетероциклоалкан может быть присоединен к фрагменту родительской молекулы посредством любого способного к замещению атома углерода или любого способного к замещению атома азота, имеющегося в циклической системе. Гетероатомы азота и серы в гетероциклических ядрах необязательно могут быть окислены, а атомы азота необязательно могут быть четвертичными. Отдельные примеры гетероциклоалкановых групп включают, однако этим не ограниваясь, морфолинил, тетрагидропиранил, пирролидинил, пиперидинил, диоксоланил, тетрагидрофуранил, тиоморфолинил, диоксанил, тетрагидротиенил, тетрагидротиопиранил, оксэтанил, пиперазинил, имидазолидинил, азетидин, азепанил, азиридинил, диазепанил, дитиоланил, дитианил, изоксазолидинил, изотиазолидинил, оксадиазолидинил, оксазолидинил, пиразолидинил, тетрагидротиенил, тиадиазолидинил, тиазолидинил, тиоморфолинил и тритианил.
Термин "гетероциклоалкен", или "гетероциклоалкенил", или "гетероциклоалкенилен" в данном описании означает моноциклический или мостиковый трех-, четырех-, пяти-, шести-, семи- или восьмичленный цикл, содержащий по меньшей мере один гетероатом, независимо выбранный из группы, включающей O, N и S, и содержащий одну или более двойных связей. Моноциклический и мостиковый гетероциклоалкен может быть присоединен к фрагменту родительской молекулы посредством любого способного к замещению атома углерода или любого способного к замещению атома азота, имеющегося в циклической системе. Гетероатомы азота и серы в гетероциклических ядрах необязательно могут быть окислены, а атомы азота необязательно могут быть четвертичными. Отдельные примеры гетероциклоалкеновых групп включают, однако этим не ограниваясь, тетрагидрооксоцинил, 1,4,5,6-тетрагидропиридазинил, 1,2,3,6-тетрагидропиридинил, дигидропиранил, имидазолинил, изотиазолинил, оксадиазолинил, изоксазолинил, оксазолинил, пиранил, пиразолинил, пирролинил, тиадиазолинил, тиазолинил, дигидро-1,3,4-тиадиазол-2-ил и тиопиранил.
Термин "фенилен" в данном описании означает двухвалентный радикал, образованный путем удаления атома водорода из фенила.
Термин "спироалкил" в данном описании означает алкилен, оба конца которого присоединены к одному и тому же атому углерода, примером которого являются С2-спироалкил, С3-спироалкил, С4-спироалкил, С5-спироалкил, С6-спироалкил, С7-спироалкил, С8-спироалкил, С9-спироалкил и т.п.
Термин "спирогетероалкил" в данном описании означает спироалкил, в котором один или два фрагмента СН2 заменены независимо выбранными O, C(O), CNOH, CNOCH3, S, S(O), SO2 или NH и один или два фрагмента CH не замещены или замещены N.
Термин "спирогетероалкенил" в данном описании означает спироалкенил, у которого один или два фрагмента СН2 заменены независимо выбранными O, C(O), CNOH, CNOCH3, S, S(O), SO2 или NH и один или два фрагмента CH не заменены или заменены N, а также означает спироалкенил, у которого один или два фрагмента СН2 не заменены или заменены независимо выбранными O, C(O), CNOH, CNOCH3, S, S(O), SO2 или NH и один или два фрагмента CH заменены N.
Термин "спироцикло" в данном описании означает два заместителя при одном и том же атоме углерода, которые вместе с атомом углерода, к которому они присоединены, образуют циклоалкановое, гетероциклоалкановое, циклоалкеновое или гетероциклоалкеновое ядро.
Термин "C2-C5спироалкил" в данном описании означает C2-спироалкил, C3-спироалкил, C4-спироалкил и C5-спироалкил.
Термин "C2-спироалкил" в данном описании означает эт-1,2-илен, оба конца которого замещают атомы водорода одного и того же фрагмента СН2.
Термин "C3-спироалкил" в данном описании означает проп-1,3-илен, оба конца которого замещают атомы водорода одного и того же фрагмента СН2.
Термин "C4-спироалкил" в данном описании означает бут-1,4-илен, оба конца которого замещают атомы водорода одного и того же фрагмента СН2.
Термин "C5-спироалкил" в данном описании означает пент-1,5-илен, оба конца которого замещают атомы водорода одного и того же фрагмента СН2.
Термин "C6-спироалкил" в данном описании означает гекс-1,6-илен, оба конца которого замещают атомы водорода одного и того же фрагмента СН2.
Термин "NH защитная группа" в данном описании означает трихлорэтоксикарбонил, трибромэтоксикарбонил, бензилоксикарбонил, пара-нитробензилкарбонил, орто-бромбензилоксикарбонил, хлорацетил, дихлорацетил, трихлорацетил, трифторацетил, фенилацетил, формил, ацетил, бензоил, трет-амилоксикарбонил, трет-бутоксикарбонил, пара-метоксибензилоксикарбонил, 3,4-диметоксибензилоксикарбонил, 4-(фенилазо)бензилоксикарбонил, 2-фурфурилоксикарбонил, дифенилметоксикарбонил, 1,1-диметилпропоксикарбонил, изопропоксикарбонил, фталоил, сукцинил, аланил, лейцил, 1-адамантилоксикарбонил, 8-хинолилоксикарбонил, бензил, дифенилметил, трифенилметил, 2-нитрофенилтио, метансульфонил, пара-толуолсульфонил, N,N-диметиламинометилен, бензилиден, 2-гидроксибензилиден, 2-гидрокси-5-хлорбензилиден, 2-гидрокси-1-нафтилметилен, 3-гидрокси-4-пиридилметилен, циклогексилиден, 2-этоксикарбонилциклогексилиден, 2-этоксикарбонилциклопентилиден, 2-ацетилциклогексилиден, 3,3-диметил-5-оксициклогексилиден, дифенилфосфорил, дибензилфосфорил, 5-метил-2-оксо-2H-1,3-диоксол-4-илметил, триметилсилил, триэтилсилил и трифенилсилил.
Термин "C(O)ОН защитная группа" в данном описании означает метил, этил, н-пропил, изопропил, 1,1-диметилпропил, н-бутил, трет-бутил, фенил, нафтил, бензил, дифенилметил, трифенилметил, пара-нитробензил, пара-метоксибензил, бис(пара-метоксифенил)метил, ацетилметил, бензоилметил, пара-нитробензоилметил, пара-бромбензоилметил, пара-метансульфонилбензоилметил, 2-тетрагидропиранил, 2-тетрагидрофуранил, 2,2,2-трихлорэтил, 2-(триметилсилил)этил, ацетоксиметил, пропионилоксиметил, пивалоилоксиметил, фталимидометил, сукцинимидометил, циклопропил, циклобутил, циклопентил, циклогексил, метоксиметил, метоксиэтоксиметил, 2-(триметилсилил)этоксиметил, бензилоксиметил, метилтиометил, 2-метилтиоэтил, фенилтиометил, 1,1-диметил-2-пропенил, 3-метил-3-бутенил, аллил, триметилсилил, триэтилсилил, триизопропилсилил, диэтилизопропилсилил, трет-бутилдиметилсилил, трет-бутилдифенилсилил, дифенилметилсилил и трет-бутилметоксифенилсилил.
Термин "ОН или SH защитная группа" в данном описании означает бензилоксикарбонил, 4-нитробензилоксикарбонил, 4-бромбензилоксикарбонил, 4-метоксибензилоксикарбонил, 3,4-диметоксибензилоксикарбонил, метоксикарбонил, этоксикарбонил, трет-бутоксикарбонил, 1,1-диметилпропоксикарбонил, изопропоксикарбонил, изобутоксикарбонил, дифенилметоксикарбонил, 2,2,2-трихлорэтоксикарбонил, 2,2,2-трибромэтоксикарбонил, 2-(триметилсилил)этоксикарбонил, 2-(фенилсульфонил)этоксикарбонил, 2-(трифенилфосфонио)этоксикарбонил, 2-фурфурилоксикарбонил, 1-адамантилоксикарбонил, винилоксикарбонил, аллилоксикарбонил, S-бензилтиокарбонил, 4-этокси-1-нафтилоксикарбонил, 8-хинолилоксикарбонил, ацетил, формил, хлорацетил, дихлорацетил, трихлорацетил, трифторацетил, метоксиацетил, феноксиацетил, пивалоил, бензоил, метил, трет-бутил, 2,2,2-трихлорэтил, 2-триметилсилилэтил, 1,1-диметил-2-пропенил, 3-метил-3-бутенил, аллил, бензил (фенилметил), пара-метоксибензил, 3,4-диметоксибензил, дифенилметил, трифенилметил, тетрагидрофурил, тетрагидропиранил, тетрагидротиопиранил, метоксиметил, метилтиометил, бензилоксиметил, 2-метоксиэтоксиметил, 2,2,2-трихлорэтоксиметил, 2-(триметилсилил)этоксиметил, 1-этоксиэтил, метансульфонил, пара-толуолсульфонил, триметилсилил, триэтилсилил, триизопропилсилил, диэтилизопропилсилил, трет-бутилдиметилсилил, трет-бутилдифенилсилил, дифенилметилсилил и трет-бутилметоксифенилсилил.
Соединения
У соединений по настоящему изобретению могут быть геометрические изомеры. Соединения по настоящему изобретению могут содержать двойные углерод-углеродные связи или двойные углерод-азотные связи в E- или Z-конфигурации, где термин "E" представляет собой заместители более высокого порядка с противоположных сторон двойной углерод-углеродной или углерод-азотной связи, а термин "Z" представляет собой заместители более высокого порядка на той же самой стороне относительно двойной углерод-углеродной или углерод-азотной связи, как определяют в соответствии правилами приоритета Кана-Ингольда-Прелога. Соединения по настоящему изобретению могут также существовать в виде смеси "E" и "Z" изомеров. Заместители в циклоалкиле или гетероциклоалкиле определяют как имеющие цис- или транс-конфигурацию. Кроме того, в настоящем изобретении рассматриваются различные изомеры и их смеси, образующиеся при размещении заместителей в циклической системе адамантана. Два заместителя в одном цикле адамантанового ядра определяются как имеющие относительную конфигурацию Z или E. Примеры см. в C.D. Jones, M. Kaselj, R.N. Salvatore, W.J. le Noble, J. Org. Chem. 1998, 63, 2758-2760 и E.L. Eliel and S.H. Wilen. (1994) Stereochemistry of Organic Compounds. New York, NY: John Wiley & Sons, Inc.
Соединения по настоящему изобретению могут содержать асимметрично замещенные атомы углерода в R- или S-конфигурации, где термины "R" и "S" определены в соответствии с рекомендациями IUPAC 1974 в разделе E, Фундаментальная Стереохимия, Pure Appl. Chem. (1976) 45, 13-10. Соединения, имеющие равные количества асимметрично замещенных атомов углерода с R- и S-конфигураций, являются рацемическими по указанным атомам углерода. Атомы с избытком одной конфигурации по сравнению с другой определяют конфигурацию, которая присутствует в болеем количестве, предпочтительно, в избытке, составляющем приблизительно 85-90%, более предпочтительно, в избытке, составляющем приблизительно 95-99%, и еще более предпочтительно, в избытке, составляющем более чем приблизительно 99%. Таким образом, настоящее изобретение включает рацемические смеси, относительные и абсолютные стереоизомеры и смеси относительных и абсолютных стереоизомеров.
В соединениях по настоящему изобретению, содержащих фрагменты NH, C(O)ОН, ОН или SH, к указанным фрагментам могут быть присоединены фрагменты, образующие пролекарство. Образующие пролекарство фрагменты удаляются в процессе метаболических процессов и в условиях in vivo высвобождают соединения, содержащие освобожденный гидроксил, аминогруппу или карбоновую кислоту. Пролекарства пригодны для регулирования таких фармакокинетических свойств соединений, как растворимость и/или гидрофобность, абсорбция в желудочно-кишечном тракте, биодоступность, способность проникать в ткани и скорость выведения из организма.
Изотопно обогащенные соединения или соединения, содержащие метки
Соединения по настоящему изобретению могут содержать изотопные метки или могут существовать в изотопно обогащенной форме, содержащей один или несколько атомов, атомная масса или массовое число которых отличается от атомной массы или массового числа наиболее распространенных в природе. Изотопы могут быть радиоактивными или не радиоактивными изотопами. Изотопы атомов, таких как водород, углерод, фосфор, сера, фтор, хлор и иод, включают, однако этим не ограниваясь, 2H, 3H, 13C, 14C, 15N, 18О, 32P, 35S, 18F, 36Cl и 125I. Соединения, которые содержат другие изотопы указанных и/или других атомов, входят в объем настоящего изобретения.
В другом варианте осуществления настоящего изобретения меченные изотопом соединения содержат изотопы дейтерий (2H), тритий (3H) или 14C. Меченные изотопом соединения по настоящему изобретению могут быть получены общими способами, известными обычным специалистам из области техники. Подобные меченные изотопом соединения удобно получать по методикам, изложенным в приведенных в данном описании примерах и схемах, заменив не содержащий метку реагент на легко доступный меченный изотопом реагент. В некоторых случаях соединения можно подвергнуть обработке содержащими изотопную метку реагентами с тем, чтобы обменять атом на его изотоп, например, атом водорода на дейтерий можно обменять действием дейтерированной кислоты, такой как D2SO4/D2O. В дополнение к вышесказанному, соответствующие методики и промежуточные соединения раскрыты, например, в Lizondo, J. et al., Drugs Fut., 21(11), 1116 (1996); Brickner, S.J. et al., J. Med. Chem., 39(3), 673 (1996); Mallesham, B. et al., Org. Lett., 5(7), 963 (2003); PCT публикациях WO 1997/010223, WO 2005/099353, WO 1995/007271, WO 2006/008754; в патентах США № 7538189; 7534814; 7531685; 7528131; 7521421; 7514068; 7511013; и опубликованных заявках на патент США № 2009/0137457; 2009/0131485; 2009/0131363; 2009/0118238; 2009/0111840; 2009/0105338; 2009/0105307; 2009/0105147; 2009/0093422; 2009/0088416 и 20090082471, и указанные способы включены в данное описание посредством ссылки.
Меченные изотопом соединения по настоящему изобретению могут использоваться в качестве стандартов, с целью определения эффективности ингибиторов Bcl-2 в анализах на связывание. Содержащие изотоп соединения используют при проведении фармацевтических исследований для in vivo исследования дальнейшей судьбы соединений в процессе метаболизма, чтобы оценить механизм действия и метаболический путь не содержащего метку родительского соединения (Blake et al. J. Pharm. Sci. 64, 3, 367-391 (1975)). Подобные исследования метаболизма важны при разработке безопасных эффективных терапевтических препаратов, поскольку в условиях in vivo как активные соединения, введенные пациенту, так и метаболиты, образовавшиеся из родительского соединения, оказываются токсичными или канцерогенными (Foster et al., Advances in Drug Research Vol. 14, pp. 2-36, Academic press, London, 1985; Kato et al., J. Labelled Comp. Radiopharmaceut., 36(10):927-932 (1995); Kushner et al., Can. J. Physiol. Pharmacol., 77, 79-88 (1999).
Кроме того, лекарственные средства, содержащие не радиоактивный изотоп, такие как дейтерийсодержащие лекарственные средства, которые называют "тяжелыми лекарственными средствами", могут использоваться для лечения заболеваний и состояний, связанных с активностью Bcl-2. Увеличение количества присутствующего в соединении изотопа сверх его естественного распространения в природе называют обогащением. Примеры величины обогащения включают от приблизительно 0,5, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 12, 16, 21, 25, 29, 33, 37, 42, 46, 50, 54, 58, 63, 67, 71, 75, 79, 84, 88, 92, 96 до приблизительно 100% мол. Замена вплоть до приблизительно 15% обычного атома тяжелым изотопом у млекопитающих, включая грызунов и собак, производится и поддерживается на период от нескольких дней до нескольких недель, вызывая минимальные наблюдаемые неблагоприятные эффекты (Czajka D.M. and Finkel A.J., Ann. N.Y. Acad. Sci. 1960 84: 770; Thomson J.F., Ann. New York Acad. Sci., 1960 84: 736; Czakja D.M. et al., Am. J. Physiol. 1961 201: 357). Было показано, что однократная замена у человека вплоть до 15-23% на жидкости с дейтерием не вызывает токсичность (Blagojevic N. et al. "Dosimetry & Treatment Planning for Neutron Capture Therapy", Zamenhof R., Solares G. and Harling O. Eds. 1994. Advanced Medical Publishing, Madison Wis. pp.125-134; Diabetes Metab. 23: 251 (1997)).
Введение меток стабильных изотопов в лекарственное средство может изменить его физико-химические свойства, такие как величина pKa и растворимость в липидах. Указанные эффекты и изменения могут вызывать фармакодинамическую реакцию молекулы лекарственного средства, если изотопное замещение воздействует на область, вовлекаемую во взаимодействие лиганда с рецептором. Несмотря на то, что некоторые из физических свойств меченной стабильным изотопом молекулы отличаются от не содержащей метку молекулы, их химические и биологические свойства те же самые, за одним важным исключением: вследствие увеличенной массы тяжелого изотопа, любое связывание с участием тяжелого изотопа с другим атомом будет прочнее, чем та же связь между легким изотопом и указанным атомом. Таким образом, включение изотопа в то место, которое связано с обменом веществ или ферментативным превращением, замедляет подобные реакции и потенциально изменяет фармакокинетический профиль или эффективность соединения, по сравнению с не содержащим изотоп соединением.
Амиды, сложные эфиры и пролекарства
Пролекарства представляют собой производные соединения активного лекарственного средства, которые разрабатывают с целью улучшить некоторые идентифицированные нежелательные физические или биологические свойства. Физическими свойствами, как правило, являются растворимость (слишком большая или недостаточная растворимость в липидах или в воде) или соответствующая стабильность, в то время как проблемные биологические свойства включают слишком быстрый метаболизм или недостаточную биодоступность, которая, в свою очередь, может быть связана с физико-химическими свойствами.
Пролекарства обычно получают a) образованием сложных эфиров, неполных сложных эфиров, эфиров угольной кислоты, нитроэфиров, амидов, производных гидроксамовых кислот, карбаматов, иминов, оснований Манниха, фосфатов, фосфатных сложных эфиров и энаминов активного лекарственного средства, b) функционализацией лекарственного средства с применением азо, гликозидных, пептидных функциональных групп и функциональные групп простых эфиров, c) за счет использования аминальных, гемиаминальных, полимерных, солевых, комплексных, фосфорамидных, ацетальных, полуацетальных и кетальных форм лекарственного средства. Примеры можно найти в документе Andrejus Korolkovas's, "Essentials of Medicinal Chemistry", John Wiley-Interscience Publications, John Wiley and Sons, New York (1988), pp. 97-118, который целиком включен в настоящее описание посредством ссылки.
Сложные эфиры можно получить из исходных соединений формулы (I), содержащих либо гидроксильную группу, либо карбоксильную группу, используя общие способы, известные специалистам. Типичные реакции указанных соединений представляют собой реакции замещения с заменой одного из гетероатомов другим атомом, например:
Схема 1

Амиды можно получить аналогичным образом из исходных соединений формулы (I), содержащих либо аминогруппу, либо карбоксильную группу. Сложные эфиры также могут взаимодействовать с аминами или аммиаком с образованием амидов:
Схема 2
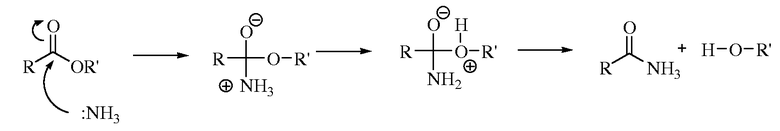
Другой путь получения амидов из соединений формулы (I) заключается в совместном нагревании карбоновых кислот и аминов.
Схема 3
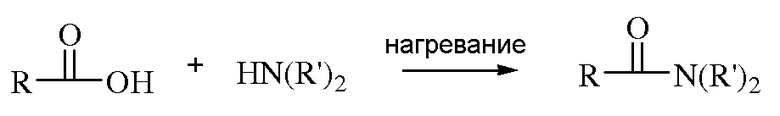
На приведенных выше схемах 2 и 3, R и R' независимо обозначают субстрат формулы (I), алкил или атом водорода.
Соответствующие группы для A1, L1, Z1A, Z2A, Z1, Z2 и Z3 в соединениях формулы (I) выбраны независимо. Приведенные варианты осуществления настоящего изобретения можно комбинировать. Подобная комбинация предусматривается и входит в объем настоящего изобретения. Например, предполагается, что варианты для любого из A1, L1, Z1A, Z2A, Z1, Z2 и Z3 можно комбинировать с вариантами, определенными для любых других из A1, L1, Z1A, Z2A, Z1, Z2 и Z3.
Один вариант осуществления настоящего изобретения касается соединений или их терапевтически приемлемых солей, пролекарств, метаболитов или солей пролекарств, которые пригодны в качестве ингибиторов антиапоптотических белков Bcl-2, при этом соединения имеют формулу (I):
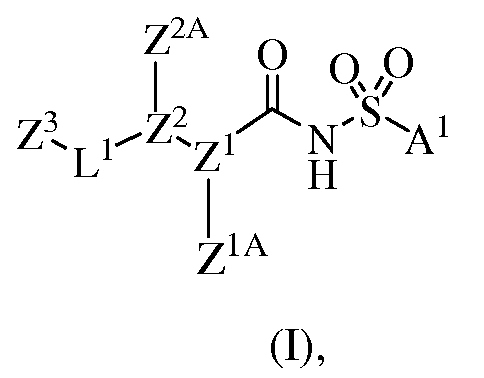
где
A1 представляет собой фурил, имидазолил, изотиазолил, изоксазолил, оксадиазолил, оксазолил, пиразинил, пиразолил, пиридазинил, 2-пиридинил, 4-пиридинил, пиримидинил, пирролил, тетразолил, тиазолил, тиадиазолил, тиенил, триазинил, триазолил, циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил; каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или A1A; A1A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
где A1 не замещен или замещен одним, или двумя, или тремя, или четырьмя, или пятью независимо выбранными заместителями R1, OR1, SR1, S(O)R1, SO2R1, C(O)R1, C(O)OR1, OC(O)R1, NHR1, N(R1)2, C(N)C(O)R1, C(O)NHR1, C(O)N(R1)2, C(O)NHOH, C(O)NHOR1, C(O)NHSO2R1, NHC(O)R1, NR1C(O)R1, NHC(O)OR1, NR1C(O)OR1, NR1C(O)NHR1, NR1C(O)N(R1)2, NHC(O)NH2, NHC(O)NHR1, NHC(O)N(R1)2, SO2NH2, SO2NHR1, SO2N(R1)2, NHS(O)R1, NHSO2R1, NR1SO2R1, NHSO2NHR1, N(CH3)SO2N(CH3)R1, (O), NH2, NO2, N3, OH, F, Cl, Br, I, CN, CF3, OCF3, CF2CF3, OCF2CF3, C(O)H, C(O)OH, C(N)NH2, C(N)NHR1, C(N)N(R1)2, CNOH, CNOCH3, C(O)NH2 или C(O)OR1A;
R1 представляет собой R2, R3, R4 или R5;
R1A представляет собой циклоалкил, циклоалкенил или циклоалкинил;
R2 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R2A; R2A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R3 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R3A; R3A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R4 представляет собой циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R4A; R4A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R5 представляет собой алкил, алкенил, или алкинил, каждый из которых не замещен или замещен одним, или двумя, или тремя независимо выбранными заместителями R6, NC(R6A)(R6B), R7, OR7, SR7, S(O)R7, SO2R7, NHR7, N(R7)2, C(O)R7, C(O)NH2, C(O)NHR7, C(O)N(R7)2, NHC(O)R7, NR7C(O)R7, NHSO2R7, NHC(O)OR7, SO2NH2, SO2NHR7, SO2N(R7)2, NHC(O)NH2, NHC(O)NHR7, NHC(O)CH(CH3)NHC(O)CH(CH3)NH2, NHC(O)CH(CH3)NHC(O)CH(CH3)NHR1, OH, (O), C(O)OH, N3, CN, NH2, CF3, CF2CF3, F, Cl, Br или I;
R6 представляет собой C2-C5-спироалкил, каждый из которых не замещен или замещен заместителями OH, (O), N3, CN, CF3, CF2CF3, F, Cl, Br, I, NH2, NH(CH3) или N(CH3)2;
R6A и R6B независимо выбраны из алкила или вместе с атомом N, к которому они присоединены, образуют R6C;
R6C представляет собой азиридин-1-ил, азетидин-1-ил, пирролидин-1-ил или пиперидин-1-ил, каждый из которых имеет один фрагмент CH2, не замененный или замененный O, C(O), CNOH, CNOCH3, S, S(O), SO2 или NH;
R7 представляет собой R8, R9, R10 или R11;
R8 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R8A; R8A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R9 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R9A; R9A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R10 представляет собой циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R10A; R10A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R11 представляет собой алкил, алкенил или алкинил, каждый из которых не замещен или замещен одним, или двумя, или тремя независимо выбранными заместителями R12, OR12, SR12, S(O)R12, SO2R12, C(O)R12, C(O)OR12, OC(O)R12, OC(O)OR12, NH2, NHR12, N(R12)2, NHC(O)R12, NR12C(O)R12, NHS(O)2R12, NR12S(O)2R12, NHC(O)OR12, NR12C(O)OR12, NHC(O)NH2, NHC(O)NHR12, NHC(O)N(R12)2, NR12C(O)NHR12, NR12C(O)N(R12)2, C(O)NH2, C(O)NHR12, C(O)N(R12)2, C(O)NHOH, C(O)NHOR12, C(O)NHSO2R12, C(O)NR12SO2R12, SO2NH2, SO2NHR12, SO2N(R12)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR12, C(N)N(R12)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R12 представляет собой R13, R14, R15 или R16;
R13 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R13A; R13A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R14 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R14A; R14A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R15 представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R15A; R15A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R16 представляет собой алкил, алкенил или алкинил;
Z1 представляет собой R26 или R27;
Z2 представляет собой R28, R29 или R30;
Z1A и Z2A, оба, отсутствуют или вместе образуют CH2, CH2CH2 или Z12A;
Z12A представляет собой C2-C6-алкен, в котором один или два фрагмента CH2 заменены NH, N(CH3), S, S(O) или SO2;
L1 представляет собой R37, OR37, SR37, S(O)R37, SO2R37, C(O)R37, C(O)OR37, OC(O)R37, OC(O)OR37, NHR37, C(O)NH, C(O)NR37, C(O)NHOR37, C(O)NHSO2R37, SO2NH, SO2NHR37, C(N)NH, C(N)NHR37;
R26 представляет собой фенилен, который не конденсирован или конденсирован с бензолом, или гетероареном, или R26A; R26A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R27 представляет собой гетероарилен, который не конденсирован или конденсирован с бензолом, или гетероареном, или R27A; R27A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R28 представляет собой фенилен, который не конденсирован или конденсирован с бензолом, гетероареном или R28A; R28A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R29 представляет собой гетероарилен, который не конденсирован или конденсирован с бензолом, или гетероареном, или R29A; R29A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R30 представляет собой циклоалкилен, циклоалкенилен, гетероциклоалкилен или гетероциклоалкенилен, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R30A; R30A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R37 представляет собой простую связь или R37A;
R37A представляет собой алкилен, алкенилен или алкинилен, каждый из которых не замещен или замещен одним, или двумя, или тремя независимо выбранными заместителями R37B, OR37B, SR37B, S(O)R37B SO2R37B, C(O)R37B, C(O)OR37B, OC(O)R37B, OC(O)OR37B, NH2, NHR37B, N(R37B)2, NHC(O)R37B, NR37BC(O)R37B, NHS(O)2R37B, NR37BS(O)2R37B, NHC(O)OR37B, NR37BC(O)OR37B, NHC(O)NH2, NHC(O)NHR37B, NHC(O)N(R37B)2, NR37BC(O)NHR37B, NR37BC(O)N(R37B)2, C(O)NH2, C(O)NHR37B, C(O)N(R37B)2, C(O)NHOH, C(O)NHOR37B, C(O)NHSO2R37B, C(O)NR37BSO2R37B, SO2NH2, SO2NHR37B, SO2N(R37B)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR37B, C(N)N(R37B)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R37B представляет собой алкил, алкенил, алкинил, фенил, гетероарил, циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил;
Z3 представляет собой R38, R39 или R40;
R38 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R38A; R38A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R39 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R39A; R39A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R40 представляет собой циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R40A; R40A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
где фрагменты, представленные группами R26 и R27, не замещены или замещены (т.е. если Z1A и Z2A отсутствуют) или дополнительно не замещены или дополнительно замещены (т.е. если Z1A и Z2A присутствуют) одним или несколькими заместителями R41, OR41, SR41, S(O)R41, SO2R41, C(O)R41, C(O)OR41, OC(O)R41, OC(O)OR41, NH2, NHR41, N(R41)2, NHC(O)R41, NR41C(O)R41, NHS(O)2R41, NR41S(O)2R41, NHC(O)OR41, NR41C(O)OR41, NHC(O)NH2, NHC(O)NHR41, NHC(O)N(R41)2, NR41C(O)NHR41, NR41C(O)N(R41)2, C(O)NH2, C(O)NHR41, C(O)N(R41)2, C(O)NHOH, C(O)NHOR41, C(O)NHSO2R41, C(O)NR41SO2R41, SO2NH2, SO2NHR41, SO2N(R41)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR41, C(N)N(R41)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R41 представляет собой R42, R43, R44 или R45;
R42 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R42A; R42A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R43 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R43A; R43A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R44 представляет собой циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R44A; R44A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R45 представляет собой алкил, алкенил или алкинил, каждый из которых не замещен или замещен одним или двумя независимо выбранными заместителями R46, OR46, SR46, S(O)R46, SO2R46, C(O)R46, C(O)OR46, OC(O)R46, OC(O)OR46, NH2, NHR46, N(R46)2, NHC(O)R46, NR46C(O)R46, NHS(O)2R46, NR46S(O)2R46, NHC(O)OR46, NR46C(O)OR46, NHC(O)NH2, NHC(O)NHR46, NHC(O)N(R46)2, NR46C(O)NHR46, NR46C(O)N(R46)2, C(O)NH2, C(O)NHR46, C(O)N(R46)2, C(O)NHOH, C(O)NHOR46, C(O)NHSO2R46, C(O)NR46SO2R46, SO2NH2, SO2NHR46, SO2N(R46)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR46, C(N)N(R46)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R46 представляет собой алкил, алкенил или алкинил, R47, R48 или R49;
R47 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R47A; R47A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R48 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R48A; R48A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R49 представляет собой циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R49A; R49A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
где фрагменты, представленные группами R42, R43, R44, R47, R48 и R49, независимо не замещены или замещены одним или несколькими независимо выбранными заместителями R50, OR50, SR50, S(O)R50, SO2R50, C(O)R50, C(O)OR50, OC(O)R50, OC(O)OR50, NH2, NHR50, N(R50)2, NHC(O)R50, NR50C(O)R50, NHS(O)2R50, NR50S(O)2R50, NHC(O)OR50, NR50C(O)OR50, NHC(O)NH2, NHC(O)NHR50, NHC(O)N(R50)2, NR50C(O)NHR50, NR50C(O)N(R50)2, C(O)NH2, C(O)NHR50, C(O)N(R50)2, C(O)NHOH, C(O)NHOR50, C(O)NHSO2R50, C(O)NR50SO2R50, SO2NH2, SO2NHR50, SO2N(R50)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR50, C(N)N(R50)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R50 представляет собой R51, R52, R53 или R54;
R51 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R51A; R51A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R52 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R52A; R52A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R53 представляет собой циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R53A; R53A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R54 представляет собой алкил, алкенил или алкинил, каждый из которых не замещен или замещен одним, или двумя, или тремя независимо выбранными заместителями R55, OR55, SR55, S(O)R55, SO2R55, C(O)R55, C(O)OR55, OC(O)R55, OC(O)OR55, NH2, NHR55, N(R55)2, NHC(O)R55, NR55C(O)R55, NHS(O)2R55, NR55S(O)2R55, NHC(O)OR55, NR55C(O)OR55, NHC(O)NH2, NHC(O)NHR55, NHC(O)N(R55)2, NR55C(O)NHR55, NR55C(O)N(R55)2, C(O)NH2, C(O)NHR55, C(O)N(R55)2, C(O)NHOH, C(O)NHOR55, C(O)NHSO2R55, C(O)NR55SO2R55, SO2NH2, SO2NHR55, SO2N(R55)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR55, C(N)N(R55)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R55 представляет собой алкил, алкенил, алкинил, фенил, гетероарил, циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил;
где каждый вышеуказанный циклический фрагмент независимо не замещен, дополнительно не замещен, замещен или дополнительно замещен одним или несколькими независимо выбранными заместителями R57, OR57, SR57, S(O)R57, SO2R57, C(O)R57, C(O)OR57, OC(O)R57, OC(O)OR57, NH2, NHR57, N(R57)2, NHC(O)R57, NR57C(O)R57, NHS(O)2R57, NR57S(O)2R57, NHC(O)OR57, NR57C(O)OR57, NHC(O)NH2, NHC(O)NHR57, NHC(O)N(R57)2, NR57C(O)NHR57, NR57C(O)N(R57)2, C(O)NH2, C(O)NHR57, C(O)N(R57)2, C(O)NHOH, C(O)NHOR57, C(O)NHSO2R57, C(O)NR57SO2R57, SO2NH2, SO2NHR57, SO2N(R57)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR57, C(N)N(R57)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R57 представляет собой R58, R59, R60 или R61;
R58 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R58A; R58A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R59 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R59A; R59A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R60 представляет собой циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R60A; R60A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R61 представляет собой алкил, алкенил или алкинил, каждый из которых не замещен или замещен одним, или двумя, или тремя независимо выбранными заместителями R62, OR62, SR62, S(O)R62, SO2R62, C(O)R62, C(O)OR62, OC(O)R62, OC(O)OR62, NH2, NHR62, N(R62)2, NHC(O)R62, NR62C(O)R62, NHS(O)2R62, NR62S(O)2R62, NHC(O)OR62, NR62C(O)OR62, NHC(O)NH2, NHC(O)NHR62, NHC(O)N(R62)2, NR62C(O)NHR62, NR62C(O)N(R62)2, C(O)NH2, C(O)NHR62, C(O)N(R62)2, C(O)NHOH, C(O)NHOR62, C(O)NHSO2R62, C(O)NR62SO2R62, SO2NH2, SO2NHR62, SO2N(R62)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR62, C(N)N(R62)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R62 представляет собой R63, R64, R65 или R66;
R63 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R63A; R63A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R64 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R64A; R64A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R65 представляет собой циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R65A; R65A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R66 представляет собой алкил, алкенил или алкинил, каждый из которых не замещен или замещен одним, или двумя, или тремя независимо выбранными заместителями R67, OR67, SR67, S(O)R67, SO2R67, C(O)R67, C(O)OR67, OC(O)R67, OC(O)OR67, NH2, NHR67, N(R67)2, NHC(O)R67, NR67C(O)R67, NHS(O)2R67, NR67S(O)2R67, NHC(O)OR67, NR67C(O)OR67, NHC(O)NH2, NHC(O)NHR67, NHC(O)N(R67)2, NR67C(O)NHR67, NR67C(O)N(R67)2, C(O)NH2, C(O)NHR67, C(O)N(R67)2, C(O)NHOH, C(O)NHOR67, C(O)NHSO2R67, C(O)NR67SO2R67, SO2NH2, SO2NHR67, SO2N(R67)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR67, C(N)N(R67)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R67 представляет собой алкил, алкенил, алкинил, фенил, гетероарил, циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил;
где фрагменты, представленные группами R58, R59, R60, R63, R64, R65 и R67, не замещены или замещены одним или несколькими независимо выбранными заместителями R68, OR68, SR68, S(O)R68, SO2R68, C(O)R68, C(O)OR68, OC(O)R68, OC(O)OR68, NH2, NHR68, N(R68)2, NHC(O)R68, NR68C(O)R68, NHS(O)2R68, NR68S(O)2R68, NHC(O)OR68, NR68C(O)OR68, NHC(O)NH2, NHC(O)NHR68, NHC(O)N(R68)2, NR68C(O)NHR68, NR68C(O)N(R68)2, C(O)NH2, C(O)NHR68, C(O)N(R68)2, C(O)NHOH, C(O)NHOR68, C(O)NHSO2R68, C(O)NR68SO2R68, SO2NH2, SO2NHR68, SO2N(R68)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR68, C(N)N(R68)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R68 представляет собой R69, R70, R71 или R72;
R69 представляет собой фенил, который не конденсирован или конденсирован с бензолом, гетероареном или R69A; R69A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R70 представляет собой гетероарил, который не конденсирован или конденсирован с бензолом, гетероареном или R70A; R70A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R71 представляет собой циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил, каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или R71A; R71A представляет собой циклоалкан, циклоалкен, гетероциклоалкан или гетероциклоалкен;
R72 представляет собой алкил, алкенил или алкинил, каждый из которых не замещен или замещен одним, или двумя, или тремя независимо выбранными заместителями R73, OR73, SR73, S(O)R73, SO2R73, C(O)R73, C(O)OR73, OC(O)R73, OC(O)OR73, NH2, NHR73, N(R73)2, NHC(O)R73, NR73C(O)R73, NHS(O)2R73, NR73S(O)2R73, NHC(O)OR73, NR73C(O)OR73, NHC(O)NH2, NHC(O)NHR73, NHC(O)N(R73)2, NR73C(O)NHR73, NR73C(O)N(R73)2, C(O)NH2, C(O)NHR73, C(O)N(R73)2, C(O)NHOH, C(O)NHOR73, C(O)NHSO2R73, C(O)NR73SO2R73, SO2NH2, SO2NHR73, SO2N(R73)2, C(O)H, C(O)OH, C(N)NH2, C(N)NHR73, C(N)N(R73)2, CNOH, CNOCH3, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I;
R73 представляет собой алкил, алкенил, алкинил, фенил, гетероарил, циклоалкил, циклоалкенил, гетероциклоалкил или гетероциклоалкенил; и
фрагменты, представленные группами R69, R70 и R71, не замещены или замещены одним или несколькими независимо выбранными заместителями NH2, C(O)NH2, C(O)NHOH, SO2NH2, CF3, CF2CF3, C(O)H, C(O)OH, C(N)NH2, OH, (O), CN, N3, NO2, CF3, CF2CF3, OCF3, OCF2CF3, F, Cl, Br или I.
В другом варианте осуществления формулы (I)
A1 представляет собой фурил, имидазолил, изотиазолил, изоксазолил, пиразолил, пирролил, тиазолил, тиадиазолил, тиенил, триазолил, гетероциклоалкил или гетероциклоалкенил; каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или A1A; A1A представляет собой гетероциклоалкен;
где A1 не замещен или замещен одним, или двумя, или тремя, или четырьмя, или пятью независимо выбранными заместителями R1, OR1, C(O)OR1, NHR1, N(R1)2, C(N)C(O)R1, C(O)NHR1, NHC(O)R1, NR1C(O)R1, (O), NO2, F, Cl, Br, I, CF3;
R1 представляет собой R2, R3, R4 или R5;
R2 представляет собой фенил;
R3 представляет собой гетероарил;
R4 представляет собой гетероциклоалкил;
R5 представляет собой алкил или алкенил, каждый из которых не замещен или замещен заместителями R7, SR7, N(R7)2, NHC(O)R7, F, Cl, Br или I;
R7 представляет собой R8, R9, R10 или R11;
R8 представляет собой фенил;
R9 представляет собой гетероарил;
R10 представляет собой гетероциклоалкил;
R11 представляет собой алкил;
Z1 представляет собой R26;
Z2 представляет собой R30;
L1 представляет собой R37;
R26 представляет собой фенилен;
R30 представляет собой гетероциклоалкилен;
R37 представляет собой R37A;
R37A представляет собой алкилен или алкенилен, каждый из которых не замещен или замещен R37B;
R37B представляет собой фенил;
Z3 представляет собой R38 или R40;
R38 представляет собой фенил;
R40 представляет собой циклоалкил или циклоалкенил;
где фрагменты, представленные группами R26 и R27, не замещены или замещены группой OR41;
R41 представляет собой R42 или R43;
R42 представляет собой фенил, который не конденсирован или конденсирован с гетероареном;
R43 представляет собой гетероарил, который не конденсирован или конденсирован с гетероареном;
где каждый вышеуказанный циклический фрагмент независимо не замещен, дополнительно не замещен, замещен или дополнительно замещен одним или несколькими независимо выбранными заместителями R57, OR57, C(O)OR57, F, Cl, Br или I;
R57 представляет собой R58 или R61;
R58 представляет собой фенил;
R61 представляет собой алкил; и
где фрагменты, представленные группой R58, не замещены или замещены одним или несколькими независимо выбранными заместителями F, Cl, Br или I.
В одном варианте воплощения формулы (I) A1 представляет собой фурил, имидазолил, изотиазолил, изоксазолил, пиразолил, пирролил, тиазолил, тиадиазолил, тиенил, триазолил, гетероциклоалкил или гетероциклоалкенил; каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или A1A; A1A представляет собой гетероциклоалкен. В другом варианте воплощения формулы (I) A1 представляет собой фурил. В другом варианте воплощения формулы (I) A1 представляет собой имидазолил. В другом варианте воплощения формулы (I) A1 представляет собой изотиазолил. В другом варианте воплощения формулы (I) A1 представляет собой изоксазолил. В другом варианте воплощения формулы (I) A1 представляет собой пиразолил. В другом варианте воплощения формулы (I) A1 представляет собой пирролил. В другом варианте воплощения формулы (I) A1 представляет собой тиазолил. В другом варианте воплощения формулы (I) A1 представляет собой тиадиазолил. В другом варианте воплощения формулы (I) A1 представляет собой тиенил. В другом варианте воплощения формулы (I) A1 представляет собой триазолил. В другом варианте воплощения формулы (I) A1 представляет собой гетероциклоалкил. В другом варианте воплощения формулы (I) A1 представляет собой гетероциклоалкенил. В другом варианте воплощения формулы (I) A1 представляет собой пиперидинил. В другом варианте воплощения формулы (I) A1 представляет собой морфолинил. В другом варианте воплощения формулы (I) A1 представляет собой дигидро-1,3,4-тиадиазол-2-ил. В другом варианте воплощения формулы (I) A1 представляет собой бензотиен-2-ил. В другом варианте воплощения формулы (I) A1 представляет собой бензотиазол-2-ил. В другом варианте воплощения формулы (I) A1 представляет собой [1,2,4]триазоло[1,5-a]пиримидин-2-ил. В другом варианте воплощения формулы (I) A1 представляет собой тетрагидротиен-3-ил. В другом варианте воплощения формулы (I) A1 представляет собой [1,2,4]триазоло[1,5-a]пиримидин-2-ил. В другом варианте воплощения формулы (I) A1 представляет собой имидазо[2,1-b][1,3]тиазол-5-ил.
В одном варианте воплощения формулы (I) A1 не замещен. В другом варианте воплощения формулы (I) A1 замещен одним, или двумя, или тремя, или четырьмя, или пятью независимо выбранными заместителями R1, OR1, C(O)OR1, NHR1, N(R1)2, C(N)C(O)R1, C(O)NHR1, NHC(O)R1, NR1C(O)R1, (О), NO2, F, Cl, Br, I или CF3. В одном варианте воплощения формулы (I) A1 не замещен. В другом варианте воплощения формулы (I) A1 замещен NHR1. В другом варианте воплощения формулы (I) A1 замещен NHR1 и NO2. В другом варианте воплощения формулы (I) A1 замещен NHR1. В другом варианте воплощения формулы (I) A1 замещен NR1C(O)R1. В другом варианте воплощения формулы (I) A1 замещен N(R1)2. В другом варианте воплощения формулы (I) A1 замещен C(N)C(O)R1 и R1. В другом варианте воплощения формулы (I) A1 замещен NHC(O)R1 и R1. В другом варианте воплощения формулы (I) A1 замещен R1. В другом варианте воплощения формулы (I) A1 замещен двумя независимо выбранными R1. В другом варианте воплощения формулы (I) A1 замещен Cl. В другом варианте воплощения формулы (I) A1 замещен CF3. В другом варианте воплощения формулы (I) A1 замещен F. В другом варианте воплощения формулы (I) A1 замещен тремя независимо выбранными R1 и C(O)OR1. В другом варианте воплощения формулы (I) A1 представляет собой замещенный R1 и C(O)OR1. В другом варианте воплощения формулы (I) A1 замещен R1 и Cl. В другом варианте воплощения формулы (I) A1 замещен R1 и Br. В другом варианте воплощения формулы (I) A1 замещен тремя независимо выбранными R1. В другом варианте воплощения формулы (I) A1 замещен C(O)NHR1. В другом варианте воплощения формулы (I) A1 замещен двумя независимо выбранными R1 и Cl. В другом варианте воплощения формулы (I) A1 замещен R1 и NO2. В другом варианте воплощения формулы (I) A1 замещен NHR1 и NO2. В другом варианте воплощения формулы (I) A1 замещен (О). В другом варианте воплощения формулы (I) A1 замещен OR1.
В одном варианте воплощения формулы (I) R1 представляет собой фенил. В другом варианте воплощения формулы (I) R1 представляет собой пиразолил. В другом варианте воплощения формулы (I) R1 представляет собой морфолинил. В другом варианте воплощения формулы (I) R1 представляет собой изоксазолил. В другом варианте воплощения формулы (I) R1 представляет собой пиперидинил. В другом варианте воплощения формулы (I) R1 представляет собой алкил, который не замещен. В другом варианте воплощения формулы (I) R1 представляет собой алкил, который замещен одним или несколькими R7, SR7, N(R7)2, NHC(O)R7 или Cl.
В одном варианте воплощения формулы (I) R7 представляет собой фенил. В одном варианте воплощения формулы (I) R7 представляет собой метил. В одном варианте воплощения формулы (I) R7 представляет собой изопропил. В одном варианте воплощения формулы (I) R7 представляет собой пирролинил. В одном варианте воплощения формулы (I) R7 представляет собой морфолинил. В одном варианте воплощения формулы (I) R7 представляет собой тетрагидропиранил.
Еще один вариант осуществления настоящего изобретения касается соединений, имеющих формулу I, которые представляют собой
4-[4-(циклогексилметил)-4-метоксипиперидин-1-ил]-N-{[5-({(1R)-3-(диметиламино)-1-[(фенилтио)метил]пропил}амино)-4-нитротиен-2-ил]сульфонил}бензамид;
N-{[5-({(1R)-3-(диметиламино)-1-[(фенилтио)метил]пропил}амино)-4-нитротиен-2-ил]сульфонил}-4-[4-метокси-4-(3-метилбензил)пиперидин-1-ил]бензамид;
N-{[5-({(1R)-3-(диметиламино)-1-[(фенилтио)метил]пропил}амино)-4-нитротиен-2-ил]сульфонил}-4-[4-(3,3-дифенилпроп-2-енил)пиперазин-1-ил]бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(4-{[2-(фенилтио)этил]амино}пиперидин-1-ил)сульфонил]бензамид;
N-[(4-{ацетил[2-(фенилтио)этил]амино}пиперидин-1-ил)сульфонил]-4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(4-{метил[2-(фенилтио)этил]амино}пиперидин-1-ил)сульфонил]бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-{[5-({(1R)-3-[изопропил(метил)амино]-1-[(фенилтио)метил]пропил}амино)-4-нитротиен-2-ил]сульфонил}бензамид;
4-(4-{[2-(4-хлорфенил)циклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-{[5-({(1R)-3-[изопропил(метил)амино]-1-[(фенилтио)метил]пропил}амино)-4-нитротиен-2-ил]сульфонил}бензамид;
4-(4-{[2-(4-хлорфенил)-5,5-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-{[5-({(1R)-3-[изопропил(метил)амино]-1-[(фенилтио)метил]пропил}амино)-4-нитротиен-2-ил]сульфонил}бензамид;
N-{[(5Z)-5-(ацетилимино)-4-метил-4,5-дигидро-1,3,4-тиадиазол-2-ил]сульфонил}-4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензамид;
N-{[2-(ацетиламино)-4-метил-1,3-тиазол-5-ил]сульфонил}-4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензамид;
N-({5-[(бензоиламино)метил]тиен-2-ил}сульфонил)-4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(6-хлоримидазо[2,1-b][1,3]тиазол-5-ил)сульфонил]бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-(морфолин-4-илсульфонил)бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(2,4-диметил-1,3-тиазол-5-ил)сульфонил]бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-{[4-фенил-5-(трифторметил)тиен-3-ил]сульфонил]бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(5-фтор-3-метил-1-бензотиен-2-ил)сульфонил]бензамид;
N-(1,3-бензотиазол-2-илсульфонил)-4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-(тиен-2-илсульфонил)бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(5,7-диметил[1,2,4]триазоло[1,5-a]пиримидин-2-ил)сульфонил]бензамид;
этил 4-{[(4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензоил)амино]сульфонил}-5-метил-1,2-дифенил-1H-пиррол-3-карбоксилат;
метил 5-{[(4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензоил)амино]сульфонил}-1-метил-1H-пиррол-2-карбоксилат;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-{[5-(1,3-диметил-1H-пиразол-5-ил)изоксазол-4-ил]сульфонил}бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(4-хлор-3-метилизотиазол-5-ил)сульфонил]бензамид;
N-[(5-бром-3-метил-1-бензотиен-2-ил)сульфонил]-4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-({5-[(E)-2-(1,2,4-оксадиазол-3-ил)винил]тиен-2-ил}сульфонил)бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-{[1-(2-хлорэтил)-3,5-диметил-1H-пиразол-4-ил]сульфонил}бензамид;
5-{[(4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензоил)амино]сульфонил}-N-(1-этилпропил)-1,3,4-тиадиазол-2-карбоксамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(5-хлор-1,3-диметил-1H-пиразол-4-ил)сульфонил]бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(4-нитро-5-пиперидин-1-илтиен-2-ил)сульфонил]бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(5-изоксазол-5-ил-2-фурил)сульфонил]бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(3,5-диметилизоксазол-4-ил)сульфонил]бензамид;
4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-2-(1H-индол-5-илокси)-N-({4-нитро-5-[(3-пирролидин-1-илпропил)амино]тиен-2-ил}сульфонил)бензамид;
4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-[(5-{[3-(диметиламино)пропил]амино}-4-нитротиен-2-ил)сульфонил]-2-(1H-индол-5-илокси)бензамид;
4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-2-(1H-индол-5-илокси)-N-({5-[(3-морфолин-4-илпропил)амино]-4-нитротиен-2-ил}сульфонил)бензамид;
N-{[5-({(1R)-3-(диметиламино)-1-[(фенилтио)метил]пропил}амино)-4-нитротиен-2-ил]сульфонил}-4-{4-[2-(трифторметил)бензилиден]пиперидин-1-ил}бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метилен]пиперидин-1-ил}-N-[(1,1-диоксидотетрагидротиен-3-ил)сульфонил]бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метилен]пиперидин-1-ил}-N-[(5-хлор-3-метил-1-бензотиен-2-ил)сульфонил]бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(5-хлор-3-метил-1-бензотиен-2-ил)сульфонил]-2-феноксибензамид;
2-(3-хлорфенокси)-4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-Ν-[(5,7-диметил[1,2,4]триазоло[1,5-a]пиримидин-2-ил)сульфонил]бензамид;
4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-[(5,7-диметил[1,2,4]триазоло[1,5-a]пиримидин-2-ил)сульфонил]-2-[(6-фтор-1H-индол-5-ил)окси]бензамид;
4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-2-[(6,7-дифтор-1H-индол-5-ил)окси]-N-[(5,7-диметил[1,2,4]триазоло[1,5-a]пиримидин-2-ил)сульфонил]бензамид;
трет-бутил (2S)-2-{[(5-{[4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-2-(1H-пирроло[2,3-b]пиридин-5-илокси)бензоил]сульфамоил}-4-метил-1,3-тиазол-2-ил)окси]метил}морфолин-4-карбоксилат;
трет-бутил (2S)-2-{[(5-{[2-(1H-бензимидазол-4-илокси)-4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)бензоил]сульфамоил}-4-метил-1,3-тиазол-2-ил)окси]метил}морфолин-4-карбоксилат;
4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-({2-[(4-фтортетрагидро-2H-пиран-4-ил)метокси]-4-метил-1,3-тиазол-5-ил}сульфонил)-2-(1H-пирроло[2,3-b]пиридин-5-илокси)бензамид;
2-(1H-бензимидазол-4-илокси)-4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-({2-[(4-фтортетрагидро-2H-пиран-4-ил)метокси]-4-метил-1,3-тиазол-5-ил}сульфонил)бензамид;
трет-бутил (2S)-2-{[(5-{[4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-2-(1H-индазол-4-илокси)бензоил]сульфамоил}-4-метил-1,3-тиазол-2-ил)окси]метил}морфолин-4-карбоксилат;
4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-({2-[(4-фтортетрагидро-2H-пиран-4-ил)метокси]-4-метил-1,3-тиазол-5-ил}сульфонил)-2-(1H-индазол-4-илокси)бензамид;
и их терапевтически приемлемые соли, пролекарства, соли пролекарств и метаболиты.
Другой вариант осуществления настоящего изобретения касается соединений или их терапевтически приемлемых солей, пролекарств, метаболитов или солей пролекарств указанных соединений, которые пригодны в качестве ингибиторов антиапоптотических белков Bcl-2, при этом указанные соединения имеют формулу (II)

где R101 представляет собой Н или имеет значения, приведенные для заместителей при R26, а значения A1 приведены в формуле (I).
В одном варианте воплощения формулы (II) A1 представляет собой фурил, имидазолил, изотиазолил, изоксазолил, пиразолил, пирролил, тиазолил, тиадиазолил, тиенил, триазолил, гетероциклоалкил или гетероциклоалкенил; каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или A1A; и A1A представляет собой гетероциклоалкен. В другом варианте воплощения формулы (II) A1 представляет собой фурил. В другом варианте воплощения формулы (II) A1 представляет собой имидазолил. В другом варианте воплощения формулы (II) A1 представляет собой изотиазолил. В другом варианте воплощения формулы (II) A1 представляет собой изоксазолил. В другом варианте воплощения формулы (II) A1 представляет собой пиразолил. В другом варианте воплощения формулы (II) A1 представляет собой пирролил. В другом варианте воплощения формулы (II) A1 представляет собой тиазолил. В другом варианте воплощения формулы (II) A1 представляет собой тиадиазолил. В другом варианте воплощения формулы (II) A1 представляет собой тиенил. В другом варианте воплощения формулы (II) A1 представляет собой триазолил. В другом варианте воплощения формулы (II) A1 представляет собой гетероциклоалкил. В другом варианте воплощения формулы (II) A1 представляет собой гетероциклоалкенил. В другом варианте воплощения формулы (II) A1 представляет собой пиперидинил. В другом варианте воплощения формулы (II) A1 представляет собой морфолинил. В другом варианте воплощения формулы (II) A1 представляет собой дигидро-1,3,4-тиадиазол-2-ил. В другом варианте воплощения формулы (II) A1 представляет собой бензотиен-2-ил. В другом варианте воплощения формулы (II) A1 представляет собой бензотиазол-2-ил. В другом варианте воплощения формулы (II) A1 представляет собой бензотиазол-2-ил. В другом варианте воплощения формулы (II) A1 представляет собой [1,2,4]триазоло[1,5-a]пиримидин-2-ил. В другом варианте воплощения формулы (II) A1 представляет собой тетрагидротиен-3-ил. В другом варианте воплощения формулы (II) A1 представляет собой [1,2,4]триазоло[1,5-a]пиримидин-2-ил. В другом варианте воплощения формулы (II) A1 представляет собой имидазо[2,1-b][1,3]тиазол-5-ил.
В одном варианте воплощения формулы (II) A1 не замещен. В другом варианте воплощения формулы (II) A1 замещен одним, или двумя, или тремя, или четырьмя, или пятью независимо выбранными заместителями R1, OR1, C(O)OR1, NHR1, N(R1)2, C(N)C(O)R1, C(O)NHR1, NHC(O)R1, NR1C(O)R1, (О), NO2, F, Cl, Br, I или CF3. В одном варианте воплощения формулы (II) A1 не замещен. В другом варианте воплощения формулы (II) A1 замещен NHR1. В другом варианте воплощения формулы (II) A1 замещен NHR1 и NO2. В другом варианте воплощения формулы (II) A1 замещен NHR1. В другом варианте воплощения формулы (II) A1 замещен NR1C(O)R1. В другом варианте воплощения формулы (II) A1 замещен N(R1)2. В другом варианте воплощения формулы (II) A1 замещен C(N)C(O)R1 и R1. В другом варианте воплощения формулы (II) A1 замещен NHC(O)R1 и R1. В другом варианте воплощения формулы (II) A1 замещен R1. В другом варианте воплощения формулы (II) A1 замещен двумя независимо выбранными R1. В другом варианте воплощения формулы (II) A1 замещен Cl. В другом варианте воплощения формулы (II) A1 замещен CF3. В другом варианте воплощения формулы (II) A1 замещен F. В другом варианте воплощения формулы (II) A1 замещен тремя независимо выбранными R1 и C(O)OR1. В другом варианте воплощения формулы (II) A1 представляет собой замещенный R1 и C(O)OR1. В другом варианте воплощения формулы (II) A1 замещен R1 и Cl. В другом варианте воплощения формулы (II) A1 замещен R1 и Br. В другом варианте воплощения формулы (II) A1 замещен тремя независимо выбранными R1. В другом варианте воплощения формулы (II) A1 замещен C(O)NHR1. В другом варианте воплощения формулы (II) A1 замещен двумя независимо выбранными R1 и Cl. В другом варианте воплощения формулы (II) A1 замещен R1 и NO2. В другом варианте воплощения формулы (II) A1 замещен NHR1 и NO2. В другом варианте воплощения формулы (II) A1 замещен (О). В другом варианте воплощения формулы (II) A1 замещен OR1.
В одном варианте воплощения формулы (II) R1 представляет собой фенил. В другом варианте воплощения формулы (II) R1 представляет собой пиразолил. В другом варианте воплощения формулы (II) R1 представляет собой морфолинил. В другом варианте воплощения формулы (II) R1 представляет собой изоксазолил. В другом варианте воплощения формулы (II) R1 представляет собой пиперидинил. В другом варианте воплощения формулы (II) R1 представляет собой алкил, который не замещен. В другом варианте воплощения формулы (II) R1 представляет собой алкил, который замещен одним или несколькими R7, SR7, N(R7)2, NHC(O)R7 или Cl.
В одном варианте воплощения формулы (II) R7 представляет собой фенил. В одном варианте воплощения формулы (II) R7 представляет собой метил. В одном варианте воплощения формулы (II) R7 представляет собой изопропил. В одном варианте воплощения формулы (II) R7 представляет собой пирролинил. В одном варианте воплощения формулы (II) R7 представляет собой морфолинил. В одном варианте воплощения формулы (II) R7 представляет собой тетрагидропиранил.
Еще один вариант осуществления настоящего изобретения касается соединений, имеющих формулу II, которые представляют собой
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(4-{[2-(фенилтио)этил]амино}пиперидин-1-ил)сульфонил]бензамид;
N-[(4-{ацетил[2-(фенилтио)этил]амино}пиперидин-1-ил)сульфонил]-4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(4-{метил[2-(фенилтио)этил]амино}пиперидин-1-ил)сульфонил]бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-{[5-({(1R)-3-[изопропил(метил)амино]-1-[(фенилтио)метил]пропил}амино)-4-нитротиен-2-ил]сульфонил}бензамид;
N-{[(5Z)-5-(ацетилимино)-4-метил-4,5-дигидро-1,3,4-тиадиазол-2-ил]сульфонил}-4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензамид;
N-{[2-(ацетиламино)-4-метил-1,3-тиазол-5-ил]сульфонил}-4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензамид;
N-({5-[(бензоиламино)метил]тиен-2-ил}сульфонил)-4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(6-хлоримидазо[2,1-b][1,3]тиазол-5-ил)сульфонил]бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-(морфолин-4-илсульфонил)бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(2,4-диметил-1,3-тиазол-5-ил)сульфонил]бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-{[4-фенил-5-(трифторметил)тиен-3-ил]сульфонил]бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(5-фтор-3-метил-1-бензотиен-2-ил)сульфонил]бензамид;
N-(1,3-бензотиазол-2-илсульфонил)-4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-(тиен-2-илсульфонил)бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(5,7-диметил[1,2,4]триазоло[1,5-a]пиримидин-2-ил)сульфонил]бензамид;
этил 4-{[(4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензоил)амино]сульфонил}-5-метил-1,2-дифенил-1H-пиррол-3-карбоксилат;
метил 5-{[(4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензоил)амино]сульфонил}-1-метил-1H-пиррол-2-карбоксилат;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-{[5-(1,3-диметил-1H-пиразол-5-ил)изоксазол-4-ил]сульфонил}бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(4-хлор-3-метилизотиазол-5-ил)сульфонил]бензамид;
N-[(5-бром-3-метил-1-бензотиен-2-ил)сульфонил]-4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-({5-[(E)-2-(1,2,4-оксадиазол-3-ил)винил]тиен-2-ил}сульфонил)бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-{[1-(2-хлорэтил)-3,5-диметил-1H-пиразол-4-ил]сульфонил}бензамид;
5-{[(4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензоил)амино]сульфонил}-N-(1-этилпропил)-1,3,4-тиадиазол-2-карбоксамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(5-хлор-1,3-диметил-1H-пиразол-4-ил)сульфонил]бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(4-нитро-5-пиперидин-1-илтиен-2-ил)сульфонил]бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(5-изоксазол-5-ил-2-фурил)сульфонил]бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(3,5-диметилизоксазол-4-ил)сульфонил]бензамид;
4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(5-хлор-3-метил-1-бензотиен-2-ил)сульфонил]-2-феноксибензамид;
и их терапевтически приемлемые соли, пролекарства, соли пролекарств и метаболиты.
Другой вариант осуществления настоящего изобретения касается соединений или их терапевтически приемлемых солей, пролекарств, метаболитов или солей пролекарств указанных соединений, которые пригодны в качестве ингибиторов антиапоптотических белков Bcl-2, при этом указанные соединения имеют формулу (III)
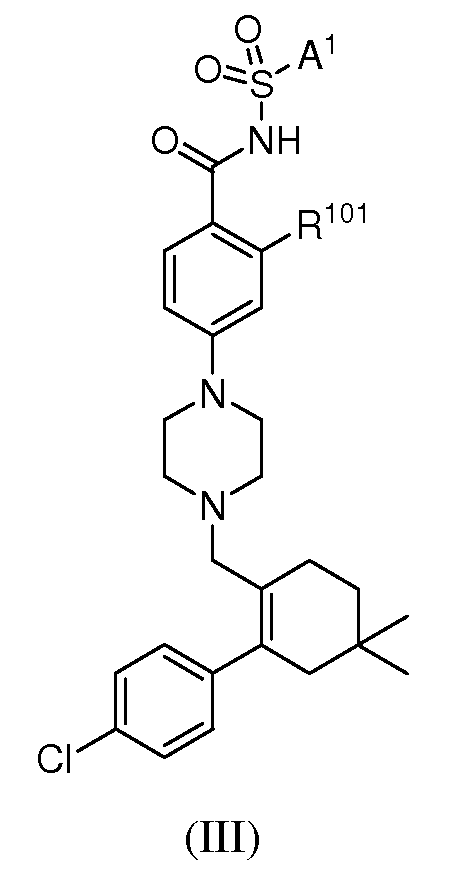
где R101 представляет собой Н или имеет значения, приведенные для заместителей при R26, а значения A1 приведены в формуле (I).
В одном варианте воплощения формулы (III) A1 представляет собой фурил, имидазолил, изотиазолил, изоксазолил, пиразолил, пирролил, тиазолил, тиадиазолил, тиенил, триазолил, гетероциклоалкил или гетероциклоалкенил; каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или A1A; A1A представляет собой гетероциклоалкен. В другом варианте воплощения формулы (III) A1 представляет собой фурил. В другом варианте воплощения формулы (III) A1 представляет собой имидазолил. В другом варианте воплощения формулы (III) A1 представляет собой изотиазолил. В другом варианте воплощения формулы (III) A1 представляет собой изоксазолил. В другом варианте воплощения формулы (III) A1 представляет собой пиразолил. В другом варианте воплощения формулы (III) A1 представляет собой пирролил. В другом варианте воплощения формулы (III) A1 представляет собой тиазолил. В другом варианте воплощения формулы (III) A1 представляет собой тиадиазолил. В другом варианте воплощения формулы (III) A1 представляет собой тиенил. В другом варианте воплощения формулы (II) A1 представляет собой триазолил. В другом варианте воплощения формулы (III) A1 представляет собой гетероциклоалкил. В другом варианте воплощения формулы (III) A1 представляет собой гетероциклоалкенил. В другом варианте воплощения формулы (III) A1 представляет собой пиперидинил. В другом варианте воплощения формулы (III) A1 представляет собой морфолинил. В другом варианте воплощения формулы (III) A1 представляет собой дигидро-1,3,4-тиадиазол-2-ил. В другом варианте воплощения формулы (III) A1 представляет собой бензотиен-2-ил. В другом варианте воплощения формулы (III) A1 представляет собой бензотиазол-2-ил. В другом варианте воплощения формулы (III) A1 представляет собой бензотиазол-2-ил. В другом варианте воплощения формулы (III) A1 представляет собой [1,2,4]триазоло[1,5-a]пиримидин-2-ил. В другом варианте воплощения формулы (III) A1 представляет собой тетрагидротиен-3-ил. В другом варианте воплощения формулы (III) A1 представляет собой [1,2,4]триазоло[1,5-a]пиримидин-2-ил. В другом варианте воплощения формулы (III) A1 представляет собой имидазо[2,1-b][1,3]тиазол-5-ил.
В одном варианте воплощения формулы (III) A1 не замещен. В другом варианте воплощения формулы (III) A1 замещен одним, или двумя, или тремя, или четырьмя, или пятью независимо выбранными заместителями R1, OR1, C(O)OR1, NHR1, N(R1)2, C(N)C(O)R1, C(O)NHR1, NHC(O)R1, NR1C(O)R1, (О), NO2, F, Cl, Br, I или CF3. В одном варианте воплощения формулы (III) A1 не замещен. В другом варианте воплощения формулы (III) A1 замещен NHR1. В другом варианте воплощения формулы (III) A1 замещен NHR1 и NO2. В другом варианте воплощения формулы (III) A1 замещен NHR1. В другом варианте воплощения формулы (III) A1 замещен NR1C(O)R1. В другом варианте воплощения формулы (III) A1 замещен N(R1)2. В другом варианте воплощения формулы (III) A1 замещен C(N)C(O)R1 и R1. В другом варианте воплощения формулы (III) A1 замещен NHC(O)R1 и R1. В другом варианте воплощения формулы (III) A1 замещен R1. В другом варианте воплощения формулы (III) A1 замещен двумя независимо выбранными R1. В другом варианте воплощения формулы (III) A1 замещен Cl. В другом варианте воплощения формулы (III) A1 замещен CF3. В другом варианте воплощения формулы (III) A1 замещен F. В другом варианте воплощения формулы (III) A1 замещен тремя независимо выбранными R1 и C(O)OR1. В другом варианте воплощения формулы (III) A1 представляет собой замещенный R1 и C(O)OR1. В другом варианте воплощения формулы (III) A1 замещен R1 и Cl. В другом варианте воплощения формулы (III) A1 замещен R1 и Br. В другом варианте воплощения формулы (III) A1 замещен тремя независимо выбранными R1. В другом варианте воплощения формулы (III) A1 замещен C(O)NHR1. В другом варианте воплощения формулы (III) A1 замещен двумя независимо выбранными R1 и Cl. В другом варианте воплощения формулы (III) A1 замещен R1 и NO2. В другом варианте воплощения формулы (III) A1 замещен NHR1 и NO2. В другом варианте воплощения формулы (III) A1 замещен (О). В другом варианте воплощения формулы (III) A1 замещен OR1.
В одном варианте воплощения формулы (III) R1 представляет собой фенил. В другом варианте воплощения формулы (III) R1 представляет собой пиразолил. В другом варианте воплощения формулы (III) R1 представляет собой морфолинил. В другом варианте воплощения формулы (III) R1 представляет собой изоксазолил. В другом варианте воплощения формулы (III) R1 представляет собой пиперидинил. В другом варианте воплощения формулы (III) R1 представляет собой алкил, который не замещен. В другом варианте воплощения формулы (III) R1 представляет собой алкил, который замещен одним или несколькими R7, SR7, N(R7)2, NHC(O)R7 или Cl.
В одном варианте воплощения формулы (III) R7 представляет собой фенил. В одном варианте воплощения формулы (III) R7 представляет собой метил. В одном варианте воплощения формулы (III) R7 представляет собой изопропил. В одном варианте воплощения формулы (III) R7 представляет собой пирролинил. В одном варианте воплощения формулы (III) R7 представляет собой морфолинил. В одном варианте воплощения формулы (III) R7 представляет собой тетрагидропиранил.
Еще один вариант осуществления настоящего изобретения касается соединений, имеющих формулу III, которые представляют собой
4-(4-{[2-(4-хлорфенил)-5,5-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-{[5-({(1R)-3-[изопропил(метил)амино]-1-[(фенилтио)метил]пропил}амино)-4-нитротиен-2-ил]сульфонил}бензамид;
4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-2-(1H-индол-5-илокси)-N-({4-нитро-5-[(3-пирролидин-1-илпропил)амино]тиен-2-ил}сульфонил)бензамид;
4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-[(5-{[3-(диметиламино)пропил]амино}-4-нитротиен-2-ил)сульфонил]-2-(1H-индол-5-илокси)бензамид;
4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-2-(1H-индол-5-илокси)-N-({5-[(3-морфолин-4-илпропил)амино]-4-нитротиен-2-ил}сульфонил)бензамид;
2-(3-хлорфенокси)-4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-Ν-[(5,7-диметил[1,2,4]триазоло[1,5-a]пиримидин-2-ил)сульфонил]бензамид;
4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-[(5,7-диметил[1,2,4]триазоло[1,5-a]пиримидин-2-ил)сульфонил]-2-[(6-фтор-1H-индол-5-ил)окси]бензамид;
4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-2-[(6,7-дифтор-1H-индол-5-ил)окси]-N-[(5,7-диметил[1,2,4]триазоло[1,5-a]пиримидин-2-ил)сульфонил]бензамид;
трет-бутил (2S)-2-{[(5-{[4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-2-(1H-пирроло[2,3-b]пиридин-5-илокси)бензоил]сульфамоил}-4-метил-1,3-тиазол-2-ил)окси]метил}морфолин-4-карбоксилат;
трет-бутил (2S)-2-{[(5-{[2-(1H-бензимидазол-4-илокси)-4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)бензоил]сульфамоил}-4-метил-1,3-тиазол-2-ил)окси]метил}морфолин-4-карбоксилат;
4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-({2-[(4-фтортетрагидро-2H-пиран-4-ил)метокси]-4-метил-1,3-тиазол-5-ил}сульфонил)-2-(1H-пирроло[2,3-b]пиридин-5-илокси)бензамид;
2-(1H-бензимидазол-4-илокси)-4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-({2-[(4-фтортетрагидро-2H-пиран-4-ил)метокси]-4-метил-1,3-тиазол-5-ил}сульфонил)бензамид;
трет-бутил (2S)-2-{[(5-{[4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-2-(1H-индазол-4-илокси)бензоил]сульфамоил}-4-метил-1,3-тиазол-2-ил)окси]метил}морфолин-4-карбоксилат;
4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-({2-[(4-фтортетрагидро-2H-пиран-4-ил)метокси]-4-метил-1,3-тиазол-5-ил}сульфонил)-2-(1H-индазол-4-илокси)бензамид;
и их терапевтически приемлемые соли, пролекарства, соли пролекарств и метаболиты.
Другой вариант осуществления настоящего изобретения касается соединений или их терапевтически приемлемых солей, пролекарств, метаболитов или солей пролекарств указанных соединений, которые пригодны в качестве ингибиторов антиапоптотических белков Bcl-2, при этом указанные соединения имеют формулу (IV)

где R102 представляет собой точку присоединения к индолу, а остальные обозначают Н или имеют значения, приведенные для заместителей при R42, а значения A1 и Z3 приведены в формуле (I).
В одном варианте воплощения формулы (IV) A1 представляет собой фурил, имидазолил, изотиазолил, изоксазолил, пиразолил, пирролил, тиазолил, тиадиазолил, тиенил, триазолил, гетероциклоалкил или гетероциклоалкенил; каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или A1A; A1A представляет собой гетероциклоалкен. В другом варианте воплощения формулы (IV) A1 представляет собой фурил. В другом варианте воплощения формулы (IV) A1 представляет собой имидазолил. В другом варианте воплощения формулы (IV) A1 представляет собой изотиазолил. В другом варианте воплощения формулы (IV) A1 представляет собой изоксазолил. В другом варианте воплощения формулы (IV) A1 представляет собой пиразолил. В другом варианте воплощения формулы (IV) A1 представляет собой пирролил. В другом варианте воплощения формулы (IV) A1 представляет собой тиазолил. В другом варианте воплощения формулы (IV) A1 представляет собой тиадиазолил. В другом варианте воплощения формулы (IV) A1 представляет собой тиенил. В другом варианте воплощения формулы (IV) A1 представляет собой триазолил. В другом варианте воплощения формулы (IV) A1 представляет собой гетероциклоалкил. В другом варианте воплощения формулы (IV) A1 представляет собой гетероциклоалкенил. В другом варианте воплощения формулы (IV) A1 представляет собой пиперидинил. В другом варианте воплощения формулы (IV) A1 представляет собой морфолинил. В другом варианте воплощения формулы (IV) A1 представляет собой дигидро-1,3,4-тиадиазол-2-ил. В другом варианте воплощения формулы (IV) A1 представляет собой бензотиен-2-ил. В другом варианте воплощения формулы (IV) A1 представляет собой бензотиазол-2-ил. В другом варианте воплощения формулы (IV) A1 представляет собой [1,2,4]триазоло[1,5-a]пиримидин-2-ил. В другом варианте воплощения формулы (IV) A1 представляет собой тетрагидротиен-3-ил. В другом варианте воплощения формулы (IV) A1 представляет собой [1,2,4]триазоло[1,5-a]пиримидин-2-ил. В другом варианте воплощения формулы (IV) A1 представляет собой имидазо[2,1-b][1,3]тиазол-5-ил.
В одном варианте воплощения формулы (IV) A1 не замещен. В другом варианте воплощения формулы (IV) A1 замещен одним, или двумя, или тремя, или четырьмя, или пятью независимо выбранными заместителями R1, OR1, C(O)OR1, NHR1, N(R1)2, C(N)C(O)R1, C(O)NHR1, NHC(O)R1, NR1C(O)R1, (О), NO2, F, Cl, Br, I или CF3. В одном варианте воплощения формулы (IV) A1 не замещен. В другом варианте воплощения формулы (IV) A1 замещен NHR1. В другом варианте воплощения формулы (IV) A1 замещен NHR1 и NO2. В другом варианте воплощения формулы (IV) A1 замещен NHR1. В другом варианте воплощения формулы (IV) A1 замещен NR1C(O)R1. В другом варианте воплощения формулы (IV) A1 замещен N(R1)2. В другом варианте воплощения формулы (IV) A1 замещен C(N)C(O)R1 и R1. В другом варианте воплощения формулы (IV) A1 замещен NHC(O)R1 и R1. В другом варианте воплощения формулы (IV) A1 замещен R1. В другом варианте воплощения формулы (IV) A1 замещен двумя независимо выбранными R1. В другом варианте воплощения формулы (IV) A1 замещен Cl. В другом варианте воплощения формулы (IV) A1 замещен CF3. В другом варианте воплощения формулы (IV) A1 замещен F. В другом варианте воплощения формулы (IV) A1 замещен тремя независимо выбранными R1 и C(O)OR1. В другом варианте воплощения формулы (IV) A1 представляет собой замещенный R1 и C(O)OR1. В другом варианте воплощения формулы (IV) A1 замещен R1 и Cl. В другом варианте воплощения формулы (IV) A1 замещен R1 и Br. В другом варианте воплощения формулы (IV) A1 замещен тремя независимо выбранными R1. В другом варианте воплощения формулы (IV) A1 замещен C(O)NHR1. В другом варианте воплощения формулы (IV) A1 замещен двумя независимо выбранными R1 и Cl. В другом варианте воплощения формулы (IV) A1 замещен R1 и NO2. В другом варианте воплощения формулы (IV) A1 замещен NHR1 и NO2. В другом варианте воплощения формулы (IV) A1 замещен (О). В другом варианте воплощения формулы (IV) A1 замещен OR1.
В одном варианте воплощения формулы (IV) R1 представляет собой фенил. В другом варианте воплощения формулы (IV) R1 представляет собой пиразолил. В другом варианте воплощения формулы (IV) R1 представляет собой морфолинил. В другом варианте воплощения формулы (IV) R1 представляет собой изоксазолил. В другом варианте воплощения формулы (IV) R1 представляет собой пиперидинил. В другом варианте воплощения формулы (IV) R1 представляет собой алкил, который не замещен. В другом варианте воплощения формулы (IV) R1 представляет собой алкил, который замещен одним или несколькими R7, SR7, N(R7)2, NHC(O)R7 или Cl.
В одном варианте воплощения формулы (IV) R7 представляет собой фенил. В одном варианте воплощения формулы (IV) R7 представляет собой метил. В одном варианте воплощения формулы (IV) R7 представляет собой изопропил. В одном варианте воплощения формулы (IV) R7 представляет собой пирролинил. В одном варианте воплощения формулы (IV) R7 представляет собой морфолинил. В одном варианте воплощения формулы (IV) R7 представляет собой тетрагидропиранил.
Другой вариант осуществления настоящего изобретения касается соединений или их терапевтически приемлемых солей, пролекарств, метаболитов или солей пролекарств указанных соединений, которые пригодны в качестве ингибиторов антиапоптотических белков Bcl-2, при этом указанные соединения имеют формулу (V)
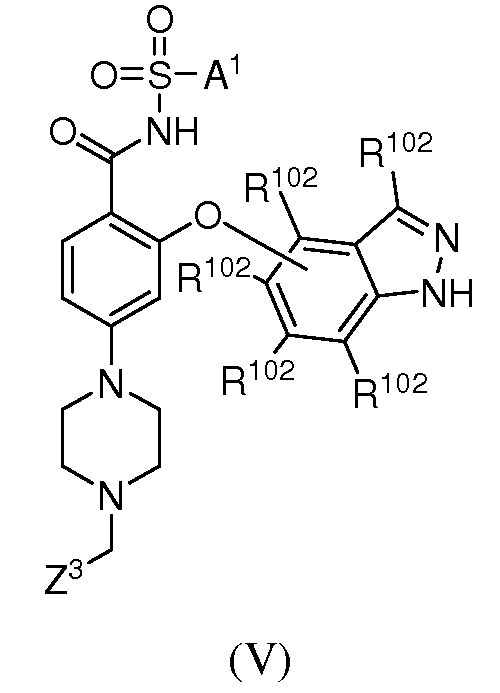
где R102 представляет собой точку присоединения к индазолу, а остальные обозначают Н или имеют значения, приведенные для заместителей при R42, а значения A1 и Z3 приведены в формуле (I).
В одном варианте воплощения формулы (V) A1 представляет собой фурил, имидазолил, изотиазолил, изоксазолил, пиразолил, пирролил, тиазолил, тиадиазолил, тиенил, триазолил, гетероциклоалкил или гетероциклоалкенил; каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или A1A; и A1A представляет собой гетероциклоалкен. В другом варианте воплощения формулы (V) A1 представляет собой фурил. В другом варианте воплощения формулы (V) A1 представляет собой имидазолил. В другом варианте воплощения формулы (V) A1 представляет собой изотиазолил. В другом варианте воплощения формулы (V) A1 представляет собой изоксазолил. В другом варианте воплощения формулы (V) A1 представляет собой пиразолил. В другом варианте воплощения формулы (V) A1 представляет собой пирролил. В другом варианте воплощения формулы (V) A1 представляет собой тиазолил. В другом варианте воплощения формулы (V) A1 представляет собой тиадиазолил. В другом варианте воплощения формулы (V) A1 представляет собой тиенил. В другом варианте воплощения формулы (V) A1 представляет собой триазолил. В другом варианте воплощения формулы (V) A1 представляет собой гетероциклоалкил. В другом варианте воплощения формулы (V) A1 представляет собой гетероциклоалкенил. В другом варианте воплощения формулы (V) A1 представляет собой пиперидинил. В другом варианте воплощения формулы (V) A1 представляет собой морфолинил. В другом варианте воплощения формулы (V) A1 представляет собой дигидро-1,3,4-тиадиазол-2-ил. В другом варианте воплощения формулы (V) A1 представляет собой бензотиен-2-ил. В другом варианте воплощения формулы (V) A1 представляет собой бензотиазол-2-ил. В другом варианте воплощения формулы (V) A1 представляет собой [1,2,4]триазоло[1,5-a]пиримидин-2-ил. В другом варианте воплощения формулы (V) A1 представляет собой тетрагидротиен-3-ил. В другом варианте воплощения формулы (V) A1 представляет собой [1,2,4]триазоло[1,5-a]пиримидин-2-ил. В другом варианте воплощения формулы (V) A1 представляет собой имидазо[2,1-b][1,3]тиазол-5-ил.
В одном варианте воплощения формулы (V) A1 не замещен. В другом варианте воплощения формулы (V) A1 замещен одним, или двумя, или тремя, или четырьмя, или пятью независимо выбранными заместителями R1, OR1, C(O)OR1, NHR1, N(R1)2, C(N)C(O)R1, C(O)NHR1, NHC(O)R1, NR1C(O)R1, (О), NO2, F, Cl, Br, I или CF3. В одном варианте воплощения формулы (V) A1 не замещен. В другом варианте воплощения формулы (V) A1 замещен NHR1. В другом варианте воплощения формулы (V) A1 замещен NHR1 и NO2. В другом варианте воплощения формулы (V) A1 замещен NHR1. В другом варианте воплощения формулы (V) A1 замещен NR1C(O)R1. В другом варианте воплощения формулы (V) A1 замещен N(R1)2. В другом варианте воплощения формулы (V) A1 замещен C(N)C(O)R1 и R1. В другом варианте воплощения формулы (V) A1 замещен NHC(O)R1 и R1. В другом варианте воплощения формулы (V) A1 замещен R1. В другом варианте воплощения формулы (V) A1 замещен двумя независимо выбранными R1. В другом варианте воплощения формулы (V) A1 замещен Cl. В другом варианте воплощения формулы (V) A1 замещен CF3. В другом варианте воплощения формулы (V) A1 замещен F. В другом варианте воплощения формулы (V) A1 замещен тремя независимо выбранными R1 и C(O)OR1. В другом варианте воплощения формулы (V) A1 представляет собой замещенный R1 и C(O)OR1. В другом варианте воплощения формулы (V) A1 замещен R1 и Cl. В другом варианте воплощения формулы (V) A1 замещен R1 и Br. В другом варианте воплощения формулы (V) A1 замещен тремя независимо выбранными R1. В другом варианте воплощения формулы (V) A1 замещен C(O)NHR1. В другом варианте воплощения формулы (V) A1 замещен двумя независимо выбранными R1 и Cl. В другом варианте воплощения формулы (V) A1 замещен R1 и NO2. В другом варианте воплощения формулы (V) A1 замещен NHR1 и NO2. В другом варианте воплощения формулы (V) A1 замещен (О). В другом варианте воплощения формулы (V) A1 замещен OR1.
В одном варианте воплощения формулы (V) R1 представляет собой фенил. В другом варианте воплощения формулы (V) R1 представляет собой пиразолил. В другом варианте воплощения формулы (V) R1 представляет собой морфолинил. В другом варианте воплощения формулы (V) R1 представляет собой изоксазолил. В другом варианте воплощения формулы (V) R1 представляет собой пиперидинил. В другом варианте воплощения формулы (V) R1 представляет собой алкил, который не замещен. В другом варианте воплощения формулы (V) R1 представляет собой алкил, который замещен одним или несколькими R7, SR7, N(R7)2, NHC(O)R7 или Cl.
В одном варианте воплощения формулы (V) R7 представляет собой фенил. В одном варианте воплощения формулы (V) R7 представляет собой метил. В одном варианте воплощения формулы (V) R7 представляет собой изопропил. В одном варианте воплощения формулы (V) R7 представляет собой пирролинил. В одном варианте воплощения формулы (V) R7 представляет собой морфолинил. В одном варианте воплощения формулы (V) R7 представляет собой тетрагидропиранил.
Еще один вариант осуществления настоящего изобретения касается соединений, имеющих формулу V, которые представляют собой
трет-бутил (2S)-2-{[(5-{[4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-2-(1H-индазол-4-илокси)бензоил]сульфамоил}-4-метил-1,3-тиазол-2-ил)окси]метил}морфолин-4-карбоксилат;
4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-({2-[(4-фтортетрагидро-2H-пиран-4-ил)метокси]-4-метил-1,3-тиазол-5-ил}сульфонил)-2-(1H-индазол-4-илокси)бензамид;
и их терапевтически приемлемые соли, пролекарства, соли пролекарств и метаболиты.
Другой вариант осуществления настоящего изобретения касается соединений или их терапевтически приемлемых солей, пролекарств, метаболитов или солей пролекарств указанных соединений, которые пригодны в качестве ингибиторов антиапоптотических белков Bcl-2, при этом указанные соединения имеют формулу (VI)

где R102 представляет собой точку присоединения к бензиндазолу, а остальные обозначают Н или имеют значения, приведенные для заместителей при R42, а значения A1 и Z3 приведены в формуле (I).
В одном варианте воплощения формулы (VI) A1 представляет собой фурил, имидазолил, изотиазолил, изоксазолил, пиразолил, пирролил, тиазолил, тиадиазолил, тиенил, триазолил, гетероциклоалкил или гетероциклоалкенил; каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или A1A; A1A представляет собой гетероциклоалкен. В другом варианте воплощения формулы (VI) A1 представляет собой фурил. В другом варианте воплощения формулы (VI) A1 представляет собой имидазолил. В другом варианте воплощения формулы (VI) A1 представляет собой изотиазолил. В другом варианте воплощения формулы (VI) A1 представляет собой изоксазолил. В другом варианте воплощения формулы (VI) A1 представляет собой пиразолил. В другом варианте воплощения формулы (VI) A1 представляет собой пирролил. В другом варианте воплощения формулы (VI) A1 представляет собой тиазолил. В другом варианте воплощения формулы (VI) A1 представляет собой тиадиазолил. В другом варианте воплощения формулы (VI) A1 представляет собой тиенил. В другом варианте воплощения формулы (VI) A1 представляет собой триазолил. В другом варианте воплощения формулы (VI) A1 представляет собой гетероциклоалкил. В другом варианте воплощения формулы (VI) A1 представляет собой гетероциклоалкенил. В другом варианте воплощения формулы (VI) A1 представляет собой пиперидинил. В другом варианте воплощения формулы (VI) A1 представляет собой морфолинил. В другом варианте воплощения формулы (VI) A1 представляет собой дигидро-1,3,4-тиадиазол-2-ил. В другом варианте воплощения формулы (VI) A1 представляет собой бензотиен-2-ил. В другом варианте воплощения формулы (VI) A1 представляет собой бензотиазол-2-ил. В другом варианте воплощения формулы (VI) A1 представляет собой [1,2,4]триазоло[1,5-a]пиримидин-2-ил. В другом варианте воплощения формулы (VI) A1 представляет собой тетрагидротиен-3-ил. В другом варианте воплощения формулы (VI) A1 представляет собой [1,2,4]триазоло[1,5-a]пиримидин-2-ил. В другом варианте воплощения формулы (VI) A1 представляет собой имидазо[2,1-b][1,3]тиазол-5-ил.
В одном варианте воплощения формулы (VI) A1 не замещен. В другом варианте воплощения формулы (VI) A1 замещен одним, или двумя, или тремя, или четырьмя, или пятью независимо выбранными заместителями R1, OR1, C(O)OR1, NHR1, N(R1)2, C(N)C(O)R1, C(O)NHR1, NHC(O)R1, NR1C(O)R1, (О), NO2, F, Cl, Br, I или CF3. В одном варианте воплощения формулы (VI) A1 не замещен. В другом варианте воплощения формулы (VI) A1 замещен NHR1. В другом варианте воплощения формулы (VI) A1 замещен NHR1 и NO2. В другом варианте воплощения формулы (VI) A1 замещен NHR1. В другом варианте воплощения формулы (VI) A1 замещен NR1C(O)R1. В другом варианте воплощения формулы (VI) A1 замещен N(R1)2. В другом варианте воплощения формулы (VI) A1 замещен C(N)C(O)R1 и R1. В другом варианте воплощения формулы (VI) A1 замещен NHC(O)R1 и R1. В другом варианте воплощения формулы (VI) A1 замещен R1. В другом варианте воплощения формулы (VI) A1 замещен двумя независимо выбранными R1. В другом варианте воплощения формулы (VI) A1 замещен Cl. В другом варианте воплощения формулы (VI) A1 замещен CF3. В другом варианте воплощения формулы (VI) A1 замещен F. В другом варианте воплощения формулы (VI) A1 замещен тремя независимо выбранными R1 и C(O)OR1. В другом варианте воплощения формулы (VI) A1 представляет собой замещенный R1 и C(O)OR1. В другом варианте воплощения формулы (VI) A1 замещен R1 и Cl. В другом варианте воплощения формулы (VI) A1 замещен R1 и Br. В другом варианте воплощения формулы (VI) A1 замещен тремя независимо выбранными R1. В другом варианте воплощения формулы (VI) A1 замещен C(O)NHR1. В другом варианте воплощения формулы (VI) A1 замещен двумя независимо выбранными R1 и Cl. В другом варианте воплощения формулы (VI) A1 замещен R1 и NO2. В другом варианте воплощения формулы (VI) A1 замещен NHR1 и NO2. В другом варианте воплощения формулы (VI) A1 замещен (О). В другом варианте воплощения формулы (VI) A1 замещен OR1.
В одном варианте воплощения формулы (VI) R1 представляет собой фенил. В другом варианте воплощения формулы (VI) R1 представляет собой пиразолил. В другом варианте воплощения формулы (VI) R1 представляет собой морфолинил. В другом варианте воплощения формулы (VI) R1 представляет собой изоксазолил. В другом варианте воплощения формулы (VI) R1 представляет собой пиперидинил. В другом варианте воплощения формулы (VI) R1 представляет собой алкил, который не замещен. В другом варианте воплощения формулы (VI) R1 представляет собой алкил, который замещен одним или несколькими R7, SR7, N(R7)2, NHC(O)R7 или Cl.
В одном варианте воплощения формулы (VI) R7 представляет собой фенил. В одном варианте воплощения формулы (VI) R7 представляет собой метил. В одном варианте воплощения формулы (VI) R7 представляет собой изопропил. В одном варианте воплощения формулы (VI) R7 представляет собой пирролинил. В одном варианте воплощения формулы (VI) R7 представляет собой морфолинил. В одном варианте воплощения формулы (VI) R7 представляет собой тетрагидропиранил.
Еще один вариант осуществления настоящего изобретения касается соединений, имеющих формулу VI, которые представляют собой
трет-бутил (2S)-2-{[(5-{[2-(1H-бензимидазол-4-илокси)-4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)бензоил]сульфамоил}-4-метил-1,3-тиазол-2-ил)окси]метил}морфолин-4-карбоксилат;
2-(1H-бензимидазол-4-илокси)-4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-({2-[(4-фтортетрагидро-2H-пиран-4-ил)метокси]-4-метил-1,3-тиазол-5-ил}сульфонил)бензамид;
и их терапевтически приемлемые соли, пролекарства, соли пролекарств и метаболиты.
Другой вариант осуществления настоящего изобретения касается соединений или их терапевтически приемлемых солей, пролекарств, метаболитов или солей пролекарств указанных соединений, которые пригодны в качестве ингибиторов антиапоптотических белков Bcl-2, при этом указанные соединения имеют формулу (VII)

где R102 представляет собой точку присоединения к пиридину, а остальные обозначают Н или имеют значения, приведенные для заместителей при R42, а значения A1 и Z3 приведены в формуле (I).
В одном варианте воплощения формулы (VII) A1 представляет собой фурил, имидазолил, изотиазолил, изоксазолил, пиразолил, пирролил, тиазолил, тиадиазолил, тиенил, триазолил, гетероциклоалкил или гетероциклоалкенил; каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или A1A; A1A представляет собой гетероциклоалкен. В другом варианте воплощения формулы (VII) A1 представляет собой фурил. В другом варианте воплощения формулы (VII) A1 представляет собой имидазолил. В другом варианте воплощения формулы (VII) A1 представляет собой изотиазолил. В другом варианте воплощения формулы (VII) A1 представляет собой изоксазолил. В другом варианте воплощения формулы (VII) A1 представляет собой пиразолил. В другом варианте воплощения формулы (VII) A1 представляет собой пирролил. В другом варианте воплощения формулы (VII) A1 представляет собой тиазолил. В другом варианте воплощения формулы (VII) A1 представляет собой тиадиазолил. В другом варианте воплощения формулы (VII) A1 представляет собой тиенил. В другом варианте воплощения формулы (VII) A1 представляет собой триазолил. В другом варианте воплощения формулы (VII) A1 представляет собой гетероциклоалкил. В другом варианте воплощения формулы (VII) A1 представляет собой гетероциклоалкенил. В другом варианте воплощения формулы (VII) A1 представляет собой пиперидинил. В другом варианте воплощения формулы (VII) A1 представляет собой морфолинил. В другом варианте воплощения формулы (VII) A1 представляет собой дигидро-1,3,4-тиадиазол-2-ил. В другом варианте воплощения формулы (VII) A1 представляет собой бензотиен-2-ил. В другом варианте воплощения формулы (VII) A1 представляет собой бензотиазол-2-ил. В другом варианте воплощения формулы (VII) A1 представляет собой [1,2,4]триазоло[1,5-a]пиримидин-2-ил. В другом варианте воплощения формулы (VII) A1 представляет собой тетрагидротиен-3-ил. В другом варианте воплощения формулы (VII) A1 представляет собой [1,2,4]триазоло[1,5-a]пиримидин-2-ил. В другом варианте воплощения формулы (VII) A1 представляет собой имидазо[2,1-b][1,3]тиазол-5-ил.
В одном варианте воплощения формулы (VII) A1 не замещен. В другом варианте воплощения формулы (VII) A1 замещен одним, или двумя, или тремя, или четырьмя, или пятью независимо выбранными заместителями R1, OR1, C(O)OR1, NHR1, N(R1)2, C(N)C(O)R1, C(O)NHR1, NHC(O)R1, NR1C(O)R1, (О), NO2, F, Cl, Br, I или CF3. В одном варианте воплощения формулы (VII) A1 не замещен. В другом варианте воплощения формулы (VII) A1 замещен NHR1. В другом варианте воплощения формулы (VII) A1 замещен NHR1 и NO2. В другом варианте воплощения формулы (VII) A1 замещен NHR1. В другом варианте воплощения формулы (VII) A1 замещен NR1C(O)R1. В другом варианте воплощения формулы (VII) A1 замещен N(R1)2. В другом варианте воплощения формулы (VII) A1 замещен C(N)C(O)R1 и R1. В другом варианте воплощения формулы (VII) A1 замещен NHC(O)R1 и R1. В другом варианте воплощения формулы (VII) A1 замещен R1. В другом варианте воплощения формулы (VII) A1 замещен двумя независимо выбранными R1. В другом варианте воплощения формулы (VII) A1 замещен Cl. В другом варианте воплощения формулы (VII) A1 замещен CF3. В другом варианте воплощения формулы (VII) A1 замещен F. В другом варианте воплощения формулы (VII) A1 замещен тремя независимо выбранными R1 и C(O)OR1. В другом варианте воплощения формулы (VII) A1 представляет собой замещенный R1 и C(O)OR1. В другом варианте воплощения формулы (VII) A1 замещен R1 и Cl. В другом варианте воплощения формулы (VII) A1 замещен R1 и Br. В другом варианте воплощения формулы (VII) A1 замещен тремя независимо выбранными R1. В другом варианте воплощения формулы (VII) A1 замещен C(O)NHR1. В другом варианте воплощения формулы (VII) A1 замещен двумя независимо выбранными R1 и Cl. В другом варианте воплощения формулы (VII) A1 замещен R1 и NO2. В другом варианте воплощения формулы (VII) A1 замещен NHR1 и NO2. В другом варианте воплощения формулы (VII) A1 замещен (О). В другом варианте воплощения формулы (VII) A1 замещен OR1.
В одном варианте воплощения формулы (VII) R1 представляет собой фенил. В другом варианте воплощения формулы (VII) R1 представляет собой пиразолил. В другом варианте воплощения формулы (VII) R1 представляет собой морфолинил. В другом варианте воплощения формулы (VII) R1 представляет собой изоксазолил. В другом варианте воплощения формулы (VII) R1 представляет собой пиперидинил. В другом варианте воплощения формулы (VII) R1 представляет собой алкил, который не замещен. В другом варианте воплощения формулы (VII) R1 представляет собой алкил, который замещен одним или несколькими R7, SR7, N(R7)2, NHC(O)R7 или Cl.
В одном варианте воплощения формулы (VII) R7 представляет собой фенил. В одном варианте воплощения формулы (VII) R7 представляет собой метил. В одном варианте воплощения формулы (VII) R7 представляет собой изопропил. В одном варианте воплощения формулы (VII) R7 представляет собой пирролинил. В одном варианте воплощения формулы (VII) R7 представляет собой морфолинил. В одном варианте воплощения формулы (VII) R7 представляет собой тетрагидропиранил.
Другой вариант осуществления настоящего изобретения касается соединений или их терапевтически приемлемых солей, пролекарств, метаболитов или солей пролекарств указанных соединений, которые пригодны в качестве ингибиторов антиапоптотических белков Bcl-2, при этом указанные соединения имеют формулу (VIII)

где каждый R102 независимо представляет собой Н или имеет значения, приведенные для заместителей при R42, а значения A1 и Z3 приведены в формуле (I).
В одном варианте воплощения формулы (VIII) A1 представляет собой фурил, имидазолил, изотиазолил, изоксазолил, пиразолил, пирролил, тиазолил, тиадиазолил, тиенил, триазолил, гетероциклоалкил или гетероциклоалкенил; каждый из которых не конденсирован или конденсирован с бензолом, гетероареном или A1A; A1A представляет собой гетероциклоалкен. В другом варианте воплощения формулы (VIII) A1 представляет собой фурил. В другом варианте воплощения формулы (VIII) A1 представляет собой имидазолил. В другом варианте воплощения формулы (VIII) A1 представляет собой изотиазолил. В другом варианте воплощения формулы (VIII) A1 представляет собой изоксазолил. В другом варианте воплощения формулы (VIII) A1 представляет собой пиразолил. В другом варианте воплощения формулы (VIII) A1 представляет собой пирролил. В другом варианте воплощения формулы (VIII) A1 представляет собой тиазолил. В другом варианте воплощения формулы (VIII) A1 представляет собой тиадиазолил. В другом варианте воплощения формулы (VIII) A1 представляет собой тиенил. В другом варианте воплощения формулы (VIII) A1 представляет собой триазолил. В другом варианте воплощения формулы (VIII) A1 представляет собой гетероциклоалкил. В другом варианте воплощения формулы (VIII) A1 представляет собой гетероциклоалкенил. В другом варианте воплощения формулы (VIII) A1 представляет собой пиперидинил. В другом варианте воплощения формулы (VIII) A1 представляет собой морфолинил. В другом варианте воплощения формулы (VIII) A1 представляет собой дигидро-1,3,4-тиадиазол-2-ил. В другом варианте воплощения формулы (VIII) A1 представляет собой бензотиен-2-ил. В другом варианте воплощения формулы (VIII) A1 представляет собой бензотиазол-2-ил. В другом варианте воплощения формулы (VIII) A1 представляет собой [1,2,4]триазоло[1,5-a]пиримидин-2-ил. В другом варианте воплощения формулы (VIII) A1 представляет собой тетрагидротиен-3-ил. В другом варианте воплощения формулы (VIII) A1 представляет собой [1,2,4]триазоло[1,5-a]пиримидин-2-ил. В другом варианте воплощения формулы (VIII) A1 представляет собой имидазо[2,1-b][1,3]тиазол-5-ил.
В одном варианте воплощения формулы (VIII) A1 не замещен. В другом варианте воплощения формулы (VIII) A1 замещен одним, или двумя, или тремя, или четырьмя, или пятью независимо выбранными заместителями R1, OR1, C(O)OR1, NHR1, N(R1)2, C(N)C(O)R1, C(O)NHR1, NHC(O)R1, NR1C(O)R1, (О), NO2, F, Cl, Br, I или CF3. В одном варианте воплощения формулы (VIII) A1 не замещен. В другом варианте воплощения формулы (VIII) A1 замещен NHR1. В другом варианте воплощения формулы (VIII) A1 замещен NHR1 и NO2. В другом варианте воплощения формулы (VIII) A1 замещен NHR1. В другом варианте воплощения формулы (VIII) A1 замещен NR1C(O)R1. В другом варианте воплощения формулы (VIII) A1 замещен N(R1)2. В другом варианте воплощения формулы (VIII) A1 замещен C(N)C(O)R1 и R1. В другом варианте воплощения формулы (VIII) A1 замещен NHC(O)R1 и R1. В другом варианте воплощения формулы (VIII) A1 замещен R1. В другом варианте воплощения формулы (VIII) A1 замещен двумя независимо выбранными R1. В другом варианте воплощения формулы (VIII) A1 замещен Cl. В другом варианте воплощения формулы (VIII) A1 замещен CF3. В другом варианте воплощения формулы (VIII) A1 замещен F. В другом варианте воплощения формулы (VIII) A1 замещен тремя независимо выбранными R1 и C(O)OR1. В другом варианте воплощения формулы (VIII) A1 представляет собой замещенный R1 и C(O)OR1. В другом варианте воплощения формулы (VIII) A1 замещен R1 и Cl. В другом варианте воплощения формулы (VIII) A1 замещен R1 и Br. В другом варианте воплощения формулы (VIII) A1 замещен тремя независимо выбранными R1. В другом варианте воплощения формулы (VIII) A1 замещен C(O)NHR1. В другом варианте воплощения формулы (VIII) A1 замещен двумя независимо выбранными R1 и Cl. В другом варианте воплощения формулы (VIII) A1 замещен R1 и NO2. В другом варианте воплощения формулы (VIII) A1 замещен NHR1 и NO2. В другом варианте воплощения формулы (VIII) A1 замещен (О). В другом варианте воплощения формулы (VIII) A1 замещен OR1.
В одном варианте воплощения формулы (VIII) R1 представляет собой фенил. В другом варианте воплощения формулы (VIII) R1 представляет собой пиразолил. В другом варианте воплощения формулы (VIII) R1 представляет собой морфолинил. В другом варианте воплощения формулы (VIII) R1 представляет собой изоксазолил. В другом варианте воплощения формулы (VIII) R1 представляет собой пиперидинил. В другом варианте воплощения формулы (VIII) R1 представляет собой алкил, который не замещен. В другом варианте воплощения формулы (VIII) R1 представляет собой алкил, который замещен одним или несколькими R7, SR7, N(R7)2, NHC(O)R7 или Cl.
В одном варианте воплощения формулы (VIII) R7 представляет собой фенил. В одном варианте воплощения формулы (VIII) R7 представляет собой метил. В одном варианте воплощения формулы (VIII) R7 представляет собой изопропил. В одном варианте воплощения формулы (VIII) R7 представляет собой пирролинил. В одном варианте воплощения формулы (VIII) R7 представляет собой морфолинил. В одном варианте воплощения формулы (VIII) R7 представляет собой тетрагидропиранил.
Еще один вариант осуществления настоящего изобретения касается соединений, имеющих формулу VIII, которые представляют собой
трет-бутил (2S)-2-{[(5-{[4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-2-(1H-пирроло[2,3-b]пиридин-5-илокси)бензоил]сульфамоил}-4-метил-1,3-тиазол-2-ил)окси]метил}морфолин-4-карбоксилат;
4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-({2-[(4-фтортетрагидро-2H-пиран-4-ил)метокси]-4-метил-1,3-тиазол-5-ил}сульфонил)-2-(1H-пирроло[2,3-b]пиридин-5-илокси)бензамид;
и их терапевтически приемлемые соли, пролекарства, соли пролекарств и метаболиты.
Фармацевтические композиции, комбинированная терапия, способы лечения и способы введения лекарственных средств
Другой вариант осуществления настоящего изобретения относится к терапевтическим композициям, включающим соединения, имеющие формулу (I), и инертный наполнитель.
Другой вариант осуществления настоящего изобретения относится к способам лечения рака у млекопитающего, который включает введение указанному млекопитающему терапевтически приемлемого количества соединения, имеющего формулу (I).
Другой вариант осуществления настоящего изобретения относится к способам лечения аутоиммунного заболевания у млекопитающего, который включает введение указанному млекопитающему терапевтически приемлемого количества соединения, имеющего формулу (I).
Еще один вариант осуществления настоящего изобретения касается композиций для лечения заболеваний, во время которых экспрессируются антиапоптотические белки Bcl-2, при этом указанные композиции включают инертный наполнитель и терапевтически эффективное количество соединения, имеющего формулу (I).
Еще один вариант осуществления настоящего изобретения касается способов лечения заболеваний у пациента, во время которых экспрессируются антиапоптотические белки Bcl-2, при этом указанные композиции включают инертный наполнитель и терапевтически эффективное количество соединения, имеющего формулу (I).
Еще один вариант осуществления настоящего изобретения касается композиций для лечения рака мочевого пузыря, рака мозга, рака молочной железы, рака костного мозга, рака шейной области, хронического лимфолейкоза, колоректального рака, рака пищевода, гепатоцеллюлярного рака, лимфобластного лейкоза, фолликулярной лимфомы, лимфолейкоза, вызываемого Т-лимфоцитами или В-клетками, меланомы, миелогенного лейкоза, миеломы, рака полости рта, рака яичников, немелкоклеточного рака легкого, рака простаты, мелкоклеточного рака легкого или рака селезенки у пациента, при этом указанные композиции включают инертный наполнитель и терапевтически эффективное количество соединения, имеющего формулу (I).
Другой вариант осуществления настоящего изобретения касается способа лечения рака мочевого пузыря, рака мозга, рака молочной железы, рака костного мозга, рака шейной области, хронического лимфолейкоза, колоректального рака, рака пищевода, гепатоцеллюлярного рака, лимфобластного лейкоза, фолликулярной лимфомы, лимфолейкоза, вызываемого Т-лимфоцитами или В-клетками, меланомы, миелогенного лейкоза, миеломы, рака полости рта, рака яичников, немелкоклеточного рака легкого, рака простаты, мелкоклеточного рака легкого или рака селезенки у пациента, при этом указанные способы включает назначение пациенту терапевтически эффективного количества соединения, имеющего формулу (I).
Еще один вариант осуществления настоящего изобретения касается композиций для лечения заболеваний, при которых экспрессируются антиапоптотические белки Bcl-2, при этом указанные композиции включают инертный наполнитель и терапевтически эффективное количество дополнительного терапевтического средства или более одного дополнительного терапевтического средства.
Еще один вариант осуществления настоящего изобретения касается способов лечения заболеваний у пациента, во время которых экспрессируются антиапоптотические белки Bcl-2, при этом указанные способы включают назначение пациенту терапевтически эффективного количества соединения, имеющего формулу (I), и терапевтически эффективного количества дополнительного терапевтического средства или более одного дополнительного терапевтического средства.
Еще один вариант осуществления настоящего изобретения касается композиций для лечения рака мочевого пузыря, рака мозга, рака молочной железы, рака костного мозга, рака шейной области, хронического лимфолейкоза, колоректального рака, рака пищевода, гепатоцеллюлярного рака, лимфобластного лейкоза, фолликулярной лимфомы, лимфолейкоза, вызываемого Т-лимфоцитами или В-клетками, меланомы, миелогенного лейкоза, миеломы, рака полости рта, рака яичников, немелкоклеточного рака легкого, хронического лимфолейкоза, миеломы, рака простаты, мелкоклеточного рака легкого или рака селезенки у пациента, при этом указанные композиции включают инертный наполнитель и терапевтически эффективное количество соединения, имеющего формулу (I), и терапевтически эффективное количество дополнительного терапевтического средства или более одного дополнительного терапевтического средства.
Еще один вариант осуществления настоящего изобретения касается способов лечения рака мочевого пузыря, рака мозга, рака молочной железы, рака костного мозга, рака шейной области, хронического лимфолейкоза, колоректального рака, рака пищевода, гепатоцеллюлярного рака, лимфобластного лейкоза, фолликулярной лимфомы, лимфолейкоза, вызываемого Т-лимфоцитами или В-клетками, меланомы, миелогенного лейкоза, миеломы, рака полости рта, рака яичников, немелкоклеточного рака легкого, хронического лимфолейкоза, миеломы, рака простаты, мелкоклеточного рака легкого или рака селезенки у пациента, при этом указанные способы включают назначение пациенту терапевтически эффективного количества соединения формулы (I) и терапевтически эффективного количества дополнительного терапевтического средства или более одного дополнительного терапевтического средства.
Метаболиты соединений формулы (I), образующиеся в процессе обмена в условиях in vitro или in vivo, также могут быть пригодны для лечения заболеваний, связанных с антиапоптотическими белками Bcl-2.
Некоторые прекурсоры соединений, которые подвергаются обмену в условиях in vitro или in vivo с образованием соединений, имеющих формулу (I), также могут быть пригодны для лечения заболеваний, связанных антиапоптотическими белками Bcl-2.
Соединения формулы (I) могут существовать как кислотно-аддитивные соли, основно-аддитивные соли или цвиттерионы. Соли соединений получают при их выделении или в процессе очистки соединений. Кислотно-аддитивными солями соединений являются такие соли, которые получают по реакции соединений с кислотой. Например, предполагается, что ацетатные, адипатные, альгинатные, бикарбонатные, цитратные, аспартатные, бензоатные, бензолсульфонатные, бисульфатные, бутиратные, камфоратные, камфорсульфонатные, диглюконатные, формиатные, фумаратные, глицерофосфатные, глутаматные, гемисульфатные, гептаноатные, гексаноатные, гидрохлоридные, гидробромидные, гидроиодидные, лактобионатные, лактатные, малеатные, мезитиленсульфонатные, метансульфонатные, нафтиленсульфонатные, никотинатные, оксалатные, памоатные, пектинатные, персульфатные, фосфатные, пикратные, пропионатные, сукцинатные, тартратные, тиоцианатные, трихлорацетатные, трифторацетатные, пара-тоуолсульфонатные и ундеканоатные соли соединений и их пролекарств входят в объем настоящего изобретения. Основно-аддитивными солями соединений являются такие соли, которые получают по реакции соединений с гидроксидом, карбонатом или бикарбонатом таких катионов, как литий, натрий, калий, кальций и магний.
Соединения формулы (I) можно вводить, например, буккально, офтальмически, перорально, осмотически, парентерально (внутримышечно, интраперитонеально, внутригрудинно, внутривенно, подкожно), ректально, местно, чрескожно или вагинально.
Терапевтически эффективные количества соединений, имеющих формулу (I), зависят от реципиента лечения, расстройства, лечение которого проводят, и серьезности расстройства, композиции, содержащей соединение, времени введения, пути введения, продолжительности лечения, действенности соединения, скорости его выведения из организма и от того, используют или не используют совместно другие лекарственные средства. Количество соединения формулы (I) по настоящему изобретению, которое используют для приготовления композиции, предназначенной для ежедневного введения пациенту в виде однократной дозы или в виде разделенных доз, составляет от приблизительно 0,03 до приблизительно 200 мг на кг массы тела. Композиции в виде однократной дозы содержат указанное количество или комбинацию частичных доз.
Соединения формулы (I) можно вводить вместе с инертным наполнителем или без инертного наполнителя. Инертные наполнители включают, например, инкапсулирующие вещества или такие добавки как агенты, ускоряющие абсорбцию, антиоксиданты, связующие соединения, буферные добавки, покрытия для таблеток, пигменты, разбавители, разрыхлители, эмульгаторы, сухие разбавители, наполнители, вкусовые добавки, увлажнители, лубриканты, ароматизаторы, консерванты, газы-вытеснители, способствующие высвобождению вещества, стерилизующие средства, подсластители, солюбилизаторы, смачивающие вещества и их смеси.
Инертные наполнители для приготовления композиций, включающих соединения формулы (I), которые предназначены для перорального введения в твердой дозировочной форме, включают, например, агар, альгиновую кислоту, гидроксид алюминия, бензиловый спирт, бензилбензоат, 1,3-бутиленгликоль, карбомеры, касторовое масло, целлюлозу, ацетат целлюлозы, масло какао, кукурузный крахмал, кукурузное масло, хлопковое масло, кросс-повидон, диглицериды, этанол, этилцеллюлозу, этиллаурат, этилолеат, сложные эфиры жирных кислот, желатин, масло из зародышей пшеницы, глюкозу, глицерин, масло земляных орехов, гидроксипропилметилцеллюлозу, изопропанол, изотонический физиологический раствор, лактозу, гидроксид магния, стеарат магния, солод, маннит, моноглицериды, оливковое масло, арахисовое масло, фосфат калия, картофельный крахмал, повидон, пропиленгликоль, раствор Рингера, сафлоровое масло, кунжутное масло, натрий-карбоксиметилцеллюлозу, фосфатные соли натрия, лаурилсульфат натрия, натриевое производное сорбита, соевое масло, стеариновые кислоты, стеарилфумарат, сахарозу, поверхностно-активные вещества, тальк, трагакант, тетрагидрофурфуриловый спирт, триглицериды, воду и их смеси. Инертные наполнители для приготовления композиций, включающих соединения формулы (I), которые предназначены для офтальмического или перорального введения в жидких дозировочных формах, включают, например, 1,3-бутиленгликоль, касторовое масло, кукурузное масло, хлопковое масло, этанол, сложные эфиры жирных кислот с сорбитаном, масло из зародышей пшеницы, арахисовое масло, глицерин, изопропанол, оливковое масло, полиэтиленгликоли, пропиленгликоли, кунжутное масло, воду и их смеси. Инертные наполнители для приготовления композиций, включающих соединения формулы (I), которые предназначены для осмотического введения, включают, например, хлорфторуглеводороды, этанол, воду и их смеси. Инертные наполнители для приготовления композиций, включающих соединения формулы (I), которые предназначены для парентерального введения, включают, например, 1,3-бутандиол, касторовое масло, кукурузное масло, хлопковое масло, декстрозу, масло из зародышей пшеницы, масло земляных орехов, липосомы, олеиновую кислоту, оливковое масло, арахисовое масло, раствор Рингера, сафлоровое масло, кунжутное масло, соевое масло, физиологический раствор по Фармакопее США или изотонический раствор хлорида натрия, воду и их смеси. Инертные наполнители для приготовления композиций, включающих соединения формулы (I), которые предназначены для ректального или вагинального введения, включают, например, масло какао, полиэтиленгликоль, воск и их смеси.
Ожидается, что соединения, имеющие формулу (I), будут пригодны для использования вместе с алкилирующими агентами, ингибиторами развития кровеносных сосудов, антителами, антиметаболитами, агентами, тормозящими процесс деления клеток, антипролиферативными агентами, противовирусными средствами, ингибиторами авроракиназы, другими ингибиторами ускорителей апоптоза (например, Bcl-xL, Bcl-w и Bfl-I), активаторами метаболических путей рецептора смерти, ингибиторами Bcr-Abl-киназы, BiTE антителами (биспецифическими активаторами Т-лимфоцитов), нагруженными лекарственными средствами антителами, модификаторами биологических реакций, ингибиторами циклин-зависимой киназы, ингибиторами клеточного цикла, ингибиторами циклооксигеназы-2, DVD, ингибиторами рецептора гомолога вирусного онкогена лейкоза (ErbB2), ингибиторами фактора роста, ингибиторами белка теплового шока (HSP)-90, ингибиторами гистондиацетилазы (HDAC), гормональными терапевтическими средствами, иммунологическими средствами, ингибиторами ингибиторов апоптотических белков (IAP), интеркалирующими антибиотиками, ингибиторами киназы, ингибиторами кинезина, ингибиторами Jak2, ингибиторами мишени рапамицина в клетках млекопитающих, микроРНК, ингибиторами митоген-активированной киназы, регулируемой внешними сигналами, мультиспецифическими связывающими белками, нестероидными противовоспалительными средствами (NSAID), ингибиторами поли-АДФ-рибозополимеразы (PARP), химиотерапевтическими средствами на основе платины, ингибиторами Polo-подобной киназы (Plk), ингибиторами фосфоинозитид-3-киназы (PI3K), ингибиторами протеосомы, аналогами пурина, аналогами пиримидина, ингибиторами рецептора тирозинкиназы, етиноидами/алкалоидами дельтоидных растений, малыми ингибиторными рибонуклеиновыми кислотами (siRNA), ингибиторами топоизомеразы, ингибиторами убиквитинлигазы и т.п., и в комбинации с одним или несколькими из указанных агентов.
BiTE антителами являются биспецифические антитела, которые направляют Т-лимфоциты на атаку раковых клеток, одновременно связывая обе указанные клетки. Затем Т-лимфоциты атакуют раковую клетку-мишень. Примеры BiTE антител включают адектумумаб (Micromet MT201), блинатумомаб (Micromet MT 103) и т.п. Не ограничивая себя какой-либо теорией, авторы настоящего изобретения полагают, что одним из механизмов, по которым Т-лимфоциты вызывают апоптоз раковой клетки-мишени, является экзоцитоз гранул цитолитических компонентов, которые включают перфорин и гранзим В. В связи с этим было показано, что Bcl-2 ослабляет индукцию апоптоза как под действием перфорина, так и гранзима B. Указанные данные позволяют предположить, что ингибирование Bcl-2 может усилить цитотоксическое действие Т-лимфоцитов, когда они нацеливаются на раковые клетки (V.R. Sutton, D.L. Vaux and J.A. Trapani, J. of Immunology 1997, 158 (12), 5783).
siRNA представляют собой молекулы, имеющие эндогенные основания РНК или химически модифицированные нуклеотиды. Модификации не отменяют клеточную активность, а, скорее, придают веществам повышенную устойчивость и/или увеличивают их внутриклеточную действенность. Примеры химических модификаций включают фосфоротиоатные группы, 2'-дезоксинуклеотиды, 2'-OCH3-содержащие рибонуклеотиды, 2'-F-рибонуклеотиды, 2'-метоксиэтилрибонуклеотиды, их комбинации и т.п. siRNA могут иметь различную длину (например, 10-200 пар оснований) и структуру (например, иметь форму шпильки, иметь одну/две спирали, петли, содержать однонитевые разрывы/двухнитевые разрывы, ошибочно-спаренные основания) и процессируются в клетках, способствуя активному подавлению транскрипции гена. Двуспиральная siRNA (dsRNA) может иметь то же самое число нуклеотидов на каждой спирали (тупые концы) или иметь асимметричные концы (“меченые” концы). 1-2 нуклеотида на “меченых” концах могут присутствовать на смысловой и/или антисмысловой спирали, а также присутствовать на 5'- и/или 3'-концах данной спирали. Например, было показано, что siRNA, нацеливающие Mcl-I, усиливают активность ABT-263 (т.е. N-(4-(4-((2-(4-хлорфенил)-5,5-диметил-1-циклогекс-1-ен-1-ил)метил)пиперазин-1-ил)бензоил)-4-(((1R)-3-(морфолин-4-ил)-1-((фенилсульфанил)метил)пропил)амино)-3-((трифторметил)сульфонил)бензолсульфонамид) или ABT-737 (т.е. N-(4-(4-((4'-хлор-(1,1'-бифенил)-2-ил)метил)пиперазин-1-ил)бензоил)-4-(((1R)-3-(диметиламино)-1-((фенилсульфанил)метил)пропил)амино)-3-нитробензолсульфонамид) во многих линиях опухолевых клеток (Tse et al., Cancer Research 2008, 68(9), 3421 и приведенные там ссылки).
Мультиспецифичные связывающие белки представляют собой связывающие белки, которые включают два или более мест связывания антигена. Мультиспецифичные связывающие белки конструируют таким образом, чтобы они имели три или более мест связывания антигена и в общем случае они являются антителами, не встречающимися в природе. Термин "мультиспецифичный связывающий белок" означает связывающий белок, который способен связывать две или более родственных или неродственных мишеней. Белки, связывающие двойной вариабельный домен (DVD), представляют собой четырехвалентные или многовалентные связывающие белки, которые включают два или более мест связывания антигена. Подобные DVD могут быть моноспецифичными (т.е. способными связывать один антиген) или мультиспецифичными (т.е. способными связывать два или более антигенов). Белки, связывающие DVD, которые включают два полипептида тяжелой цепи DVD и два полипептида легкой цепи DVD, обозначают как DVD Ig. Каждая половина DVD Ig включает полипептид тяжелой цепи DVD, полипептид легкой цепи DVD и два участка связывания антигена. Каждый участок связывания включает вариабельный домен тяжелой цепи и вариабельный домен легкой цепи, при этом в общей сложности 6 CDR принимают участие в процессе связывания антигена на один участок связывания антигена. Мультиспецифичные DVD включают белки, связывающие DVD, которые связывают DLL4 и VEGF, или C-met и EFGR, или ErbB3 и EGFR.
Алкилирующие агенты включают алтретамин, AMD-473, AP-5280, апазикон, бендамустин, бросталлицин, бусулфан, карбокон, кармустин (BCNU), хлорамбуцил, CLORETAZINE® (ларомустин, VNP 40101M), циклофосфамид, декарбазин, эстрамустин, фотемустин, глуфосфамид, ифосфамид, KW-2170, ломустин (CCNU), мафосфомид, мелфалан, митобронитол, митолактол, нимустин, N-оксид азотистого иприта, ранимустин, темозоломид, тиотепу, TREANDA® (бендамустин), треосульфан, рофосфамид и т.п.
Ингибиторы развития кровеносных сосудов включают ингибиторы эндотелийспецифичной рецепторной киназы (Tie-2), ингибиторы рецептора эпидермального фактора роста (EGFR), ингибиторы рецептора инсулинового фактора роста-2 (IGFR-2), ингибиторы матричной металлопротеиназы-2 (MMP-2), ингибиторы матричной металлопротеиназы-9 (MMP-9), ингибиторы рецептора фактора роста тромбоцитов (PDGFR), аналоги тромбоспондина, ингибиторы рецепторной киназы фактора роста эндотелия сосудов (VEGFR) и т.п.
Антиметаболиты включают ALIMTA® (пеметрексед динатрия, LY231514, MTA), 5-азацитидин, XELODA® (капецитабин), кармофур, LEUSTAT® (кладрибин), клофарабин, цитарабин, цитарабина окфосфат, цитозин арабинозид, децитабин, дефероксамин, доксифлуридин, эфлорнитин, EICAR (5-этинил-1-β-D-рибофуранозилимидазол-4-карбоксамид), еноцитабин, этнилцитидин, флударабин, 5-фтороурацил один или в комбинации с лейковорином, GEMZAR® (гемцитабин), гидроксимочевину, ALKERAN (мелфалан), меркаптопурин, 6-меркаптопуринрибозид, метотрексат, микофеноловую кислоту, неларабин, нолатрексед, окфосфат, пелитрексол, пентостатин, ралтитрексед, рибаварин, триапин, триметрексат, S-1, тиазофурин, тегафур, TS-1, видарабин, UFT и т.п.
Противовирусные средства включают ритонавир, гидроксихлорохин и т.п.
Ингибиторы авроракиназы ABT-348, AZD-1152, MLN-8054, VX-680, ингибиторы аврора-A-специфичной киназы, ингибиторы аврора-B-специфичной киназы и ингибиторы пан-авроракиназы и т.п.
Ингибиторы белка Bcl-2 включают AT-101 ((-)госсипол), GENASENSE® (G3139 или облимерсен (Bcl-2-нацеливающий антисмысловой олигонуклеотид)), IPI-194, IPI-565, N-(4-(4-((4'-хлор-(1,1'-бифенил)-2-ил)метил)пиперазин-1-ил)бензоил)-4-(((1R)-3-(диметиламино)-1-((фенилсульфанил)метил)пропил)амино)-3-нитробензолсульфонамид) (ABT-737), N-(4-(4-((2-(4-хлорфенил)-5,5-диметил-1-циклогекс-1-ен-1-ил)метил)пиперазин-1-ил)бензоил)-4-(((1R)-3-(морфолин-4-ил)-1-((фенилсульфанил)метил)пропил)амино)-3-((трифторметил)сульфонил)бензолсульфонамид (ABT-263), GX-070 (обатолакс) и т.п.
Ингибиторы Bcr-Abl-киназы включают DASATINIB® (BMS-354825), GLEEVEC® (иматиниб) и т.п.
Ингибиторы CDK включают AZD-5438, BMI-1040, BMS-032, BMS-387, CVT-2584, флавопиридол, GPC-286199, MCS-5A, PD0332991, PHA-690509, селициклиб (CYC-202, R-росковитин), ZK-304709 и т.п.
Ингибиторы COX-2 включают ABT-963, ARCOXIA® (эторикоксиб), BEXTRA® (валдекоксиб), BMS347070, CELEBREX® (целекоксиб), COX-189 (лумиракоксиб), CT-3, DERAMAXX® (деракоксиб), JTE-522, 4-метил-2-(3,4-диметилфенил)-1-(4-сульфамоилфенил-1H-пиррол), MK-663 (эторикоксиб), NS-398, парекоксиб, RS-57067, SC-58125, SD-8381, SVT-2016, S-2474, T-614, VIOXX® (рофекоксиб) и т.п.
Ингибиторы EGFR включают ABX-EGF, иммунолипосомы против EGFR, EGF-вакцину, EMD-7200, ERBITUX® (цетуксимаб), HR3, IgA антитела, IRESSA® (гефитиниб), TARCEVA® (эрлотиниб или OSI-774), TP-38, слитый белок EGFR, TYKERB® (лапатиниб) и т.п.
Ингибиторы рецептора ErbB2 включают CP-724-714, CI-1033 (канертиниб), HERCEPTIN® (трастузумаб), TYKERB® (лапатиниб), OMNITARG® (2C4, петузумаб), TAK-165, GW-572016 (ионафарниб), GW-282974, EKB-569, PI-166, dHER2 (вакцина HER2), APC-8024 (вакцина HER-2), биспецифичные антитела против HER/2neu, B7.her2IgG3, трифункциональные биспецифические антитела AS HER2, mAB AR-209, mAB 2B-1 и т.п.
Ингибиторы гистондеацетилазы включают депсипептид, LAQ-824, MS-275, трапоксин, субероиланилидгидроксамовую кислоту (SAHA), TSA, вальпроевую кислоту и т.п.
Ингибиторы HSP-90 включают 17-AAG-nab, 17-AAG, CNF-101, CNF-1010, CNF-2024, 17-DMAG, гелданамицин, IPI-504, KOS-953, MYCOGRAB® (рекомбинантное антитело человека к HSP-90), NCS-683664, PU24FC1, PU-3, радицикол, SNX-2112, STA-9090 VER49009 и т.п.
Ингибиторы ингибиторов апоптотических белков включают HGS1029, GDC-0145, GDC-0152, LCL-161, LBW-242 и т.п.
Антитела, нагруженные лекарственными средствами, включают анти-CD22-MC-MMAF, анти-CD22-MC-MMAE, анти-CD22-MCC-DM1, CR-011-vcMMAE, PSMA-ADC, MEDI-547, SGN-19Am SGN-35, SGN-75 и т.п.
Активаторы метаболических путей рецепторов смерти включают антитела или другие агенты, которые нацеливают TRAIL или рецепторы смерти (в частности, DR4 и DR5), такие как апомаб, конатумумаб, ETR2-ST01, GDC0145, (лексатумумаб), HGS-1029, LBY-135, PRO-1762 и трастузумаб.
Ингибиторы кинезина включают ингибиторы Eg5, такие как AZD4877, ARRY-520; ингибиторы CENPE, такие как GSK923295A и т.п.
Ингибиторы JAK-2 включают CEP-701 (лезауртиниб), XL019 и INCB018424 и т.п.
Ингибиторы MEK включают ARRY-142886, ARRY-438162 PD-325901, PD-98059 и т.п.
Ингибиторы mTOR включают AP-23573, CCI-779, эверолимус, RAD-001, рапамицин, темсиролимус, ингибиторы АТФ-конкурирующего TORC1/TORC2, включая PI-103, PP242, PP30, Torin 1 и т.п.
Нестероидные противовоспалительные средства включают AMIGESIC® (салсалат), DOLOBID® (дифлунизал), MOTRIN® (ибупрофен), ORUDIS® (кетопрофен), RELAFEN® (набуметон), FELDENE® (пироксикам), крем ибупрофена, ALEVE® (напроксен) и NAPROSYN® (напроксен), VOLTAREN® (диклофенак), INDOCIN® (индометацин), CLINORIL® (сулиндак), TOLECTIN® (толметин), LODINE® (этодолак), TORADOL® (кеторолак), DAYPRO® (оксапрозин) и т.п.
Ингибиторы PDGFR включают C-451, CP-673, CP-868596 и т.п.
Химиотерапевтические средства на основе платины включают цисплатин, ELOXATIN® (оксалиплатин), эптаплатин, лобаплатин, недаплатин, PARAPLATIN® (карбоплатин), сатраплатин, пикоплатин и т.п.
Ингибиторы Polo-подобной киназы включают BI-2536 и т.п.
Ингибиторы фосфоинозитид-3-киназы (PI3K) включают вортманнин, LY294002, XL-147, CAL-120, ONC-21, AEZS-127, ETP-45658, PX-866, GDC-0941, BGT226, BEZ235, XL765 и т.п.
Аналоги тромбоспондина включают ABT-510, ABT-567, ABT-898, TSP-1 и т.п.
Ингибиторы VEGFR включают AVASTIN® (бевацизумаб), ABT-869, AEE-788, ANGIOZYME™ (рибосома, которая подавляет развитие кровеносных сосудов (производители - компании Ribozyme Pharmaceuticals (Boulder, CO.) и Chiron, (Emeryville, CA)), акситиниб (AG-13736), AZD-2171, CP-547,632, IM-862, MACUGEN (пегаптамиб), NEXAVAR® (сорафениб, BAY43-9006), пазопаниб (GW-786034), ваталаниб (PTK-787, ZK-222584), SUTENT® (сунитиниб, SU-11248), VEGF trap, ZACTIMA™ (вандетаниб, ZD-6474), GA101, офатумумаб, ABT-806 (mAb-806), ErbB3-специфичные антитела, BSG2-специфичные антитела, DLL4-специфичные антитела и C-met-специфичные антитела и т.п.
Антибиотики включают интеркалирующие антибиотики акларубицин, актиномицин D, амрубицин, аннамицин, адриамицин, BLENOXANE® (блеомицин), даунорубицин, CAELYX® или MYOCET® (липосомальный доксорубицин), элсамитруцин, эпирбуцин, гларбуицин, ZAVEDOS® (идарубицин), митомицин C, неморубицин, неокарциностатин, пепломицин, пирарубицин, ребеккамицин, стималамер, стрептозоцин, VALSTAR® (валрубицин), зиностатин и т.п.
Ингибиторы топоизомеразы включают акларубицин, 9-аминокамптотецин, амонафид, амсакрин, бекатекацин, белотекан, BN-80915, CAMPTOSAR® (иринотекана гидрохлорид), камптотецин, CARDIOXANE® (дексразоксин), дифломотекан, эдотекарин, ELLENCE® или PHARMORUBICIN® (эпирубицин), этопозид, эксатекан, 10-гидроксикамптотецин, гиматекан, луртотекан, митоксантрон, оратецин, пирарбуцин, пиксантрон, рубитекан, собузоксан, SN-38, тафлупозид, топотекан и т.п.
Антитела включают AVASTIN® (бевацизумаб), CD40-специфичные антитела, chTNT-1/B, деносумаб, ERBITUX® (цетуксимаб), HUMAX-CD4® (занолимумаб), IGF1R-специфичные антитела, линтузумаб, PANOREX® (едреколомаб), RENCAREX® (WX G250), RITUXAN® (ритуксимаб), тицилимумаб, трастузимаб, CD20 антитела типа I и II и т.п.
Гормональные терапевтические средства включают ARIMIDEX® (анастрозол), AROMASIN® (ексеместан), арзоксифен, CASODEX® (бикалутамид), CETROTIDE® (цетрореликс), дегареликс, деслорелин, DESOPAN® (трилостан), дексаметазон, DROGENIL® (флутамид), EVISTA® (ралоксифен), AFEMA™ (фадрозол), FARESTON® (торемифен), FASLODEX® (фулвестрант), FEMARA® (летрозол), форместан, глюкокортикоиды, HECTOROL® (доксеркальциферол), RENAGEL® (севеламер карбонат), лазофоксифен, лейпролид ацетат, MEGACE® (мегестерол), MIFEPREX® (мифепристон), NILANDRON™ (нилутамид), NOLVADEX® (тамоксифен цитрат), PLENAXIS™ (абареликс), преднизон, PROPECIA® (финастерид), рилостан, SUPREFACT® (бусерелин), TRELSTAR® (рилизинг-фактор лютеинизирующего гормона (LHRH)), VANTAS® (имплант гистрелина), VETORYL® (трилостан или модрастан), ZOLADEX® (фосрелин, госерелин) и т.п.
Дельтоиды и ретиноиды включают сеокалцитол (EB 1089, CB 1093), лексакальцитрол (KH1060), фенретинид, PANRETIN® (алиретиноин), ATRAGEN® (липосомальный третиноин), TARGRETIN® (бексаротен), LGD-1550 и т.п.
Ингибиторы PARP включают ABT-888 (велипариб), олапариб, KU-59436, AZD-2281, AG-014699, BSI-201, BGP-15, INO-1001, ONO-2231 и т.п.
Растительные алкалоиды включают, однако этим не ограниваясь, винкристин, винбластин, виндезин, винорелбин и т.п.
Ингибиторы протеосомы включают VELCADE® (бортезомиб), MG132, NPI-0052, PR-171 и т.п.
Примеры иммунологических препаратов включают интерфероны и другие средства, укрепляющие иммунную систему. Интерфероны включают интерферон альфа, интерферон альфа-2a, интерферон альфа-2b, интерферон бета, интерферон гамма-1a, ACTIMMUNE® (интерферон гамма-1b) или интерферон гамма-n1, их комбинации и т.п. Другие агенты включают ALFAFERONE®, (IFN-α), BAM-002 (окисленный глутатион), BEROMUN® (тазонермин), BEXXAR® (тозитумомаб), CAMPATH® (алемтузумаб), CTLA4 (цитотоксический лимфоцитарный антиген 4), декарбазин, денилейкин, эпратузумаб, GRANOCYTE® (ленограстим), лентинан, лейкоцитарный альфа интерферон, имиквимод, MDX-010 (анти-CTLA-4), вакцину меланомы, митумомаб, молграмостим, MYLOTARG™ (гемтузумаб озогамицин), NEUPOGEN® (филграстим), OncoVAC-CL, OVAREX® (ореговомаб), пемтумомаб (Y-muHMFGl), PROVENGE® (сипулейцел-T), саргарамостим, сизофилан, тецелейкин, THERACYS® (бацилла Кальметта-Герена), убенимекс, VIRULIZIN® (иммунотерапевтический препарат от компании Lorus Pharmaceuticals), Z-100 (специфическое вещество Мурайяма (SSM)), WF-10 (тетрахлордекаоксид (TCDO)), PROLEUKIN® (алдеслейкин), ZADAXIN® (тималфазин), ZENAPAX® (даклизумаб), ZEVALIN® (90Y-ибритумомаб тиуксетан) и т.п.
Модификаторы биологической реакции представляют собой агенты, которые модифицируют защитные механизмы живых организмов или биологические реакции, такие как выживание, рост или дифференцировка тканевых клеток с тем, чтобы направить их на приобретение противоопухолевой активности, и включают крестин, лентинан, сизофиран, пицибанил PF-3512676 (CpG-8954), убенимекс и т.п.
Аналоги пиримидина включают цитарабин (ara C, или арабинозид C), цитозина арабинозид, доксифлуридин, FLUDARA® (флударабин), 5-FU (5-фторурацил), флоксуридин, GEMZAR® (гемцитабин), TOMUDEX® (ратитрексед), TROXATYL™ (триацетилуридин троксацитабин) и т.п.
Аналоги пурина включают LANVIS® (тиогуанин) и PURI-NETHOL® (меркаптопурин).
Агенты, тормозящие процесс деления клеток, включают батабулин, эпотилон D (KOS-862), N-(2-((4-гидроксифенил)амино)пиридин-3-ил)-4-метоксибензолсульфонамид, иксабепилон (BMS 247550), паклитаксел, TAXOTERE® (доцетаксел), PNU100940 (109881), патупилон, XRP-9881 (ларотаксел), винфлунин, ZK-EPO (синтетический эпотилон) и т.п.
Ингибиторы убиквитинлигазы включают ингибиторы MDM2, такие как нутлины, ингибиторы NEDD8, такие как MLN4924 и т.п.
Соединения по настоящему изобретению могут также использоваться в качестве агентов, повыщающих чувствительность к радиоактивным веществам, которые усиливают эффективность радиотерапии. Примеры радиотерапии включают внешнюю лучевую радиотерапию, телетерапию, брахитерапию и радиотерапию с использованием герметичного, негерметичного источника т.п.
Кроме того, соединения, имеющие формулу (I), можно объединять с другими химиотерапевтическими средствами, такими как ABRAXANE™ (ABI-007), ABT-100 (ингибитор фарнезилтрансферазы), ADVEXIN® (вакцина Ad5CMV-p53), ALTOCOR® или MEVACOR® (ловастатин), AMPLIGEN® (poly I:poly C12U, синтетическая РНК), APTOSYN® (эксисулинд), AREDIA® (памидроновая кислота), арглабин, L-аспарагиназа, атаместан (1-метил-3,17-дион-андроста-1,4-диен), AVAGE® (тазаротен), AVE-8062 (производное комбреастатина), BEC2 (мутимомаб), кахектин или кахексин (фактор некроза опухолей), канваксин (вакцина), CEAVAC® (раковая вакцина), CELEUK® (целмолейкин), CEPLENE® (гистамина гидрохлорид), CERVARIX® (вакцина вируса папилломы человека), CHOP® (C: CYTOXAN® (циклофосфамид); H: ADRIAMYCIN® (гидроксидоксорубицин); O: Vincristine (ONCOVIN®); P: преднизон), CYPAT™ (ципротерон ацетат), комбрестатин A4P, DAB(389)EGF (каталитические и транслокационные домены токсина дифтерии, слитые посредством линкера His-Ala с эпидермальным фактором роста человека) или TransMID-107R™ (токсины дифтерии), дакарбазин, дактиномицин, 5,6-диметилксантенон-4-уксусная кислота (DMXAA), енилурацил, EVIZON™ (скваламин лактат), DIMERICINE® (липосомальный лосьон T4N5), дискодермолид, DX-8951f (эксатекан мезилат), энзастаурин, EPO906 (эпитилон B), GARDASIL® (квадривалентная рекомбинатная вакцина против вируса папилломы человека (типы 6, 11, 16, 18)), GASTRIMMUNE®, GENASENSE®, GMK (вакцина конъюгата ганглиозида), GVAX® (вакцина рака простаты), халофугинон, гистерелин, гидроксикарбамид, ибандроновая кислота, IGN-101, IL-13-PE38, IL-13-PE38QQR (цинтредекин безутодокс), экзотоксин IL-13-псевдомоноза, интерферон-α, интерферон-γ, JUNOVAN™ или MEPACT™ (мифамуртид), лонафарниб, 5,10-метилентетрагидрофолат, милтефозин (гексадецилфосфохолин), NEOVASTAT® (AE-941), NEUTREXIN® (триметрексат глюкуронат), NIPENT® (пентостатин), ONCONASE® (фермент рибонуклеаза), ONCOPHAGE® (терапия с помощью вакцины против меланомы), ONCOVAX® (вакцина IL-2), ORATHECIN™ (рубитекан), OSIDEM® (клеточная терапия на основе антител), OVAREX® MAb (мышиное моноклональное антитело), паклитаксел, PANDIMEX™ (сапонины агликона из содержащего женьшень 20(S)протопанаксадиола (aPPD) и 20(S) протопанаксатриола (aPPT)), панитумумаб, PANVAC®-VF (экспериментальный препарат вакцины рака), пегаспаргаза, PEG интерферон A, феноксодиол, прокарбазин, ребимастат, REMOVAB® (катумаксомаб), REVLIMID® (леналидомид), RSR13 (эфапроксирал), SOMATULINE® LA (лантреотид), SORIATANE® (ацитретин), стауроспорин (Streptomyces staurospores), талабостат (PT100), TARGRETIN® (бексаротен), TAXOPREXIN® (DHA-паклитаксел), TELCYTA® (канфосфамид, TLK286), темилифен, TEMODAR® (темозоломид), тесмилифен, талидомид, THERATOPE® (STn-KLH), тимитак (2-амино-3,4-дигидро-6-метил-4-оксо-5-(4-пиридилтио)хиназолина дигидрохлорид), TNFERADE™ (носитель аденовектор: ДНК, содержащий ген фактора некроза опухолей α), TRACLEER® или ZAVESCA® (бозентан), третиноин (ретин-A), тетрандрин, TRISENOX® (триоксид мышьяка), VIRULIZIN®, украин (проиводные алкалоидов из растения большой чистотел), витаксин (антитело против alphavbeta3), XCYTRIN® (мотексафин гадолиний), XINLAY™ (астрасентан), XYOTAX™ (паклитаксел полиглумекс), YONDELIS® (трабектидин), ZD-6126, ZINECARD® (декстразоксан), ZOMETA® (золендроновая кислота), зорубицин и т.п.
Данные
Определение пригодности соединений формулы (I) в качестве агентов, которые связываются с антиапоптотическими белками Bcl-2 и ингибируют их, проводят с использованием анализа по методу резонансного переноса энергии флуоресценции с временным разрешением (TR-FRET). Антитело Tb-anti-GST приобретают у компании Invitrogen (номер по каталогу PV4216).
Синтез зондов
Все реагенты, если не указано иное, используют в том виде, в котором они получены от производителя. Реагенты для синтеза пептидов, включая диизопропилэтиламин (DIEA), дихлорметан (DCM), N-метилпирролидон (NMP), гексафторфосфат 2-(1H-бензотриазол-1-ил)-1,1,3,3-тетраметилурония (HBTU), N-гидроксибензотриазол (HOBt) и пиперидин, получены от компании Applied Biosystems, Inc. (ABI), Foster City, CA или American Bioanalytical, Natick, MA. Предварительно заполненные картриджи 9-флуоренилметоксикарбонил(Fmoc)-аминокислота (Fmoc-Ala-OH, Fmoc-Cys(Trt)-OH, Fmoc-Asp(tBu)-OH, Fmoc-Glu(tBu)-OH, Fmoc-Phe-OH, Fmoc-GIy-OH, Fmoc-His(Trt)-OH, Fmoc-Ile-OH, Fmoc-Leu-OH, Fmoc-Lys(Boc)-OH, Fmoc-Met-OH, Fmoc-Asn(Trt)-OH, Fmoc-Pro-OH, Fmor-Gln(Trt)-OH, Fmoc-Arg(Pbf)-OH, Fmoc-Ser(tBu)-OH, Fmoc-Thr(tBu)-OH, Fmoc-Val-OH, Fmoc-Trp(Boc)-OH, Fmoc-Tyr(tBu)-OH) получают от компании ABI или Anaspec, San Jose, CA. Смолу для синтеза пептидов (смола Fmoc-Rink amide MBHA) и Fmoc-Lys(Mtt)-OH получают от компании Novabiochem, San Diego, CA. Моноизомер сложного сукцинимидильного эфира 6-карбоксифлуоресцеина (6-FAM-NHS) получают от компании Anaspec. Трифторуксусную кислоту (TFA) получают от компании Oakwood Products, West Columbia, SC. Тиоанизол, фенол, триизопропилсилан (TIS), 3,6-диокса-1,8-октандитиол (DODT) и изопропанол получают от компании Aldrich Chemical Co., Milwaukee, WI. Масс-спектры матрично-активированной лазерной десорбции/ионизации (MALDI-MS) регистрируют на приборе Applied Biosystems Voyager DE-PRO MS). Масс-спектры при электрораспылении (ESI-MS) регистрируют на приборе Finnigan SSQ7000 (Finnigan Corp., San Jose, CA) как в режиме положительных, так и отрицательных ионов.
Общая методика проведения твердофазного синтеза пептидов (SPPS)
Пептиды синтезируют, используя не более 250 мкмол. предварительно заполненной смолы Ванга на реактор, в автоматическом синтезаторе пептидов ABI 433A с проведением циклов конденсации в масштабе 250 мкмол. Fastmoc™. Используют предварительно заполненные картриджи, содержащие 1 ммоль стандартных Fmoc-аминокислот, за исключением позиции присоединения флуорофора, где в картридж помещают 1 ммоль Fmoc-Lys (Mtt)-OH, осуществляя контроль методом обратной связи по удельной электропроводности. N-концевое ацетилирование проводят в картридже, используя 1 ммоль уксусной кислоты, в стандартных условиях реакции конденсации.
Удаление 4-метилтритила (Mtt) из лизина
Смолу из синтезатора трижды промывают дихлорметаном и сохраняют во влажном состоянии. Затем через смолу в течение 30 мин пропускают поток 150 мл смеси 95:4:1 дихлорметан:триизопропилсилан:трифторуксусная кислота. Смесь приобретает темно-желтый цвет, а затем становится бледно-желтой. Через слой смолы в течение более 15 мин пропускают ток 100 мл N,N-диметилформамида. Затем смолу трижды промывают N,N-диметилформамидом и отфильтровывают. Тесты с использованием нингидрина показывают сильный сигнал первичного амина.
Нанесение на смолу метки 6-карбоксифлуоресцеина-NHS (6-FAM-NHS)
Смолу обрабатывают 2 эквивалентами 6-FAM-NHS в 1% растворе DIEA/N,N-диметилформамид и перемешивают или встряхивают в течение ночи при температуре окружающей среды. По окончании смолу осушают, трижды промывают N,N-диметилформамидом, еще трижды промывают (1×DCM и 1×метанол) и сушат, получая смолу оранжевого цвета, которая дает отрицательную реакцию с нингидрином.
Общая методика отщепления и удаления защиты из прикрепленного к смоле пептида
Пептиды отщепляют от смолы, встряхивая течение 3 час при температуре окружающей среды в коктейле для расщепления, содержащем 80% TFA, 5% воды, 5% тиоанизола, 5% фенола, 2,5% TIS и 2,5% TDT (1 мл на 0,1 г смолы). Смолу удаляют фильтрованием и дважды промывают TFA. TFA из фильтратов упаривают и продукт осаждают эфиром (10 мл на 0,1 г смолы), извлекают центрифугированием, дважды промывают эфиром (10 мл на 0,1 г смолы) и сушат, получая сырой пептид.
Общая методика очистки пептидов
Сырые пептиды очищают с помощью системы ВЭЖХ компании Gilson, используя при анализе программное обеспечение Unipoint® (Gilson, Inc., Middleton, WI), на колонке, наполненной по технологии радиальной компрессии, которая включает два сегмента 25×100 мм, заполненные частицами Delta-Pak™ C18 размером 15 мкм и размерами пор 100Å, а элюирование проводят, используя один из указанных ниже методов градиентного элюирования. В процессе очистки на одну инжекцию берут от одного до двух миллилитров сырого раствора пептида (10 мг/мл в 90%-ном ДМСО/вода). Пики, содержащие продукт(ы) из каждого прогона, объединяют и лиофилизуют. Все препаративные рабочие циклы проводят со скоростью подачи 20 мл/мин, используя для элюирования буфер A: 0,1% TFA - вода и буфер B: ацетонитрил.
Общая методика проведения препаративной ВЭЖХ
Аналитическую ВЭЖХ проводят в системе Hewlett-Packard 1200 series с диодно-матричным детектором и флуоресцентным детектором Hewlett-Packard 1046A, используя версию А.03.04 программного обеспечения HPLC 3D ChemStation (Hewlett-Packard, Palo Alto, CA) на 4,6×250 мм колонке YMC, заполненной частицами ODS-AQ размером 5 мкм и порами 120Å, а элюирование проводят, используя один из указанных ниже методов градиентного элюирования после предварительного элюирования в начальных условиях в течение 7 мин. В качестве растворителей для элюирования используют буфер A: 0,1% TFA-вода и буфер B: ацетонитрил. Объемная скорость потока для всех градиентов составляет 1 мл/мин.
F-Bak: Пептидный зонд ацетил-(SEQ ID NO: 1)GQVGRQLAIIGDK(6-FAM)-(SEQ ID NO: 2) INR-NH2
Смолу Fmoc-Rink amide MBHA удлиняют, используя общую методику синтеза пептидов, получая защищенный связанный со смолой пептид (1,020 г). Группу Mtt удаляют, вводят метку 6-FAM-NHS, отщепляют и защиту удаляют, как указано выше, получая сырой продукт в виде твердого вещества оранжевого цвета (0,37 г). Полученный продукт очищают методом ВЭЖХ c обращенной фазой (RP-HPLC). Фракции в главном пике исследуют методом аналитической RP-HPLC, чистые фракции выделяют и лиофилизуют, при этом из основного пика получают указанное в названии соединение (0,0802 г) в виде твердого вещества желтого цвета; MALDI-MS m/z=2137,1 [(M+H)+].
Альтернативный синтез пептидного зонда F-Bak: ацетил-(SEQ ID NO: 1)GQVGRQLAIIGDK(6-FAM)-(SEQ ID NO: 2) INR-NH2
Содержащий защиту пептид помещают на 0,25 ммоль смолы Fmoc-Rink amide MBHA (Novabiochem) в автоматическом синтезаторе пептидов Applied Biosystems 433A и осуществляют циклы конденсации Fastmoc™, используя предварительно заполненные 1 ммоль аминокислоты картриджи, за исключением меченного флуоресцеином (6-FAM) лизина, где в картридж помещают 1 ммоль Fmoc-Lys(4-метилтритил). N-концевую ацетильную группу вводят, помещая 1 ммоль уксусной кислоты в картридж и проводя конденсацию, как указано выше. Селективное удаление 4-метилтритильной группы осуществляют с помощью раствора 95:4:1 DCM:TIS:TFA (об./об./об.), который пропускают через смолу в течение более 15 мин, а затем гасят потоком диметилформамида. Моноизомер 6-карбоксифлуоресцеин-NHS вводят во взаимодействие с боковой цепью лизина в 1% растворе DIEA в N,N-диметилформамиде, а окончание процесса подтверждают испытанием с нингидрином. Пептид отщепляют от смолы, удаляют защиту из боковых цепей обработкой смесью 80:5:5:5:2,5:2,5 TFA/вода/фенол/тиоанизол/триизопропилсилан: 3,6-диокса-1,8-октандитиол (об./об./об./об./об./об), и сырой пептид извлекают осаждением диэтиловым эфиром. Сырой пептид очищают высокоэффективной жидкостной хроматографией с обращенной фазой, а его чистоту и идентичность подтверждают аналитической высокоэффективной жидкостной хроматографией с обращенной фазой и масс-спектрометрией по методу матрично-активированной лазерной десорбции/ионизации (m/z=2137,1 ((M+H)+)).
Анализ по методу резонансного переноса энергии флуоресценции с временным разрешением (TR-FRET)
Отдельные соединения последовательно разбавляют в диметилсульфоксиде (ДМСО), начиная с концентрации 50 мкМ (2× начальная концентрация; 10%-й ДМСО), и 10 мкл переносят на 384-луночный планшет. Затем в каждую лунку добавляют 10 мкл смеси белок/зонд/антитело до конечной концентрации, приведенной в таблице 1. Затем образцы смешивают на качалке в течение 1 мин и инкубируют в течение дополнительных 3 час при комнатной температуре. Для каждого анализа проводят добавление зонд/антитело и белок/зонд/антитело вводят на каждый аналитический планшет в качестве отрицательного и положительного, контроля, соответственно. Флуоресценцию измеряют на приборе Envision (Perkin Elmer), используя фильтр возбуждения 340/35 нм, и эмиссионные фильтры 520/525 (пептид F-Bak) и 495/510 нм (содержащее Tb-метку антитело против гистидина) эмиссионные фильтры. Константы ингибирования (Ki) приведены ниже в таблице 2, и их определяют, используя уравнение Ванга (Wang Z.-X. An Exact Mathematical Expression for Describing Competitive Binding of Two Different Ligands to a Protein Molecule. FEBS Lett. 1995, 360:111-4).
Константа ингибирования (Ki) представляет собой константу диссоциации комплекса фермент-ингибитор или молекулы белок/небольшая молекула, где небольшая молекула подавляет связывание одного белка с другим белком. Так, большое значение Ki указывает на низкое сродство связывания, а малое значение Ki указывает на высокое сродство связывания.
В таблице 2 приведены данные о константах ингибирования для ингибирования связывания пептидного зонда Bak BH3 к белку Bcl-2, и они показывают, что соединения по настоящему изобретению обладают высоким сродством связывания к антиапоптотическому белку Bcl-2. Таким образом, предполагают, что настоящие соединения пригодны для лечения заболеваний, при которых экспрессируются антиапоптотические белки Bcl-2.
Ожидается, что поскольку соединения, имеющие формулу I, связываются с Bcl-2, то они также пригодны в качестве связующих веществ для антиапоптотических белков, обладающих близкой структурной гомологией к Bcl-2, таким как, например, антиапоптотические белки Bcl-XL, Bcl-w, Mcl-1 и Bfl-1/A1.
Вовлечение белков Bcl-2 в развитие рака мочевого пузыря, рака мозга, рака молочной железы, рака костного мозга, рака шейной области, хронического лимфолейкоза, колоректального рака, рака пищевода, гепатоцеллюлярного рака, лимфобластного лейкоза, фолликулярной лимфомы, лимфолейкоза, вызываемого Т-лимфоцитами или В-клетками, меланомы, миелогенного лейкоза, миеломы, рака полости рта, рака яичников, немелкоклеточного рака легкого, рака простаты, мелкоклеточного рака легкого, рака простаты, рака селезенки и т.п. описано в одновременно находящейся на рассмотрении заявке PCT US 2004/36770, опубликованной как WO 2005/049593, и заявке PCT US 2004/37911, опубликованной как WO 2005/024636.
Вовлечение белков Bcl-2 в иммунные и аутоиммунные заболевания описано в Current Allergy and Asthma Reports 2003, 3, 378-384; British Journal of Haematology 2000, 110(3), 584-90; Blood 2000, 95(4), 1283-92; и New England Journal of Medicine 2004, 351(14), 1409-1418.
Вовлечение белков Bcl-2 в развитие артрита раскрыто в находящейся на рассмотрении предварительной заявке на патент США № 60/988479.
Вовлечение белков Bcl-2 в отторжение трансплантата костного мозга раскрыто в находящейся на рассмотрении заявке на патент США № 11/941196.
Сверхэкспрессия белков Bcl-2 коррелирует с резистентностью к химиотерапии, клиническим результатом, прогрессированием болезни, общим прогнозом дальнейшего течения болезни или их комбинациях при различных видах рака и расстройствах иммунной системы. Виды рака включают, однако этим не ограниваясь, гематологические и солидные типы опухолей, такие как акустическая неврома, острый лейкоз, острый лимфобластный лейкоз, острый миелогенный лейкоз (моноцитарный, миелобластный, аденокарциномный, ангиосаркомный, астроцитомный, миеломоноцитарный и промиелоцитарный), острый Т-лимфоцитарный лейкоз, базальноклеточная карцинома, карцинома желчных протоков, рак мочевого пузыря, рак мозга, рак молочной железы (включая рак молочной железы с положительным эстрогенрецепторным статусом), бронхогенная карцинома, лимфома Беркитта, рак шейной области, хондросаркома, хордома, хориокарцинома, хронический лейкоз, хронический лимфоцитарный лейкоз, хронический миелоцитарный (гранулоцитарный) лейкоз, хронический миелогенный лейкоз, рак толстой кишки, колоректальный рак, краниофарингиома, цистаденокарцинома, диспролиферативные изменения (дисплазии и метаплазии), эмбриональная карционома, внутриматочный рак, эндотелиосаркома, эпендимома, карцинома эпителия, эритролейкемия, рак пищевода, рак молочной железы с положительным эстрогенрецепторным статусом, наследственная тромбоцитемия, опухоль Эвинга, фибросаркома, рак желудка, опухоль половых клеток яичек, обусловленная беременностью трофобластическая опухоль, глиобластома, рак головы и шеи, болезнь тяжелых цепей, гемангиобластома, гепатома, гепатоцеллюлярный рак, гормон-нечувствительный рак простаты, лейомиосаркома, липосаркома, рак легкого (включая мелкоклеточный рак легкого и немелкоклеточный рак легкого), лимфангиоэндотелио-саркома, лимфангиосаркома, лимфобластный лейкоз, лимфома (лимфома, включая диффузную В-крупноклеточную лимфому, фолликулярную лимфому, лимфому Ходжкина и неходжкинскую лимфому), злокачественные развития болезней и гиперпролиферативные заболевания мочевого пузыря, молочной железы, толстой кишки, легкого, яичников, поджелудочной железы, простаты, кожи и матки, злокачественные развития болезней, вызываемые Т-лимфоцитами или В-клетками, лейкоз, медуллярная карцинома, медуллобластома, меланома, менингиома, мезотелиома, множественная миелома, миелогенный лейкоз, миелома, миксосаркома, нейробластома, олигодендроглиома, рак ротовой полости, остеогенная саркома, рак яичников, рак поджелудочной железы, папиллярная аденокарцинома, периферическая Т-лимфоцитарная лимфома, пинеалома, истинная полицитемия, рак простаты (включая гормон-нечувствительный (резистентный) рак простаты), ректальный рак, почечно-клеточный рак, ретинобластома, рабдомиосаркома, саркома, рак сальной железы, семинома, рак кожи, мелкоклеточная карцинома легкого, солидные опухоли (карциномы и саркомы), рак желудка, плоскоклеточная карцинома, синовиома, рак потовых желез, рак яичек (включая опухоль половых клеток яичек), рак щитовидной железы, макроглобулинемия Вальденстрема, опухоли яичек, рак матки, опухоль Вильмса и т.п.
Ожидается также, что соединения, имеющие формулу (I), ингибируют рост клеток, экспрессирующих белки Bcl-2, полученные из детского рака или опухоли, включая эмбриональную рабдомиосаркому, детский острый лимфобластный лейкоз, детский острый миелогенный лейкоз, детскую альвеолярную рабдомиосаркому, детскую анапластическую эпендимому, детскую анапластическую крупноклеточную лимфому, детскую анапластическую медуллобластому, детскую нетипичную, тератоидную/палочковидную опухоль центральной нервной системы, детский бифенотипический острый лейкоз, детскую лимфому Беркитта, детские виды рака из опухолей семейства Эвинга, такие как примитивные нейроэктодермальные опухоли, детская рассеянная анапластическая опухоль Вильмса, детская опухоль Вильмса с благоприятным гистологическим строением, детская глиобластома, детская медуллобластома, детская нейробластома, миелоцитоматоз, вызванный детской нейробластомой, детский пред-В-клеточный рак (такой как лейкоз), детская остеосаркома, детская палочковидная почечная опухоль, детская рабдомиосаркома и детский Т-лимфоцитарный рак, такой как лимфома и рак кожи и т.п.
Аутоиммунные расстройства включают синдром приобретенного иммунодефицита (СПИД), аутоиммунный лимфопролиферативный синдром, гемолитическую анемию, воспалительные заболевания и тромбоцитопению, острое или хроническое иммунопатологическое заболевание, связанное с трансплантацией органов, болезнь Аддисона, аллергические заболевания, облысение, очаговую алопецию, атероматозное заболевание/артериосклероз, атеросклероз, артрит (включая остеоартрит, ювенильный хронический артрит, септический артрит, лайм-артрит, псориатический артрит и реактивный артрит), аутоиммунное буллезное заболевание, абеталипопротеинемию, заболевания, родственные приобретенному иммунодефициту, связанное с трансплантацией органов острое иммунопатологическое заболевание, приобретенный акроцианоз, острые и хронические паразитарные или инфекционные процессы, острый панкреатит, острую почечную недостаточность, острую ревматическую лихорадку, острый поперечный миелит, аденокарциномы, предсердные эктопические систолы, (острый) респираторный дистресс-синдром у взрослых, комплекс СПИД-деменция, алкогольный цирроз, индуцированное алкоголем поражение печени, индуцированный алкоголем гепатит, аллергический конъюнктивит, аллергический контактный дерматит, аллергический ринит, аллергию и астму, отторжение аллотрансплантата, недостаточность альфа-1-антитрипсина, болезнь Альцгеймера, амиотрофический боковой склероз, анемию, стенокардию, ассоциированную с анкилозирующим спондилитом болезнь легких, дегенерацию клеток переднего рога спинного мозга, опосредованную антителами цитотоксичность, антифосфолипидный синдром, аллергические реакции на противорецепторные антитела, аневризмы аорты и периферических сосудов, рассечение аорты, артериальную гипертензию, артериосклероз, артериовенозную фистулу, артропатию, астению, астму, атаксию, атопическую аллергию, мерцательную аритмию (стойкую или пароксизмальную), трепетание предсердий, атриовентрикулярную блокаду, атрофический аутоиммунный гипотиреоз, аутоиммунную гемолитическую анемию, аутоиммунный гепатит, аутоиммунный гепатит типа-1 (классический аутоиммунный или липоидный гепатит), аутоиммунно-опосредованную гипогликемию, аутоиммунную нейтропению, аутоиммунную тромбоцитопению, аутоиммунное заболевание щитовидной железы, В-клеточную лимфому, отторжение костного трансплантата, отторжение трансплантата костного мозга (BMT), облитерирующий бронхиолит, межжелудочковую блокаду, ожоги, кахексию, сердечные аритмии, синдром временной остановки сердца, опухоли сердца, кардиомиопатию, воспалительную реакцию при искусственном кровообращении, отторжение трансплантата хряща, церебеллярные кортикальные дегенерации, церебеллярные расстройства, хаотическую или мультиочаговую предсердную тахикардию, ассоциированные с химиотерапией расстройства, хламидию, холеостаз, хронический алкоголизм, хронический активный гепатит, синдром хронической усталости, хроническое иммунное заболевание, ассоциированное с трансплантацией органов, хроническую эозинофильную пневмонию, хронические воспалительные патологии, хронический кожно-слизистый кандидоз, хроническое обструктивное заболевание легких (COPD), хроническую интоксикацию салицилатом, рак ободочной и прямой кишки, общий транзиторный иммунодефицит (общую транзиторную гипогаммаглобулинемию), конъюнктивит, ассоциированную с заболеванием соединительной ткани интерстициальную болезнь легких, контактный дерматит, положительную гемолитическую анемию Кумбса, легочное сердце, болезнь Крейтцфельдта-Якоба, криптогенный аутоиммунный гепатит, криптогенный фиброзирующий альвеолит, отрицательный в культуре сепсис, муковисцидоз, расстройства, связанные с терапией цитокинами, болезнь Крона, деменцию боксеров, демиелинизирующие заболевания, лихорадку Денге, геморрагическую лихорадку, дерматит, дерматическую склеродермию, дерматологические состояния, ассоциированную с дерматомиозитом/полимиозитом болезнь легких, диабет, диабетическое артериосклеротическое заболевание, сахарный диабет, заболевание с диффузными тельцами Леви, дилатационную кардиомиопатию, дилатационную застойную кардиомиопатию, дискоидную красную волчанку, нарушения базальных ганглий, диссеминированное внутрисосудистое свертывание, синдром Дауна в среднем возрасте, индуцированную лекарственным средством интерстициальную болезнь легких, индуцированный лекарственным средством гепатит, индуцированные лекарственными средствами нарушения движения, которые вызываются лекарственными средствами, блокирующими рецепторы дофамина в ЦНС, чувствительность к лекарственным средствам, экзему, энцефаломиелит, эндокардит, эндокринопатию, энтеропатический синовит, эпиглоттит, инфекцию вирусом Эпштейна-Барра, эритромелалгию, экстрапирамидные и церебеллярные нарушения, семейный гематофагоцитарный лимфоцитарный гистиоцитоз, отторжение имплантата эмбриональной вилочковой железы, атаксию Фридрейха, функциональные периферические артериальные расстройства, женское бесплодие, фиброз, фибротическое заболевание легких, грибковый сепсис, газовую гангрену, язву желудка, гигантоклеточный артериит, гломерулонефрит, гломерулонефритиды, синдром Гудпасчера, зобный аутоиммунный гипотиреоз (болезнь Хашимото), подагрический артрит, отторжение трансплантата любого органа или ткани, реакцию “трансплантат-против-хозяина”, грамотрицательный сепсис, грамположительный сепсис, гранулемы, вызываемые внутриклеточными организмами, стрептококковую инфекцию группы В (GBS), болезнь Грейвса, ассоциированную с гемосидерозом болезнь легких, ворсинчатоклеточный лейкоз, волосатоклеточный лейкоз, болезнь Халлеррордена-Шпатца, тиреоидит Хашимото, сенную лихорадку, отторжение трансплантата сердца, гемохроматоз, гематопоэтические злокачественные заболевания (лейкоз и лимфому), гемолитическую анемию, гемолитический уремический синдром/тромболитическую тромбоцитопеническую пурпуру, кровотечение, болезнь Шенлейна-Геноха, гепатит A, гепатит B, гепатит C, ВИЧ-инфекцию/ВИЧ-невропатию, болезнь Ходжкина, гипопаратиреоз, хорею Гентингтона, гиперкинетические нарушения движения, аллергические реакции, аллергический пневмонит, гипертиреоз, гипокинетические нарушения движения, диагностику гипоталамо-гипофизарно-надпочечниковой оси, идиопатическую болезнь Аддисона, идиопатическую лейкопению, идиопатический легочный фиброз, идиопатическую тромбоцитопению, идиосинкразическую болезнь печени, детскую спинально-мышечную атрофию, инфекционные болезни, воспаление аорты, воспалительную болезнь кишечника, инсулинозависимый сахарный диабет, интерстициальный пневмонит, иридоциклит/увеит/неврит зрительного нерва, ишемическое/реперфузионное повреждение, ишемический инсульт, ювенильную пернициозную анемию, ювенильный ревматоидный артрит, ювенильную спинально-мышечную атрофию, саркому Капоши, болезнь Кавасаки, отторжение трансплантата почки, инфекции микобактерией Legionella, лейшманиоз, проказу, повреждения кортикоспинальной системы, IgA-зависимый линейный дерматоз, липидему, отторжение трансплантата печени, боррелиоз Лайма, лимфедерму, лимфатический отек при болезни легких, малярию, неустановленное или неуточненное мужское бесплодие, злокачественный гистиоцитоз, злокачественную меланому, менингит, менингококкемию, микроскопический васкулит почек, мигренозную головную боль, митохондриальное мультисистемное расстройство, заболевание смешанной соединительной ткани, ассоциированную с заболеванием смешанной соединительной ткани болезнь легких, моноклональную гаммопатию, множественную миелому, множественные системные дегенерации (болезнь Менцеля, болезнь Дежерина-Томаса, болезнь Ши-Драгера и болезнь Мачадо-Джозефа), миалгический энцефалит/синдром хронической усталости, тяжелую псевдопаралитическую миастению, микроскопический васкулит почек, комплекс Mycobacterium avium, туберкулезную бациллу, синдром миелодисплазии, инфаркт миокарда, ишемические нарушения миокарда, карцинома носоглотки, хроническое заболевание легких новорожденных, нефрит, нефроз, нефротический синдром, нейродегенеративные заболевания, нейрогенные I мышечные атрофии, нейрогенную лихорадку, неалкогольный стеатогепатит, закупорку брюшной аорты и ее ответвлений, окклюзивные артериальные нарушения, отторжение трансплантатов органов, орхит/эпидидимит, процедуры после лечения орхита/вазэктомии, органомегалию, остеоартроз, остеопороз, угасание функции яичников, отторжение трансплантата поджелудочной железы, паразитарные заболевания, отторжение трансплантата паращитовидной железы, болезнь Паркинсона, воспалительное заболевание почечных лоханок, пузырчатку обыкновенную, листовидную пузырчатку, пемфигоид, круглогодичный ринит, заболевание перикарда, периферическое атеросклеротическое заболевание, периферические васкулярные расстройства, перитонит, пернициозную анемию, факогенный увеит, интерстициальную плазмоклеточную пневмонию, пневмонию, синдром Кроу-Фукаса (POEMS) (полиневропатия, органомегалия, эндокринопатия, моноклональная гаммопатия и синдром с поражением кожи), постперфузионный синдром, постгемодиализный синдром, посткардиотомный синдром после инфаркта миокарда, постинфекционное интерстициальное заболевание легких, преждевременное угасание функции яичников, первичный билиарный цирроз, первичный склерозирующий гепатит, первичную микседему, первичную легочную гипертензию, первичный склерозирующий холангит, первичный васкулит, прогрессирующий супрануклеарный паралич, псориаз, псориаз типа 1, псориаз типа 2, псориатическую артропатию, легочную гипертензию, вторичную относительно заболевания соединительной ткани, легочную манифестацию нодозного полиартериита, поствоспалительное интерстициальное заболевание легких, лучевой фиброз, лучевую терапию, феномен и болезнь Рейно, болезнь Рейно, болезнь Рефсума, тахикардию с регулярными узкими комплексами QRS-зубцов, болезнь Рейтера, неуточненное заболевание почек, реноваскулярную гипертензию, реперфузионное повреждение, рестриктивную кардиомиопатию, ассоциированную с ревматоидным артритом интерстициальную болезнь легких, ревматоидный спондилит, саркоидоз, синдром Шмидта, склеродермию, сенильную хорею, сенильную деменцию, ассоциированную с тельцами Леви, синдром сепсиса, септический шок, сероотрицательные артропатии, шок, серповидно-клеточную анемию, ассоциированную с болезнью Шегрена болезнь легких, синдром Шегрена, отторжение аллотрансплантата кожи, синдром с поражением кожи, отторжение трансплантата тонкой кишки, аутоиммунность спермы, рассеянный склероз (всех подтипов), спинную атаксию, спинально-церебеллярные дегенерации, спондилоартропатию, спондилоартропатию, спорадическую плюригландулярную недостаточность типа I, плюригландулярную недостаточность типа II, болезнь Стилла, стрептококковый миозит, удар, структурные повреждения мозжечка, подострый склерозирующий панэнцефалит, метастатическую офтальмию, обморок, сердечно-сосудистый сифилис, системную анафилаксию, синдром системной воспалительной реакции, системный ювенильный ревматоидный артрит, системную красную волчанку, ассоциированную с системной красной волчанкой болезнь легких, системный склероз, ассоциированную с системным склерозом интерстициальную болезнь легких, Т-клеточный или острый лимфоцитарный лейкоз (по классификации FAB), болезнь Такаясу/артериит, телангиэктазию, Th2 типа- и Th1 типа-опосредованные заболевания, облитерирующий тромбоангиит, тромбоцитопению, тиреоидит, токсичность, синдром токсического шока, трансплантаты, травму/кровотечение, аутоиммунный гепатит типа-2 (гепатит с антителами против LKM), инсулинорезистентность типа В с черным акантозом, аллергические реакции типа III, аллергию типа IV, артропатию язвенного колита, язвенный колит, нестабильную стенокардию, уремию, уросепсис, крапивницу, увеит, вальвулярные сердечные заболевания, варикозные вены, васкулит, васкулитное диффузное заболевание легких, венозные заболевания, венозный тромбоз, фибрилляцию желудочков, витилиго, острое заболевание печени, вирусные и грибковые инфекции, острый энцефалит с поражением витальных функций/асептический менингит, гемафагоцитарный синдром, ассоциированный с высоким риском смертельного исхода, гранулематоз Вегенера, синдром Вернике-Корсакова, заболевание Вильсона, отторжение ксенотрансплантата любого органа или любой ткани, иерсинии и ассоциированную с сальмонеллой артропатию и т.п.
Схемы и эксперименты
Следующие сокращения имеют указанные значения. ADDP означает 1,1'-(азодикарбонил)дипиперидин; AD-mix-β означает смесь (DHQD)2PHAL, K3Fe(CN)6, K2CO3 и K2SO4; 9-BBN означает 9-борабицикло(3.3.1)нонан; Boc означает трет-бутоксикарбонил; (DHQD)2PHAL означает гидроксихинидин 1,4-фталазиндиила диэтиловый эфир; DBU означает 1,8-диазабицикло[5.4.0]ундец-7-ен; DIBAL означает диизобутилалюмогидрид; DIEA означает диизопропилэтиламин; DMAP означает N,N-диметиламинопиридин; ДМФА (DMF) означает N,N-диметилформамид; dmpe означает 1,2-бис(диметилфосфино)этан; ДМСО означает диметилсульфоксид; dppb означает 1,4-бис(дифенилфосфино)бутан; dppe означает 1,2-бис(дифенилфосфино)этан; dppf означает 1,1'-бис(дифенилфосфино)ферроцен; dppm означает 1,1-бис(дифенилфосфино)метан; EDAC-HCl означает гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодимида; Fmoc означает флуоренилметоксикарбонил; HATU означает гексафторфосфат O-(7-азабензотриазол-1-ил)-N,N',N',N'-тетраметилурония; HMPA означает гексаметилфосфороамид; ИПС означает изопропиловый спирт; MP-BH3 означает макропористый триэтиламмоний метилполистирол цианоборгидрид; TEA означает триэтиламин; TFA означает трифторуксусную кислоту; ТГФ означает тетрагидрофуран; NCS означает N-хлорсукцинимид; NMM означает N-метилморфолин; NMP означает N-метилпирролидон; PPh3 означает трифенилфосфин.
Следующие схемы приведены с целью предоставить, как полагают авторы настоящего изобретения, наиболее полезные и наиболее понятные описания методик и концептуальных аспектов настоящего изобретения. Соединения по настоящему изобретению можно получить с использованием методов химического синтеза, примеры которых приведены в настоящем описании. Следует понимать, что порядок стадий в процессах может быть различным, и что реагенты, растворители и условия проведения реакций можно заменить на те, которые специально указаны, а также следует понимать, что уязвимые фрагменты могут быть, если необходимо, защищены и освобождены от защиты.
Схема 1

Соединения формулы (4) могут быть получены, как показано на СХЕМЕ 1, и могут использоваться, как показано на схеме 8, для получения соединений формулы (I), которые являются представителями соединений по настоящему изобретению. Соединения формулы (I), где R представляет собой алкил, могут быть преобразованы в соединения формулы (2) с помощью реагента Z3L1MgX1, где X1 представляет собой атом галогена, в таком растворителе, однако этим не ограниваясь, как простой эфир или тетрагидрофуран. Соединения формулы (3) могут быть получены из соединений формулы (2) с помощью сильного основания, такого как NaH и R57X2, где X2 представляет собой атом галогена, а значение R57 приведено в данном описании. После того, как соединения формулы (3) обрабатывают водным раствором NaOH или LiOH, получают соединения формулы (4).
Схема 2

Как показано на схеме 2, соединения формулы (5) могут вступать во взаимодействие с соединениями формулы (6) и восстановителем с образованием соединений формулы (7). Примеры восстановителей включают боргидрид натрия, цианоборгидрид натрия, триацетоксиборгидрид натрия, привитый к полимеру цианоборгидрид и т.п. Реакцию, как правило, проводят в таком растворителе, однако этим не ограниваясь, как метанол, тетрагидрофуран и дихлорметан или в их смеси. Соединения формулы (8) можно получить из соединений формулы (7), как указано на схеме 1, и их можно использовать, как указано на схеме 8, для получения соединений формулы I.
Схема 3

Из соединений формулы (9), если их ввести в реакцию с соединением формулы (10), где X означает галогенид или трифлат, и основанием, можно получить соединения формулы (11). Основания, пригодные для проведения реакции, включают триэтиламин, диизопропилэтиламин и т.п. Соединения формулы (13), где значение Y приведено в данном описании для заместителей при Z3, можно получить из соединений формулы (11) и соединений формулы (12) в условиях конденсации Сузуки, известных специалистам из области техники и легко доступных из литературы. Соединения формулы (14) можно получить из соединений формулы (13), как указано на СХЕМЕ 1, и их можно использовать, как указано на СХЕМЕ 8, для получения соединений формулы I.
Схема 4

Как показано на схеме 4, соединения формулы (17) можно получить из соединений формулы (15) и соединений формулы (16), где R представляет собой алкил, а значение R38 приведено в данном описании, в условиях конденсации Сузуки, известных специалистам из области техники и легко доступных из литературы. Соединения формулы (17) можно восстановить в соединения формулы (18) с помощью такого восстановителя как LiAlH4, в таком растворителе, однако этим не ограниваясь, как диэтиловый эфир или ТГФ. Соединения формулы (19) можно получить из соединений формулы (18) с помощью периодинана Десса-Мартина или в условиях реакции окисления Сверна, известных специалистам из области техники и легко доступных из литературы. Соединения формулы (19) могут вступать во взаимодействие с соединением формулы (5) и восстановителем с получением соединений формулы (20). Примеры восстановителей включают боргидрид натрия, цианоборгидрид натрия, триацетоксиборгидрид натрия, привитый к полимеру цианоборгидрид и т.п. Реакцию обычно проводят в таком растворителе, однако этим не ограниваясь, как метанол, тетрагидрофуран, 1,2-дихлорэтан и дихлорметан или их смеси. Соединения формулы (21) можно получить из соединений формулы (20), как указано на СХЕМЕ 1, и их можно использовать, как указано на СХЕМЕ 8, для получения соединений формулы I.
Схема 5

Как показано на схеме 5, соединения формулы (22), где R представляет собой алкил, можно превратить в соединения формулы (23) по реакции первого указанного соединения, где X1 представляет собой Cl, Br, I или CF3SO3 -, и соединения формулы R41-OH и катализатора в присутствии или в отсутствие основания. Примеры катализаторов включают комплекс трифторметансульфоната меди(I) с толуолом, PdCl2, Pd(OAc)2 и Pd2(dba)3. Примеры первых основания включают триэтиламин, N,N-диизопропилэтиламин, Cs2CO3, Na2CO3, K3PO4 и их смеси.
Соединения формулы (22) можно также превратить в соединения формулы (23) по реакции первого указанного соединения, где X1 представляет собой Cl, F или NO2, и соединения формулы R41-OH с первым основанием. Примеры первых основания включают триэтиламин, N,N-диизопропилэтиламин, Cs2CO3, Na2CO3, K3PO4 и их смеси.
Схема 6

Соединения формулы (18) можно ввести во взаимодействие с мезилхлоридом и основанием, таким как, однако этим не ограниваясь, триэтиламин, с последующей обработкой N-трет-бутоксикарбонилпиперазином с получением соединений формулы (24). Соединения формулы (25) можно получить по реакции соединений формулы (24) с триэтилсиланом и трифторуксусной кислотой. Соединения формулы (25) можно ввести во взаимодействие с соединением формулы (26) и HK2PO4 и получить соединения формулы (27), в таком растворителе, однако этим не ограниваясь, как диметилсульфоксид. Соединения формулы (28) можно получить из соединений формулы (27), как указано на схеме 1, и их можно использовать, как указано на схеме 8, для получения соединений формулы I.
Схема 7
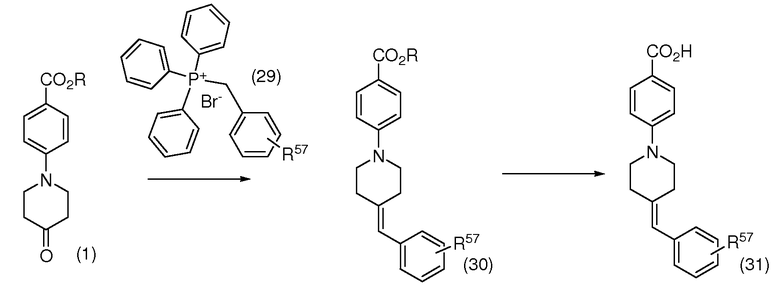
Как показано на схеме 7, соединения формулы (1) можно ввести во взаимодействие с соответствующим трифенилфосфонийбромидом формулы (29) и основанием, таким, однако этим не ограниваясь, как гидрид натрия или н-бутиллитий, и получить соединения формулы (30). Реакцию обычно проводят в растворителе, таком как ТГФ или ДМСО. Соединения формулы (31) можно получить из соединений формулы (30), как указано на СХЕМЕ 1, и их можно использовать, как указано на схеме 8, для получения соединений формулы I.
Схема 8

Как показано на схеме 8, соединения формулы (32), которые можно получить, как указано в данном описании, можно превратить в соединения формулы (33) по реакции первого указанного соединения с аммиаком. Соединения формулы (33) можно превратить в соединения формулы (I) взаимодействием первого указанного соединения с соединениями формулы (4), (8), (14), (21), (28), (31) или (37) и конденсирующим агентом в присутствии или в отсутствие основания. Примеры конденсирующих агентов включают гидрохлорид 1-этил-3-[3-(диметиламино)пропил]карбодиимида, 1,1'-карбонилдиимидазол и гексафторфосфат бензотриазол-1-илоксипирролидинофосфония. Примеры первых оснований включают триэтиламин, N,N-диизопропилэтиламин, 4-(диметиламино)пиридин и их смеси.
Схема 9

Соединения формулы (33), полученные как указано на СХЕМЕ 1, можно также превратить в соединения формулы (I) по реакции первого указанного соединения и соединений формулы (34) и первого основания. Примеры первых основания включают, однако этим не ограниваясь, триэтиламин, N,N-диизопропилэтиламин, 4-(диметиламино)пиридин и их смеси.
Схема 10

Как показано на схеме 10, соединения формулы (35), где L представляет собой простую связь, алкил, O, S, S(O), S(O)2, NH и т.д., могут вступать в реакцию с соединениями формулы (36) с образованием соединений формулы (37). Реакцию обычно проводят при повышенных температурах в таком растворителе, однако этим не ограниваясь, как диметилсульфоксид, и может потребоваться использовать основание, такое, однако этим не ограниваясь, как фосфат калия, карбонат калия и т.п. Соединения формулы (38) можно получить из соединений формулы (37), как указано на СХЕМЕ 1, и их можно использовать, как указано на СХЕМЕ 8, для получения соединений формулы I.
Схема 11
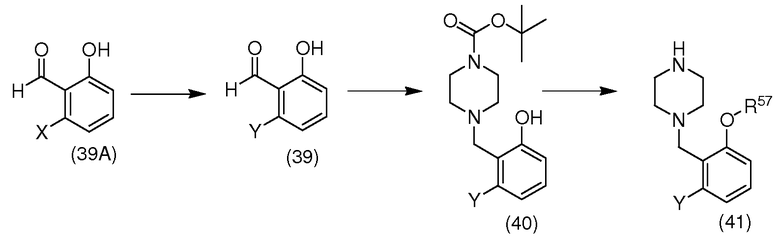
Соединения формулы (39), где значение Y указано в данном описании для заместителей при Z3, можно получить из соединений формулы (39А), где X представляет собой галогенид или трифлат, и Y-B(OH)2 в условиях реакции конденсации Сузуки, известных специалистам из области техники и легко доступных из литературы. Соединения формулы (39) можно ввести во взаимодействие с трет-бутил пиперазин-1-карбоксилатом и восстановителем, таким как триацетоксиборгидрид натрия, и получить соединение формулы (40). Реакцию обычно проводят в таком растворителе, однако этим не ограниваясь, как метиленхлорид. Соединения формулы (41) можно получить из соединения формулы (40) путем реакции последнего с соединением R57X, где X представляет собой галогенид, и NaH в таком растворителе как N,N-диметилформамид, а затем полученное вещество можно обработать триэтилсиланом и трифторуксусной кислотой в дихлорметане. Соединения формулы (41) можно использовать, как указано на схеме 10, где L1-Z3 приведен в формуле (41).
Схема 12

Как показано на схеме 12, замещенный пиперазин-2-он, где R57 представляет собой алкил, можно ввести во взаимодействие с соединениями формулы (6) и восстановителем, таким как триацетоксиборгидрид натрия в дихлорметане, и получить соединения формулы (42). Соединения формулы (42) можно восстановить в соединения формулы (43) с использованием такого восстановителя, однако этим не ограниваясь, как алюмогидрид лития, в таком растворителе, однако этим не ограниваясь, как тетрагидрофуран. Соединения формулы (43) можно использовать, как указано на схеме 10, где L1-Z3 приведены в формуле (43).
Следующие примеры приведены с целью предоставить, как полагают авторы настоящего изобретения, наиболее полезные и наиболее понятные описания методик и концептуальных аспектов настоящего изобретения. Отдельные соединения называют в соответствии с ACD/ChemSketch Version 5.06 (05 июня 2001, Advanced Chemistry Development Inc., Toronto, Ontario) или ChemDraw® Ver. 9.0.5 (CambridgeSoft, Cambridge, MA). Промежуточные соединения называют в соответствии с ChemDraw® Ver. 9.0.5 (CambridgeSoft, Cambridge, MA).
ПРИМЕР 1
4-[4-(Циклогексилметил)-4-метоксипиперидин-1-ил]-N-{[5-({(1R)-3-(диметиламино)-1-[(фенилтио)метил]пропил}амино)-4-нитротиен-2-ил]сульфонил}бензамид
ПРИМЕР 1А
(R)-Бензил 4-(диметиламино)-1-гидрокси-4-оксобутан-2-илкарбамат
Раствор 3-(S)-((карбобензилокси)амино)-γ-бутиролактона (получают в соответствии с методикой, приведенной в McGarvey, G.J.; Williams, J.M.; Hiner, R.N.; Matsubara, Y.; Oh, T., J. Am. Chem. Soc., 1986, 108, 4943-4952, 7,72 г) в ТГФ (100 мл) насыщают газообразным диметиламином, перемешивают при комнатной температуре в течение 16 час и концентрируют. Остаток фильтруют через слой силикагеля, элюируя 50% раствором ацетона в гексане, и получают требуемый продукт.
Пример 1В
(R)-Бензил 4-(диметиламино)-4-оксо-1-(фенилтио)бутан-2-илкарбамат
Раствор соединения по примеру 1А (8,45 г) в толуоле (15 мл) обрабатывают трибутилфосфином (9,76 мл) и дифенилдисульфидом (7,30 г) и нагревают до 80°С в течение 16 час. Реакционную смесь концентрируют и очищают колоночной хроматографией на силикагеле, проводя градиентное элюирование в диапазоне 0-50% этилацетата в гексане, и получают требуемый продукт.
ПРИМЕР 1С
(R)-3-Амино-N,N-диметил-4-(фенилтио)бутанамид
Суспензию соединения по примеру 1В (10,60 г) в 50 мл 30%-го раствора HBr/уксусная кислота оставляют перемешиваться на ночь при комнатной температуре. Полученную гомогенную реакционную смесь концентрируют, разбавляют водой (200 мл) и 5% раствором HCl (100 мл) и промывают диэтиловым эфиром (3×). рН водной фазы доводят до значения примерно 8-9 твердым Na2CO3 и экстрагируют дихлорметаном (5×). Органические фазы объединяют, сушат (MgSO4), фильтруют и концентрируют, получая требуемый продукт.
ПРИМЕР 1D
(R)-N1,N1-Диметил-4-(фенилтио)бутан-1,3-диамин
Раствор соединения по примеру 1С (8,68 г) в ТГФ (200 мл) обрабатывают комплексом BH3-диметилсульфоксид (18,2 мл) при комнатной температуре, оставляют перемешиваться на ночь, медленно добавляют метанол (20 мл), а затем 2 н. раствор HCl (50 мл), оставляют перемешиваться на ночь и концентрируют. Полученный остаток очищают хроматографией на силикагеле, элюируя 5% 7N NH3/CH3OH в дихлорметане, и получают требуемый продукт.
ПРИМЕР 1Е
(R)-5-(Диметиламино)-1-(фенилтио)бутан-2-иламино)-4-нитротиофен-2-сульфонамид
Смесь 2-хлор-3-нитротиофен-5-сульфонамида (2,18 г), соединения по Примеру 1D (1,14 г) и триэтиламина (1 г) перемешивают в диоксане (30 мл) при 90°С в течение 24 час. Раствор разбавляют этилацетатом, промывают раствором NaH2PO4 и насыщенным раствором соли, сушат над Na2SO4, фильтруют и концентрируют. Продукт получают растиранием в этилацетате.
ПРИМЕР 1F
Этил 4-(4-(циклогексилметил)-4-гидроксипиперидин-1-ил)бензоат
К раствору циклогексилметилмагнийбромида (1,90 мл в 2М растворе в ТГФ) при -78°С добавляют этил 4-(4-оксо-1-пиперидинил)бензоат (получают в соответствии с методикой, приведенной в Synthesis 1981, 606-608, 0,30 г) и оставляют на ночь нагреваться до комнатной температуры. Реакционную смесь перераспределяют между этилацетатом и насыщенным водным раствором NH4Cl и водный слой экстрагируют этилацетатом (2×). Органические слои объединяют, сушат (MgSO4), фильтруют и концентрируют. Полученный остаток очищают хроматографией на силикагеле, элюируя 20% этилацетатом, и получают продукт.
ПРИМЕР 1G
Этил 4-(4-(циклогексилметил)-4-метоксипиперидин-1-ил)бензоат
К раствору соединения по Примеру 1F (380 мг) в ТГФ (5 мл) добавляют NaH (96 мг, 60%-я дисперсия в минеральном масле), нагревают до 50°С в течение 2 час и обрабатывают гексаметилфосфорамидом (1 мл), а затем добавляют MeI (1 мл). Реакционную смесь оставляют на ночь кипеть с обратным холодильником, охлаждают до 0°С и разбавляют насыщенным водным раствором NaHSO4 (10 мл). Образовавшуюся двухфазную смесь разделяют, водную фазу дважды экстрагируют эфиром, органические вытяжки объединяют, промывают водой и насыщенным раствором соли. Сушат над MgSO4, смесь концентрируют в вакууме и очищают хроматографией на силикагеле, элюируя 15% раствором этилацетата в гексанах.
ПРИМЕР 1H
4-(4-(Циклогексилметил)-4-метоксипиперидин-1-ил)бензойная кислота
Раствор соединения по примеру 1G (300 мг) в диоксане (5 мл) обрабатывают 1 н. раствором NaOH (2 мл), оставляют перемешиваться на ночь, подкисляют 1 н. раствором HCl, экстрагируют этилацетатом (3×), сушат (MgSO4) и фильтруют. Концентрированием фильтрата получают требуемый продукт.
ПРИМЕР 1I
4-[4-(Циклогексилметил)-4-метоксипиперидин-1-ил]-N-{[5-({(1R)-3-(диметиламино)-1-[(фенилтио)метил]пропил}амино)-4-нитротиен-2-ил]сульфонил}бензамид
Соединение по примеру 1E (60 мг), соединение по примеру 1H (65 мг), гидрохлорид 1-этил-3-[3-(диметиламино)пропил]карбодиимида (65 мг) и 4-диметиламинопиридин (22 мг) перемешивают в CH2Cl2 (4 мл) в течение 24 час. Реакционную смесь охлаждают и очищают хроматографически на силикагеле, элюируя 50-100% раствором этилацетата в гексане, а затем смесью 1/10/89 триэтиламин/метанол/этилацетат.
1Н ЯМР (400 МГц, ДМСО-d6) δ 9,06 (ушир.с, 1H), 7,77 (д, 2H), 7,44 (c, 1H), 7,35 (д, 2H), 7,26 (дд, 2H), 7,11 (т, 1H), 6,84 (д, 2H), 3,60 (м, 1H), 3,45 (м, 2H), 3,32 (м, 1H), 3,07 (м, 4H), 2,97 (м, 2H), 2,77 (м, 1H), 2,66 (м, 1H), 2,43 (c, 6H), 2,05 (м, 2H), 1,75 (м, 2H), 1,59 (м, 2H), 1,48 (м, 2H), 1,33 (м, 2H), 1,17 (м, 6H), 0,94 (м, 2H).
ПРИМЕР 2
N-{[5-({(1R)-3-(Диметиламино)-1-[(фенилтио)метил]пропил}амино)-4-нитротиен-2-ил]сульфонил}-4-[4-метокси-4-(3-метилбензил)пиперидин-1-ил]бензамид
ПРИМЕР 2А
Этил 4-(4-гидрокси-4-(3-метилбензил)пиперидин-1-ил)бензоат
Указанное соединение получают, заменив циклогексилметилмагнийбромид в примере 1F на 3-метилбензилмагнийхлорид.
ПРИМЕР 2В
Этил 4-(4-метокси-4-(3-метилбензил)пиперидин-1-ил)бензоат
Указанное соединение получают, заменив в примере 1G соединение по примеру 1F на соединение по примеру 2А.
ПРИМЕР 2С
4-(4-Метокси-4-(3-метилбензил)пиперидин-1-ил)бензойная кислота
Указанное соединение получают, заменив в примере 1H соединение по примеру 1G на соединение по примеру 2B.
ПРИМЕР 2D
N-{[5-({(1R)-3-(Диметиламино)-1-[(фенилтио)метил]пропил}амино)-4-нитротиен-2-ил]сульфонил}-4-[4-метокси-4-(3-метилбензил)пиперидин-1-ил]бензамид
Указанное соединение получают, заменив в примере 1I соединение по примеру 1H на соединение по примеру 2C.
1Н ЯМР (400 МГц, ДМСО-d6) δ 9,00 (ушир.с, 1H), 7,76 (д, 2H), 7,44 (c, 1H), 7,35 (д, 2H), 7,26 (дд, 2H), 7,16 (м, 2H), 6,89 (м, 3H), 6,82 (д, 2H), 4,05 (м, 1H), 3,61 (м, 1H), 3,48 (м, 2H), 3,32 (м, 2H), 3,27 (c, 3H), 3,17 (c, 2H), 3,07 (м, 1H), 2,92 (м, 2H), 2,74 (c, 6H), 2,27 (c, 3H), 2,07 (м, 2H), 1,67 (м, 2H), 1,52 (м, 2H).
ПРИМЕР 3
N-{[5-({(1R)-3-(Диметиламино)-1-[(фенилтио)метил]пропил}амино)-4-нитротиен-2-ил]сульфонил}-4-[4-(3,3-дифенилпроп-2-енил)пиперазин-1-ил]бензамид
ПРИМЕР 3А
Этил 4-(4-(3,3-дифенилаллил)пиперазин-1-ил)бензоат
Суспензию этил 4-пиперазин-1-илбензоата (1,36 г) и 3,3-дифенилакрилового альдегида (1,56 г) в дихлорметане (10 мл) и метаноле (10 мл) обрабатывают привитым на полимер цианоборгидридом (2,47 ммоль/г, 6 г), встряхивают при комнатной температуре в течение 24 час и фильтруют. Смолу промывают раствором 1:1 дихлорметан/метанол (10 мл × 3), фильтраты объединяют и концентрируют. Концентрат очищают хроматографией на силикагеле, проводя элюирование в градиенте 10-50% этилацетат/гексаны, и получают требуемый продукт.
ПРИМЕР 3В
4-(4-(3,3-Дифенилаллил)пиперазин-1-ил)бензойная кислота
Указанное соединение получают, заменив в примере 1H соединение по примеру 1G на соединение по примеру 3А.
ПРИМЕР 3С
N-{[5-({(1R)-3-(Диметиламино)-1-[(фенилтио)метил]пропил}амино)-4-нитротиен-2-ил]сульфонил}-4-[4-(3,3-дифенилпроп-2-енил)пиперазин-1-ил]бензамид
Указанное соединение получают, заменив в примере 1I соединение по примеру 1H на соединение по примеру 3В.
1Н ЯМР (500 МГц, ДМСО-d6) δ 10,25 (ушир.с, 1H), 9,08 (ушир.с, 1H), 7,78 (д, 2H), 7,43 (м, 2H), 7,35 (м, 3H), 7,30 (д, 2H), 7,20-7,29 (м, 5H), 7,16 (м, 3H), 6,84 (д, 2H), 6,22 (т, 1H), 3,59 (м, 1H), 3,45 (м, 4H), 3,32 (м, 4H), 3,03 (м, 4H), 2,78 (м, 1H), 2,65 (м, 1H), 2,42 (c, 6H), 2,07 (м, 2H).
ПРИМЕР 4
4-{4-[(4'-Хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(4-{[2-(фенилтио)этил]амино}пиперидин-1-ил)сульфонил]бензамид
Пример 4А
Этил 4-(пиперазин-1-ил)бензоат
Суспензию пиперазина (129,2 г, 1,5 мол.), этил-4-фторбензоата (84 г, 0,5 мол.) и карбоната калия (103,65 г, 0,75 мол.) в ДМСО (200 мл) перемешивают в атмосфере N2 при 120°С в течение 6 час. Затем реакционную смесь охлаждают до комнатной температуры, выливают в воду (800 мл) и перемешивают в течение 30 мин. Требуемый продукт выделяют фильтрованием и передают на следующую стадию без дальнейшей очистки.
ПРИМЕР 4В
Этил 4-(4-(2-бромбензил)пиперазин-1-ил)бензоат
Раствор соединения по примеру 4А (23,43 г, 100,0 ммоль), 2-бромбензилбромида (26,24 г, 105,0 ммоль) и диизопропилэтиламина (20,94 мл, 120,0 ммоль) в ацетонитриле (200 мл) перемешивают при комнатной температуре в течение двух часов. Образовавшийся осадок отделяют фильтрованием и получают требуемый продукт, который используют без дальнейшей очистки.
ПРИМЕР 4C
Этил 4-(4-((4'-хлорбифенил-2-ил)метил)пиперазин-1-ил)бензоат
Суспензию соединения по примеру 4B (13,83 г, 34,3 ммоль), 4-хлорфенилбороновой кислоты (7,04 г, 45,0 ммоль), дихлорида бис(трифенилфосфин)палладия(II) (0,481 г, 0,686 ммоль, 2% мол.) и 2М водный раствор Na2CO3 (22,5 мл, 45,0 ммоль) в смеси дихлорметан/Н2О/этанол (7:3:2, 200 мл) нагревают до температуры 90°С в течение 4,5 час и разбавляют этилацетатом (200 мл). Слои разделяют и органическую фазу сушат (над MgSO4), фильтруют и концентрируют. Остаток очищают хроматографией на силикагеле, проводя градиентное элюирование в смеси 5%-40% этилацетат/гексаны, и получают требуемый продукт.
ПРИМЕР 4D
4-(4-((4'-Хлорбифенил-2-ил)метил)пиперазин-1-ил)бензойная кислота
Суспензию соединения по примеру 4C (13,0 г, 29,9 ммоль) и моногидрата LiOH (3,78 г, 90,0 ммоль) в диоксане (250 мл) и воде (100 мл) нагревают до 95°С в течение 16 час, концентрируют досуха, добавляют воду (600 мл), нагревают до температуры 80°С и отфильтровывают. Фильтрат обрабатывают 1М раствором HCl (90 мл) и образовавшийся осадок отделяют фильтрованием, получая требуемый продукт.
ПРИМЕР 4Е
трет-Бутил 4-оксопиперидин-1-илсульфонилкарбамат
Хлорсульфонилизоцианат (1,044 г, 7,353 ммоль) добавляют к дихлорметану (20 мл) и полученную смесь охлаждают до 0°С. Добавляют трет-бутанол (544 мг, 7,353 ммоль) в дихлорметане (3 мл) и образовавшийся раствор перемешивают при 0°С в течение 30 мин. Полученный раствор затем добавляют в отдельную колбу, содержащую гидрохлорид 4-пиперидона (1,00 г, 7,353 ммоль) и триэтиламин (3,1 мл, 22,059 ммоль) в дихлорметане (20 мл), охлажденном до 0°С. По окончании добавления раствору дают нагреться до комнатной температуры и перемешивают в течение двух часов. Затем смесь перераспределяют между дихлорметаном и насыщенным водным раствором хлорида аммония. Водный слой трижды экстрагируют дихлорметаном, органические экстракты объединяют и сушат над безводным сульфатом магния. Раствор концентрируют и очищают колоночной флэш-хроматографией на силикагеле, элюируя в градиенте от 0% этилацетата в дихлорметане до 20% этилацетата в дихлорметане.
ПРИМЕР 4F
4-Оксопиперидин-1-илсульфонамид
Соединение по примеру 4Е (500 мг) растворяют в 1,4-диоксане (4 мл), обрабатывают 4М раствором HCl (4 мл) и перемешивают при комнатной температуре в течение трех часов. Раствор концентрируют и очищают колоночной флэш-хроматографией на силикагеле, элюируя в градиенте от 0% ацетонитрила (в дихлорметане) до 40% ацетонитрила (в дихлорметане).
ПРИМЕР 4G
4-(4-((4'-Хлорбифенил-2-ил)метил)пиперазин-1-ил)-N-(4-оксопиперидин-1-илсульфонил)бензамид
Указанное соединение получают, заменив в примере 1I соединение по примеру 1E соединением по примеру 4F, а соединение по примеру 1H соединением по примеру 4D.
ПРИМЕР 4H
4-{4-[(4'-Хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(4-{[2-(фенилтио)этил]амино}пиперидин-1-ил)сульфонил]бензамид
Соединение по примеру 4G (100 мг, 0,176 ммоль), 2-(фенилтио)этанамин (30 мг, 0,194 ммоль), триацетоксиборгидрид натрия (56 мг, 0,264 ммоль) и уксусную кислоту (11 мкл, 0,194 ммоль) добавляют к 1,2-дихлорэтану (2 мл) и перемешивают при комнатной температуре в течение шести часов. Растворитель удаляют в вакууме, а к остатку добавляют воду. Осадок отфильтровывают, сушат, растворяют в смеси диметилсульфоксид/метанол, содержащей несколько капель триэтиламина, и очищают методом препаративной ВЭЖХ на колонке Phenomenex Luna C8(2) 5 мкм 100Å AXIA column (30×75 мм). Используют градиент ацетонитрила (А) и 0,1%-го раствора трифторуксусной кислоты в воде (В) при скорости потока 50 мл/мин (0-0,5 мин: 10% А, 0,5-7,0 мин: линейный градиент 10-95% А, 7,0-10,0 мин: 95% А, 10,0-12,0 мин: линейный градиент 95-10% А).
1Н ЯМР (400 МГц, ДМСО-d6) δ 11,53 (ушир.с, 1H), 8,92 (ушир.с, 2H), 7,76 (д, 2H), 7,70 (ушир.с, 1H), 7,48 (м, 4H), 7,38-7,26 (м, 7H), 7,24-7,17 (м, 1H), 4,18 (ушир.с, 2H), 3,74 (д, 4H), 3,21-3,16 (м, 6H), 3,08 (ушир.с, 4H), 2,87 (т, 4H), 2,04 (д, 2H), 1,48 (м, 2H).
ПРИМЕР 5
N-[(4-{Ацетил[2-(фенилтио)этил]амино}пиперидин-1-ил)сульфонил]-4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензамид
Соединение по примеру 4H (30 мг, 0,0426 ммоль), уксусный ангидрид (4,3 мг, 0,0426 ммоль) и триэтиламин (18 мкл, 0,128 ммоль) добавляют к дихлорметану (1 мл) и перемешивают при комнатной температуре в течение четырех часов. Растворитель удаляют в вакууме, остаток растворяют в смеси диметилсульфоксид/метанол и очищают методом препаративной ВЭЖХ на колонке Phenomenex Luna C8(2) 5 мкм 100Å AXIA column (30×75 мм). Используют градиент ацетонитрила (А) и 0,1%-го раствора трифторуксусной кислоты в воде (В) при скорости потока 50 мл/мин (0-0,5 мин: 10% А, 0,5-7,0 мин: линейный градиент 10-95% А, 7,0-10,0 мин: 95% А, 10,0-12,0 мин: линейный градиент 95-10% А).
1Н ЯМР (400 МГц, ДМСО-d6) δ 11,50 (ушир.с, 1H), 7,82 (д, 2H), 7,74 (ушир.с, 1H), 7,52 (д, 4H), 7,40 (т, 4H), 7,35-7,25 (м, 3H), 7,18 (дт, 1H), 6,94 (д, 2H), 4,26 (ушир.с, 2H), 3,96 (т, 1H), 3,75 (д, 4H), 3,28 (дт, 4H), 3,10-2,85 (м, 8H), 2,04 (c, 2H), 1,88 (c, 1H), 1,75-1,56 (м, 4H).
ПРИМЕР 6
4-{4-[(4'-Хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(4-{метил[2-(фенилтио)этил]амино}пиперидин-1-ил)сульфонил]бензамид
Соединение по примеру 4H (30 мг, 0,0426 ммоль), формальдегид (37%-й раствор в воде, 10 мкл, 0,128 ммоль) и триацетоксиборгидрид натрия (14 мг, 0,0639 ммоль) добавляют к ацетонитрилу (0,8 мл) и воде (0,2 мл). Растворитель удаляют в вакууме, остаток растворяют в смеси диметилсульфоксид/метанол и очищают методом препаративной ВЭЖХ на колонке Phenomenex Luna C8(2) 5 мкм 100Å AXIA column (30×75 мм). Используют градиент ацетонитрила (А) и 0,1%-го раствора трифторуксусной кислоты в воде (В) при скорости потока 50 мл/мин (0-0,5 мин: 10% А, 0,5-7,0 мин: линейный градиент 10-95% А, 7,0-10,0 мин: 95% А, 10,0-12,0 мин: линейный градиент 95-10% А).
1Н ЯМР (400 МГц, ДМСО-d6) δ 11,32 (ушир.с, 1H), 9,84 (ушир.с, 1H), 7,54 (д, 2H), 7,49 (ушир.с, 1H), 7,26 (д, 4H), 7,12 (д, 4H), 7,11-7,07 (м, 3H), 6,99 (т, 1H), 6,69 (д, 2H), 3,98 (ушир.с, 2H), 3,56 (д, 2H), 3,33-3,11 (м, 4H), 3,09-2,91 (м, 7H), 2,68 (т, 4H), 2,49 (c, 3H), 1,72 (д, 2H), 1,38 (ушир.с, 2H).
ПРИМЕР 7
4-{4-[(4'-Хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-{[5-({(1R)-3-[изопропил(метил)амино]-1-[(фенилтио)метил]пропил}амино)-4-нитротиен-2-ил]сульфонил}бензамид
ПРИМЕР 7А
(R)-Бензил 4-оксо-1-(фенилтио)бутан-2-илкарбамат
В трехгорлую круглодонную колбу емкостью 100 мл помещают соединение по примеру 1В (3,75 г, 10,0 ммоль) и в атмосфере аргона с помощью шприца добавляют бис(циклопентадиенил)цирконий хлорид гидрид (3,85 г, 15,0 ммоль) в 50 мл безводного ТГФ (воздух из системы вытесняют тремя циклами откачивания в вакууме и заполнения аргоном). Смесь перемешивают при комнатной температуре в течение 20 мин, при этом раствор становится прозрачным. Анализ методом ТСХ указывает на окончание реакции, и смесь концентрируют. Остаток помещают на слой силикагеля и промывают смесью гексан/этилацетат (1:1, 300 мл). После концентрирования получают указанное в названии соединение.
ПРИМЕР 7В
(R)-Бензил 4-(изопропил(метил)амино)-1-(фенилтио)бутан-2-илкарбамат
В круглодонную колбу емкостью 250 мл, содержащую соединение по примеру 7А (2,87 г, 8,71 ммоль), добавляют 50 мл 1,2-дихлорэтана, метилизопропиламин (1,92 г, 26,25 ммоль) и триацетоксиборгидрид натрия (3,0 г, 14,1 ммоль). Смесь в атмосфере N2 перемешивают при комнатной температуре в течение двух часов. Смесь разбавляют этилацетатом (200 мл) и промывают 2 н. раствором NaOH, водой, насыщенным раствором соли и сушат над Na2SO4. Растворитель удаляют в вакууме и получают указанное в названии соединение.
ПРИМЕР 7С
(R)-N1-Изопропил-N1-метил-4-(фенилтио)бутан-1,3-диамин
Соединение по примеру 7В (0,56 г, 1,47 ммоль) растворяют в ацетонитриле (10 мл) и добавляют триметилсилилиодид (400 мкл). Смесь оставляют на ночь перемешиваться при комнатной температуре. Прерывают реакцию, добавив метанол, концентрируют в вакууме, остаток растворяют в этилацетате (200 мл) и дважды промывают 1,5%-ным раствором HCl (50 мл). Водные слои объединяют и подщелачивают твердым NaOH, а затем экстрагируют этилацетатом (100 мл × 3). Объединенные экстракты промывают насыщенным раствором соли и сушат над Na2SO4. После упаривания растворителя получают указанное в названии соединение.
ПРИМЕР 7D
(R)-5-(4-Изопропил(метил)амино)-1-(фенилтио)бутан-2-иламино)-4-нитротиофен-2-сульфонамид
В склянку, содержащую соединение по примеру 7С (0,43 г, 1,69 ммоль) добавляют 2-хлор-3-нитротиофен-5-сульфонамид (0,409 г, 1,69 ммоль) и ДМСО (5 мл), а затем добавляют диизопропилэтиламин (1 мл, 5,74 ммоль). Смесь оставляют на ночь перемешиваться при температуре 60°С, разбавляют смесь этилацетатом и промывают водным раствором NaHCO3, водой и насыщенным раствором соли. После сушки над Na2SO4 и упаривания растворителя остаток помещают в колонку со слоем силикагеля и элюируют смесью этилацетат/дихлорметан (насыщенной аммиаком) и получают указанное в названии соединение.
ПРИМЕР 7Е
4-{4-[(4'-Хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-{[5-({(1R)-3-[изопропил(метил)амино]-1-[(фенилтио)метил]-пропил}амино)-4-нитротиен-2-ил]сульфонил}бензамид
Указанное в названии соединение получают, как указано в примере 1I, заменив соединение по примеру 1Е и соединение по примеру 1Н на соединение по примеру 7D и соединение по примеру 4D, соответственно.
1Н ЯМР (300 МГц, ДМСО-d6) δ ppm 8,98 (м, 1H), 7,83 (м, 2H), 7,70 (м, 1H), 7,52 (м, 4H), 7,35 (м, 6H), 7,16 (м, 4H), 6,96 (м, 2H), 3,77 (м, 2H), 3,59 (м, 5H), 3,21 (м, 7H), 2,64 (т, 3H), 2,52 (д, 6H), 1,19 (д, 4H).
ПРИМЕР 8
4-(4-{[2-(4-Хлорфенил)циклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-{[5-({(1R)-3-[изопропил(метил)амино]-1-[(фенилтио)метил]пропил}амино)-4-нитротиен-2-ил]сульфонил}бензамид
ПРИМЕР 8А
Этил 2-(трифторметилсульфонилокси)циклогекс-1-енкарбоксилат
К охлажденной (0°С) суспензии NaH (0,983 г 60%-й дисперсии в минеральном масле, которую промывают три раза гексаном) в эфире (50 мл) при перемешивании добавляют этил 2-оксоциклогексанкарбоксилат (3,2 г, 20,5 ммоль). Смесь перемешивают при 0°С в течение 30 мин, а затем добавляют ангидрид трифторметансульфоновой кислоты (4,2 мл, 25 ммоль). Смесь оставляют на ночь перемешиваться при комнатной температуре. Разбавляют смесь эфиром (200 мл) и промывают 5% раствором HCl, водой и насыщенным раствором соли. После сушки над Na2SO4 и упаривания растворителя получают сырой продукт, который используют без дальнейшей очистки.
ПРИМЕР 8В
Этил 2-(4-хлорфенил)циклогекс-1-енкарбоксилат
К раствору соединения по примеру 8А (2,88 г, 10 ммоль), 4-хлорфенилбороновой кислоты (1,88 г, 12 ммоль) и тетракис(трифенилфосфин)палладия(0) (0,578 г, 0,5 ммоль) в толуоле (40 мл) и этаноле (10 мл) добавляют 2н. раствор Na2CO3 (10 мл). Смесь оставляют на ночь кипеть с обратным холодильником. Разбавляют смесь эфиром (300 мл) и промывают водой, насыщенным раствором соли и сушат над Na2SO4. После упаривания растворителя остаток помещают в колонку и элюируют 3% этилацетатом в гексане, получая указанное в названии соединение.
ПРИМЕР 8С
(2-(4-Хлорфенил)циклогекс-1-енил)метанол
К раствору соединения по примеру 8В (1,6 г, 6,38 ммоль) в эфире (20 мл) добавляют LiAlH4 (1,2 г, 32 ммоль). Смесь перемешивают при комнатной температуре в течение четырех часов. Смесь осторожно подкисляют 5% раствором HCl, экстрагируют этилацетатом (100 мл × 3), промывают водой, насыщенным раствором соли и сушат над Na2SO4. После упаривания растворителя сырой продукт помещают в колонку и элюируют 10% этилацетатом в гексане, получая указанное в названии соединение.
ПРИМЕР 8D
2-(4-Хлорфенил)циклогекс-1-енкарбальдегид
К раствору оксалилхлорида (1,1 г, 8,63 ммоль) в дихлорметане (30 мл) при температуре -78°С добавляют диметилсульфоксид (6,12 мл, 86 ммоль). Смесь перемешивают при температуре -78°С в течение 30 мин, а затем добавляют раствор соединения по примеру 8С (1,2 г, 5,75 ммоль) в дихлорметане (10 мл). Смесь перемешивают при температуре -78°С еще в течение 2 час, а затем добавляют триэтиламин (10 мл). Смесь оставляют перемешиваться на ночь и дают температуре подняться до комнатной. Разбавляют смесь эфиром (300 мл) и промывают водой, насыщенным раствором соли и сушат над Na2SO4. После упаривания растворителя и очистки на колонке (5% этилацетата в гексане) получают указанное в названии соединение.
ПРИМЕР 8Е
Этил 4-(4-((2-(4-хлорфенил)циклогекс-1-енил)метил)пиперазин-1-ил)бензоат
К соединению по примеру 8D (100 мг, 0,484 ммоль) и соединению по примеру 4А (177 мг, 0,484 ммоль) в 1,2-дихлорэтане (10 мл) добавляют триацетоксиборгидрид натрия (154 мг, 0,726 ммоль). Смесь оставляют перемешиваться на ночь при комнатной температуре. Разбавляют смесь этилацетатом (200 мл) и промывают 2% раствором NaOH, водой и насыщенным раствором соли. После сушки над Na2SO4 растворитель концентрируют в вакууме, остаток помещают в колонку и элюируют 30% этилацетата в гексане, получая указанное в названии соединение.
ПРИМЕР 8F
4-(4-((2-(4-Хлорфенил)циклогекс-1-енил)метил)пиперазин-1-ил)бензойная кислота
К раствору соединения по примеру 8Е (254 мг, 0,457 ммоль) в тетрагидрофуране (4 мл), метаноле (2 мл) и воде (2 мл) добавляют моногидрат гидроксида лития (126 мг, 3 ммоль). Смесь оставляют перемешиваться на ночь при комнатной температуре. Затем смесь нейтрализуют 5% раствором HCl и разбавляют этилацетатом (200 мл). После промывки насыщенным раствором соли раствор сушат над Na2SO4. Упариванием растворителя получают указанное в названии соединение.
ПРИМЕР 8G
4-(4-{[2-(4-Хлорфенил)циклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-{[5-({(1R)-3-[изопропил(метил)амино]-1-[(фенилтио)метил]пропил}амино)-4-нитротиен-2-ил]сульфонил}бензамид
Указанное в названии соединение получают, как указано в примере 1I, заменив соединение по примеру 1Е и соединение по примеру 1Н соединением по примеру 7D и соединением по примеру 8F, соответственно. 1Н ЯМР (300 МГц, ДМСО-d6) δ 8,97 (м, 1H), 7,83 (м, 2H), 7,68 (м, 1H), 7,42 (м, 2H), 7,30 (м, 2H), 7,17 (м, 5H), 6,97 (м, 2H), 3,91 (м, 2H), 3,66 (м, 3H), 3,18 (м, 7H), 2,87 (м, 3H), 2,64 (т, 3H), 2,51 (д, 6H), 2,24 (м, 4H), 1,72 (м, 3H), 1,18 (м, 6H).
ПРИМЕР 9
4-(4-{[2-(4-Хлорфенил)-5,5-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-{[5-({(1R)-3-[изопропил(метил)амино]-1-[(фенилтио)метил]пропил}амино)-4-нитротиен-2-ил]сульфонил}бензамид
ПРИМЕР 9А
Метил 5,5-диметил-2-оксоциклогексанкарбоксилат
К суспензии промытого гексаном NaH (0,72 г, 60%, 18 ммоль) в тетрагидрофуране (30 мл) добавляют раствор 4,4-диметилциклогексанона (2,0 г, 15,6 ммоль) в тетрагидрофуране (20 мл). Полученную суспензию перемешивают при комнатной температуре в течение 30 мин. Затем по каплям с помощью шприца добавляют диметилкарбонат (6,31 мл, 75 ммоль). Смесь кипятят с обратным холодильником в течение четырех час. Подкисляют смесь 5% раствором HCl и экстрагируют дихлорметаном (100 мл × 3), а затем промывают водой, насыщенным раствором соли и сушат над Na2SO4. После концентрирования сырой продукт помещают в колонку и элюируют 10% раствором этилацетата в гексане, получая указанное в названии соединение.
ПРИМЕР 9В
Метил 5,5-диметил-2-(трифторметилсульфонилокси)циклогекс-1-енкарбоксилат
Указанное в названии соединение получают аналогично примеру 8А, заменив этил 2-оксоциклогексанкарбоксилат соединением по примеру 9А.
ПРИМЕР 9С
Метил 2-(4-хлорфенил)-5,5-диметилциклогекс-1-енкарбоксилат
Указанное в названии соединение получают аналогично примеру 8В, заменив соединение по примеру 8А соединением по примеру 9В.
ПРИМЕР 9D
(2-(4-Хлорфенил)-5,5-диметилциклогекс-1-енил)метанол
Указанное в названии соединение получают аналогично примеру 8С, заменив соединение по примеру 8В соединением по примеру 9С.
ПРИМЕР 9Е
2-(4-Хлорфенил)-5,5-диметилциклогекс-1-енкарбальдегид
Указанное в названии соединение получают аналогично примеру 8D, заменив соединение по примеру 8C соединением по примеру 9D.
ПРИМЕР 9F
Этил 4-(4-((2-(4-хлорфенил)-5,5-диметилциклогекс-1-енил)метил)пиперазин-1-ил)бензоат
Указанное в названии соединение получают аналогично примеру 8E, заменив соединение по примеру 8D соединением по примеру 9E.
ПРИМЕР 9G
4-(4-((2-(4-Хлорфенил)-5,5-диметилциклогекс-1-енил)метил)пиперазин-1-ил)бензойная кислота
Указанное в названии соединение получают аналогично примеру 8F, заменив соединение по примеру 8E соединением по примеру 9F.
ПРИМЕР 9H
4-(4-{[2-(4-Хлорфенил)-5,5-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-{[5-({(1R)-3-[изопропил(метил)амино]-1-[(фенилтио)метил]пропил}амино)-4-нитротиен-2-ил]сульфонил}бензамид
Указанное в названии соединение получают, как указано в примере 1I, заменив соединение по примеру 1Е и соединение по примеру 1Н соединением по примеру 7D и соединением по примеру 9G, соответственно.
1Н ЯМР (300 МГц, ДМСО-d6) δ 8,96 (м, 1H), 7,83 (м, 2H), 7,67 (м, 1H), 7,42 (м, 2H), 7,29 (м, 2H), 7,17 (м, 6H), 6,97 (м, 2H), 3,90 (м, 2H), 3,61 (м, 8H), 3,19 (м, 3H), 2,65 (м, 3H), 2,23 (м, 5H), 2,04 (м, 2H), 1,48 (м, 2H), 1,19 (м, 6H), 1,00 (c, 6H).
ПРИМЕР 10
N-{[(5Z)-5-(Ацетилимино)-4-метил-4,5-дигидро-1,3,4-тиадиазол-2-ил]сульфонил}-4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензамид
Соединение по данному примеру получают, заменив в примере 1I соединение 1Н соединением по примеру 4D и взяв (Z)-N-(3-метил-5-сульфамоил-1,3,4-тиадиазол-2(3Н)илиден)ацетамид вместо соединения по примеру 1Е.
1Н ЯМР (300 МГц, ДМСО-d6) δ 7,74 (д, 2H), 7,48 (м, 5H), 7,38 (м, 2H), 7,24 (м, 1H), 6,83 (д, 2H), 3,84 (c, 2H), 3,17 (м, 4H), 2,40 (м, 4H), 1,82 (c, 6H).
ПРИМЕР 11
N-{[2-(Ацетиламино)-4-метил-1,3-тиазол-5-ил]сульфонил}-4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензамид
ПРИМЕР 11А
N-(4-Метил-5-сульфамоилтиазол-2-ил)ацетамид
2-Ацетамидо-4-метилтиазол-5-сульфонилхлорид (0,50 г, 1,96 ммоль) растворяют в ТГФ (7 мл), охлаждают до 0°С и добавляют концентрированный раствор NH4OH (0,7 мл). Через 3 час реакционную смесь концентрируют, разбавляют водой и экстрагируют смесью CHCl3/метанол. Органический слой сушат над Na2SO4. После фильтрования и концентрирования получают продукт, который используют в примере 11В.
ПРИМЕР 11В
N-{[2-(Ацетиламино)-4-метил-1,3-тиазол-5-ил]сульфонил}-4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензамид
Соединение по данному примеру получают, заменив в примере 1I соединение по примеру 1Н соединением по примеру 4D и взяв соединение 11А вместо соединения по примеру 1Е, за исключением того, что для очистки используют метод ВЭЖХ на колонке С18, 250×50 мм, 10 мкм, проводя элюирование в градиенте 20-100% CH3CN против 0,1%-го раствора TFA в воде, при этом получают продукт в виде трифторацетатной соли.
1Н ЯМР (300 МГц, ДМСО-d6) δ 12,60 (c, 1H), 12,30 (очень шир.c, 1H), 9,60 (очень шир.c, 1H), 7,80 (д, 2H), 7,75 (ушир.с, 1H), 7,52 (м, 4H), 7,40 (д, 2H), 7,36 (м, 1H), 6,94 (д, 2H), 4,38 (ушир.с, 1H), 3,85 (ушир.с, 1H), 3,40-2,80 (огибающая, 8H), 2,52 (c, 3H), 2,18 (c, 3H).
ПРИМЕР 12
N-({5-[(Бензоиламино)метил]тиен-2-ил}сульфонил)-4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензамид
ПРИМЕР 12А
N-((5-Сульфамоилтиофен-2-ил)метил)бензамид
Соединение по данному примеру получают, заменив в примере 11А 2-ацетамидо-4-метилтиазол-5-сульфонилхлорид на 5-(бензамидометил)тиофен-2-сульфонилхлорид.
ПРИМЕР 12В
N-({5-[(Бензоиламино)метил]тиен-2-ил}сульфонил)-4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензамид
Соединение по данному примеру получают, заменив в примере 1I соединение по примеру 1Н соединением по примеру 4D и взяв соединение 12А вместо соединения по примеру 1Е, за исключением того, что очистку проводят так, как описано в примере 11В.
1Н ЯМР (300 МГц, ДМСО-d6) δ 12,20 (очень шир.c, 1H), 9,60 (очень шир.c, 1H), 9,26 (т, 1H), 7,87 (д, 2H), 7,79 (м, 3H), 7,67 (д, 1H), 7,51 (м, 7H), 7,40 (д, 2H), 7,36 (м, 1H), 7,09 (д, 1Н), 6,90 (д, 2H), 4,64 (д, 2H), 4,38 (ушир.с, 1H), 3,85 (ушир.с, 1H), 3,40-2,80 (огибающая, 8H).
ПРИМЕР 13
4-{4-[(4'-Хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(6-хлоримидазо[2,1-b][1,3]тиазол-5-ил)сульфонил]бензамид
Соединение по данному примеру получают, заменив в примере 1I соединение по примеру 1Н соединением по примеру 4D и взяв 6-хлоримидазо[2,1-b]тиазол-5-сульфонамид вместо соединения по примеру 1Е, за исключением того, что очистку проводят так, как описано в примере 11В.
1Н ЯМР (300 МГц, ДМСО-d6) δ 9,60 (очень шир.c, 1H), 8,04 (д, 1H), 7,79 (м, 3H), 7,63 (д, 1H), 7,51 (м, 4H), 7,40 (д, 2H), 7,36 (м, 1H), 6,92 (д, 2H), 4,38 (ушир.с, 1H), 3,85 (ушир.с, 1H), 3,40-2,80 (огибающая, 8H).
ПРИМЕР 14
4-{4-[(4'-Хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-(морфолин-4-илсульфонил)бензамид
Соединение по данному примеру получают, заменив в примере 1I соединение по примеру 1Н соединением по примеру 4D и взяв морфолин-4-сульфонамид вместо соединения по примеру 1Е, за исключением того, что очистку проводят так, как описано в примере 11В.
1Н ЯМР (300 МГц, ДМСО-d6) δ 11,58 (ушир.с, 1H), 9,60 (очень шир.c, 1H), 7,82 (д, 2H), 7,75 (ушир.с, 1H), 7,55 (м, 4H), 7,40 (д, 2H), 7,36 (м, 1H), 6,96 (д, 2H), 4,38 (ушир.с, 1H), 3,85 (ушир.с, 1H), 3,61 (м, 4H), 3,40-2,80 (огибающая, 8H), 3,25 (м, 4H).
ПРИМЕР 15
4-{4-[(4'-Хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(2,4-диметил-1,3-тиазол-5-ил)сульфонил]бензамид
Соединение по данному примеру получают, заменив в примере 1I соединение по примеру 1Н соединением по примеру 4D и взяв 2,4-диметилтиазол-5-сульфонамид вместо соединения по примеру 1Е, за исключением того, что очистку в данном случае проводят так, как описано в примере 11В.
1Н ЯМР (300 МГц, ДМСО-d6) δ 12,40 (очень шир.c, 1H), 9,60 (очень шир.c, 1H), 7,80 (д, 2H), 7,75 (ушир.с, 1H), 7,55 (м, 4H), 7,40 (д, 2H), 7,36 (м, 1H), 6,94 (д, 2H), 4,38 (ушир.с, 1H), 3,85 (ушир.с, 1H), 3,40-2,80 (огибающая, 8H), 2,65 (c, 3H), 2,55 (c, 3H).
ПРИМЕР 16
4-{4-[(4'-Хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-{[4-фенил-5-(трифторметил)тиен-3-ил]сульфонил]бензамид
ПРИМЕР 16А
4-Фенил-5-(трифторметил)тиофен-3-сульфонамид
Соединение по данному примеру получают, заменив 2-ацетамидо-4-метилтиазол-5-сульфонилхлорид в примере 11А на 4-фенил-5-(трифторметил)тиофен-3-сульфонилхлорид.
ПРИМЕР 16В
4-{4-[(4'-Хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-{[4-фенил-5-(трифторметил)тиен-3-ил]сульфонил]бензамид
Соединение по данному примеру получают, заменив в примере 1I соединение по примеру 1Н соединением по примеру 4D, а соединение по примеру 1Е соединением по примеру 16А, за исключением того, что очистку в данном случае проводят так, как описано в примере 11В.
1Н ЯМР (300 МГц, ДМСО-d6) δ 11,85 (очень шир.c, 1H), 9,60 (очень шир.c, 1H), 8,80 (c,1Н), 7,77 (ушир.с, 1H), 7,60 (д, 2H), 7,53 (м, 4H), 7,40 (м, 3H), 7,35 (м, 3H), 7,16 (д, 2H), 6,89 (д, 2H), 4,38 (ушир.с, 1H), 3,85 (ушир.с, 1H), 3,40-2,80 (огибающая, 8H).
ПРИМЕР 17
4-{4-[(4'-Хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(5-фтор-3-метил-1-бензотиен-2-ил)сульфонил]бензамид
Пример 17А
5-Фтор-3-метилбензо[b]тиофен-2-сульфонамид
Соединение по данному примеру получают, заменив 2-ацетамидо-4-метилтиазол-5-сульфонилхлорид в примере 11А на 5-фтор-3-метилбензо[b]тиофен-2-сульфонилхлорид.
ПРИМЕР 17В
4-{4-[(4'-Хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(5-фтор-3-метил-1-бензотиен-2-ил)сульфонил]бензамид
Соединение по данному примеру получают, заменив в примере 1I соединение по примеру 1Н соединением по примеру 4D, а соединение по примеру 1Е соединением по примеру 17А, за исключением того, что очистку в данном случае проводят так, как описано в примере 11В.
1Н ЯМР (300 МГц, ДМСО-d6) δ 12,60 (очень шир.c, 1H), 9,60 (очень шир.c, 1H), 8,12 (дд, 1H), 7,85 (д, 1H) 7,80 (м, 3H), 7,52 (м, 4H), 7,46 (дд, 1H), 7,40 (д, 2H), 7,36 (м, 1H), 6,92 (д, 2H), 4,38 (ушир.с, 1H), 3,85 (ушир.с, 1H), 3,40-2,80 (огибающая, 8H), 2,66 (c, 3H).
ПРИМЕР 18
N-(1,3-Бензотиазол-2-илсульфонил)-4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензамид
ПРИМЕР 18А
Бензо[d]тиазол-2-сульфонамид
Бензо[d]тиазол-2-сульфонамид получают, как описано в Roblin, Jr, R.O.; Clapp, J.W., J. Am. Chem. Soc. 1950, 72, 4890-4892.
ПРИМЕР 18В
N-(1,3-Бензотиазол-2-илсульфонил)-4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензамид
Соединение по данному примеру получают, заменив в примере 1I соединение по примеру 1Н соединением по примеру 4D, а соединение по примеру 1Е соединением по примеру 18А, за исключением того, что очистку в данном случае проводят так, как описано в примере 11В.
1Н ЯМР (500 МГц, ДМСО-d6) δ 11,79 (ушир.с, 1H), 8,17 (д, 1H), 8,03 (д, 1H), 7,78 (д, 2H), 7,74 (ушир.с, 1H), 7,55 (м, 6H), 7,40 (д, 2H), 7,34 (д, 1H), 6,87 (д, 2H), 4,36 (м, 2H), 3,80 (м, 2H), 3,42 (м, 2H), 3,05 (м, 2H), 2,90 (м, 2H).
ПРИМЕР 19
4-{4-[(4'-Хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-(тиен-2-илсульфонил)бензамид
Соединение по данному примеру получают, заменив в примере 1I соединение по примеру 1Н на соединение по примеру 4D, а соединение по примеру 1Е на тиофен-2-сульфонамид, за исключением того, что очистку в данном случае проводят так, как описано в примере 11В.
1Н ЯМР (500 МГц, ДМСО-d6) δ 12,33 (ушир.с, 1H), 8,02 (дд, 1H), 7,82 (дд, 1H), 7,78 (д, 2H), 7,75 (ушир.с, 1H), 7,54 (м, 4H), 7,39 (д, 2H), 7,34 (м, 1H), 7,20 (дд, 1H), 6,94 (д, 2H), 4,33 (м, 2H), 3,89 (м, 2H), 3,25 (м, 2H), 3,12 (м, 2H), 2,91 (м, 2H).
ПРИМЕР 20
4-{4-[(4'-Хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(5,7-диметил[1,2,4]триазоло[1,5-a]пиримидин-2-ил)сульфонил]бензамид
ПРИМЕР 20А
5,7-Диметил-[1,2,4]триазоло[1,5-a]пиримидин-2-сульфонамид
Соединение по данному примеру получают, заменив 2-ацетамидо-4-метилтиазол-5-сульфонилхлорид в примере 11А на 5,7-диметил-[1,2,4]триазоло[1,5-a]пиримидин-2-сульфонилхлорид.
ПРИМЕР 20В
4-{4-[(4'-Хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(5,7-диметил[1,2,4]триазоло[1,5-a]пиримидин-2-ил)сульфонил]бензамид
Соединение по данному примеру получают, заменив в примере 1I соединение по примеру 1Н соединением по примеру 4D, а соединение по примеру 1Е соединением по примеру 20А, за исключением того, что очистку в данном случае проводят так, как описано в примере 11В.
1Н ЯМР (300 МГц, ДМСО-d6) δ 9,60 (очень шир.c, 1H), 7,81 (д, 2H), 7,75 (ушир.с, 1H), 7,55 (м, 4H), 7,40 (д, 2H), 7,39 (c, 1H), 7,36 (м, 1H), 6,94 (д, 2H), 4,38 (ушир.с, 1H), 3,85 (ушир.с, 1H), 3,40-2,80 (огибающая, 8H), 2,78 (c, 3H), 2,62 (c, 3H).
ПРИМЕР 21
Этил 4-{[(4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензоил)амино]сульфонил}-5-метил-1,2-дифенил-1H-пиррол-3-карбоксилат
ПРИМЕР 21А
Этил 5-метил-1,2-дифенил-4-сульфамоил-1Н-пиррол-3-карбоксилат
Соединение по данному примеру получают, заменив 2-ацетамидо-4-метилтиазол-5-сульфонилхлорид в примере 11А на метил 5-(хлорсульфонил)-1-метил-1Н-пиррол-2-карбоксилат.
ПРИМЕР 21В
Этил 4-{[(4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензоил)амино]сульфонил}-5-метил-1,2-дифенил-1H-пиррол-3-карбоксилат
Соединение по данному примеру получают, заменив в примере 1I соединение по примеру 1Н соединением по примеру 4D, а соединение по примеру 1Е соединением по примеру 21А, за исключением того, что очистку в данном случае проводят так, как описано в примере 11В.
1Н ЯМР (300 МГц, ДМСО-d6) δ 11,70 (ушир.с, 1H), 9,60 (очень шир.с, 1H), 7,90 (д, 2H), 7,77 (ушир.с, 1H), 7,53 (м, 4H), 7,40 (м, 6H), 7,27 (м, 2H), 7,20 (м, 3H), 7,09 (м, 2H), 6,92 (д, 2H), 4,38 (ушир.с, 1H), 4,00 (кв, 2H), 3,85 (ушир.с, 1H), 3,40-2,80 (огибающая, 8H), 2,35 (c, 3H), 0,90 (т, 3H).
ПРИМЕР 22
Метил 5-{[(4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензоил)амино]сульфонил}-1-метил-1H-пиррол-2-карбоксилат
ПРИМЕР 22А
Метил 1-метил-5-сульфамоил-1Н-пиррол-2-карбоксилат
Соединение по данному примеру получают, заменив 2-ацетамидо-4-метилтиазол-5-сульфонилхлорид в примере 11А на метил 5-(хлорсульфонил)-1-метил-1Н-пиррол-2-карбоксилат.
ПРИМЕР 22В
Метил 5-{[(4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензоил)амино]сульфонил}-1-метил-1H-пиррол-2-карбоксилат
Соединение по данному примеру получают, заменив в примере 1I соединение по примеру 1Н соединением по примеру 4D, а соединение по примеру 1Е соединением по примеру 22А, за исключением того, что очистку в данном случае проводят так, как описано в примере 11В.
1Н ЯМР (300 МГц, ДМСО-d6) δ 11,90 (ушир.с, 1H), 9,60 (очень шир.c, 1H), 7,85 (д, 1H), 7,78 (м, 3H), 7,55 (м, 4H), 7,40 (д, 2H), 7,36 (м, 1H), 7,15 (д, 1H), 7,92 (д, 2H), 4,38 (ушир.с, 1H), 3,90 (c, 3H), 3,85 (ушир.с, 1H), 3,78 (c, 3H), 3,40-2,80 (огибающая, 8H).
ПРИМЕР 23
4-{4-[(4'-Хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-{[5-(1,3-диметил-1H-пиразол-5-ил)изоксазол-4-ил]сульфонил}бензамид
ПРИМЕР 23А
5-(1,3-Диметил-1Н-пиразол-5-ил)изоксазол-4-сульфонамид
Соединение по данному примеру получают, заменив 2-ацетамидо-4-метилтиазол-5-сульфонилхлорид в примере 11А на 5-(1,3-диметил-1Н-пиразол-4-ил)изоксазол-4-сульфонилхлорид.
ПРИМЕР 23В
4-{4-[(4'-Хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-{[5-(1,3-диметил-1H-пиразол-5-ил)изоксазол-4-ил]сульфонил}бензамид
Соединение по данному примеру получают, заменив в примере 1I соединение по примеру 1Н соединением по примеру 4D, а соединение по примеру 1Е соединением по примеру 23А, за исключением того, что очистку в данном случае проводят так, как описано в примере 11В.
1Н ЯМР (300 МГц, ДМСО-d6) δ 11,90 (ушир.с, 1H), 9,60 (очень шир.c, 1H), 8,90 (c, 1H), 8,56 (c, 1H), 7,78 (м, 3H), 7,55 (м, 4H), 7,40 (д, 2H), 7,36 (м, 1H), 7,92 (д, 2H), 4,38 (ушир.с, 1H), 3,85 (ушир.с, 1H), 3,83 (c, 3H), 3,40-2,80 (огибающая, 8H), 2,37 (c, 3H).
ПРИМЕР 24
4-{4-[(4'-Хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(4-хлор-3-метилизотиазол-5-ил)сульфонил]бензамид
Соединение по данному примеру получают, заменив в примере 1I соединение по примеру 1Е на 4-хлор-3-метилизотиазол-5-сульфонамид, а соединение по примеру 1Н на соединение по примеру 4D.
1Н ЯМР (300 МГц, ДМСО-d6) δ 2,36 (c, 3H), 2,87-3,10 (м, 4H), 3,71-3,90 (м, 4H), 4,33-4,50 (м, 2H), 6,81-6,91 (м, 2H), 7,35-7,46 (м, 3H), 7,47-7,63 (м, 4H), 7,72-7,84 (м, 3H), 9,45 (c, 1H).
ПРИМЕР 25
N-[(5-Бром-3-метил-1-бензотиен-2-ил)сульфонил]-4-{4-[(4'-хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензамид
Соединение по данному примеру получают, заменив в примере 1I соединение по примеру 1Н соединением по примеру 4D, а соединение по примеру 1Е 5-бром-3-метилбензо[b]тиофен-2-сульфонамидом, за исключением того, что очистку в данном случае проводят так, как описано в примере 11В.
1Н ЯМР (300 МГц, ДМСО-d6) δ 12,60 (очень шир.c, 1H), 9,60 (очень шир.c, 1H), 8,19 (д, 1H), 8,05 (д, 1H), 7,80 (м, 3H), 7,70 (дд, 1H), 7,52 (м, 4H), 7,40 (д, 2H), 7,36 (м, 1H), 6,92 (д, 2H), 4,38 (ушир.с, 1H), 3,85 (ушир.с, 1H), 3,40-2,80 (огибающая, 8H), 2,66 (c, 3H).
ПРИМЕР 26
4-{4-[(4'-Хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-({5-[(E)-2-(1,2,4-оксадиазол-3-ил)винил]тиен-2-ил}сульфонил)бензамид
Соединение по данному примеру получают, заменив в примере 1I соединение по примеру 1Е на 5-(2-[1,2,4]оксадиазол-3-илвинил)тиофен-2-сульфонамид, а соединение по примеру 1Н на соединение по примеру 4D.
1Н ЯМР (300 МГц, ДМСО-d6) δ 2,73-2,99 (м, 2H), 3,00-3,22 (м, 2H), 3,73-4,03 (м, 4H), 4,23-4,49 (м, 2H), 6,89-6,99 (м, 2H), 7,26-7,45 (м, 4H), 7,48-7,58 (м, 4H), 7,61 (д, 1H), 7,71-7,83 (м, 5H), 7,83-7,92 (м, 1H), 9,62 (c, 1H).
ПРИМЕР 27
4-{4-[(4'-Хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-{[1-(2-хлорэтил)-3,5-диметил-1H-пиразол-4-ил]сульфонил}бензамид
Соединение по данному примеру получают, заменив в примере 1I соединение по примеру 1Е на 1-(2-хлорэтил)-3,5-диметил-1Н-пиразол-4-сульфонамид, а соединение по примеру 1Н на соединение по примеру 4D.
1Н ЯМР (300 МГц, ДМСО-d6) δ 2,02-2,09 (м, 3H), 2,29-2,35 (м, 3H), 2,77-2,97 (м, 2H), 2,98-3,17 (м, 2H), 3,81-4,00 (м, 6H), 4,28-4,45 (м, 4H), 6,86-6,99 (м, 2H), 7,32-7,44 (м, 3H), 7,48-7,60 (м, 4H), 7,71-7,82 (м, 3H), 9,52 (c, 1H), 12,01 (c, 1H).
ПРИМЕР 28
5-{[(4-{4-[(4'-Хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}бензоил)амино]сульфонил}-N-(1-этилпропил)-1,3,4-тиадиазол-2-карбоксамид
Соединение по данному примеру получают, заменив в примере 1I соединение по примеру 1Е на 5-(1-этилпропилкарбамоил)-[1,3,4]тиадиазол-2-сульфонамид, а соединение по примеру 1Н на соединение по примеру 4D.
1Н ЯМР (300 МГц, ДМСО-d6) δ 0,80 (т, 6H), 1,36-1,71 (м, 4H), 2,37-2,45 (м, 1H), 2,84-3,11 (м, 4H), 3,44-3,56 (м, 2H), 3,71-3,92 (м, 2H), 4,30-4,46 (м, 2H), 6,80-6,95 (м, 2H), 7,29-7,44 (м, 3H), 7,47-7,65 (м, 4H), 7,69-7,89 (м, 3H), 9,45 (c, 1H), 12,59-12,83 (м, 1H).
ПРИМЕР 29
4-{4-[(4'-Хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(5-хлор-1,3-диметил-1H-пиразол-4-ил)сульфонил]бензамид
Соединение по данному примеру получают, заменив в примере 1I соединение по примеру 1Е на 5-хлор-1,3-диметил-1Н-пиразол-4-сульфонамид, а соединение по примеру 1Н на соединение по примеру 4D.
1Н ЯМР (300 МГц, ДМСО-d6) δ 2,36 (c, 3H), 2,79-2,98 (м, 2H), 3,00-3,19 (м, 2H), 3,51-3,59 (м, 2H), 3,77 (c, 3H), 3,84-4,03 (м, 2H), 4,28-4,56 (м, 2H), 6,86-7,02 (м, 2H), 7,30-7,45 (м, 3H), 7,48-7,64 (м, 4H), 7,71-7,88 (м, 3H), 9,53 (c, 1H).
ПРИМЕР 30
4-{4-[(4'-Хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(4-нитро-5-пиперидин-1-илтиен-2-ил)сульфонил]бензамид
ПРИМЕР 30А
4-Нитро-5-(пиперидин-1-ил)тиофен-2-сульфонамид
Соединение по данному примеру получают, заменив в примере 1Е соединение по примеру 1D пиперидином.
ПРИМЕР 30В
4-{4-[(4'-Хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(4-нитро-5-пиперидин-1-илтиен-2-ил)сульфонил]бензамид
Соединение по данному примеру получают, заменив в примере 1I соединение по примеру 1Н соединением по примеру 4D, а соединение по примеру 1Е соединением по примеру 30А, за исключением того, что очистку в данном случае проводят так, как описано в примере 11В.
1Н ЯМР (500 МГц, ДМСО-d6) δ 11,79 (ушир.с, 1H), 7,93 (c, 1H), 7,80 (д, 2H), 7,74 (м, 1H), 7,52 (м, 4H), 7,39 (д, 2H), 7,34 (м, 1H), 6,94 (д, 2H), 4,25 (м, 2H), 3,56 (м, 4H), 3,35 (м, 4H), 3,25 (м, 2H), 2,91 (м, 2H), 1,7 (м, 4H), 1,61 (м, 2H).
ПРИМЕР 31
4-{4-[(4'-Хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(5-изоксазол-5-ил-2-фурил)сульфонил]бензамид
ПРИМЕР 31А
5-(Изоксазол-5-ил)фуран-2-сульфонамид
Соединение по данному примеру получают, заменив 2-ацетамидо-4-метилтиазол-5-сульфонилхлорид в примере 11А на 5-(изоксазол-5-ил)фуран-2-сульфонилхлорид.
ПРИМЕР 31В
4-{4-[(4'-Хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(5-изоксазол-5-ил-2-фурил)сульфонил]бензамид
Соединение по данному примеру получают, заменив в примере 1I соединение по примеру 1Н соединением по примеру 4D, а соединение по примеру 1Е соединением по примеру 31А, за исключением того, что очистку в данном случае проводят так, как описано в примере 11В.
1Н ЯМР (300 МГц, ДМСО-d6) δ 9,60 (очень шир.c, 1H), 8,76 (д, 1H), 7,80 (д, 2H), 7,75 (м, 1H), 7,55 (м, 4H), 7,40 (д, 2H), 7,42 (ушир.с, 1H), 7,36 (м, 2H), 7,96 (д, 1H), 7,92 (д, 2H), 4,38 (ушир.с, 1H), 3,85 (ушир.с, 1H), 3,40-2,80 (огибающая, 8H).
ПРИМЕР 32
4-{4-[(4'-Хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(3,5-диметилизоксазол-4-ил)сульфонил]бензамид
Соединение по данному примеру получают, заменив в примере 1I соединение по примеру 1Н соединением по примеру 4D, а соединение по примеру 1Е 3,5-диметилизоксазол-4-сульфонамидом, за исключением того, что очистку в данном случае проводят так, как описано в примере 11В.
1Н ЯМР (500 МГц, ДМСО-d6) δ 12,33 (ушир.с, 1H), 7,80 (д, 2H), 7,74 (м, 1H), 7,53 (м, 4H), 7,40 (м, 2H), 7,34 (м, 1H), 6,94 (д, 2H), 4,27 (м, 2H), 3,84 (м, 2H), 3,55 (м, 2H), 3,25 (м, 2H), 2,96 (м, 2H), 2,68 (c, 3H), 2,38 (c, 3H).
ПРИМЕР 33
4-(4-{[2-(4-Хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-2-(1H-индол-5-илокси)-N-({4-нитро-5-[(3-пирролидин-1-илпропил)амино]тиен-2-ил}сульфонил)бензамид
ПРИМЕР 33А
Этил 2-(1Н-индол-5-илокси)-4-фторбензоат
Этил 2,4-дифторбензоат (12,75 г), К3РО4 (14,54 г) и 5-гидроксииндол (9,12 г) перемешивают при температуре 110°С в диглиме (125 мл) в течение 24 час. Реакционную смесь охлаждают и выливают в эфир. Раствор три раза промывают 1М раствором NaOH, насыщенным раствором соли и сушат. Затем раствор концентрируют, сырой продукт выливают в гексан, перемешивают и отфильтровывают, получая целевой продукт.
ПРИМЕР 33В
Метил 4,4-диметил-2-(трифторметилсульфонилокси)циклогекс-1-енкарбоксилат
К суспензии промытого гексаном NaH (17 г) в дихлорметане (700 мл) по каплям добавляют 5,5-диметил-2-метоксикарбонилциклогексанон (38,5 г) при температуре 0°С. Перемешивают еще в течение 30 мин, а затем смесь охлаждают до температуры -78°С и добавляют ангидрид трифторметансульфоновой кислоты (40 мл). Реакционной смеси дают нагреться до комнатной температуры, а затем перемешивают еще в течение 24 час. Органический слой промывают насыщенным раствором соли, сушат и концентрируют, получая целевой продукт.
ПРИМЕР 33С
Метил 2-(4-хлорфенил)-4,4-диметилциклогекс-1-енкарбоксилат
Соединение по примеру 33В (62,15 г), 4-хлорфенилбороновую кислоту (32,24 г), CsF (64 г) и тетракис(трифенилфосфин)палладий(0) (2 г) в смеси диметоксиметан/метанол (600 мл) нагревают до температуры 70°С в течение 24 час. Смесь концентрируют. Добавляют эфир (4 х 200 мл) и смесь отфильтровывают. Эфирные растворы объединяют и конденсируют, получая целевой продукт.
ПРИМЕР 33D
(2-(4-Хлорфенил)-4,4-диметилциклогекс-1-енил)метанол
К смеси LiBH4 (13 г), соединения по примеру 33С (53,8 г) и эфира (400 мл) медленно с помощью шприца добавляют метанол (25 мл). Полученную смесь перемешивают при комнатной температуре в течение 24 час. Реакцию прерывают, добавив 1 н. раствор HCl при охлаждении льдом. Разбавляют смесь водой и экстрагируют эфиром (3×100 мл). Экстракты объединяют, сушат и концентрируют. Сырой продукт хроматографируют на силикагеле, элюируя смесью 0-30% этилацетат/гексаны.
ПРИМЕР 33Е
Трет-бутил 4-((2-(4-хлорфенил)-4,4-диметилциклогекс-1-енил)метил)пиперазин-1-карбоксилат
К смеси соединения по примеру 33D (10,0 г) и TEA (12,2 мл) в CH2Cl2 (300 мл) при температуре 0°С с помощью шприца добавляют мезилхлорид (3,11 мл) и полученную смесь перемешивают в течение одной минуты. Добавляют N-трет-бутоксикарбонилпиперазин (8,17 г) и реакционную смесь перемешивают при комнатной температуре в течение 24 час. Образовавшуюся суспензию промывают насыщенным раствором соли, сушат и концентрируют. Сырой продукт хроматографируют на силикагеле, элюируя смесью 10-20% этилацетат/гексаны.
ПРИМЕР 33F
1-((2-(4-Хлорфенил)-4,4-диметилциклогекс-1-енил)метил)пиперазин
Соединение по примеру 33Е (2,0 г) и триэтилсилан (0,3 мл) перемешивают в течение одного часа в 40 мл трифторуксусной кислоты. Раствор концентрируют, переносят в раствор Na2CO3 и полученную смесь дважды экстрагируют CH2Cl2. Экстракты объединяют, промывают насыщенным раствором соли, сушат и концентрируют.
ПРИМЕР 33G
Этил 2-(1Н-индол-5-илокси)-4-(4-((2-(4-хлорфенил)-4,4-диметилциклогекс-1-енил)метил)пиперазин-1-ил)бензоат
Соединение по примеру 33А (225 мг), соединение по примеру 33F (240 мг) и НК2РО4 (131 мг) перемешивают в диметилсульфоксиде (4 мл) при температуре 135°С в течение 24 час. Реакционную смесь разбавляют этилацетатом, три раза промывают водой, промывают насыщенным раствором соли, сушат и концентрируют. Сырой продукт хроматографируют на силикагеле, элюируя смесью 30% этилацетат/гексаны.
Пример 33H
2-(1Н-Индол-5-илокси)-4-(4-((2-(4-хлорфенил)-4,4-диметилциклогекс-1-енил)метил)пиперазин-1-ил)бензойная кислота
Соединение по данному примеру получают, заменив соединение по примеру 1G в примере 1H на соединение по примеру 33G.
ПРИМЕР 33I
4-Нитро-5-(3-пирролидин-1-ил)пропиламино)тиофен-2-сульфонамид
Соединение по данному примеру получают, заменив соединение по примеру 1D в примере 1Е на 1-(3-аминопропил)пирролидин.
ПРИМЕР 33J
4-(4-{[2-(4-Хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-2-(1H-индол-5-илокси)-N-({4-нитро-5-[(3-пирролидин-1-илпропил)амино]тиен-2-ил}сульфонил)бензамид
Соединение по данному примеру получают, заменив в примере 1I соединение по примеру 1Е на соединение по примеру 33I, а соединение по примеру 1Н на соединение по примеру 33H.
1Н ЯМР (400 МГц, ДМСО-d6) δ 11,12 (c, 1Н),9,50 (ушир.с, 1H), 9,28 (т, 1H), 7,80 (c, 1H), 7,58 (д, 1H), 7,40-7,35 (м, 4H), 7,15 (д, 1H), 7,08 (д, 2H), 6,85 (дд, 1H), 6,71 (дд, 1H), 6,37 (т, 1H), 6,24 (д, 1H), 3,52 (м, 4H), 3,35-3,23 (м, 4H), 3,17 (м, 4H), 2,97 (м, 4H), 2,18 (т, 2H), 2,00 (м, 8H), 1,84 (м, 2H), 1,44 (т, 2H), 0,93 (c, 6H).
ПРИМЕР 34
4-(4-{[2-(4-Хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-[(5-{[3-(диметиламино)пропил]амино}-4-нитротиен-2-ил)сульфонил]-2-(1H-индол-5-илокси)бензамид
ПРИМЕР 34А
5-(3-(Диметиламино)пропиламино)-4-нитротиофен-2-сульфонамид
Соединение по данному примеру получают, заменив соединение по примеру 1D в примере 1E на 3-(диметиламино)-1-пропиламин.
ПРИМЕР 34B
4-(4-{[2-(4-Хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-[(5-{[3-(диметиламино)пропил]амино}-4-нитротиен-2-ил)сульфонил]-2-(1H-индол-5-илокси)бензамид
Соединение по данному примеру получают, заменив в примере 1I соединение по примеру 1Е на соединение по примеру 34А, а соединение по примеру 1Н на соединение по примеру 33H.
1Н ЯМР (400 МГц, ДМСО-d6) δ 10,95 (c, 1H), 9,15 (ушир.с, 1H), 7,58 (д, 1H), 7,43 (c, 1H), 7,35-7,27 (м, 4H), 7,03 (д, 2H), 7,01 (дд, 1H), 6,74 (дд, 1H), 6,53 (дд, 1H), 6,31 (т, 1H), 6,15 (д, 1H), 2,94 (м, 6H), 2,72 (c, 2H), 2,63 (м, 6H), 2,20-2,12 (м, 8H), 1,94 (м, 4H), 1,37 (т, 2H), 0,91 (c, 6H).
ПРИМЕР 35
4-(4-{[2-(4-Хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-2-(1H-индол-5-илокси)-N-({5-[(3-морфолин-4-илпропил)амино]-4-нитротиен-2-ил}сульфонил)бензамид
ПРИМЕР 35А
5-(3-Морфолинопропиламино)-4-нитротиофен-2-сульфонамид
Соединение по данному примеру получают, заменив соединение по примеру 1D в примере 1E на 3-(4-морфолино)-1-пропиламин.
ПРИМЕР 35В
4-(4-{[2-(4-Хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-2-(1H-индол-5-илокси)-N-({5-[(3-морфолин-4-илпропил)амино]-4-нитротиен-2-ил}сульфонил)бензамид
Соединение по данному примеру получают, заменив в примере 1I соединение по примеру 1Е на соединение по примеру 35А, а соединение по примеру 1Н на соединение по примеру 33H.
1Н ЯМР (400 МГц, ДМСО-d6) δ 11,04 (c, 1H), 9,45 (ушир.с, 1H), 7,61 (c, 1H), 7,56 (д, 1H), 7,35-7,30 (м, 4H), 7,09 (дд, 1H), 7,04 (д, 2H), 6,80 (дд, 1H), 6,61 (дд, 1H), 6,34 (т, 1H), 6,16 (д, 1H), 3,62 (т, 4H), 3,30 (м, 2H), 3,02 (т, 4H), 2,78 (ушир.с, 2H), 2,54 (м, 6H), 2,25 (м, 4H), 2,14 (т, 2H), 1,95 (c, 2H), 1,83 (м, 2H), 1,38 (т, 2H), 0,91 (c, 6H).
ПРИМЕР 36
N-{[5-({(1R)-3-(Диметиламино)-1-[(фенилтио)метил]пропил}амино)-4-нитротиен-2-ил]сульфонил}-4-{4-[2-(трифторметил)бензилиден]пиперидин-1-ил}бензамид
ПРИМЕР 36А
Этил 4-(4-(2-(трифторметил)бензилиден)пиперидин-1-ил)бензоат
Суспензию 2-(трифторметил)бензил трифенилфосфонийбромида (получают по методике, приведенной в J. Chem. Soc., Perkin Trans. 1 1995, 18, 2293-2308) (0,737 г) в ТГФ (10 мл) обрабатывают н-бутиллитием (724 мкл 1,6М раствора в гексане) при температуре 0°С, добавляют этил 4-(4-оксо-1-пиперидинил)бензоат (получают по методике, приведенной в Synthesis 1981, 606-608, 0,32 г) и оставляют на ночь постепенно нагреваться до комнатной температуры. Реакционную смесь перераспределяют между этилацетатом и насыщенным водным раствором NH4Cl и водный слой экстрагируют этилацетатом (2×). Органические слои объединяют, сушат (над MgSO4), фильтруют и концентрируют. Полученный остаток очищают хроматографией на силикагеле, элюируя 10% этилацетатом в гексане, и получают требуемый продукт.
ПРИМЕР 36В
4-(4-(2-(Трифторметил)бензилиден)пиперидин-1-ил)бензойная кислота
Соединение по данному примеру получают, заменив соединение по примеру 1G в примере 1H на соединение по примеру 36А.
ПРИМЕР 36С
N-{[5-({(1R)-3-(Диметиламино)-1-[(фенилтио)метил]пропил}амино)-4-нитротиен-2-ил]сульфонил}-4-{4-[2-(трифторметил)бензилиден]пиперидин-1-ил}бензамид
Соединение по данному примеру получают, заменив в примере 1I соединение по примеру 1Н на соединение по примеру 36В.
1Н ЯМР (400 МГц, ДМСО-d6) δ 9,40 (ушир.с, 1H), 8,91 (д, 1H), 7,79 (д, 2H), 7,72 (д, 1H), 7,64 (дд, 1H), 7,46 (м, 2H), 7,35 (м, 3H), 7,26 (м, 2H), 7,17 (т, 1H), 6,88 (д, 2H), 6,49 (c, 1H), 3,60 (м, 1H), 3,25-3,50 (м, 5H), 2,99 (м, 1H), 2,91 (м, 1H), 2,74 (c, 6H), 2,64 (c, 6H), 2,44 (м, 2H), 2,27 (м, 2H), 2,11 (м, 2H).
ПРИМЕР 37
4-{4-[(4'-Хлор-1,1'-бифенил-2-ил)метилен]пиперидин-1-ил}-N-[(1,1-диоксидотетрагидротиен-3-ил)сульфонил]бензамид
ПРИМЕР 37А
(4'-Хлорбифенил-2-ил)метанол
Смесь 2-йодбензилового спирта (11,0 г), 4-хлорфенилбензолбороновой кислоты (8,5 г) и [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладия(II) (800 мг) в Na2CO3 (2М раствор, 94 мл) и диоксане (300 мл) нагревают до температуры 80°С в течение 24 час. Смесь охлаждают, слои разделяют и органический слой концентрируют. Полученный остаток очищают хроматографией на силикагеле, элюируя 20% этилацетатом в гексане, и получают требуемый продукт.
ПРИМЕР 37В
2-(Бромметил)-4'-хлорбифенил
К смеси соединения по примеру 37А (7,9 г) и LiBr (3,45 г) в ДМФА (100 мл) при температуре 0°С добавляют PBr3 (3,77 мл) и реакционную смесь перемешивают в течение 1 час. Реакционную смесь выливают в воду (400 мл) и экстрагируют эфиром (3×200 мл). Эфирные вытяжки объединяют, промывают 3 раза водой, насыщенным раствором соли, сушат над Na2SO4 и концентрируют, получая указанное в названии соединение.
ПРИМЕР 37С
[(4'-Хлор-1,1'-бифенил-2-ил)метил](трифенил)фосфонийбромид
Смесь соединения по примеру 37В (8,05 г) и трифенилфосфина (7,5 г) в ксилоле (100 мл) нагревают до температуры 110°С в течение одного часа. Реакционную смесь охлаждают и фильтруют, а твердое вещество промывают толуолом и сушат в вакууме, получая указанное в названии соединение.
ПРИМЕР 37D
Этил 4-(1,4-диокса-8-азаспиро[4.5]декан-8-ил)бензоат
Этил 4-фторбензоат (36,16 г, 215 ммоль), 1,4-диокса-8-азаспиро[4.5]декан (35,40 г, 247 ммоль) и карбонат калия (29,72 г, 215 ммоль) добавляют к N,N-диметилацетамиду (500 мл) и нагревают до температуры 100°С в течение 16 час. Раствор охлаждают, фильтруют, добавляют к 2М раствору HCl и экстрагируют 50% раствором этилацетата (в гексанах). Органические слои промывают водой, насыщенным раствором соли и сушат над безводным сульфатом натрия. Раствор концентрируют и очищают флэш-хроматографией на силикагеле, элюируя в градиенте от 20% этилацетата (в гексанах) до 30% этилацетата (в гексанах).
ПРИМЕР 37Е
Этил 4-(4-оксопиперидин-1-ил)бензоат
Соединение по примеру 37D (16,23 г, 55,71 ммоль) растворяют в толуоле (85 мл) и добавляют 1М раствор HCl (85 мл). Раствор нагревают до температуры 95°С в течение трех часов и охлаждают. Добавляют 50%-й этилацетат (раствор в гексанах) и фазы разделяют. Органическую фазу промывают водой, насыщенным раствором соли и сушат над безводным сульфатом натрия. Растворитель удаляют и полученное вещество используют без дальнейшей очистки.
ПРИМЕР 37F
Этил 4-(4-((4'-хлорбифенил-2-ил)метилен)пиперидин-1-ил)бензоат
Гидрид натрия (60% в минеральном масле, 1,617 г, 40,4 ммоль) добавляют к диметилсульфоксиду (265 мл) и нагревают до температуры 80°С в течение 30 мин. Продолжая нагревание до температуры 80°С, добавляют соединение по примеру 37С, а затем соединение по примеру 37Е. Нагревание до температуры 80°С продолжают еще в течение 45 мин. Раствор охлаждают, выливают в воду и три раза экстрагируют диэтиловым эфиром. Эфирные экстракты объединяют и промывают водой, насыщенным раствором соли и сушат над безводным сульфатом натрия. Раствор концентрируют и очищают флэш-хроматографией на силикагеле, элюируя в градиенте от 10% этилацетата (в гексанах) до 20% этилацетата (в гексанах).
ПРИМЕР 37G
4-(4-((4'-Хлорбифенил-2-ил)метилен)пиперидин-1-ил)бензойная кислота
Соединение по данному примеру получают, заменив соединение по примеру 4C в примере 4D на соединение по примеру 37F.
ПРИМЕР 37H
4-{4-[(4'-Хлор-1,1'-бифенил-2-ил)метилен]пиперидин-1-ил}-N-[(1,1-диоксидотетрагидротиен-3-ил)сульфонил]бензамид
Соединение по данному примеру получают, заменив в примере 1I соединение по примеру 1Е на 1,1-диоксид тетрагидротиофен-3-сульфонамида, а соединение по примеру 1Н на соединение по примеру 37G.
1Н ЯМР (400 МГц, ДМСО-d6) δ 7,79 (д, 2H), 7,48 (дт, 2H), 7,42-7,33 (м, 4H), 7,31-7,23 (м, 2H), 6,85 (д, 2H), 6,13 (c, 1H), 4,33 (м, 1H), 3,35-3,22 (м, 4H), 3,20-3,06 (м, 4H), 2,30 (м, 6H).
ПРИМЕР 38
4-{4-[(4'-Хлор-1,1'-бифенил-2-ил)метилен]пиперидин-1-ил}-N-[(5-хлор-3-метил-1-бензотиен-2-ил)сульфонил]бензамид
Соединение по данному примеру получают, заменив в примере 1I соединение по примеру 1Е на 5-хлор-3-метилбензо[b]тиофен-2-сульфонамид, а соединение по примеру 1Н на соединение по примеру 37G.
1Н ЯМР (400 МГц, ДМСО-d6) δ 8,09 (д, 1H), 7,90 (c, 1H), 7,77 (д, 2H), 7,58-7,52 (м, 2H), 7,47 (дт, 2H), 7,41-7,33 (м, 4H), 7,28 (м, 1H), 6,91 (д, 2H), 6,13 (c, 1H), 3,42 (м, 2H), 3,26 (м, 2H), 2,62 (c, 3H), 2,28 (м, 4H).
ПРИМЕР 39
4-{4-[(4'-Хлор-1,1'-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(5-хлор-3-метил-1-бензотиен-2-ил)сульфонил]-2-феноксибензамид
ПРИМЕР 39А
Этил 4-фтор-2-феноксибензоат
Соединение по данному примеру получают, заменив 5-гидроксииндол в примере 33А на фенол.
ПРИМЕР 39В
4'-Хлорбифенил-2-карбальдегид
2-Бромбензальдегид (25,05 мл, 40,0 г, 216 ммоль) добавляют к толуолу, дегазируют и продувают азотом. Добавляют 4-хлорфенилбороновую кислоту (43,9 г, 281 ммоль), дегазированный 2М раствор карбоната натрия (757 мл, 1513 ммоль) и тетракис(трифенилфосфин)палладий(0) (5,00 г, 4,32 ммоль). Смесь нагревают с обратным холодильником в течение 2,5 час, охлаждают и фазы разделяют. Органический слой экстрагируют 2М раствором карбоната натрия, а водный слой вновь экстрагируют этиловым эфиром. Органические вытяжки объединяют, сушат солью, а затем безводным сульфатом натрия. Раствор концентрируют и очищают колоночной флэш-хроматографией на силикагеле, проводя элюирование в градиенте от 5% этилацетата (в гексанах) до 10% этилацетата (в гексанах).
ПРИМЕР 39С
Трет-бутил 4-((4'-хлорбифенил-2-ил)метил)пиперазин-1-карбоксилат
Соединение по данному примеру получают, заменив в примере 7В соединение по примеру 7А на соединение по примеру 39В, а метилизопропиламин на 1-(трет-бутоксикарбонил)пиперазин.
ПРИМЕР 39D
1-((4'-Хлорбифенил-2-ил)метил)пиперазин
Соединение по данному примеру получают, заменив соединение по примеру 33Е в примере 33F на соединение по примеру 39С.
ПРИМЕР 39Е
Этил 4-(4-((4'-хлорбифенил-2-ил)метил)пиперазин-1-ил)-2-феноксибензоат
Соединение по данному примеру получают, заменив в примере 33G соединение по примеру 33A на соединение по примеру 39A, а соединение по примеру 33F на соединение по примеру 39D.
ПРИМЕР 39F
4-(4-((4'-Хлорбифенил-2-ил)метил)пиперазин-1-ил)-2-феноксибензойная кислота
Соединение по данному примеру получают, заменив соединение по примеру 1G в примере 1H на соединение по примеру 39E.
ПРИМЕР 39G
4-{4-[(4'-Хлор-1,1'-бифенил-2-ил)метилен]пиперидин-1-ил}-N-[(5-хлор-3-метил-1-бензотиен-2-ил)сульфонил]бензамид
Соединение по данному примеру получают, заменив в примере 1I соединение по примеру 1Е на 5-хлор-3-метилбензо[b]тиофен-2-сульфонамид, а соединение по примеру 1Н на соединение по примеру 39F.
1Н ЯМР (400 МГц, ДМСО-d6) δ 8,06 (д, 1H), 7,98 (д, 1H), 7,60-7,34 (м, 9H), 7,27-7,18 (м, 3H), 6,94 (т, 1H), 6,83 (д, 2H), 6,75 (дд, 1H), 6,36 (д, 1H), 3,48 (м, 2H), 3,16 (ушир.с, 4H), 2,54 (c, 3H), 2,43 (ушир.с, 4H).
ПРИМЕР 40
2-(3-Хлорфенокси)-4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-Ν-[(5,7-диметил[1,2,4]триазоло[1,5-a]пиримидин-2-ил)сульфонил]бензамид
ПРИМЕР 40А
Этил 2-(3-хлорфенокси)-4-фторбензоат
Этил 2,4-дифторбензоат (6,0 г), К3РО4 (7,5 г) и 3-хлорфенол (4,1 г) перемешивают при температуре 110°С в диглиме (25 мл) в течение 24 час. Смесь охлаждают и выливают в эфир. Раствор три раза промывают 1М раствором NaOH, затем насыщенным раствором соли и сушат. Раствор концентрируют. Концентрат хроматографируют на силикагеле, элюируя смесью 10% этилацетат/гексан.
ПРИМЕР 40В
Метил 4,4-диметил-2-(трифторметилсульфонилокси)циклогекс-1-енкарбоксилат
К суспензии промытого гексаном NaH (17 г) в дихлорметане (700 мл) при 0°С по каплям добавляют 5,5-диметил-2-метоксикарбонилциклогексанон (38,5 г). Смесь перемешивают в течение 30 мин, затем охлаждают до температуры -78°С и добавляют трифторуксусный ангидрид (40 мл). Нагревают смесь до комнатной температуры и перемешивают в течение 24 час. Экстракт промывают насыщенным раствором соли, сушат и концентрируют.
ПРИМЕР 40С
Метил 2-(4-хлорфенил)-4,4-диметилциклогекс-1-енкарбоксилат
Соединение по примеру 40В (62,15 г), 4-хлорфенилбороновую кислоту (32,24 г), CsF (64 г) и тетракис(трифенилфосфин)палладий(0) (2 г) в смеси 2:1 диметоксиэтан/метанол (600 мл) нагревают до температуры 70°С в течение 24 час. Смесь концентрируют. Добавляют эфир, смесь отфильтровывают и концентрируют.
ПРИМЕР 40D
(2-(4-Хлорфенил)-4,4-диметилциклогекс-1-енил)метанол
К смеси LiBH4 (13 г), соединения по примеру 40С (53,8 г) и эфира (400 мл) медленно с помощью шприца добавляют метанол (25 мл). Смесь перемешивают при комнатной температуре в течение 24 час. Прерывают реакцию, добавив 1 н. раствор HCl при охлаждении льдом. Смесь разбавляют водой и экстрагируют эфиром (3×100 мл). Экстракты сушат и концентрируют. Концентрат хроматографируют на силикагеле, элюируя смесью 0-30% этилацетат/гексан.
ПРИМЕР 40Е
Трет-бутил 4-((2-(4-хлорфенил)-4,4-диметилциклогекс-1-енил)метил)пиперазин-1-карбоксилат
Мезилхлорид (7,5 мл) с помощью шприца добавляют к соединению по примеру 40D (29,3 г) и триэтиламину (30 мл) в CH2Cl2 (500 мл) при температуре 0°С, а затем смесь перемешивают в течение 1 мин. Добавляют N-трет-бутоксикарбонилпиперазин (25 г) и полученную смесь перемешивают при комнатной температуре в течение 24 час. Суспензию промывают насыщенным раствором соли, сушат и концентрируют. Концентрат хроматографируют на силикагеле, элюируя смесью 10-20% этилацетат/гексаны.
ПРИМЕР 40F
1-((2-(4-Хлорфенил)-4,4-диметилциклогекс-1-енил)метил)пиперазин
Соединение по примеру 40Е (3,0 г) и триэтилсилан (1 мл) перемешивают в дихлорметане (30 мл) и трифторуксусной кислоте (30 мл) в течение 2 час. Смесь концентрируют, растворяют в эфире и вновь концентрируют.
ПРИМЕР 40G
Этил 2-(3-Хлорфенокси)-4-(4-((2-(4-хлорфенил)-4,4-диметилциклогекс-1-енил)метил)пиперазин-1-ил)бензоат
Соединение по примеру 40А (1,2 г), соединение по примеру 40F (1,4 г) и НК2РО4 (0,9 г) перемешивают в ДМСО (2 мл) при температуре 130°С в течение 24 час. Разбавляют смесь этилацетатом, трижды промывают водой, промывают насыщенным раствором соли, сушат и концентрируют. Концентрат хроматографируют на силикагеле, элюируя смесью 20% этилацетат/гексаны.
ПРИМЕР 40Н
2-(3-Хлорфенокси)-4-(4-((2-(4-хлорфенил)-4,4-диметилциклогекс-1-енил)метил)пиперазин-1-ил)бензойная кислота
Соединение по примеру 40G (400 мг) перемешивают в 12 мл смеси 5:1 диоксан/2М LiOH при температуре 90°С в течение 7 час. Раствор охлаждают и концентрируют. Добавляют воду, доводят рН до значения 4 1М раствором HCl и экстрагируют этилацетатом. Экстракт промывают насыщенным раствором соли, сушат (над Na2SO4) и концентрируют.
ПРИМЕР 40I
5,7-Диметил-[1,2,4]триазоло[1,5-a]пиримидин-2-сульфонамид
5,7-Диметил-[1,2,4]триазоло[1,5-a]пиримидин-2-сульфонилхлорид (2,9 г, получают по способу, приведенному в EP 142152 (А2, А3)) растворяют в ТГФ (40 мл), охлаждают до 0°С, концентрируют и добавляют NH4OH (4,0 мл). Реакционную смесь при охлаждении перемешивают в течение 10 мин, а затем 30 мин при комнатной температуре. Жидкость над осадком декантируют, а твердые вещества перераспределяют между водой и смесью CHCl3/изопропиловый спирт (3/1). Водный слой дополнительно дважды экстрагируют смесью CHCl3/изопропиловый спирт (3/1). Органические экстракты объединяют, сушат (над Na2SO4) и концентрируют.
ПРИМЕР 40J
2-(3-Хлорфенокси)-4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-Ν-[(5,7-диметил[1,2,4]триазоло[1,5-a]пиримидин-2-ил)сульфонил]бензамид
Соединение по примеру 40H (170 мг), соединение по примеру 40I (68 мг), гидрохлорид 1-этил-3-(3-диметиламино)пропил)карбодиимида (113 мг) и 4-диметиламинопиридин (72 мг) перемешивают в CH2Cl2 (3 мл) в течение 24 час. Концентрируют, вновь растворяют в смеси ДМСО/метанол и проводят очистку методом препаративной ВЭЖХ, используя колонку С18, 250×50 мм, 10 мкм, и проводя элюирование в градиенте 20-100% CH3CN против 0,1%-го раствора TFA в воде. Полученную соль нейтрализуют, перераспределяя между CH2Cl2 и насыщенным раствором NaHCO3.
1Н ЯМР (500 МГц, ДМСО-d6) δ 7,82 (д, 1H), 7,38 (д, 2H), 7,20 (c, 1H), 7,13 (дд, 1H), 7,08 (д, 2H), 6,87 (д, 1H), 6,76 (дд, 1H), 6,43 (c, 1H), 6,42 (д, 1H), 6,36 (c, 1H), 3,13(ушир.с, 4H), 2,80 (ушир.с, 2H), 2,68 (c, 3H), 2,59 (c, 3H), 2,25 (ушир.с, 4H), 2,19 (ушир.м, 2H), 1,98 (c, 2H), 1,40 (т, 2H), 0,93 (c, 6H).
ПРИМЕР 41
4-(4-{[2-(4-Хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-[(5,7-диметил[1,2,4]триазоло[1,5-a]пиримидин-2-ил)сульфонил]-2-[(6-фтор-1H-индол-5-ил)окси]бензамид
ПРИМЕР 41А
Этил 4-фтор-2-(6-фтор-1Н-индол-5-илокси)бензоат
Соединение по данному примеру получают, заменив 3-хлорфенол в примере 40А на 6-фтор-5-гидроксииндол (получают по способу, приведенному в WO 02/12227).
ПРИМЕР 41В
Этил 4-(4-((2-(4-хлорфенил)-4,4-диметилциклогекс-1-енил)метил)пиперазин-1-ил)-2-(6-фтор-1Н-индол-5-илокси)бензоат
Соединение по данному примеру получают, заменив в примере 40G соединение по примеру 40А на соединение по примеру 41А.
ПРИМЕР 41С
4-(4-((2-(4-Хлорфенил)-4,4-диметилциклогекс-1-енил)метил)пиперазин-1-ил)-2-(6-фтор-1Н-индол-5-илокси)бензойная кислота
Соединение по данному примеру получают, заменив в примере 40H соединение по примеру 40G на соединение по примеру 41B.
ПРИМЕР 41D
4-(4-{[2-(4-Хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-[(5,7-диметил[1,2,4]триазоло[1,5-a]пиримидин-2-ил)сульфонил]-2-[(6-фтор-1H-индол-5-ил)окси]бензамид
Соединение по данному примеру получают, заменив в примере 40J соединение по примеру 40H на соединение по примеру 41C.
1Н ЯМР (500 МГц, ДМСО-d6) δ 11,07 (c, 1H), 7,78 (д, 1H), 7,36 (д, 2H), 7,30 (м, 1H), 7,24 (д, 1H), 7,20 (c, 1H), 7,08 (д, 3H), 6,59 (дд, 1H), 6,30 (c, 1H), 6,05 (c, 1H), 2,95 (ушир.с, 4H), 2,75 (ушир.с, 2H), 2,68 (c, 3H), 2,59 (c, 3H), 2,22 (ушир.с, 4H), 2,17 (ушир.м, 2H), 1,95 (c, 2H), 1,40 (т, 2H), 0,93 (c, 6H).
ПРИМЕР 42
4-(4-{[2-(4-Хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-2-[(6,7-дифтор-1H-индол-5-ил)окси]-N-[(5,7-диметил[1,2,4]триазоло[1,5-a]пиримидин-2-ил)сульфонил]бензамид
ПРИМЕР 42А
Этил 2-(6,7-дифтор-1Н-индол-5-илокси)-4-фторбензоат
Соединение по данному примеру получают, заменив в примере 40А 3-хлорфенол на 6,7-дифтор-5-гидроксииндол (получают по способу, приведенному в WO 02/12227).
ПРИМЕР 42В
Этил 4-(4-((2-(4-хлорфенил)-4,4-диметилциклогекс-1-енил)метил)пиперазин-1-ил)-2-(6,7-дифтор-1Н-индол-5-илокси)бензоат
Соединение по данному примеру получают, заменив в примере 40G соединение по примеру 40А на соединение по примеру 42А.
ПРИМЕР 42С
4-(4-((2-(4-Хлорфенил)-4,4-диметилциклогекс-1-енил)метил)пиперазин-1-ил)-2-(6,7-дифтор-1Н-индол-5-илокси)бензойная кислота
Соединение по данному примеру получают, заменив в примере 40H соединение по примеру 40G на соединение по примеру 42B.
ПРИМЕР 42D
4-(4-{[2-(4-Хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-2-[(6,7-дифтор-1H-индол-5-ил)окси]-N-[(5,7-диметил[1,2,4]триазоло[1,5-a]пиримидин-2-ил)сульфонил]бензамид
Соединение по данному примеру получают, заменив в примере 40J соединение по примеру 40H на соединение по примеру 42C.
1Н ЯМР (500 МГц, ДМСО-d6) δ 11,58 (c, 1H), 7,80 (д, 1H), 7,33 (д, 2H), 7,31 (c, 1H), 7,17 (c, 1H), 7,03 (д, 2H), 6,70 (д, 1H), 6,65 (дд, 1H), 6,35 (м, 1H), 6,19(c, 1H), 3,00 (ушир.с, 4H), 2,71 (ушир.с, 2H), 2,68 (c, 3H), 2,59 (c, 3H), 2,20 (ушир.с, 4H), 2,17 (ушир.м, 2H), 1,95 (c, 2H), 1,39 (т, 2H), 0,93 (c, 6H).
ПРИМЕР 43
Трет-бутил (2S)-2-{[(5-{[4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-2-(1H-пирроло[2,3-b]пиридин-5-илокси)бензоил]сульфамоил}-4-метил-1,3-тиазол-2-ил)окси]метил}морфолин-4-карбоксилат
ПРИМЕР 43А
5-Бром-1-(триизопропилсилил)-1Н-пирроло[2,3-b]пиридин
К смеси 5-бром-1Н-пирроло[2,3-b]пиридина (15,4 г) в тетрагидрофуране (250 мл) добавляют 1М раствор гексаметилдисилазида лития в тетрагидрофуране (86 мл), а еще через 10 мин добавляют TIPS-Cl (триизопропилхлорсилан) (18,2 мл). Полученную смесь перемешивают при комнатной температуре в течение 24 час. Разбавляют реакционную смесь эфиром и полученный раствор дважды промывают водой. Экстракты сушат (Na2SO4), фильтруют и концентрируют. Сырой продукт хроматографируют на силикагеле, элюируя смесью 10% этилацетат/гексаны.
ПРИМЕР 43В
1-(Триизопропилсилил)-1Н-пирроло[2,3-b]пиридин-5-ол
К смеси соединения по примеру 43А (24,3 г) в тетрагидрофуране (500 мл) при температуре -78°С добавляют 2,5М раствор н-бутиллития (30,3 мл). Через 2 мин добавляют триметилборат (11,5 мл) и дают смеси в течение 1 час нагреться до комнатной температуры. Выливают реакционную смесь в воду, экстрагируют три раза этилацетатом, органические вытяжки объединяют, промывают насыщенным раствором соли и концентрируют. Сырой продукт растворяют в тетрагидрофуране (200 мл) при 0°С, добавляют 1М раствор NaOH (69 мл), а затем 30%-й водный раствор Н2О2 (8,43 мл) и полученный раствор перемешивают в течение 1 час. Добавляют Na2S2O3 (10 г), доводят рН до значения 4-5 концентрированной HCl и твердым NaH2PO4. Раствор дважды экстрагируют этилацетатом, экстракты объединяют, промывают насыщенным раствором соли, сушат (над Na2SO4), фильтруют и концентрируют. Сырой продукт хроматографируют на силикагеле, элюируя смесью 5-25% этилацетат/гексаны.
ПРИМЕР 43С
Метил 2-(1Н-пирроло[2,3-b]пиридин-5-илокси)-4-фторбензоат
Смесь соединения по примеру 43В (8,5 г), метил 2,4-дифторбензоата (7,05 г) и К3РО4 (9,32 г) в диглиме (40 мл) перемешивают при температуре 115°С в течение 24 час. Реакционную смесь охлаждают, разбавляют эфиром (600 мл) и промывают два раза водой, насыщенным раствором соли и концентрируют. Сырой продукт хроматографируют на силикагеле, элюируя смесью 2-50% этилацетат/гексаны.
ПРИМЕР 43D
Метил 2-(1Н-пирроло[2,3-b]пиридин-5-илокси)-4-(4-((2-(4-хлорфенил)-4,4-диметилциклогекс-1-енил)метил)пиперазин-1-ил)бензоат
Смесь соединения по примеру 43C (1,55 г), соединения по примеру 43F (2,42 г) и НК2РО4 (1,42 г) в диметилсульфоксиде (20 мл) при температуре 135°С перемешивают в течение 24 час. Реакционную смесь охлаждают, разбавляют эфиром (400 мл) и три раза промывают 1М раствором NaOH, насыщенным раствором соли и концентрируют. Сырой продукт хроматографируют на силикагеле, элюируя смесью 10-50% этилацетат/гексаны.
ПРИМЕР 43E
2-(1Н-Пирроло[2,3-b]пиридин-5-илокси)-4-(4-((2-(4-хлорфенил)-4,4-диметилциклогекс-1-енил)метил)пиперазин-1-ил)бензойная кислота
Соединение по примеру 43D (200 мг) в диоксане (10 мл) и 1М водный раствор NaOH (6 мл) при температуре 50°С перемешивают в течение 24 час. Реакционную смесь охлаждают, добавляют раствор NaH2PO4 и три раза экстрагируют этилацетатом. Экстракты объединяют, промывают насыщенным раствором соли и концентрируют, получая чистый продукт.
ПРИМЕР 43F
2-Хлор-4-метилтиазол-5-сульфонамид
Раствор 2-хлор-4-метилтиазол-5-сульфонилхлорида (1,0 г) в изопропиловом спирте (10 мл) охлаждают на бане со льдом. Затем медленно добавляют гидроксид аммония (2,89 мл). Полученный раствор оставляют перемешиваться на ночь при комнатной температуре. Раствор концентрируют, остаток смешивают с водой (10 мл) и экстрагируют этилацетатом (2×20 мл). Сырой продукт очищают на колонке с силикагелем, элюируя смесью 60% этилацетат-гексан.
ПРИМЕР 43G
(S)-Трет-бутил 2-((4-метил-5-сульфамоилтиазол-2-илокси)метил)морфолин-4-карбоксилат
К раствору (S)-трет-бутил 2-(гидроксиметил)морфолин-4-карбоксилата (123 мг) в безводном тетрагидрофуране (5 мл) добавляют гидрид натрия (60%-я дисперсия в минеральном масле, 94 мг). Перемешивают смесь при комнатной температуре в течение 30 мин, а затем добавляют соединение по примеру 43F (100 мг). Смесь оставляют на ночь перемешиваться при комнатной температуре. Прерывают реакцию, добавив воду (15 мл) и экстрагируют этилацетатом. Сырой продукт очищают на колонке с силикагелем, элюируя смесью 60% этилацетата в гексане, и получают указанное в названии соединение.
ПРИМЕР 43H
Трет-бутил (2S)-2-{[(5-{[4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-2-(1H-пирроло[2,3-b]пиридин-5-илокси)бензоил]сульфамоил}-4-метил-1,3-тиазол-2-ил)окси]метил}морфолин-4-карбоксилат
Соединение по данному примеру получают, заменив в примере 1I соединение по примеру 1H на соединение по примеру 43E, а соединение по примеру 1E на соединение по примеру 43G.
1Н ЯМР (500 МГц, пиридин-d5) δ 13,00 (c, 1H), 8,43 (д, 1H), 8,11 (д, 1H), 7,68 (д, 1H), 7,67 (т, 1H), 7,45 (д, 2H), 7,08 (д, 2H), 6,76 (дд, 1H), 6,54 (д, 1H), 6,50 (дд, 1H), 4,52-4,45 (м, 2H), 3,90-3,70 (м, 4H), 3,47 (дт, 1H), 3,07 (м, 4H), 2,98-2,84 (м, 2H), 2,77 (c, 2H), 2,76 (c, 3H), 2,26 (м, 2H), 2,14 (м, 4H), 1,97 (c, 2H), 1,52 (c, 9H), 1,39 (т, 2H), 0,94 (c, 6H).
ПРИМЕР 44
Трет-бутил (2S)-2-{[(5-{[2-(1H-бензимидазол-4-илокси)-4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)бензоил]сульфамоил}-4-метил-1,3-тиазол-2-ил)окси]метил}морфолин-4-карбоксилат
ПРИМЕР 44А
Метил 4-фтор-2-(3-фтор-2-нитрофенокси)бензоат
К раствору метил 4-фтор-2-гидроксибензоата (3,0 г) в тетрагидрофуране (65 мл) порциями добавляют трет-бутоксид калия (1,979 г). Полученный раствор перемешивают при температуре окружающей среды в течение 30 мин, а затем по каплям добавляют раствор 1,3-дифтор-2-нитробензола (2,338 г) в тетрагидрофуране (15 мл). Через 1 час реакционную смесь нагревают до кипения и кипятят с обратным холодильником в течение 18 час. Реакцию гасят водой (10 мл), разбавляют насыщенным раствором соли (75 мл) и дважды экстрагируют метиленхлоридом (75 мл). Сырой продукт выделяют концентрированием и очищают на силикагеле, проводя ступенчатое градиентное элюирование смесями 10, 20, 50% этилацетата в гексане.
ПРИМЕР 44B
Метил 2-(3-(бис(4-метоксифенил)метиламино)-2-нитрофенокси)-4-фторбензоат
К раствору соединения по примеру 44А (3,82 г) и бис(4-метоксифенил)метанамина (4,51 г) в N-метил-2-пирролидиноне (65 мл) добавляют N-этил-N-изопропилпропан-2-амин (4,30 мл) и полученную смесь нагревают до температуры 100°С в течение 24 час. Сырой продукт, который выделяют концентрированием, очищают на силикагеле, проводя ступенчатое градиентное элюирование смесями 10, 25, 65% этилацетата в гексане.
ПРИМЕР 44C
Метил 2-(2-амино-3-(бис(4-метоксифенил)метиламино)фенокси)-4-фторбензоат
К раствору соединения по примеру 44B (2,76 г) в тетрагидрофуране (125 мл) в стальной бутыли добавляют никелевый катализатор (2,76 г). Смесь перемешивают в течение 1 час под давлением водорода 30 фунтов на квадратный дюйм при температуре окружающей среды. Смесь отфильтровывают через мембрану из нейлона, чтобы удалить катализатор, и после упаривания растворителя получают указанное в названии соединение (2,54 г).
ПРИМЕР 44D
Метил 2-(1-(бис(4-метоксифенил)метил)-1Н-бензо[d]имидазол-4-илокси)-4-фторбензоат
К раствору соединения по примеру 44C (1,25 г) в триэтил ортоформиате (30 мл) добавляют концентрированную хлористоводородную кислоту (0,75 мл). Полученную смесь перемешивают в течение 18 час, прерывают реакцию, медленно добавляя 50%-й насыщенный раствор карбоната натрия (100 мл), и экстрагируют этилацетатом (2×100 мл). Сырой продукт выделяют концентрированием и очищают на силикагеле, проводя ступенчатое градиентное элюирование смесями 25, 50 и 70% этилацетата в гексане.
ПРИМЕР 44E
Метил 2-(1-(бис(4-метоксифенил)метил)-1Н-бензо[d]имидазол-4-илокси)-4-(пиперазин-1-ил)бензоат
Раствор соединения по примеру 44D (500 мг) и пиперазин (420 мг) в диметилсульфоксиде (9 мл) нагревают до температуры 100°С в течение 3 час. Сырой продукт выделяют концентрированием, а затем промывают водой и очищают на силикагеле, проводя ступенчатое градиентное элюирование смесями 5, 10% метанола в метиленхлориде.
ПРИМЕР 44F
2-(4-Хлорфенил)-4,4-диметилциклогекс-1-енкарбальдегид
Указанное соединение получают, заменив соединение по примеру 8C в примере 8D на соединение по примеру 33D.
ПРИМЕР 44G
Метил 2-(1-(бис(4-метоксифенил)метил)-1Н-бензо[d]имидазол-4-илокси)-4-(4-((2-(4-хлорфенил)-4,4-диметилциклогекс-1-енил)метил)пиперазин-1-ил)бензоат
К раствору соединения по примеру 44E (430 мг) и соединения по примеру 44F (259 мг) в дихлорметане (13 мл) порциями добавляют триацетоксиборгидрид натрия (323 мг). Перемешивают в течение 42 час, реакцию прерывают, медленно добавив насыщенный водный раствор бикарбоната натрия (80 мл), и экстрагируют метиленхлоридом (2×70 мл). Сырой продукт выделяют концентрированием и очищают на силикагеле, проводя ступенчатое градиентное элюирование смесями 0, 2, 10% метанола в метиленхлориде.
ПРИМЕР 44H
2-(1-(Бис(4-метоксифенил)метил)-1Н-бензо[d]имидазол-4-илокси)-4-(4-((2-(4-хлорфенил)-4,4-диметилциклогекс-1-енил)метил)пиперазин-1-ил)бензойная кислота
К раствору соединения по примеру 44G (545 мг) в смеси метанола (7,50 мл) и тетрагидрофурана (7,50 мл) добавляют раствор гидроксида натрия (269 мг) в воде (3,0 мл). Реакционную смесь нагревают до температуры 50°С в течение 18 час и концентрируют. Остаток смешивают с водой (100 мл), доводят рН до величины приблизительно 7 1М водным раствором хлористоводородной кислоты, а затем смесь экстрагируют 10% раствором метанола в метиленхлориде (10×50 мл).
ПРИМЕР 44I
8-[4-[[2-(4-Хлорфенил)-4,4-диметил-1-циклогекс-1-енил]метил]-1-пиперазинил]-11Н-бенз[b]имидазо[1,5,4-ef][1,5]бензоксазепин-11-он
Раствор соединения по примеру 44G (4,5 г) в безводном дихлорметане (100 мл) охлаждают на бане со льдом и добавляют каталитическое количество N,N-диметилформамида. Затем по каплям добавляют раствор оксалилдихлорида (1,231 мл) в безводном метиленхлориде (5 мл). Баню со льдом убирают и реакционную смесь перемешивают в течение 1 час. Реакцию прерывают, добавив лед (около 150 мл) и насыщенный водный раствор бикарбоната натрия (100 мл). Затем смесь дополнительно разбавляют насыщенным водным раствором бикарбоната натрия (200 мл) и метиленхлоридом (200 мл). Сырой продукт выделяют концентрированием органического слоя, остаток очищают на силикагеле, проводя ступенчатое градиентное элюирование смесями 0, 10, 25 и 100% этилацетата в метиленхлориде.
ПРИМЕР 44J
Трет-бутил (2S)-2-{[(5-{[2-(1H-бензимидазол-4-илокси)-4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)бензоил]сульфамоил}-4-метил-1,3-тиазол-2-ил)окси]метил}морфолин-4-карбоксилат
К раствору соединения по примеру 43G (35 мг) в безводном тетрагидрофуране (4 мл) добавляют 2,3,4,6,7,8,9,10-октагидропиримидо[1,2-a]азепин (19,95 мкл). Полученную смесь перемешивают при комнатной температуре в течение 30 мин. Добавляют соединение по примеру 44I (49,2 мг) и раствор оставляют на ночь перемешиваться при комнатной температуре. Раствор концентрируют. Остаток вновь растворяют в смеси диметилсульфоксид-метанол и очищают методом ВЭЖХ (Waters LC4000 Prep system, колонка C 18), используя в качестве подвижной фазы 10 мМ забуференной ацетатом аммония смеси вода-ацетонитрил.
1Н ЯМР (500 МГц, пиридин-d5) δ 8,55 (c, 1H), 8,00 (д, 1H), 7,53 (д, 1H), 7,44 (д, 2H), 7,27 (т, 1H), 7,22 (м, 2H), 7,07 (д, 2H), 6,73 (д, 1H), 6,71 (дд, 1H), 4,52-4,45 (м, 2H), 3,90-3,70 (м, 4H), 3,47 (дт, 1H), 3,04 (м, 4H), 2,98-2,83 (м, 2H), 2,77 (c, 2H), 2,76 (c, 3H), 2,26 (м, 2H), 2,15 (м, 4H), 1,97 (c, 2H), 1,52 (c, 9H), 1,39 (т, 2H), 0,94 (c, 6H).
ПРИМЕР 45
4-(4-{[2-(4-Хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-({2-[(4-фтортетрагидро-2H-пиран-4-ил)метокси]-4-метил-1,3-тиазол-5-ил}сульфонил)-2-(1H-пирроло[2,3-b]пиридин-5-илокси)бензамид
ПРИМЕР 45A
2-((4-Фтортетрагидро-2Н-пиран-4-ил)метокси)-4-метилтиазол-5-сульфонамид
Соединение по данному примеру получают, заменив (S)-трет-бутил 2-(гидроксиметил)морфолин-4-карбоксилат в примере 43G на 4-фтортетрагидро-2Н-пиран-4-ил)метанол.
ПРИМЕР 45B
4-(4-{[2-(4-Хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-({2-[(4-фтортетрагидро-2H-пиран-4-ил)метокси]-4-метил-1,3-тиазол-5-ил}сульфонил)-2-(1H-пирроло[2,3-b]пиридин-5-илокси)бензамид
Соединение по данному примеру получают, заменив в примере 1I соединение по примеру 1H на соединение по примеру 43E, а соединение по примеру 1E на соединение по примеру 45A.
1Н ЯМР (500 МГц, пиридин-d5) δ 13,01 (c, 1H), 8,43 (д, 1H), 8,15 (д, 1H), 7,70 (д, 1H), 7,65 (т, 1H), 7,45 (д, 2H), 7,08 (д, 2H), 6,77 (дд, 1H), 6,55 (д, 1H), 6,50 (дд, 1H), 4,52 (дд, 2H), 3,83-3,79 (м, 2H), 3,72-3,70 (м, 2H), 3,07 (м, 4H), 2,80 (c, 3H), 2,78 (c, 2H), 2,26 (м, 2H), 2,15 (м, 4H), 1,97 (c, 2H), 1,82-1,75 (м, 4H), 1,39 (т, 2H), 0,94 (c, 6H).
ПРИМЕР 46
2-(1H-Бензимидазол-4-илокси)-4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-({2-[(4-фтортетрагидро-2H-пиран-4-ил)метокси]-4-метил-1,3-тиазол-5-ил}сульфонил)бензамид
Соединение по данному примеру получают, заменив в примере 44J соединение по примеру 43G на соединение по примеру 45A.
1Н ЯМР (500 МГц, пиридин-d5) δ 8,56 (c, 1H), 8,02 (д, 1H), 7,53 (д, 1H), 7,44 (д, 2H), 7,27 (т, 1H), 7,21 (м, 2H), 7,08 (д, 2H), 6,74 (д, 1H), 6,71 (дд, 1H), 4,54 (дд, 2H), 3,84-3,79 (м, 2H), 3,73-3,70 (м, 2H), 3,05 (м, 4H), 2,79 (c, 3H), 2,78 (c, 2H), 2,26 (м, 2H), 2,16 (м, 4H), 1,98 (c, 2H), 1,82-1,75 (м, 4H), 1,39 (т, 2H), 0,94 (c, 6H).
ПРИМЕР 47
(S)-Трет-бутил 2-(((5-(N-(2-(1H-индазол-4-илокси)-4-(4-((2-(4-хлорфенил)-4,4-диметилциклогекс-1-енил)метил)пиперазин-1-ил)бензоил)сульфамоил)-4-метилтиазол-2-илокси)метил)морфолин-4-карбоксилат
ПРИМЕР 47A
Трет-бутил 4-гидрокси-1Н-индазол-1-карбоксилат и трет-бутил 4-гидрокси-2Н-индазол-2-карбоксилат
4-Гидроксииндазол (3,94 г) добавляют к тетрагидрофурану (250 мл) и полученную смесь охлаждают до 0°С на бане со льдом. Добавляют гидрид натрия (60%-я дисперсия в минеральном масле, 1,23 г) и смесь перемешивают при 0°С в течение 5 мин. Дают раствору нагреться до комнатной температуры и перемешивают еще в течение 20 мин. Вновь охлаждают раствор до 0°С на бане со льдом и добавляют трет-бутилдиметилхлорсилан (4,65 г). Дают раствору нагреться до комнатной температуры и перемешивают еще в течение 16 час. Упаривают растворитель в вакууме, остаток фильтруют в вакууме через слой силикагеля и промывают этилацетатом. Растворы объединяют и концентрируют. Полученный остаток смешивают с ацетонитрилом (200 мл), ди-трет-бутилдикарбонатом (7,06 г) и 4-(диметиламино)пиридином (0,359 г). Образовавшийся раствор перемешивают при комнатной температуре в течение трех часов и растворитель удаляют в вакууме. К остатку добавляют тетрагидрофуран (200 мл), тетрабутиламмонийфторид (1М раствор в тетрагидрофуране, 82 мл). После перемешивания при комнатной температуре в течение четырех дней растворитель удаляют в вакууме, а остаток растворяют в этилацетате. Полученный раствор промывают насыщенным водным раствором хлорида аммония и насыщенным раствором соли, а затем сушат над безводным сульфатом натрия. Раствор фильтруют через силикагель и растворитель удаляют в вакууме, получая указанное в названии соединение.
ПРИМЕР 47B
Метиловый эфир 4-фтор-2-(1Н-индазол-4-илокси)бензойной кислоты
К раствору соединения по примеру 47A (5,56 г) в диглиме (200 мл) добавляют трет-бутоксид калия (1М раствор в тетрагидрофуране, 30,8 мл). Раствор перемешивают при комнатной температуре в течение 15 мин. Добавляют метил 2,4-дифторбензоат и раствор перемешивают при температуре 115°С в течение 16 час. Раствор охлаждают и растворитель удаляют в вакууме. Остаток растворяют в дихлорметане (100 мл) и добавляют трифторуксусную кислоту (22,6 мл). Полученный раствор перемешивают при комнатной температуре в течение 16 час. Растворитель удаляют в вакууме, остаток растворяют в этилацетате и промывают насыщенным водным раствором бикарбоната натрия, органический слой отделяют и сушат над безводным сульфатом натрия. Соединение очищают флэш-хроматографией на силикагеле, используя вначале 30%-й раствор этилацетата (в гексанах), а затем повышают до 40% этилацетата (в гексанах).
ПРИМЕР 47C
Метиловый эфир 2-(1Н-индазол-4-илокси)-4-пиперазин-1-илбензойной кислоты
Соединение по данному примеру получают, заменив в примере 44E соединение по примеру 44D на соединение по примеру 47B.
ПРИМЕР 47D
Метиловый эфир 4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-енилметил}пиперазин-1-ил)-2-(1Н-индазол-4-илокси)бензойной кислоты
Соединение по данному примеру получают, заменив в примере 44G соединение по примеру 44E на соединение по примеру 47C.
ПРИМЕР 47E
2-(1Н-Индазол-4-илокси)-4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-енил)метил)пиперазин-1-ил)бензойная кислота
Соединение по данному примеру получают, заменив в примере 44H соединение по примеру 44G на соединение по примеру 47D.
ПРИМЕР 47F
(S)-Трет-бутил 2-(((5-(N-(2-(1H-индазол-4-илокси)-4-(4-((2-(4-хлорфенил)-4,4-диметилциклогекс-1-енил)метил)пиперазин-1-ил)бензоил)сульфамоил)-4-метилтиазол-2-илокси)метил)морфолин-4-карбоксилат
Соединение по данному примеру получают, заменив в примере 1I соединение по примеру 1H на соединение по примеру 47E, а соединение по примеру 1E на соединение по примеру 43G.
1Н ЯМР (500 МГц, пиридин-d5) δ 8,36 (c, 1H), 8,11 (д, 1H), 7,47 (д, 2H), 7,38 (д, 1H), 7,22 (м, 2H), 7,11 (д, 2H), 6,88-6,80 (м, 2H), 6,62 (д, 1H), 4,52-4,45 (м, 2H), 3,90-3,70 (м, 4H), 3,45 (дт, 1H), 3,15 (м, 4H), 2,98-2,83 (м, 2H), 2,82 (c, 2H), 2,63 (c, 3H), 2,30 (м, 2H), 2,23 (м, 4H), 1,99 (c, 2H), 1,52 (c, 9H), 1,39 (т, 2H), 0,94 (c, 6H).
ПРИМЕР 48
2-(1H-Индазол-4-илокси)-4-(4-((2-(4-хлорфенил)-4,4-диметилциклогекс-1-енил)метил)пиперазин-1-ил)-N-(2-((4-фтортетрагидро-2H-пиран-4-ил)метокси)-4-метилтиазол-5-илсульфонил)бензамид
Соединение по данному примеру получают, заменив в примере 1I соединение по примеру 1H на соединение по примеру 47E, а соединение по примеру 1E на соединение по примеру 45A.
1Н ЯМР (500 МГц, пиридин-d5) δ 8,36 (c, 1H), 8,14 (д, 1H), 7,47 (д, 2H), 7,38 (д, 1H), 7,22 (м, 2H), 7,11 (д, 2H), 6,88-6,80 (м, 2H), 6,62 (д, 1H), 4,52 (дд, 2H), 3,84-3,78 (м, 2H), 3,73-3,70 (дт, 2H), 3,15 (м, 4H), 2,82 (c, 2H), 2,67 (c, 3H), 2,30 (м, 2H), 2,23 (м, 4H), 1,99 (c, 2H), 1,82-1,75 (м, 4H), 1,41 (т, 2H), 0,96 (c, 6H).
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНДУЦИРУЮЩИЕ АПОПТОЗ СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ РАКА И ИММУННЫХ И АУТОИММУННЫХ ЗАБОЛЕВАНИЙ | 2010 |
|
RU2539587C2 |
| АПОПТОЗ-ИНДУЦИРУЮЩИЕ СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ РАКА И ИММУННЫХ И АУТОИММУННЫХ ЗАБОЛЕВАНИЙ | 2009 |
|
RU2527450C2 |
| BCL-2-СЕЛЕКТИВНЫЕ АПОПТОЗ-ИНДУЦИРУЮЩИЕ СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ РАКА И ИММУННЫХ ЗАБОЛЕВАНИЙ | 2010 |
|
RU2542994C2 |
| ИНДУЦИРУЮЩИЕ АПОПТОЗ АГЕНТЫ ДЛЯ ЛЕЧЕНИЯ РАКА И ИММУННЫХ И АУТОИММУННЫХ ЗАБОЛЕВАНИЙ | 2010 |
|
RU2535203C2 |
| АПОПТОЗ-ИНДУЦИРУЮЩИЕ СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ РАКА И ИММУННЫХ И АУТОИММУННЫХ ЗАБОЛЕВАНИЙ | 2010 |
|
RU2554346C2 |
| СЕЛЕКТИВНЫЕ К BCL-2 АГЕНТЫ, ВЫЗЫВАЮЩИЕ АПОПТОЗ, ДЛЯ ЛЕЧЕНИЯ РАКА И ИММУННЫХ ЗАБОЛЕВАНИЙ | 2013 |
|
RU2621052C2 |
| ИНДУЦИРУЮЩИЕ АПОПТОЗ СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННОЙ ОПУХОЛИ И ИММУННЫХ И АУТОИММУННЫХ ЗАБОЛЕВАНИЙ | 2010 |
|
RU2573832C2 |
| ИНДУЦИРУЮЩИЕ АПОПТОЗ СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННОЙ ОПУХОЛИ И ИММУННЫХ И АУТОИММУННЫХ ЗАБОЛЕВАНИЙ | 2015 |
|
RU2628885C2 |
| ИНДУЦИРУЮЩИЕ АПОПТОЗ СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННОЙ ОПУХОЛИ И ИММУННЫХ И АУТОИММУННЫХ ЗАБОЛЕВАНИЙ | 2010 |
|
RU2535347C2 |
| ПРОИЗВОДНЫЕ ПИРРОЛО[2,3-b]ПИРИДИНА, ИНГИБИРУЮЩИЕ АКТИВНОСТЬ АНТИАПОПТИЧЕСКИХ БЕЛКОВ Bcl-2 | 2011 |
|
RU2567857C2 |
Изобретение относится к соединению формулы I или его терапевтически приемлемым солям, где А1 представляет собой фурил, имидазолил, изотиазолил, изоксазолил, пиразолил, пирролил, тиазолил, тиадиазолил, тиенил, триазолил, пиперидинил, морфолинил, дигидро-1,3,4-тиадиазол-2-ил, бензотиен-2-ил, бензотиазол-2-ил, тетрагидротиен-3-ил, [1,2,4]триазоло[1,5-а]пиримидин-2-ил или имидазо[2,1-b][1,3]-тиазол-5-ил; где А1 незамещен или замещен одним, или двумя, или тремя, или четырьмя или пятью заместителями, независимо выбранными из R1, OR1, C(O)OR1, NHR1, N(R1)2, C(N)C(O)R1, C(O)NHR1, NHC(O)R1, NR1C(O)R1, (O), NO2, F, Cl, Br и CF3; R1 представляет собой R2, R3, R4 или R5; R2 представляет собой фенил; R3 представляет собой пиразолил или изоксазолил; R4 представляет собой пиперидинил; R5 представляет собой C1-C10алкил или C2-C10алкенил, каждый из которых не замещен или замещен заместителями, выбранными из R7, SR7, N(R7)2, NHC(O)R7, F и Cl; R7 представляет собой R8, R9, R10 или R11; R8 представляет собой фенил; R9 представляет собой оксадиазолил; R10 представляет собой морфолинил, пирролидинил или тетрагидропиранил; R11 представляет собой C1-C10алкил; Z1 представляет собой фенилен; Z2 представляет собой пиперидин, не замещенный или замещенный OCH3, или пиперазин; Z1A и Z2A оба отсутствуют; L1 представляет собой C1-C10алкил или C2-C10алкенил, каждый из которых не замещен или замещен R37B; R37B представляет собой фенил; Z3 представляет собой R38 или R40; R38 представляет собой фенил; R40 представляет собой циклогексил или циклогексенил; где фенилен, представленный Z1 не замещен или замещен группой OR41; R41 представляет собой R42 или R43; R42 представляет собой фенил, который не конденсирован или конденсирован с пирролилом, имидазолилом или пиразолом; R43 представляет собой пиридинил, который не конденсирован или конденсирован с пирролилом; где каждый вышеуказанный циклический фрагмент, представленный R2, R3, R4, R8, R9, R10, R38, R40, R42 и R43, независимо не замещен или замещен одним или несколькими заместителями, независимо выбранными из R57, OR57, С(О)OR57, F, Cl CF3 и Br; R57 представляет собой R58 или R61; R58 представляет собой фенил; R61 представляет собой C1-C10алкил; и где фенил, представленный группой R58, не замещен или замещен одним или несколькими заместителями, независимо выбранными из F и Cl. Также изобретение относится к фармацевтической композиции, содержащей указанные соединения, и к способу лечения заболеваний, при которых экспрессируются антиапоптотические белки Bcl-2. 4 н. и 3 з.п. ф-лы, 2 табл., 48 пр.
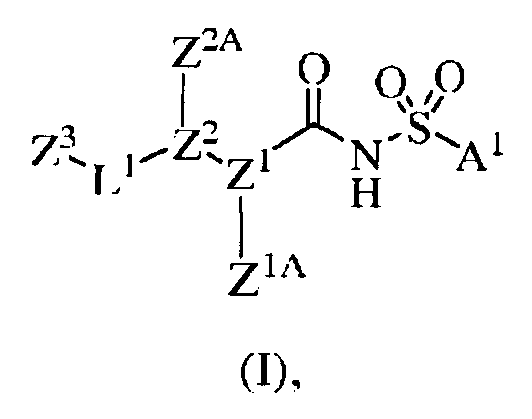
1. Соединение формулы I

или его терапевтически приемлемые соли, где
А1 представляет собой фурил, имидазолил, изотиазолил, изоксазолил, пиразолил, пирролил, тиазолил, тиадиазолил, тиенил, триазолил, пиперидинил, морфолинил, дигидро-1,3,4-тиадиазол-2-ил, бензотиен-2-ил, бензотиазол-2-ил, тетрагидротиен-3-ил, [1,2,4]триазоло[1,5-а]пиримидин-2-ил или имидазо[2,1-b][1,3]-тиазол-5-ил;
где А1 незамещен или замещен одним, или двумя, или тремя, или четырьмя или пятью заместителями, независимо выбранными из R1, OR1, C(O)OR1, NHR1, N(R1)2, C(N)C(O)R1, C(O)NHR1, NHC(O)R1, NR1C(O)R1, (O), NO2, F, Cl, Br и CF3;
R1 представляет собой R2, R3, R4 или R5;
R2 представляет собой фенил;
R3 представляет собой пиразолил или изоксазолил;
R4 представляет собой пиперидинил;
R5 представляет собой C1-C10алкил или C2-C10алкенил, каждый из которых не замещен или замещен заместителями, выбранными из R7, SR7, N(R7)2, NHC(O)R7, F и Cl;
R7 представляет собой R8, R9, R10 или R11;
R8 представляет собой фенил;
R9 представляет собой оксадиазолил;
R10 представляет собой морфолинил, пирролидинил или тетрагидропиранил;
R11 представляет собой C1-C10алкил;
Z1 представляет собой фенилен;
Z2 представляет собой пиперидин, не замещенный или замещенный OCH3, или пиперазин;
Z1A и Z2A оба отсутствуют;
L1 представляет собой C1-C10алкил или C2-C10алкенил, каждый из которых не замещен или замещен R37B
R37B представляет собой фенил;
Z3 представляет собой R38 или R40;
R38 представляет собой фенил;
R40 представляет собой циклогексил или циклогексенил;
где фенилен, представленный Z1 не замещен или замещен группой OR41;
R41 представляет собой R42 или R43;
R42 представляет собой фенил, который не конденсирован или конденсирован с пирролилом, имидазолилом или пиразолом;
R43 представляет собой пиридинил, который не конденсирован или конденсирован с пирролилом;
где каждый вышеуказанный циклический фрагмент, представленный R2, R3, R4, R8, R9, R10, R38, R40, R42 и R43, независимо не замещен или замещен одним или несколькими заместителями, независимо выбранными из R57, OR57, С(О)OR57, F, Cl, CF3 и Br;
R57 представляет собой R58 или R61;
R58 представляет собой фенил;
R61 представляет собой C1-C10алкил; и
где фенил, представленный группой R58, не замещен или замещен одним или несколькими заместителями, независимо выбранными из F и Cl.
2. Соединение по п.1 или его терапевтически приемлемая соль, где соединение имеет формулу II
 ,
,
где R101 представляет собой Н или OR41.
3. Соединение по п.1 или его терапевтически приемлемая соль, где соединение имеет формулы III
 ,
,
где R101 представляет собой Н или OR41.
4. Соединение по п.1 или его фармацевтически приемлемая соль, где указанное соединение выбрано из
4-[4-(циклогексилметил)-4-метоксипиперидин-1-ил]-N-{[5-({(1R)-3-(диметиламино)-1-[(фенилтио)метил]пропил}амино)-4-нитротиен-2-ил]сульфонил}бензамида;
N-{[5-({(1R)-3-(диметиламино)-1-[(фенилтио)метил]пропил}амино)-4-нитротиен-2-ил]сульфонил}-4-[4-метокси-4-(3-метилбензил)пиперидин-1-ил]бензамида;
N-{[5-({(1R)-3-(диметиламино)-1-[(фенилтио)метил]пропил}амино)-4-нитротиен-2-ил]сульфонил}-4-[4-(3,3-дифенилпроп-2-енил)пиперазин-1-ил]бензамида;
4-{4-[(4′-хлор-1,1′-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(4-{[2-(фенилтио)этил]амино}пиперидин-1-ил)сульфонил]бензамида;
N-[(4-{ацетил[2-(фенилтио)этил]амино}пиперидин-1-ил)сульфонил]-4-{4-[(4′-хлор-1,1′-бифенил-2-ил)метил]пиперазин-1-ил}бензамида;
4-{4-[(4′-хлор-1,1′-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(4-{метил[2-(фенилтио)этил]амино}пиперидин-1-ил)сульфонил]бензамида;
4-{4-[(4′-хлор-1,1′-бифенил-2-ил)метил]пиперазин-1-ил}-N-{[5-({(1R)-3-[изопропил(метил)амино]-1-[(фенилтио)метил]пропил}амино)-4-нитротиен-2-ил]сульфонил}бензамида;
4-(4-{[2-(4-хлорфенил)циклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-{[5-({(1R)-3-[изопропил(метил)амино]-1-[(фенилтио)метил]пропил}амино)-4-нитротиен-2-ил]сульфонил}бензамида;
4-(4-{[2-(4-хлорфенил)-5,5-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-{[5-({(1R)-3-[изопропил(метил)амино]-1-[(фенилтио)метил]пропил}амино)-4-нитротиен-2-ил]сульфонил}бензамида;
N-{[(5Z)-5-(ацетилимино)-4-метил-4,5-дигидро-1,3,4-тиадиазол-2-ил]сульфонил}-4-{4-[(4′-хлор-1,1′-бифенил-2-ил)метил]пиперазин-1-ил}бензамида;
N-{[2-(ацетиламино)-4-метил-1,3-тиазол-5-ил]сульфонил}-4-{4-[(4′-хлор-1,1′-бифенил-2-ил)метил]пиперазин-1-ил}бензамида;
N-({5-[(бензоиламино)метил]тиен-2-ил}сульфонил)-4-{4-[(4′-хлор-1,1′-бифенил-2-ил)метил]пиперазин-1-ил}бензамида;
4-{4-[(4′-хлор-1,1′-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(6-хлоримидазо[2,1-b][1,3]тиазол-5-ил)сульфонил]бензамида;
4-{4-[(4′-хлор-1,1′-бифенил-2-ил)метил]пиперазин-1-ил}-N-(морфолин-4-илсульфонил)бензамида;
4-{4-[(4′-хлор-1,1′-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(2,4-диметил-1,3-тиазол-5-ил)сульфонил]бензамида;
4-{4-[(4′-хлор-1,1′-бифенил-2-ил)метил]пиперазин-1-ил}-N-{[4-фенил-5-(трифторметил)тиен-3-ил]сульфонил]бензамида;
4-{4-[(4′-хлор-1,1′-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(5-фтор-3-метил-1-бензотиен-2-ил)сульфонил]бензамида;
N-(1,3-бензотиазол-2-илсульфонил)-4-{4-[(4′-хлор-1,1′-бифенил-2-ил)метил]пиперазин-1-ил}бензамида;
4-{4-[(4′-хлор-1,1′-бифенил-2-ил)метил]пиперазин-1-ил}-N-(тиен-2-илсульфонил)бензамида;
4-{4-[(4′-хлор-1,1′-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(5,7-диметил[1,2,4]триазоло[1,5-а]пиримидин-2-ил)сульфонил]бензамида;
этил 4-{[(4-{4-[(4′-хлор-1,1′-бифенил-2-ил)метил]пиперазин-1-ил}бензоил)амино]сульфонил}-5-метил-1,2-дифенил-1Н-пиррол-3-карбоксилата;
метил 5-{[(4-{4-[(4′-хлор-1,1′-бифенил-2-ил)метил]пиперазин-1-ил}бензоил)амино]сульфонил}-1-метил-1Н-пиррол-2-карбоксилата;
4-{4-[(4′-хлор-1,1′-бифенил-2-ил)метил]пиперазин-1-ил}-N-{[5-(1,3-диметил-1Н-пиразол-5-ил)изоксазол-4-ил]сульфонил}бензамида;
4-{4-[(4′-хлор-1,1′-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(4-хлор-3-метилизотиазол-5-ил)сульфонил]бензамида;
N-[(5-бром-3-метил-1-бензотиен-2-ил)сульфонил]-4-{4-[(4′-хлор-1,1′-бифенил-2-ил)метил]пиперазин-1-ил}бензамида;
4-{4-[(4′-хлор-1,1′-бифенил-2-ил)метил]пиперазин-1-ил}-N-({5-[(E)-2-(1,2,4-оксадиазол-3-ил)винил]тиен-2-ил}сульфонил)бензамида;
4-{4-[(4′-хлор-1,1′-бифенил-2-ил)метил]пиперазин-1-ил}-N-{[1-(2-хлорэтил)-3,5-диметил-1Н-пиразол-4-ил]сульфонил}бензамида;
5-{[(4-{4-[(4′-хлор-1,1′-бифенил-2-ил)метил]пиперазин-1-ил}бензоил)амино]сульфонил}-N-(1-этилпропил)-1,3,4-тиадиазол-2-карбоксамида;
4-{4-[(4′-хлор-1,1′-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(5-хлор-1,3-диметил-1Н-пиразол-4-ил)сульфонил]бензамида;
4-{4-[(4′-хлор-1,1′-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(4-нитро-5-пиперидин-1-илтиен-2-ил)сульфонил]бензамида;
4-{4-[(4′-хлор-1,1′-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(5-изоксазол-5-ил-2-фурил)сульфонил]бензамида;
4-{4-[(4′-хлор-1,1′-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(3,5-диметилизоксазол-4-ил)сульфонил]бензамида;
4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-2-(1Н-индол-5-илокси)-N-({4-нитро-5-[(3-пирролидин-1-илпропил)амино]тиен-2-ил}сульфонил)бензамида;
4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-[(5-{[3-(диметиламино)пропил]амино}-4-нитротиен-2-ил)сульфонил]-2-(1Н-индол-5-илокси)бензамида;
4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-2-(1Н-индол-5-илокси)-N-({5-[(3-морфолин-4-илпропил)амино]-4-нитротиен-2-ил}сульфонил)бензамида;
N-{[5-({(1R)-3-(диметиламино)-1-[(фенилтио)метил]пропил}амино)-4-нитротиен-2-ил]сульфонил}-4-{4-[2-(трифторметил)бензилиден]пиперидин-1-ил}бензамида;
4-{4-[(4′-хлор-1,1′-бифенил-2-ил)метилен]пиперидин-1-ил}-N-[(1,1-диоксидотетрагидротиен-3-ил)сульфонил]бензамида;
4-{4-[(4′-хлор-1,1′-бифенил-2-ил)метилен]пиперидин-1-ил}-N-[(5-хлор-3-метил-1-бензотиен-2-ил)сульфонил]бензамида;
4-{4-[(4′-хлор-1,1′-бифенил-2-ил)метил]пиперазин-1-ил}-N-[(5-хлор-3-метил-1-бензотиен-2-ил)сульфонил]-2-феноксибензамида;
2-(3-хлорфенокси)-4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-[(5,7-диметил[1,2,4]триазоло[1,5-а]пиримидин-2-ил)сульфонил]бензамида;
4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-[(5,7-диметил[1,2,4]триазоло[1,5-а]пиримидин-2-ил)сульфонил]-2-[(6-фтор-1Н-индол-5-ил)окси]бензамида;
4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-2-[(6,7-дифтор-1Н-индол-5-ил)окси]-N-[(5,7-диметил[1,2,4]триазоло[1,5-а]пиримидин-2-ил)сульфонил]бензамида;
трет-бутил (2S)-2-{[(5-{[4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-2-(1Н-пирроло[2,3-b]пиридин-5-илокси)бензоил]сульфамоил}-4-метил-1,3-тиазол-2-ил)окси]метил}морфолин-4-карбоксилата;
трет-бутил (2S)-2-{[(5-{[2-(1Н-бензимидазол-4-илокси)-4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)бензоил]сульфамоил}-4-метил-1,3-тиазол-2-ил)окси]метил}морфолин-4-карбоксилата;
4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-({2-[(4-фтортетрагидро-2Н-пиран-4-ил)метокси]-4-метил-1,3-тиазол-5-ил}сульфонил)-2-(1Н-пирроло[2,3-b]пиридин-5-илокси)бензамида;
2-(1Н-бензимидазол-4-илокси)-4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-({2-[(4-фтортетрагидро-2Н-пиран-4-ил)метокси]-4-метил-1,3-тиазол-5-ил}сульфонил)бензамида;
трет-бутил (2S)-2-{[(5-{[4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-2-(1Н-индазол-4-илокси)бензоил]сульфамоил}-4-метил-1,3-тиазол-2-ил)окси]метил}морфолин-4-карбоксилата;
4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-({2-[(4-фтортетрагидро-2Н-пиран-4-ил)метокси]-4-метил-1,3-тиазол-5-ил}сульфонил)-2-(1Н-индазол-4-илокси)бензамида.
5. 4-(4-{[2-(4-хлорфенил)-4,4-диметилциклогекс-1-ен-1-ил]метил}пиперазин-1-ил)-N-({2-[(4-фтортетрагидро-2Н-пиран-4-ил)метокси]-4-метил-1,3-тиазол-5-ил}сульфонил)-2-(1H-пирроло[2,3-b]пиридин-5-илокси)бензамид или его терапевтически приемлемая соль.
6. Фармацевтическая композиция для лечения рака мочевого пузыря, рака мозга, рака молочной железы, рака костного мозга, рака шейной области, хронического лимфолейкоза, колоректального рака, рака пищевода, гепатоцеллюлярного рака, лимфобластного лейкоза, фолликулярной лимфомы, лимфолейкоза, вызываемого Т-лимфоцитами или В-клетками, меланомы, миелогенного лейкоза, миеломы, рака полости рта, рака яичников, немелкоклеточного рака легкого, рака простаты, мелкоклеточного рака легкого или рака селезенки, содержащая инертный наполнитель и терапевтически эффективное количество соединения или его терапевтически приемлемой соли по п.1 или 5.
7. Способ лечения рака мочевого пузыря, рака мозга, рака молочной железы, рака костного мозга, рака шейной области, хронического лимфолейкоза, колоректального рака, рака пищевода, гепатоцеллюлярного рака, лимфобластного лейкоза, фолликулярной лимфомы, лимфолейкоза, вызываемого Т-лимфоцитами или В-клетками, меланомы, миелогенного лейкоза, миеломы, рака полости рта, рака яичников, немелкоклеточного рака легкого, рака простаты, мелкоклеточного рака легкого или рака селезенки у пациента, включающий введение пациенту терапевтически эффективного количества соединения или его терапевтически приемлемой соли по п.1 или 5.
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| MILAN BRUNCKO et al.: "Studies leading to potent | |||
Авторы
Даты
2015-01-10—Публикация
2010-01-15—Подача