Настоящее изобретение в основном относится к микроорганизмам. В частности, настоящее изобретение относится к микроорганизмам, подвергнутым воздействию высокой температуры, например к пробиотикам и заквасочным культурам для молочной продукции, а также к применениям этих бактерий. Одно из воплощений настоящего изобретения относится к микроорганизмам, подвергнутым воздействию высокой температуры, например к пробиотикам и заквасочным культурам для молочной продукции, и их использованию в получении композиций для лечения или предотвращения воспалительных расстройств.
Пробиотикам часто дают следующее определение: «живые микроорганизмы, которые будучи введены в организм-хозяин в подходящих количествах приносят пользу здоровью» (нормативы Управления по контролю качества пищевых продуктов, медикаментов и косметических средств США и Всемирной организации здравоохранения). Соответственно, большинство публикаций касаются живых пробиотиков. Однако в ряде исследований изучалось благотворное влияние на здоровье, оказываемое нереплицирующимися бактериями, и в большинстве из них были получены указания на то, что инактивация пробиотиков, например путем тепловой обработки, приводит к потере желаемой пользы для здоровья (Rachmilewitz, D., et al., 2004, Gastroenterology 126:520-528; Castagliuolo, et al., 2005, FEMS Immunol.Med.Microbiol. 43:197-204; Gill, H. S. and K. J. Rutherford, 2001,Br.J.Nutr. 86:285-289; Kaila, M., et al., 1995, Arch.Dis.Child 72:51-53.).
Тем не менее некоторые исследования показали, что инактивированные пробиотики могут в некоторой степени сохранять позитивное влияние на здоровье (Rachmilewitz, D., et al., 2004, Gastroenterology 126:520-528; Gill, H.S. and K. J. Rutherfurd, 2001, Br.J.Nutr. 86:285-289).
Об использовании пробиотиков для лечения и предотвращения воспалительных заболеваний желудочно-кишечного тракта сообщалось в печати, и недавно опубликован обзор на эту тему (Dotan, I. and D. Rachmilewitz. 2005; Curr.Opin.Gastroenterol, 21:426-430). Например, показано, что высококонцентрированная смесь из восьми живых бактерий-пробиотиков (VSL#3) эффективна для профилактики (Gionchetti, P., et al., 2003, Gastroenterology 124:1202-1209) и лечения (Gionchetti, P., et al., 2000, Gastroenterology 119:305-309; Mimura, Т., et al., 2004, Gut 53:108-114) рецидивирующего или устойчивого воспаления тонкокишечного кармана (паучита) после хирургического вмешательства у человека. Примечательна работа Rachmilewitz, D., et al., (2004, Gastroenterology 126:520-528), в которой использовалась животная модель, а именно мыши с язвенным колитом, индуцированным декстрансульфатом натрия (DSS); эти авторы сообщают, что введение живых или же подвергнутых воздействию гамма-излучения VSL#3 защищало животных от колита, a VSL#3, инактивированные путем тепловой обработки, защитным эффектом не обладали. Сходным образом, подвергнутые тепловой обработке L.crispatus не защищали от DSS-индуцированного колита, тогда как в живом виде эти бактерии явно снижали потерю массы тела и активность миелопероксидазы (МРО) в кишечнике (Castagliuolo, et al., 2005, FEMS Immunol.Med.Microbiol. 43:197-204). Эти исследования позволяют полагать, что в отношении воспалительных процессов в кишечнике пробиотики в живом виде эффективнее, чем в нереплицирующемся.
Установлено, что инактивированные бактерии L.reuteri (убитые путем тепловой обработки или подвергнутые воздействию гамма-излучения) не способны снижать индуцированное фактором некроза опухолей (TNF-α) образование интерлейкина-8 (IL-8) клетками Т84, в то время как в живом виде эти бактерии оказывают выраженное благотворное действие (Ма, D., et а1., 2004, Infect.Immun. 72:5308-5314).
Ясно, что инактивированные пробиотики значительно проще использовать на практике, например в пищевой промышленности, и/или хранить. Поэтому весьма перспективным представляется открытие того, что потребление инактивированных пробиотиков может положительно влиять на организм, хотя, конечно, этот эффект, как правило, слабее, чем у живых бактерий, а то и вовсе отсутствует.
Сообщалось о получении нереплицирующихся штаммов бактерий-пробиотиков путем воздействия на соответствующие живые бактерии высокой температуры, гамма-излучения, ультрафиолетового излучения или же химических агентов (формалина, параформальдегида). Но вряд ли найдутся работы, в которых бы сравнивалась зависимость биологических функций получаемых нереплицирующихся бактерий от применяемого способа инактивации. Помимо упомянутого выше исследования, в одной работе сообщалось, что бактерии, подвергнутые воздействию гамма-излучения, и бактерии, прошедшие тепловую обработку, индуцировали различные уровни секреции цитокинов эпителиальными клетками in vitro (Wong, С.and Z. Ustunol. 2006, J.Food Prot, 69:2285-2288).
Однако испробованные на практике и описанные в литературе методики превращения пробиотических штаммов в нереплицирующиеся, как правило, не применимы или с трудом применимы в промышленных условиях, в особенности в пищевой промышленности.
Способ изготовления большинства имеющихся в продаже продуктов, содержащих пробиотики, включает тепловую обработку. Было бы поэтому рационально проводить тепловую обработку пробиотиков вместе с изготовливаемым продуктом или по меньшей мере сходным образом так, чтобы пробиотики сохраняли или улучшали свои положительные свойства или даже приобретали новые полезные для потребляющего их организма свойства.
Но описанные в литературе способы тепловой обработки, применяемые для инактивации бактерий, предполагают, как правило, длительное (от 20 минут до 1 часа или более) воздействие температуры от 40 до 100°С, что непросто осуществить в промышленных масштабах. Кроме того, такая тепловая обработка приводила, как правило, к потере пробиотической активности, по меньшей мере частичной.
В промышленных масштабах применяется непродолжительная тепловая обработка, например ультрапастеризация (асептическая пастеризация). Такая тепловая обработка уменьшает бактериальную нагрузку в продукте и время его изготовления, тем самым снижая степень порчи питательных веществ.
Следовательно, было бы весьма желательно располагать препаратами микробных клеток, получаемыми из жизнеспособных микроорганизмов, например бактерий-пробиотиков или заквасочных культур для молочной продукции, которые можно было бы подвергать тепловой обработке таким же образом, как изготовляемые продукты, и которые обретали бы или улучшали полезные для здоровья потребителя свойства, например, способствующие предотвращению или лечению воспалительных расстройств.
Таким образом, одной из задач настоящего изобретения является обеспечение композиции, содержащей микроорганизмы, например бактерии-пробиотики или заквасочные культуры для молочной продукции, которые можно подвергать тепловой обработке в промышленных условиях для сокращения количества жизнеспособных бактериальных клеток и которые в результате этой тепловой обработки обретают или улучшают полезные для здоровья потребителя свойства.
Авторы настоящего изобретения неожиданно обнаружили, что эту задачу можно решить при помощи объекта изобретения по независимым пунктам формулы изобретения. Дальнейшее развитие настоящее изобретение получает по зависимым пунктам формулы изобретения.
Авторы настоящего изобретения впервые продемонстрировали, что микроорганизмы, например пробиотические штаммы бактерий или заквасочные культуры для молочной продукции, прошедшие кратковременную тепловую обработку при высокой температуре, обладают противовоспалительными иммуногенными свойствами безотносительно к своим исходным свойствам. В частности, в результате такой тепловой обработки может развиваться новый противовоспалительный профиль либо улучшается имеющийся.
Таким образом, теперь возможно получать нереплицирующиеся микроорганизмы, обладающие противовоспалительными иммуногенными свойствами, путем применения определенных параметров тепловой обработки, соответствующих обычно применяемым в промышленных условиях режимам тепловой обработки, даже если исходные живые микроорганизмы не характеризовались как противовоспалительные штаммы.
Этот эффект наблюдался, например, у ряда микроорганизмов, а именно пробиотических представителей лактобацилл и бифидобактерий, а также заквасочных культур для молочной продукции.
Нереплицирующиеся пробиотические микроорганизмы обладают тем преимуществом, что ими легче манипулировать нежели соответствующими живыми штаммами. Кроме того, они гораздо лучше выдерживают хранение и для них требуются менее строгие условия упаковки.
Нереплицирующиеся пробиотические микроорганизмы позволили бы разработать разнообразные продукты, которые по своей природе не допускают добавления живых пробиотиков без дополнительных мер их защиты. Это имеет значение, например, в производстве зерновых батончиков, фруктовых соков, ультрапастеризованных напитков, напитков с длительным сроком хранения и др.
Кроме того, если у потребителя ослаблена иммунная система, живые пробиотики можно применять лишь в исключительных случаях из-за риска развития бактериемии. В настоящем документе авторы предлагают метод получения нежизнеспособных бактерий, обладающих противовоспалительными свойствами безотносительно их исходному иммуногенному профилю.
Также нереплицирующиеся пробиотические микроорганизмы позволяют осуществлять растворение в горячем виде, например, порошкообразных композиций, с сохранением полезных для здоровья потребителя свойств.
Насколько известно авторам изобретения, ранее не сообщалось о применении кратковременной высокотемпературной обработки для получения нереплицирующихся бактерий с противовоспалительными свойствами.
Соответственно, в одном из воплощений данного изобретения предлагается композиция, содержащая микроорганизмы, подвергнутые кратковременному воздействию высокой температуры - по меньшей мере 71,5°С в течение по меньшей мере 1 секунды.
В настоящем изобретении предпочтительно используются пищевые микроорганизмы. Микроорганизм называется пищевым, если официально допускается его потребление человеком или животным.
В одном из воплощений данного изобретения микроорганизмы могут быть пробиотиками.
В контексте настоящего изобретения пробиотиками называются «препараты микробных клеток или компонентов микробных клеток, благотворно влияющие на состояние здоровья или жизнедеятельность организма-хозяина» (Salminen S, Ouwehand A. Benno Y. et al “Probiotics: how should they be defined” Trends Food Sci. Technol. 1999:10107-10).
В другом воплощении данного изобретения микроорганизмы могут быть заквасочными культурами для молочной продукции.
По данному изобретению микроорганизмы подвергаются кратковременной высокотемпературной обработке - предпочтительно при температуре от около 71,5 до около 150°С в течение времени от около 1 до около 120 секунд.
Более предпочтительна тепловая обработка микроорганизмов при температуре от около 90 до около 140°С, например в диапазоне 90-120°С, в течение времени от около 1 до около 30 секунд.
В одном воплощении данного изобретения такая высокотемпературная обработка превращает микроорганизмы в по меньшей мере частично нереплицирующиеся.
Термин «нереплицирующиеся микроорганизмы» включает микроорганизмы, например бактерии-пробиотики или заквасочные культуры для молочной продукции, которые прошли тепловую обработку. Это включает инактивированные, мертвые, нежизнеспособные и/или представленные фрагментами (например, ДНК, метаболитами, цитоплазматическими соединениями и/или материалом клеточной стенки) микроорганизмы.
Термин «нереплицирующиеся» означает, что жизнеспособные клетки и/или колониеобразующие единицы не выявляются обычно применяемыми методами посева/культивирования. Такие методы описаны в руководстве: James Monroe Jay, Martin J. Loessner, David A. Golden. 2005. Modem food microbiology. 7th edition, Springer Science, New York, N.Y. 790 p. Как правило, отсутствие жизнеспособных клеток демонстрируется следующим образом: не наблюдается видимых глазом колоний на агаре или увеличения мутности в жидкой культуральной среде после высевания препаратов бактериальных клеток в различных концентрациях (нереплицирующиеся образцы) и инкубации при подходящих условиях (аэробных и/или анаэробных в течение по меньшей мере 24 часов).
Высокотемпературную обработку можно проводить при нормальном атмосферном давлении, но также и при высоком давлении. Обычно давление находится в диапазоне от 1 до 50 бар, предпочтительно от 1 до 10 бар, еще более предпочтительно от 2 до 5 бар. Такое давление предпочтительно, если пробиотики подвергают тепловой обработке в среде, которая при нагревании жидкая либо твердая. Какое давления окажется наилучшим, зависит от природы композиции, в которую должны войти данные микроорганизмы, и от прилагаемой температуры.
Высокотемпературную обработку по данному изобретению можно осуществлять в диапазоне температур около 71,5-150°С, предпочтительно около 90-120°С, еще более предпочтительно около 120-140°С.
Высокотемпературную обработку по данному изобретению можно осуществлять в течение короткого периода времени продолжительностью около 1-120 секунд, предпочтительно около 1-30 секунд, еще более предпочтительно около 5-15 секунд.
Указанные временные рамки относятся ко времени, в течение которого микроорганизмы, например пробиотики и заквасочные культуры для молочной продукции, подвергаются воздействию данной температуры. Отметим, что время теплового воздействия может различаться в зависимости от природы и количества композиции, в которую должны войти пробиотики, и от конструкции используемого нагревательного оборудования.
Однако обычно композиция по данному изобретению и/или микроорганизмы подвергаются кратковременной высокотемпературной обработке (HTST), мгновенной пастеризации или ультрапастеризации (UHT).
Обработка, обозначаемая аббревиатурой UHT (ультрапастеризация), подразумевает кратковременное воздействие очень высокой температуры, в результате которой достигается по меньшей мере частичная стерилизация; ее продолжительность составляет около 1-10 секунд, в течение которых температура превышает 135°С (275°F), что требуется для гибели бактериальных спор в молоке. Например, в молоке, подвергнутом воздействию температуры выше 135°С, бактериальная нагрузка за необходимое для обработки время (2-5 секунд) снижается в той мере, которая делает возможным функционирование в непрерывном потоке.
Системы для ультрапастеризации бывают двух основных типов - прямые и непрямые. В прямых системах продукт обрабатывают путем инжекции либо нагнетания пара, а в непрямых системах продукт нагревают, используя теплообменник (пластинчатый, трубчатый или скребковый). Комбинации систем ультрапастеризации могут применяться на любой стадии или на ряде стадий процесса изготовления продукта.
Кратковременная высокотемпературная обработка (HTST) определяется следующим образом: это метод пастеризации, предназначенный для снижения количества жизнеспособных микроорганизмов в молоке на 5 порядков, т.е. убивающий 99,9999% их. Такая обработка считается достаточной для уничтожения почти всех дрожжевых и плесневых клеток и обычных бактерий, вызывающих порчу молочных продуктов, а также обеспечивающей разрушение обычных патогенных организмов, устойчивых к нагреванию. В процессе HTST-обработки молоко нагревают до 71,7°С в течение 15-20 секунд.
Мгновенная пастеризация - это метод тепловой пастеризации скоропортящихся напитков, таких как овощные и фруктовые соки, пиво и молочные продукты. Ее проводят перед заполнением емкостей для продукта, чтобы уничтожить вызывающие его порчу микроорганизмы, повысить его безопасность и продлить срок хранения. Для этого жидкость в непрерывном контролируемом потоке подвергается воздействию температуры от 71,5°С до 74°С в течение 15-30 секунд.
В контексте настоящего изобретения термин «кратковременная высокотемпературная обработка» включает, например, кратковременную высокотемпературную пастеризацию (HTST), ультрапастеризацию (UHT) и мгновенную пастеризацию.
Утратив способность к репликации в результате кратковременной высокотемпературной обработки, полученные нереплицирующиеся пробиотики проявляют улучшенные или новые полезные свойства, о чем говорилось выше.
Эффективно любое количество нереплицирующихся микроорганизмов, обсуждавшихся выше. Но, как правило, считается желательным, чтобы нереплицирующимися стали по меньшей мере 90% пробиотических организмов, предпочтительно по меньшей мере 95%, более предпочтительно по меньшей мере 98%, наиболее предпочтительно по меньшей мере 99%, еще лучше по меньшей мере 99,9%, в идеале - все пробиотики становятся нереплицирующимися.
В одном из воплощений настоящего изобретения все микроорганизмы являются нереплицирующимися.
В рамках настоящего изобретения можно использовать все микроорганизмы. Предпочтительно, чтобы используемые микроорганизмы были приемлемы в пищевых продуктах. Типичные микроорганизмы, приемлемые в пищевых продуктах, - это пробиотики.
Предпочтительно в настоящем изобретении используются пробиотики, выбираемые из группы, состоящей из представителей родов Bifidobacterium, Lactobacillus, Lactococcus, Streptococcus, Candida или их смесей.
Например, пробиотики согласно настоящему изобретению можно выбирать из группы, состоящей из Bifidobacterium longum, Bifidobacterium lactis, Bifidobacterium animalis, Bifidobacterium breve, Bifidobacterium infantis, Bifidobacterium adolescentis, Lactobacillus acidophilus, Lactobacillus casei, Lactobacillus paracasei, Lactobacillus salivarius, Lactobacillus reuteri, Lactobacillus rhamnosus, Lactobacillus johnsonii, Lactobacillus plantarum, Lactobacillus fermentum, Lactococcus lactis и/или их смесей.
Заквасочные культуры для молочной продукции согласно настоящему изобретению можно выбирать из группы, состоящей из Propionibacterium, Streptococcus thermophilus, Lactococcus lactis, Lactococcus diacetylactis, Lactococcus cremoris, Lactobacillus bulgaricus, Lactobacillus helveticus, Lactobacillus delbrueckii и их смесей.
Существенно важно, что пробиотики подвергаются высокотемпературной обработке, например воздействию температуры 71,5-150°С, в течение короткого времени (1-120 секунд). Такой обработке можно подвергать жизнеспособные и/или нежизнеспособные пробиотики.
Можно проводить неоднократную высокотемпературную обработку, например воздействие температурой 71,5-150°С в течение короткого времени (1-120 секунд).
В одном воплощении настоящего изобретения пробиотки выбирают из группы, состоящей из родов Bifidobacterium, Lactobacillus и Escherichia или их сочетаний.
Типичные примеры бифидобактерий - Bifidobacterium longum, Bifidobacterium breve или Bifidobacterium lactis. Типичные примеры лактобацилл - Lactobacillus paracasei, Lactobacillus casei, Lactobacillus acidophilus или Lactobacillus rhamnosus. Типичный пример Escherichia - штаммы Escherichia coli с желаемыми полезными свойствами.
В одном воплощении данного изобретения заквасочными культурами для молочной продукции служат Streptococcus thermophilus, Lactobacillus helveticus, Lactobacillus delbrueckii у. Lactococcus lactis.
Конкретнее, пробиотики можно выбирать, например, из группы, состоящей из Bifidobacterium longum NCC 3001, Bifidobacterium longum NCC 2705, Bifidobacterium breve NCC 2950, Bifidobacterium lactis NCC 2818, Lactobacillus paracasei NCC 2461, Lactobacillus casei NCC 4006, Lactobacillus casei ACA-DC 6002 (NCC 1825), Lactobacillus rhamnosus NCC 4007, Lactobacillus acidophilus NCC 3009, Escherichia coli Nissle 1917 или их сочетаний.
Также заквасочные культуры для молочной продукции можно выбирать, например, из группы, состоящей из Streptococcus thermophilus NCC 2019, Streptococcus thermophilus NCC 2059, Lactobacillus delbrueckii subsp.bulgaricus NCC 15 и Lactococcus lactis NCC 2287.
Все штаммы согласно изобретению депонированы согласно Будапештскому договору под следующими регистрационными номерами:
Композиции согласно настоящему изобретению включают микроорганизмы, подвергнутые кратковременному воздействию высокой температуры, в количестве, достаточном для по меньшей мере частичного лечения воспалительных расстройств и/или их осложнений. Количество микроорганизмов, необходимое и достаточное для осуществления этой задачи, называется «терапевтически эффективная доза». Количество микроорганизмов, эффективное для достижения такой цели, зависит от ряда факторов, известных специалистам в данной области техники, например от степени тяжести заболевания, массы тела больного и общего состояния его здоровья, а также от характера пищевого продукта, в составе которого находятся микроорганизмы.
При применении в профилактических целях композиции согласно изобретению вводят в организм потребителя, подверженного воспалительному расстройству или иным образом испытывающего риск такого заболевания, в количестве, достаточном для по меньшей мере частичного снижения риска развития воспалительных расстройств. Такое количество микроорганизмов называется «профилактически эффективная доза». Опять-таки конкретное количество зависит от ряда индивидуальных факторов, например, от общего состояния здоровья больного, его массы тела, а также от характера пищевого продукта, в составе которого находятся микроорганизмы.
Специалистам в данной области техники не составит труда подобрать нужную терапевтически эффективную дозу и/или профилактически эффективную дозу.
Как правило, композиция согласно изобретению содержит микроорганизмы, подвергнутые кратковременному воздействию высокой температуры, в терапевтически эффективной дозе и/или в профилактически эффективной дозе.
В типичном случае терапевтически эффективная доза и/или профилактически эффективная доза составляет от 0,005 мг/сут до 1000 мг/сут нереплицирующихся микроорганизмов, подвергнутых кратковременному воздействию высокой температуры.
В конкретном выражении нереплицирующиеся микроорганизмы, подвергнутые кратковременному воздействию высокой температуры, могут присутствовать в композиции согласно изобретению в количестве, соответствующем 104-1012 эквивалентов КОЕ на 1 г композиции в сухом состоянии. Ясно, что нереплицирующиеся микроорганизмы не образуют колоний, так что это определение следует понимать как количество нереплицирующихся микроорганизмов, полученное из 104-1012 КОЕ/г реплицирующихся бактерий. Это включает микроорганизмы инактивированные, нежизнеспособные или мертвые либо присутствующие в виде фрагментов (ДНК, клеточная стенка, компоненты цитоплазмы). Иными словами, количество микроорганизмов, содержащихся в композиции по данному изобретению, выражается как колониеобразующая способность (КОЕ) такого количества микроорганизмов, как если бы все эти микроорганизмы были живыми безотносительно к тому, являются ли они на деле нереплицирующимися (инактивированными или мертвыми, фрагментированными или представленными смесью каких-либо или всех этих состояний).
Предпочтительно микроорганизмы согласно изобретению присутствуют в композиции в количестве, эквивалентном от 104 до 109 КОЕ/г композиции в сухом состоянии, еще более предпочтительно - в количестве, эквивалентном от 105 до 108 КОЕ/г композиции в сухом состоянии.
Композиция согласно изобретению может быть в любом виде. Она может быть предназначена для перорального или иного энтерального введения, для парентерального введения (подкожно или внутримышечно), интравагинального, интраректального, местного или внутриглазного введения. Это может быть, например, фармацевтическая композиция, нутрицевтик, биологически активная добавка, косметическая композиция, корм для животных, пищевой продукт или напиток.
Пищевые продукты согласно изобретению включают молочные продукты, например продукты молочнокислого брожения (йогурт, пахта и др.); мороженое; концентрированное молоко; молоко; сливки; ароматизированные молочные напитки; напитки на основе молочной сыворотки; верхушечные украшения для десертов; заменители сливок для кофе; шоколад; сырные продукты; супы; соусы; пюре; дрессинги; пудинги; кремы; продукты для детского питания; питательные смеси (например, для полнорационного питания: для грудных детей, для детей старше года, для подростков, взрослых, пожилых или тяжело больных людей; зерновые продукты и зерновые батончики (мюсли).
Напитки согласно изобретению включают, например, молочные или йогуртовые напитки, кисломолочные напитки, белковые напитки, кофе, чай, энергетические напитки, соевые напитки, фруктовые и/или овощные напитки, фруктовые и/или овощные соки.
Косметические композиции согласно изобретению могут включать, например, лосьоны, шампуни, глазные капли, кремы.
Биологически активные добавки или лекарственные средства могут быть, например, в форме таблеток, капсул, пастилок, саше, гелей или жидкостей (например, питательных растворов).
Композиции по данному изобретению могут также содержать защитные гидроколлоиды (например, камеди, белки, модифицированный крахмал), связующие агенты, пленкообразующие агенты, инкапсулирующие агенты/материалы, материалы клеточных стенок, компоненты межклеточного матрикса, покрытия, эмульгаторы, поверхностно-активные вещества, солюбилизирующие агенты (масла, жиры, воска, лецитины и др.), абсорбенты, носители, наполнители, со-соединения, диспергирующие агенты, увлажняющие агенты, технологически вспомогательные вещества (растворители), текучие агенты, вкусомаскирующие агенты, утяжеляющие агенты, желирующие агенты, гелеобразующие агенты, антиоксиданты и противомикробные агенты. Они могут также содержать традиционные фармацевтические добавки и адъюванты, вспомогательные вещества и разбавители, включая (но не ограничиваясь перечисленным) воду, желатин любого происхождения, растительные камеди, лигнинсульфонат, тальк, сахара, крахмал, аравийскую камедь, растительные масла, полиалкиленгликоли, ароматизирующие агенты, консерванты, стабилизаторы, эмульгаторы, буферные агенты, смазывающие агенты, красители, увлажняющие агенты, наполнители и прочее.
Также композиции согласно изобретению могут содержать органический или неорганический носитель, пригодный для перорального или иного энтерального введения, равно как и витамины, микроэлементы и другие питательные вещества, требующиеся организму в малых количествах, в соответствии с государственными установлениями, например с рекомендуемыми нормами потребления питательных веществ, принятыми в США.
Композиции согласно изобретению могут также содержать другие агенты, в зависимости от предназначения той или иной композиции. Например, для уменьшения дискомфорта, обусловленного воспалительным расстройством, в композицию могут быть добавлены обезболивающие или жаропонижающие агенты.
Для стабилизации композиции и ее составляющих могут добавляться стабилизирующие агенты.
Для придания композиции приятного запаха/вкуса могут быть добавлены ароматизирующие агенты, и/или для придания композиции отличительного либо привлекательного цвета - красители.
В композиции по данному изобретению можно добавлять пребиотики. Пребиотики могут поддерживать рост пробиотиков до того момента, когда их превращают в нереплицирующиеся. Пребиотики могут также действовать синергически с жизнеспособными бактериями-пробиотиками, которые присутствуют в композиции и/или могут быть в нее добавлены.
Термин «пребиотики» означает неперевариваемые компоненты пищи, способствующие росту полезных для здоровья микроорганизмов и/или пробиотиков в кишечнике. Они не расщепляются в желудке и/или в верхних отделах кишечника и не всасываются в желудочно-кишечном тракте потребителя, а подвергаются брожению под действием кишечной микрофлоры и/или пробиотиков. Пребиотики охарактеризован, например, в работе Glenn R. Gibson and Marcel B. Roberfroid, Dietary Modulation of the Human Colonic Microbiota: Introducing the Concept of Prebiotics, J. Nutr. 1995 125:1401-1412.
Выбор пребиотиков для применения согласно изобретению ничем конкретным не ограничен; пребиотики, используемые согласно изобретению, включают все пищевые вещества, способствующие росту пробиотиков или полезных для здоровья микроорганизмов в кишечнике. Предпочтительно пребиотики по данному изобретению выбирают из группы, состоящей из олигосахаридов, в число которых при необходимости входят фруктоза, галактоза, манноза; пищевые волокна, в частности растворимые волокна, соевые волокна; инулин или их смеси. Предпочтительными пребиотиками согласно изобретению являются фруктоолигосахариды (FOS), галактоолигосахариды (GOS), изомальтоолигосахариды (IMO), ксилоолигосахариды (XOS), арабиноксилоолигосахариды (AXOS), маннанолигосахариды (MOS), соевые олигосахариды, гликозилсахароза (GS), лактосахароза (LS), лактулоза (LA), палатинозолигосахариды (РАО), мальтоолигосахариды, камеди и/или их гидролизаты, пектины и/или их гидролизаты.
В композиции согласно изобретению можно также добавлять дополнительные пробиотики. Дополнительно могут быть добавлены любые пробиотические микроорганизмы. Предпочтительно пробиотики для этой цели выбирают из группы, состоящей из Bifidobacterium, Lactobacillus, Lactococcus, Enterococcus, Streptococcus, Kluyveromyces, Saccharoymces, Candida, Escherichia; в частности выбирают из группы, состоящей из Bifidobacterium longum, Bifidobacterium lactis, Bifidobacterium animalis, Bifidobacterium breve, Bifidobacterium infantis, Bifidobacterium adolescentis, Lactobacillus acidophilus, Lactobacillus casei, Lactobacillus paracasei, Lactobacillus salivarius, Lactobacillus lactis, Lactobacillus reuteri, Lactobacillus rhamnosus, Lactobacillus johnsonii, Lactobacillus plantarum, Lactobacillus salivarius, Lactococcus lactis, Enterococcus faecium, Saccharomyces cerevisiae, Saccharomyces boulardii, Escherichia coli или их смесей; предпочтительно дополнительные пробиотики выбирают из группы, состоящей из Bifidobacterium longum NCC 3001 (ATCC BAA-999), Bifidobacterium longum NCC 2705 (CNCM 1-2618), Bifidobacterium longum NCC 490 (CNCM 1-2170), Bifidobacterium lactis NCC 2818 (CNCM 1-3446), Bifidobacterium breve NCC 2950 (CNCM 1-3865), Lactobacillus paracasei NCC 2461 (CNCM 1-2116), Lactobacillus johnsonii NCC 533 (CNCM 1-1225), Lactobacillus rhamnosus GG (ATCC53103), Lactobacillus rhamnosus NCC 4007 (CGMCC 1.3724), Enterococcus faecium SF65 (NCC 2768; NCIMB10415) и их смесей.
Композиции согласно изобретению могут предназначаться для любого млекопитающего, но предпочтительно они предназначены для людей и домашних питомцев.
Композиция согласно изобретению может также содержать все необходимые в суточном рационе витамины и минеральные вещества в значимых для питания количествах. Для определенных витаминов и минеральных веществ установлены минимально необходимые количества. Примеры минеральных веществ, витаминов и других питательных веществ, при необходимости входящих в состав композиций по данному изобретению, включают витамин А, витамин B1, витамин В2, витамин В6, витамин B12, витамин Е, витамин К, витамин С, витамин D, фолиевую кислоту (витамин В9), инозит (витамин B8), ниацин (никотиновую кислоту, или витамин РР), биотин (витамин В7), пантотеновую кислоту (витамин B5), холин (витамин В4), кальций, фосфор, йод, железо, магний, медь, цинк, марганец, хлорид, калий, натрий, селен, хром, молибден, таурин и L-карнитин. Минеральные вещества обычно включают в композицию в форме солей. Присутствие в композиции те или иных минеральных веществ и витаминов и их количества зависят от того, для кого предназначена данная композиция.
Композиция согласно изобретению может содержать по меньшей мере один источник белков, по меньшей мере один источник углеводов и по меньшей мере один источник липидов.
В качестве источника белков можно использовать любой подходящий пищевой белок, например животные белки (например, белки молока, белки мяса и белки яиц); растительные белки (например, белки сои, белки пшеницы, белки риса и белки гороха); смеси свободных аминокислот или их сочетания.
Особенно предпочтительны молочные белки (например, казеин и сывороточные белки) и соевые белки. Что касается сывороточных белков, то источник белков может быть на основе кислой либо сладкой сыворотки или их смеси и может включать альфа-лактальбумин и бета-лактоглобулин в желаемом соотношении.
Предпочтительно, особенно в случае смесей для детского питания, чтобы источник белков был на основе модифицированной сладкой сыворотки. Сладкая сыворотка - вполне доступный побочный продукт изготовления сыров; она часто используется в производстве смесей для детского питания на основе коровьего молока.
Белки в композиции согласно изобретению могут быть интактными либо гидролизованными или же представлять собой смесь интактных и гидролизованных белков. Желательно использовать частично гидролизованные белки (степень гидролиза 2-20%).
Если нужны гидролизованные белки, то процесс гидролиза можно осуществить желаемым образом, применяя известные в данной области методы. Например, можно получить гидролизат сывороточного белка путем ферментативного гидролиза соответствующей фракции сыворотки в одну или несколько стадий.
Если композиция согласно изобретению содержит источник белков, то количество в ней белка или белкового эквивалента составляет, как правило, от 1,6 до 7,5 г/100 ккал энергосодержания композиции.
В частности, в случае питательных смесей источник белков должен обеспечивать минимальные потребности организма в незаменимых аминокислотах.
Если композиция по данному изобретению содержит источник углеводов, то природа используемых углеводов ничем конкретным не ограничивается. Можно использовать любой подходящий углевод, например сахарозу, лактозу, глюкозу, фруктозу, сухая кукурузная патока, мальтодекстрины, крахмал и их смеси. Можно использовать комбинации различных источников углеводов. Предпочтительно углеводы обеспечивают от 30 до 80% энергосодержания композиции. Например, композиция по данному изобретению может содержать источник углеводов в количестве 9-18 г/100 ккал энергосодержания композиции.
Если композиция согласно изобретению содержит источник липидов, то природа используемых липидов ничем конкретным не ограничивается. Если композиция по данному изобретению содержит источник липидов, то он может обеспечивать от 5 до 70% энергосодержания композиции. В композицию можно включать длинноцепочечные n-3 и/или n-6 полиненасыщенные жирные кислоты, например DHA, ARA и/или ЕРА. Нужный состав жиров может быть достигнут при использовании смеси улучшенного рапсового масла, кукурузного масла, подсолнечного масла с высоким содержанием олеиновой кислоты, а также триглицеридов со средней длиной цепи. Композиция по данному изобретению может содержать источник липидов в количестве 1,5-7 г/100 ккал энергосодержания композиции.
В композиции по данному изобретению можно также включать пищевые волокна. Пищевые волокна могут быть растворимыми и нерастворимыми; как правило, предпочтительна смесь волокон этих двух групп. Приемлемые источники пищевых волокон включают сою, горох, овес, пектины, гуаровую камедь, аравийскую камедь, фруктоолигосахариды, галактоолигосахариды, сиалиллактозу и олигосахариды, происходящие из молока животных. Предпочтительно использовать смесь инулина с короткоцепочечными фруктоолигосахаридами.
Композиции по настоящему изобретению могут быть получены любым способом, известным в данной области техники. Например, если композиция представляет собой питательную смесь, как, например, смесь для кормления грудных детей, то она может быть приготовлена путем соединения и смешивания в нужном соотношении источника белков, источника углеводов и источника жиров. Если требуется, в полученную смесь могут быть добавлены эмульгаторы. На этой стадии можно также добавлять витамины и минеральные вещества, но обычно их включают в композицию позже во избежание их теплового разрушения. Какие-либо липофильные витамины, эмульгаторы и прочие соединения можно растворять в источнике жиров до смешивания его с прочими компонентами. Затем для достижения жидкой консистенции может добавляться вода - предпочтительно вода, очищенная путем обратного осмоса.
Полученную жидкую смесь можно подвергнуть тепловой обработке для снижения бактериальной нагрузки. Например, ее можно быстро нагреть до температуры от около 120°С до около 140°С и держать при этой температуре от около 5 до около 30 секунд. Такую процедуру можно проделать путем инжекции пара или с помощью теплообменника, например пластинчатого теплообменника.
Жидкую смесь затем охлаждают до температуры от около 60°С до около 85°С; это можно проделать методом сверхбыстрого охлаждения. Полученную жидкую смесь затем гомогенизируют; это осуществляется, например, в две стадии (на первой стадии при давлении от около 7 МПа до около 40 МПа, на второй стадии при давлении от около 2 МПа до около 14 МПа). Гомогенизированную смесь далее охлаждают для добавления термочувствительных компонентов, например витаминов и минеральных веществ.
На этой стадии обычно стандартизуют рН и содержание сухого вещества. Гомогенизированную смесь помещают в подходящую сушильную установку (например, для распылительной сушки или для сублимационной сушки) и превращают в порошок. Содержание влаги в полученном порошке должно быть не более около 5 масс.%.
Пробиотики для использования согласно изобретению можно культивировать любым приемлемым методом и подготавливать к включению в состав питательной композиции путем, например, путем сублимационной сушки или распылительной сушки. Подготовленные пробиотики можно добавлять в композицию до того, как ее подвергают тепловой обработке для снижения бактериальной обсемененности. В результате пробиотики становятся по меньшей мере частично нереплицирующимися. Или же пробиотики отдельно подвергают кратковременной высокотемпературной обработке, так что они становятся нереплицирующимися, а уже затем в жидком виде или в форме порошка включают в состав композиции.
Выбранные пробиотики можно культивировать любым подходящим методом и подготавливать к включению в состав питательной композиции путем, например, сублимационной сушки или распылительной сушки. Или же можно приобрести у специализированных производителей бактериальные препараты, уже подготовленные в желаемой форме для включения в состав пищевых продуктов.
Исследуя иммуногенные свойства живых и прошедших кратковременную высокотемпературную обработку препаратов бактерий-пробиотиков, авторы настоящего изобретения определяли способность этих пробиотиков индуцировать секрецию определенных цитокинов клетками крови человека.
Иммуногенные свойства жизнеспособных пробиотиков сравнивали с таковыми бактериальных клеток, подвергнутых кратковременной высокотемпературной обработке. Было обнаружено, что прошедшие тепловую обработку пробиотики индуцируют иные уровни секреции цитокинов, нежели соответствующие живые препараты.
Пробиотики, подвергнутые кратковременному воздействию высокой температуры, индуцировали секрецию меньших количеств провоспалительных цитокинов (TNF-α, IFN-гамма, IL-12p40), в то же время поддерживая или индуцируя более интенсивную секрецию IL-10, чем соответствующие живые препараты. В результате отношение IL-12p40/IL-10 в случае прошедших тепловую обработку пробиотиков было ниже, чем в случае соответствующих живых клеток. В противоположность этому бактерии, подвергнутые воздействию температуры 85°С в течение 20 минут, вызывали более высокие уровни секреции провоспалительных цитокинов и менее высокий уровень IL-10, чем живые клетки; в результате создавалось более высокое отношение IL-12p40/IL-10. Это свидетельствует, что в данном изобретении существен режим тепловой обработки.
Отношение IL-12p40/IL-10, получаемое при инкубации мононуклеарных клеток периферической крови (РВМС) с пробиотиками in vitro, обладает предсказательной силой в отношении противовоспалительного действия in vivo (Foligne, В., et а1., 2007, World J.Gastroenterol. 13:236-243).
Настоящее изобретение также относится к композициям согласно изобретению для лечения или предотвращения воспалительных расстройств.
Соответственно, одно из воплощений данного изобретения состоит в применении композиции согласно изобретению для получения продукта, предназначенного для лечения или предотвращения воспалительных расстройств.
Какие именно воспалительные расстройства можно лечить или предотвращать при помощи композиций согласно изобретению, ничем конкретным не ограничивается.
Например, такие расстройства могут быть выбраны из группы, состоящей из острых воспалительных состояний (как, например, сепсис); ожогов; хронических воспалительных процессов, как, например воспалительные заболевания кишечника (болезнь Крона, язвенный колит, паучит); некротизирующего энтероколита; воспалительных заболеваний кожи, как, например воспалительные процессы, вызванные ультрафиолетовым излучением или воздействием химических веществ, экземы, аллергического воспаления кожи; синдрома раздраженного кишечника; воспалительных процессов в глазах; аллергии, астмы; воспалительных процессов, связанных с ожирением; неспецифических воспалительных процессов, связанных со старением, и их сочетаний.
Настоящее изобретение также охватывает способ получения микроорганизмов, например пробиотиков и/или заквасочных культур для молочной продукции, в частности жизнеспособных пробиотиков и/или жизнеспособных заквасочных культур для молочной продукции, обладающих противовоспалительным действием, или способ усиления противовоспалительного действия микроорганизмов, в частности жизнеспособных пробиотиков и/или жизнеспособных заквасочных культур для молочной продукции, включающий стадию кратковременной обработки этих микроорганизмов высокой температурой - по меньшей мере 71,5°С в течение по меньшей мере 1 секунды, например воздействие температуры от около 71,5°С до около 150°С в течение времени от около 1 до около 120 секунд.
Если жизнеспособные пробиотики и/или жизнеспособные заквасочные культуры для молочной продукции используются этим способом, то кратковременная высокотемпературная обработка приводит к тому, что по меньшей мере часть пробиотиков и/или заквасочных культур для молочной продукции становится нереплицирующейся.
Кратковременная высокотемпературная обработка может приводить к превращению в нереплицирующиеся клетки по меньшей мере 90%, предпочтительно по меньшей мере 95%, более предпочтительно по меньшей мере 98%, наиболее предпочтительно по меньшей мере 99%, лучше всего по меньшей мере 99,9%, в идеале все пробиотические клетки становятся нереплицирующимися.
В одном из предпочтительных воплощений настоящего изобретения этот способ включает стадию добавления жизнеспособных пробиотиков в композицию согласно изобретению и кратковременное воздействие на содержащую пробиотики композицию высокой температуры.
Микроорганизмы по данному изобретению могут подвергаться тепловой обработке также до включения в состав продукта.
Композиция по данному изобретению может быть любой; например, это может быть пищевой или питательный продукт или напиток, в который включаются пробиотики.
По данному изобретению также предлагается способ получения композиции, содержащей микроорганизмы, например пробиотики и/или заквасочные культуры для молочной продукции, предпочтительно жизнеспособные пробиотики и/или жизнеспособные заквасочные культуры для молочной продукции, обладающие противовоспалительными свойствами, или улучшения имеющихся противовоспалительных свойств, включающий стадию кратковременной высокотемпературной обработки указанных микроорганизмов при по меньшей мере 71,5°С в течение 1 секунды, например при температуре от около 71,5°С до 150°С в течение времени от около 1 до около 120 секунд.
Стадия кратковременной высокотемпературной обработки может осуществляться с помощью промышленного оборудования, но также и в домашних условиях при помощи, например, парогенератора. В последнем случае противовоспалительное действие продукт может приобретать непосредственно перед его потреблением.
Специалистам в данной области техники должно быть ясно, что можно свободно комбинировать все описанные здесь признаки настоящего изобретения, не выходя за пределы его объема, раскрытого в настоящем документе. В частности, признаки, относящиеся к применению и способам согласно изобретению, применимы к способам и композициям согласно изобретению и наоборот.
Другие преимущества и признаки настоящего изобретения следуют из нижеследующих примеров и иллюстраций.
Краткое описание фигур
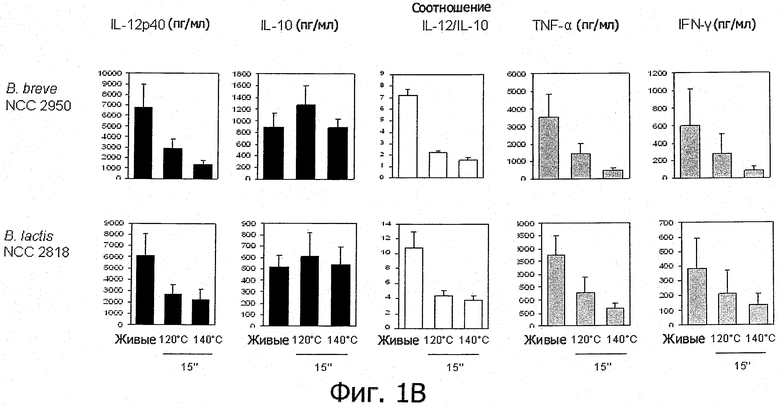
Фигуры 1А и 1В иллюстрируют усиление противовоспалительных свойств у пробиотиков, подвергнутых кратковременному воздействию высокой температуры.
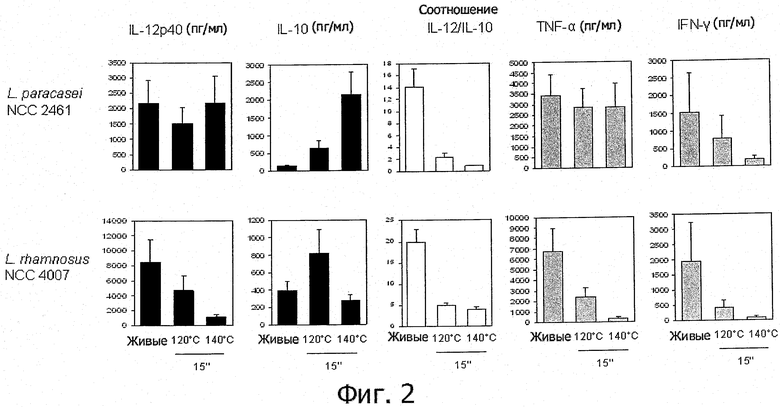
Фигура 2 иллюстрирует тот факт, что не обладающие противовоспалительными свойствами пробиотические штаммы после кратковременной высокотемпературной обработки приобретают противовоспалительные свойства, а именно у них наблюдается выраженный противовоспалительный иммуногенный профиль in vitro,
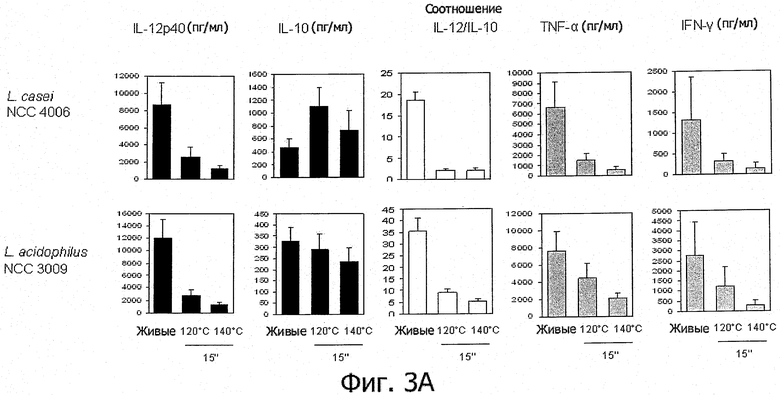
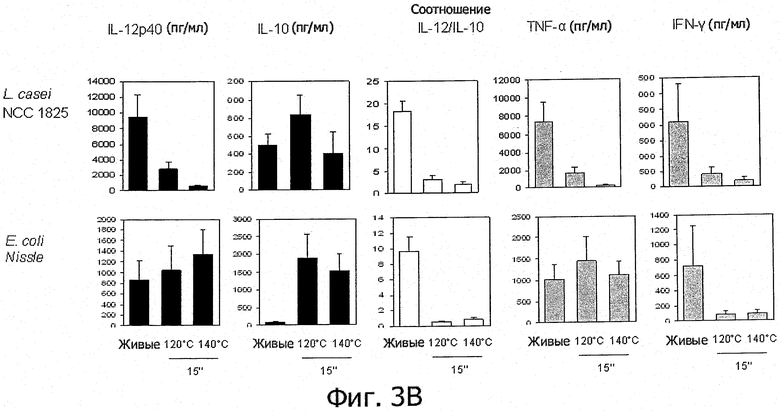
Фигуры 3А и 3В иллюстрируют тот факт, что пробиотические штаммы, используемые в имеющихся в продаже продуктах, после кратковременной высокотемпературной обработки проявляют усиленные или новые противовоспалительные иммуногенные свойства in vitro,
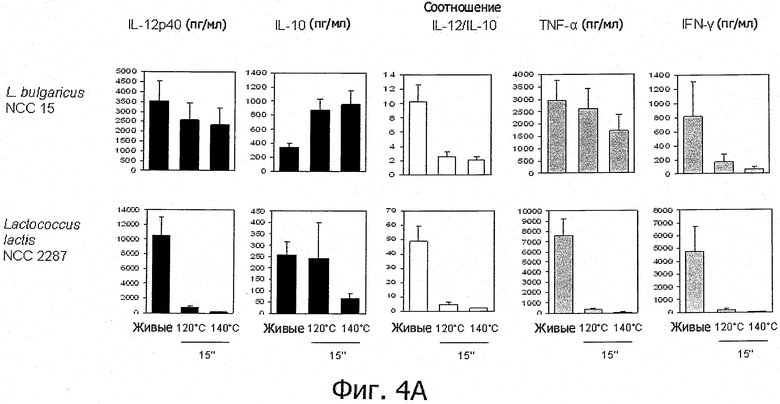
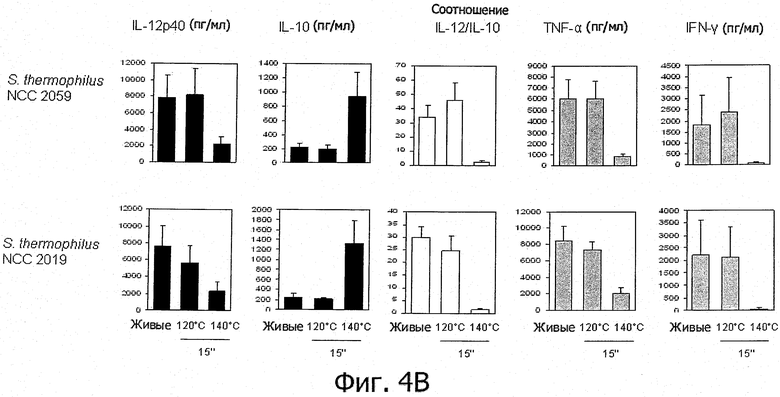
Фигуры 4А и 4В иллюстрируют тот факт, что штаммы заквасочных культур для молочной продукции (например, Lc1) после тепловой обработки при высокой температуре проявляют усиленные или новые противовоспалительные иммуногенные свойства in vitro.
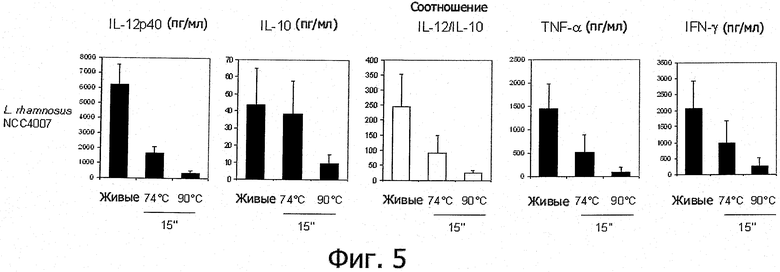
Фигура 5 иллюстрирует тот факт, что не обладающие противовоспалительными свойствами пробиотические штаммы после обработки типа HTST проявляют противовоспалительные иммуногенные свойства in vitro.
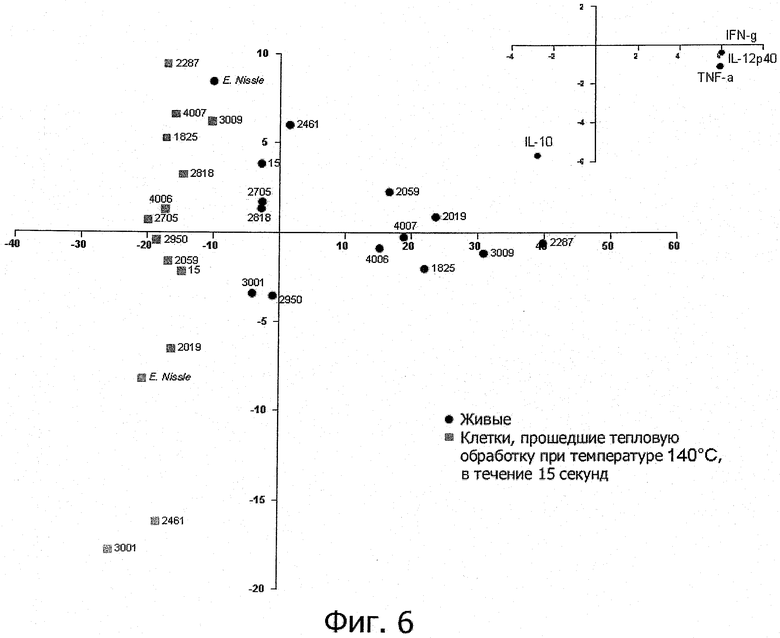
Фигура 6 изображает результаты анализа методом главных компонент данных, полученных в опытах с мононуклеарными клетками периферической крови (РВМС), которые секретировали цитокины (IL-12p40, IFN-γ, TNF-α, IL-10) под влиянием штаммов пробиотиков и заквасочных культур для молочной продукции, прошедших тепловую обработку (при температуре 140°С в течение 15 секунд) или же в нативной форме. Каждое условное обозначение (кружок либо квадратик) соответствует одному штамму - (нативному либо прошедшему тепловую обработку) - и идентифицируется регистрационным номером в коллекции культур компании Nestle (NCC) или названием данного штамм (курсивом).
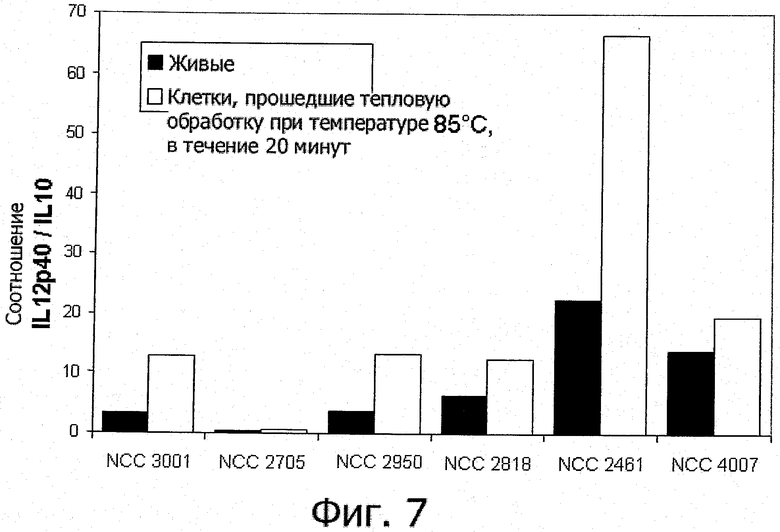
Фигура 7 показывает значения отношения IL-12p40/IL-10 для нативных и прошедших тепловую обработку (при температуре 85°С в течение 20 минут) штаммов. В целом тепловая обработка при температуре 85°С в течение 20 минут приводит к увеличению отношения IL-12p40/IL-10 в противоположность кратковременной тепловой обработке по данному изобретению (фигуры 1, 2, 3, 4 и 5).
Примеры
Методики
Получение бактериальных препаратов
Обычно считается, что полезное для здоровья влияние на иммунную систему организма-хозяина, оказываемое живыми пробиотиками, является штаммспецифичным. Было показано, что штаммы пробиотиков, индуцирующие высокие уровни интерлейкина-10 и/или низкие уровни провоспалительных цитокинов in vitro (определение в системе с РВМС), оказываются мощными противовоспалительными агентами in vivo (Foligne, В., et aL, 2007, World J.Gastroenterol. 13:236-243).
Для изучения противовоспалительных свойств пробиотиков после тепловой обработки использовались следующие штаммы: Bifidobacterium longum NCC 3001, Bifidobacterium longum NCC 2705, Bifidobacterium breve NCC 2950, Bifidobacterium lactis NCC 2818, Lactobacillus paracasei NCC 2461, Lactobacillus rhamnosus NCC 4007, Lactobacillus casei NCC 4006, Lactobacillus acidophilus NCC 3009, Lactobacillus casei ACA-DC 6002 (NCC 1825) и Escherichia coli Nissle. Испытывались также некоторые штаммы заквасочных культур для молочной продукции, используемые для изготовления продуктов молочнокислого брожения в компании Nestle, содержащих пробиотик Lc1: Streptococcus thermophilus NCC 2019, Streptococcus thermophilus NCC 2059, Lactobacillus bulgaricus NCC 15 and Lactococcus lactis NCC 2287.
Бактериальные клетки культивировали в биореакторах объемом 5-15 л в условиях, оптимизированных для каждого из используемых штаммов. При этом использовали все обычно применяемые для культивирования бактерий культуральные среды. Такие среды известны специалистам в данной области техники. Когда рН доходил до 5,5 непрерывно добавляли 30%-ный раствор щелочи (NaOH или Ca(OH)2). Когда требовались анаэробные условия, свободное пространство реактора заполняли CO2. Клетки Е coli культивировали в стандартных аэробных условиях.
Бактериальные клетки собирали путем центрифугирования (5000 g при 4°С) и ресуспендировали в фосфатном буферном растворе (PBS) в таком объеме, чтобы получить конечную концентрацию около 109-1010 КОЕ/мл. Часть препаратов замораживали при 80°С в 15%-ном глицерине. Остальные клетки подвергали тепловой обработке следующим образом:
- Очень высокая температура (UHT): 140°С в течение 15 секунд; непрямая инжекция пара;
- Высокая температура в течение короткого времени (HTST): 74°С, 90°С и 120°С в течение 15 секунд; непрямая инжекция пара;
- Относительно низкая температура в течение относительно продолжительного времени: 85°С в течение 20 минут на водяной бане.
После тепловой обработки образцы замораживали и хранили при -80°С вплоть до использования.
Определение иммуногенных свойств бактериальных препаратов in vitro.
Определяли иммуногенные свойства живых и подвергнутых тепловой обработке бактериальных препаратов, а именно их способность индуцировать секрецию определенных цитокинов клетками крови человека in vitro. Мононуклеарные клетки периферической крови (РВМС) выделяли из клеточного материала после фильтрования крови. После разделения клеток в градиенте плотности мононуклеарные клетки собирали и дважды промывали сбалансированным солевым раствором Хэнка. Затем клетки ресуспендировали в среде Дульбекко, модифицированной по способу Искова (IMDM, Sigma), в которую добавляли фетальную телячью сыворотку 10% (Bioconcept, Paris, France), 1% L-глутамин (Sigma), 1% пенициллин/стрептомицин (Sigma) и 0,1% гентамицин (Sigma). Затем образцы РВМС (7×105 клеток на лунку) инкубировали с живыми и подвергнутыми тепловой обработке бактериями (в количестве, эквивалентном 7×10 КОЕ на одну лунку) в 48-луночных планшетах в течение 36 часов. Определяли влияние живых и подвергнутых тепловой обработке бактерий на РВМС от 8 разных доноров в двух отдельных экспериментах. Через 36 часов инкубации культуральные планшеты замораживали и держали при -20°С вплоть до определения цитокинов. Профили цитокинов определяли параллельно (то есть в одном и том же эксперименте с одной и той же партией РВМС) для живых бактерий и для подвергнутых тепловой обработке таких же бактерий,
Уровни цитокинов - гамма-интерферона (INF-γ), интерлейкина-12р40 (IL-12p40), альфа-фактора некроза опухолей (TNF-α) и интерлейкина-10(IL-10) определяли в супернатанте культуральной среды через 36 часов инкубации путем иммуноферментного анализа ELISA (человеческий IL-10 R&D DuoSet, человеческий IL-12p40 BD OptEIA, человеческий TNF-α BD OptEIA, человеческий INF-γ BD OptEIA), следуя инструкциям производителя. Гамма-интерферон, интерлейкин-12р40 и альфа-фактор некроза опухолей представляют собой провоспалительные цитокины, а интерлейкин-10 является мощным противовоспалительным агентом. Результаты экспериментов выражали как среднее значение (пг/мл)+/- стандартная ошибка среднего (SEM) для 4 разных доноров; представлены два отдельных эксперимента с четырьмя донорами каждый. Для каждого штамма рассчитывали отношение IL-12p40/IL-10, имеющее предсказательную силу относительно противовоспалительного эффекта in vivo (Foligne, В., et а1., 2007, World J.Gastroenterol. 13:236-243).
Полученные для каждого штамма численные значения уровней цитокинов (пг/мл), определеные методом ELISA (см.выше) подставляли в программу BioNumerics v5.10 (Applied Maths, Smt-Martens-Latem, Belgium). На этом массиве данных проводили анализ методом главных компонент (РСА), включая вычитание средних значений и деление на отклонение.
Результаты
Противовоспалительные свойства, создаваемые ультравысокотемпературной (UHTV кратковременной высокотемпературной (HTST) обработкой
Изучаемые штаммы пробиотиков подвергали обработке очень высокой температурой (ультрапастеризации - UHT), кратковременной обработке высокой температурой (HTST) и воздействию температуры 85°С в течение 20 минут и сравнивали их иммуногенные свойства с таковыми живых клеток in vitro. При инкубации с человеческими мононуклеарными клетками периферической крови (РВМС) живые микроорганизмы (пробиотики и/или заквасочные культуры для молочной продукции) индуцировали различные уровни секреции цитокинов (Фигуры 1, 2, 3, 4 и 5). В результате тепловой обработки этих микроорганизмов изменялись уровни цитокинов, продуцируемых РВМС, причем зависимым от температуры образом. После кратковременной высокотемпературной обработки (120°С или 140°С в течение 15 секунд) получались нереплицирующиеся бактерии, обладающие противовоспалительными иммуногенными свойствами (фигуры 1, 2, 3 и 4). Штаммы, подвергнутые UHT-обработке (140°С, 15 с), индуцировали менее интенсивную секрецию провоспалительных цитокинов (TNF-α, IFN-γ, IL-12p40), в то же время поддерживая или индуцируя дополнительное (по сравнению с соответствующими живыми препаратами) образование IL-10. В результате для всех штаммов, прошедших обработку UHT, значения отношения IL-12p40/IL-10 были ниже, чем для живых клеток (фигуры 1, 2, 3 и 4). Это наблюдение справедливо также для бактерий, прошедших обработку HTST, а именно воздействие температуры 120°С в течение 15 с (фигуры 1, 2, 3 и 4) либо 74°С и 90°С в течение 15 с (фигура 5). Различные тепловые обработки (UHT или HTST) оказывали сходное влияние на иммуногенные свойства in vitro пробиотических штаммов (фигуры 1, 2, 3 и 5) и заквасочных культур для молочной продукции (фигура 4). Анализ методом главных компонент результатов изменений секреции цитокинов клетками РВМС под влиянием живых и прошедших тепловую обработку (140°С, 15 с) пробиотических штаммов и заквасочных культур для молочной продукции показал, что все живые штаммы распределяются по шкале «х» (фигура 6); это показывает, что in vitro бактерии индуцируют секрецию провоспалительных цитокинов в очень разной степени - от низкой (левая сторона) до высокой (правая сторона). На этом графике штаммы, прошедшие тепловую обработку, группируются слева, что демонстрирует более слабую индукцию провоспалительных цитокинов. Напротив, бактерии, подвергнутые воздействию температуры 85°С в течение 20 минут, индуцировали секрецию больших количеств провоспалительных цитокинов и меньших - IL-10, чем живые клетки; в результате наблюдались более высокие значения отношения IL-12p40/IL-10 (Фигура 7).
Противовоспалительные свойства усиливаются или создаются в результате обработки типа UHT и HTST.
Штаммы, прошедшие обработку UHT и HTST, проявляют противовоспалительные свойства независимо от соответственных исходных (живых клеток) иммуногенных свойств. Показано, что у пробиотических штаммов, обладающих противовоспалительными свойствами in vivo и проявляющих противовоспалительные свойства in vitro (В. longum NCC 3001, В. longum NCC 2705, В. breve NCC 2950, В. lactis NCC 2818), после кратковременной высокотемпературной обработки противовоспалительные свойства in vitro усиливались. Как иллюстрирует фигура 1, для штаммов Bifidobacterium, прошедших обработку UHT, отношение IL-12p40/IL-10 было ниже, чем для соответствующих живых клеток; это демонстрирует улучшение противовоспалительных свойств образцов, подвергнутых обработке UHT. Еще более примечательно, что подтвердилось также возникновение противовоспалительных свойств в результате обработки UHT и HTST у не обладавших противовоспалительными свойствами живых штаммов. Для живых клеток L. rhamnosus NCC 4007 и L, paracasei NCC 2461 наблюдалось высокое отношение IL-12p40/IL-10 in vitro (фигуры 2 и 5). Было показано, что у мышей эти два штамма не защищают от колита, индуцируемого TNBS, Для L, rhamnosus NCC 4007 и L. paracasei NCC 2461 отношение IL-12p40/IL-10 значительно снижалось после кратковременной высокотемпературной обработки (UHT или HTST), достигая такого же низкого уровня, как в случае штаммов Bifidobacterium. Эти низкие значения отношения IL-12p40/IL-10 обусловлены низким уровнем секреции IL-12р40 в сочетании с неизменной (L.rhamnosus NCC 4007) или существенно более высокой степенью индукции секреции IL-10 (L.paracasei NCC 2461) (фигура 2).
Следовательно:
- Противовоспалительные свойства живых микроорганизмов могут быть усилены тепловой обработкой типа UHT и HTST (например, В. longum NCC 2705, В. longum NCC 3001, В. breve NCC 2950, В. lactis NCC 2818);
- Противовоспалительные свойства могут возникнуть у живых микроорганизмов, не обладавших противовоспалительным эффектом (например, L.rhamnosus NCC 4007, L.paracasei NCC 2461, заквасочные культуры S.thermophilus NCC 2019) в результате тепловой обработки типа UHT и HTST;
- Противовоспалительные свойства также продемонстрированы у штаммов, выделенных из имеющихся в продаже продуктов (фигуры 3А и В), включая пробиотический штамм Е.coli.
Влияние обработки типа UHT/HTST было сходным для всех испытанных пробиотиков и заквасочных культур для молочной продукции, например лактобацилл, бифидобактерий и стрептококков.
Обработку типа UHT/HTST применяли к ряду лактобацилл, бифидобактерий и стрептококков, проявляющих различные иммуногенные свойства in vitro. После обработки типа UHT/HTST все штаммы индуцировали меньшую секрецию провоспалительных цитокинов, чем соответствующие живые клетки (фигуры 1, 2, 3, 4, 5 и 6); это демонстрирует, что влияние обработки типа UHT/HTST на иммуногенные свойства получающихся нереплицирующихся бактерий может быть отнесено ко всем пробиотикам, в частности к лактобациллам и бифидобактериям, а также к определенным штаммам Е.coli и ко всем заквасочным культурам для молочной продукции, в частности к стрептококкам, лактококкам и лактобациллам.

Настоящее изобретение относится к микробиологии, а именно к области использования бактерий, и описывает композицию, содержащую микроорганизмы, способ получения пробиотиков с противовоспалительным действием и способ получения противовоспалительной композиции, содержащей пробиотики. Композиция по изобретению характеризуется содержанием микроорганизмов, подвергнутых кратковременной высокотемпературной обработке при 120-140°С в течение 5-15 секунд. Изобретение может быть использовано для получения композиций для лечения или предотвращения воспалительных расстройств, для получения пробиотиков для молочной продукции. 3 н. и 7 з.п. ф-лы, 7 ил.
1. Композиция для профилактики или лечения воспалительных расстройств, содержащая микроорганизмы, подвергнутые высокотемпературной обработке при 120-140°С в течение короткого периода времени 5-15 секунд, в которой микроорганизмы выбирают из группы, состоящей из пробиотиков, заквасок молочных культур или их сочетаний, где пробиотики и/или закваски молочных культур выбирают из группы, состоящей из Bifidobacterium longum NCC 3001, Bifidobacterium longum NCC 2705, Bifidobacterium breve NCC 2950, Bifidobacterium lactis NCC 2818, Lactobacillus paracasei NCC 2461, Lactobacillus rhamnosus NCC 4007, Streptococcus thermophilus NCC 2019, Streptococcus thermophilus NCC 2059, Lactobacillus casei NCC 4006, Lactobacillus casei ACA-DC 6002 (NCC 1825), Lactobacillus acidophilus NCC 3009, Escherichia coli Nissle, Lactobacillus bulgaricus NCC 15, Lactococcus lactis NCC 2287 или их комбинаций.
2. Композиция по п. 1, в которой по меньшей мере 90%, предпочтительно по меньшей мере 95%, более предпочтительно по меньшей мере 98%, наиболее предпочтительно по меньшей мере 99%, лучше всего по меньшей мере 99,9%, в идеале все пробиотические клетки и/или клетки заквасок молочных культур являются нереплицирующимися.
3. Композиция по п. 1, которая может быть введена в организм перорально, энтерально, парентерально, например подкожно или внутримышечно, интравагинально, интраректально, местно или интраокулярно.
4. Композиция по любому из пп. 1-3, предназначенная для людей или домашних питомцев.
5. Композиция по п. 2, в которой содержится от около 0,005 мг до около 1000 мг нереплицирующихся микроорганизмов на суточную дозу.
6. Композиция по п. 1, в которой воспалительное расстройство выбирают из группы, состоящей из острых воспалительных состояний, как, например, сепсис; ожогов; хронических воспалительных процессов, как, например, воспалительные заболевания кишечника (например, болезнь Крона, язвенный колит, паучит); некротизирующего колита; синдрома раздраженного кишечника; воспалительных поражений кожи, как, например, воспаление, вызванное воздействием ультрафиолетового излучения или химических веществ, экземы, аллергического воспаления кожи; воспалительных процессов в глазах; аллергии, астмы; воспалительных процессов, связанных с ожирением; неспецифических воспалительных процессов, связанных со старением, и их сочетаний.
7. Способ получения пробиотиков и/или заквасок молочных культур с противовоспалительным действием или для усиления противовоспалительного действия пробиотиков и/или заквасок молочных культур, включающий стадию подвергания пробиотиков и/или заквасок молочных культур высокотемпературной обработке при 120-140°С в течение короткого периода времени 5-15 секунд, в котором пробиотики и/или закваски молочных культур выбирают из группы, состоящей из Bifidobacterium longum NCC 3001, Bifidobacterium longum NCC 2705, Bifidobacterium breve NCC 2950, Bifidobacterium lactis NCC 2818, Lactobacillus paracasei NCC 2461, Lactobacillus rhamnosus NCC 4007, Streptococcus thermophilus NCC 2019, Streptococcus thermophilus NCC 2059, Lactobacillus casei NCC 4006, Lactobacillus casei ACA-DC 6002 (NCC 1825), Lactobacillus acidophilus NCC 3009, Escherichia coli Nissle, Lactobacillus bulgaricus NCC 15, Lactococcus lactis NCC 2287 или их комбинаций.
8. Способ по п. 7, в котором кратковременная высокотемпературная обработка приводит к превращению по меньшей мере 90%, предпочтительно по меньшей мере 95%, более предпочтительно по меньшей мере 98%, наиболее предпочтительно по меньшей мере 99%, лучше всего по меньшей мере 99,9%, в идеале всех пробиотических клеток и/или клеток заквасок молочных культур в нереплицирующиеся.
9. Способ получения композиции, содержащей пробиотики и/или закваски молочных культур, обладающих противовоспалительными свойствами, или для улучшения уже имеющихся противовоспалительных свойств, включающий стадию подвергания пробиотиков и/или заквасок молочных культур высокотемпературной обработке при 120-140°С в течение короткого периода времени 5-15 секунд, в котором пробиотики и/или закваски молочных культур выбирают из группы, состоящей из Bifidobacterium longum NCC 3001, Bifidobacterium longum NCC 2705, Bifidobacterium breve NCC 2950, Bifidobacterium lactis NCC 2818, Lactobacillus paracasei NCC 2461, Lactobacillus rhamnosus NCC 4007, Streptococcus thermophilus NCC 2019, Streptococcus thermophilus NCC 2059, Lactobacillus casei NCC 4006, Lactobacillus casei ACA-DC 6002 (NCC 1825), Lactobacillus acidophilus NCC 3009, Escherichia coli Nissle, Lactobacillus bulgaricus NCC 15, Lactococcus lactis NCC 2287 или их комбинаций.
10. Способ по п. 9, который предусматривает добавление жизнеспособных пробиотиков и/или заквасок молочных культур в композицию и подвергание композиции, содержащей пробиотики и/или закваски молочных культур, кратковременной высокотемпературной обработке при 120-140°С в течение 5-15 секунд.
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
Авторы
Даты
2015-02-20—Публикация
2010-05-07—Подача