Группа изобретений относится к области химической технологии кремнийорганических соединений и может найти промышленное применение при получении новых функциональных материалов, обладающих люминесцентными свойствами. Более конкретно, изобретение относится к новым разветвленным олигоарилсиланам с реакционно-способными концевыми группами и способу их получения.
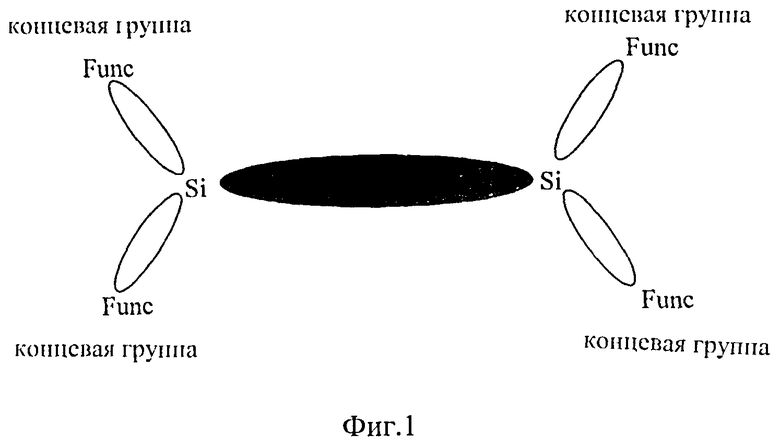
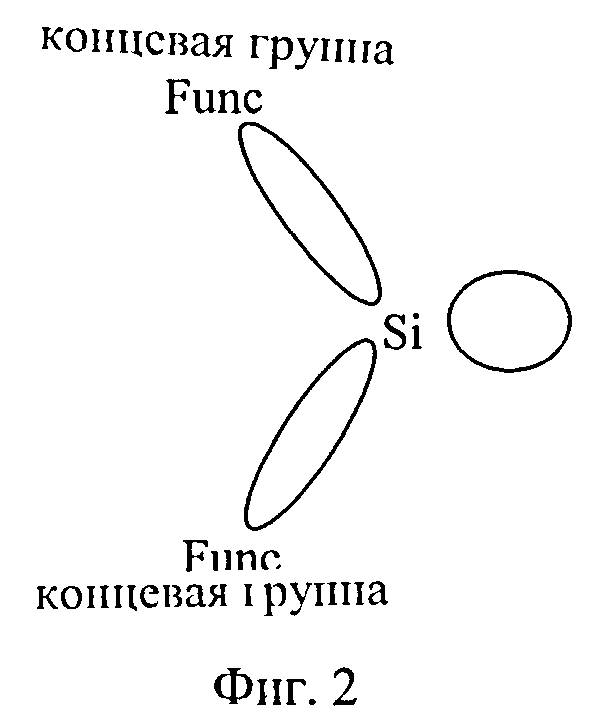
Под разветвленными олигоарилсиланами с реакционно-способными концевыми группами в рамках данного изобретения следует понимать такие олигоарилсиланы, которые представляют собой высокоупорядоченные пространственно сверхразветвленные полностью ациклические образования, имеющие реакционно-способные группы на периферии молекулы (Фиг. 1). В данном изобретении такие молекулы получают постадийно. Для этого сначала получают "ветви", которые называются монодендронами и содержат одну функциональную группу в фокальной точке и одну или несколько реакционно-способных групп на периферии (Фиг.2). Полученные монодендроны присоединяют к дифункциональному ариленовому или гетероариленовому центру с образованием олигоарилсиланов. При этом исходные монодендроны могут быть получены как конвергентным, так и дивергентным методом.
В отличие от классических полимеров, разветвленные олигоарилсиланы с реакционно-способными концевыми группами, в рамках данного изобретения, являются индивидуальными соединениями, что позволяет их выделять с чистотой, доступной для низкомолекулярных соединений. Это особенно важно для органической электроники и фотоники. Специфическая трехмерная архитектура таких макромолекул придает им также ряд ценных свойств, таких как хорошая растворимость и пленкообразование, в сочетании с возможностью регулировать их оптические и электрические характеристики за счет направленного молекулярного дизайна.
Под арилсиланами в данном изобретении понимаются соединения, имеющие непосредственную связь кремний-арил или кремний-гетероарил. Известны линейные и разветвленные арилсиланы, а также линейные и разветвленные полимеры на их основе с арилсилановыми фрагментами в основной цепи или в качестве боковых заместителей.
Разветвленные олигоарилсиланы, описываемые в рамках данного изобретения, близки по строению к органическим дендримерам. Органические светоизлучающие дендримеры и устройства на их основе известны, например, из Европейского патента ЕР 1027398 В1, патентов США US 6,558,818 В1 и US 6,720,093 B2. Используемые дендримеры могут содержать и силиконовые фрагменты, и гетероариленовые. Однако синтез дендримеров трудоемкий и затратный процесс.
Описан разветвленный олигоарилсилан, имеющий следующую структурную формулу (Adv. Funct. Mater. 2005.15.1799-1805):
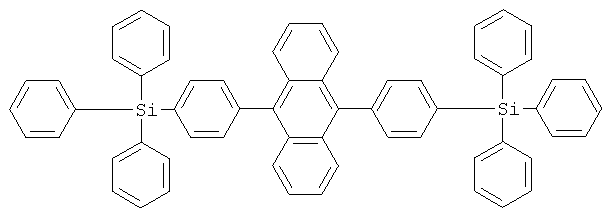
Этот разветвленный олигоарилсилан, в отличие от заявленных олигоарилсиланов, содержит четыре фенильных фрагмента, присоединенных к атому кремния. Известно, что синтез четырехзамещенных арилсиланов затруднен. В рамках данного изобретения заявляются молекулы, содержащие трехзамещенные арилсиланы, что значительно упрощает получение таких молекул.
Наиболее близким по строению к заявляемым разветвленным олигоарилсиланам с реакционно-способными концевыми группами являются олигоарилсиланы следующей общей формулы (Патент RU 2396290):
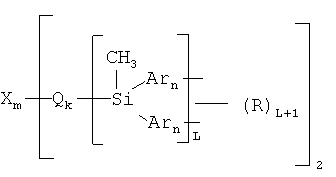
Эти олигоарилсиланы имеют в качестве R заместители из ряда: линейные или разветвленные C1-С20 алкильные группы; линейные или разветвленные C1-C20 алкильные группы, разделенные по крайней мере одним атомом кислорода; линейные или разветвленные C1-C20 алкильные группы, разделенные по крайней мере одним атомом серы; разветвленные С3-С20 алкильные группы, разделенные по крайней мере одним атомом кремния; С2-С20 алкенильные группы. В отличие от известных олигоарилсиланов в рамках данного изобретения заявляются химические структуры, у которых в качестве R включен атом кремния с различными заместителями, причем одним из них обязательно является заместитель из ряда: винил, 3-пропен-1-ил, 4-бутен-1-ил, 5-пентен-1-ил, 6-гексен-1-ил, 8-октен-1-ил, 11-ундецен-1-ил. Наличие реакционно-способных групп на периферии молекул позволяет их встраивать в полимерные цепи, а следовательно, придавать полимерным материалам новые оптические свойства.
Задачей заявляемого изобретения является получение нового технического результата, заключающегося в синтезе новых разветвленных олигоарилсиланов с реакционно-способными концевыми группами, содержащих как минимум пять функциональных арилсилановых звеньев, обладающих набором свойств, благодаря чему их можно использовать в качестве люминесцентных материалов для органической электроники и фотоники. К таким свойствам, в рамках данного изобретения, следует отнести: высокую эффективность люминесценции, эффективный внутримолекулярный перенос энергии с одних фрагментов молекулы на другие и повышенную термостабильность.
Кроме того, задачей изобретения является разработка нового способа получения заявленных разветвленных олигоарилсиланов с реакционно-способными концевыми группами, позволяющего получить продукты заданного строения высокой чистоты и пригодного к применению в промышленных условиях.
Задача решается тем, что получены новые разветвленные олигоарилсиланы с реакционно-способными концевыми группами общей формулы (I)
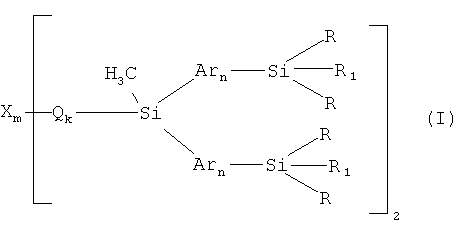
где R означает одинаковые или различные заместители из ряда: линейные или разветвленные C1-C20 алкильные группы; С2-С20 алкенильные группы;
R1 означает заместитель из ряда: винил, 3-пропен-1-ил, 4-бутен-1-ил, 5-пентен-1-ил, 6-гексен-1-ил, 8-октен-1-ил, 11-ундецен-1-ил;
Ar означает одинаковые или различные ариленовые или гетероариленовые радикалы, выбранные из ряда: замещенный или незамещенный тиенил-2,5-диил общей
формулы (II-a) 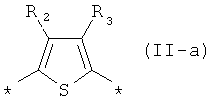 , замещенный или незамещенный фенил-1,4-диил общей формулы (II-б)
, замещенный или незамещенный фенил-1,4-диил общей формулы (II-б) 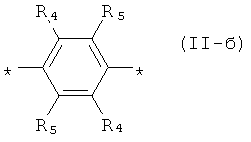 , замещенный или незамещенный 1,3-оксазол- 2,5-диил общей формулы (II-в)
, замещенный или незамещенный 1,3-оксазол- 2,5-диил общей формулы (II-в) 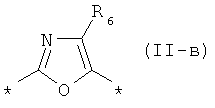 , где R2, R3, R4, R5, R6, независимо друг от друга означают Н или заместитель из вышеуказанного ряда для R,Q означает радикал из вышеуказанного ряда для Ar;
, где R2, R3, R4, R5, R6, независимо друг от друга означают Н или заместитель из вышеуказанного ряда для R,Q означает радикал из вышеуказанного ряда для Ar;
Х означает по крайней мере один радикал, выбранный из вышеуказанного ряда для Ar и/или радикал из ряда: 2,1,3-бензотиодиазол-4,7-диил общей формулы (II-г) 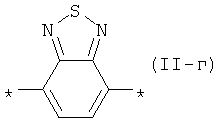 , антрацен-9,10-диил формулы (II-д)
, антрацен-9,10-диил формулы (II-д) 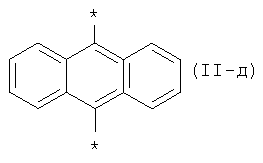 , 1,3,4-оксадиазол-2,5-диил общей формулы (II-е)
, 1,3,4-оксадиазол-2,5-диил общей формулы (II-е) 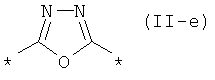 , 1-фенил-2-пиразолин-3,5-диил общей формулы (II-ж)
, 1-фенил-2-пиразолин-3,5-диил общей формулы (II-ж) 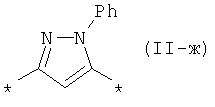 , перилен-3,10-диил общей формулы (II-з)
, перилен-3,10-диил общей формулы (II-з)
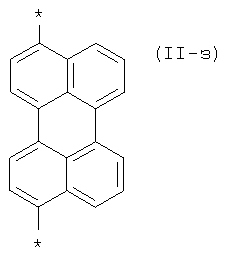
n означает целое число из ряда от 2 до 4;
m означает целое число из ряда от 1 до 3;
k означает целое число из ряда от 1 до 3.
Следует отметить, что атомы кремния является точками разрыва сопряжения (Organometallics 2007, 26, 5165-5173) как между внутренней и внешней частью молекулы, так и между отдельными фрагментами, из которых состоит внешняя часть молекулы. При этом длина сопряжения олигоарилсиланового фрагмента во внутренней части молекулы больше длины сопряжения любого из олигоарилсилановых фрагментов во внешней части молекулы, что обеспечивает эффективный перенос энергии с внешней на внутреннюю часть молекулы. Для осуществления такого эффективного переноса энергии необходимо, чтобы спектр люминесценции олигоарилсилановых фрагментов внешней части молекулы хорошо перекрывался со спектром поглощения олигоарилсиланового фрагмента внутренней части.
Положения, отмеченные в формулах (II-a) - (II-з) знаком * (звездочка) являются точками соединения, в которых структурные фрагменты (II-a) - (II-з) связаны друг с другом в форме линейных сопряженных олигомерных цепей Arn (или Xm или Qk) или концами цепей Arn (или Qk), связанных с атомами кремния в точках ветвления или концами цепей Arn, связанных с концевыми заместителями R и R1.
Схематичное изображение разветвленных олигоарилсиланов с реакционно-способными концевыми группами представлено на Фиг.1, где закрашенным овалом обозначена внутренняя часть молекулы, а незакрашенными овалами - внешние люминофоры. Предпочтительными значениями для R являются линейные или разветвленные C1-C20 алкильные группы, например, метил, этил, н-пропил, изо-пропил, н-бутил, m-бутил, изо-бутил, втор-бугил, н-пентил, 1-метилбутил, 2-метилбутил, 3-метилбутил, 1-этилпропил, 1,1-диметилпропил, 2,2-диметилпропил, н-гексил, н-гептил, н-октил, 2-этилгексил, н-нонил, н-децил, н-ундецил, н-додецил. Наиболее предпочтительные значения R: метил, этил, н-гексил.
Предпочтительными значениями R1 являются линейные С2-С20 алкенильные группы, например, винил, 3-пропен-1-ил, 4-бутен-1-ил, 5-пентен-1-ил, 6-гексен-1-ил, 8-октен-1-ил, 11-ундецен-1-ил. Наиболее предпочтительные значения R1: винил, 6-гексен-1-ил и 11-ундецен-1-ил.
Предпочтительными значениями Ar являются: незамещенный тиенил-2,5-диил общей формулы (II-а), где R1=R2=Н; замещенный тиенил-2,5-диил общей формулы (II-а), где R1=Н, в частности, 3-метилтиенил-2,5-диил, 3-этилтиенил-2,5-диил, 3-пропилтиенил-2,5-диил, 3-бутилтиенил-2,5-диил, 3-пентилтиенил-2,5-диил, 3-гексилтиенил-2,5-диил, 3-(2-этилгексил)тиенил-2,5-диил; незамещенный фенил-1,4-диил общей формулы (II-б), где R3=R4=Н; замещенный фенил-1,4-диил общей формулы (II-б), где R3=Н, в частности, (2,5-диметил)фенил-1,4-диил, (2,5-диэтил)фенил-1,4-диил, (2,5-дипропил)фенил-1,4-диил, (2,5-дибутил)фенил-1,4-диил, (2,5-дипенил)фенил-1,4-диил, (2,5-дигексил)фенил-1,4-диил, 2,5-бис(2-этилгексил)фенил-1,4-диил, (2,5-диметокси)фенил-1,4-диил, (2,5-диэтокси)фенил-1,4-диил, (2,5-дипроокси)фенил-1,4-диил, (2,5-диизопроокси)фенил-1,4-диил, (2,5-дибутокси)фенил-1,4-диил, (2,5-дипентилокси)фенил-1,4-диил, (2,5-дигексилокси)фенил-1,4-диил, 2,5-бис(2-этилгексилокси)фенил-1,4-диил. Наиболее предпочтительные значения Ar: незамещенный тиенил-2,5-диил и незамещенный фенил-1,4-диил.
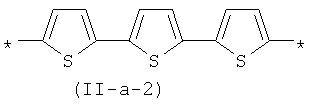
В контексте данного изобретения под Arn понимается любое сочетание из n звеньев одинаковых или различных Ar, выбранных из вышеприведенного ряда. Предпочтительными значениями такого сочетания являются n одинаковых незамещенных тиенил-2,5-диильных фрагментов, соединенных друг с другом в положениях 2 и 5, например, 2,2'-битиенил-2,5'-диил (II-a-1), 2,2':5',2"-тертиенил-2,5"-диил: 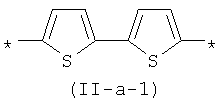
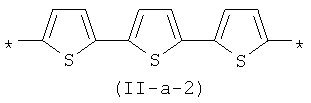
Другим предпочтительным значением такого сочетания являются комбинация различных незамещенных или 2,5-замещенных фенильных фрагментов, соединенных друг с другом в положениях 1 и 4, и различных незамещенных 1,3-оксазол-2,5-диильных фрагментов таким образом, что их общее количество равно n, например, при n, равном 2, формула (11-1), при n, равном 3, любая из формул (II-2) - (II-4):
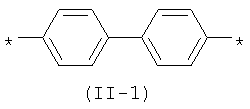
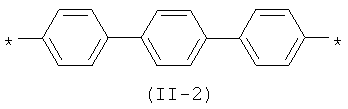
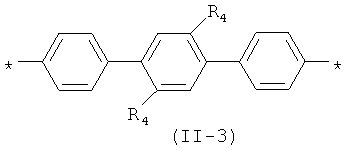
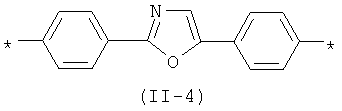
В контексте данного изобретения под Qk понимается любое сочетание из k звеньев одинаковых или различных Q, выбранных из вышеприведенного ряда. Предпочтительными значениями такого сочетания являются незамещенный тиенил-2,5-диил (II-а-3), незамещенный фенил-1,4-диил (II-б-1), k одинаковых незамещенных тиенил-2,5-диильных фрагментов, соединенных друг с другом в положениях 2 и 5, например, 2,2'-битиенил-2,5'-диил (II-a-1), 2,2':5',2"-тертиенил-2,5"-диил (II-a-2):
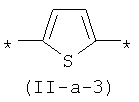
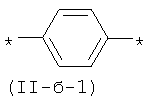
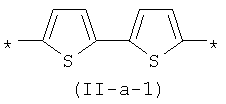
В контексте данного изобретения под Xm понимается любое сочетание из m звеньев одинаковых или различных X, выбранных из вышеприведенного ряда. Предпочтительными значениями таких звеньев являются незамещенный фенил-1,4-диил (II-б-1), незамещенный 1,3-оксазол-2,5-диил, незамещенный тиенил-2,5-диил (II-а-3), антрацен-9,10-диил (11-д), 1,3,4-оксадиазол-2,5-диил (II-е), 2,1,3-бензотиодиазол-4,7-диил.
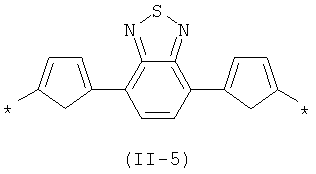
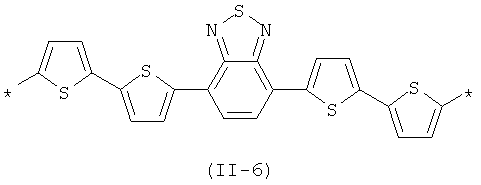
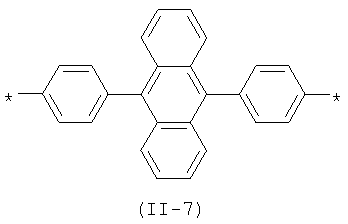
В контексте данного изобретения под Xm(Qk)2 понимается любое сочетание из m звеньев одинаковых или различных Х и k звеньев одинаковых или различных Q, выбранных из вышеприведенных рядов. Предпочтительными значениями сочетания таких звеньев являются: 2,1,3-бензотиодиазол-4,7-диилбис(тиен-2,5-диил) (11-5), 2,1,3-бензотиодиазол-4,7-диилбис(2,2'-битиен-5',5-диил) (11-6), антрацен-9,10-диилбис(фенилен-1,4-диил) (11-7), антрацен-9,10-диилбис(тиен-2,5-диил) (11-8), 2,2'-[1,4-фениленбис(1,3-оксазол-2,5-диилфенилен-4,1-диил (II-9):

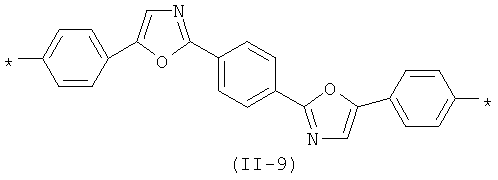
Положения, отмеченные в формулах (II-а-1) - (II-а-3) и (II-1) - (II-9) знаком * (звездочка) являются точками соединения, в которых структурные фрагменты (II-a) -(II-з) связаны друг с другом в форме линейных сопряженных олигомерных цепей Arn, Xm Qk или концами цепей Arn или Xm(Qk)2, связанных с атомами кремния в точках ветвления или с концевыми заместителями R и R1.
Представленные значения R, R1, Ar, Arn, Q, Qk, X, Xm являются частными случаями и не исчерпывают все возможные значения и все возможные сочетания n, m, k значений Ar, Q, X между собой.
В частности, в формуле (I) R может означать метил, тогда общая формула имеет следующий вид:
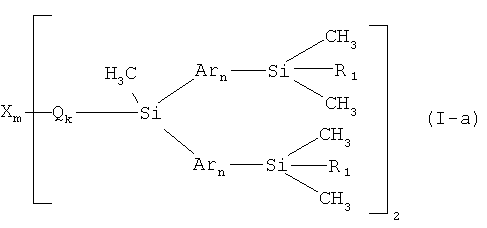
где X, Q, R1, n, m, k имеют вышеуказанные значения.
В частности, в формуле (I) R1 может означать винил, тогда общая формула имеет следующий вид:
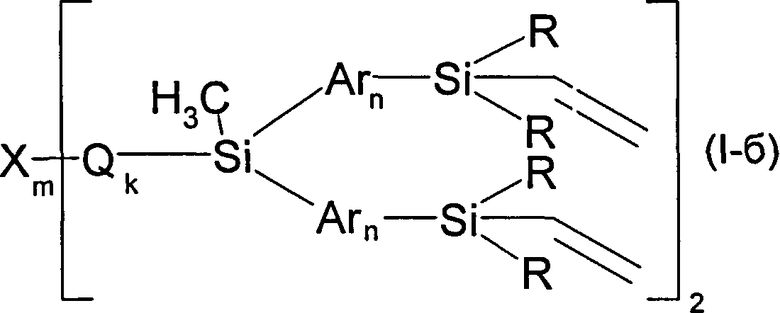
где X, Q, R, n, m, k имеют вышеуказанные значения.
В частности, в формуле (I) Ar может означать тиенил-2,5-диил, выбранный из ряда соединений формулы (II-а), тогда общая формула имеет следующий вид:
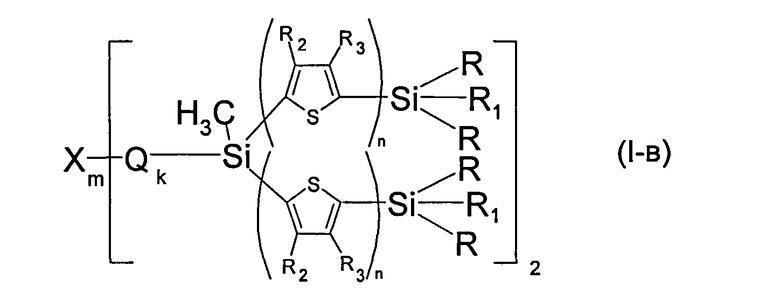
где X, Q, R, R1, R2, R3,n, m, k имеют вышеуказанные значения.
В частности, в формуле (I) Х может означать антрацен-9,10-диил (II-д), с условием, что Q означает фенил- 1,4-диил, выбранный из ряда соединений формулы (II-б), m равно 1, k равно 1, тогда общая формула имеет следующий вид:
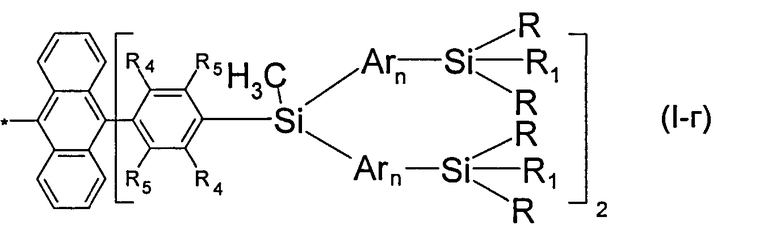
где Ar, R, R1, R4, R5, n имеют вышеуказанные значения.
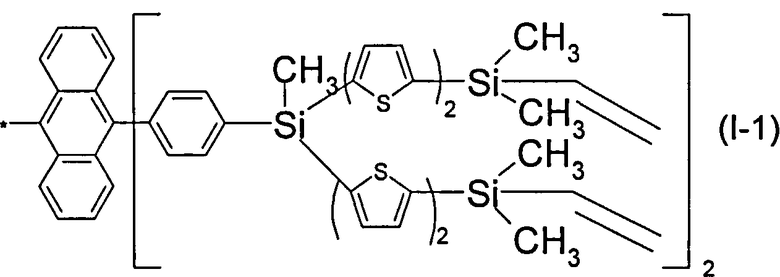
В этом случае, например, при Ar равно незамещенный тиенил-2,5-диил, R=СН3, R1=С2Н3, R3=R4=Н, n=2 реакционно-способный разветвленный олигоарилсилан с винильными концевыми группами (Фиг.3) может быть представлен формулой (I-1):
В частности, в формуле (I) X может означать 2,1,3-бензотиодиазол-4,7-диил (II-г), m равно 1, k равно 1, тогда общая формула имеет следующий вид:
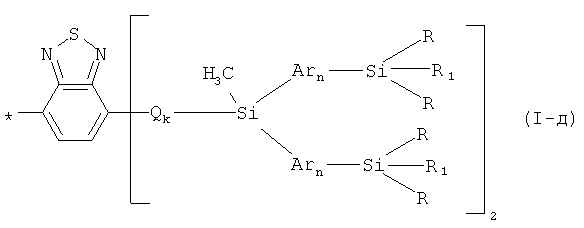
где Q, Ar, R, R1, n имеют вышеуказанные значения.
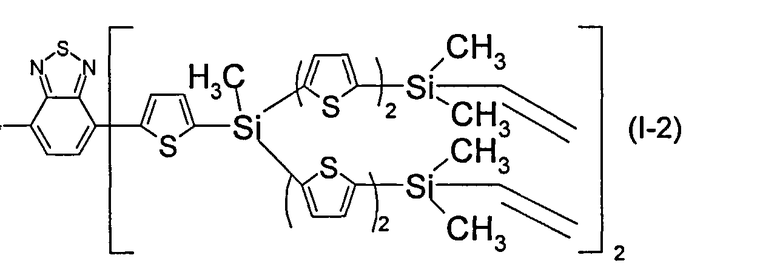
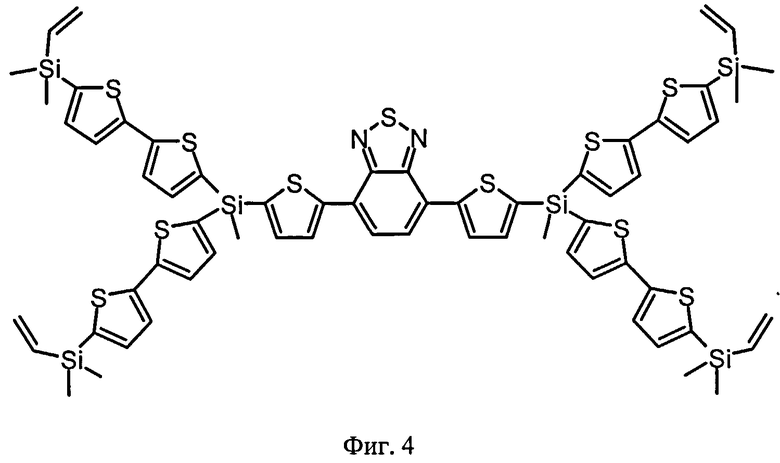
В этом случае, например, при Q равно Ar равно незамещенный тиенил-2,5-диил, R=СН3, R1=С2Н3, n=2 реакционно-способный разветвленный олигоарилсилан с винильными концевыми группами (Фиг.4) может быть представлен формулой (1-2):
В частности, в формуле (I) X может означать 2,1,3-бензотиодиазол-4,7-диил (II-г), m равно 1, k равно 2, тогда общая формула имеет следующий вид:
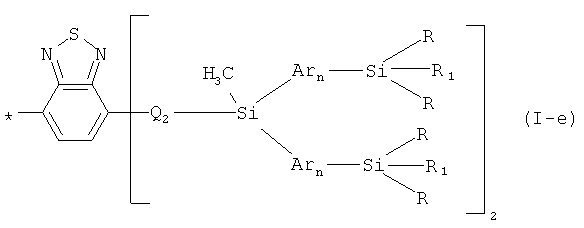
где Q, Ar, R, R1, R2, R3, n имеют вышеуказанные значения.
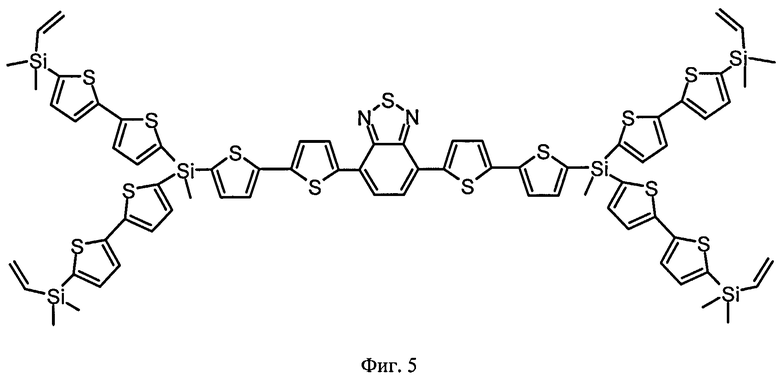
В этом случае, например, при Ar=незамещенный тиенил-2,5-диил, R=СН3, R1=С2Н3, R3=R4=Н, n=2 реакционно-способный разветвленный олигоарилсилан с винильными концевыми группами (Фиг.5) может быть представлен формулой (I-3):
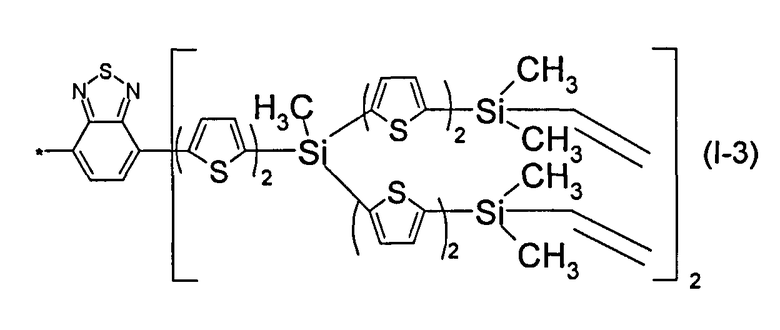
Заявленные разветвленные олигоарилсиланы с реакционно-способными концевыми группами содержат одинаковые или различные арил- или гетероарилсилановые группировки, обладающие эффективной люминесценцией. Это может быть проиллюстрировано спектрами поглощения и люминесценции их разбавленных растворов (см, например, Фиг.6, 7, 8). Оптические характеристики ряда разветвленных олигоарилсиланов с реакционно-способными концевыми группами представлены в таблице. Как видно из приведенных спектральных данных, заявленные разветвленные олигоарилсиланы обладают широким спектром поглощения, характеризующимся двумя максимумами, высоким квантовым выходом люминесценции и эффективным внутримолекулярным переносом энергии. Под высоким квантовым выходом в рамках данного изобретения понимается квантовый выход люминесценции в разбавленном растворе не менее 30%, преимущественно не менее 50%. Под эффективным внутримолекулярным переносом энергии понимается эффективность не менее 70%, преимущественно не менее 90%. Приведенные данные являются только примерами, и ни в коей мере не ограничивают характеристик заявленных разветвленных олигоарилсиланов.
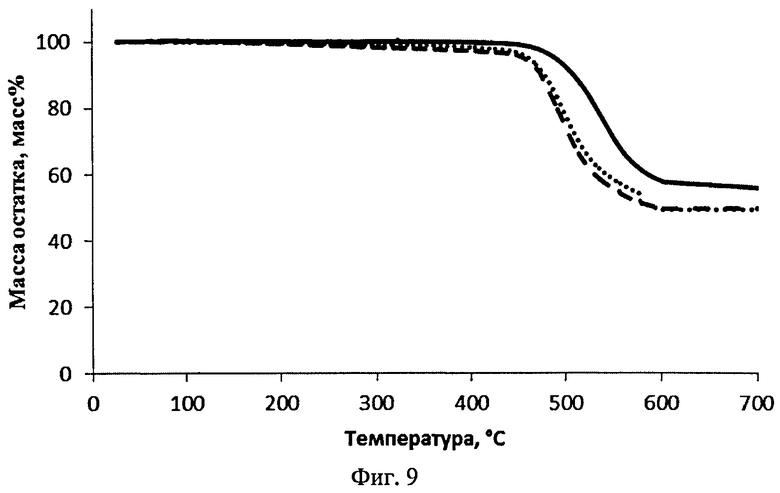
Отличительной особенностью заявленных олигоарилсиланов является их высокая термическая устойчивость, определяемая в рамках данного изобретения как температура 1% потери массы при нагревании вещества в аргоне. Данная температура для различных частных случаев составляет не менее 200°С, предпочтительно не менее 400°С. Данные термогравиметрического анализа (ТГА), иллюстрирующие высокую термостабильность заявленных олигоарилсиланов на примере соединений I-1 (пример 7), I-2 (пример 8) и 1-3(пример 9), соответственно, приведены на Фиг.9.
Задача решается также тем, что разработан способ получения разветвленных олигоарилсиланов с реакционно-способными концевыми группами общей формулы (I), заключающийся в том, что соединение общей формулы (III)
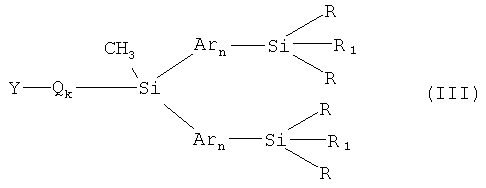
где Y означает остаток борной кислоты или ее эфира, или Br, или I, R, R1, Ar, Q, n, k имеют вышеуказанные значения, взаимодействуют в условиях реакции Сузуки с реагентом общей формулы (IV)
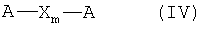 ,
,
где А означает
Br или I, при условии, что Y означает остаток борной кислоты или ее эфира,
или
остаток борной кислоты или ее эфира, при условии, что Y означает Br или I.
X, m имеют вышеуказанные значения.
Под реакцией Сузуки подразумевается взаимодействие арил- или гетероарилгалогенида с арил- или гетероарилборорганическим соединением (Suzuki, Chem. Rev. 1995. V.95. Р.2457-2483) в присутствие основания и катализатора, содержащего металл VIII подгруппы. Как известно, для данной реакции в качестве основания могут выступать любые доступные основания, такие как гидроксиды, например, NaOH, КОН, LiOH, Ba(OH)2, Са(ОН)2; алкоксиды, например, NaOEt, KOEt, LiOEt, NaOMe, KOMe, LiOMe; соли щелочных металлов угольной кислоты, например, карбонаты, гидрокарбонаты, ацетаты, цитраты, ацетилацетонаты, глицинаты натрия, калия, лития или карбонаты других металлов, например, Cs2CO3, Tl2CO3; фосфаты, например, фосфаты натрия, калия, лития. Предпочтительным основанием является карбонат натрия. Основания используются в виде водных растворов или суспензий в органических растворителях, таких как толуол, диоксан, этанол, диметилформамид или в их смесях. Предпочтительны водные растворы основания. Также в реакции Сузуки в качестве катализаторов могут использоваться любые подходящие соединения, содержащие металлы VIII подгруппы таблицы Менделеева. Предпочтительными металлами являются Pd, Ni, Pt. Наиболее предпочтительным металлом является Pd. Катализатор или катализаторы предпочтительно используются в количестве от 0,01 мол.% до 10 мол.%. Наиболее предпочтительное количество катализаторов от 0,5 мол.% до 5 мол.% по отношению к молярному количеству соединения с меньшей молярной массой, вступающего в реакцию. Наиболее доступными катализаторами являются комплексы металлов VIII подгруппы. В частности, стабильные на воздухе комплексы палладия (0), комплексы палладия, восстанавливающиеся непосредственно в реакционном сосуде металлоорганическими соединениями (алкил литиевыми или магнийорганическими соединениями) или фосфинами до палладия (0), такие как комплексы палладия (2) с трифенилфосфином или другими фосфинами. Например, PdCl2(PPh3)2, PdBr2(PPh3)2, Pd(OAc)2 или их смеси с трифенилфосфином. Предпочтительно использовать коммерчески доступный Pd(PPh3)4 с или без добавления донолшп ельных фосфипов. В качестве фосфинов предпочтительно использовать PPh3, PEtPh2, PMePh2, PEt2Ph, PEt3. Наиболее предпочтителен трифенилфосфин.
Общая схема процесса может быть представлена следующим образом:
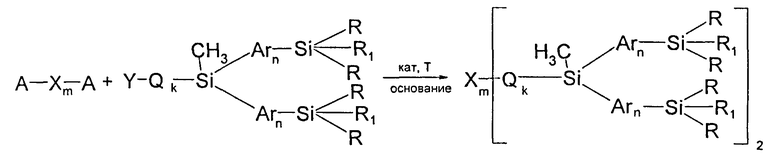
где А, X, Y, Q, Ar, R, R1, n, m n k имеют вышеуказанные значения.
В частности, Y в соединении формулы (III) может означать остаток циклического эфира борной кислоты - 4,4,5,5-тетраметил-1,3,2-диоксаборолан общей формулы (V) 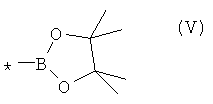 , тогда разветвленный олнгоарилснлан получают по следующей общей схеме:
, тогда разветвленный олнгоарилснлан получают по следующей общей схеме:
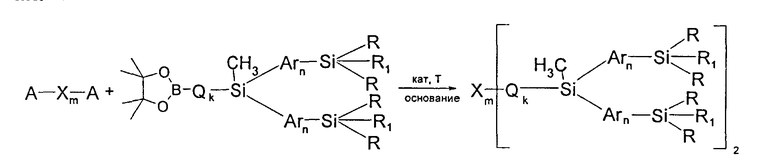
где А, X, Q, Ar, R, n, m, k и L имеют вышеуказанные значения, выбранный из ряда: 4,4,5,5-тетраметил-1,3,2-диоксаборолан общей формулы (V-a) 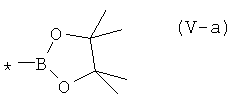 , 1,3,2-диоксаборолан общей формулы (V-б)
, 1,3,2-диоксаборолан общей формулы (V-б) 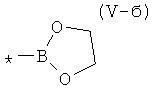 , 1,2,3-диоксаборинан обшей формулы (V-в)
, 1,2,3-диоксаборинан обшей формулы (V-в) 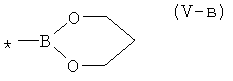 , 5,5-днметил-1,2,3-диоксаборннан общей формулы (V-г)
, 5,5-днметил-1,2,3-диоксаборннан общей формулы (V-г) 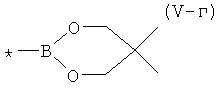
В частности, в соединении формулы (IV) Л может означать Br, тогда разветвленный олигоарплсилан получают по следующей общей схеме:

где X, Y, Q, Ar, R, R1, n, m и k имеют вышеуказанные значения.
В частности, в соединении формулы (IV) Х может означать антрацен-9,10-днил (II-д), с условием, что радикал Q означает фенил-1,4-диил, выбранный из ряда соединений формулы (II-б), m равно l,k равно 1, тогда разветвленный олнгоарилсилан получают по следующей общей схеме:
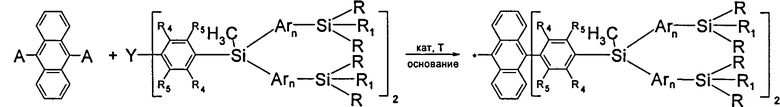
где A, Y, Ar, R, R1, R4, R5, n имеют вышеуказанные значения.
В частности, в соединении формулы (IV) Х может означать 2,1,3-бензотиодиазол-4,7-диил (II-г), с условием, что радикал Q означает незамещенный тиенил-2,5-диил, m равно 1, тогда разветвленный олигоарилсилан получают по следующей общей схеме:
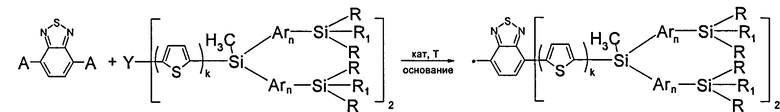
где А, Y, Ar, R, R1, n имеют вышеуказанные значения.
Вышеописанные взаимодействия можно проводить в органических растворителях или смесях растворителей, не взаимодействующих с реагирующими агентами. Например, реакцию можно проводить в среде органического растворителя, выбранного из ряда эфиров: тетрагидрофуран, диоксан, диметиловый эфир этиленгликоля, диэтиловый эфир этиленгликоля, диметиловый эфир диэтиленгликоля; или из ряда ароматических соединений: бензол, толуол, ксилол, или из ряда алканов: пентан, гексан, гептан, или из ряда спиртов: метанол, этанол, изопропанол, бутанол, или из ряда апротонных полярных растворителей: диметилформамид, диметилсульфоксид. Смесь из двух или более растворителей так же может быть использована. Наиболее предпочтительные растворители - толуол, тетрагидрофуран, этанол, диметилформамид или их смесь. При этом взаимодействие исходных компонентов может проходить при температуре в пределах от +20°С до +200°С при стехиометрическом мольном соотношении функциональных групп исходных компонентов либо избытка одного из них. Предпочтительно взаимодействие проводят при температуре в пределах от +40°С до +150°С. Наиболее предпочтительно взаимодействие проводят при температуре в пределах от +60°С до +120°С.
После окончания реакции продукт выделяют по известным методикам. Например, добавляют воду и органический растворитель. Органическую фазу отделяют, промывают водой до нейтральной реакции и высушивают, после чего растворитель упаривают. В качестве органического растворителя может быть использован любой не смешивающийся или ограниченно смешивающийся с водой растворитель, например, выбранный из ряда эфиров: диэтиловый эфир, метилтретбутиловый эфир, или выбранный из ряда ароматических соединений: бензол, толуол, ксилол, или выбранный из ряда хлорорганиченских соединений: дихлорметан, хлороформ, четыреххлористый углерод, хлорбензол. Также для выделения могут использоваться смеси органических растворителей. Выделение продукта можно производить и без применения органических растворителей, например, отгонкой растворителей из реакционной смеси, отделением продукта от водного слоя фильтрованием, центрифугированием или любым другим известным методом.
Очистку сырого продукта проводят любым известным методом, например препаративной хроматографией в адсорбционном или эксклюзионом режиме, перекристаллизацией, дробным осаждением, дробным растворением или их любой комбинацией.
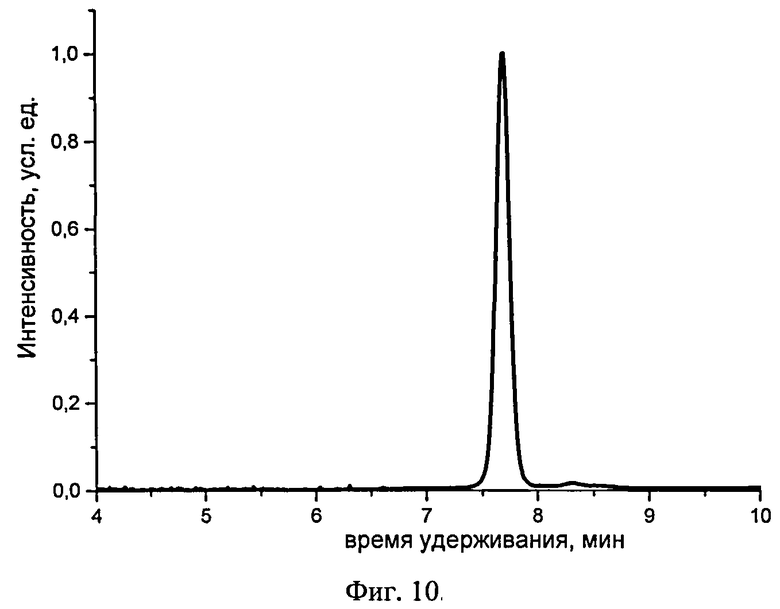
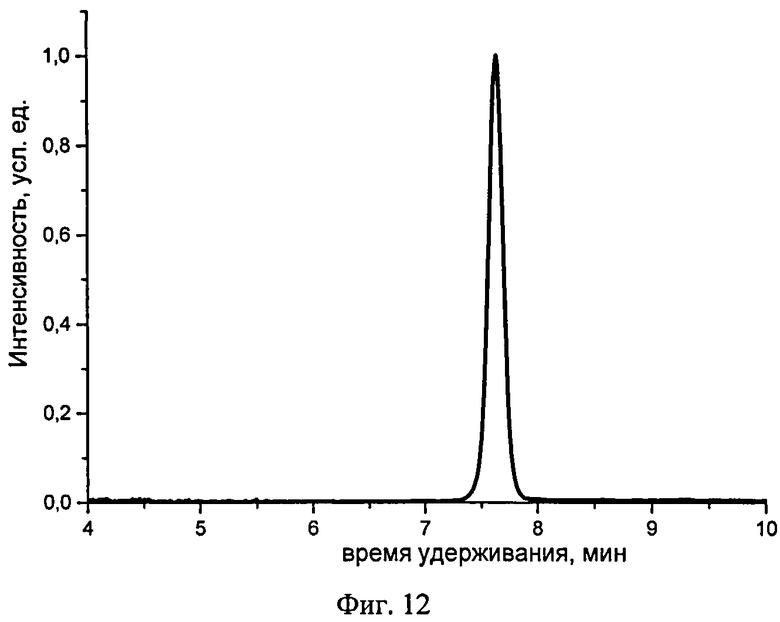
Чистоту и строение синтезированных соединений подтверждают совокупностью данных физико-химического анализа, хорошо известных специалистам, таких как хроматографические, спектроскопические, масс-спектроскопические, элементного анализа. Наиболее предпочтительным подтверждением чистоты и структуры разветвленных олигоарилсиланов с реакционно-способными концевыми группами являются ЯМР-спектры на ядрах 1Н, 13С и 29Si, а также ГПХ. Кривые ГПХ разветвленных олигоарилсиланов с реакционно-способными концевыми группами соответствуют узкому монодисперсному распределению по молекулярному весу (см., например. Фиг.10, Фиг.11, Фиг.12).
На Фиг.1 представлено схематическое изображение разветвленных олигоарилсиланов с реакционно-способными концевыми группами.
На Фиг.2 представлено схематическое изображение соединений общей формулы (III)
На Фиг.3 представлено схематическое изображение структурной формулы разветвленного олигоарилсилана с реакционно-способными концевыми группами I-1 (по примеру 7).
На Фиг.4. представлено схематическое изображение структурной формулы разветвленного олигоарилсилана с реакционно-способными концевыми группами I-2 (по примеру 8).
На Фиг.5 представлено схематическое изображение структурной формулы разветвленного олигоарилсилана с реакционно-способными концевыми группами I-3 (по примеру 9).
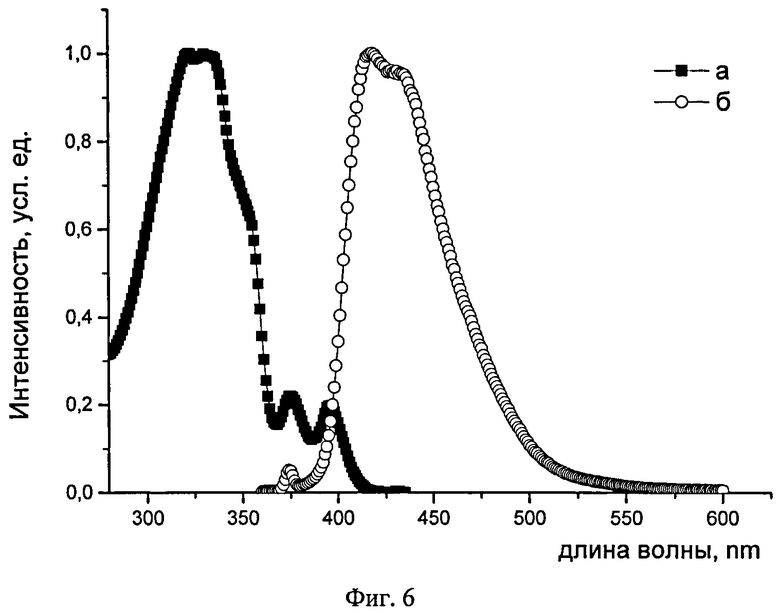
На Фиг.6 представлены спектры поглощения (а) и люминесценции (б) разбавленного раствора олигоарилсилана I-11 (по примеру 7) в ТГФ.
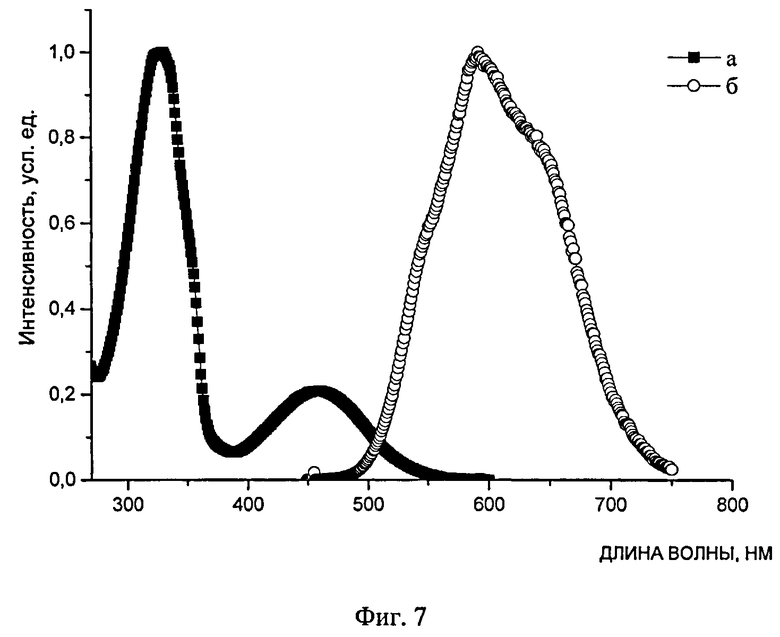
На Фиг.7 представлены спектры поглощения (а) и люминесценции (б) разбавленного раствора олигоарилсилана I-21 (по примеру 8) в ТГФ.
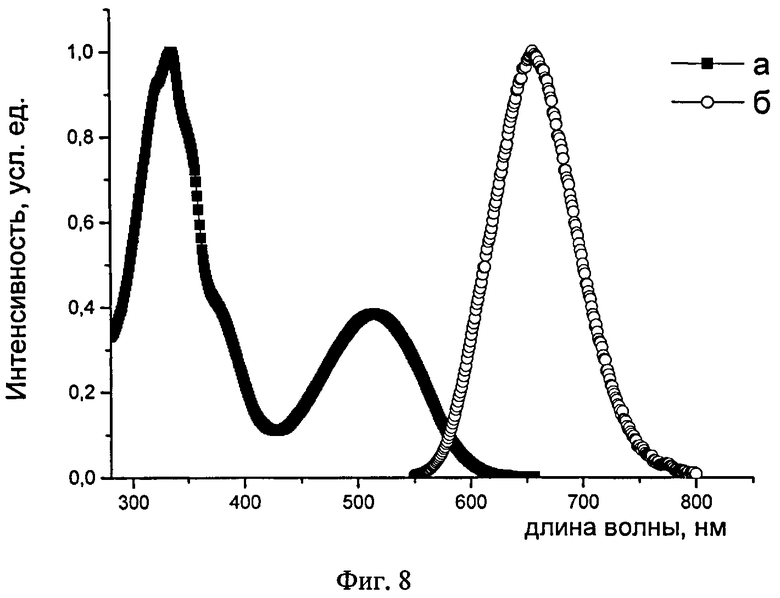
На Фиг.8 представлены спектры поглощения (а) и люминесценции (б) разбавленного раствора олигоарилсилана I-31 (по примеру 9) в ТГФ.
На Фиг.9 представлена ТГА кривые соединений по примерам 7, 8, 9 и их обозначение, соответственно: ―,…,----.
На Фиг.10 представлена ГПХ кривая чистого соединения I-1.
На Фиг.11 представлена ГПХ кривая чистого соединения I-2.
На Фиг.12 представлена ГПХ кривая чистого соединения I-3. В таблице приведены оптические свойства разветвленных олигоарилсиланов с реакционно-способными концевыми группами по примерам 7, 8, 9 в разбавленных растворах, в том числе максимумы спектров поглощения и люминесценции, квантовый выход люминесценции, характеризующий ее эффективность.
Изобретение может быть проиллюстрировано нижеприведенными примерами. При этом использовали коммерчески доступные реагенты и растворители. Исходные реагенты 4,7-дибром-2,1,3-бензотиадиазол и 4,7-бис(5-бромотиофен-2-ил)бензо-2,1,3-тиадиазол получали по известным методикам (Adv. mater. 2003. V.15(12). P.988-991). Другие исходные соединения получали согласно нижеприведенным примерам. Все реакции проводили в безводных растворителях в атмосфере аргона.
Синтез исходных реагентов
Пример 1. Синтез диметил-тиен-2-ил-винилсилана (VI)
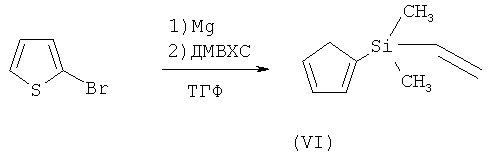
Раствор 29.69 мл (0.307 моль) 2-бром-тиофена в 500 мл сухого ТГФ добавили к суспензии 7.83 г (0.322 моль) магния в 30 мл ТГФ. Полученный реагент Гриньяра добавили к раствору 37 г (0.307 моль) диметидвинилхлорсилана при температуре ниже 0°С. Реакционную смесь перемешивали в течение четырех часов. Осадок отфильтровали, растворитель отогнали. Продукт очищали перегонкой (Ткип=185°С).
Выход: 38.20 г (74% от теоретически возможного). 1Н ЯМР (CDCI3, δ, м.д., J/Гц): 0.42 (с, 6Н), 5.84 (m, 2Н), 6.25 (m, 1Н), 7.23 (дд, 1Н, J1=3.7 Гц, J2=4.9 Гц), 7.31 (д, 1 Н, J=3.7 Гц),7.64(д,1Н, J=4.9 Гц).
Пример 2. Синтез метил-(2,2'-битиен-5-ил)дихлорсилана (VII)
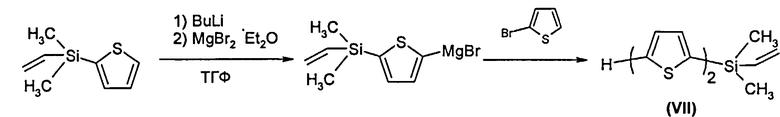
К раствору 20.00 г (0.12 моль) соединения VI в 200 мл ТГФ прибавили 67 мл (0.12 моль) 2.5 М раствора н-бутиллития в гексане при температуре -70°С. Реакционную смесь перемешивали в течение двух часов, после чего добавили раствор эфирного комплекса бромида магния, свежеприготовленного из 3.49 г (0.14 моль) магния и 24.55 г (0.13 моль) дибромэтана и 60 мл диэтилового эфира. Полученный таким образом реактив Гриньяра прибавили к раствору 19,37 г (0,12 ммоль) 2-бромотиофена и 450 мг (0,59 ммоль) Pd(dppf)Cl2 в 150 мл абсолютного ТГФ при температуре 0°С. После стандартного выделения реакции и очистки методом перегонки в вакууме (Ткип=112°С/0.25 мбар) получили 9.58 г (32% от теоретически возможного) соединения VII. 1Н ЯМР (CDCl3, δ, м.д., J/Гц): 0.42 (с, 6Н), 5.84 (m, 2Н), 6.25 (m, 1Н), 7.02 (дд, 1Н, J1=3.7 Гц, J2=5.5 Гц), 7.16 (д, 1 Н, J=3.7 Гц), 7.18-7.24 (перекрывающиеся сигналы, 2 Н), 7.26 (д,1Н, J=3.1 Гц).
Пример 3. Синтез (4-бромфенил)[бис(5'-[винил(диметил)силил]-2,2'-битиенил-5-ил)]метилсилана (III-1)

К раствору 2.4 г (9.6 ммоль) соединения VII в ТГФ добавили 3.8 мл (9.6 ммоль) 2.5 М раствора н-бутиллития в гексане при температуре -78°С. После чего добавили 1.29 г (4.7 ммоль) диметил-(4-бромфенил)хлорсилан. Через 15 минут перемешивания реакционной смеси при охлаждении реакционный выход составил 78% (по данным ГПХ). После стандартного выделения реакции и очистки методом колоночной хроматографии выход хроматографически чистого продукта составил 2.3 г (70% от теоретически возможного). ЯМР (CDC13, δ, м.д., J/Гц): 0.42 (с, 12Н), 0,92 (с.3Н), 5.84 (m, 4H), 6.25 (m, 2H), 7.15 (д, 2Н, J1=3.1 Гц), 7.23 (д, 2 Н, J=3.7 Гц), 7.27-7.30 (перекрывающиеся сигналы, 4 Н), 7.50 (дд, 4H, J1=12.8 Гц, J2=4.2 Гц).
Пример 4. Синтез (2-тиенил)[бис(5'-[винил(диметил)силил]-2,2'-битиенил-5-ил)]метилсилана (VIII)
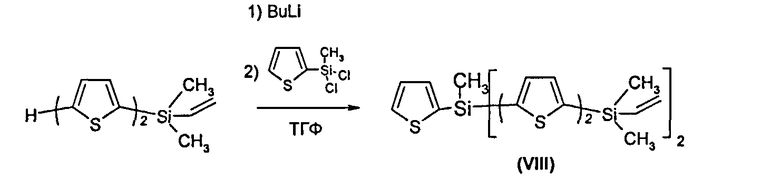
Соединение VIII получали аналогично методике синтеза соединения III-1 из 4.2 г (16.8 ммоль) соединения VII, 6.7 мл 2.5 М раствора н-бутиллития (16.8 ммоль) в гексане, 1.23 г (7.9 ммоль) метилтиенилдихлорсилана и 200 мл ТГФ. Через 50 минут перемешивания реакционной смеси реакционный выход составил 75% (по данным ГПХ). После выделения и очистки было получено 3.04 г (61% от теоретически возможного) хроматографически чистого соединения VIII. 1Н ЯМР (ДМСО-CCl4, δ, м.д., J/Гц): 0.37 (с, 12Н), 0.96 (с, 3Н), 5.86 (m, 4H), 6.28 (m, 2H), 7.25 (д, 2H, J1=3.7 Гц), 7.32 (дд, 1Н, J1=4.9 Гц, J2=3.7 Гц) 7.40 (д, 2 Н, J=3.7 Гц), 7.44 (д, 2 Н, J=3.7 Гц), 7.47 (д, 2 Н, J=3.7 Гц), 7.53 (д. 1 Н, J=3.1 Гц), 8.02 (д, 1 Н, J=4.9 Гц).
Пример 5. Синтез 2,2'-антрацен-9,10-диилбис (4,4,5,5-тетраметил-1,3,2-диоксиборолана) (IX)
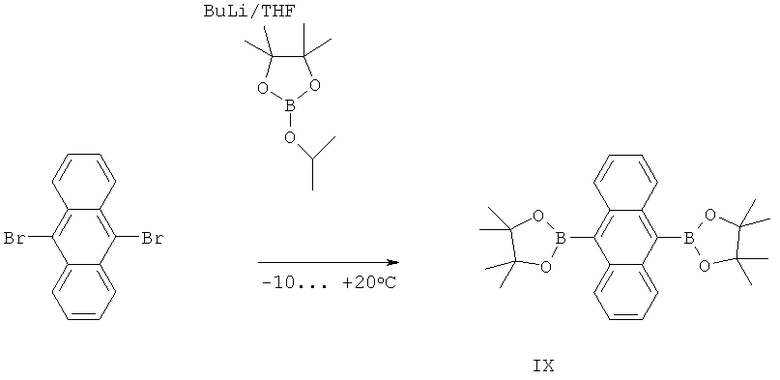
К раствору 1 г.9,10-дибромантрацена в 100 мл ТГФ прикапали 7.44 мл 1.6 М раствора ter-BuLi в гексане, поддерживая температуру ниже 0°С. Затем прибавляется 1.21 мл 2-изопропокси-4,4,5,5-тетраметил-1,3,2-диоксиборолан. Температура поднимается до комнатной и добавляется 200 мл дистиллированной воды, 300 мл диэтилового эфира и 2 мл 1N раствора НС1. После стандартного выделения реакции и очистки методом перекристаллизации выход чистого продукта составил 0.568 г (52% от теоретически возможного). 1Н ЯМР (250 МГц, δ в CDCl3, ТМС/м.д.): 1.59 (с, 24Н), 7.45 (дд, 4Н, J1=6.7 Гц, J2=3.1 Гц), 8.35 (дд, 4Н, J1=6.7 Гц, J2=3.1 Гц).
Пример 6. Синтез бис(5'-[винил(диметил)силил]-2,2'-битиенил-5-ил))(метил)[2-(4,4,5,5-тетраметил-1,3,2-диоксиборолан-2-ил)-тиен-5-ил]силана (III-2)
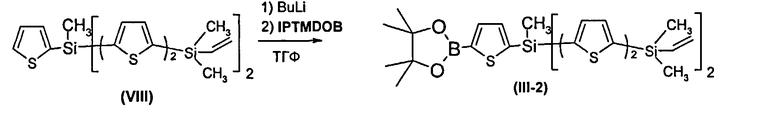
К раствору 2.65 г.соединения VIII в 40 мл ТГФ прикапали 1.8 мл 2.5 М раствора BuLi в гексане, поддерживая температуру ниже -70°С. Затем прибавляется 0.79 мл 2-изопропокси-4,4,5,5-тетраметил-1,3,2-диоксиборолан. Температура поднимается до комнатной и добавляется 200 мл дистиллированной воды, 300 мл диэтилового эфира и 4 мл IN раствора HCl. После стандартного выделения реакции выход 80%-ного продукта составил 3.08 г (97% от теоретически возможного). 1Н ЯМР (ДМСО-CCl4, δ, м.д., J/Гц): 0.38 (с, 12Н), 0.97 (с, 3Н), 1.28 (с, 12Н), 5.86 (m, 4Н), 6.28 (m, 2Н), 7.25 (д, 2Н, J1=3.7 Гц), 7.40 (д, 2 Н, J=3.7 Гц), 7.44 (д, 2 Н, J=3.7 Гц), 7.47 (д, 2 Н, J=3.7 Гц), 7.6 (д, 1 Н, J=3.1 Гц), 7.70 (д, 1 Н, J=3.1 Гц).
Синтез разветвленных олигоарилсиланов с реакционно-способными концевыми группами
Общая методика синтеза разветвленных олигоарилсиланов с реакционно-способными концевыми группами: к раствору 1.0 ммоль соединения III в толуоле прибавляют 0.45 ммоль соединения IV, 0.05 ммоль катализатора, содержащего металлы VIII подгруппы таблицы Менделеева, и 3.0 ммоль основания. Перемешивают в течение нескольких часов при температуре 80°С-120°С. После окончания реакции продукт выделяют по известным методикам. Продукт очищают методом колоночной хроматографии на силикагеле.
Пример 7. Синтез разветвленного олигоарилсилана с реакционно-способными концевыми группами (структура 1-1)
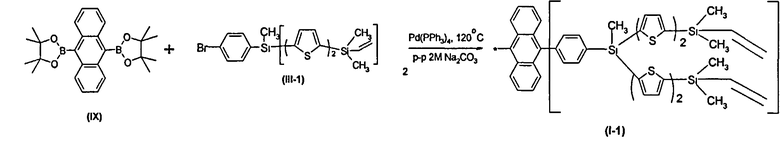
Разветвленный олигоарилсилан с реакционно-способными концевыми группами I-1 получали по общей методике синтеза из 1.6 г соединения III-1, 0.5 г соединения IX, 0.15 г катализатора Pd(PPh3)4, 2 мл 2М раствора Na2CO3 в воде и 20 мл толуола. После выделения и очистки было получено 0.18 г (15% от теоретически возможного) чистого разветвленного олигоарилсилана с реакционно-способными концевыми группами (I-1). ЯМР (CDCl3, δ, м.д., J/Гц): 0.41 (с, 24Н), 0,92 (с.6Н), 5.84 (m, 8H), 6.25 (m, 4H), 7.16 (д, 4Н, J1=3.7 Гц), 7. 32 (д, 4 Н, J=3.7 Гц), 7.35-7.40 (перекрывающиеся сигналы, 12 Н), 7.51 (д, 4 Н, J=7.9 Гц), 7.69 (д, 2Н, J=3.1), 7.72 (д, 2Н, J=3.1 Гц), 7.87 (д, 4H, J=7.9 Гц).
Пример 8. Синтез разветвленного олигоарилсилаиа с реакционно-способными концевыми группами (структура I-2)
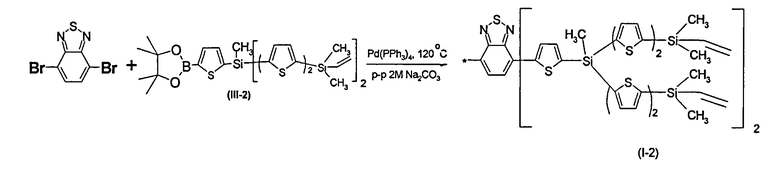
Разветвленный олигоарилсилан I-2 получали по общей методике синтеза из 1.4 г соединения III-1, 0.21 г 4,7-дибром-2,1,3-бензотиадиазола, 0.05 г катализатора Pd(PPh3)4, 2,5 мл 2М раствора Na2CO3 в воде и 20 мл толуола. После выделения и очистки было получено 0.185 г (19% от теоретически возможного) чистого разветвленного олигоарилсилана с реакционно-способными концевыми группами (I-2). 1Н ЯМР (250 МГц. δ в CDCl3, ТМС/м.д.): ЯМР (CDCl3, δ, м.д., J/Гц): 0.41 (с, 24Н), 1,02 (с.6Н), 5.84 (m, 8H), 6.25 (m, 4H), 7.16 (д, 4Н, J1=3.7 Гц). 7.28-7.40 (перекрывающиеся сигналы, 12 Н), 7.52 (д, 2 Н, J=3.7 Гц), 7.91 (с, 2Н), 8.24 (д, 2Н, J=3.7 Гц).
Пример 9. Синтез разветвленного олигоарилсилана с реакционно-способными концевыми группами (структура I-3)
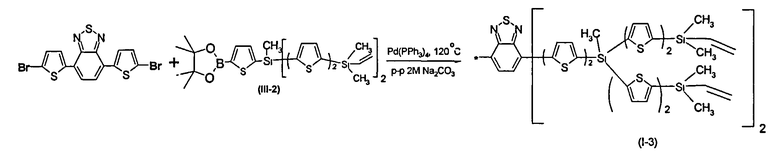
Разветвленный олигоарилсилан с реакционно-способными концевыми группами I-3 получали по общей методике синтеза из 1.27 г соединения III-2, 0.3 г 4,7-бис(5-бромотиофен-2-ил)бензо-2,1,3-тиадиазола, 0.05 г катализатора Pd(PPh3)4, 1 мл 2М раствора Na2CO3 в воде и 15 мл толуола. После выделения и очистки было получено 0.175 г (17% от теоретически возможного) чистого разветвленного олигоарилсилана (I-3). ЯМР (CDCl3, δ, м.д., J/Гц): 0.41 (с, 24Н), 1,02 (с.6Н), 5.84 (m, 8H), 6.25 (m, 4H), 7.16 (д, 4H, J1=3.7 Гц), 7.28-7.40 (перекрывающиеся сигналы, 16 Н), 7.42 (д, 2 Н, J=3.7 Гц), 7.86 (с, 2Н), 8.04 (д, 2Н, J=3.7 Гц).
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЕ РАЗВЕТВЛЕННЫЕ ОЛИГОАРИЛСИЛАНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2013 |
|
RU2524960C1 |
| РАЗВЕТВЛЕННЫЕ ОЛИГОАРИЛСИЛАНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2008 |
|
RU2396290C1 |
| Олигоарилсилановые люминофоры на основе бензотиадиазола и способ их получения | 2017 |
|
RU2671572C1 |
| РАЗВЕТВЛЕННЫЕ ОЛИГОАРИЛСИЛАНЫ НА ОСНОВЕ ТЕТРАФЕНИЛБУТАДИЕНА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2018 |
|
RU2716826C2 |
| Способ получения разветвленных олигоарилсиланов на основе фенилоксазолов | 2016 |
|
RU2620088C1 |
| ПОЛИАРИЛСИЛАНОВЫЕ ДЕНДРИМЕРЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2007 |
|
RU2353629C1 |
| ДЕНДРОНИЗОВАННЫЕ ПОЛИАРИЛСИЛАНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2010 |
|
RU2466156C2 |
| ФОТОЛЮМИНЕСЦЕНТНЫЙ ПОЛИМЕРНЫЙ СОЛНЕЧНЫЙ ФОТОЭЛЕМЕНТ | 2012 |
|
RU2528052C2 |
| ПОЛИАРИЛСИЛАНОВЫЕ МОНОДЕНДРОНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2007 |
|
RU2348657C1 |
| ОРГАНИЧЕСКИЕ СВЕТОИЗЛУЧАЮЩИЕ ДИОДЫ С БЕЛЫМ СПЕКТРОМ ИЗЛУЧЕНИЯ | 2013 |
|
RU2555193C2 |


Группа изобретений относится к разветвленным олигоарилсиланам с реакционноспособными концевыми группами и способу их получения. Предложены разветвленные олигоарилсиланы с реакционно-способными концевыми группами общей формулы (I), где R выбран из линейных или разветвленных C1-C20 алкильных групп; С2-С20 алкенильных групп; R1 означает винил, 3-пропен-1-ил, 4-бутен-1-ил, 5-пентен-1-ил, 6-гексен-1-ил, 8-октен-1-ил или 11-ундецен-1-ил; Ar означает одинаковые или различные ариленовые или гетероариленовые радикалы, выбранные из ряда: замещенный или незамещенный тиенил-2,5-диил, замещенный или незамещенный фенил-1,4-диил, замещенный или незамещенный 1,3-оксазол-2,5-диил, Q означает радикал из вышеуказанного ряда для Ar, Х означает по крайней мере один радикал, выбранный из вышеуказанного ряда для Ar и/или радикал из ряда: 2,1,3-бензотиодиазол-4,7-диил, антрацен-9,10-диил, 1,3,4-оксадиазол-2,5-диил, 1-фенил-2-пиразолин-3,5-диил, перилен-3,10-диил; n означает целое число от 2 до 4; m означает целое число от 1 до 3; k означает целое число от 1 до 3. Предложен также способ получения указанных олигоарилсиланов. Технический результат - возможность получения новых соединений, отличающихся высокой эффективностью люминесценции, эффективным внутримолекулярным переносом энергии с одних фрагментов молекулы на другие и повышенной термостабильностью. 2 н. и 18 з.п. ф-лы, 12 ил., 1 табл., 9 пр.

1. Разветвленные олигоарилсиланы с реакционно-способными концевыми группами общей формулы (I)
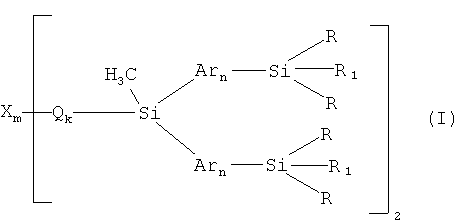
где R означает одинаковые или различные заместители из ряда: линейные или разветвленные C1-C20 алкильные группы; С2-С20 алкенильные группы;
R1 означает заместитель из ряда: винил, 3-пропен-1-ил, 4-бутен-1-ил, 5-пентен-1-ил, 6-гексен-1-ил, 8-октен-1-ил, 11-ундецен-1-ил;
Ar означает одинаковые или различные ариленовые или гетероариленовые радикалы, выбранные из ряда: замещенный или незамещенный тиенил-2,5-диил общей формулы (II-а)  , замещенный или незамещенный фенил-1,4-диил общей формулы (II-б)
, замещенный или незамещенный фенил-1,4-диил общей формулы (II-б)  , замещенный или незамещенный 1,3-оксазол-2,5-диил общей формулы (II-в)
, замещенный или незамещенный 1,3-оксазол-2,5-диил общей формулы (II-в)  , где R2, R3, R4, R5, R6, независимо друг от друга означают Н или заместитель из вышеуказанного ряда для R;
, где R2, R3, R4, R5, R6, независимо друг от друга означают Н или заместитель из вышеуказанного ряда для R;
Q означает радикал из вышеуказанного ряда для Ar;
Х означает по крайней мере один радикал, выбранный из вышеуказанного ряда для Ar и/или радикал из ряда: 2,1,3-бензотиодиазол-4,7-диил общей формулы (II-г)  , антрацен-9,10-диил формулы (II-д)
, антрацен-9,10-диил формулы (II-д)  , 1,3,4-оксадиазол-2,5-диил общей формулы (II-е)
, 1,3,4-оксадиазол-2,5-диил общей формулы (II-е)  , 1-фенил-2-пиразолин-3,5-диил общей формулы (II-ж)
, 1-фенил-2-пиразолин-3,5-диил общей формулы (II-ж)  , перилен-3,10-диил общей формулы (II-з)
, перилен-3,10-диил общей формулы (II-з)
 ;
;
n означает целое число из ряда от 2 до 4;
m означает целое число из ряда от 1 до 3;
k означает целое число из ряда от 1 до 3.
2. Разветвленные олигоарилсиланы с реакционно-способными концевыми группами по п.1, отличающиеся тем, что R означает метил.
3. Разветвленные олигоарилсиланы с реакционно-способными концевыми группами по п.1, отличающиеся тем, что R1 означает винил.
4. Разветвленные олигоарилсиланы с реакционно-способными концевыми группами по п.1, отличающиеся тем, что Ar означает тиенил-2,5-диил, выбранный из ряда соединений формулы (II-а).
5. Разветвленные олигоарилсиланы с реакционно-способными концевыми группами по п.1, отличающиеся тем, что Х означает антрацен-9,10-диил (II-д), с условием, что Q означает фенил-1,4-диил, выбранный из ряда соединений формулы (II-б), m равно 1, k равно 1.
6. Разветвленные олигоарилсиланы с реакционно-способными концевыми группами по п.1, отличающиеся тем, что Х означает 2,1,3-бензотиодиазол-4,7-диил (II-г), m равно l, k равно 1.
7. Разветвленные олигоарилсиланы с реакционно-способными концевыми группами по п.1, отличающиеся тем, что Х означает 2,1,3-бензотиодиазол-4,7-диил (II-г), m равно l, k равно 2.
8. Разветвленные олигоарилсиланы с реакционно-способными концевыми группами по любому из пп.1-7, отличающиеся тем, что они имеют квантовый выход люминесценции не менее 30%, преимущественно не менее 50%.
9. Разветвленные олигоарилсиланы с реакционно-способными концевыми группами по любому из пп.1-7, отличающиеся тем, что они обладают внутримолекулярным переносом энергии с эффективностью не менее 70%, преимущественно не менее 90%.
10. Разветвленные олигоарилсиланы с реакционно-способными концевыми группами по любому из пп.1-7, отличающиеся тем, что они термостабильны до температуры не менее 200°С, предпочтительно не менее 400°С.
11. Способ получения разветвленных олигоарилсиланов с реакционно-способными концевыми группами по пп.1-10, заключающийся в том, что соединение общей формулы (III)
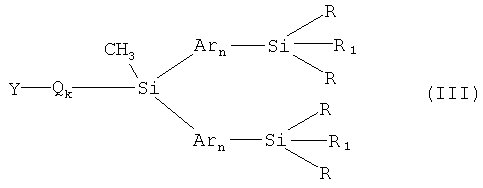
где Y означает остаток борной кислоты или ее эфира или Br или I,
R, R1, Ar, Q, n, k имеют вышеуказанные значения,
взаимодействуют в условиях реакции Сузуки с реагентом общей формулы (IV)
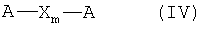 ,
,
где А означает:
Br или I, при условии, что Y означает остаток борной кислоты или ее эфира,
или
остаток борной кислоты или ее эфира, при условии, что Y означает Br или I;
X и m имеют вышеуказанные значения.
12. Способ по п.11, отличающийся тем, что эфиром борной кислоты, является эфир, выбранный из ряда: 4,4,5,5-тетраметил-1,3,2-диоксаборолан общей формулы (V-a)  , 1,3,2-диоксаборолан общей формулы (V-б)
, 1,3,2-диоксаборолан общей формулы (V-б)  , 1,2,3-диоксаборинан общей формулы (V-в)
, 1,2,3-диоксаборинан общей формулы (V-в)  , 5,5-диметил-1,2,3-диоксаборинан общей формулы (V-г)
, 5,5-диметил-1,2,3-диоксаборинан общей формулы (V-г)  .
.
13. Способ по п.11, отличающийся тем, что А в соединении формулы (IV) означает Br.
14. Способ по п.11, отличающийся тем, что Х в соединении формулы (IV) означает антрацен-9,10-диил (II-д), с условием, что радикал Q означает фенил-1,4-диил, выбранный из ряда соединений формулы (II-б), m равно 1, k равно 1.
15. Способ по п.11, отличающийся тем, что Х означает 2,1,3-бензотиодиазол-4,7-диил (II-г), с условием, что радикал Q означает незамещенный тиенил-2,5-диил, m равно 1.
16. Способ по любому из пп.11-15, отличающийся тем, что взаимодействие компонентов осуществляют при температуре от 20 до 200°С, предпочтительно при температуре от 60 до 120°С.
17. Способ по любому из пп.11-15, отличающийся тем, что взаимодействие компонентов проводят в среде органического растворителя, выбранного из ряда толуол, тетрагидрофуран, этанол, диметилформамид или их смесей.
18. Способ по любому из пп.11-15, отличающийся тем, что полученные разветвленные олигоарилсиланы с реакционно-способными концевыми группами имеют квантовый выход люминесценции не менее 30%, преимущественно не менее 50%.
19. Способ по любому из пп.11-15, отличающийся тем, что полученные разветвленные олигоарилсиланы с реакционно-способными концевыми группами обладают внутримолекулярным переносом энергии с эффективностью не менее 70%, преимущественно не менее 90%.
20. Способ по любому из пп.11-15, отличающийся тем, что полученные разветвленные олигоарилсиланы с реакционно-способными концевыми группами термостабильны до температуры не менее 200°С, предпочтительно не менее 400°С.
| РАЗВЕТВЛЕННЫЕ ОЛИГОАРИЛСИЛАНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2008 |
|
RU2396290C1 |
| US 6617040 B2, 09.09.2003 | |||
| JP 9157358 A, 17.06.1997 | |||
| US 20100187980 A1, 29.07.2010 | |||
Авторы
Даты
2015-03-20—Публикация
2012-12-05—Подача