ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Данная заявка основана и имеет преимущество приоритета предварительной заявки США № 61/244736, поданной 22 сентября 2009 г., которая включена в настоящее описание в полном объеме путем ссылки.
УРОВЕНЬ ТЕХНИКИ
В области фармацевтических препаратов существует класс препаратов для доставки лекарственных средств, которые предназначены для высвобождения биологически активных компонентов в течение требуемого периода времени после однократного введения. Депо-препарат - одно из названий, применяемых для описания таких препаратов продленного действия. Депо-препараты можно производить разными способами. Обычный подход к получению депо-препарата или имплантата состоит в производстве твердой матрицы, которая включает в себя биологически активный компонент и инертный полимерный наполнитель. Целью применения инертного полимерного наполнителя в имплантате является ограничение поступления воды, которое в свою очередь регулирует растворение биологически активного компонента с последующим высвобождением биологически активного компонента из имплантированной матрицы. Кроме физических и химических свойств биологически активного компонента свой вклад в скорость высвобождения биологически активного компонента вносит количество биологически активного компонента в имплантате. То есть увеличение количества биологически активного компонента увеличивает скорость его высвобождения. К сожалению, некоторые имплантируемые препараты нуждаются в присутствии внутри высокого количества биологически активного компонента, чтобы имелось достаточное количество биологически активного компонента, способное удовлетворять требованиям обеспечения дозы и продолжительности действия препарата при конкретных медицинских показаниях. Однако высокое количество биологически активного компонента, включенное внутрь имплантата, может вызывать слишком быстрое высвобождение биологически активного компонента, или высвобождение биологически активного компонента может происходить даже с нерегулируемой скоростью.
В связи с этим существует потребность в новых имплантируемых устройствах, которые можно загружать различными, включая высокие, количествами биологически активного компонента, при этом все еще сохраняя удовлетворительный профиль высвобождения, такой как профиль пролонгированного высвобождения или профиль высвобождения с низким начальным выбросом в том числе. Такие и другие потребности удовлетворяются с помощью настоящего изобретения.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Описаны имплантируемые устройства с различными вариантами загрузки биологически активного компонента, которые можно выбирать и применять для создания заданного профиля высвобождения конкретного биологически активного компонента из имплантируемого устройства.
Преимущества изобретения будут частично изложены в представленном ниже описании и частично будут очевидны из описания или могут быть изучены путем практического осуществления описанных ниже аспектов. Описанные ниже преимущества будут реализованы и достигнуты с помощью элементов и комбинаций, в частности, перечисленных в прилагаемой формуле изобретения. Следует понимать, что как вышеизложенное общее описание, так и последующее подробное описание являются только иллюстративными и поясняющими и не являются ограничивающими.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На фиг. 1 показан вид в перспективе поперечного сечения типичного имплантируемого устройства, содержащего ядро, окруженное мембранной оболочкой.
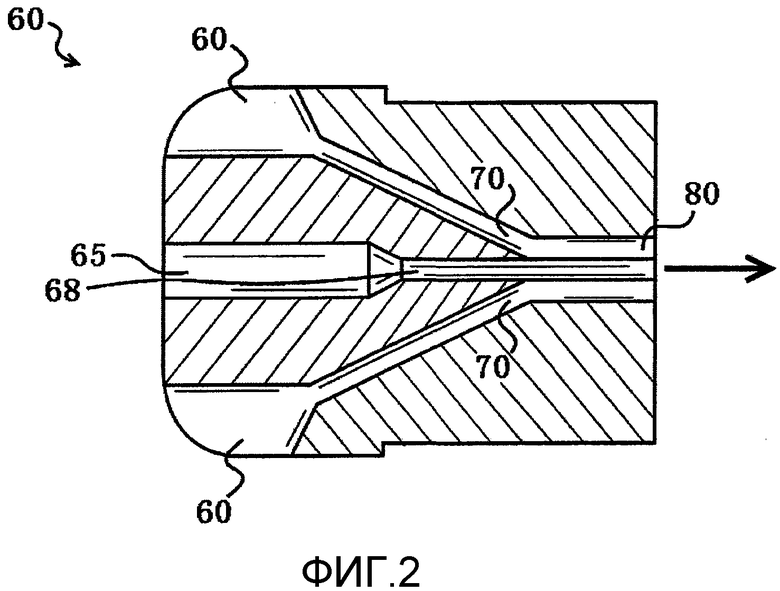
На фиг. 2 показан вид сверху поперечного сечения устройства для совместной экструзии, которое можно применять для изготовления имплантируемого устройства, содержащего ядро, окруженное мембранной оболочкой.
ПОДРОБНОЕ ОПИСАНИЕ
Перед описанием и раскрытием настоящих соединений, композиций, композитов, изделий, устройств и/или способов следует понимать, что описанные ниже аспекты не ограничиваются конкретными соединениями, композициями, композитами, изделиями, устройствами, способами или применениями, которые, по сути, могут, конечно, меняться. Также следует понимать, что применяемая здесь терминология служит только целям описания конкретных аспектов изобретения и не должна считаться ограничивающей.
В данном описании и формуле изобретения, следующих далее, будет сделана ссылка на ряд терминов, для которых следует указать следующие значения.
Будет понятно, что на всем протяжении описания, если контекст не требует иного, слово "содержат" или его варианты, такие как "содержит" или "содержащие", подразумевает охват указанного числа или стадии или группы чисел или стадий, но нельзя исключать любое другое число или стадию или группу чисел или стадий.
Следует заметить, что применяемые в описании и прилагаемой формуле изобретения формы единственного числа "a," "an" и "the" включают в себя многочисленные объекты ссылки, если контекст в явной форме не требует иного. Таким образом, например, ссылка на "биологически активный компонент" включает в себя смеси двух или более таких средств и т.п.
Термин "необязательный" или "необязательно" означает, что в дальнейшем описанный случай или обстоятельство могут случиться или могут не случиться и что описание включает в себя все примеры, в которых случай или обстоятельство случаются, и примеры, в которых они не случаются.
В настоящем документе диапазоны могут обозначаться как "приблизительно" от одного конкретного значения (и/или) до "приблизительно" другого конкретного значения. Когда такой диапазон обозначен, еще один аспект включает в себя значения от одного конкретного значения (и/или) до другого конкретного значения. Аналогично, когда значения обозначаются в виде приблизительных цифр путем применения предшествующего слова "приблизительно", следует понимать, что конкретное значение образует еще один аспект. Кроме того, следует понимать, что предельные значения каждого из диапазонов значимы как в отношении другого предельного значения, так и независимо от другого предельного значения.
Массовый процент компонента, если специально не указано иначе, рассчитывается исходя из общей массы препарата или композиции, в которую включен компонент.
Термин "высвобождаемое средство" относится к средству, которое может смешиваться вместе с описанным полимером и затем высвобождаться из него, например, по мере разрушения полимера.
Термин "биологически активный компонент" относится к средству, которое обладает биологической активностью. Биологически активное средство можно применять для обработки, постановки диагноза, лечения, облегчения боли, предупреждения заболевания (то есть профилактически), улучшения, модулирования или оказания иного благоприятного воздействия на заболевание, расстройство, инфекцию и т.п. "Высвобождаемый биологически активный компонент" относится к биологически активному компоненту, который может высвобождаться из описанного полимера. Биологически активные компоненты также включают в себя те вещества, которые воздействуют на структуру или функцию субъекта или пролекарство, которое становится биологически активным или биологически активным в большей степени после его размещения в заданной физиологической среде.
Описанные соединения, композиции и компоненты, которые можно применять для получения препарата, можно применять в сочетании с препаратом или можно применять в препарате, представляют собой продукты описанных способов и композиций. Здесь описаны упомянутые и другие материалы, и следует понимать, что когда описываются комбинации, подгруппы, взаимодействия, группы и т.д. таких материалов, считается, что каждая из таких комбинаций конкретно здесь описана, несмотря на то что при конкретной ссылке каждая из различных самостоятельных и объединенных комбинаций и комбинация таких соединений может не быть описана в явной форме. Например, если описывается и обсуждается ряд разных полимеров и средств, конкретно рассматривается каждое из них и любая их комбинация и комбинация полимера и средства, если специально не указано иначе. Таким образом, если описан класс молекул A, B и C, а также класс молекул D, E и F и описан пример комбинации молекул A-D, то даже если каждая из комбинаций молекул индивидуально не перечислена, каждая является индивидуальной и рассматривается совместно. Таким образом, на основании описания A, B и C; D, E и F и примера комбинации A-D в данном примере конкретно рассматривается и должна считаться описанной каждая из комбинаций A-E, A-F, B-D, B-E, B-F, C-D, C-E и C-F. Аналогичным образом также конкретно рассматривается и считается описанной любая подгруппа или комбинация подгрупп. Таким образом, например, подгруппа A-E, B-F и C-E конкретно рассматривается и должна считаться описанной на основании описания A, B и C; D, E и F; и примера комбинации A-D. Такая концепция относится ко всем аспектам данного изобретения, включая, но не ограничиваясь перечисленным, стадии способов изготовления и применения описанных композиций. Таким образом, если существуют различные дополнительные стадии, которые могут осуществляться, следует понимать, что каждая из таких дополнительных стадий может осуществляться в любом конкретном варианте осуществления или комбинации вариантов осуществления описанных способов и что каждая такая комбинация конкретно рассматривается и должна считаться описанной.
Обычно имплантируемые устройства согласно изобретению содержат продольную основную часть и ближний и дальний концы (и торцевые поверхности на ближнем и дальнем концах). Продольная основная часть содержит биологически совместимый и/или биоразлагаемый полимер. Продольная основная часть содержит продольную поверхность ядра, которая может представлять собой: (i) частично или полностью открытую поверхность, (ii) поверхность, частично или полностью покрытую биологически активным компонентом, (iii) поверхность, частично или полностью окруженную (то есть не открытую) полимерной оболочкой (которая может содержать или не содержать биологически активный компонент и поверхность которой может быть покрыта биологически активным компонентом или может не содержать биологически активный компонент), или представлять собой комбинацию (i), (ii) и (iii).
Биологически активный компонент загружают в имплантируемое устройство согласно конкретному варианту загрузки в зависимости от требуемого профиля высвобождения. Путем изменения варианта загрузки биологически активного компонента в имплантируемых устройствах согласно изобретению профили высвобождения можно адаптировать к конкретной потребности и можно обеспечивать сложные профили высвобождения.
Обычно биологически активный компонент может присутствовать в имплантате (то есть в продольной основной части и/или полимерной оболочке) или на любой поверхности имплантата. Обычно биологически активный компонент может: (i) наноситься в виде покрытия только на одну или несколько торцевых поверхностей на ближнем или дальнем концах, (ii) наноситься в виде покрытия на одну или несколько торцевых поверхностей на ближнем или дальнем концах и только на часть наружной поверхности продольной основной части или на всю наружную поверхность продольной основной части, (iii) наноситься в виде покрытия на часть продольной основной части или всю продольную основную часть, но не покрывать обе торцевые поверхности, (iv) растворяться или диспергироваться во внутреннем ядре (когда оно присутствует), (v) растворяться или диспергироваться в продольной основной части, (vi) растворяться или диспергироваться в полимерной оболочке (когда она присутствует), (vii) отсутствовать на полимерной оболочке (когда она присутствует), или присутствует любая из комбинаций (i)-(viii).
В одном из аспектов изобретения имплантируемое устройство может загружаться по объему. В таком аспекте изобретения биологически активный компонент растворяется или диспергируется по всему объему продольной основной части. Поверхности имплантируемого устройства могут покрываться биологически активным компонентом или могут не содержать биологически активный компонент. Такой аспект может включать в себя примеры, в которых продольная основная часть образует внутреннее ядро и окружена полимерной оболочкой.
В еще одном аспекте изобретения продольная основная часть содержит внутреннее ядро с продольной поверхностью ядра, окруженной полимерной оболочкой, и открытыми торцевыми поверхностями на ближнем и дальнем концах, которые не окружены полимерной оболочкой. Полимерная оболочка содержит продольную наружную поверхность, которая практически коэкстенсивна продольной поверхности ядра. Внутреннее ядро содержит биоразлагаемый полимер, содержащий растворенный или диспергированный в нем биологически активный компонент. В одном из примеров полимерная оболочка не содержит биологически активный компонент. В других примерах полимер может содержать растворенный или диспергированный в нем биологически активный компонент. Например, со ссылкой на фиг. 1, имплантируемое устройство 100 содержит продольную основную часть 130, содержащую внутреннее ядро 110, в которое загружается биологически активный компонент, и продольную поверхность ядра, которая окружена полимерной оболочкой 150 и коэкстенсивна полимерной оболочке 150, которая содержит наружную поверхность полимерной оболочки 140. Имплантируемое устройство также содержит покрытие 120 из биологически активного компонента на торцевых поверхностях на ближнем и/или дальнем конце, включая часть торцевой поверхности, образованную наружной полимерной оболочкой (но не внутри полимерной оболочки), и часть торцевой поверхности, образованную внутренним ядром. В подобном варианте осуществления изобретения биологически активный компонент также может наноситься в виде покрытия на продольную поверхность в добавление к покрытию, наносимому на торцевую поверхность. В еще одном варианте осуществления изобретения биологически активный компонент может наноситься в виде покрытия на продольную поверхность и не покрывать ближнюю и дальнюю поверхности. В еще одном варианте осуществления изобретения биологически активный компонент может присутствовать внутри (то есть в растворенном или диспергированном состоянии) как в ядре, так и в полимерный оболочке. В таком варианте осуществления изобретения концентрация лекарственного средства в ядре и окружающей полимерной оболочке может быть одинаковой или разной.
В еще одном аспекте изобретения продольная основная часть содержит внутреннее ядро с продольной поверхностью ядра, окруженной полимерной оболочкой, и открытыми торцевыми поверхностями на ближнем и дальнем концах, которые не окружены полимерной оболочкой. Полимерная оболочка содержит наружную продольную поверхность, которая практически коэкстенсивна продольной поверхности ядра. Внутреннее ядро содержит биоразлагаемый полимер и не содержит биологически активного компонента или не содержит растворенного или диспергированного в нем биологически активного компонента. В таком аспекте биологически активный компонент можно наносить в виде покрытия на одну или несколько наружных поверхностей, включая одну или несколько продольных наружных поверхностей, торцевую поверхность на ближнем конце, торцевую поверхность на дальнем конце или их комбинацию, включая те примеры, в которых биологически активный компонент наносится на часть каждой открытой поверхности имплантируемого устройства или на все открытые поверхности имплантируемого устройства.
В еще одном аспекте изобретения имплантируемое устройство содержит продольную основную часть, которая может иметь продольную поверхность, которая окружена или не окружена полимерной мембранной оболочкой и, таким образом, остается открытой. В таком аспекте изобретения продольная основная часть растворяется или диспергируется, а биологически активный компонент присутствует только на одной или нескольких торцевых поверхностях на ближнем или дальнем конце.
В одном из аспектов изобретения имплантируемое устройство, имеющее определенный порядок расположения ядра/оболочки, можно получать с помощью способа, включающего в себя: a) формирование ядра требуемой формы из смеси биоразлагаемого полимера и необязательно биологически активного компонента (если требуется загрузка внутреннего ядра); b) формирование мембранной оболочки, окружающей ядро; c) обнажение торцевых поверхностей на ближнем и дальнем конце путем удаления той части мембранной оболочки, которая окружает торцевые поверхности.
Для варианта ядро/оболочка, в котором биологически активный компонент растворяется или диспергируется во внутреннем ядре, формирование ядра имплантируемого устройства можно осуществлять путем первоначального смешивания, по меньшей мере, одного биоразлагаемого полимера и, по меньшей мере, одного биологически активного компонента с получением смеси. Смешивание биоразлагаемого полимера и биологически активного компонента можно осуществлять с применением способов, известных в данной области техники. Например, полимер и биологически активный компонент можно подвергать сухому смешиванию (то есть смешиванию частиц полимера и компонента), например, с применением V-смесителя Паттерсона-Келли или гранулировать перед стадией переработки, то есть перед формированием ядра требуемой формы. Предполагается, что другие компоненты, например, такие как инертные наполнители, можно смешивать с полимером и биологически активным компонентом перед переработкой смеси в ядро.
Стадия смешивания может включать в себя применение растворителя. Однако в других аспектах изобретения смешивание биоразлагаемого полимера и биологически активного компонента не включает в себя применение растворителя. Если избегать применения растворителя во время смешивания, можно реализовать ряд преимуществ. Во-первых, применение растворителя во время смешивания требует дополнительной стадии переработки для удаления растворителя. Во-вторых, если система доставки имплантируется субъекту, выбранный растворитель должен быть биологически совместимым, если какое-либо остаточное количество растворителя остается в устройстве. Растворитель может неблагоприятно воздействовать на морфологию системы доставки в целом, что может приводить к нежелательной схеме высвобождения. Растворитель может неблагоприятно воздействовать на стабильность биологически активного компонента во время процесса производства. Наконец, уровень растворителя требует контроля, поскольку он должен быть достаточно низким, чтобы соответствовать нормативным рекомендациям.
Переработку смеси во внутреннее ядро можно осуществлять в таких условиях, чтобы биологически активный компонент равномерно смешивался, диспергировался или растворялся в полимере или только в определенных порциях полимера. Из смесей можно производить внутреннее ядро требуемой формы различными способами, например, такими как экструзия расплава, литье под давлением, формование прессованием или прессование смеси на валковом прессе с получением требуемой формы или структуры. Способы производства, использующие прессование, могут включать в себя, но не ограничиваются таблетированием. В зависимости от условий переработки биоразлагаемый полимер, применяемый в качестве исходного материала на стадии смешивания, может представлять собой тот же самый полимер, который присутствует в конечном устройстве, или может представлять собой другой полимер. Например, полимер во время переработки (в ядро) может подвергаться реакциям полимеризации или деполимеризации, которые в конечном итоге могут приводить к полимеру, отличающемуся от полимера, который применялся до начала переработки (в ядро). Таким образом, применяемый здесь термин "полимер", включающий в себя как биологически совместимый полимер, так и биоразлагаемый полимер, охватывает полимеры, применяемые в качестве исходных материалов, а также конечный полимер, присутствующий в конечном устройстве.
В одном из аспектов изобретения сначала производят внутреннее ядро требуемой формы, как обсуждалось выше (с биологически активным компонентом или без него), а затем формируют мембранную оболочку, которая окружает ядро. В других аспектах изобретения, обсуждаемых ниже, внутреннее ядро и мембранную оболочку можно производить вместе, например, с помощью совместной экструзии, обеспечивая при этом имплантируемое устройство. Когда сначала формируют внутреннее ядро, мембранную оболочку в дальнейшем можно формировать с применением способов, известных в данной области техники. В одном из аспектов изобретения мембранную оболочку можно формировать на внутреннем ядре путем нанесения полимера распылением или путем нанесения покрытия окунанием в раствор, содержащий биологически совместимый полимер (и необязательно биологически активный компонент). В таком аспекте изобретения мембранную оболочку можно формировать около всего внутреннего ядра таким образом, чтобы внутреннее ядро не имело открытой поверхности. После формирования мембранной оболочки часть мембранной оболочки можно удалять, например, путем растворения или физического отрезания части мембранной оболочки, чтобы обеспечить открытую поверхность внутреннего ядра (то есть торцевую поверхность на ближнем или дальнем конце). В других аспектах изобретения мембранную оболочку можно формировать, окружая только часть ядра таким образом, чтобы после формирования мембранной оболочки ядро содержало открытую поверхность.
В еще одном аспекте изобретения имплантируемое устройство можно получать путем совместной экструзии, например, с помощью способа, включающего в себя: a) экструзию биоразлагаемого полимера, или в альтернативном варианте смеси биоразлагаемого полимера и биологически активного компонента, через внутреннее коаксиальное литьевое отверстие для формирования ядра; b) формирование непрерывной композитной заготовки путем одновременной совместной экструзии биологически совместимого полимера, или в альтернативном варианте смеси биологически совместимого полимера и биологически активного компонента, через наружное коаксиальное литьевое отверстие для нанесения практически коэкстенсивной мембранной оболочки, окружающей ядро; с) разрезание непрерывной композитной заготовки со стадии (b) на один или несколько брусков, содержащих продольную поверхность и две торцевые поверхности. Например, таким способом можно получать имплантируемое устройство, показанное на фиг. 1.
Со ссылкой на фиг. 2 способ совместной экструзии можно осуществлять с помощью различных устройств для совместной экструзии, известных в данной области техники. На фиг. 2 показано поперечное сечение 60 такого устройства. При способе совместной экструзии полимер или смесь, которую можно формировать, как обсуждалось выше, протекает через внутреннее коаксиальное литьевое отверстие 65, в то время как биологически совместимый полимер или смесь, из которой будет формироваться мембранная оболочка, протекает через наружное коаксиальное литьевое отверстие 60. Внутреннее 65 и наружное 60 коаксиальные литьевые отверстия затем суживаются на участках пресс-формы 68 и 70, где биологически совместимый полимер или смесь и биоразлагаемый полимер или смесь биоразлагаемого полимера/биологически активного компонента объединяются и принимают требуемую форму имплантируемого устройства, которая в данном примере представляет собой цилиндр. Затем непрерывная композитная заготовка, полученная совместной экструзией, покидает устройство в точке выхода 80. После совместной экструзии непрерывную композитную заготовку, полученную совместной экструзией, можно разрезать на один или несколько брусков, содержащих продольную поверхность и две торцевые поверхности, как обсуждалось выше и как показано на фиг. 1. Таким образом, после разрезания непрерывной заготовки, полученной совместной экструзией, можно формировать имплантируемое устройство путем разрезания непрерывной заготовки на отдельные бруски, каждый из которых содержит продольную поверхность и торцевую поверхность на ближнем и дальнем концах, как обсуждалось выше. Непрерывную заготовку можно разрезать на столько брусков, сколько требуется для получения нужного числа имплантируемых устройств или имплантируемых устройств нужной продольной длины.
Имплантируемые устройства, которые не имеют определенного порядка расположения ядра/оболочки, можно получать с помощью более простых экструзионных способов, например с применением экструзии с применением простой пресс-формы и разрезания заготовки на один или несколько брусков, как обсуждалось выше.
Имплантируемые устройства в некоторых аспектах изобретения содержат покрытия из биологически активного компонента на одной или нескольких поверхностях устройства. Покрытие из биологически активного компонента можно наносить на имплантируемое устройство путем приготовления соответствующего раствора дисперсии биологически активного компонента в растворителе и последующего нанесения полученного раствора на одну или несколько открытых поверхностей имплантируемого устройства. Нанесение раствора можно осуществлять путем распыления, окунания, нанесения раствора кистью и т.д. на требуемую поверхность имплантируемого устройства с последующей возможностью испарения растворителя, если требуется.
Различные биологически совместимые или биоразлагаемые полимеры можно применять для формирования имплантируемых устройств, включая полимеры, применяемые для мембранной оболочки и/или применяемые в качестве полимера внутреннего ядра. Биологически совместимый полимер также может представлять собой биоразлагаемый полимер. В одном из аспектов изобретения биологически совместимый полимер может представлять собой один или несколько сложных полиэфиров, полигидроксиалканоатов, полигидроксибутиратов, полидиоксанонов, полигидроксивалератов, полиангидридов, сложных полиортоэфиров, полифосфазенов, полифосфатов, сложных полифосфоэфиров, полидиоксанонов, сложных полифосфоэфиров, полифосфатов, полифосфонатов, полифосфатов, полигидроксиалканоатов, поликарбонатов, полиалкилкарбонатов, полиортокарбонатов, сложных полиэфирамидов, полиамидов, полиаминов, полипептидов, полиуретанов, полиалкиленалкилатов, полиалкиленоксалатов, полиалкиленсукцинатов, жирных полигидроксикислот, полиацеталей, полицианоакрилатов, поликеталей, полиэфир-эфирных сополимеров, простых полиэфиров, полиалкиленгликолей, полиалкиленоксидов, полиэтиленгликолей, полиэтиленоксидов, полипептидов, полисахаридов или поливинилпирролидонов. Другие полимеры, не относящиеся к биоразлагаемым полимерам, но надежные и биологически совместимые, включают в себя без ограничения сополимер этилена и винилацетата, политетрафторэтилен, полипропилен, полиэтилен и т.п. Аналогичным образом, другие подходящие полимеры, не относящиеся к биоразлагаемым, включают в себя, без ограничения, силиконы и полиуретаны.
Биоразлагаемый полимер, который образует внутреннее ядро или мембранную оболочку (когда присутствует), может включать в себя любой из биоразлагаемых полимеров, перечисленных выше, или любой другой биоразлагаемый полимер, известный в данной области техники. В дополнительном аспекте изобретения биологически совместимый и/или биоразлагаемый полимер может представлять собой поли(лактид), поли(гликолид), сополимер лактида с гликолидом, поли(капролактон), сложный поли(ортоэфир), поли(фосфазен), поли(гидроксибутират) или сополимер, содержащий поли(гидроксибутарат), сополимер лактида и капролактона, поликарбонат, сложный полиэфирамид, полиангидрид, поли(диоксанон), поли(алкиленалкилат), сополимер полиэтиленгликоля и сложного полиортоэфира, биоразлагаемый полиуретан, поли(аминокислоту), полиамид, сложный полиэфирамид, полиэфир-эфирный сополимер, полиацеталь, полицианоакрилат, сополимер поли(оксиэтилена)/поли(оксипропилена), полиацетали, поликетали, сложные полифосфоэфиры, полигидроксивалераты или сополимер, содержащий полигидроксивалерат, полиалкиленоксалаты, полиалкиленсукцинаты, поли(малеиновая кислота) и их сополимеры, терполимеры, комбинации или их смеси.
В еще одном дополнительном аспекте изобретения применимые биоразлагаемые и биологически совместимые полимеры представляют собой полимеры, которые содержат один или несколько остатков молочной кислоты, гликолевой кислоты, лактида, гликолида, капролактона, гидроксибутирата, гидроксивалератов, диоксанонов, полиэтиленгликоля (PEG), полиэтиленоксида или их комбинацию. В еще одном дополнительном аспекте изобретения применимые биоразлагаемые полимеры представляют собой полимеры, которые содержат один или несколько остатков лактида, гликолида, капролактона или их комбинацию.
В одном из аспектов изобретения применимые биоразлагаемые и биологически совместимые полимеры представляют собой полимеры, которые содержат один или несколько блоков гидрофильных или водорастворимых полимеров, включая, но, не ограничиваясь перечисленным, полиэтиленгликоль (PEG) или поливинилпирролидон (PVP) в комбинации с одним или несколькими блоками другого биологически совместимого или биоразлагаемого полимера, который содержит лактид, гликолид, капролактон или их комбинацию.
В конкретных аспектах изобретения биоразлагаемый и/или биологически совместимый полимер может содержать один или несколько лактидных остатков. В этой связи полимер может содержать любой лактидный остаток, включая все рацемические и стереоспецифические формы лактида, включая, но, не ограничиваясь перечисленным, L-лактид, D-лактид и D,L-лактид или их смесь. Применимые полимеры, содержащие лактид, включают в себя, но не ограничиваются перечисленным, поли(L-лактид), поли(D-лактид) и поли(DL-лактид); и сополимер лактида с гликолидом, включая сополимер L-лактида с гликолидом, сополимер D-лактида с гликолидом и сополимер DL-лактида с гликолидом; или сополимеры, терполимеры, комбинации или их смеси. Лактид/гликолидные полимеры можно удобно получать полимеризацией в расплаве через раскрытие кольца лактидного и гликолидного мономеров. Кроме того, рацемические полимеры DL-лактид, L-лактид и D-лактид имеются в продаже. L-полимеры являются более кристаллическими и всасываются более медленно, чем DL-полимеры. В добавление к сополимерам, содержащим гликолид и DL-лактид или L-лактид, сополимеры L-лактида и DL-лактида имеются в продаже. Гомополимеры лактида или гликолида также имеются в продаже.
Когда биоразлагаемый и/или биологически совместимый полимер представляет собой сополимер лактида с гликолидом, поли(лактид), или поли(гликолид), количество лактида и гликолида в полимере может меняться. В дополнительном аспекте изобретения биоразлагаемый полимер содержит от 0 до 100 мол.%, от 40 до 100 мол.%, от 50 до 100 мол.%, от 60 до 100 мол.%, от 70 до 100 мол.% или от 80 до 100 мол.% лактида и от 0 до 100 мол.%, от 0 до 60 мол.%, от 10 до 40 мол.%, от 20 до 40 мол.% или от 30 до 40 мол.% гликолида, где количество лактида и гликолида составляет 100 мол.%. В дополнительном аспекте изобретения биоразлагаемый полимер может представлять собой поли(лактид), сополимер лактида с гликолидом в отношении 95:5, сополимер лактида с гликолидом в отношении 85:15, сополимер лактида с гликолидом в отношении 75:25, сополимер лактида с гликолидом в отношении 65:35 или сополимер лактида с гликолидом в отношении 50:50, где отношения представляют собой мольные отношения.
В дополнительном аспекте изобретения биоразлагаемый и/или биологически совместимый полимер может представлять собой поли(капролактон) или сополимер лактида с капролактоном. В одном из аспектов изобретения полимер может представлять собой сополимер лактида с капролактоном, который в различных аспектах изобретения может представлять собой сополимер лактида с капролактоном в отношении 95:5, сополимер лактида с капролактоном в отношении 85:15, сополимер лактида с капролактоном в отношении 75:25, сополимер лактида с капролактоном в отношении 65:35 или сополимер лактида с капролактоном в отношении 50:50, где отношения представляют собой мольные отношения.
Когда либо биоразлагаемые, либо биологически совместимые полимеры содержат полимеры на основе лактидов, полимеры на основе лактидов могут содержать любой лактидный остаток, включая все рацемические и стереоспецифические формы лактидов, включая, но, не ограничиваясь перечисленным, L-лактид, D-лактид и D,L-лактид, или их смесь. Применимые полимеры, содержащие лактид, включают в себя, но не ограничиваются перечисленным, поли(L-лактид), поли(D-лактид) и поли(DL-лактид); и сополимер лактида с гликолидом, включая сополимер L-лактида с гликолидом, сополимер D-лактида с гликолидом и сополимер DL-лактида с гликолидом; или их сополимеры, терполимеры, их комбинации или их смеси. Лактид/гликолидные полимеры можно получать путем раскрытия кольца лактидных и гликолидных мономеров. Кроме того, рацемические DL-лактидные, L-лактидные и D-лактидные полимеры имеются в продаже. L-полимеры являются более кристаллическими и всасываются более медленно, чем DL-полимеры. В добавление к сополимерам, содержащим гликолид и DL-лактид или L-лактид, сополимеры L-лактида и DL-лактида имеются в продаже. Гомополимеры лактида или гликолида также имеются в продаже.
В некоторых аспектах изобретения может быть желательно, чтобы осуществлялся контакт или смешивание описанного биоразлагаемого и/или биологически совместимого полимера с одним или несколькими пластификаторами, чтобы изменить физические свойства (например, снизить Tg) полученной композиции. Пластификаторы, которые можно применять, включают в себя все утвержденные FDA пластификаторы, такие как бензилбензоаты, ацетаты целлюлозы, ацетофталаты целлюлозы, хлорбутанол, декстрины, дибутилсебацинат, диметилсебацинат, ацетилфталаты, диэтилфталат, дибутилфталат, дипропилфталат, диметилфталат, диоктилфталат, метилцеллюлоза, этилцеллюлоза, гидроксилэтилцеллюлоза, гидроксипропилцеллюлоза, гидроксипропилметилцеллюлозы, желатин, глицерины, глицерилмоностеарат, моноглицериды, моно- и диацетилированные моноглицериды, глицерин, маннит, минеральные масла и ланолиновые спирты, вазелин и ланолиновые спирты, касторовое масло, растительные масла, кокосовое масло, полиэтиленгликоль, полиметакрилаты и их сополимеры, поливинилпирролидон, пропиленкарбонаты, пропиленгликоль, сорбит, основы суппозиториев, диацетин, триацетин, триэтаноламин, сложные эфиры лимонной кислоты, триэтилцитрат, ацетилтриэтилцитрат, ацетилтрибутилцитрат, триэтилцитрат и сложные эфиры фосфорной кислоты.
Биоразлагаемый полимер может разрушаться и при этом дает возможность высвобождаться средству из внутреннего ядра имплантируемого устройства. В композициях можно применять различные высвобождаемые средства. Обычно можно применять любое средство, для которого желательно постепенное высвобождение. Таким образом, высвобождаемое средство может представлять собой биологически активный компонент, косметическое вещество, такое как жидкое косметическое средство, или другое вещество, такое как сельскохозяйственный продукт. Высвобождаемое средство может растворяться или диспергироваться в полимере и может присутствовать в любом подходящем количестве, которое обычно будет зависеть от предполагаемого применения композиции.
С имплантируемыми устройствами можно применять целый ряд биологически активных компонентов. Биологически активный компонент можно смешивать, подмешивать или иным образом объединять с биоразлагаемым полимером внутреннего ядра, мембранной оболочки и/или наносить в виде покрытия на одну или несколько поверхностей, как обсуждалось выше. В одном из аспектов изобретения биологически активный компонент можно предварительно смешивать с сахаром, например высушивать при распылении с сахаром до образования определенной частицы. В еще одном аспекте изобретения, по меньшей мере, часть биологически активного компонента можно растворять в биоразлагаемом полимере. В дополнительном аспекте изобретения, по меньшей мере, часть биологически активного компонента можно диспергировать в биоразлагаемом полимере внутреннего ядра и/или мембранной оболочки (когда она присутствует).
Смешивание биологически активного компонента и полимера можно осуществлять с дополнительным растворителем (отличающимся от полимера) или без него, как обсуждалось выше. Количество биологически активного компонента, включенное в композицию, меняется в зависимости от конкретного лекарственного средства, требуемого терапевтического воздействия и требуемой продолжительности воздействия. Считается, что поскольку различные композиции обеспечивают схемы приема лекарственного средства для различных целей терапии, не существует нормируемого низшего или высшего ограничения на количество лекарственного средства, включаемого в композицию. Низшее ограничение обычно будет зависеть от активности лекарственного средства и продолжительности его высвобождения из устройства. Специалисты в фармацевтических областях могут определить токсические уровни данного лекарственного средства, а также минимальную эффективную дозу.
Можно применять различные формы биологически активного компонента, которые способны высвобождаться из имплантируемого устройства в организме субъекта. В описанные здесь устройства могут быть включены жидкий или твердый биологически активный компонент. Биологически активные компоненты могут быть водорастворимыми или водонерастворимыми. В некоторых аспектах изобретения биологически активный компонент, по меньшей мере, очень слабо растворяется в воде и предпочтительно является в меру водорастворимым. Биологически активные компоненты могут включать в себя соли активного ингредиента. В связи с этим биологически активные компоненты могут представлять собой кислые, основные или амфотерные соли. Они могут представлять собой неионные молекулы, полярные молекулы или молекулярные комплексы, способные образовывать водородные связи. Биологически активный компонент можно включать в устройства, например, в форме незаряженной молекулы, молекулярного комплекса, соли, простого эфира, сложного эфира, амида, конъюгата полимер-лекарственное средство или в другой форме, чтобы обеспечить эффективную биологическую или физиологическую активность.
Примеры биологически активных компонентов, которые можно включать в устройства, включают в себя, но не ограничиваются перечисленным, небольшие молекулы, пептиды, белки, такие как гормоны, ферменты, антитела, фрагменты антител, конъюгаты антител, нуклеиновые кислоты, такие как аптамеры, иРНК, si-РНК, ДНК, РНК, антисмысловая нуклеиновая кислота или т.п., аналоги антисмысловых нуклеиновых кислот или т.п., ФРЭС-ингибиторы, макроциклические лактоны, агонисты допамина, антагонисты допамина, низкомолекулярные соединения, высокомолекулярные соединения или конъюгированные биологически активные компоненты. Биологически активные компоненты, предполагаемые для применения в описанных композициях, включают в себя анаболические средства, антациды, противоастматические средства, противохолестериновые и противолипидные средства, антикоагулянты, антисудорожные препараты, противодиарейные средства, противорвотные средства, противоинфекционные средства, включая противобактериальные и противомикробные средства, противовоспалительные средства, противоманиакальные средства, антиметаболиты, средства против тошноты, противоопухолевые средства, средства против ожирения, жаропонижающие и болеутоляющие средства, антиспастические средства, антитромботические средства, средства от кашля, средства от урикемии, антиангинальные средства, противогистаминные средства, препараты для подавления аппетита, биопрепараты, церебральные дилататоры, коронарные дилататоры, бронходилататоры, цитотоксические средства, противоотечные средства, диуретики, диагностические средства, эритропоэтические средства, отхаркивающие средства, желудочно-кишечные успокаивающие средства, гипергликемические средства, снотворные средства, гипогликемические (сахароснижающие) средства, иммуномодулирующие средства, ионообменные смолы, слабительные средства, минеральные пищевые добавки, муколитические средства, лекарственные средства для нервно-мышечных болезней, периферические вазодилататоры, психотропные средства, седативные средства, возбуждающие средства, тиреоидные и антитиреоидные средства, средства, стимулирующие рост тканей, маточные релаксанты, витамины или антигенные материалы.
Другие биологически активные компоненты включают в себя ингибиторы андрогенов, полисахариды, факторы роста, гормоны, факторы антиангиогенеза, декстрометорфан, гидробромид декстрометорфана, носкапин, цитрат карбетапентана, гидрохлорид хлофедианола, малеат хлорфенирамина, тартрат фениндамина, малеат пириламина, сукцинат доксиламина, цитрат фенилтолоксамина, гидрохлорид фенилэфрина, гидрохлорид фенилпропаноламина, гидрохлорид псевдоэфедрина, эфедрин, кодеинфосфат, кодеинсульфат, морфин, минеральные пищевые добавки, холестирамин, N-ацетилпрокаинамид, ацетаминофен, аспирин, ибупрофен, гидрохлорид фенилпропаноламина, кофеин, гвайфенезин, гидроксид алюминия, гидроксид магния, пептиды, полипептиды, белки, аминокислоты, гормоны, интерфероны, цитокины и вакцины.
Лекарственные средства, которые можно применять в качестве биологически активных компонентов в композициях, включают в себя, но не ограничиваются перечисленным, пептидные лекарственные средства, белковые лекарственные средства, терапевтические антитела, десенсибилизирующие материалы, антигены, противоинфекционные средства, такие как антибиотики, противомикробные средства, противовирусные, противобактериальные, антипаразитарные, противогрибковые вещества и их комбинацию, противоаллергенные препараты, андрогенные стероиды, противоотечные средства, снотворные средства, стероидные противовоспалительные средства, антихолинергики, симпатомиметики, седативные средства, миотики, антидепрессанты, транквилизаторы, вакцины, эстрогены, прогестагенные средства, гуморальные средства, простагландины, болеутоляющие средства, противоспастические средства, противомалярийные препараты, противогистаминные средства, кардиоактивные средства, нестероидные противовоспалительные средства, антипаркинсонические средства, противогипертонические средства, адреноблокаторы, диетологические средства и бензофенантридиновые алкалоиды. Средство дополнительно может представлять собой вещество, способное действовать как стимулятор, седативное средство, снотворное, болеутоляющее, противосудорожное средство и т.п.
Другие биологически активные компоненты включают в себя, но не ограничиваются перечисленным, болеутоляющие средства, такие как ацетаминофен, ацетилсалициловая кислота и т.п.; анестезирующие средства, такие как лидокаин, ксилокаин и т.п.; анорексики, такие как дексадрин, тартрат фендиметразина и т.п.; противоревматические средства, такие как метилпреднизолон, ибупрофен и т.п.; противоастматические средства, такие как сульфат тербуталина, теофиллин, эфедрин и т.п.; антибиотики, такие как сульфизоксазол, пенициллин G, ампициллин, цефалоспорины, амикацин, гентамицин, тетрациклины, хлорамфеникол, эритромицин, клиндамицин, изониазид, рифампин и т.п.; противогрибковые препараты, такие как амфотерицин B, нистатин, кетоконазол и т.п.; противовирусные препараты, такие как ацикловир, амантадин и т.п.; противораковые средства, такие как циклофосфамид, метотрексат, этретинат и т.п.; антикоагулянты, такие как гепарин, варфарин и т.п.; противосудорожные препараты, такие как фенитоин натрий, диазепам, и т.п.; антидепрессанты, такие как изокарбоксазид, амоксапин и т.п.; противогистаминные средства, такие как дифенгидрамин HCl, хлорфенирамин малеат и т.п.; гормоны, такие как инсулин, прогестины, эстрогены, кортикоиды, глюкокортикоиды, андрогены и т.п.; транквилизаторы, такие как торазин, диазепам, хлорпромазин HCl, резерпин, хлордиазепоксид HCl и т.п.; противоспастические средства, такие как алкалоиды белладонны, гидрохлорид дицикломина и т.п.; витамины и минералы, такие как незаменимые аминокислоты, кальций, железо, калий, цинк, витамин B12 и т.п.; сердечно-сосудистые средства, такие как празозин HCl, нитроглицерин, пропранолол HCl, гидралазин HCl, панкрелипаза, янтарная кислота, дегидрогеназа и т.п.; пептиды и белки, такие как LHRH, соматостатин, кальцитонин, гормон роста, пептиды типа глюкагона, рилизинг-фактор гормона роста, ангиотензин, FSH, EGF, костный морфогенетический белок (BMP), эритропоэтин (EPO), интерферон, интерлейкин, коллаген, фибриноген, инсулин, Фактор VIII, Фактор IX, энбрел (Enbrel®), ритуксан (Rituxan®), герцептин (Herceptin®), альфа-глюкозидаза, церезим/цередаза (Cerazyme/Ceredose®), вазопрессин, ACTH, человеческий сывороточный альбумин, гамма-глобулин, структурные белки, белки препаратов крови, комплексные белки, ферменты, антитела, моноклональные антитела и т.п.; простагландины; нуклеиновые кислоты; углеводы; жиры; наркотики, такие как морфин, кодеин и т.п., психотерапевтические препараты; противомалярийные препараты, L-ДОФА, диуретики, такие как фуросемид, спиронолактон и т.п.; противоязвенные лекарственные средства, такие как рантидин HCl, циметидин HCl и т.п.
Биологически активный компонент также может представлять собой иммуномодулятор, включая, например, цитокины, интерлейкины, интерферон, колониестимулирующий фактор, фактор некроза опухоли и т.п.; аллергены, такие как кошачья перхоть, аллерген березовой пыльцы, клещ домашней пыли, аллерген пыльцы травы и т.п.; антигены бактериальных организмов, таких как Streptococcus pneumoniae, Haemophilus influenzae, Staphylococcus aureus, Streptococcus pyrogenes, Corynebacterium diphteriae, Listeria monocytogenes, Bacillus anthracis, Clostridium tetani, Clostridium botulinum, Clostridium perfringens, Neisseria meningitides, Neisseria gonorrhoeae, Streptococcus mutans, Pseudomonas aeruginosa, Salmonella typhi, Haemophilus parainfluenzae, Bordetella pertussis, Francisella tularensis, Yersinia pestis, Vibrio cholerae, Legionella pneumophila, Mycobacterium tuberculosis, Mycobacterium leprae, Treponema pallidum, Leptspirosis interrogans, Borrelia burgddorferi, Campylobacter jejuni и т.п.; антигены таких вирусов, как натуральная оспа, грипп A и B, респираторно-синцитиальный вирус, парагриппозная инфекция, корь, ВИЧ, атипичная пневмония (SARS), ветряная оспа, простой герпес 1 и 2, цитомегаловирус, вирус Эпштейна-Барра, ротавирус, риновирус, аденовирус, папилломавирус, вирус полиомиелита, паротит, бешенство, коревая краснуха, коксаки-вирусы, лошадиный энцефалит, японский энцефалит, желтая лихорадка, лихорадка Рифт-Валли, лимфоцитарный хориоменингит, гепатит B и т.п.; антигены грибков, простейших и паразитарных организмов, таких как Cryptococcuc neoformans, Histoplasma capsulatum, Candida albicans, Candida tropicalis, Nocardia asteroids, Rickettsia ricketsii, Rickettsia typhi, Mycoplasma pneumoniae, Chlamyda psitiaci, Chlamydia trachomatis, Plasmodium falciparum, Trypanasoma brucei, Entamoeba histolytica, Toxoplasma gondii, Trichomonas vaginalis, Schistosoma mansoni и т.п. Такие антигены могут находиться в форме цельных убитых организмов, пептидов, белков, гликопротеинов, углеводов или их комбинаций.
В дополнительном конкретном аспекте изобретения биологически активный компонент содержит антибиотик. Антибиотик может представлять собой, например, один или несколько таких антибиотиков, как амикацин, гентамицин, канамицин, неомицин, нетилмицин, стрептомицин, тобрамицин, паромомицин, анзамицины, гелданамицин, гербимицин, карбацефем, лоракарбеф, карбапенемы, эртапенем, дорипенем, имипенем/циластатин, меропенем, цефалоспорины (первого поколения), цефадроксил, цефазолин, цефалотин или цефалотин, цефалексин, цефалоспорины (второго поколения), цефаклор, цефамандол, цефокситин, цефпрозил, цефуроксим, цефалоспорины (третьего поколения), цефиксим, цефдинир, цефдиторен, цефоперазон, цефотаксим, цефподоксим, цефтазидим, цефтибутен, цефтизоксим, цефтриаксон, цефалоспорины (четвертого поколения), цефепим, цефалоспорины (пятого поколения), цефтобипрол, гликопептиды, тейкопланин, ванкомицин, макролиды, азитромицин, кларитромицин, диритромицин, эритромицин, рокситромицин, тролеандомицин, телитромицин, спектиномицин, монобактамы, азтреонам, пенициллины, амоксициллин, ампициллин, азлоциллин, карбенициллин, клоксациллин, диклоксациллин, флуклоксациллин, мезлоциллин, метициллин, нафциллин, оксациллин, пенициллин, пиперациллин, тикарциллин, полипептиды, бацитрацин, колистин, полимиксин B, хинолоны, ципрофлоксацин, эноксацин, гатифлоксацин, левофлоксацин, ломефлоксацин, моксифлоксацин, норфлоксацин, офлоксацин, тровафлоксацин, сульфонамиды, мафенид, пронтозил (устаревший), сульфацетамид, сульфаметизол, сульфанамид (устаревший), сульфасалазин, сульфизоксазол, триметоприм, триметоприм-сульфаметоксазол (ко-тримоксазол) (TMP-SMX), тетрациклины, включая демеклоциклин, доксициклин, миноциклин, окситетрациклин, тетрациклин и другие; арсфенамин, хлорамфеникол, клиндамицин, линкомицин, этамбутол, фосфомицин, фузидовая кислота, фуразолидон, изониазид, линезолид, метронидазол, мупироцин, нитрофурантоин, платенсимицин, пиразинамид, хинупристин/далфопристин, рифампицин (рифампин в США), тинидазол, ропинерол, ивермектин, моксидектин, афамеланотид, циленгитид или их комбинация. В одном из аспектов изобретения биологически активный компонент может представлять собой комбинацию рифампицина (рифампин в США) и миноциклина.
В некоторых аспектах изобретения само устройство может представлять собой носитель и/или может быть объединено с другими носителями или добавками. Также можно применять другие фармацевтические носители. Примеры твердых носителей, отличающихся от полимера (если он является твердым), включают в себя лактозу, сульфат кальция, сахарозу, тальк, желатин, агар, пектин, камедь, стеарат магния и стеариновую кислоту. Примерами жидких носителей, отличающихся от полимера (если он является жидким), являются сахарный сироп, арахисовое масло, оливковое масло и вода. Примеры газообразных носителей включают в себя диоксид углерода и азот. Другие фармацевтически приемлемые носители или компоненты, которые можно смешивать с биологически активным компонентом, могут включать в себя, например, жирную кислоту, сахар или соль.
В одном из аспектов изобретения композиция может находиться в наборе. Набор может содержать подходящую упаковку или контейнер для композиций. Примеры включают в себя, без ограничения, стерильную упаковку. Поскольку описанные композиции подходят для применения в качестве композиций для инъекций, набор может включать в себя заранее упакованное устройство для инъекций, содержащее устройство для инъекций, в которое загружено имплантируемое устройство. Подходящие устройства для инъекций включают в себя, без ограничения, шприцы, троакары и другие устройства.
Как обсуждалось выше, имплантированные устройства можно применять для введения биологически активного компонента субъекту, который нуждается в лечении, например, для лечения расстройства, для лечения которого может быть эффективно применение биологически активного компонента. Композиции можно вводить в любую ткань или флюид субъекта. Аналогичным образом способ введения может представлять собой любой подходящий способ, например подкожную инъекцию, пероральное введение, парентеральное введение, энтеральное (брюшное) введение и т.п. В некоторых аспектах изобретения жидкие композиции, содержащие один или несколько полимеров низкой вязкости, можно вводить субъекту в виде инъекции. Характер вводимой композиции обычно будет выбираться исходя из требуемой дозировки биологически активного компонента, которая будет значительно меняться в зависимости от расстройства, но может легко определяться специалистом в фармацевтических областях.
"Эффективное количество" композиции относится к количеству композиции, которое будет обеспечивать желаемый терапевтический результат. Таким образом, эффективное количество будет значительно меняться в зависимости от композиции, биологически активного компонента и расстройства или состояния, которое подлежит лечению. Фактически эффективное количество и размер дозировки композиции, вводимой субъекту, можно определять с учетом физических и физиологических факторов, таких как масса тела, тяжесть состояния, тип заболевания, подлежащего лечению, предыдущее или параллельное терапевтическое вмешательство, идиопатия пациента, и может зависеть от способа введения. В зависимости от дозировки и способа введения число ведений предпочтительной дозировки и/или эффективного количества может меняться в соответствии с ответной реакцией субъекта. Эффективное количество описанной фармацевтической композиции может определить специалист в данной области.
В некоторых неограничивающих примерах доза может содержать приблизительно от 1 микрограмма/кг массы тела до приблизительно 5 микрограмм/кг массы тела, приблизительно до 10 микрограмм/кг массы тела, приблизительно до 50 микрограмм/кг массы тела, приблизительно до 100 микрограмм/кг массы тела, приблизительно до 200 микрограмм/кг массы тела, приблизительно до 350 микрограмм/кг массы тела, приблизительно до 500 микрограмм/кг массы тела, приблизительно до 1 миллиграмма/кг массы тела, приблизительно до 5 миллиграмм/кг массы тела, приблизительно до 10 миллиграмм/кг массы тела, приблизительно до 50 миллиграмм/кг массы тела, приблизительно до 100 миллиграмм/кг массы тела, приблизительно до 200 миллиграмм/кг массы тела, приблизительно до 350 миллиграмм/кг массы тела, приблизительно до 500 миллиграмм/кг массы тела, приблизительно до 1000 мг/кг массы тела или более в расчете на одно введение и находится в любом диапазоне, полученном в указанных диапазонах. В неограничивающих примерах дозу можно вводить в любом полученном диапазоне из числа перечисленных здесь, в диапазоне приблизительно от 5 мг/кг массы тела до приблизительно 100 мг/кг массы тела, приблизительно от 5 микрограмм/кг массы тела до приблизительно 500 миллиграмм/кг массы тела и т.д. исходя из описанных выше чисел.
Биологически активный компонент может присутствовать в имплантируемом устройстве при любом подходящем массовом проценте, включая введение более высоких массовых процентов, такое как введение до 40 масс.% в расчете на массу имплантируемого устройства или на массу устройства. В одном из аспектов изобретения имплантируемые устройства можно применять для изменения фармакокинетики биологически активного компонента.
Композиции, содержащие имплантируемые устройства, можно вводить любому желательному субъекту. Субъект может представлять собой позвоночное животное, такое как млекопитающее, рыба, птица, рептилия или амфибия. Субъектом для описанных здесь способов может являться, например, человек, примат, отличный от человека, лошадь, свинья, кролик, собака, овца, коза, корова, кошка, морская свинка или грызун. Условия не учитывают конкретный возраст или пол. Таким образом, предполагается, что изобретение охватывает взрослых и новорожденных субъектов, а также зародышей, будь то самец или самка. Композиции также можно вводить любым подходящим способом, включая парентеральный, пероральный способ, в том числе. В одном из предпочтительных аспектов изобретения композицию можно водить субъекту в виде инъекции.
Можно изготовить различные модификации и варианты описанных здесь соединений, композитов, наборов, изделий, устройств, композиций и способов. Другие аспекты описанных здесь соединений, композитов, наборов, изделий, устройств, композиций и способов будут очевидны из описания и практического осуществления описанных здесь соединений, композитов, наборов, изделий, устройств, композиций и способов. Считается, что описание и примеры должны рассматриваться как иллюстративные.

Изобретение относится к медицине. Описаны имплантируемые устройства с различными вариантами загрузки биологически активного компонента, которые можно выбирать и применять для создания профиля пролонгированного высвобождения или профиля высвобождения с низким начальным выбросом биологически активного компонента из имплантированного устройства. 10 з.п. ф-лы, 2 ил.
1. Имплантируемое устройство, содержащие продольную основную часть, имеющую внутреннее ядро, содержащее продольную поверхность, окруженную полимерной оболочкой, и открытые торцевые поверхности на ближнем и дальнем концах, которые не окружены полимерной оболочкой;
в котором полимерная оболочка содержит продольную наружную поверхность, которая практически коэкстенсивна продольной поверхности внутреннего ядра;
в котором, по меньшей мере, внутреннее ядро или полимерная оболочка содержит биоразлагаемый полимер;
в котором как внутреннее ядро, так и полимерная оболочка содержат растворенный или диспергированный в них биологически активный компонент; и
в котором внутреннее ядро и полимерная оболочка имеют соответствующие концентрации биологически активного компонента, причем концентрация биологически активного компонента в полимерной оболочке отличается от концентрации биологически активного компонента во внутреннем ядре; и
причем биологически активный компонент внутреннего ядра и полимерной оболочки присутствует в имплантируемом устройстве до 40% в расчете на массу имплантируемого устройства.
2. Имплантируемое устройство по п.1, в котором на одну или несколько торцевых поверхностей на ближнем конце, дальнем конце или на продольную наружную поверхность нанесено покрытие из биологически совместимого или биоразлагаемого полимера.
3. Имплантируемое устройство по п.1, в котором на одну или несколько торцевых поверхностей на ближнем конце, дальнем конце или на продольную наружную поверхность нанесен в виде покрытия биологически активный компонент, который является тем же самым или отличается от биологически активного компонента, растворенного или диспергированного во внутреннем ядре и/или полимерной мембранной оболочке.
4. Имплантируемое устройство по п.1, в котором полимерная оболочка содержит полимер, который создает защитную мембрану вокруг внутреннего ядра.
5. Имплантируемое устройство по п.1, в котором внутреннее ядро продольной основной части содержит поли(лактид), поли(гликолид), поли(капролактон), сополимер лактида с гликолидом или их смесь, комбинацию или сополимер.
6. Имплантируемое устройство по п.1, в котором полимерная оболочка продольной основной части содержит поли(лактид), поли(гликолид), поли(капролактон), сополимер лактида с гликолидом или их смесь, комбинацию или сополимер.
7. Имплантируемое устройство по п.1, в котором как внутреннее ядро, так и полимерная оболочка содержат биоразлагаемый полимер.
8. Имплантируемое устройство по п.7, в котором как внутреннее ядро, так и полимерная оболочка продольной основной части содержат поли(лактид), поли(гликолид), поли(капролактон), сополимер лактида с гликолидом или их смесь, комбинацию или сополимер.
9. Имплантируемое устройство по п.1, в котором биологически активный компонент является водорастворимым.
10. Имплантируемое устройство по п.1, в котором биологически активный компонент является водонерастворимым.
11. Имплантируемое устройство по п.1, в котором имплантируемое устройство сконфигурировано для загружения в устройство для инъекции.
| US 2007116738 A1, 24.05.2007 | |||
| Способ и приспособление для нагревания хлебопекарных камер | 1923 |
|
SU2003A1 |
| Станок для изготовления деревянных ниточных катушек из цилиндрических, снабженных осевым отверстием, заготовок | 1923 |
|
SU2008A1 |
Авторы
Даты
2015-04-10—Публикация
2010-09-22—Подача