Изобретение относится к медицине, конкретно к респираторной медицине, и может быть использовано в медицинских учреждениях, оснащенных радиодиагностическими лабораториями.
Тромбоэмболия легочной артерии (ТЭЛА), согласно данным Всемирной организации здравоохранения, является третьей по распространенности причиной смерти при сердечно-сосудистых заболеваниях после острого коронарного синдрома и инсульта [1]. Следует сказать, что своевременная терапия ТЭЛА позволяет уменьшить летальность при этом заболевании в 3-4 раза [2]. Общеизвестно, что гемодинамические нарушения, вызываемые ТЭЛА, обусловлены уменьшением емкости сосудистого русла с последующим повышением сосудистого сопротивления в малом круге кровообращения (МКК), развитием легочной гипертензии и правожелудочковой недостаточности [3]. По данным международного регистра ICOPER, именно дисфункция правого желудочка является основной причиной внутригоспитальной летальности пациентов острой ТЭЛА [4]. Таким образом, главным патофизиологическим фактором, который определяет тяжесть заболевания и краткосрочный прогноз течения заболевания, является именно наличие или отсутствие правожелудочковой недостаточности. При этом, как показали результаты исследований Rutger W. van der Meer с соавт., отсутствие признаков дисфункции ПЖ имеет 100% отрицательное предсказательное значение в отношении неблагоприятных исходов ТЭЛА в течение 3 месяцев наблюдения [5].
Хроническое течение тромбоэмболии легочной артерии (в последние годы используют термин хроническая постэмболическая легочная гипертензия) обусловлено постепенным ростом давления в легочной артерии, вызванным нелизированными тромбоэмболами, дальнейшей их структурной перестройкой, а также периодическими обострениями тромбоэмболии мелких ветвей легочной артерии с развитием повторных инфарктов легких, что приводит к увеличению легочно-сосудистого сопротивления, повышению давления в малом круге кровообращения, развитию правожелудочковой сердечной недостаточности [6].
В последние годы для диагностики острой ТЭЛА все чаще используют рентгеноконтрастную компьютерно-томографическую ангиографию (РКТА), которая практически полностью заменила прямую рентгеноконтрастную ангиопульмонографию [7]. Однако применение контрастных средств противопоказано больным, предрасположенным к аллергическим реакциям, с почечной недостаточностью, миеломной болезнью, а также беременным и кормящим женщинам [8]. Важно отметить, что по данным Международной комиссии по радиологической защите лучевая нагрузка на организм пациента при РКТ-ангиографии органов грудной клетки относительно высока и составляет от 2,0 до 6,0 мЗв [9].
Исторически первым и длительное время «золотым стандартом» в диагностике ХПЭЛГ была ангиопульмонография. Основными ангиографическими признаками этого заболевания являются сужения и рубцовые перемычки (перетяжки, webs) - следствие неполной реканализации просвета сосуда, а также «обрывы» сосудов, часто имеющие мешкообразную форму, - результат полной окклюзии соответствующей ветви легочной артерии. В отличие от острой ТЭЛА, дефекты наполнения не характерны для этой патологии, а если встречаются, то расположены всегда эксцентрично, непосредственно на стенке сосуда. С появлением современных многоспиральных компьютерных томографов ангиография утратила свое былое значение, поскольку, с одной стороны, является инвазивным методом и чревата рядом осложнений, а с другой, КТ позволяет получить представление не только о степени поражения легочной артерии, но и о состоянии легочной ткани, что делает ее более информативным методом исследования [10]. Тем не менее, ряд заболеваний имеет схожую картину по данным методов визуальной диагностики: саркома легочной артерии, хронический фиброзирующий медиастинит, артериит Такаясу. Однако в ряде случаев различия в клинической и визуальной картине столь незначительны, что окончательный диагноз можно установить только во время операции [11].
Таким образом, рентгеноконтрастная компьютерная томография занимает лидирующие позиции в диагностике как острой ТЭЛА, так и ХТЭЛГ, которая позволяет оценить не только специфические изменения в сосудистом русле легких, но и выявить дисфункцию правого желудочка сердца. Однако в проанализированной нами литературе адекватного прототипа дифференциальной диагностики острой ТЭЛА и ХТЭЛГ нами не обнаружено. Кроме того, как ранее нами подчеркивалось, несмотря на все достоинства рентгеноконтрастных методов исследования, имеется ряд негативных моментов, которые ограничены или противопоказано их применение немалой категории больных [8].
Радионуклидные способы выявления вентиляционно-перфузионных нарушений и оценки функции сердца завоевывают все большую популярность в диагностике и оценке результатов лечения ТЭЛА.
Подозрение на тромбоэмболию легочной артерии является абсолютным показанием к проведению перфузионной пульмоносцинтиграфии (П).
Достоверность диагноза тромбоэмболии ветвей легочной артерии значительно увеличивается при сочетании перфузионной и вентиляционной (В) сцинтиграфии легких. Наличие нарушений перфузии и нормальной легочной вентиляции (полное В/П-несоответствие) является классической картиной проявления ТЭЛА. Совпадение перфузионных нарушений легких с вентиляционными (полное В/П-соответствие) исключает тромбоэмболию легочной артерии.
Известен хорошо зарекомендовавший сцинтиграфический способ оценки функциональной активности сердца - равновесная радионуклидная вентрикулография (РРНВГ), которая по информативности в определении сократительной способности левого желудочка не уступает рентгеноконтрастной вентрикулографии.
Недостатком данного способа является невозможность в полной мере оценить функцию правого желудочка сердца.
В последние годы все большей популярностью в оценке функции правого желудочка пользуется ЭКГ-синхронизированная радионуклидная томографическая вентрикулография (РТВГ). Данный метод позволяет получать трехмерное изображение желудочков сердца. Это в свою очередь создает возможность более точного вычисления объемных показателей правого желудочка, а также его систолической и диастолической функции. Однако применительно к диагностике правожелудочковой недостаточности у больных с острой и хронической тромбоэмболией легочной артерии данный метод не применялся в связи с широким внедрением для этих целей методов рентгеноконтрастной компьютерной томовентрикулографии [11].
Недостатком радионуклидных методов исследования, применительно к дифференциальной диагностике острой и хронической ТЭЛА, является отсутствие единых методических приемов проведения исследования, обработки получаемой информации и, как следствие этого, неоднозначная трактовка результатов, вследствие чего применительно к дифференцированию и прогнозу течения указанных заболеваний данный метод не нашел своего применения.
Адекватного прототипа в проанализированной литературе не обнаружено.
Задачей предлагаемого изобретения является создание способа дифференциальной диагностики острой тромбоэмболии легочной артерии и хронической постэмболической легочной гипертензии.
Поставленная задача решается путем проведения вентиляционно-перфузионной сцинтиграфии легких и равновесной радионуклидной вентрикулографии в томографическом режиме, с последующим качественным анализом вентиляционно-перфузионных пульмоносцинтиграмм, определением вентиляционно-перфузионного соответствия (В/П), соотношения поперечных размеров радиоактивного пула крови правого желудочка сердца к левому (ПЖ/ЛЖ). При полном В/П-несоответствии, четкости контуров выявленных перфузионных дефектов накопления радиофармпрепарата (РФП), а также при соотношении поперечных размеров радиоактивного пула крови правого желудочка сердца к левому (ПЖ/ЛЖ) менее 1,0 диагностируют острую ТЭЛА, при неполном В/П-соответствии, неправильности формы, нечеткости контуров перфузионных дефектов накоплении РФП, перераспределении перфузионного радиофармпрепарата в верхние отделы легких, а также увеличении показателя ПЖ/ЛЖ выше 1,0 диагностируют хроническую постэмболическую легочную гипертензию.
Новым в предлагаемом способе является: проведение равновесной радионуклидной вентрикулографии в томографическом режиме с последующим определением соотношения поперечных размеров радиоактивного пула крови правого желудочка сердца к левому (ПЖ/ЛЖ).
Комплексное радионуклидное исследование легких и сердца позволяет оценить легочную вентиляцию и перфузию, а также функцию правого желудочка сердца. При различных заболеваниях легких, в частности острой и хронической ТЭЛА, в разной степени нарушаются звенья этого сложного физиологического механизма.
Техническим результатом предлагаемого в качестве изобретения способа является повышение точности дифференциальной диагностики острой тромбоэмболии легочной артерии и хронической постэмболической легочной гипертензии для своевременного назначения оптимальной терапии.
Тот факт, что клиническое проявление и рентгенологические данные указанных патологических состояний во многом идентичны, то применение комплексного радионуклидного исследования позволит дифференцировать острую ТЭЛА от ХПЭЛГ. Подобное предположение обусловлено тем, что гемодинамические нарушения, вызываемые ТЭЛА, обусловлены уменьшением емкости сосудистого русла с последующим повышением сосудистого сопротивления в малом круге кровообращения (МКК), развитием легочной гипертензии и правожелудочковой недостаточности, которая является основной причиной внутригоспитальной летальности [4]. Таким образом, главным патофизиологическим фактором, который определяет тяжесть заболевания и краткосрочный прогноз течения острой ТЭЛА, является именно наличие или отсутствие правожелудочковой дисфункции.
Патоморфологическим субстратом хронической ТЭЛА являются нелизированные тромбоэмболы, которые со временем плотно срастаются со стенкой сосуда и покрываются слоем неоинтимы. Дальнейшая структурная перестройка тромбоэмбола ведет к формированию соединительнотканых тяжей, бляшек и перегородок в легочных сосудах, что приводит к увеличению сосудистого сопротивления и росту давления в легочной артерии, в результате чего развивается правожелудочковая недостаточность, которая является причиной летального исхода у таких пациентов [6]. В дополнение к этому при указанной патологии тромбоэмболия легочной артерии носит, как правило, рецидивирующий характер, что приводит к развитию микроинфарктных пневмоний с развитием в дальнейшем хронической дыхательной недостаточности. В связи с этим, к увеличенному легочно-сосудистому сопротивлению присоединяется и хроническая дыхательная недостаточность, что способствует прогрессированию правожелудочковой недостаточности.
Следовательно, сцинтиграфические показатели, отражающие микроциркуляторные и вентиляционные нарушения в легких, дисфункцию ПЖ при острой и хронической ТЭЛА, будут иметь существенные различия.
Новые признаки проявили в заявляемой совокупности новые свойства, явным образом не вытекающие из уровня техники в данной области и не являющиеся очевидными для специалиста.
Идентичной совокупности признаков не обнаружено в патентной и научно-медицинской литературе.
Предлагаемый способ может быть использован в здравоохранении для повышения качества диагностики и лечения легочных заболеваний.
Исходя из вышеизложенного, следует считать предлагаемое изобретение соответствующим критериям «Новизна», «Изобретательский уровень», «Промышленная применяемость».
Изобретение будет понятно из следующего описания и предложенных к нему рисунков.
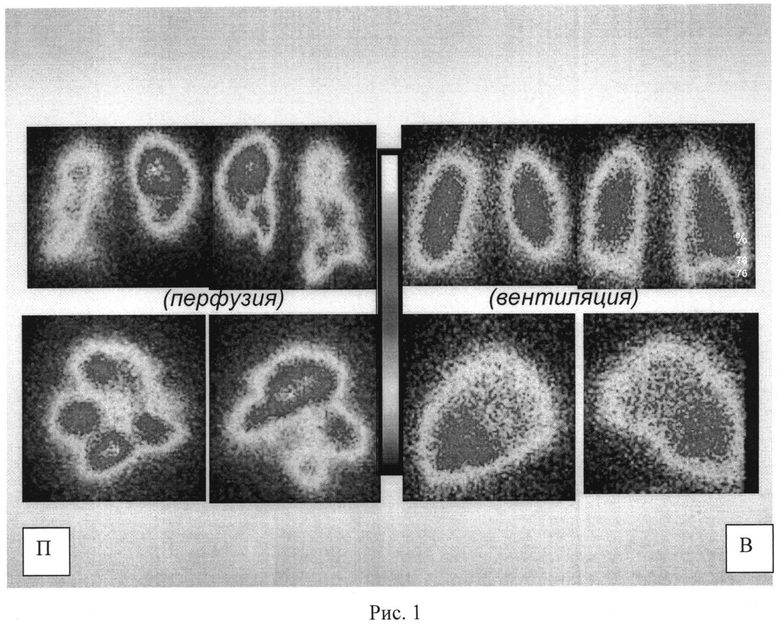
На рис. 1 представлены множественные несовпадающие дефекты накопления РФП в легких (полное В/П-несоответствие) с относительно четкими контурами перфузионных нарушений, а также показателя соотношения поперечных размеров радиоактивного пула крови правого желудочка сердца к левому (ПЖ/ЛЖ=29,0/38,4=0,75-<1,0), что свидетельствует об острой тромбоэмболии легочной артерии.
П - перфузионные пульмоносцинтиграммы; В - вентиляционные пульмоносцинтиграммы; Т - поперечные томовентрикулограммы радиоактивного пула крови; ПЖ - правый желудочек; ЛЖ - левый желудочек.
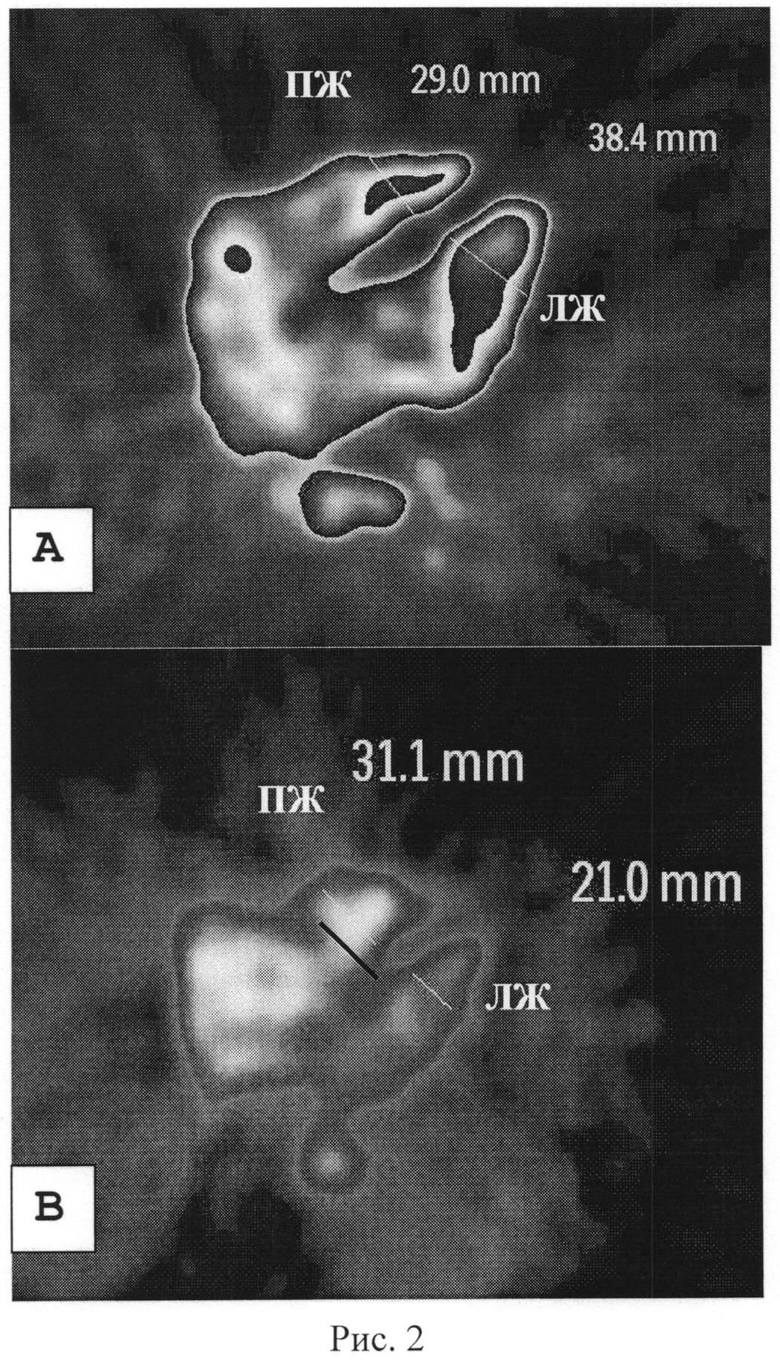
На рис. 2 представлены поперечные срезы изображения радиоактивного кровяного пула по данным радионуклидных томовентрикулограмм. Линиями отмечены размеры радиоактивного пула крови правого и левого желудочков сердца по малой оси. А - пациент без признаков дисфункции ПЖ; Б - пациент с признаками дисфункции ПЖ (ПЖ/ЛЖ=31,1/21,0=1,48>1,0).
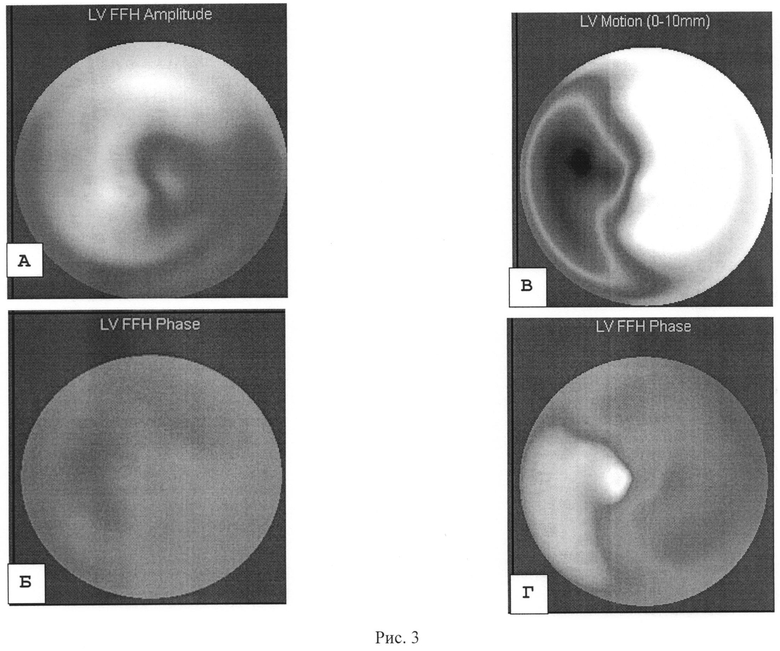
На рис. 3 представлены полярные карты радионуклидных томовентрикулограмм амплитудных (А, Г) и фазовых (Б, В) сокращений желудочков сердца в норме (А, Б), при гипокинезе (В) и диссинхронии (Г) межжелудочковой перегородки.
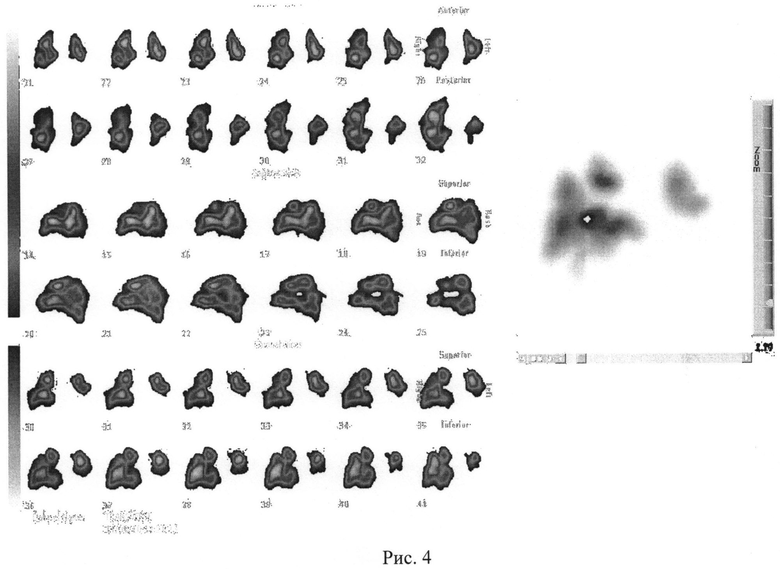
На рис. 4 представлена перфузионная томосцинтиграфия легких с 99mcTc - макротехом больной Ч. В правом легком отмечаются клиновидные дефекты перфузии в проекции 2, 6, 10 бронхолегочных сегментов. В левом легком отмечается снижение перфузии в проекции 1, 2 и субсегментарно 6, 9 бронхолегочных сегментов. Дефекты перфузии четкие, с ровными контурами, клиновидной формы, соответствующие бронхолегочным сегментам. Количество пораженных бронхолегочных сегментов = 7.
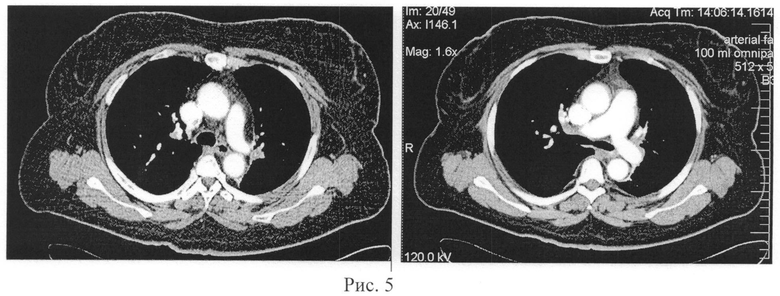
На рис. 5 представлена КТ-ангиопульмонограмма пациентки Ч. с острой ТЭЛА. На томограммах органов грудной клетки в аксиальной проекции с в/в болюсным контрастированием выявляются: тромбы верхнедолевой артерии правого легкого, верхнедолевой артерии левого легкого, легочный ствол и главные легочные артерии незначительно расширены.
На рис. 6 представлена перфузионная сцинтиграфия легких с 99mcTc - макротехом больного К. Визуально границы между дефектами перфузии и условно интактной легочной тканью нечеткие, отмечается мозаичность перфузии. Количество пораженных бронхолегочных сегментов=5
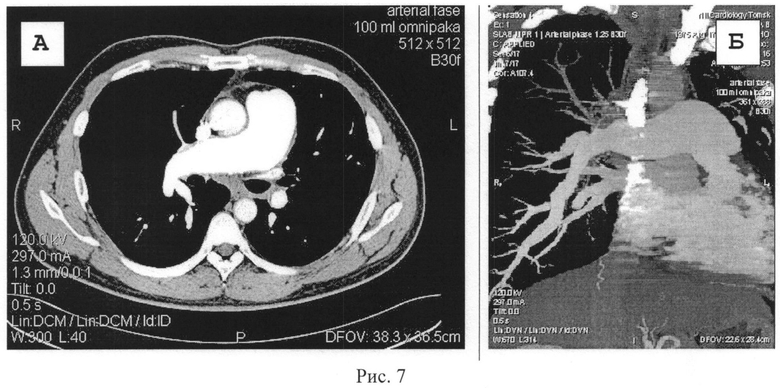
На рис. 7 представлена КТ-ангиопульмонограмма пациента К. с хронической постэмболической легочной гипертензией. На томограммах органов грудной клетки в аксиальной проекции (А) с в/в болюсным контрастированием и на MIP-реконструкции (Б) выявляется: значительное расширение легочного ствола и правой легочной артерии, обеднение легочного рисунка в верхней доле правого легкого, значительное расширение артериальных сосудов нижней доли.
Способ осуществляют следующим образом.
При выполнении перфузионной сцинтиграфии легких в качестве радиоактивного индикатора используют макроагрегаты альбумина (МАА) человеческой сыворотки, меченные 99mcTc («Макротех», Диамед, Россия). В условиях процедурного кабинета, в кубитальную вену руки вводят свежеприготовленный раствор РФП в дозе от 55,5 до 148 МБк в объеме 0,5-3 мл. Запись сцинтиграфического исследования проводят через 5-10 мин после инъекции радиофармпрепарата. Планарное исследование выполняется в 6 стандартных проекциях: передней и задней прямой (ANT и POST), правой и левой латеральной (RL и LL), правой и левой передне-косой (RAO и LAO). Исследование в томографическом режиме выполняют при положении детекторов по отношению друг к другу на 180°; оборот гентри составляет 360°; всего производится запись 128 проекций в матрицу 64×64 пикселя. Время на одну проекцию составляло 15 секунд. После окончания исследования нативные данные подвергались обработке (AutoSPECT + ver: 3.5; алгоритм реконструкции 3D-OSEM), в результате которой получали серию поперечных, фронтальных и сагиттальных пульмонотомосцинтиграмм.
Интерпретация полученных данных основана на сопоставлении результатов вентиляционной и перфузионной сцинтиграфии легких. Патогномоничной для ТЭЛА картиной является наличие областей с нормальной вентиляцией и сниженной перфузией. Для ТЭЛА характерны дефекты перфузии треугольной формы, с четкими контурами, соответствующие по расположению бассейну тромбированного сосуда. Отсутствие перфузионных дефектов, независимо от состояния вентиляции, а также наличие совпадающих вентиляционно-перфузионных дефектов с высокой вероятностью исключают ТЭЛА.
Лучевая нагрузка на все тело при проведении вентиляционно-перфузионной сцинтиграфии легких составляла от 0,28-0,9 мЗв.
Перед проведением радионуклидной равновесной томовентрикулографии (РТВГ) осуществляется метка эритроцитов в условиях «in vivo». Для этого в левую кубитальную вену руки вводится 2-2,5 мл стерильного раствора пирофосфата (препарат «Пирфотех», фирмы «Диамед», Россия). Затем, через 15 мин после инъекции вводится в/в раствор 99mcTc - натрия пертехнетата в дозе 540 мБк, пациент укладывается на томографический стол, на переднюю грудную стенку пациента устанавливают электроды ЭКГ-синхронизирующего устройства. Положение электродов следующее: отрицательный электрод фиксирован непосредственно под правой ключицей по среднеключичной линии; положительный электрод - выше реберного края, на 2-4 см ниже позиций V4, V5 или V6; заземляющий электрод - в той же позиции, только с правой стороны. После наложения электродов проводят визуальный анализ наличия комплексов QRS на экране синхронизирующего устройства.
Детекторы гамма-камеры устанавливают в положение 90° по отношению друг к другу. Томографический стол гамма-камеры устанавливают так, чтобы центр детекторов соответствовал области сердца. Запись информации выполняется в матрицу 64×64 пикселя в 64 проекциях (время экспозиции одной проекции 45 сек, оборот гентри 180°).
Представительный сердечный цикл (RR-интервал) разделен на 16 кадров. Синхронизация записи сокращения сердца с ЭКГ осуществляется в фиксированном режиме, синхронно с учетом коррекции аритмии и без него.
Обработка томовентрикулограмм включает в себя формирование аксиальных срезов исследуемой области (по серии нативных изображений) и последующую реконструкцию сечений сердца по короткой оси при помощи программы AutoSPECT + ver: 3.5 (фильтр Butterworth).
Анализ полученной информации осуществляли при помощи специализированной программы Quantitative Blood Pool SPECT 2.0 (Cedars-Sinai Medical Center).
Выявления дисфункции правых отделов сердца у пациентов с ТЭЛА осуществляется вычислением отношения поперечных размеров правого желудочка сердца к левому (RV/LV) на реконструируемых усредненных аксиальных томографических срезах РТВГ (рис. 2).
Пример 1
Больная Ч. 47 лет, история болезни №8680.
Проходила обследование и лечение в отделении сердечно-сосудистой хирургии НИИ кардиологии СО РАМН с 22.11.10 г. по 07.12.10 г. с диагнозом: Острый тромбоз большой подкожной вены с обеих сторон. Варикозное расширение вен нижних конечностей. Хроническая венозная недостаточность 2 ст. Осложнение: субмассивная ТЭЛА с обеих сторон. Сопутствующие заб.: Гипертоническая болезнь Пет., риск 3. Ожирение 3 ст. Миома матки.
Начало и развитие настоящего заболевания: жалобы на слабость и головокружение, чувство дискомфорта за грудиной, давящая боль с иррадиацией за грудину. Жалобы сохранялись около 1 часа, после чего ощутила нарастающую нехватку воздуха. Приняла 1 таблетку нитроглицерина, однако состояние улучшилось незначительно. Вскоре боль и слабость усилились, вновь появилось головокружение. В горизонтальном положении почувствовала некоторое облегчение. В порядке скорой медицинской помощи доставлена в специализированное медицинское учреждение.
При объективном обследовании: Общее состояние пациентки удовлетворительное. Органы дыхания: Перкуторно - звук легочный. Дыхание жесткое. Хрипов нет. ЧДД 18 в/мин. Сердечно-сосудистая система: Перкуторно - границы сердца: левая совпадает с верхушечным толчком, располагается по срединно-ключичной линии в V межреберье, верхняя - во II межреберье справа по правому краю грудины, правая - по правому краю грудины. Тоны сердца ясные, ритмичные. ЧСС - 80 уд/мин. Артериальное давление 130/80 мм рт.ст. Пульс 80 в/мин удовлетворительного наполнения, ровный.
Электрокардиография: признаки гипертрофии левого желудочка.
Рентгенография органов грудной клетки: ЛВГ 1 ст. Пневмофиброз. Умеренное увеличение левых отделов сердца.
Дуплексное сканирование вен нижних конечностей: Нижняя полая вена, подвздошные вены проходимы с обеих сторон, патологических структур в просвете не определяется. Кровоток синхронизирован с дыхательным циклом. Бедренные, подколенные вены с обеих сторон проходимы, патологических структур в просвете не выявлено, компрессивность сохранена. Берцовые вены проходимы, компрессивность сохранена. Спонтанный кровоток по берцовым венам отсутствует, при дистальной компрессии удовлетворительный. Подкожные вены: с обеих сторон в просвете большой подкожной вены лоцируются гетерогенные структуры, компрессивность большой подкожной вены снижена, регистрируется фрагментарный кровоток.
Заключение: признаков тромбоза глубоких вен не выявлено. Признаки тромбоза в бассейне большой подкожной вены с обеих сторон, частичная реканализация.
Д - димер: положительный.
Перфузионная сцинтиграфия легких (рис. 4): На серии пульмоносцинтиграмм, полученных при выполнении исследования в томографическом режиме, визуализируются оба легких. В правом легком отмечаются клиновидные дефекты перфузии в проекции 2, 6, 10 бронхолегочных сегментов. В левом легком отмечается снижение перфузии в проекции 1, 2 и субсегментарно 6, 9 бронхолегочных сегментов. Субмассивная ТЭЛА ветвей обоих легких.
Рентгеновская компьютерная томография органов грудной клетки с контрастным усилением (рис. 5): Тромбоэмболия обеих легочных артерий, тотальная окклюзия обеих нижне-долевых артерий и ветвей базальной пирамиды, кроме артерии S8 слева, дефекты контрастирования в верхне-долевых артериях с обеих сторон, язычковых артериях слева, в артериях S6 с обеих сторон.
Эхокардиография: ЛП - 39 мм, ПЖ - 32 мм, МЖП - 10, мм, ЗСЛЖ - 10,5 мм, ММ - 159 г, ИММ - 79 г/м2, КДО - 81 мл, КСО - 33 мл, ФВ - 59%, СДПЖ - 53 мм рт.ст., MKreg- 0-1 ст., TKreg - 1 ст.
Умеренная дилатация правых отделов сердца, незначительное расширение легочного ствола, признаков гипертрофии правого желудочка нет. Глобальная сократимость ЛЖ в норме, правого желудочка нормальная или незначительно снижена. Нарушений локальной сократимости не выявлено. Трикуспидальная регургитация 1 ст., створки тонкие. Диастолическая дисфункция (замедление расслабления миокарда). Систолическое давление правого желудочка умеренно повышено. Перикард не изменен.
Радионуклидная томовентрикулография: По данным сцинтиграфического исследования объемные, скоростные показатели, а также фракция выброса левого желудочка сердца в пределах нормы. Фракция выброса правого желудочка в пределах нормы. Отмечается увеличение КДО и КСО ПЖ. Зоны диссинхронии отмечаются в области верхушки и базальных отделов передней стенки ПЖ. Отношение поперечных размеров радиоактивного пула крови правого желудочка сердца к левому (ПЖ/ЛЖ) составило 0,76 (рис. 2A).
Таким образом, с учетом среднего объема поражения легочного русла, наличия дефектов перфузии с четкими контурами, отношение ПЖ/ЛЖ меньше 1,0, выявленные изменения можно трактовать как сцинтиграфические признаки острой ТЭЛА.
Пример 2
Больной К. 35 лет, история болезни №4593.
Проходил обследование и лечение в кардиохирургическом отделении НИИ кардиологии СО РАМН с 07.06.11 г. по 18.07.11 г. с диагнозом: Хроническая тромбоэмболия ветвей легочной артерии. Сопутствующие заб.: Наследственная тромбофилия. Вторичная полицитемия (гипоксемическая). Реактивная гепатопатия.
Жалобы при поступлении: на одышку смешанного характера, ощущение перебоев в работе сердца, общую слабость, повышение артериального давления (180/110 мм рт.ст.), сухой кашель.
Начало и развитие настоящего заболевания: Считает себя больным с 2002 г. после перенесенной пневмонии. В последующем отметил появление одышки, слабости. При обследовании у участкового терапевта по поводу вышеуказанных жалоб обнаружено повышение гемоглобина и эритроцитов в общем анализе крови. Проконсультирован гематологом, находился на обследовании в гематологическом отделении в феврале 2011 г., выставлен диагноз наследственной тромбофилии.
Рентгенография органов грудной клетки: Очагово-инфильтративных изменений ткани не выявлено. Нарушение гемодинамики малого круга по смешанному типу - ЛВГ - 1 ст., ЛАГ - 2 ст. Корни умеренно расширенные - правая нисходящая артерия - 1,9 см, структурные. Сердце умеренно увеличено в поперечнике, талия выбухает за счет дуги легочной артерии.
Перфузионная сцинтиграфия легких (рис. 6): Сцинтиграфические признаки нарушения капиллярного кровотока в проекции 6, 8, 9 и 10 бронхолегочных сегментов левого легкого и проекции 3 бронхолегочного сегмента правого легкого.
Дуплексное сканирование вен нижних конечностей: Нижняя полая вена, вены нижних конечностей проходимы. Просвет свободный. Тромбов нет. Кровоток симметричный, удовлетворительный.
Эхокардиография: ЛП - 40 мм, ПЖ - 36 мм, МЖП - 8,5 мм, ЗСЛЖ - 8,5 мм, ММ - 122 г, ИММ - 69 г/м2, КДОЛЖ - 89 мл, КСОЛЖ - 24 мл, ФВЛЖ - 73%, СДПЖ - 42 мм рт.ст., MKreg - 0-1 ст., TKreg - 1 ст.
Умеренная дилатация правых отделов. Умеренная гипертрофия правого желудочка. Асинхронное сокращение стенок ЛЖ. Общая сократимость ЛЖ в норме, сократимость ПЖ умеренно снижена. Нарушений локальной сократимости нет. Диастолическая дисфункция (замедление расслабления миокарда). Митральная регургитация 0-1 ст., створки тонкие. Несколько расширено фиброзное кольцо трикуспидального клапана, створки тонкие, подвижные, регургитация 1 ст. Небольшое повышение СДПЖ. Жидкости в перикарде и плевральных полостях нет.
Радионуклидная томовентрикулография: При визуальном анализе изображения сердечно-сосудистого кровяного пула на радионуклидных томовентрикулограммах отмечается расширение легочного ствола и главных легочных артерий. Правые отделы сердца увеличены в размерах, в большей степени правое предсердие. Имеет место увеличение объемных показателей (КДО и КСО), уменьшение УО и ФВ правого желудочка. Скоростные показатели ПЖ снижены. При визуальном анализе амплитудной и фазовой полярных карт левого желудочка отмечается снижение сократимости и диссинхрония межжелудочковой перегородки (рис. 3В, Г). Отношение поперечных размеров радиоактивного пула крови правого желудочка сердца к левому (ПЖ/ЛЖ) составило 1,48 (рис. 2Б).
По данным сцинтиграфического исследования объемные показатели, а также фракция выброса левого желудочка сердца в пределах нормы.
Рентгеновская компьютерная томография органов грудной клетки с контрастным усилением (Рис. 7): Умеренный диффузный пневмофиброз, участки локального пневмофиброза в обоих легких, высокая легочная гипертензия, дефект контрастирования верхне-долевой артерии справа, язычковых артерий слева, выраженная асимметрия сосудистого рисунка обоих легких, резкое сужение артерий верхней и средней долей справа, язычковых сегментов слева, S6, S10 слева, в нижней доле справа. Неровность контуров легочного ствола, участки линейного обызвествления в проксимальном отделе правой легочной артерии, утолщение стенок правой легочной артерии, плевро-диафрагмальные спайки с обеих сторон, больше слева.
Таким образом, наличие систоло-диастолической дисфункции и повышенное систолическое давление в правом желудочке в сочетании с нечеткими дефектами перфузии и перераспределением РФП в верхние отделы легких, превышение показателя отношения ПЖ/ЛЖ выше 1,0, можно расценивать как патогномоничный признак хронической постэмболической легочной гипертензии.
Известно, что клинические признаки в большинстве случаев не позволяют дифференцировать острую и хроническую формы тромбоэмболии. Предлагаемый способ в сравнение по точности с прототипом позволяет провести дифференциальную диагностику между острой тромбоэмболии и хронической постэмболической легочной гипертензией и, как следствие, своевременно назначить адекватную терапию.
Способ апробирован по данным полного клинико-инструментального исследования на 62 больных с острой тромбоэмболией легочной артерии и 20 больных с хронической постэмболической легочной гипертензией.
ЛИТЕРАТУРА
1. Guidelines on diagnosis and management of acute pulmonary embolism. Task Force on Pulmonary Embolism, European Society of Cardiology / A. Torbicki, E. J. R. van Beek, B. Charbonnier et al. // European Heart Journal. 2000. Vol. 21. P. 1301-1336.
2. Рич С. Тромбоэмболия легочной артерии // Кардиология в таблицах и схемах / под ред. М. Фрида, С. Грайнс. М.: Практика, 1996. С. 538-548.
3. European Society of Cardiology Committee for Practice Guidelines (CPG). Guidelines on the diagnosis and management of acute pulmonary embolism: the Task Force for the Diagnosis and Management of Acute Pulmonary Embolism of the European Society of Cardiology (ESC) / A. Torbicki, A. Perrier, S. Konstantinides et al. // Eur. Heart J. 2008. Vol.29, №18. P. 2276-2315.
4. Goldhaber S.Z., Visani L., De Rosa M. Acute pulmonary embolism: clinical outcomes in the International Cooperative Pulmonary Embolism Registry (ICOPER) // Lancet. 1999. Vol. 353. P. 1386-1389.
5. Right Ventricular Dysfunction and Pulmonary Obstruction Index at Helical CT: Prediction of Clinical Outcome during 3-month Follow-up in Patients with Acute Pulmonary Embolism. Radiology / R.W. Van der Meer, Μ. T. Pattynama Peter et al. // Cardiac Imaging. 2005. Vol.235, №3. P. 800-802.
6. Флебология / Под ред. B.C. Савельева. Μ.: Медицина, 2001. 660 с.
7. Schoepf UJ. Diagnosing pulmonary embolism: time to rewrite the textbooks // Int. J. Cardiovasc. Imaging. 2005. Vol. 21. P. 155-163.
8. International Atomic Energy Agency Consultants′ Group. Is the lung scan alive and well? Facts and controversies in defining the role of lung scintigraphy for the diagnosis of pulmonary embolism in the era of MDCT / J.H. Reid, E.E. Coche, T. Inoue et al. // Eur. J. Nucl. Med. Mol. Imaging. 2009. Vol. 36. P. 505-521.
9. Holm L.-E., Cox R. Published on behalf of the International Commission on Radiological Protection (ICRP) by Elsevier Ltd. 2007.
10. Панькова Α.Η. Радионуклидная диагностика нарушений микроциркуляции малого круга кровообращения и дисфункции правого желудолчка у пациентов с тромбоэмболией легочной артерии. // Дисс. на соиск. уч. ст. к.м.н. Томск, 2011, с. 65-92.
11. Яблонский П.К., Павлушков Е.В., Федорова Т.Α., Головин В.Н. Хроническая тромбоэмболическая легочная гипертензия // Новые Санкт-Петербургские врачебные ведомости. 2009. №2 (48). С. 52-59.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ВЕДЕНИЯ ПАЦИЕНТОВ ПРИ ТРОМБОЭМБОЛИИ ЛЕГОЧНОЙ АРТЕРИИ | 2013 |
|
RU2526469C1 |
| СПОСОБ КЛИНИЧЕСКОГО ОПРЕДЕЛЕНИЯ ВЕРОЯТНОСТИ НЕМАССИВНОЙ ТРОМБОЭМБОЛИИ ЛЕГОЧНОЙ АРТЕРИИ У ПАЦИЕНТОК, ПРИНИМАЮЩИХ КОМБИНИРОВАННЫЕ ОРАЛЬНЫЕ КОНТРАЦЕПТИВЫ | 2015 |
|
RU2601661C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ОСТРОЙ ТРОМБОЭМБОЛИИ ЛЕГОЧНОЙ АРТЕРИИ ВЫСОКОГО И ПРОМЕЖУТОЧНОГО ВЫСОКОГО РИСКА | 2022 |
|
RU2797848C1 |
| СПОСОБ ОПТИМИЗАЦИИ ДИАГНОСТИКИ ТРОМБОЭМБОЛИИ ЛЕГОЧНОЙ АРТЕРИИ | 2006 |
|
RU2334468C1 |
| Способ количественной оценки нарушений перфузии миокарда правого желудочка по данным однофотонно-эмиссионной компьютерной томографии | 2016 |
|
RU2628367C1 |
| СПОСОБ ДИАГНОСТИКИ ТРОМБОЭМБОЛИИ МЕЛКИХ ВЕТВЕЙ ЛЕГОЧНОЙ АРТЕРИИ У ПАЦИЕНТОВ С ИМПЛАНТИРОВАННЫМИ VVI-ЭЛЕКТРОКАРДИОСТИМУЛЯТОРАМИ | 2004 |
|
RU2257848C1 |
| СПОСОБ КЛИНИЧЕСКОГО ОПРЕДЕЛЕНИЯ ВЕРОЯТНОСТИ НЕМАССИВНОЙ ТРОМБОЭМБОЛИИ ЛЕГОЧНОЙ АРТЕРИИ У ПАЦИЕНТОК, ПРИНИМАЮЩИХ МЕНОПАУЗАЛЬНУЮ ГОРМОНОТЕРАПИЮ | 2015 |
|
RU2596056C1 |
| СПОСОБ КЛИНИЧЕСКОГО ОПРЕДЕЛЕНИЯ ВЕРОЯТНОСТИ ТРОМБОЭМБОЛИИ ЛЕГОЧНОЙ АРТЕРИИ У ПАЦИЕНТОВ С АТРИОВЕНТРИКУЛЯРНОЙ БЛОКАДОЙ, КОРРИГИРОВАННОЙ ЭЛЕКТРОКАРДИОСТИМУЛЯТОРОМ | 2005 |
|
RU2288641C1 |
| СПОСОБ ЛУЧЕВОЙ ДИАГНОСТИКИ ТРОМБОЭМБОЛИИ ЛЕГОЧНЫХ АРТЕРИЙ | 2013 |
|
RU2541270C1 |
| СПОСОБ ВЕДЕНИЯ ПАЦИЕНТОВ ПРИ ТРОМБОЭМБОЛИИ ЛЕГОЧНОЙ АРТЕРИИ | 2013 |
|
RU2506899C1 |

Изобретение относится к медицине и может быть использовано в медицинских учреждениях, оснащенных радиодиагностическими лабораториями. Цель изобретения - повышение точности способа диагностики отстрой тромбоэмболии легочной артерии и хронической постэмболической легочной гипертензии. Для дифференциальной диагностики острой тромбоэмболии легочной артерии и хронической постэмболической легочной гипертензии дополнительно к вентиляционно-перфузионной пульмоносцинтиграфии проводят равновесную радионуклидную вентрикулографию в томографическом режиме с последующим определением показателя соотношения поперечных размеров радиоактивного пула крови правого желудочка сердца к левому (ПЖ/ЛЖ), а также анализом фазовых полярных карт и фазовых гистограмм. При полном В/П-несоответствии, четкости контуров выявленных перфузионных дефектов накопления радиофармпрепарата (РФП), отсутствии снижения сократимости и диссинхронии в области межжелудочковой перегородки и показателя ПЖ/ЛЖ ниже 1,0 диагностируют острую тромбоэмболию легочной артерии с благоприятным прогнозом. При неполном В/П-соответствии, неправильности формы, нечеткости контуров перфузионных дефектов накоплении РФП, перераспределении перфузионного радиофармпрепарата в верхние отделы легких, наличии снижения сократимости и диссинхронии в области межжелудочковой перегородки, а также увеличении показателя ПЖ/ЛЖ свыше 1,0 диагностируют хроническую постэмболическую легочную гипертензию с неблагоприятным прогнозом. 7 ил.
Способ дифференциальной диагностики острой тромбоэмболии легочной артерии и хронической постэмболической легочной гипертензии, характеризующийся тем, что проводят вентиляционно-перфузионную пульмоносцинтиграфию и равновесную радионуклидную вентрикулографию в томографическом режиме, определяют показатель соотношения поперечных размеров радиоактивного пула крови правого желудочка сердца к левому (ПЖ/ЛЖ) и при полном вентиляционно-перфузионном (В/П)-несоответствии, четкости контуров выявленных перфузионных дефектов накопления радиофармпрепарата (РФП), а также при значении показателя соотношения поперечных размеров радиоактивного пула крови правого желудочка сердца к левому (ПЖ/ЛЖ) ниже 1,0 диагностируют острую тромбоэмболию легочной артерии, а при неполном вентиляционно-перфузионном (В/П)-соответствии, неправильности формы, нечеткости контуров перфузионных дефектов накопления радиофармпрепарата (РФП), перераспределении перфузионного радиоиндикатора в верхние отделы легких, а также увеличении показателя соотношения поперечных размеров радиоактивного пула крови правого желудочка сердца к левому (ПЖ/ЛЖ) выше 1,0 диагностируют хроническую постэмболическую легочную гипертензию.
| Панькова А.Н | |||
| Радионуклидная диагностика нарушений микроциркуляции малого круга кровообращения и дисфункции правого желудочка у пациентов с тромбоэмболией легочной артерии | |||
| Дисс | |||
| на соиск | |||
| уч.ст | |||
| к.м.н | |||
| Томск, 2011, с | |||
| Разборное приспособление для накатки на рельсы сошедших с них колес подвижного состава | 1920 |
|
SU65A1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ОСТРЫХ ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ ЛЕГКИХ И ТРОМБОЭМБОЛИЙ МЕЛКИХ ВЕТВЕЙ ЛЕГОЧНОЙ АРТЕРИИ | 2005 |
|
RU2310385C2 |
| Клименко А.А | |||
| и др | |||
| Хроническая постэмболическая легочная гипертензия: новые аспекты формирования | |||
Авторы
Даты
2015-04-10—Публикация
2014-03-13—Подача