Область изобретения
Изобретение относится к продуктам, композициям, способам и применениям, которые являются полезными для предотвращения образования биопленок и воздействия на них.
Предпосылки изобретения
Микробная биопленка представляет собой сообщество микробных клеток, погруженных во внеклеточный матрикс полимерных веществ и прикрепленных к биологической или небиотической поверхности. В этих биопленках можно найти целый ряд микроорганизмов (бактерии, грибы и/или простейшие и ассоциированные с ними бактериофаги и другие вирусы). Биопленки повсеместно распространены в природе и могут быть обнаружены в широком диапазоне сред. Научные и медицинские организации все в большей мере признают участие биопленок во многих инфекциях, особенно их вклад в устойчивость инфекций к лечению.
Биопленки являются этиологическими факторами множества заболеваний у млекопитающих и вовлечены в 80% инфекций у людей. Примеры включают кожные и раневые инфекции, инфекции среднего уха, инфекции желудочно-кишечного тракта, инфекции перитонеальной мембраны, инфекции мочеполовых путей, инфекции мягких тканей ротовой полости, образование зубного налета, глазные инфекции (в том числе контаминацию контактных линз), эндокардит, инфекции при муковисцидозе и инфекции имплантированных медицинских устройств, таких как суставные протезы, зубные имплантаты, катетеры и сердечные имплантаты.
В типичных случаях в качестве моделей для исследования чувствительности к антимикробным воздействиям используют планктонные микробы (то есть микроорганизмы, суспендированные или растущие в жидкой среде), как указано Институтом клинических и лабораторных стандартов (Clinical and Laboratory Standard Institute, CLSI) и Европейским комитетом по тестированию чувствительности к антимикробным воздействиям (European Committee on Antimicrobial Succeptibility Testing, EUCAST). Микробы в биопленках значительно более устойчивы к антимикробным воздействиям, чем их планктонные аналоги. Однако нет стандартизованного способа исследования чувствительности микробов биопленки к антибиотикам.
Образование биопленки не ограничено только способностью микробов прикрепляться к поверхности. Микробы, растущие в биопленке, способны взаимодействовать больше между собой, чем с реальным физическим субстратом, на котором биопленка развилась исходно. Например, этот феномен способствует переносу генов при конъюгации, который происходит с большей скоростью между клетками в биопленках, чем между планктонными клетками. Это создает повышенную возможность для горизонтального переноса генов между бактериями и важно потому, что может облегчать перенос устойчивости к антибиотикам или генов, определяющих вирулентность, от устойчивых к чувствительным микробам. Бактерии могут общаться между собой по системе, известной как «quorum sensing» («чувство кворума»), когда сигнальные молекулы высвобождаются в среду, и их концентрацию могут детектировать окружающие микробы. Quorum sensing делает возможной для бактерии координацию их поведения, что повышает их способность выживать. Реакции на quorum sensing включают адаптацию к доступности питательных веществ, защиту от других микроорганизмов, которые могут конкурировать за те же питательные вещества, и избегание токсичных соединений, потенциально опасных для бактерии. Это очень важно для патогенных бактерий во время инфицирования хозяина (например, людей, других животных или растений) для координации их вирулентности с тем, чтобы избегать иммунного ответа хозяина, чтобы быть способными к успешному заражению.
Образование биопленки играет ключевую роль во многих инфекционных заболеваниях, таких как муковисцидоз и периодонтит, в инфекциях кровотока и мочевых путей и в последствиях присутствия имплантированных медицинских устройств. Предполагаемые механизмы, посредством которых ассоциированные с биопленкой микроорганизмы вызывают заболевания у своего хозяина, включают следующее: (1) замедленное проникновение антимикробного агента через матрикс биопленки, (2) открепление клеток или клеточных агрегатов от биопленок на имплантированном медицинском устройстве, (3) продуцирование эндотоксинов, (4) устойчивость к иммунной системе хозяина, (5) предоставление ниши для генерации устойчивых организмов посредством горизонтального переноса генов устойчивости к антимикробным воздействиям и/или генов детерминантов вирулентности (6) измененную скорость роста (то есть, метаболическая спячка) (Donlan and Costerton, Clin Microbiol Rev 15: 167-193, 2002; Parsek and Singh, Annu Rev Microbiol 57: 677-701, 2003; Costerton JW, Resistance of biofilms to stress. In The Biofilm Primer'. (Springer Berlin Heidelberg), pp.56-64, 2007).
Недавние экспериментальные данные свидетельствуют о том, что в пределах биопленок существуют мелкие субпопуляции специализированных не метаболизирующих устойчивых клеток (покоящихся клеток). Считается, что эти клетки могут быть ответственными за высокую устойчивость/толерантность биопленки к антимикробным агентам. Толерантные ко многим лекарственным средствам устойчивые клетки присутствуют как в планктонных, так и в биопленочных популяциях, и оказывается, что дрожжи и бактерии выработали аналогичные стратегии, которые придают этим субпопуляциям функцию выживания. Защита, обеспечиваемая полимерным матриксом, позволяет устойчивым клеткам избегать выведения и служить в качестве источника для репопуляции. Есть свидетельства того, что устойчивые клетки в значительной степени являются ответственными за устойчивость микробных биопленок ко множеству лекарственных средств (LaFleur et al., Antimicrob Agents Chemother. 50: 3839-46, 2006; Lewis, Nature Reviews Microbiology 5, 48-56 2007).
Сохраняется необходимость в улучшенных способах терапии для предупреждения образования биопленки и лечения заболеваний, ассоциированных с микробными биопленками.
Изложение сущности изобретения
В соответствии с первым аспектом настоящего изобретения, предложен продукт, содержащий по меньшей мере два агента против биопленки, где по меньшей мере один агент против биопленки представляет собой антимикробный пептид. Другой агент против биопленки представляет собой диспергирующий агент или антиадгезивный агент.
Термин "агент против биопленки" использован здесь для описания агента, который способен разрушать микробную биопленку или ингибировать ее рост. Агент против биопленки может нарушать структуру биопленки, например внеклеточного слизистого матрикса, или может разрушать микробные клетки или ингибировать их рост в пределах биопленки.
В этом изобретении дополнительно предложен способ предотвращения образования биопленки в среде, включающий стадию введения антимикробного пептида в эту среду. Преимущественно, этот способ включает стадию введения в эту среду продукта в соответствии с этим изобретением.
В этом изобретении дополнительно предложен способ профилактического или терапевтического лечения микробной инфекции, особенно микробной биопленки, включающий введение терапевтически эффективного количества антимикробного пептида, например катионного пептида. В типичных случаях этот способ включает последовательное или комбинированное введение в терапевтически эффективном количестве:
первого агента против биопленки и
второго агента против биопленки, отличного от первого;
причем по меньшей мере один из первого и второго агентов против биопленки представляет собой антимикробный пептид, например, катионный пептид.
Указанные активные агенты можно вводить в виде свободных или фиксированных комбинаций. Свободные комбинации можно предоставлять в виде упаковок комбинаций, содержащих все активные агенты в свободных комбинациях. Фиксированные комбинации часто представляют собой таблетки или капсулы.
Настоящее изобретение также включает применение антимикробных пептидов или комбинаций активных агентов, указанных выше, в изготовлении лекарственного средства для лечения микробной инфекции, особенно инфекции, вызванной микробной биопленкой.
Эти продукты обладают преимуществом в том, что они демонстрируют антибактериальную активность против, среди прочего, устойчивых клеток, присутствующих в биопленках, что является существенной стадией на пути к уничтожению биопленок.
Агенты по этому изобретению можно вводить в форме фармацевтически приемлемых солей. Фармацевтически приемлемые соли по настоящему изобретению можно синтезировать из исходного соединения, которое содержит основную или кислотную группировку, общепринятыми химическими способами. Обычно такие соли можно получать взаимодействием форм этих соединений, представляющих собой свободную кислоту или основание, со стехиометрическим количеством надлежащего основания или кислоты в воде или в органическом растворителе или в их смеси; обычно неводные среды, такие как простой эфир, этилацетат, этанол, изопропанол или ацетонитрил, являются предпочтительными. Перечни подходящих солей можно найти в Remington's Pharmaceutical Sciences, 17th ed., Mack Publishing Company, Easton, Pa., US, 1985, p.1418, описание которого включено сюда посредством ссылки; см. также Stahl et al, Eds, "Handbook of Pharmaceutical Salts Properties Selection and Use", Verlag Helvetica Chimica Acta and Wiley-YCH, 2002. Фраза "фармацевтически приемлемый" использована здесь по отношению к тем соединениям, веществам, композициям и/или лекарственным формам, которые являются, в пределах обоснованного медицинского суждения, подходящими для применения в контакте с тканями человека или, возможно, животного без избыточной токсичности, раздражения, аллергической реакции или другой проблемы или осложнения, в соответствии с разумным соотношением польза/риск.
Это изобретение, таким образом, включает фармацевтически приемлемые соли раскрытых соединений, где исходное соединение модифицировано путем получения его солей с кислотой или основанием, например общепринятых нетоксичных солей или солей четвертичного аммония, которые образованы, например, из неорганических или органических кислот или оснований. Примеры таких солей присоединения кислоты включают ацетат, адипат, альгинат, аспартат, бензоат, бензосульфонат, бисульфат, бутират, цитрат, камфорат, камфоросульфонат, циклопентанпропионат, диглюконат, додецилсульфат, этансульфонат, фумарат, глюкогептаноат, глицерофосфат, гемисульфат, гептаноат, гексаноат, гидрохлорид, гидробромид, гидройодид, 2-гидроксиэтансульфонат, лактат, малеат, метансульфонат, 2-нафталинсульфонат, никотинат, оксалат, памоат, пектинат, персульфат, 3-фенилпропионат, пикрат, пивалат, пропионат, сукцинат, тартрат, тиоцианат, тозилат и ундеканоат. Соли основания включают соли аммония, соли щелочного металла, такие как соли натрия и калия, соли щелочноземельного металла, такие как соли кальция и магния, соли с органическими основаниями, такие как соли дициклогексиламина, N-метил-О-глюкамина, и соли с аминокислотами, такими как аргинин, лизин и так далее. Также, основные азотсодержащие группы можно переводить в четвертичные такими агентами, как низшие алкилгалогениды, такие как метил-, этил-, пропил- и бутилхлориды, -бромиды и -йодиды; диалкилсульфаты, такие диметил-, диэтил-, дибутил- и диамилсульфаты, длинноцепочечные галогениды, такие как децил-, лаурил-, миристил- и стеарилхлориды, -бромиды и -йодиды, аралкилгалогениды, такие как бензил- и фенэтилбромиды, и другие.
Следовательно, это изобретение включает фармацевтические продукты, обычно содержащие по меньшей мере:
первый агент против биопленки и
второй агент против биопленки, отличный от первого,
причем по меньшей мере один из первого и второго агентов против биопленки представляет собой антимикробный пептид, например, катионный пептид.
Первый агент против биопленки
Первый агент против биопленки может быть антимикробным пептидом, например антибактериальным пептидом. Предпочтительно, первый агент против биопленки представляет собой антимикробный пептид, здесь ниже обозначаемый как "первый антимикробный агент". Первый антимикробный агент может содержать аминокислоты в соответствии с формулой I:
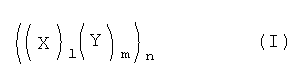 ,
,
где l и m представляют собой целые числа от 1 до 10, например от 1 до 5; n представляет собой целое число от 1 до 10; X и Y, которые могут быть одинаковыми или разными, независимо представляют собой гидрофобную или катионную аминокислоту.
Предпочтительно, первый антимикробный агент содержит аминокислоты в соответствии с формулой (I), где X и Y представляют собой катионные аминокислоты.
Антимикробный пептид может содержать от 2 до 200 аминокислот, например, от 3, 4, 5, 6 или 7 до 100 аминокислот, включая от 3, 4, 5, 6 или 7 до 10, 15, 20, 25, 30, 35, 40, 45 или 50 аминокислот. В соответствии с одним из воплощений, антимикробный пептид содержит от 3 или 4 до 50 аминокислот. Альтернативно, пептид может содержать более чем 27 аминокислот, в типичных случаях от 27 до 300 аминокислот, подходящим образом от 27 до 200 аминокислот.
Этот пептид может содержать от 100 до 200 аминокислот, от 20 до 100, 20 и 45 аминокислот, например 20, 25, 30, 35, 40, 42 или 45 аминокислот. Этот пептид может содержать от 3 до 15 аминокислот, например от 5 до 15 аминокислот.
При использовании здесь термин "гидрофобный" относится к аминокислоте, имеющей боковую цепь, которая является незаряженной при физиологических pH, которая является неполярной и которая обычно отталкивается водным раствором.
При использовании здесь термин "катионный" относится к аминокислотам, имеющим суммарный заряд, который больше чем 0 или равен 0. Обычно термин "катионный" относится к аминокислотам, имеющим суммарный заряд, который больше чем ноль.
Обычно гидрофобный аминокислотный остаток имеет гидрофобность большую чем -1,10 или равную -1,10, и заряд больший чем 0 или равный 0.
Гидрофобные аминокислоты могут включать лейцин, фенилаланин, пролин, аланин, триптофан, валин, изолейцин и метионин.
Предпочтительно, X и/или Y представляют собой катионные аминокислоты, например выбранные из группы, состоящей из гистидина, аргинина и лизина. Еще предпочтительнее, X и/или Y представляют собой аргинин или лизин. X и/или Y можно выбрать из не встречающихся в природе аминокислот, например, катионной аминокислоты орнитина.
X и/или Y могут представлять собой оптические изомеры катионной аминокислоты, какая определена здесь, например, D- или L-аминокислоты. Более того, X и/или Y могут быть чередующимися аминокислотами.
Аминокислоты могут быть встречающимися в природе или синтетическими. Это изобретение также включает известные изомеры (структурные, стерео-, конформационные и конфигурационные) и структурные аналоги указанных аминокислот и их модификации, либо природные (например, посттрансляционная модификация), либо химические, что включает, без ограничения, фосфорилирование, гликозилирование, сульфонилирование и/или гидроксилирование.
В соответствии с одним из воплощений пептид может включать одну или более чем одну замену катионных или гидрофобных аминокислот X и Y. Однако этот пептид должен преимущественно содержать катионные или гидрофобные аминокислоты X и Y. В типичных случаях пептид может содержать от 1 до 5 замен, подходящим образом от 1 до 3 замен, обычно одну замену. Замены могут быть концевыми или неконцевыми.
Эти замены могут состоять из аминокислот или отличаться от аминокислот. Замены могут быть заряженными или незаряженными. В типичных случаях одна или более чем одна замена представляет собой незаряженную аминокислоту. Альтернативно или дополнительно одна или более чем одна замена может не представлять собой аминокислоту, например, цистеамин.
Предпочтительно, X и Y являются одинаковыми и представляют собой лизин или аргинин.
В соответствии с одним воплощением, пептид содержит преимущественно аминокислоты, представляющие собой аргинин, которые можно заменить одной или более чем одной аминокислотой, которая не представляет собой аргинин.
Обычно пептид содержит от 7 до 20 аминокислот, представляющих собой аргинин, возможно замененных 1-5 аминокислотами, не представляющими собой аргинин, в типичных случаях, 3-5 заменами, не представляющими собой аргинин.
Альтернативно, пептид может содержать от 7 до 20 аминокислот, представляющих собой лизин, возможно замененные 1-5 аминокислотами, не представляющими собой лизин, в типичных случаях, 3-5 заменами, не представляющими собой лизин.
В соответствии с дополнительным воплощением пептид может содержать от 27 до 300 аминокислот, представляющих собой лизин, обычно от 27 до 200 аминокислот, представляющих собой лизин. В типичных случаях пептид не содержит неконцевых замен аминокислотами, не представляющими собой лизин.
В пептиде формулы (I) l и m могут представлять собой 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, и n может представлять собой 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10.
В пептиде формулы (I) l может представлять собой 1, n может представлять собой 1, и m может быть между 4 и 9, например, m может представлять собой 3, 4, 5, 6, 7, 8 или 9.
В пептиде формулы (I) l, n и/или m могут быть между 1 и 5, например 1, 2, 3, 4 или 5.
В пептиде формулы (I) l и m могут представлять собой целое число между 0 и 7, и n может представлять собой целое число между 1 и 10.
В пептиде формулы (I) l и m может представлять собой 0, 1 или 2, и n может представлять собой целое число между 1 и 10.
В пептиде формулы (I) X и Y могут быть одинаковыми, l может представлять собой 0, m может представлять собой 1, и n может представлять собой 3, 4, 5, 6, 7, 8, 9 или 10.
В пептиде формулы (I) X и Y могут быть одинаковыми, l и m могут представлять собой 1, и n может представлять собой 2, 3, 4 или 5.
В пептиде формулы (I) X и Y могут быть одинаковыми, l может представлять собой 1, m может представлять собой 2, и n может представлять собой 1, 2, 3 или 4.
В пептиде формулы (I) X и Y могут быть одинаковыми, l и m могут представлять собой 2, и n может представлять собой 1, 2, 3 или 4.
Предпочтительно, первый антимикробный агент содержит пептидную последовательность, выбранную из группы, состоящей из полилизина и полиаргинина.
В одном из воплощений первый антимикробный агент содержит полилизин.
В альтернативном воплощении первый антимикробный агент содержит полиаргинин.
В соответствии с дополнительным аспектом настоящего изобретения предложено применение первого антимикробного агента в лечении для предотвращения образования биопленки.
В типичных случаях первый антимикробный агент находится в форме продукта по этому изобретению, как описано ниже.
Второй агент против биопленки
Второй агент против биопленки может представлять собой любой агент, который ингибирует образование биопленки. Например, второй агент против биопленки может ингибировать бактериальную адгезию, гидрофобность или продукцию слизи. Второй агент против биопленки можно выбрать из диспергирующего агента и антиадгезивного агента.
В соответствии с одним из воплощений настоящего изобретения, второй агент против биопленки не представляет собой пептид.
Термин "диспергирующий агент" включает любой агент, способный диспергировать частицы биопленки. В частности, диспергирующий агент может способствовать дисперсии слизи, продуцируемой микробами, такими как бактерии, слизи, которая формирует часть биопленки, например слизи, продуцируемой клетками, к которым прилипают микробы биопленки, и микробов биопленки, таких как бактерии.
Диспергирующий агент может представлять собой муколитический агент. Муколитический агент может представлять собой фермент, например ДНКазу, альгиназу, протеазу или карбогидразу. Альтернативно муколитический агент может представлять собой малую молекулу, например амин, такой как аминотиол, или кислоту, такую как этилендиаминтетрауксусная кислота (ЭДТА). Амин можно выбрать из ацетилцистеина и цистеамина (cysteamine).
Термин "антиадгезивный агент" включает любой агент, способный ингибировать адгезию между клетками, белками и организмами, например микробами, предотвращая тем самым образование биопленки или способствуя саморазрушению биопленки. В частности, антиадгезивный агент может предотвращать адгезию к поверхности или субстрату всех типов клеток, встречающихся в микробных биопленках, в частности, свободноживущих микробов, т.е., планктонных клеток. Антиадгезивные агенты могут включать, без ограничения, гиалуронан, гепарин или Карбопол 934.
Вторым агентом против биопленки может быть антибактериальный агент. Антибактериальный агент может представлять собой муколитический агент, например, муколитический агент, имеющий как муколитическую, так и антибактериальную активность. Предпочтительно, антибактериальный агент представляет собой цистеамин.
Продукты по изобретению
Продукт по настоящему изобретению может содержать антимикробный пептид.
Предпочтительный продукт содержит антимикробный пептид и муколитический агент.
Соотношение первого агента против биопленки и второго агента против биопленки в продуктах по этому изобретению может составлять от 1:10 до 10:1; обычно по меньшей мере 2:1, например, по меньшей мере 3:1 или 4:1. В соответствии с одним из воплощений, соотношение первого агента против биопленки и второго агента против биопленки представляет собой приблизительно 1:1. Предпочтительно, первый агент против биопленки представляет собой катионный пептид, а второй агент против биопленки представляет собой муколитический агент, и соотношение катионный пептид: муколитический агент находится в диапазоне от 2:1 до 4:1. В соответствии с дополнительным воплощением, это соотношение может быть приблизительно 1:1.
Активные агенты можно вводить одновременно, последовательно или раздельно. Активные агенты можно предоставлять в виде комбинированной упаковки. Комбинированная упаковка может содержать продукт по этому изобретению вместе с инструкциями для одновременного, раздельного или последовательного введения каждого активного агента. Для последовательного введения активные агенты можно вводить в любом порядке.
Активные агенты продукта по этому изобретению можно предоставлять в виде фармацевтических композиций, дополнительно содержащих один или более чем один фармацевтически приемлемый разбавитель, эксципиент и/или носитель. Это относится как к фиксированным, так и к свободным комбинациям.
Активные агенты по настоящему изобретению можно вводить любым подходящим путем, известным специалистам, предпочтительно в форме фармацевтической композиции, адаптированной к такому пути, и в дозе, эффективной для назначенного лечения. Активные соединения и композицию можно, например, вводить парентерально, перорально, интраназально, внутрибронхиально, энтерально, через кожу, сублингвально, ректально, вагинально, в глаз или местно. Предусмотрено как локальное, так и системное введение.
В целях парентерального введения ("парентеральный" при использовании здесь относится к способам введения, которые включают внутривенную, внутримышечную, энтеральную, внутрибрюшинную, внутригрудинную, подкожную и внутрисуставную инъекцию и инфузию, причем внутривенное введение (включая непрерывное внутривенное введение) является наиболее предпочтительным) можно использовать растворы в водном пропиленгликоле, а также стерильные водные растворы соответствующих водорастворимых солей. Такие водные растворы могут быть подходящим образом забуференными, если необходимо, и жидкий разбавитель сначала делают изотоническим с использованием достаточного количества физиологического раствора или глюкозы. Эти водные растворы являются особенно подходящими для целей внутривенной, внутримышечной, подкожной и внутрибрюшинной инъекции. В этой связи все используемые стерильные водные среды легко получать стандартными методиками, хорошо известными специалистам.
Продукты по этому изобретению можно также вводить интраназальным путем или ингаляцией, и их удобно доставлять в форме сухой порошковой ингаляции или аэрозольного спрея из контейнера под давлением, насоса, спрея, пульверизатора, распылителя с применением или без применения подходящего пропеллента.
Альтернативно, продукты по этому изобретению можно вводить в форме суппозитория или пессария, или их можно наносить местно в форме геля, гидрогеля, лосьона, раствора, крема, мази или порошка. Продукты по этому изобретению можно вводить в кожу или через кожу, например, с использованием кожного пластыря, депо или подкожной инъекции. Их можно также вводить легочным или ректальным путями.
Для перорального введения фармацевтическая композиция может быть в форме, например, таблетки, капсулы, суспензии или жидкости. Фармацевтическую композицию предпочтительно получают в стандартной лекарственной форме, содержащей конкретное количество активного ингредиента. Примерами таких стандартных форм являются капсулы, таблетки, порошки, гранулы или суспензии с общепринятыми добавками, такими как лактоза, маннит, кукурузный крахмал или картофельный крахмал; со связующими агентами, такими как кристаллическая целлюлоза, производные целлюлозы, гуммиарабик, кукурузный крахмал или желатины; с разрыхлителями, такими как кукурузный крахмал, картофельный крахмал или карбоксиметилцеллюлоза в натриевой форме; и со смазывающими агентами, такими как тальк или стеарат магния. Активный ингредиент можно также вводить инъекцией в виде композиции, где в качестве подходящего носителя можно использовать, например, физиологический раствор, декстрозу или воду.
Продукты по этому изобретению могут также находить применение в виде или в составе перорального препарата, где продукт приготовлен в виде препарата с носителем, например, выбранном из пленок, лент, гелей, микросфер, лепешек, жевательных резинок, зубных паст или порошков и ополаскивателей рта.
Количество терапевтически активного соединения, которое вводят, и режим дозировки для лечения заболевания соединениями и/или композициями по этому изобретению зависят от множества разных факторов, включая возраст, массу, пол и медицинское состояние субъекта, тяжесть заболевания, путь и частоту введения и конкретное используемое соединение, а также фармакокинетические свойства индивида, которого лечат, и таким образом могут широко варьировать. Дозировка должна обычно быть снижена, если соединения вводят местно, а не системно, и для профилактики, а не для лечения. Такие средства лечения можно вводить так часто, как это необходимо, и в течение времени, определенного врачом как необходимое для лечения. Специалист в данной области должен понимать, что режим дозировки или терапевтически эффективное количество ингибитора для введения могут быть оптимизированы для каждого индивида. Фармацевтические композиции могут содержать активный ингредиент в диапазоне от примерно 0,1 до 2000 мг, предпочтительно в диапазоне от примерно 0,5 до 500 мг и, наиболее предпочтительно, между примерно 1 и 200 мг. Может быть подходящей суточная доза от примерно 0,01 до 100 мг/кг массы тела, предпочтительно между примерно 0,1 и примерно 50 мг/кг массы тела и, наиболее предпочтительно, от примерно 1 до 20 мг/кг массы тела. Суточную дозу можно вводить в виде от одной четырех доз в сутки.
Продукты по этому изобретению предпочтительно вводят в дыхательные пути. Таким образом, настоящее изобретение также предлагает аэрозольные фармацевтические препараты, содержащие продукт по этому изобретению. Также предложен распылитель или ингалятор, содержащий продукт по этому изобретению.
Дополнительно, продукты по этому изобретению можно вводить в виде лекарственных форм для постоянного высвобождения и тому подобных. Препараты можно составлять так, что они высвобождают активные агенты, например, в конкретной части кишечного или респираторного тракта, возможно, в течение некоторого периода времени. Покрытия, оболочки и защитные матрицы можно получать, например, из полимерных веществ, таких как полилактид-гликоляты, липосомы, микроэмульсии, микрочастицы, наночастицы или воски. Эти покрытия, оболочки и защитные матрицы являются полезными для покрытия имплантированных устройств, например, стентов, катетеров, трубок для перитонеального диализа, дренирующих устройств и тому подобного.
Продукты по этому изобретению могут включать синергетически эффективные количества каждого определенного здесь активного агента. Это изобретение, таким образом, включает продукты, содержащие синергетически эффективное количество (1) первого агента против биопленки, (2) второго агента против биопленки, который отличается от первого агента против биопленки и представляет собой в типичных случаях антимикробный пептид. Этот продукт можно применять в изготовлении лекарственного средства для одновременного, раздельного или последовательного введения указанных агентов в лечении микробной инфекции, например биопленочной инфекции. "Синергетически" при использовании здесь описывает действие двух или более чем двух агентов продукта по этому изобретению, совместное действие которых может дать больший эффект, чем предполагаемый суммарный эффект агентов, используемых по отдельности.
В дополнительном аспекте этого изобретения предложен субстрат, на который наносят или к которому присоединяют продукт по этому изобретению. Предпочтительно, этот субстрат является подходящим для нанесения на раны или доставки к месту раны. Предпочтительно, субстрат позволяет переносить активные агенты продукта по этому изобретению от субстрата к ткани раны для реализации их антибиопленочного эффекта. Этот субстрат может представлять собой повязку, например, повязку на рану. Эта повязка может содержать тканое вещество, или она может представлять собой вещество, подобное коллагену. Субстрат может быть в любой подходящей форме для нанесения на рану, в типичных случаях субстрат может быть в форме гидрогеля, коллоида, мази, крема, геля, пены или спрея.
Продукты по этому изобретению могут также находить применение в качестве или в составе дезинфектанта или биоцида. В этом контексте, пептид или фармацевтические композиции по этому изобретению можно наносить, либо по отдельности, либо в комбинации с другими дезинфицирующими агентами, на поверхность, подлежащую обработке. При использовании здесь "поверхность, подлежащая обработке" может представлять собой субстрат, как определено здесь, и может включать медицинские устройства и имплантированные устройства, например, стенты, катетеры, трубки для перитонеального диализа, дренирующие устройства, протезы суставов, зубные имплантаты и тому подобное.
Способы и применение
В этом изобретении предложен способ предотвращения образования биопленки в среде, включающий стадию введения продукта в соответствии с этим изобретением в среду. Этот способ может представлять собой способ in vivo или ex vivo.
В соответствии с одним из воплощений этот способ включает стадию введения антимикробного пептида.
Преимуществом является то, что этот способ включает стадию введения
первого агента против биопленки и
второго агента против биопленки, отличного от первого, причем по меньшей мере один из первого и второго агента против биопленки представляет собой антимикробный пептид, например, катионный пептид.
Среда может содержать любой образующий биопленку микроорганизм, выбранный из бактерий, грибов, дрожжей, вирусов и простейших.
В типичных случаях микроорганизм представляет собой бактерию, например, грамположительную или грамотрицательную бактерию. Бактериальный патоген может происходить из бактериальных видов, выбранных из группы, состоящей из следующего: Staphylococcus spp., например Staphylococcus aureus, Staphylococcus epidermidis; Enterococcus spp., например Enterococcus faecalis; Streptococcus pyogenes; Listeria spp.; Pseudomonas spp.; Mycobacteria spp., например Mycobacteria tuberculosis; Enterobacter spp.; Campylobacter spp.; Salmonella spp.; Streptococcus spp., например Streptococcus Группы A или B, Streptococcus pneumoniae; Helicobacter spp., например Helicobacter pylori; Neisseria spp., например Neisseria gonorrhea, Neisseria meningitidis; Borrelia burgdorferi; Shigella spp., например Shigella flexneri; Escherichia coli; Haemophilus spp., например Haemophilus influenzae; Chlamydia spp., например Chlamydia trachomatis, Chlamydia pneumoniae, Chlamydia psittaci; Francisella tularensis; Bacillus spp., например Bacillus anthracis; Clostridia spp., например Clostridium botulinum; Yersinia spp., например Yersinia pestis; Treponema spp.; Burkholderia spp.; например Burkholderia mallei и В pseudomallei.
В частности, бактерия может включать Pseudomonas spp., например Pseudomonas aeruginosa; Staphylococcus spp., например Staphylococcus aureus и Staphylococcus epidermidis; Haemophilus spp., например Haemophilus influenzae; Burkholderia spp., например Burkholderia cepacia; Streptococcus spp., Propionibacterium spp., например Propionibacterium acnes. Предпочтительно бактерия выбрана из Pseudomonas spp., например Pseudomonas aeruginosa и Staphylococcus spp., например Staphylococcus aureus и Staphylococcus epidermidis.
Вирусный патоген может происходить из вируса, выбранного из группы, состоящей из: вируса иммунодефицита человека (ВИЧ 1 и 2); вируса T-клеточного лейкоза человека (HTLV 1 и 2); вируса Эбола; вируса папилломы человека (например, ВПЧ-2, ВПЧ-5, ВПЧ-8 ВПЧ-16, ВПЧ-18, ВПЧ-31, ВПЧ-33, ВПЧ-52, ВПЧ-54 и ВПЧ-56); паповавируса; риновируса; полиовируса; герпесвируса; аденовируса; вируса Эпштейна-Барр; вируса гриппа, вирусов гепатита B и C, вирусов осповакцины, ротавируса или коронавиуса, вызывающего тяжелый острый респираторный синдром (SARS).
Паразитарный патоген может происходить из паразитарных патогенов, выбранных из группы, состоящей из Trypanosoma spp.(Trypanosoma cruzi, Trypanosoma brucei), Leishmania spp., Giardia spp., Trichomonas spp., Entamoeba spp., Naegleria spp., Acanthamoeba spp., Schistosoma spp., Plasmodium spp., Cryptosporidium spp., Isospora spp., Balantidium spp., Loa Loa, Ascaris lumbricoides, Dirofilaria immitis, Toxoplasma ssp., например Toxoplasma gondii. Грибной патоген может происходить из грибного патогена из рода Candida spp., (например С.albicans), Epidermophyton spp., Exophiala spp., Microsporum spp., Trichophyton spp., (например T.rubrum и T.interdigitale), Tinea spp., Aspergillus spp., Blastomyces spp., Blastoschizomyces spp., Coccidioides spp., Cryptococcus spp., Histoplasma spp., Paracoccidiomyces spp., Sporotrix spp., Absidia spp., Cladophialophora spp., Fonsecaea spp., Phialophora spp., Lacazia spp., Arthrographis spp., Acremonium spp., Actinomadura spp., Apophysomyces spp., Emmonsia spp., Basidiobolus spp., Beauveria spp., Chrysosporium spp., Conidiobolus spp., Cunninghamella spp., Fusarium spp., Geotrichum spp., Graphium spp., Leptosphaeria spp., Malassezia spp., Mucor spp., Neotestudina spp., Nocardia spp., Nocardiopsis spp., Paecilomyces spp., Phoma spp., Piedraia spp., Pneumocystis spp., Pseudallescheria spp., Pyrenochaeta spp., Rhizomucor spp., Rhizopus spp., Rhodotorula spp., Saccharomyces spp., Scedosporium spp., Scopulariopsis spp., Sporobolomyces spp., Syncephalastrum spp., Trichoderma spp., Trichosporon spp., Ulocladium spp., Ustilago spp., Verticillium spp., Wangiella spp.
В соответствии с дополнительным воплощением, микроорганизм может представлять собой гриб, в частности Candida.
Способ по этому изобретению можно использовать для минимизации и, предпочтительно, предотвращения образования биопленок во многих различных средах, включая, без ограничения, домашнее хозяйство, рабочее место, лабораторию, промышленную среду, водную среду (например, трубопроводные системы), медицинские устройства, в том числе имплантированные устройства, такие как определено здесь, зубоврачебные устройства или зубные имплантаты, организм животного, например организм человека.
Способ по этому изобретению можно, таким образом, использовать для предупреждения образования налета и кариеса на зубе или на зубном имплантате человека, например, зубном протезе, в ротовой полости.
Способ по этому изобретению можно использовать для предотвращения или ограничения образования биопленки в человеческом организме, особенно при лечении микробных инфекций. Заболевания, ассоциированные с биопленочными инфекциями, могут включать местные инфекции, инфекции ротовой полости и системные инфекции. Местные инфекции могут включать раны, язвы и патологические изменения, например кожные ранения, такие как порезы или ожоги, и заболевания, ассоциированные с ними.
Инфекции ротовой полости могут включать гингивит, периодонтит и мукозит.
Системные инфекции могут включать муковисцидоз и другие заболевания, ассоциированные с инфекциями слизистых, например, желудочно-кишечные, мочеполовые или респираторные инфекции.
Другой аспект этого изобретения относится к способам лечения, предупреждения или замедления прогрессии заболевания или состояния, ассоциированного с присутствием микробной биопленочной инфекции у млекопитающего, особенно человека, путем введения терапевтически эффективного количества продукта по этому изобретению млекопитающему.
"Эффективное" количество или "терапевтически эффективное количество" означает количество одной или более чем одной активной субстанции, которое, в пределах обоснованного медицинского суждения, является достаточным для достижения желаемого эффекта без избыточной токсичности, раздражения, аллергической реакции или другой проблемы или осложнения, в соответствии с разумным соотношением польза/риск.
В соответствии с одним из аспектов настоящего изобретения способ включает стадию введения антимикробного пептида.
Преимущественно, этот способ включает стадию введения
первого агента против биопленки и
второго агента против биопленки, отличного от первого,
причем по меньшей мере один из первого и второго агента против биопленки представляет собой антимикробный пептид, например катионный пептид.
В этом изобретении дополнительно предложено применение продукта по этому изобретению в изготовлении лекарственного средства для профилактического или терапевтического лечения микробной инфекции, в частности, микробной биопленочной инфекции, комбинацией активных агентов, указанных выше.
Дополнительно в настоящем изобретении предложено применение антимикробного пептида, описанного выше, в изготовлении лекарственного средства для профилактического или терапевтического лечения микробной инфекции, в частности, микробной биопленочной инфекции.
Таким образом, продукт по этому изобретению может быть полезным в предупреждении, замедлении прогрессирования или лечении заболевания или состояния, выбранного из группы, состоящей из кожных и раневых инфекций, инфекций среднего уха, инфекций желудочно-кишечного тракта, инфекций перитонеальной мембраны, инфекций мочеполовых путей, инфекции мягких тканей ротовой полости, образования зубного налета, глазных инфекций (в том числе контаминации контактных линз), эндокардита, инфекций при муковисцидозе и инфекций имплантированных медицинских устройств, таких как описанные здесь.
Изобретение также включает способы лечения, при которых продукт по этому изобретению вводят млекопитающему вместе с одним или более чем одним другим антибактериальным агентом, например антибиотиком.
Авторы настоящего изобретения неожиданно обнаружили, что определенные диспергирующие агенты, в частности, муколитические агенты ингибируют рост устойчивых клеток в биопленке. Таким образом, это изобретение также включает способ лечения/предотвращения образования биопленки в среде, включающий введение муколитического агента, например цистеамина, в указанную среду. Этот муколитический агент можно вводить по отдельности или в комбинации с другим антимикробным агентом, например антимикробным пептидом.
В этом изобретении также предложен способ профилактического или терапевтического лечения микробной инфекции, в частности, микробной биопленки, включающий введение в терапевтически эффективном количестве диспергирующего агента, в частности, муколитического агента, например цистеамина.
В этом изобретении дополнительно предложено применение диспергирующего агента, в частности, муколитического агента, например цистеамина, изготовление лекарственного средства для лечения микробной инфекции, в частности, микробной биопленочной инфекции.
Активные агенты, указанные в этом описании, могут существовать в разных формах, таких как свободные кислоты, свободные основания, сложные эфиры и другие пролекарственные формы, например, соли и таутомеры, и это изобретение включает все варианты форм этих агентов.
По всему описанию и в формуле изобретения этого описания грамматическая форма единственного числа охватывает форму множественного числа, если контекст не требует иного. В частности, при использовании в описании единственного числа следует понимать, что подразумевается форма как множественного, так и единственного числа, если контекстом не предусмотрено иного.
Признаки, целые числа, характеристики, соединения, химические группировки или группы, описанные в связи с конкретным аспектом, воплощением или примером этого изобретения, надо понимать как применимые к любому другому аспекту, воплощению или примеру, описанному здесь, при отсутствии несоответствия с ним.
По всему описанию и в формуле изобретения этого описания слова "включают" и "содержат" и их вариации, например, "включающий" и "включает", означают "включая без ограничения" и не предназначены исключать другие группировки, добавки, компоненты, целые числа или стадии (и не исключают их).
Обычно термин "приблизительно" предназначен охватывать диапазон 10% или менее чем 10% любой приблизительной величины, к которой он относится.
Дополнительные аспекты и воплощения этого изобретения указаны в следующем далее описании и формуле изобретения.
Изобретение будет теперь описано только с использованием Примеров и со ссылкой на следующие чертежи, в которых:
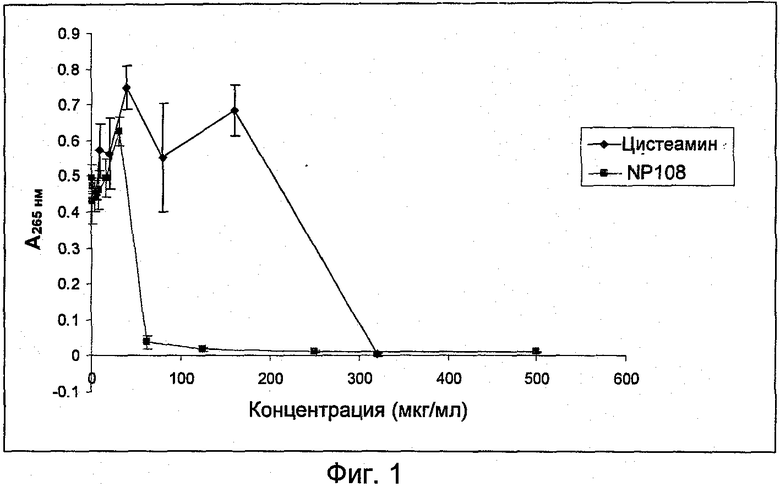
На Фиг.1 представлена антибактериальная активность NP108 и NM001 (цистеамина) в отношении планктонных клеток P.aeruginosa АТСС ВАА-47.
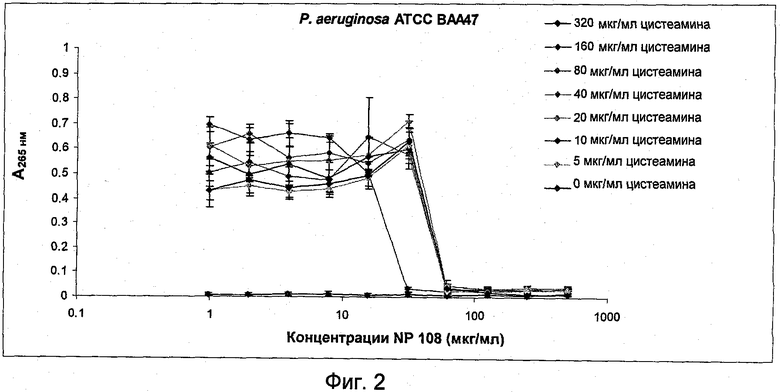
На Фиг.2 представлена антибактериальная активность комбинации NP108 и NM001 (цистеамина) в отношении планктонных клеток P. aeruginosa АТСС ВАА-47.
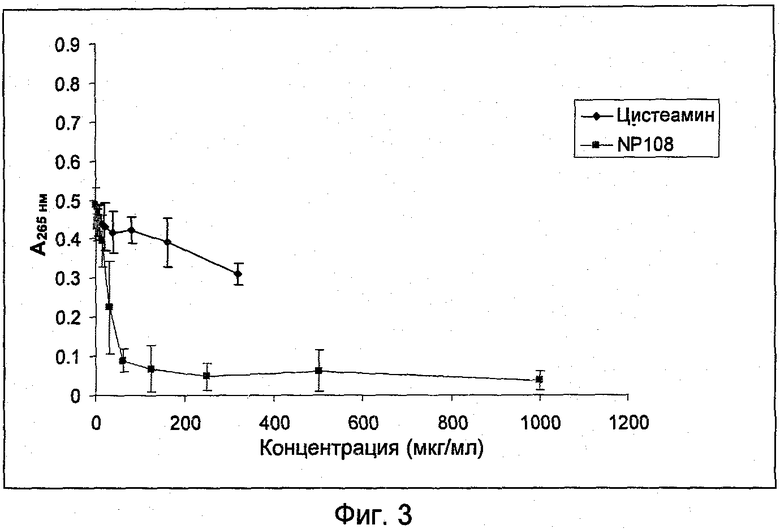
На Фиг.3 представлена антибактериальная активность NP108 и NM001 (цистеамина) в отношении планктонных клеток S.aureus DSM 11729.
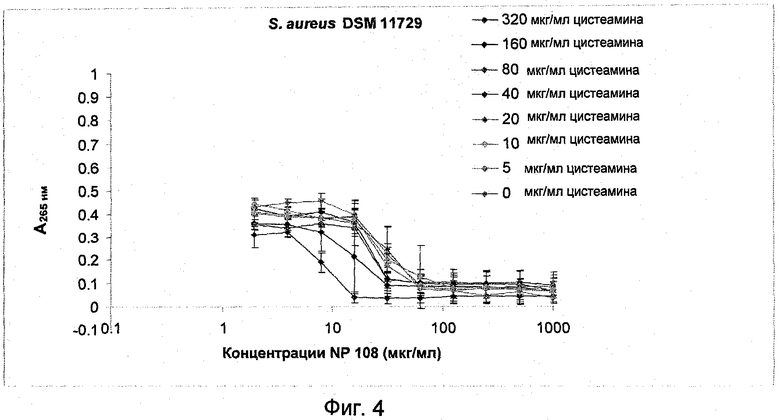
На Фиг.4 представлена антибактериальная активность комбинации NP108 и NM001 (цистеамина) в отношении планктонных клеток S.aureus DSM 11729.
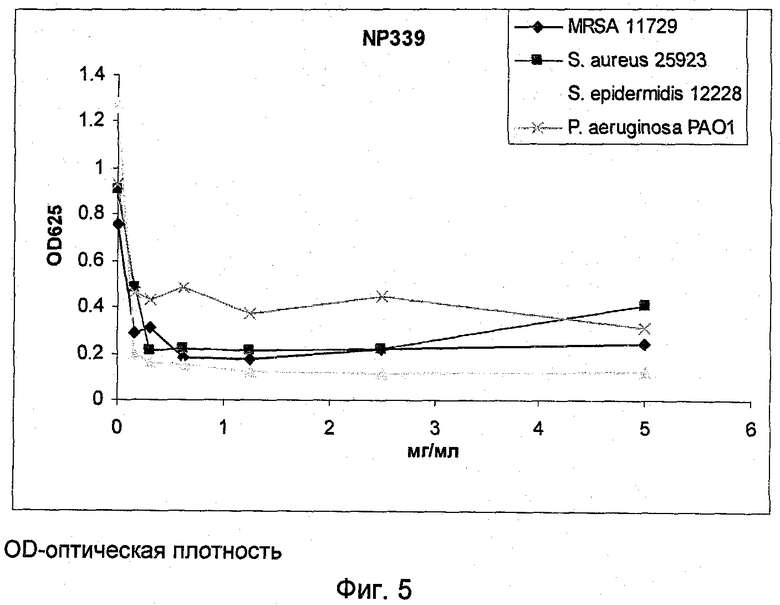
На Фиг.5 представлена активность NP339 в отношении биопленочных клеток грамположительных и грамотрицательных бактерий.
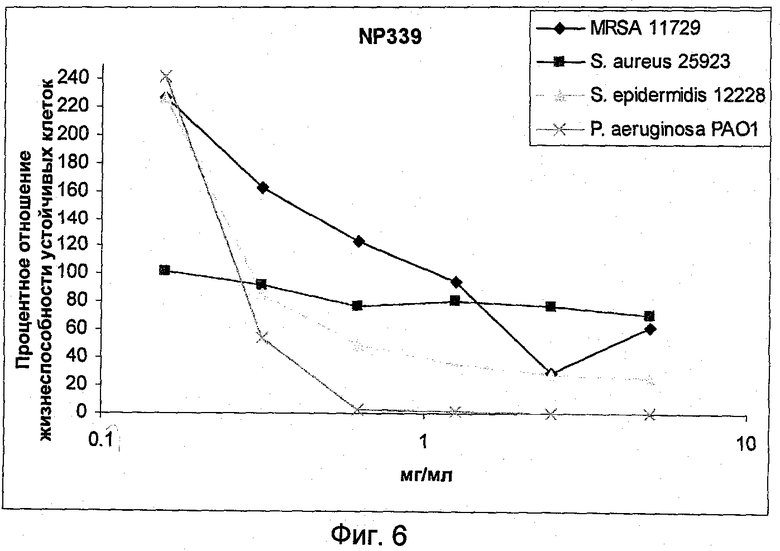
На Фиг.6 представлена активность NP339 в отношении устойчивых клеток грамположительных и грамотрицательных бактерий.
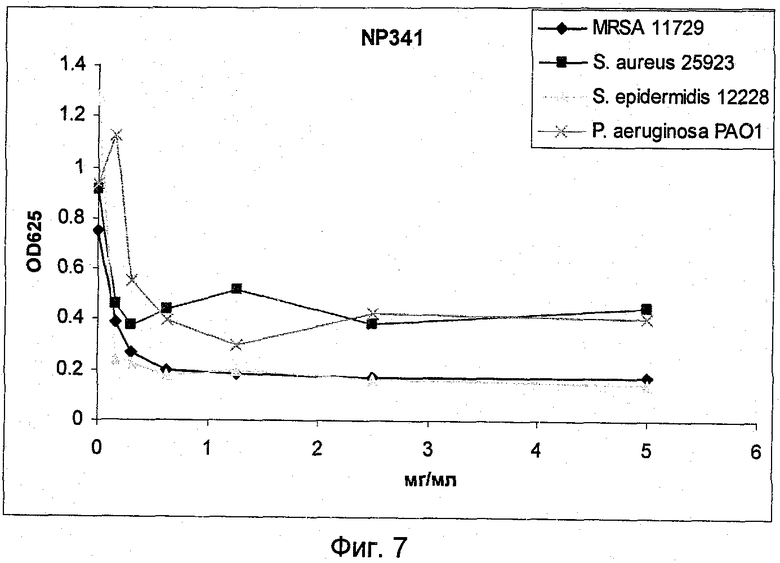
На Фиг.7 представлена активность NP341 в отношении биопленочных клеток грамположительных и грамотрицательных бактерий.
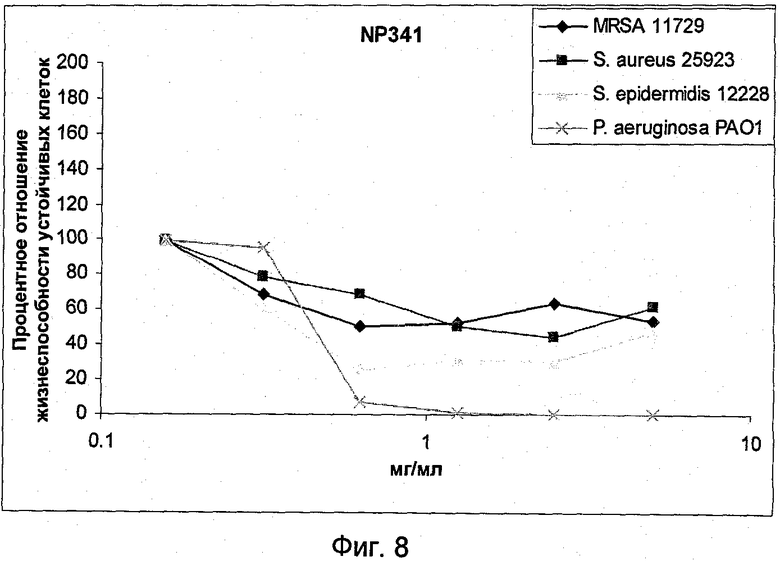
На Фиг.8 представлена активность NP341 в отношении устойчивых клеток грамположительных и грамотрицательных бактерий.
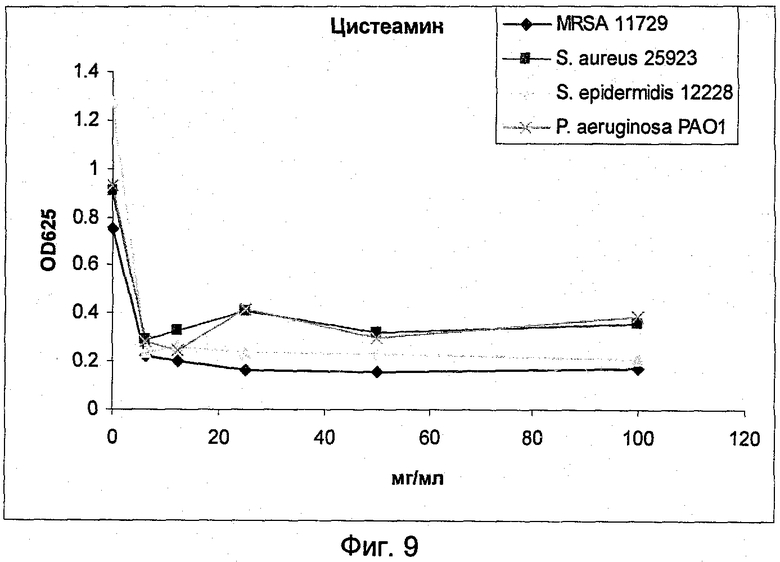
На Фиг.9 представлена активность NM001 (цистеамина) в отношении биопленочных клеток грамположительных и грамотрицательных бактерий.
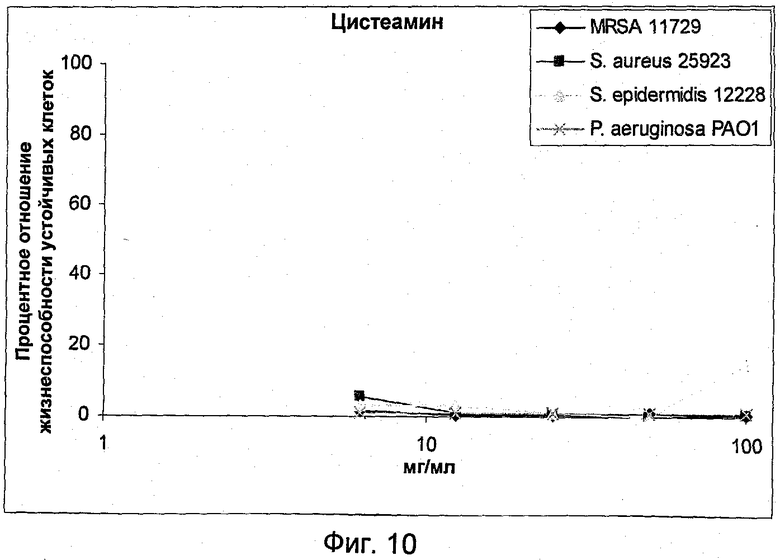
На Фиг.10 представлена активность NM001 (цистеамина) в отношении устойчивых клеток грамположительных и грамотрицательных бактерий.
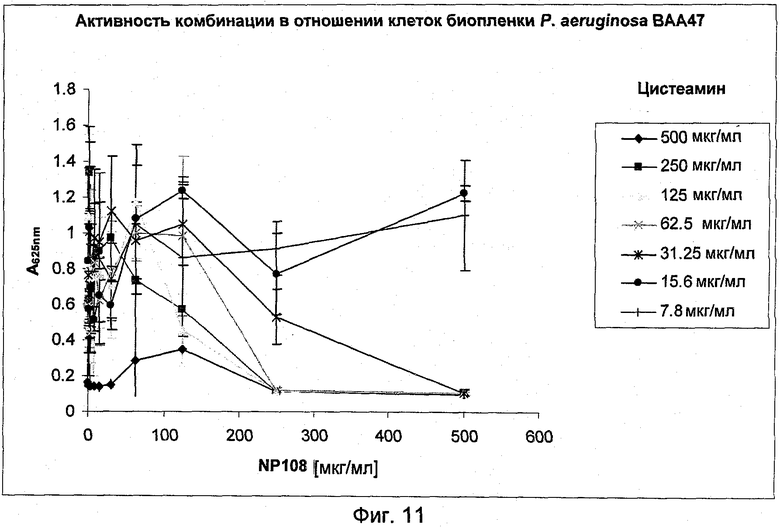
На Фиг.11 представлена антибактериальная активность комбинации NP108 и NM001 (цистеамина) в отношении биопленочных клеток P.aeruginosa АТСС ВАА-47.
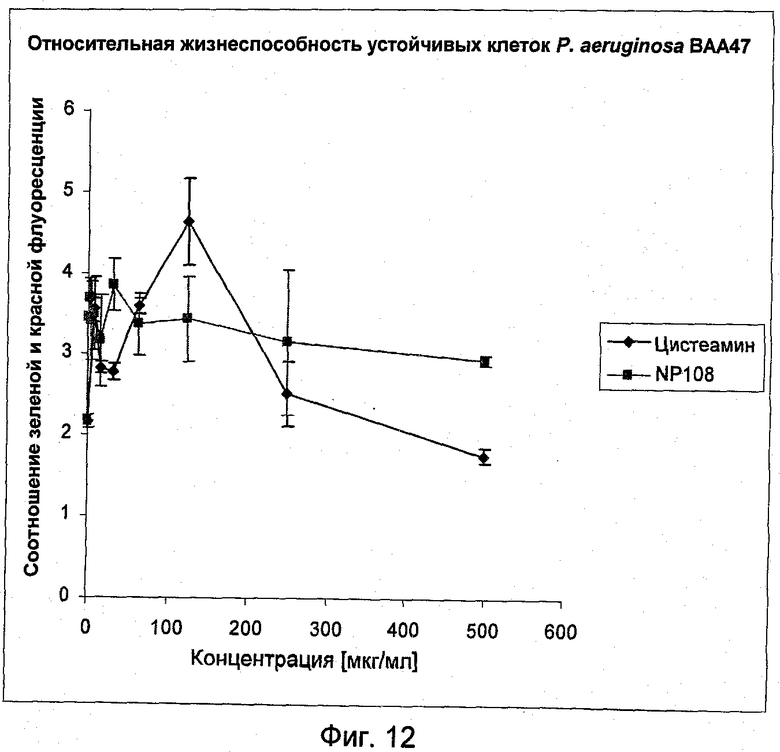
На Фиг.12 представлена антибактериальная активность NP108 и NM001 (цистеамина) в отношении устойчивых клеток P.aeruginosa АТСС ВАА-47.
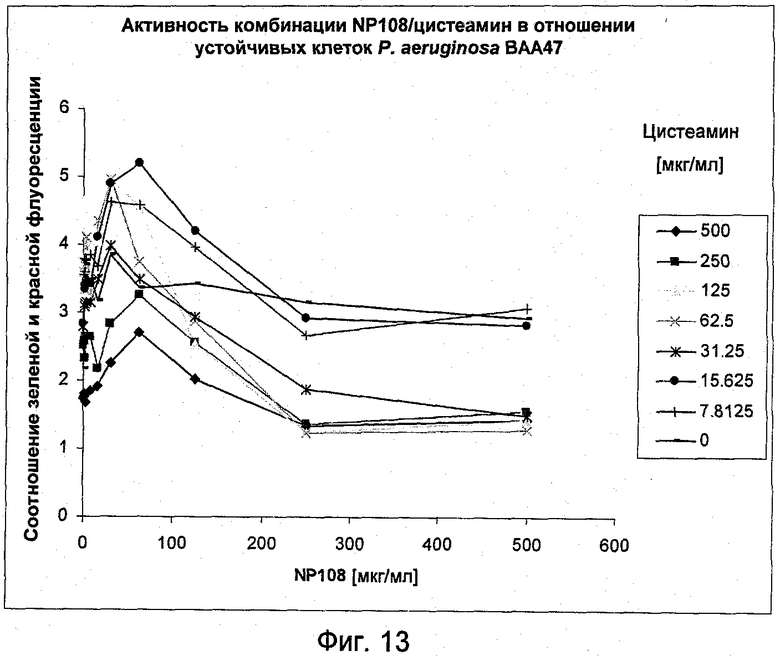
На Фиг.13 представлена антибактериальная активность комбинации NP108 и NM001 (цистеамина) в отношении устойчивых клеток P.aeruginosa АТСС ВАА-47.
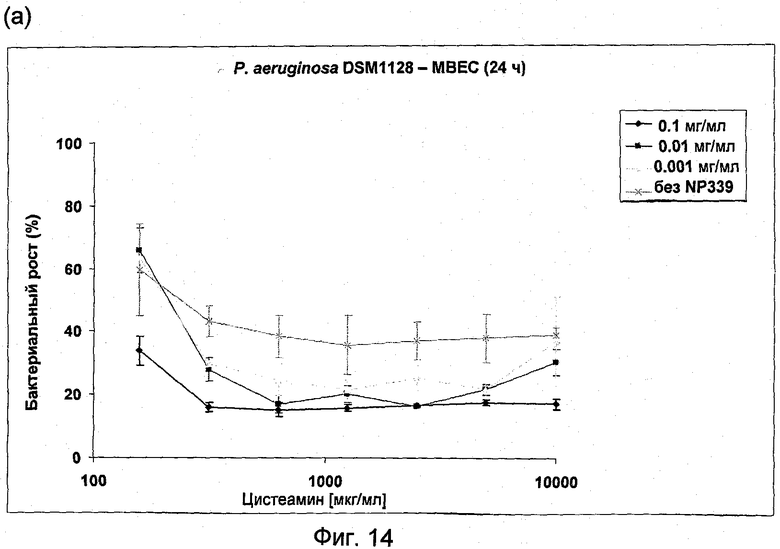
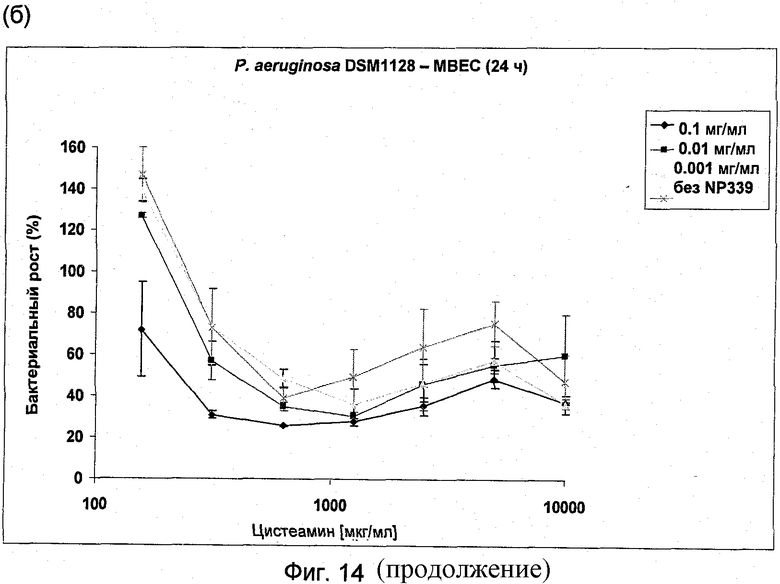
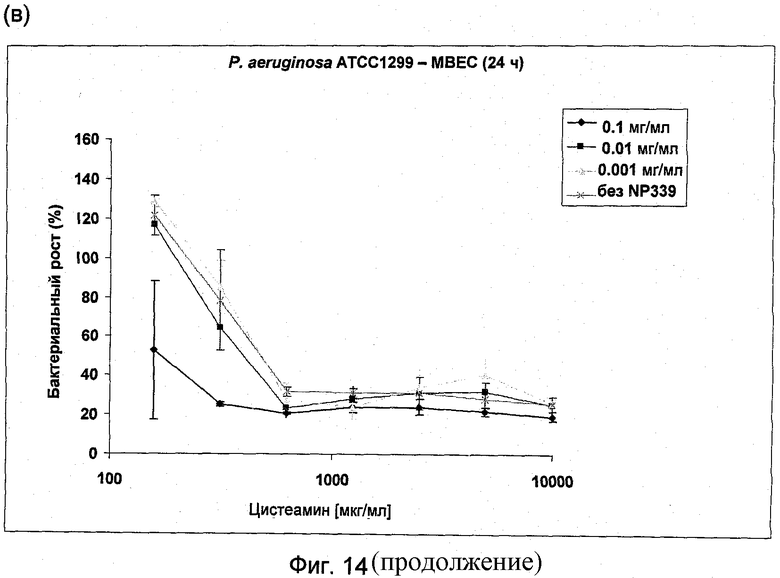
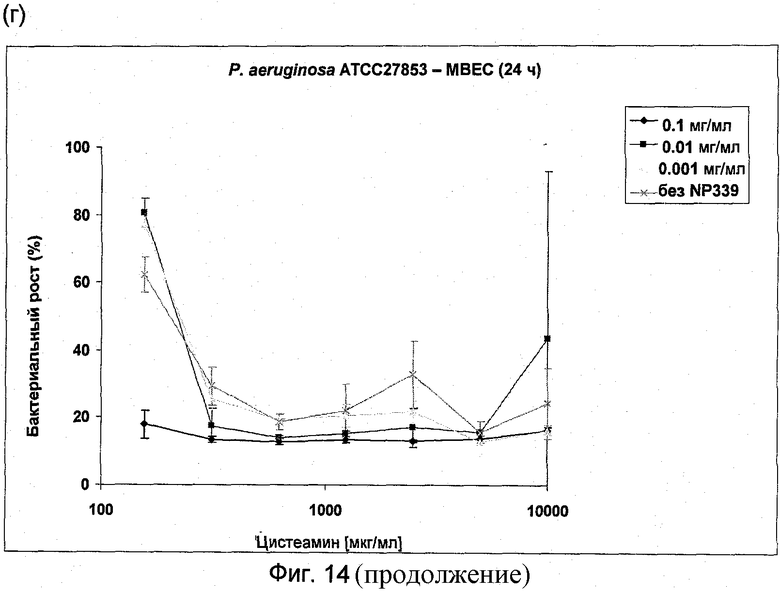
На Фиг.14 представлена антибактериальная активность комбинации NP339 и NM001 (цистеамина) в отношении биопленочных клеток (а) P.aeruginosa DSM 1128, (б) P.aeruginosa АТСС ВАА-47, (в) P.aeruginosa DSM 1299 и (г) P.aeruginosa АТСС 27853.
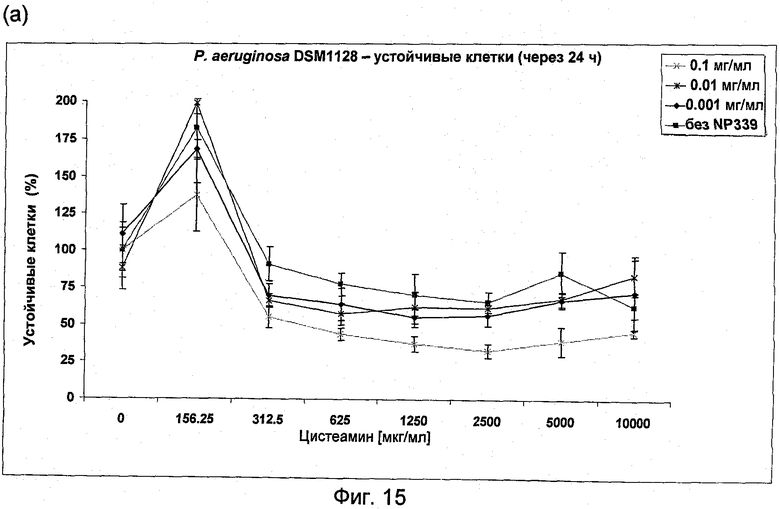
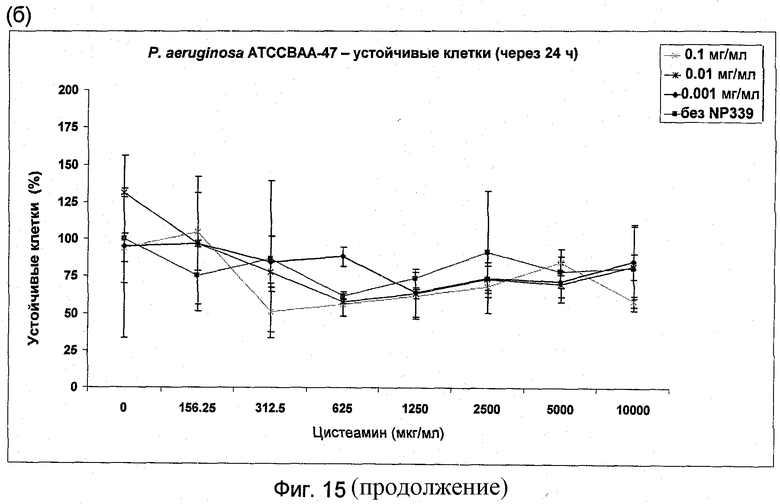
На Фиг.15 представлена антибактериальная активность комбинации NP339 и NM001 (цистеамина) в отношении устойчивых клеток (а) P.aeruginosa DSM 1128 и (б) P.aeruginosa АТСС ВАА-47.
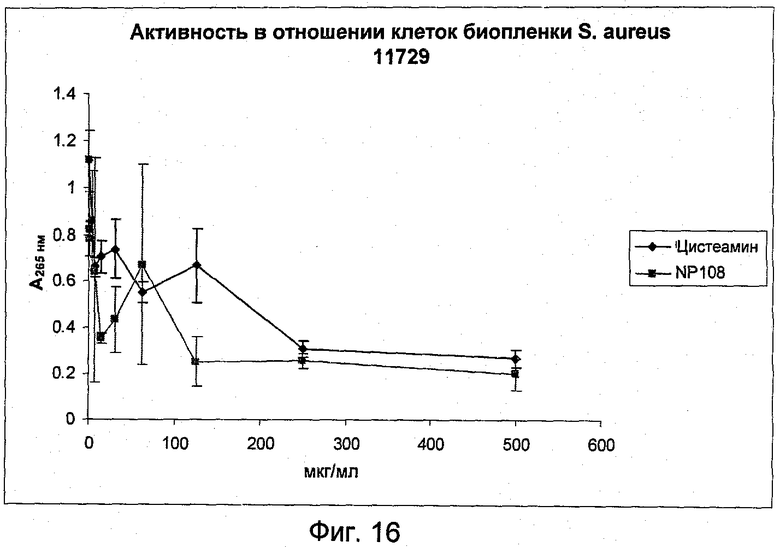
На Фиг.16 представлена антибактериальная активность NP108 и NM001 (цистеамина) в отношении биопленочных клеток S.aureus DSM 11729.
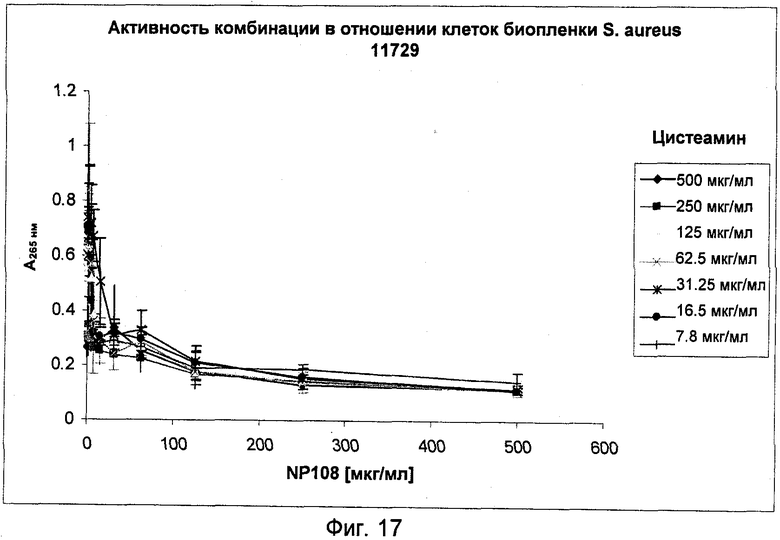
На Фиг.17 представлена антибактериальная активность комбинации NP108 и NM001 (цистеамина) в отношении биопленочных клеток S.aureus DSM 11729.
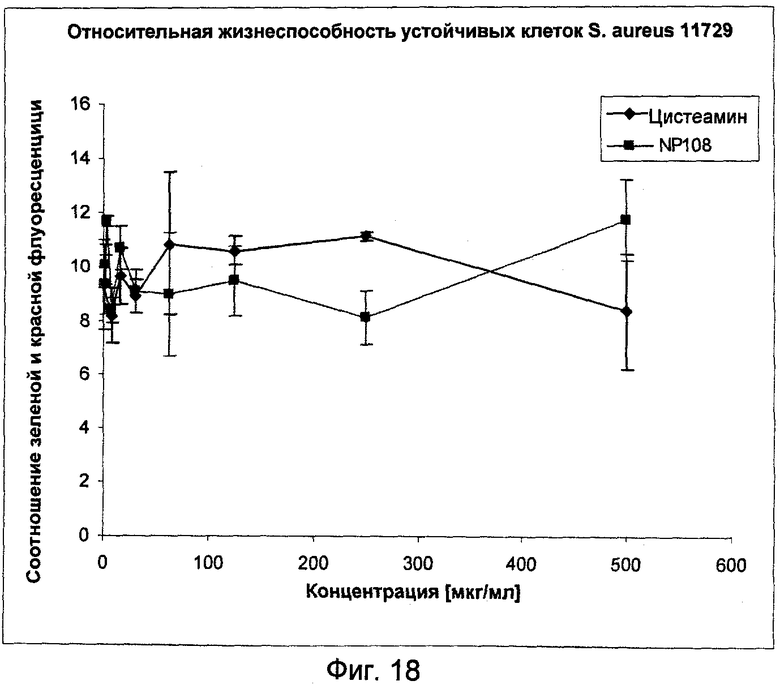
На Фиг.18 представлена антибактериальная активность NP108 и NM001 (цистеамина) в отношении устойчивых клеток S.aureus DSM 11729.
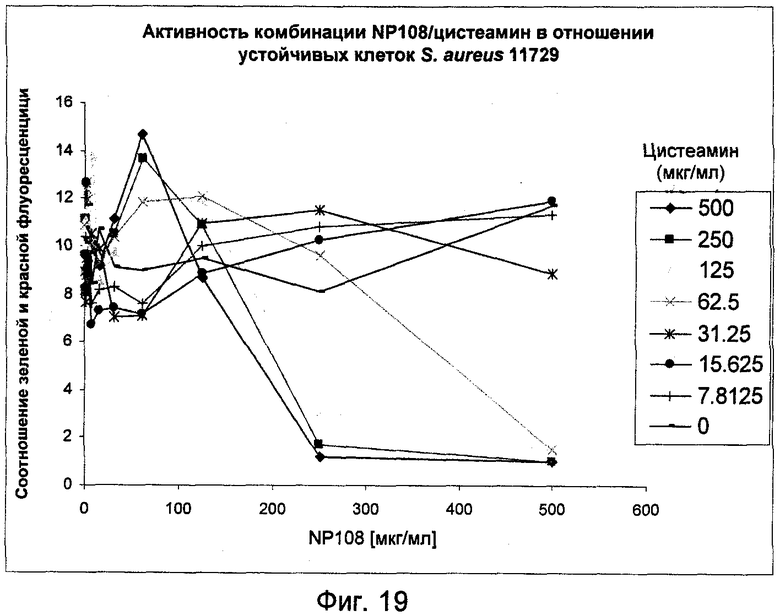
На Фиг.19 представлена антибактериальная активность комбинации NP108 и NM001 (цистеамина) в отношении устойчивых клеток S.aureus DSM 11729.
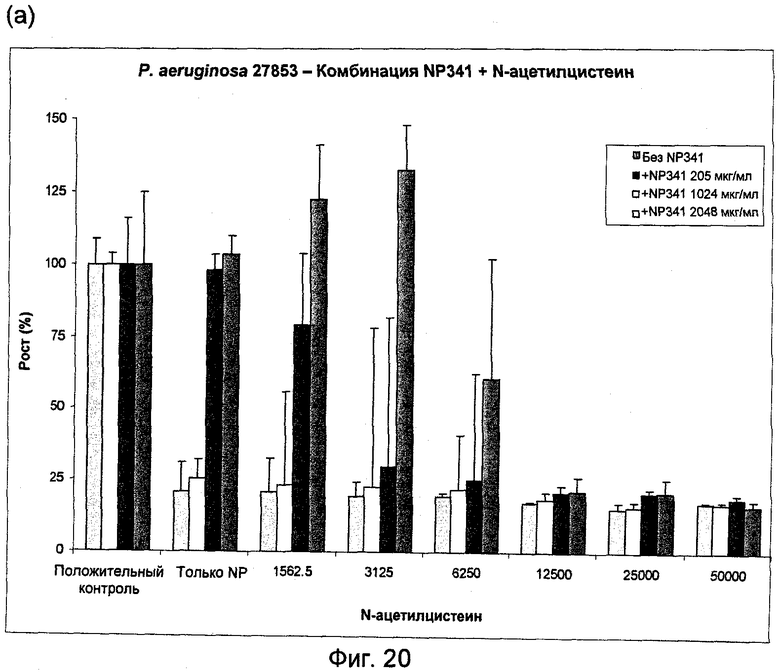
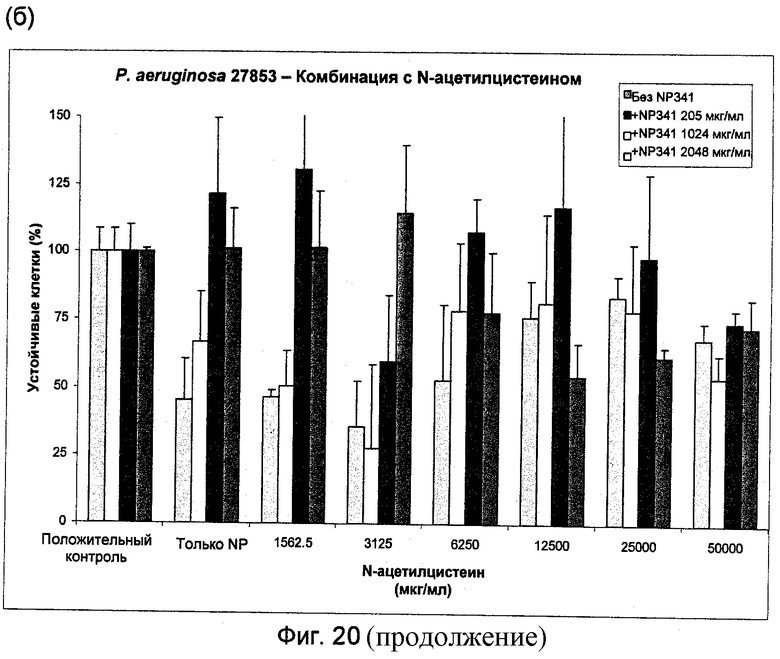
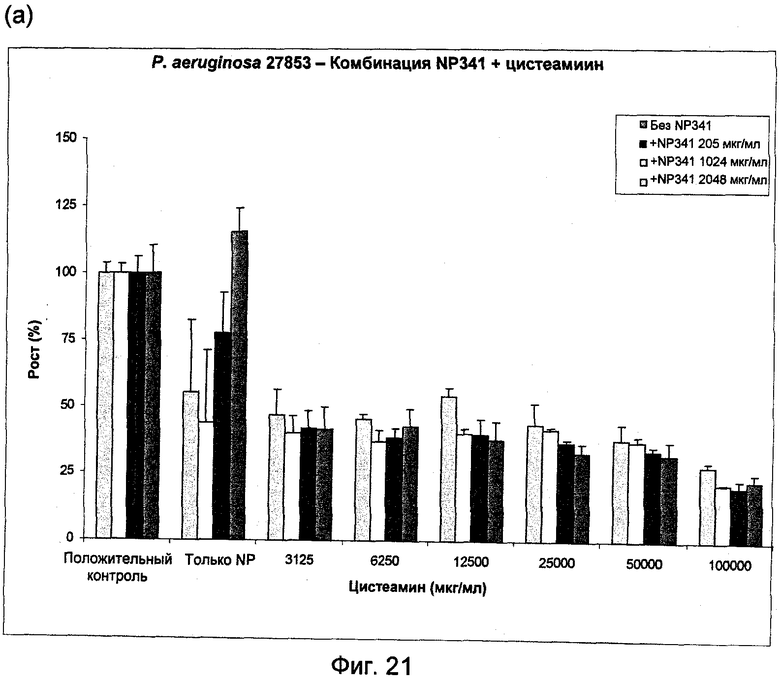
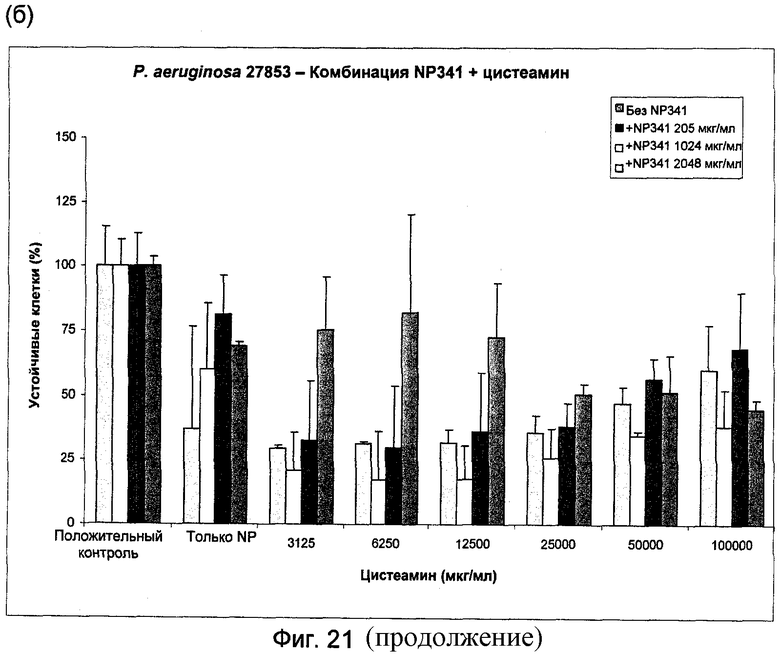
На Фиг.20 и 21 представлена активность муколитических агентов N-ацетилцистеин (Фиг.20(a) и 20(б)) и NM001 (цистеамин) (Фиг.21(a) и 21(б)) в отдельности и в комбинации с NP341 в отношении планктонных клеток Р.aeruginosa 27853.
На Фиг.22а представлена необработанная контрольная биопленка S.aureus через 24 часа.
На Фиг.22б: представлена биопленка S.aureus через 24 часа после обработки NM001 (цистеамином) при 2 мг/мл.
На Фиг.22в: представлена биопленка S.aureus через 24 часа после обработки Колистином при 0,2 мг/мл.
На Фиг.22г: представлена биопленка S.aureus через 24 часа после обработки пептидом NP108 при 2 мг/мл.
На Фиг.23а: представлена необработанная контрольная биопленка S. aureus через 24 часа.
На Фиг.23б: представлена биопленка S.aureus через 24 часа после обработки NM001 (цистеамином) при 2 мг/мл.
На Фиг.23в: представлена биопленка S.aureus через 24 часа после обработки Колистином при 0,2 мг/мл.
На Фиг.23г: представлена биопленка S. aureus через 24 часа после обработки пептидом NP108 при 2 мг/мл.
На Фиг.24а: представлена необработанная контрольная биопленка Р.aeruginosa через 24 часа.
На Фиг.24б: представлена биопленка P.aeruginosa через 24 часа после обработки NM001 (цистеамином) при 2 мг/мл.
На Фиг.24в: представлена биопленка P.aeruginosa через 24 часа после обработки Колистином при 0,2 мг/мл.
На Фиг.24г: представлена биопленка P.aeruginosa через 24 часа после обработки пептидом NP108 при 2 мг/мл.
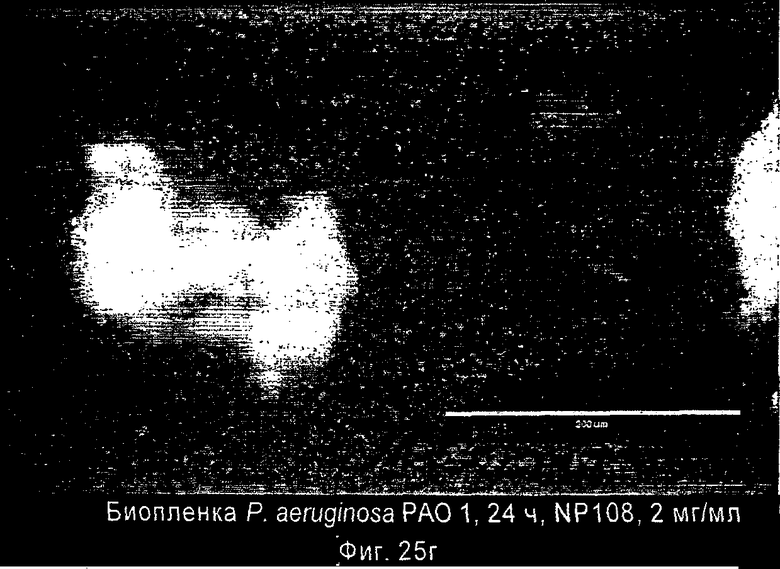
На Фиг.25а: представлена необработанная контрольная биопленка Р.aeruginosa через 24 часа.
На Фиг.25б: представлена биопленка P.aeruginosa через 24 часа после обработки NM001 (цистеамином) при 2 мг/мл.
На Фиг.25в: представлена биопленка P.aeruginosa через 24 часа после обработки Колистином при 0,2 мг/мл.
На Фиг.25г: представлена биопленка P.aeruginosa через 24 часа после обработки пептидом NP108 при 2 мг/мл.
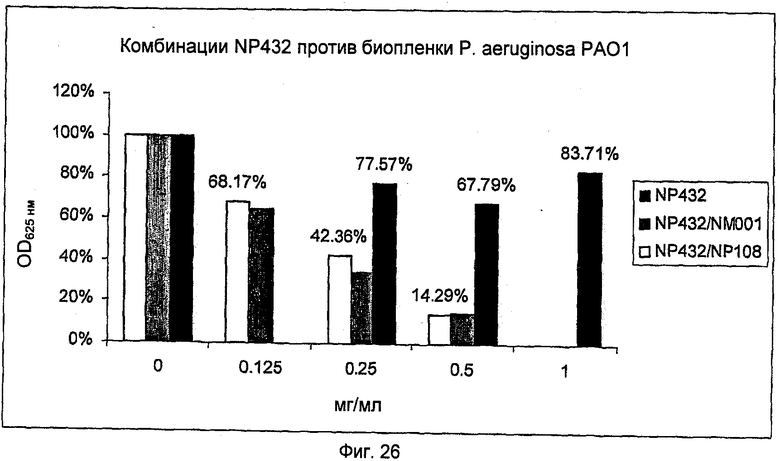
На Фиг.26: представлена активность NP432 одного и в комбинации с NM001 (цистеамином) или в комбинации с NP108 в отношении биопленки P.aeruginosa РА01.
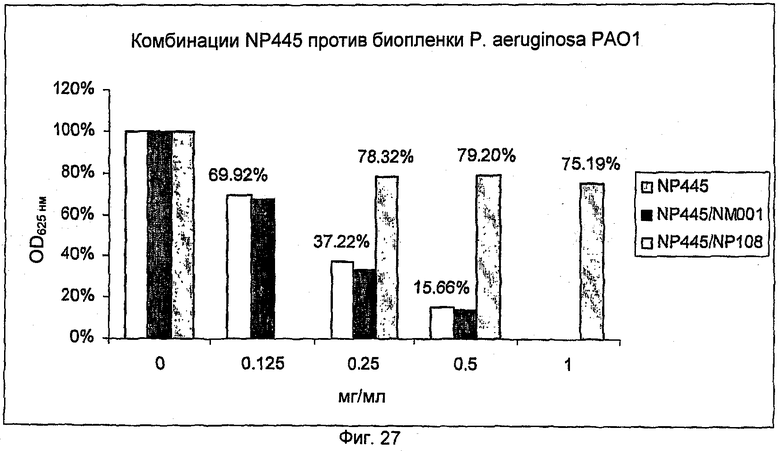
На Фиг.27 представлена активность NP445 одного и в комбинации с NM001 (цистеамином) или в комбинации с NP108 в отношении биопленки P.aeruginosa РА01.
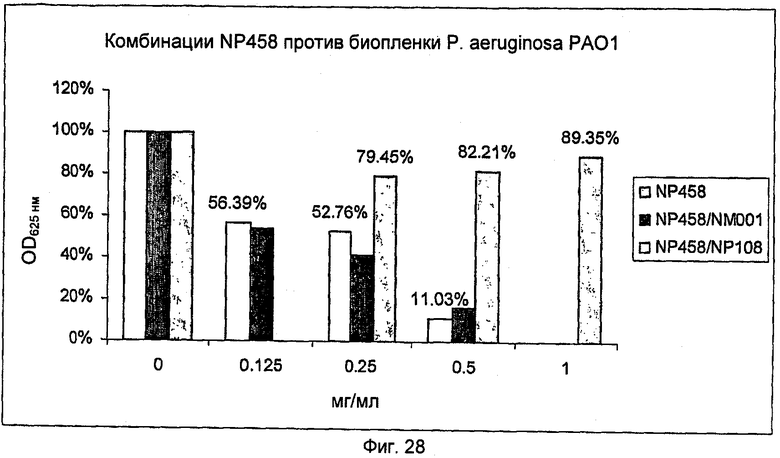
На Фиг.28 представлена активность NP458 одного и в комбинации с NM001 (цистеамином) или в комбинации с NP108 в отношении биопленки P.aeruginosa РА01.
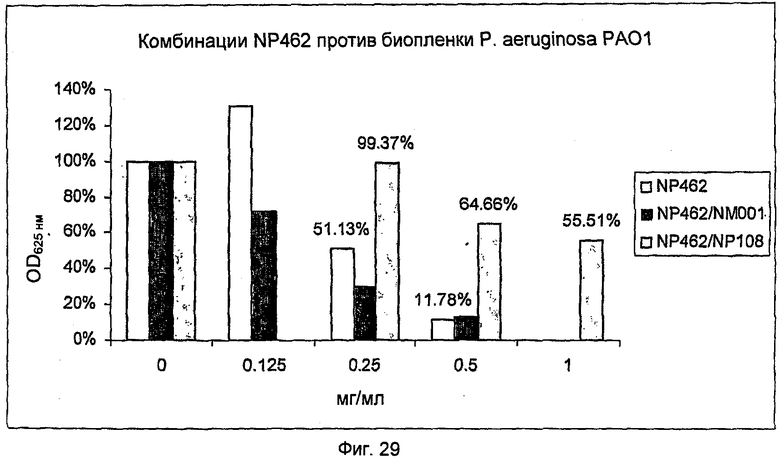
На Фиг.29 представлена активность NP462 одного и в комбинации с NM001 (цистеамином) или в комбинации с NP108 в отношении биопленки P.aeruginosa РА01.
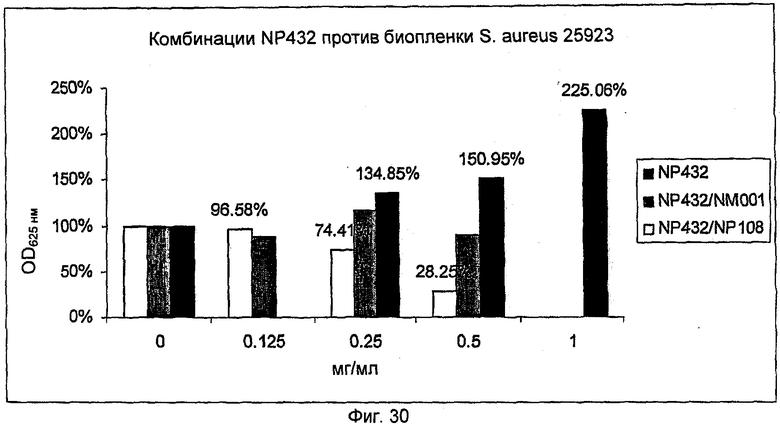
На Фиг.30 представлена активность NP432 одного и в комбинации с NM001 (цистеамином) или в комбинации с NP108 в отношении биопленки S.aureus АТСС25923.
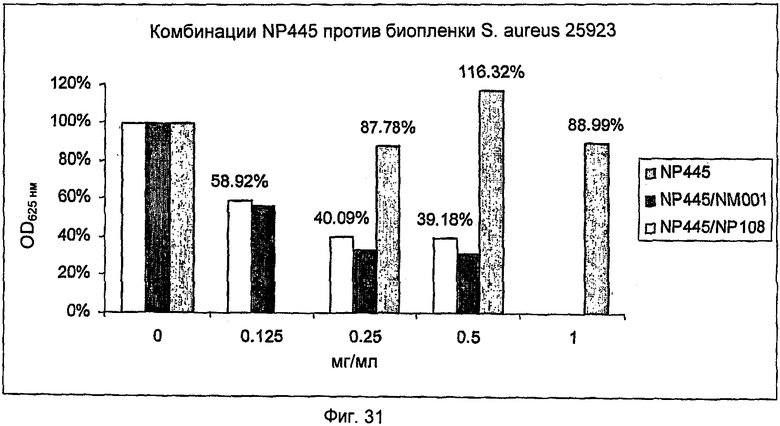
На Фиг.31 представлена активность NP445 одного и в комбинации с NM001 (цистеамином) или в комбинации с NP108 в отношении биопленки S.aureus АТСС25923.
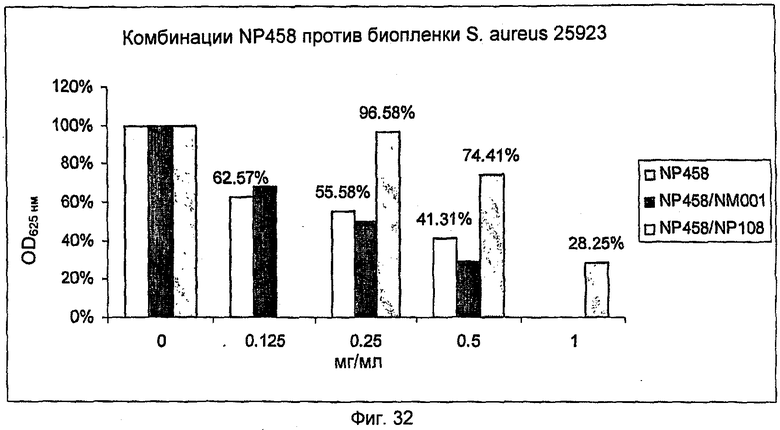
На Фиг.32 представлена активность NP458 одного и в комбинации с NM001 (цистеамином) или в комбинации с NP108 в отношении биопленки S.aureus АТСС25923.
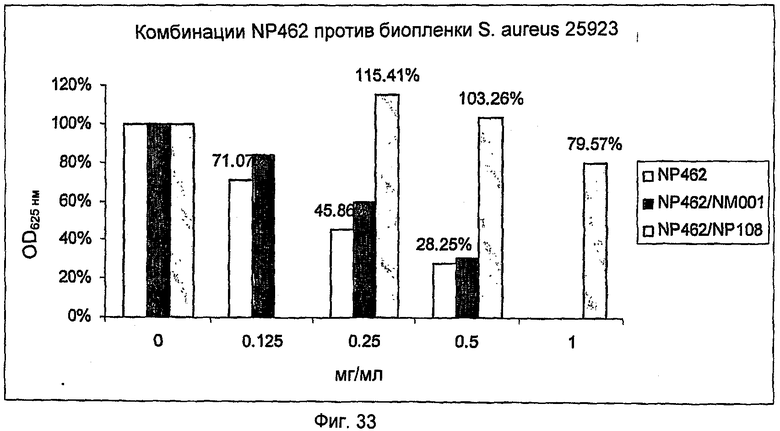
На Фиг.33 представлена активность NP462 одного и в комбинации с NM001 (цистеамином) или в комбинации с NP108 в отношении биопленки S.aureus 25923.
В Таблице 1 представлено резюме по активности тестированных антимикробных агентов в отношении грамотрицательных штаммов P.aeruginosa и грамположительных Staphylococcus spp.
В Таблице 2 представлено резюме по активности тестированных антимикробных агентов в отношении S.epidermidis, S.aureus и P.aeruginosa.
ПРИМЕРЫ
Активность антимикробных агентов в отношении бактериальных биопленок
Материалы и методы
1.1 Бактериальные штаммы
В этом исследовании использовали Pseudomonas aeruginosa АТСС27853, P.aeruginosa ВАА-47 (PA01), P.aeruginosa DSM 1128, P.aeruginosa DSM 1299 и S.epidermidis ATCC35984, S.epidermidis ATCC12228 Staphylococcus aureus 25923 и метициллин-устойчивый Staphylococcus aureus DSM 11729 (MRSA) (DSMZ, Брауншвейг, Германия). Получали четыре клинических изолята Р.aeruginosa (NH57388A-D, Hoffmann et al., 2005, 2007) и использовали для тестирования на чувствительность к антимикробным средствам.
1.2 Получение антимикробных соединений
Антимикробные агенты, тестированные в этом исследовании, представляли собой катионный пептид NP108, который соответствует поли-L-лизину гидробромиду 10-20 кДа, и цистеамин (NM001). Оба агента получали от Sigma-Aldrich (Gillingham, UK), маточные растворы готовили при 20 мг/мл в чистой воде 14-18 МОм.см (очистная система для воды Purite НР40, Oxon, UK). Сразу после растворения препараты стерилизовали фильтрованием при использовании 0,22 - мкм фильтров (Millipore, Watford, Англия) и хранили при - 20°C.
Также исследовали следующие антимикробные пептиды NovaBiotics:
Эти антимикробые пептиды NovaBiotics были синтезированы в NeoMPS (Страсбург, Франция) способом Fmoc и имели чистоту по меньшей мере 95%.
1.3 Получение бактериального инокулята
Бактериальный инокулят приготавливали разведением из активно растущих культур в бульоне Мюллера-Хинтона, стандартизованных при использовании 0,5 стандарта мутности МакФарланда, как описано в CLSI для способа М26-А.
1.4 Определение минимальной ингибирующей концентрации (МИК)
Для определения предупреждения образования биопленки бактериальный инокулят и антимикробные агенты добавляли в планшеты одновременно. Планшеты инкубировали при 37°С в течение 24 ч, и оптическую плотность считывали при 625 нм на считывателе микротитровальных планшетов (BioTec Powerwave XS, Winooski, США). МИК определяли как самую низкую концентрацию антимикробного агента, показывающую полное ингибирование бактериального роста.
1.5 Определение фракционной ингибирующей концентрации (ФИК)
ФИК соответствует коэффициенту взаимодействия, показывающему, является ли комбинация антимикробных агентов синергетической, аддитивной, антагонистической или нейтральной. ФИК определяли сравнением активности агента в комбинации (МИК агента А+агента В) с активностью этого агента по отдельности (МИК агент А или агента В) следующим образом (Singh et а/., 2000):
FIC=МИКА[Комбинация]/МИКА[отдельно]+МИКВ[комбинация]/МИКВ[отдельно]
Об аддитивных комбинациях двух антимикробных агентов свидетельствует индекс ФИК, равный 1, тогда как индекс ФИК меньше 1 указывает на синергетическую комбинацию. Нейтральные комбинации будут давать значение ФИК между 1 и 4, причем индекс ФИК выше 4 указывает на антагонистические эффекты между двумя антимикробными агентами.
ФИК также вычисляли для оценки взаимодействия двух антимикробных агентов в комбинации против бактериальных биопленок. Те же формулы применимы при использовании МУБК вместо МИК.
1.6 Определение минимальной уничтожающей биопленку концентрации (МУБК)
Суммарный объем 100 мкл бактериального инокулята в бульоне Мюллера-Хинтона добавляли в каждую лунку 96-луночных планшетов (зараженные планшеты (challenge plates)), и планшеты инкубировали при 37°С в течение 24 ч на ротационном встряхивателе (Grant-Bio PS-3D, Shepreth, Англия) при 24 об/мин для создания возможности образования биопленки.
Затем промывали зараженные планшеты один раз стерильным забуференным фосфатами физиологическим раствором (PBS) (1×), и добавляли к зараженным планшетам двукратные серийные разведения антимикробных агентов в бульоне Мюллера-Хинтона. Зараженные планшеты инкубировали при 37°С в течение 24 ч на роторном встряхивателе (Grant-bio PS-3D, Shepreth, Англия) при 24 об/мин.
Супернатанты из каждого зараженного планшета переносили в свежие планшеты, и оптическую плотность измеряли при 625 нм на считывателе микротитровальных планшетов (BioTek Powerwave XS, Winooski, США). МУБК определяли по самой низкой концентрации антимикробных агентов, показывающей отсутствие бактериального роста.
1.7 Оценка устойчивых клеток в биопленках
После переноса супернатанта из зараженных планшетов промывали биопленки один раз стерильным PBS (1х), и добавляли в лунки зараженных планшетов по 100 мкл раствора для флуоресцентного окрашивания живых/мертвых клеток BacLight (Invitrogen, Paisley, Великобритания), содержащего 4 мкМ SYT09 и 20 мкМ йодид пропидия (PI) в стерильном PBS (1×). Планшеты инкубировали при комнатной температуре в темноте в течение 15 мин, и флуоресценцию считывали при 485 нм (возбуждение)/528 нм (испускание) и 485 нм (возбуждение)/645 нм (испускание) для флуоресценции SYT09 и PI соответственно на флуоресцентном считывателе микротитровальных планшетов (BioTec Synergy НТ, Winooski, США) с чувствительностью, установленной на 50, и с донной ориентации оптики. Прямое наблюдение биопленок при использовании флуоресцентного микроскопа Axiovert 40 (Zeiss, Gottingen, Германия) позволяло идентифицировать присутствие живых и мертвых бактерий, и изображения биопленок получали при увеличении от 100- до 400-кратного.
Относительную жизнеспособность устойчивых клеток определяли по соотношениям результатов измерения флуоресценции живых/мертвых клеток, и для подтверждения присутствия или отсутствия живых клеток использовали микроскопию.
2 Результаты
2.1 Предотвращение образования биопленки
Для оценки предотвращения образования биопленки грамположительными и грамотрицательными бактериями, бактериальный инокулят и антимикробные агенты добавляли в планшеты одновременно. Диапазон концентраций антимикробных агентов составлял 0-500 мкг/мл для NP108 и 0-320 мкг/мл для цистеамина в отношении грамотрицательных бактерий P.aeruginosa АТСС ВАА-47 и 0-1000 мкг/мл для NP108 и 0-320 мкг/мл для цистеамина в отношении грамположительных MRSA.
2.1.1 Активность в отношении P. aeruginosa АТСС ВАА-47
МИК составляла 62,5 мкг/мл у NP108 и 320 мкг/мл у цистеамина. NP108 оказывал бактерицидные свойства при 250 мкг/мл, тогда как цистеамин не оказывал бактерицидные свойства при концентрации до 320 мкг/мл (данные не показаны).
В присутствии 160 мкг/мл цистеамина МИК у NP108 снижалась до 31,25 мкг/мл. Когда концентрация цистеамина была удвоена (т.е. 320 мкг/мл), рост не наблюдали независимо от концентрации NP108.
Определение ФИК для этой комбинации показывает, что эти антимикробные агенты имеют аддитивные эффекты (ФИК=1). Более того, бактерицидную активность получали в присутствии 125 мкг/мл NP108 и 320 мкг/мл цистеамина (данные не показаны), что подтверждает аддитивный эффект этих агентов.
2.1.2 Активность в отношении S. aureus DSM 11729
МИК составляла 125 мкг/мл у NP108 и больше 320 мкг/мл у цистеамина. NP108 оказывал бактерицидные свойства при 125 мкг/мл, тогда как цистеамин не оказывал бактерицидные свойства при концентрации до 320 мкг/мл (данные не показаны).
Увеличение концентраций цистеамина показало более сильное ингибирование роста при любой данной концентрации NP108. В присутствии 40 мкг/мл цистеамина МИК у NP108 снижалась до 31,25 мкг/мл и до 15,625 мкг/мл при добавлении 320 мкг/мл цистеамина.
Определение ФИ К для этой комбинации показывает, что эти антимикробные агенты имеют наименьшие аддитивные эффекты (ФИК меньше 1). Более того, бактерицидную активность достигали в присутствии 31,25 мкг/мл NP108 и не менее чем 160 мкг/мл цистеамина, а также 62,5 мкг/мл NP108 и не менее чем 80 мкг/мл цистеамина (данные не показаны), что подтверждает аддитивный эффект этих агентов.
Приложение 1 показывает динамику активности коротких линейных аргининовых пептидов (NP339, NP340, NP341 и NP352) в отношении планктонных клеток S.aureus DSM 11729.
В Приложении 2 приведено резюме по активности NP108, цистеамина, обоих соединений в комбинации, а также по активности NP339 и NP341 в отношении планктонных клеток S.aureus DSM 11729 и P.aeruginosa ВАА-47.
2.2 Разрушение образованных биопленок
Оценку активности NP108 и цистеамина в отношении бактериальных биопленок осуществляли с биопленками в возрасте 24 часа, и также определяли активность обоих соединений в комбинации. Активность антимикробных агентов в отношении бактериальных биопленок определяли по их активности в отношении биопленочных клеток и устойчивых клеток.
2.2.1 Активность NP339 в отношении бактериальных биопленок
На Фиг.5 показана высокая активность NP339 в отношении биопленок 3 видов Staphylococcus, соответствующая МУБК от 156 до 625 мкг/мл. Увеличение оптической плотности при самой высокой дозе NP339 в отношении S.aureus 25923, вероятно, представляет собой артефакт комплексной и гетерогенной природы микробных биопленок. Напротив, NP339 снижал рост Р.aeruginosa ВАА-47 (РА01), но даже самая высокая протестированная доза (т.е. 5 мг/мл) не была достаточной для ингибирования 100% биопленочных клеток.
На Фиг.6 представлены данные, доказывающие, что NP339 является активным в отношении устойчивых клеток. В отличие от активности NP339 в отношении биопленочных клеток 4 тестированных штаммов, он был менее активным в отношении устойчивых клеток видов Staphylococcus, чем в отношении таковых P.aeruginosa ВАА-47 (РА01). NP339 был способен ингибировать жизнеспособность устойчивых клеток P. aeruginosa ВАА-47 (РА01) при 625 мкг/мл.
2.2.2 Активность NP341 в отношении бактериальных биопленок
Так же, как NP339 (Фиг.5), NP341 показал значительное снижение жизнеспособности биопленочных клеток. МУБК для MRSA 11729 и S.epidermidis 12228 составляла 625 мкг/мл. NP341 снижал жизнеспособность биопленочных клеток P.aeruginosa MRSA 11729 и ВАА-47 (РА01) в два-три раза.
Как видно в случае NP339, жизнеспособность устойчивых клеток Р.aeruginosa полностью ингибировалась при 625 мкг/мл NP341. Жизнеспособность устойчивых клеток 3 видов Staphylococcus снижалась на 25-50%.
2.2.3 Активность цистеамина в отношении бактериальных биопленок
На Фиг.9 представлены данные, доказывающие, что цистеамин имеет антимикробную активность в отношении биопленочных клеток тестированных грамположительных и грамотрицательных бактерий.
На Фиг.10 показана активность цистеамина в отношении устойчивых клеток тестированных грамотрицательных и грамположительных бактерий.
Представленные здесь результаты показывают антимикробную активность линейных коротких катионных пептидов NP339 и NP341 в отношении биопленок грамположительных и грамотрицательных бактерий. Эти соединения оказались более эффективными в отношении биопленочных клеток грамположительных бактерий при сравнении с грамотрицательными бактериями, тогда как в отношении устойчивых клеток картина обратная. Цистеамин показал активность в отношении биопленочных клеток при высоких концентрациях, однако он подавлял жизнеспособность как грамположительных, так и грамотрицательных устойчивых клеток при наименьших тестированных концентрациях (т.е. 6,25 мг/мл).
2.2.4 Активность NP108 и цистеамина в комбинации в отношении Р. aeruginosa АТСС ВАА-47
Комбинация этих двух антимикробных агентов показала полное ингибирование бактериального роста в присутствии 250 мкг/мл NP108 и от 62,5 до 500 мкг/мл цистеамина. Добавление 31,25 мкг/мл цистеамина к 500 мкг/мл NP108 имело такой же эффект, тогда как 31,25 мкг/мл цистеамина плюс 250 мкг/мл NP108 показало только частичное ингибирование бактериального роста.
ФИК, полученная с этими величинами МУБК (МУБКNP-отдепьно] больше 500 мгк/мл, МУБКNP108[в комбинации] 250 мгк/мл, МУБКцистеамин[в комбинации] 62,5 мгк/мл, МУБКцистеамин[отдельно] больше 100,00 мкг/мл), была примерно 0,5, что указывает на синергетический эффект между этими двумя антимикробными агентами. Это соответствует результатам по активности комбинации NP108/цистеамин в отношении планктонных клеток (Фиг.2).
Активность NP108 и цистеамина в отношении устойчивых Клеток оценивали с использованием способа флуоресцентного окрашивания для определения относительной жизнеспособности клеток. Использованными связывающимися с нуклеиновыми кислотами флуоресцентными молекулами были SYT09 и PI, которые проникают во все бактериальные клетки (зеленая флуоресценция) и в клетки с нарушенной мембраной (красная флуоресценция), соответственно. Поэтому соотношение зеленой (живые) и красной (мертвые) испускаемой флуоресценции является показателем относительной жизнеспособности бактериальной популяции и используется как показатель присутствия оставшихся живых клеток, соответствующих устойчивым клеткам, в биопленке.
На Фиг.12 показано, что относительная жизнеспособность биопленок, обработанных либо NP108, либо цистеамином, оставалась значительной, указывая на отсутствие активности этих соединений в отношении устойчивых клеток P. aeruginosa АТСС ВАА-47.
На Фиг.13 представлены данные, доказывающие, что комбинация NP108 и цистеамина показала более высокую активность в отношении устойчивых клеток P.aeruginosa АТСС ВАА-47, чем каждое соединение по отдельности (Фиг.12). Наиболее эффективные комбинации в отношении этих клеток представляли собой 250-500 мкг/мл NP108 и 62,5-500 мкг/мл цистеамина. Эти комбинации показали самую низкую относительную жизнеспособность в биопленках. Такие же результаты получены с 31,25 мкг/мл NP108 и 500 мкг/мл цистеамина, причем наблюдали только частичное ингибирование с 250 мкг/мл цистеамина.
Активность этих соединений в отношении устойчивых клеток показывает сходство с профилем оптимальных комбинаций, полученным в отношении биопленочных клеток (Фиг.11). Более того, прямые микроскопические наблюдения флуоресцентно окрашенных биопленок подтвердили активность этих комбинаций в отношении устойчивых клеток, поскольку живые клети не наблюдали в присутствии 250-500 мкг/мл NP108 и 62,5-500 мкг/мл цистеамина (данные не показаны).
2.2.5 Активность NP339 и цистеамина в комбинации в отношении Р.aeruginosa
На Фиг.14(а)-(г) показана активность 3 концентраций NP339: 1 мкг/мл, 10 мкг/мл и 100 мкг/мл в комбинации с увеличивающимися концентрациями цистеамина до 10 мг/мл в отношении 4 штаммов Pseudomonas aeruginosa.
Эти данные отчетливо демонстрируют повышенную антимикробную активность NP339 в отношении биопленочных клеток P.aeruginosa в комбинации с цистеамином. Следующие фигуры показывают примеры активности этих комбинаций в отношении устойчивых клеток двух из этих штаммов.
На Фиг.16 показана активность NP108 и цистеамина в отношении биопленочных клеток S.aureus DSM 11729. МУБК для цистеамина составляла 250 мкг/мл, тогда как NP108 ингибировал рост этих же клеток при 125 мкг/мл.
Комбинация NP108 и цистеамина показала полное ингибирование бактериального роста в присутствии 31,25 мкг/мл NP108 и 62,5 мкг/мл цистеамина и частичное ингибирование с более низкими концентрациями любого из этих соединений (Фиг.17). Следовательно, ФИК, полученная с этими же МУБК (МУБКNP108[отдельно] 125 мкг/мл, МУБКNP108[в комбинации] 31,25 мкг/мл, МУБКцистеамир[отдельно] 250 мкг/мл, МУБКцистеамин[в комбинации] 62,5 мкг/мл), была 0,5, что указывает на синергетический эффект между этими двумя антимикробными агентами против биопленки этих грамположительных бактерий. Такие же результаты наблюдали для биопленки грамотрицательных бактерий (Фиг.11). Это также соответствует полученным результатам по активности комбинации NP108 / цистеамин в отношении планктонных клеток S.aureus DSM 11729 (Фиг.4).
Как и в случае отсутствия активности, наблюдаемой для устойчивых клеток P.aeruginosa АТСС ВАА-47 (Фиг.12), относительная жизнеспособность биопленок S.aureus DSM 11729, обработанных либо NP108, либо цистеамином, оставалась значительной, указывая на отсутствие активности этих соединений в низких концентрациях в отношении устойчивых клеток этих грамположительных бактерий (Фиг.18).
Комбинация NP108 и цистеамина показала более высокую активность в отношении устойчивых клеток S.aureus DSM 11729, чем любое из этих соединений по отдельности (Фиг.19). Наиболее эффективные комбинации в отношении этих клеток представляли собой 250-500 мкг/мл NP108 и 125-250 мкг/мл цистеамина. Эти комбинации показали самую низкую относительную жизнеспособность в биопленках. Такие же результаты получены с 62,5 мкг/мл NP108 и 500 мкг/мл цистеамина. Комбинации с более низкими концентрациями любого из этих соединений показали высокую относительную жизнеспособность в биопленках.
В отличие от результатов с грамотрицательными устойчивыми клетками, прямые микроскопические наблюдения флуоресцентно окрашенных биопленок S.aureus DSM 11729 свидетельствовали о присутствии оставшихся в живых клеток при самых высоких объединенных концентрациях of NP108 и цистеамина (данные не показаны).
В Таблице 1 приведено резюме по активности коротких аргининовых пептидов NP339, NP341, поли-L-лизина NP108, цистеамина и комбинации NP108 с цистеамином в отношении грамположительных и грамотрицательных бактерий.
Приложение 1: Эти данные (не показаны) демонстрируют активность коротких линейных аргининовых пептидов в течение 48-часового периода в отношении планктонных клеток метициллин-устойчивых S.aureus (MRSA) DSM 11729. Диапазон тестированных концентраций, показанный в подписях, представлен в мг/мл. Эти данные (не показаны) демонстрируют активность коротких линейных аргининовых пептидов в течение 48-часового периода в отношении планктонных клеток метициллин-устойчивых S.aureus (MRSA) DSM 11729. Показанная динамика активности демонстрирует, что ингибирование бактериального роста связана с дозой антимикробного агента и с временем его действия на клетки. Полную бактерицидную активность наблюдали для NP339, NP 340 и NP352 при концентрациях выше 0,5 мг/мл в течение 48-часового периода; 0,125 и 0,25 мг/мл показали полное ингибирование в течение периода по меньшей мере 24 ч, а более низкие концентрации, такие как 0,06 и 0,03 мг/мл, показали полное ингибирование в течение периодов по меньшей мере 20 ч и 15 ч, соответственно. Такие же результаты получены с NP341, за исключением, что доза 0,25 мг/мл показала полное ингибирование в течение 48-часового периода.
Приложение 2: Однако в комбинации с 3-6 мг/мл N-ацетилцистеина требуется только 205 мкг/мл NP341 для достижения МУБК (Фиг.20а). Такую же повышенную активность для комбинации этих 2 соединений наблюдали в отношении устойчивых клеток: доза 1024 мкг/мл NP341+3128 мкг/мл N-ацетилцистеина ингибировала примерно 75% устойчивых клеток, что гораздо выше, чем ингибирование, которое получено с любым из этих двух соединений по отдельности (Фиг.20б).
Комбинация цистеамина или N-ацетилцистеина с NP341 показывает повышенную антибактериальную активность при сравнении с активностью любого соединения по отдельности. МУБК в отношении P.aeruginosa АТСС27853 была больше 2 мг/мл у NP341, взятого по отдельности, и больше 100 мг/мл у цистеамина (Фиг.21а). Это показывает отсутствие совместного эффекта у этих двух соединений в отношении биопленочных клеток Р.aeruginosa АТСС27853. Однако такое совместное действие наблюдали в отношении устойчивых клеток: доза 205 мкг/мл NP341+3 мг/мл цистеамина ингибировала примерно 75% устойчивых клеток, что гораздо лучше, чем любое из этих двух соединений по отдельности (Фиг.21б).
При использовании в комбинации с NP339 наблюдали, что добавление цистеамина даже в малых количествах помогает снижать величины МУБК у NP339 (Фиг.14а-г). Более интересно, комбинация NP339 и цистеамина также показала повышенную активность против устойчивых клеток P.aeruginosa DSM 1128 и P.aeruginosa ВАА-47 (Фиг.15а-б).
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ АНТИБИОТИК И ДИСПЕРГИРУЮЩЕЕ СРЕДСТВО ИЛИ АНТИАДГЕЗИВНЫЙ АГЕНТ | 2011 |
|
RU2607660C2 |
| Композиция, содержащая антибиотик и диспергирующее средство или антиадгезивный агент | 2011 |
|
RU2739249C2 |
| ПЕПТИДЫ И ИХ ПРИМЕНЕНИЕ | 2011 |
|
RU2590706C2 |
| АНТИМИКРОБНЫЕ АГЕНТЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2011 |
|
RU2570387C2 |
| Способ разрушения и предотвращения образования бактериальных биопленок комплексом антимикробных пептидов насекомых | 2017 |
|
RU2664708C1 |
| ПРЕПАРАТ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ, ВЫЗВАННЫХ БАКТЕРИЯМИ | 2020 |
|
RU2754610C1 |
| АНТИМИКРОБНЫЙ ПЕПТИД И ЕГО ПРИМЕНЕНИЕ | 2014 |
|
RU2699712C1 |
| СРЕДСТВО ДЛЯ СЕЛЕКТИВНОГО ВЛИЯНИЯ НА БИОПЛЕНКООБРАЗОВАНИЕ МИКРООРГАНИЗМАМИ | 2016 |
|
RU2646488C2 |
| Антибактериальное покрытие на ортопедический имплантат из титана и его сплавов и способ его получения (варианты) | 2023 |
|
RU2816023C1 |
| Антимикробные антибиопленочные композиции и способы их применения | 2014 |
|
RU2662764C2 |











Группа изобретений относится к области фармацевтики и медицины и касается применения цистеамина в лечении микробной инфекции, вызванной микробной биопленкой, а также к продукту, содержащему по меньшей мере два агента против биопленки, где по меньшей мере один агент против биопленки представляет собой антимикробный пептид, а второй агент против биопленки представляет собой цистеамин. Также предложено применение этого продукта в лечении микробной инфекции и способ предотвращения образования микробной биопленки в среде. Группа изобретений обеспечивает повышенную антибактериальную активность в сравнении с активностью любого соединения по отдельности. 8 н. и 5 з.п. ф-лы, 33 ил., 2 табл.
1. Применение цистеамина в лечении микробной инфекции, в частности инфекции, вызванной микробной биопленкой, или заболевания или состояния, ассоциированного с ней.
2. Антимикробный продукт, содержащий по меньшей мере два агента против биопленки, где по меньшей мере один агент против биопленки представляет собой антимикробный пептид и по меньшей мере один другой агент против биопленки представляет собой цистеамин, где антимикробный пептид выбран из NP108, NP339, NP341, NP432, NP445, NP458 и NP462.
3. Продукт по п. 2 для применения в качестве дезинфектанта или биоцида.
4. Продукт по п. 2 для применения в качестве лекарственного средства.
5. Антимикробный субстрат, на который нанесен или к которому присоединен цистеамин или продукт по п. 2.
6. Антимикробная фармацевтическая композиция, содержащая цистеамин или продукт по п. 2 и один или более чем один фармацевтически приемлемый разбавитель, эксципиент и/или носитель.
7. Применение продукта по п. 2 в лечении микробной инфекции или заболевания или состояния, ассоциированного с ней.
8. Применение по п. 1 или 7, где инфекция или заболевание или состояние, ассоциированное с ней, выбраны из группы, состоящей из кожных и раневых инфекций, инфекций среднего уха, инфекций желудочно-кишечного тракта, инфекций перитонеальной мембраны, инфекций мочеполовых путей, инфекций мягких тканей ротовой полости, образования зубного налета, глазных инфекций, эндокардита, инфекций при муковисцидозе и инфекций имплантированных медицинских устройств.
9. Способ предотвращения образования микробной биопленки в среде, включающий стадию введения в указанную среду продукта по п. 2 или субстрата по п. 5.
10. Способ лечения или предотвращения образования микробной биопленки в среде, включающий введение в указанную среду эффективного количества цистеамина.
11. Способ по любому из пп. 9-10, где указанная среда содержит микроорганизм, образующий биопленку, выбранный из бактерий, грибов, дрожжей, вирусов и простейших.
12. Способ по п. 11, где среда представляет собой ротовую полость.
13. Способ профилактического или терапевтического лечения микробной инфекции, включающий последовательное или совместное введение в терапевтически эффективном количестве:
первого агента против биопленки и
второго агента против биопленки, отличного от первого;
где по меньшей мере один агент против биопленки представляет собой антимикробный пептид и по меньшей мере один другой агент против биопленки представляет собой цистеамин, где антимикробный пептид выбран из NP108, NP339, NP341, NP432, NP445, NP458 и NP462.
| WO2007050565 A2, 03.05.2007 | |||
| WO2008093058 A2, 07.08.2008 | |||
| WO2007062272 A1, 31.05.2007 |
Авторы
Даты
2015-04-20—Публикация
2010-03-31—Подача